PENGENALAN DAN PENERAPAN
HPLC DALAM ANALISIS INDUSTRI
DAN LINGKUNGAN
“I call such a preparation a chromatogram
and the corresponding method the
chromatographic method.” — M.S. Tswett
KROMATOGRAFI
FASE GERAK (mobile phase)
FASE GERAK (mobile phase)
UJI
PREPARATIF UJI
Kategori interaksi
1. Adsorbsi
Senyawa diserap oleh permukaan padatan dan terjadi
keseimbangan jumlah solut pada fasa diam dan fasa gerak
2. Partisi
Lapisan cairan sebagai fasa diam yang diembankan pada
suatu padatan akan mendistribusi senyawa yang akan
dipisahkan dan membentuk keseimbangan dengan fasa
gerak
3. Molekular eksklusi/permeasi gel/gel fltrasi
Pemisahan berdasarkan ukuran molekul, dimana pada
keadaan ideal tidak ada keterikatan senyawa pada fasa diam
4. Penukaran ion
Senyawa ion dengan muatan berlawanan akan terikat pada
fasa diam melalui gaya elektrostatik
5. Afnitas
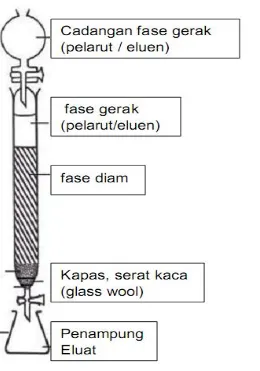
Kromatograf kolom
Gambar kolom kromatograf
Kolom terbuat dari gelas diisi dengan fase diam berupa serbuk penyerap (seperti selulosa, silika gel, poliamida). Fase diam dialiri (dielusi) dengan fase gerak berupa pelarut.
Faktor-faktor yang mempengaruhi pemisahan dengan kromatograf kolom adalah:
• fase diam yang digunakan
• kepolaran pelarut (fase gerak), ukuran kolom (diameter dan panjang kolom)
Kromatografi
KolomiTerbuka
iii
Color
Sistem pemasukan sampel: manual, tidak
volumetrik Injector
Waktu analisis lama, mengandalkan gaya
gravitasi dan kapiler pompa
Hasil pemisahan kurang baik pengemasan
kolom
Kesulitan pengamatan hasil pemisahan untuk
analit tidak berwarna Detektor
Komponen HPLC
POMPA ( PENDORONG FASA GERAK)
TEMPAT INJEKSI (AUTO SAMPLER)
KOLOM (FASA DIAM)
Komponen HPLC
•
Sistem pengalir fasa gerak
Mendorong/memompa fasa gerak sehingga bisa
mengalir ke seluruh sistem instrumen dengan laju alir
konstan (0,1-2 mL/menit)
•
Injektor/autosampler
Memasukkan sampel ke dalam sistem aliran fasa gerak
•
Kolom
Tabung stainless steel yang diisi fasa diam berfungsi
untuk memisahkan komponen-kompone dalam sampel
•
Detektor
Sensor optik yang akan mendeteksi perubahan secara
karakteristik solven yang melalui
•
Data system
Pompa untuk optimasi
•
Butuh 2 pompa tekanan
tinggi dan pengatur
gradien (mahal)
•
Dibatasi oleh sistem
dua pelarut
•
Laju alir yang berbeda
Pompa untuk optimasi
•
Sistem pelarut yang
lebih banyak dg
kekuatan dan
selektivitas yang
berbeda (lebih feksibel)
•
Perubahan laju alir
teratasi
•
Hanya butuh 1 pompa
(murah)
•
Pelarut disemprotkan
Klasifkasi HPLC
1. Partisi (liquid-liquid chromatography)
2. Adsorpsi (liquid-solid
chromatography)
3. Pertukaran ion (ion chromatography)
4. Size exclusion chromatography
5. Afnity chromatography
6. Chiral chromatography
Separation mechanism
Type of stationary
Normal phase
Fasa gerak (polar)
Triethylene glycol
Water
Hexane
Propyl ether
Hydrocarbon
Typical application of High
Performance Partition
chromatography
Field Typical mixture separated
Pharmaceutical Antibiotics, steroids, analgesics
Biochemicals Amino acids, proteins, carbohydrates, lipids Food products Artifcial sweeteners, antioxidants, afatoxins,
additives
Industrial chemicals Condensed
aromatics
, surfactants, propellants, dyesPollutants Pesticides, herbicides, phenols, PCBs Forensic chemistry Drugs, poisons, blood alcohol, narcotics
Clinical medicine Drugs metabolits, urine extracts, estrogens, bile acids
Fase diam
Fase diam Mekanisme sorpsi Kerakteristik
Silika yg tidak dimodifkasi
Adsorpsi, fase normal Polar, waktu retensi bervariasi karena ada air yg diserap
Fase terikat (ODS,
okta desil silan) Partisi, fase terbalik Non polar, mampu memisahkan sejumlah besar solut
Fase terikat
aminopropil Partisi yang dimodifkasi Polar, memisahkan senyawa karbohidrat
Fase terikat asam
sulfonat Penukar kation Tranfer massa lambat, puncak melebar
Fase terikat amin
kuarterner Penukar anion -Fase terikat silika dg
porositas terkendali Eklusi ukuran Fase gerak organik Polimer Partisi, eklusi,
pertukaran ion
Fase
•
N-heksana
•
Sikloheksana
•
Tetraklorometa
na
•
Triklorometana
•
diklorometana
•
Metil benzene
•
Tetrahidrofura
GENERAL
TYPES
Mengukur perubahan sifat fsika fasa gerak + solut secara keseluruhan
Sensitif hanya terhadap beberapa
sifat solut
Bulk property (general detectors)
Solute property (selective detectors)
Karakteristik solut Sensitivitas dan
Detektor
Yang umum dipakai
Detektor Ultraviolet / Visible (UV/VIS) :
untuk senyawa yang dapat menyerap
sinar UV-Vis
Detektor Fluorescence (RF) : komponen
yang keluar dari kolom dikenai sinar UV
dan akan berfuorosensi
Detektor Konduktivitas (CDD) : untuk
senyawa ionik
Detektor Refraktive Indeks (RID) : setiap
senyawa memiliki indek bias spesifk
Refractive Indeks
UV-Vis Fluorescence MS
Response Universal Selective Selective Selective
Sensitivity 4 microgram 5 nanogram 3 picogram 1 picogram
Linear Range 10 10 10 10
Flow Sensitive Yes No No Yes
Temperature sensitive
Rs : nilai resolusi
Ukuran kemampuan kolom untuk memisahkan dua
Kelebihan HPLC
•
Dapat digunakan untuk senyawa non
volatile dan senyawa dengan BM tinggi
•
Biasanya digunakan pada suhu kamar
sehingga aman bagi senyawa yang tidak
tahan panas
•
Fase gerak dapat diubah dengan mencapur
berbagai pelarut dengan berbagai
komposisi
•
Dapat digunakan untuk menganalisis
•
Sulit mengidentifkasi senyawa jika tidak
memiliki larutan standar
harus
dihubungkan dengan MS
•
Jika campuran sangat komplek maka
resolusi yang baik sulit diperoleh
Bidang aplikasi HPLC
•
Obat-obatan dan farmasi (parasetamol,
amoksilin)
•
Bahan pengawet (formalin)
•
Zat aditif (sakarin, asam benzoat)
•
Antioksidan
•
Zat-zat aktif pada produk makanan
(kafein)
•
Produk perawatan (senyawa fenolik)
•
Pestisida (residu pestisida diazinon pada
Gambar senyawa fenolik dalam produk perawatan (personal care products)
Contoh kromatogram analisis obat dalam
urin
Tetrahidrokanabi
nol (THC) : zat
aktif dalam
Pengujian Campuran Zat
Aktif Obat Menggunakan
Penentuan Kondisi Metode
HPLC
1. Penentuan kesesuaian sistem
Rasio fase gerak, laju alir, panjang gelombang,
2. Pembuatan kurva kalibrasi
3. Validasi metode
•
Kecermatan atau ketepatan (Akurasi)
•
Keseksamaan atau ketelitian (Presisi)
•
Linieritas
Penentuan Kondisi Metode
HPLC
1. Penentuan kesesuaian sistem
Uji ini menggunakan pengulangan injeksi sebanyak
6 kali larutan standar 0.2 mg/L dilanjutkan
penghitungan nilai waktu retensi dan AUC (Area
Under the Curve) dan penentuan RSD
2. Pembuatan kurva kalibrasi
3. Validasi metode
•
Kecermatan
•
Keseksamaan
•
Linieritas
•
LOD
Kondisi Pengujian
•
Metode elusi isokratik
•
Optimasi pelarut
–
Air deionisasi
–
Air deionisasi panas (60-70°C)
–
Air deionisasi:asetonitril (9:1)
–
Air deionisasi:asetonitril (8:2)
•
Optimasi fase gerak (eluen)
–
Air deionisasi (100 v/v)
–
Air deionisasi:asetonitril (90:10 v/v)
–
Air deionisasi:asetonitril (80:20 v/v)
•
Laju alir optimum injeksi larutan standar dengan
konsentrasi tertentu pada variasi kecepatan 0.2 – 1
mL/menit
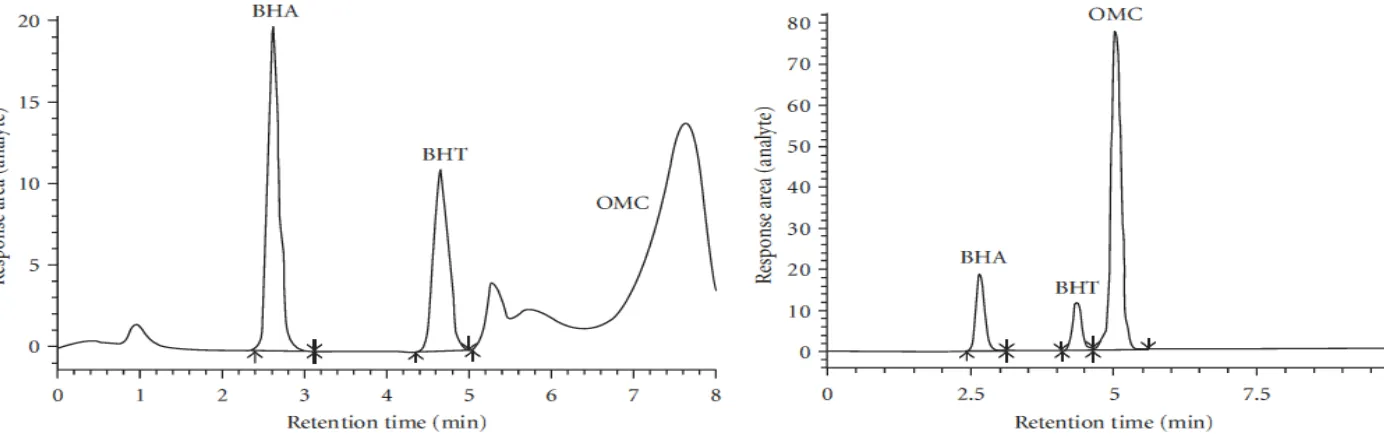
Kromatogram zat aktif obat dalam sampel
Kromatogram zat aktif obat standar (1mg/mL) dalam matriks