BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Uraian tumbuhan meliputi sistematika tumbuhan, nama daerah, nama
asing, morfologi tumbuhan dan manfaat tumbuhan. 2.1.1 Sistematika tumbuhan
Sistematika tumbuhan pugun tanoh adalah sebagai berikut (Anonim, 2009):
Divisi : Spermatophyta Subdivisi : Angiospermae
Kelas : Dicotyledoneae Subkelas : Asteridae Ordo : Scrophulariales
Famili : Scrophulariaceae Genus : Curanga
Spesies : Curanga fel-terrae (Lour) Merr.
Sinonim : Curanga amara Vahl., Picria fel-terrae Lour.
2.1.2 Nama daerah
Nama daerah dari tumbuhan ini adalah pugun tanoh (Dairi), tamah raheut (Sunda), kukurang (Maluku), dan papaita (Ternate) (Anonim, 2009).
2.1.3 Nama asing
Nama asing dari tumbuhan ini adalah sagai-uak (Filipina), gelumak susu, hempedu tanah, rumput kerak nasi (Malaysia), kong saden (Laos) dan thanh
(Vietnam) (Anonim, 2007).
2.1.4 Morfologi tumbuhan
Pugun tanoh merupakan tanaman berbatang basah, berbaring dan tumbuh merambat. Tumbuhan pugun tanoh memiliki tinggi 40 sampai 60 cm. Batangnya
dengan cabang-cabang yang ramping, jarang, tegak atau melata, berakar di buku-buku, dan berbulu halus. Daunnya berbulu halus, berbentuk bundar telur dengan
panjang 3-6 cm dan lebar 2-3 cm, ujung daun agak melancip dan tepi daun beringgit. Tangkai daunnya tumbuh berhadapan, permukaannya tidak berbulu, dan tipis. Bunga berupa tandan di ujung atau di batang, jumlah bunga 2-16, mahkota
bunga menabung, dan berbibir rangkap (Anonim, 2009). 2.1.5 Manfaat tumbuhan
Pugun tanoh digunakan sebagai obat diabetes (Harfina, 2013), meningkatkan nafsu makan, diuretik (Anonim, 2011), antiinflamasi (Juwita, 2009) dan sesak napas (asma) (Sugiarto dan Putera, 2008). Di Filipina, rebusan daun
pugun tanoh digunakan sebagai obat penurun panas, terutama untuk malaria, obat mual dan sakit perut (Anonim, 2011).
2.2 Ekstraksi
Ekstraksi adalah suatu cara untuk menarik satu atau lebih zat dari bahan asal dengan menggunakan pelarut. Umumnya zat berkhasiat tersebut dapat ditarik,
namun khasiatnya tidak berubah. Tujuan utama ekstraksi adalah mendapatkan atau memisahkan sebanyak mungkin zat-zat yang memiliki khasiat pengobatan dari zat-zat yang tidak dibutuhkan, agar lebih mudah dipergunakan (kemudahan
diabsorpsi, rasa, dan pemakaian) dan disimpan dibandingkan simplisia asal, dan tujuan pengobatannya lebih terjamin. Hasil ekstraksi disebut dengan ekstrak, yaitu
sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati
atau simplisia hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan (Depkes, 1995).
2.2.1 Metode ekstraksi
Ekstraksi dengan menggunakan pelarut dapat dilakukan dengan beberapa cara yaitu :
a. Cara dingin i. Maserasi
Maserasi adalah cara penarikan simplisia dengan merendam simplisia tersebut
dalam cairan penyari dengan beberapa kali pengocokan atau pengadukan pada
temperatur kamar, sedangkan remaserasi merupakan pengulangan penambahan
pelarut setelah dilakukan penyaringan maserat pertama, dan seterusnya (Ditjen POM, 2000).
ii. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar (Ditjen POM, 2000).
b. Cara panas i. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik (Ditjen POM, 2000).
ii. Sokletasi
Sokletasi adalah ekstraksi kontinu menggunakan alat soklet, dimana
pelarut akan terdestilasi dari labu menuju pendingin, kemudian jatuh membasahi
dan merendam sampel dalam tabung soklet, kemudian setelah pelarut mencapai tinggi tertentu maka akan turun ke labu destilasi setelah melewati pipa sifon, demikian berulang-ulang (Ditjen POM, 2000).
Keuntungan dari metode ini adalah ekstraksi simplisia dapat dilakukan dengan sempurna dan pelarut yang digunakan lebih sedikit dibandingkan metode
lainnya (Voigt, 1995). iii. Digesti
Digesti adalah maserasi dengan pengadukan kontinu pada temperatur yang
lebih tinggi dari temperatur ruangan, yaitu secara umum dilakukan pada temperatur 40-50oC (Ditjen POM, 2000).
iv. Infus
Infus adalah sediaan cair yang dibuat dengan menyari simplisia nabati dengan air pada suhu 900C selama 15 menit (Depkes RI, 1979).
v. Dekok
Dekok adalah sediaan cair yang dibuat dengan menyari simplisia nabati dengan air pada waktu yang lebih lama ± 30 menit dangan temperatur sampai titik
didih air (Ditjen POM, 2000).
2.3 Saluran Pernapasan
Saluran pernapasan atau tractus respiratorius (respiratory tract) adalah bagian tubuh manusia yang berfungsi sebagai tempat lintasan dan tempat pertukaran gas yang diperlukan untuk proses pernapasan. Saluran ini berpangkal
pada hidung atau mulut dan berakhir pada paru-paru (Wibowo, 2008).
Sistem pernapasan terdiri atas saluran pernapasan bagian atas dan saluran
pernapasan bagian bawah. Saluran pernapasan bagian atas berfungsi dalam
menyaring, menghangatkan, dan melembapkan udara yang dihirup. Saluran ini terdiri dari hidung, faring, dan laring. Sedangkan saluran pernapasan bagian bawah berfungsi untuk mengalirkan udara. Saluran ini terdiri dari trakea, bronkus,
bronkiolus dan alveolus (Hidayat dan Uliyah, 2008).
Otot polos saluran pernapasan adalah jaringan yang memiliki fungsi
fisiologis untuk menjaga kekakuan dari saluran pernapasan, yang dapat membantu menstabilkan saluran pernapasan saat terjadinya perubahan tekanan intrapleural. Kontraksi otot polos ini menyebabkan menyempitnya saluran pernapasan dan
menghambat aliran udara, sehingga menyebabkan asma (Martin, 2005).
2.4 Trakea
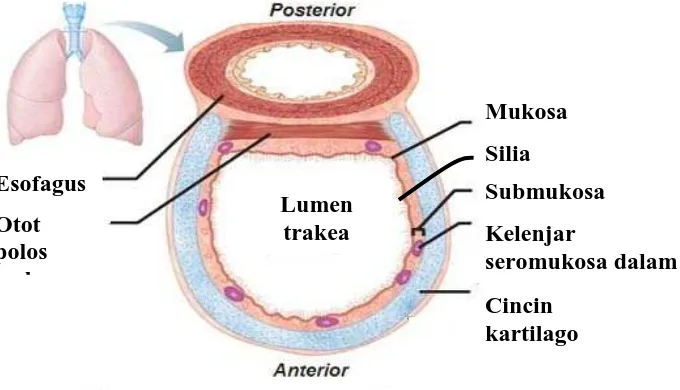
Trakea atau batang tenggorok adalah tuba dengan panjang 10 cm sampai 12 cm dan diameter 2,5 cm serta terletak di permukaan anterior dari esofagus (Gambar 2.1). Trakea berjalan dari laring sampai kira-kira ketinggian vertebra
koralis kelima dan di tempat ini bercabang menjadi dua bronkus (bronki) (Suryo, 2010).
Dinding trakea terdiri dari 3 lapisan (Suryo, 2010). Adapun 3 lapisan tersebut yaitu:
a. Lapisan luar, terdiri dari jaringan ikat;
b. Lapisan tengah, terdiri dari otot polos dan cincin tulang rawan; dan c. Lapisan dalam, terdiri dari jaringan epithelium bersilia.
Trakea terdiri dari 16 sampai 20 cincin kartilago/tulang rawan berbentuk-C yang dihubungkan oleh jaringan ikat dan otot polos. Tulang rawan berfungsi mempertahankan agar trakea tetap terbuka; karena itu, ujung posterior dari cincin
trakea dihubungkan oleh otot polos, yaitu di tempat trakea menempel pada esophagus, yang memisahkannya dari tulang belakang (Slonane, 2004). Trakea
dilapisi oleh epithelium bersilia pada lapisan dalamnya. Silia ini akan bergerak menuju ke atas ke arah laring; maka dengan gerakan ini debu dan butir-butir halus lainnya yang turut masuk bersama dengan udara dapat dikeluarkan (Pearce, 2009).
Trakea marmut terisolasi dapat digunakan untuk menguji aktivitas reseptor muskarinik, histaminergik dan adrenergik. Selain itu, model ini dapat digunakan untuk menguji senyawa yang menghambat bronkospasme. Hal ini digunakan
untuk mendeteksi β-simpatomimetik, penyekat reseptor H1 dan reseptor
muskarinik (Vogel, 2002).
2.5 Asma
Asma adalah suatu penyakit dengan adanya penyempitan saluran pernapasan yang berhubungan dengan hiperaktivitas otot polos, hipersekresi
mukus, edema dinding saluran pernapasan, dan infiltrasi sel inflamasi yang disebabkan berbagai macam rangsangan. Gejala klinis penyakit ini berupa
kesukaran bernapas yang disebabkan oleh penyempitan saluran pernapasan.
Penyempitan saluran napas bersifat dinamis, derajat penyempitan dapat berubah, baik secara spontan maupun karena pemberian obat, dan kelainan dasarnya berupa gangguan imunologi (Alsagaff, 2010).
Penyebab dari hiperaktivitas otot polos saluran pernapasan salah satunya terjadi karena pengaktifan jalur saraf muskarinik oleh asetilkolin yang dapat
menstimulasi kontraksi otot polos. Pemberian antagonis reseptor muskarinik akan menghambat efek asetilkolin dengan cara berikatan dengan reseptor muskarinik sehingga dapat menghambat kontraksi otot polos dan mengurangi sekresi kelenjar
submukosa saluran pernapasan (Supriyatno, 2010). Namun, obat seperti teofilin dapat juga merelaksasi otot polos saluran pernapasan secara langsung dengan
menghambat fosfodiesterase yang memecah cAMP (Katzung, 2001).
2.6 Asetilkolin
Asetilkolin merupakan molekul ester-kolin yang pertama diidentifikasi
sebagai neurotransmitter. Asetilkolin (ACh) disintesis di dalam susunan saraf pusat oleh saraf yang badan selnya terdapat pada batang otak. ACh yang dihasilkan kemudian akan dilepas dari ujung presinaptik dan menduduki
reseptornya. ACh diambil kembali (re-uptake) ke ujung presinaptik setelah mengalami degradasi menjadi kolin dan asetat oleh enzim asetilkolinesterase.
ACh sebagai neurotransmitter dalam sistem motorik dan sistem saraf otonom harus dihilangkan dan diaktivasi dalam waktu tertentu (Katzung, 2001).
Enzim-enzim yang berperan dalam sintesis dan degradasi ACh.
a. Choline Acetyltransferase (kolin asetiltransferase)
Enzim ini mengkatalisa asetilasi kolin dengan asetil koenzim A (disintesis
di mitokondria dan tersedia dalam jumlah banyak di ujung saraf) sehingga
membentuk asetilkolin, kemudian asetilkolin ditransportasikan dari sitoplasma ke dalam vesikel-vesikel oleh sebuah antiporter sepanjang akson sampai ujungnya (Taylor dan Brown, 2006). Perkiraan jumlah ACh dalam vesikel sinaptik berkisar
antara 1.000-50.000 molekul setiap vesikel. Dalam satu ujung saraf terdapat 300.000 atau lebih vesikel (Fawcett, 2002).
b. Acetylcholinesterase (Asetilkolin esterase, AChE)
AChE terdapat pada saraf kolinergik. Enzim ini mempunyai dua sisi pengikatan keduanya penting untuk degradasi ACh. Daerah anionik berfungsi
untuk pengikatan sebuah molekul ACh pada enzim. Begitu ACh terikat, reaksi hidrolisis terjadi pada sisi aktif yang disebut daerah esteratik. Di sini ACh terurai
menjadi kolin dan asam asetat. Kolin kemudian diambil lagi melalui sistem uptake kolin pada membran presinaps. Kolin ditransportasikan dari plasma ke dalam terminal neuron oleh pembawa membran bergantung – natrium (McCormick,
1989; Taylor dan Brown, 2006).
2.7 Reseptor Kolinergik
Reseptor kolinergik banyak dijumpai di sistem saraf otonom perifer. Ligan
dari reseptor kolinergik adalah neurotransmiter asetilkolin (ACh). Reseptor kolinergik terbagi 2 tipe, yaitu reseptor nikotinik dan reseptor muskarinik.
2.7.1 Reseptor nikotinik
Reseptor nikotinik merupakan reseptor yang terhubung dengan kanal ion dan terdiri dari lima subunit yaitu subunit α1, α2, β, γ, dan δ yang masing-masing
berkontribusi membentuk kanal ion dan memiliki tempat ikatan untuk molekul asetilkolin. Reseptor ini terdapat di neuromuscular junction, ganglia otonom,
medula adrenal, dan susunan saraf pusat. Paling banyak ditemukan di
neuromuscular junction. Neuromuscular junction adalah sinaps yang terjadi
antara saraf motorik dengan serabut otot (Rahardjo, 2009).
2.7.2 Reseptor muskarinik
Reseptor muskarinik terdistribusi luas di seluruh tubuh dan mendukung berbagai fungsi vital, di otak, sistem saraf otonom terutama saraf parasimpatis.
Reseptor muskarinik merupakan reseptor yang terhubung dengan protein G, terdiri dari 5 subtipe yaitu: M1, M2, M3, M4, M5. Reseptor M1, M3, dan M5
terhubung dengan protein Gq, sedangkan reseptor M2 dan M4 terhubung dengan
protein Gi dan dengan suatu kanal ion. Respons yang timbul dari aktivasi reseptor muskarinik oleh ACh dapat berbeda, tergantung pada subtipe reseptor dan
lokasinya (Rahardjo, 2009).
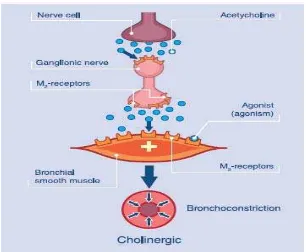
Gambar 2.2 Aktivasi reseptor muskarinik (sumber: www.COPDexchange.co.uk) Aktivasi reseptor M3 oleh asetilkolin menyebabkan kontraksi pada saluran
pernafasan seperti yang terlihat pada Gambar 2.2 (Barnes, 1993; Karyono, 2006). Aktivasi reseptor M3 akan mengaktifkan phospolipase C (PLC) melalui
penggabungan dengan protein Gq. Aktifnya PLC akan meningkatkan hidrolisis komponen fosfolipid minor membran plasma yang disebut phospatidylinositol 4,5-biphosphat (PIP2). PIP2 dipecah menjadi pembawa pesan kedua (second
messengers) yaitu inositol 1,4,5-trisphosphate (IP3) dan diacylglycerol (DAG).
IP3 adalah second messenger yang larut air dan menyebar dalam sitosol (Katzung,
2001). IP3 akan menduduki reseptor IP3 pada calcium store di sarcoplasmatic
reticulum (SR) sehingga menginduksi pelepasan kalsium dari SR ke dalam
sitosol. Hal ini mengakibatkan jumlah kalsium intraseluler meningkat (Hall,
2000).
DAG, produk lain dari hidrolisis PIP2, mampu mengaktifkan protein
kinase C (PKC). Aktifnya PKC akan membuka gerbang kalsium sehingga terjadi peningkatan influks kalsium (Ikawati, 2006). Peningkatan Ca2+ di sitosol akan membentuk kompleks Ca2+-kalmodulin yang mengaktifkan myosin light chain
kinase (MLCK) yang akan memfosforilasi myosin light chain (MLC), akibatnya
terjadi interaksi miosin dengan aktin yang menghasilkan kontraksi otot polos saluran pernapasan (Oenema, 2013).
2.8 Fosfodiesterase
Siklik nukleotida cyclic adenosine-3',5' monophosphate (cAMP) adalah
second messenger yang penting dalam regulasi aktivitas sel. Di saluran
pernapasan cAMP mengatur tonus otot polos, sekresi mediator dan aktivasi sel-sel inflamasi. Meningkatnya konsentrasi cAMP intraseluler akan menyebabkan
terjadinya bronkorelaksasi. Konsentrasi cAMP intraseluler ditentukan oleh stimulasi reseptor pada permukaan sel dan degradasi cAMP menjadi 5’-AMP oleh
fosfodiesterase (PDE) (Raff, et al., 2002). Degradasi cAMP oleh PDE dapat
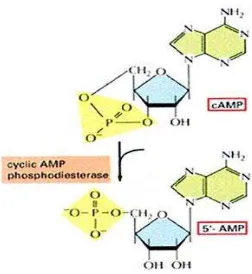
dilihat pada Gambar 2.3. Fosfodiesterase adalah enzim yang mengkatalisis hidrolisis ikatan ester pada molekul fosfat, seperti pada oligo- dan poli- nukleotida (Pudjaatmaka, 2002; Feneck, 2007).
Gambar 2.3 Hidrolisis cAMP oleh fosfodiesterase (Raff, et al., 2002) Terdapat lima jenis isoenzim PDE yang telah dibedakan berdasarkan
spesifisitas substrat dan pengembangan inhibitor selektif. Pada otot polos trakea dan bronkus manusia, telah diidentifikasi adanya PDE I, II, III, IV dan V. Pada
percobaan secara in vivo menggunakan marmut, diketahui bahwa penghambatan terhadap PDE III, IV dan V dapat menyebabkan bronkorelaksasi. Penghambatan PDE III menyebabkan relaksasi otot polos saluran napas, baik saat tonus spontan
atau tonus yang disebabkan oleh induksi karbakol. Sedangkan penghambatan PDE IV tidak menurunkan tonus spontan tetapi dapat menurunkan tonus yang
disebabkan oleh induksi karbakol (Barnes, 1995).
Kombinasi inhibitor PDE III dan IV yang paling efektif dalam merelaksasi otot polos saluran napas. Hal ini menunjukkan bahwa kerjasama dua isoenzim PDE III dan IV diperlukan untuk efek bronkodilator yang optimal. Inhibitor PDE
V, juga efektif sebagai bronkodilator, yang menunjukkan bahwa cGMP juga terlibat dalam relaksasi otot polos saluran napas (Barnes, 1995; Hall, 2000).
2.9 Teofilin
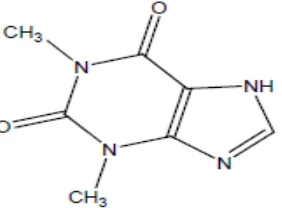
Rumus struktur teofilin dapat dilihat pada Gambar 2.4.
Gambar 2.4 Struktur teofilin (Depkes RI, 1995)
Nama Kimia : 1,3-dimethyl-3,7-dihydro-1H-purine-2,6-dione Rumus Molekul : C7H8N4O2
Berat Molekul : 180,17
Pemerian : Serbuk hablur, putih, tidak berbau, rasa pahit, stabil di udara
Kelarutan : Sukar larut dalam air, tetapi lebih mudah larut dalam air panas, mudah larut dalam larutan alkali hidroksida dan
dalam amonium hidroksida, agak sukar larut dalam etanol, dalam kloroform dan dalam eter (Depkes RI, 1995).
Teofilin merupakan derivat xantin yang menyebabkan relaksasi otot polos, terutama otot polos bronkus, serta merangsang otot jantung, dan meningkatkan diuresis. Adapun mekanisme kerja dari teofilin yaitu dengan cara menghambat enzim
fosfodiesterase sehingga mencegah pemecahan cAMP dan cGMP masing-masing
menjadi 5’-AMP dan 5’-GMP. Penghambatan fosfodiesterase menyebabkan
akumulasi cAMP dan cGMP dalam sel sehingga menyebabkan relaksasi otot polos,
termasuk otot polos bronkus (Katzung, 2006). Sehingga teofilin digunakan sebagai bronkodilator yang diperlukan pada serangan asma yang berlangsung lama. Selain
itu, teofilin juga digunakan sebagai profilaksis terhadap serangan asma (Ward, et al., 2008).
Teofilin mempunyai efek samping berupa mual dan muntah, gangguan
sistem saraf pusat (gelisah dan gangguan tidur), juga efek kardiovaskular, seperti takikardia, aritmia dan hipotensi (Schmitz, et al., 2003).
2.10 Organ Terisolasi
Organ terisolasi adalah suatu metode percobaan in vitro. Pada prinsipnya penelitian ini menggunakan organ yang direndam dalam larutan fisiologis yang
sesuai, temperatur diatur atau dikondisikan pada kondisi yang sama dari mana organ tersebut berasal serta pengaturan aliran oksigen. Percobaan organ terisolasi
ini menggunakan alat organ bath (Perry, 1970).
Percobaan dengan organ terisolasi mempunyai keuntungan tidak dipengaruhi oleh faktor farmakokinetika, dengan demikian obat yang digunakan
relatif lebih sedikit dosisnya dibandingkan in vivo. Percobaan dengan organ terisolasi lebih ditekankan untuk mengobservasi mekanisme pada sel target
sebagai tempat kerja. Hasil yang didapat dari percobaan organ terisolasi adalah
respon kontraktilitas terhadap rangsangan yang diberikan. Respon kontraktilitas dapat direkam dan dapat diukur untuk selanjutnya dapat dibuat kurva dosis respons. Untuk mendapatkan hasil percobaan yang akurat, maka diperlukan
persiapan yang baik dan seluruh percobaan harus betul-betul terkontrol. Hewan percobaan yang digunakan dibunuh tanpa anestesi sehingga tidak memengaruhi
kontraktilitasnya. Organ yang diambil segera dimasukkan ke dalam cairan fisiologis dan dikontrol oksigenasinya dan dihubungkan ke transduser dan diteruskan ke alat pencatat misalnya, kymograph atau maclab computer
(Syamsudin dan Darmono, 2011).