PENDAHULUAN
Tanaman tebu (Saccharum officinarum L.) merupakan salah satu komoditas pertanian yang men-empati posisi penting, karena 70% produksi gula dunia berasal dari tanaman tebu (Khan and Khatri, 2006). Oleh karenanya investasi di industri gula ber-basis tebu dinilai cukup prospektif untuk dilakukan (Suryana et al.,2005). Hal tersebut terlihat dari jum-lah produksi gula Indonesia yang tidak sebanding den-gan jumlah konsumsi. Berdasarkan data Ikatan Ahli Gula Indonesia (IKAGI), produksi gula konsumsi bulan Januari—Oktober 2011 hanya sebesar 2,11 juta ton. Sementara konsumsi gula dalam negeri sekitar 2,7—2,8 juta ton/tahun (Julian, 2011). Untuk menu-tupi defisit gula konsumsi tersebut, haruus dilakukan impor gula dari luar negeri. Selain itu, menurut De-wan Gula Indonesia (DGI) sejak tahun 2008—2010 terjadi penurunan luas areal tanam tebu dari 436.504 Ha (2008) menjadi 422.935 Ha (2009), dan pada ta-hun 2010 menjadi 418.259 Ha (Julian, 2011).
Untuk memenuhi kebutuhan gula dalam neg-eri sekaligus mengurangi impor gula, dan mewujud-kan swasembada gula tahun 2014, maka salah satu usaha yang dilakukan yaitu melalui perluasan areal tanaman tebu. Perluasan areal yang sedang dilaku-kan saat ini meliputi daerah Sumatera, Kalimantan, Sulawesi, dan Jawa (Yakub, 2011). Perluasan tana-man tebu dalam areal yang besar harus didukung oleh ketersediaan bibit yang bermutu tinggi dalam jumlah
INDUKSI DAN PROLIFERASI KALUS, SERTA INDUKSI TUNAS Ronald Bunga Mayang1, Dwi Hapsoro2 dan Yusnita2
1Mahasiswa Magister Agronomi Fakultas Pertanian Universitas Lampung 2Dosen Fakultas Pertanian Universitas Lampung
Email: ronald.bm007@gmail.com
yang besar. Salah satu cara perbanyakan tanaman yang mampu menghasilkan bibit dalam jumlah besar, seragam, dan dalam waktu yang relatif singkat adalah dengan cara kultur in vitro.
Kultur in vitro meliputi tahap-tahap penana-man eksplan, induksi kalus, proliferasi kalus, induksi tunas, induksi akar, hardening in vitro, dan aklimati-sasi yang kemudian diperoleh tanaman yang siap di-tanam di lapang. Setiap tahapan mulai dari induksi kalus hingga pembentukan akar mungkin membutuh-kan media kultur dengan zat pengatur tumbuh yang berbeda-beda baik jenis maupun konsentrasinya.
Media kultur merupakan salah satu penentu keberhasilan perbanyakan tanaman secara kultur ja-ringan (Gamborg and Phillips, 1995; Yusnita, 2003). Media dasar yang umum digunakan dalam kultur in vitro adalah yang mengandung unsur hara makro, mikro, sukrosa, vitamin, asam amino, bahan organik, dan zat pengatur tumbuh. Induksi kalus embriogenik dapat dilakukan pada media Murashige dan Skoog (full atau half-strength) dengan penambahan auksin, seperti 2,4-dichlorophenoxyacetic acid (2,4-D) (Ri-val dan Parveez, 2005; George et al., 2008). Sito-kinin dalam kultur jaringan terbukti dapat memacu diferensiasi tunas (Farid, 2003). Golongan sitokinin yang umum digunakan adalah BA (6-benzyladenine) dan kinetin.
Untuk memacu kalus berproliferasi lebih cepat, biasanya ditambahkan senyawa kompleks sebagai sumber N organik ke dalam media kultur jaringan. ABSTRACT
IN VITRO
PLANT REGENERATION OF SUGARCANE (
Saccharum officinarum
L.): CALLUS
INDUCTION, PROLIFERATION, AND SHOOT INDUCTION. This research is a series of activities that
studies the embryogenesis for somatic clonal reproduction plant sugarcane multiplication in vitro which
in-cludes the callus induction of explant pieces rolls up the leaves, the proliferation of embriogenic callus, and
shoots induction of embriogenic callus. Those of three researchs were conducted in a series. This experiment
were carried out in The Plant Science Laboratory, the Faculty of Agriculture, the University of Lampung,
Indonesia, from Oktober 2010 until April 2011. All experiments were conducted in a completely
random-ized design. Treatments of Experiment I were 2,4-D concentrations (0, 1, 2, and 3 mg/l) with and without
250 mg/l of casein hydrolysate, while those of Experiment II were combinations of those two chemicals,
2,4-D concentrations (1, 2, and 3 mg/l) with and without 250 mg/l of casein hydrolysate. Treatments of
Experiment III were BA concentrations (1 mg/l and 2.5 mg/l). Results of the experiments showed that the
best callus induction was achieved using MS media containing 3 mg/l 2,4-D, and callus induction was not
significantly affected by casein hidrolysates. Concentrations of 2,4-D did not significantly influence em
-bryogenic callus proliferation. The best shoot proliferation was attained in MS media containing 2.5 mg/l.
Keywords
: Benzyladenine (BA), 2,4-D, Casein Hydrolisate, sugarcane, and culture in vitro.
D E F
Salah satu sumber N organik yang biasa digunakan adalah kasein hidrolisat yang merupakan gabungan dari 20 jenis asam amino dan amonium (Trigiano dan Gray, 2010). Kasein hidrolisat yang berperan seb-agai sumber asam amino dan oligopeptida merupakan suatu produk yang dibuat dari protein keju (Siregar et al, 2010).
Penelitian ini bertujuan untuk mempelajari pen-garuh pemberian 2,4-D dan kasein hidrolisat dalam media dasar pada induksi kalus, pengaruh media in-duksi kalus pada proliferasi kalus, dan pengaruh pem-berian BA dalam media dasar pada induksi tunas.
BAHAN DAN METODE Tempat dan Waktu Penelitian
Penelitian ini dilakukan di Laboratorium Kul-tur Jaringan Fakultas Pertanian Universitas Lampung mulai bulan Oktober 2010 sampai dengan April 2011. Eskplan
Eksplan yang digunakan dalam penelitian ini berupa potongan gulungan daun muda pada pucuk tanaman tebu bagian terdalam yang berukuran 0,5—1 cm. Sumber eksplan adalah tanaman tebu (Saccha-rum officina(Saccha-rum L.) klon Ragnar yang didapat dari PT. Gunung Madu Plantation. Eksplan ini digunakan untuk percobaan induksi kalus. Untuk percobaan pro-liferasi kalus, eksplan yang digunakan adalah kalus embriogenik yang didapatkan dari hasil induksi kalus. Untuk percobaan induksi tunas, digunakan kalus em-briogenik yang didapatkan dari proliferasi kalus. Media
Media dasar untuk induksi kalus, proliferasi kalus, dan induksi tunas adalah media Murashige dan Skoog (MS). Media yang digunakan berupa media cair yang di masukkan ke dalam botol berukuran 250 ml, sebanyak 35 ml. Sterilisasi media dilakukan den-gan autoclave tekanan 1,55 kg f cm-2 selama12 menit.
pertama adalah tanpa dan dengan pemberian kasein hidrolisat (CH) 250 mg l-1 dan faktor kedua adalah konsentrasi 2,4-D dengan empat taraf, yaitu 0, 1, 2, dan 3 mg l-1. Unit percobaan terdiri dari 1 botol kultur yang berisi 1 eksplan tebu yang diulang 8 kali. Penga-matan dilakukan pada umur 2 bulan setelah penana-man eksplan dengan variabel banyaknya kalus yang terbentuk yang ditentukan dengan cara skoring den-gan enam level, yaitu 0 (tidak ada), 1 (sangat sedikit), 2 (sedikit), 3 (sedang), 4 (banyak), dan 5 (sangat ban-yak) seperti yang dicontohkan pada Gambar 1. Proliferasi
Tahap proliferasi kalus dilaksanakan dengan menggunakan rancangan teracak sempurna (RTS) yang disusun secara faktorial 2 x 3. Faktor pertama adalah tanpa dan dengan pemberian kasein hidrolisat (CH) 250 mg l-1 dan faktor kedua adalah konsentrasi 2,4-D dengan tiga taraf, yaitu 1, 2, dan 3 mg l-1. Se-tiap unit percobaan terdiri dari 1 botol kultur yang berisi satu clump kalus per botol, yang diulang 7 kali. Pengamatan dilakukan pada kultur berumu 1 bulan setelah tanam pada media proliferasi, dengan mengu-kur diameter dan bobot kalus yang terbentuk.
Induksi Tunas
Tahap induksi tunas dilaksanakan dengan menggunakan rancangan teracak sempurna (RTS) dengan perlakuan dua taraf konsentrasi BA, yaitu 1 mg l-1 dan 2,5 mg l-1. Setiap unit percobaan terdiri dari 19 botol kultur, yang masing-masing botolnya berisi 1 clump kalus sebagai eksplan. Pengamatan dilakukan pada 2 bulan setelah tanam pada media induksi tunas secara visual dengan menggunakan sistem skor. Skor yang digunakan didasarkan pada banyaknya jumlah tunas yang tumbuh pada kalus (skor 0: tidak tumbuh tunas, skor 1: sedikit, skor 2: sedang, skor 3: banyak, dan skor 4: sangat banyak), seperti yang dicontohkan pada Gambar 2.
A B C
Gambar 1. Penentuan skor pembentukan kalus pada 2
bulan setelah tanam. (A) kalus skor 0, (B) kalus skor 1, (C) kalus skor 2, (D) kalus skor 3, (E) kalus skor 4, dan (F) kalus skor 5
A B C
D E F
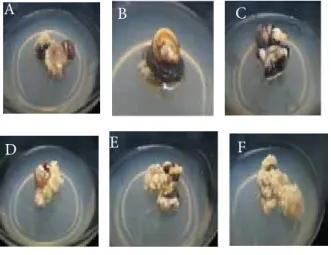
Gambar 2. Penentuan skor pembentukan tunas pada
umur 2 bulan setelah tanam. (A) tunas skor 0, (B) tunas skor 1, (C) tunas skor 2, (D) tunas skor 3, (E) tunas skor 4, dan (F) tunas skor 5
Induksi Kalus
Tahap induksi kalus dilaksanakan dengan menggunakan rancangan teracak sempurna (RTS) dengan yang disusun secara faktorial 2 x 4. Faktor
HASIL DAN PEMBAHASAN Induksi Kalus
Hasil rekapitulasi analisis ragam terhadap ukuran kalus yang terbentuk pada eksplan selama 2 bulan menunjukkan bahwa penambahan 2,4-D pada berbagai konsentrasi dapat mempengaruhi ukuran ka-lus yang terbentuk. Sedangkan pemberian CH tidak mempengaruhi ukuran kalus.
Pengaruh penambahan 2,4-D pada ukuran ka-lus yang terbentuk disajikan dalam Gambar 2 dan Gambar 3. Dari Gambar 2 terlihat bahwa penambah-an 2,4-D pada taraf 3 mg/l menghasilkpenambah-an skor ukurpenambah-an kalus tertinggi (3,75), yang selanjutnya berturut-turut diikuti oleh taraf 2 mg/l (2,94), lalu 1 mg/l (1,63), dan tanpa pemberian 2,4-D (0). Gambar 3 menunjukkan pertumbuhan kalus tanaman tebu dengan pemberian beberapa konsentrasi 2,4-D dengan atau tanpa kasein hidrolisat pada media dasar MS pada umur 6 minggu setelah tanam.
Penambahan kasein hidrosilat tidak berpen-garuh pada proses induksi kalus eksplan tanaman tebu. Hal ini terbukti bahwa semua konsentrasi 2,4-D mampu menginduksi kalus, baik yang diperlaku-kan dengan atau tanpa kasein hidrosilat. Fenomena tersebut dimungkinkan, karena kasein hidrolisat ti-dak mempengaruhi proses pembentukan kalus, tetapi berefek pada proses pembentukan embrio somatik pada kalus tua (setelah proses proliferasi) (Nasir et al., 2011). Selain itu, Shaheen dan Mirza (1989) me-nyatakan bahwa kasein hidrosilat meningkatkan jum-lah tunas yang terbentuk. Hasil yang serupa diperoleh pada penelitian Supriyatdi (2010), yang penelitiannya menunjukkan bahwa pemberian kasen hidrolisat 200 mg/l pada saat induksi kalus meningkatkan jumlah tu-nas rata-rata per eksplan sekitas satu tutu-nas.
Berbeda dengan kasein hidrolisat, penamba-han 2,4-D terbukti mempengaruhi ukuran kalus yang terbentuk. Ukuran kalus yang terbesar dihasilkan oleh perlakuan 3 mg/l 2,4-D dan yang terendah
di-Gambar 3. Pengaruh konsentrasi 2,4-D pada ukuran
ka-lus. Ukuran kalus dinilai dengan skor h(0—5) yang diuraikan dalam metode penelitian. Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasar-kan uji BNT 0,05. 0 mg/l 2,4-D & 0 mg/lCH 1 mg/l 2,4-D & 0 mg/l CH 1 mg/l 2,4-D & 0 mg/l CH 3 mg/l 2,4-D & 0 mg/l CH 0 mg/l 2,4-D & 250 mg/lCH 1 mg/l 2,4-D & 250 mg/l CH 2 mg/l 2,4-D & 250 mg/l CH 3 mg/l 2,4-D & 250 mg/l CH
tunjukkan oleh perlakuan yang tidak menggunakan 2,4-D. Hasil serupa juga diutarakan oleh Ali et al. (2008), yang menyatakan bahwa pemberian konsen-trasi 3 mg/l 2,4-D dapat memberikan hasil terbaik dalam memaksimalkan induksi kalus dan proliferasi kalus yang dihasilkan baik dari eksplan daun segar maupun tunas meristem apikal. Selain itu, George, et al. (2008) menyebutkan bahwa 2,4-D merupakan auksin kuat dengan efektivitas yang tinggi dalam in-duksi kalus.
Proliferasi Kalus
Hasil analisis ragam menunjukkan bahwa penambahan taraf konsentrasi 2,4-D dan CH tidak memberikan pengaruh yang nyata pada variabel di-ameter kalus dan bobot kalus. Tidak terdapat inter-aksi antara konsentrasi 2,4-D dan CH pada setiap variabel yang diamati. Pengaruh konsentrasi 2,4-D dan kasein hidrolisat terhadap proliferasi kalus pada diameter dan bobot kalus disajikan pada Tabel 1. Ber-dasarkan data pada Tabel 1, tidak terlihat perbedaan yang signifikan pada diameter dan bobot kalus yang dihasilkan antara media dengan atau tanpa kasein hi-drolisat.
Berdasarkan data pada Tabel 1 tidak terlihat perbedaan yang signifikan pada diameter dan bobot kalus yang dihasilkan antara media dengan atau tanpa Gambar 4. Penampakan kalus primer pada media
MS dan 2,4-D dengan atau tanpa kasein hidrol-isat pada umur 2 bulan
Tabel 1. Pengaruh Konsentrasi 2,4-D dan Kasein Hidrolisat pada Media Induksi Kalus terhadap Proliferasi Kalus pada Umur 1 Bulan Setelah Tanam
No Media Induksi Kalus Diameter (cm) Bobot (g) 1 Dengan kasein hidrolisat
1 mg/l 2,4-D 1,64 0,83
2 mg/l 2,4-D 1,77 0,98
3 mg/l 2,4-D 1,82 0,98
2 Tanpa kasein hidrolisat
1 mg/l 2,4-D 1,46 0,80
2 mg/l 2,4-D 1,82 0,97
3 mg/l 2,4-D 1,76 0,95
kasein hidrolisat. Kondisi tersebut menunjukkan bah-wa pada proses proliferasi, media tanam asal kalus dikulturkan, yaitu dengan pemberian 2,4-D dengan atau tanpa kasein hidrolisat tidak mempengaruhi be-sar diameter kalus yang beproliferasi. Demikian juga dengan bobot kalus yang dihasilkan tidak dipengaruhi konsentrasi 2,4-D dan kasein hidrolisat. Hasil yang diperoleh tersebut diduga karena jenis media tanam yang digunakan selama proses proliferasi hanya ter-diri dari satu jenis media, yaitu MS dengan pemberian 3 mg/l 2,4-D. Selain itu, ukuran kalus yang digunak-an pada awal proliferasi diseragamkdigunak-an yaitu dengdigunak-an ukuran 0,5—0,8 cm, sehingga mempunyai kisaran ukuran yang relatif sama. Akibatnya respon yang di-hasilkan pada semua perlakuan menjadi relatif sama. Induksi Tunas
Hasil analisis ragam menunjukkan bahwa penambahan BA untuk semua konsentrasi pada media mempengaruhi pembentukan tunas pada clump kalus sebagaimana tersaji pada Gambar 5. Pada Gambar 5 terlihat bahwa rata-rata jumlah tunas yang terben-tuk paling tinggi ditunjukkan pada perlakuan 2,5mg/l BA, yaitu skor 3. Perlakuan 1 mg/l BA menghasil-kan jumlah tunas yang lebih sedikit, yaitu skor 1,77. Pada Gambar 6 dapat dilihat penampilan visual jum-lah tunas yang terbentuk untuk perlakuan 1 mg/l dan 2,5 mg/l BA.
Penambahan BA pada media MS meningkat-kan jumlah tunas yang terbentuk pada clump kalus umur 2 bulan setelah tanam pada media induksi tunas. Jumlah tunas yang dihasilkan per clump kalus dalam skor pada media MS yang ditambah 2,5 mg/l BA meningkat hampir 2 kali lipat dari pemberian 1 mg/l BA, yaitu dari skor 1,77 menjadi skor 3. Fenomena ini sesuai dengan yang didapatkan oleh Behera dan Sahoo (2009), yang melaporkan bahwa persentase eksplan yang membentuk tunas dan jumlah tunas per eksplan, mengalami kenaikan dengan meningkatnya konsentrasi BA dari 0,5—2,5 mg/l, yang selanjutnya mengalami penurunan kembali pada konsentrasi 3—4 mg/l. Febrianie (2008) melaporkan bahwa media MS dengan 2,5 mg/l BA menghasilkan jumlah tunas adventif tebu terbanyak.
Kesamaan pola di atas, diduga karena efek dari BA yang dapat merangsang pembentukan tunas. Sitokinin dalam kegiatan kultur jaringan telah ter-bukti dapat menstimulasi terjadinya pembelahan sel, proliferasi kalus, pembentukan tunas, mendorong proliferasi meristem ujung, menghambat pembentu-kan akar, dan mendorong pembentupembentu-kan klorofil pada kalus (Nuryani, 2006). Ditambahkan oleh George et al. (2008) bahwa induksi tunas dan proliferasi tunas dapat dirangsang dengan hanya menggunakan BA. BA merupakan sitokinin sintetik yang tidak diproduk-si dalam tubuh tanaman dan merupakan analog diproduk- sito-kinin alami yang peranannya sangat penting dalam mengatur pertumbuhan dan morfogenesis eksplan di dalam kultur (Murashige, 1974).
Gambar 5. Pengaruh konsentrasi BA pada jumlah tunas. Jumlah tunas dinilai dengan skor (0—5) yang diuraikan dalam metode penelitian. Nilai yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan uji BNT 0,05.
MSBA1 MSBA2.5
Gambar 6. Penampilan tunas yang terbentuk dari
ka-lus pada media MS yang mengandung benziladenin ( BA) 1 mg/l dan 2,5 mg/l pada umur 2 bulan setelah tanam pada media induksi tunas
KESIMPULAN
Berdasarkan data hasil pengamatan yang telah dikemukakan, dapat disimpulkan sebagai beri-kut: (1) Penambahan 3 mg/l 2,4-D pada media MS menginduksi kalus dengan ukuran tertinggi, (2) Pen-garuh konsentrasi 2,4-D terhadap ukuran kalus yang terbentuk tidak dipengaruhi oleh konsentrasi kasein hidrolisat, (3) Konsentrasi 2,4-D dan penambahan kasein hidrolisat dalam media induksi kalus tidak berpengaruh terhadap diameter dan bobot kalus yang berproliferasi, dan (4) Penambahan 2,5 mg/l BA pada media induksi tunas menghasilkan jumlah tunas ter-banyak.
DAFTAR PUSTAKA
Ali, A., S. Naz, F.A. Siddiqui, and J. Iqbal. 2008. Rapid clonal multiplication of sugarcane (Sac-charum officinarum L.) through callogenesis and organogenesis. Pakistan Journal Botany. 4(1): 123—128.
Behera, K.K. and S. Sahoo. 2009. Rapid In vitro mi-cro propagation of sugarcane (Saccharum of-ficinarum L. cv-Nayana) through callus culture. Nature and Science. 7(4): 1-10.
Farid, M. 2003. Perbanyakan tebu (Saccharum of-ficinarum L.) secara in vitro pada berbagai kon-sentrasi IBA dan BAP. J. Sains & Teknologi. 3(30): 103—109.
Febrianie, A. P. 2008. Pengaruh benziladenin (BA) pada pembentukan tunas dari kalus tebu (Sac-charum officinarum L.) secara in vitro melalui organogenesis. Skripsi. Universitas Lampung. Bandar Lampung.
Gamborg, O.L. and G.C. Phillips. 1995. Plant Cell, Tissue and Organ Culture: Fundamental Meth-ods. Springer Lab Manual. Germany.
George, E.F., M.A. Hall, dan G.J.D. Klerk. 2008. Plant Propagation by Tissue Culture 3rd Edi-tion. Springer. Netherlands.
Julian. 2011. Produksi Gula Jalan di Tempat. http:// www.agroindonesia.co.id. Diakses 26 De-sember 2011.
Khan, I.A., and A. Khatri. 2006. Plant regeneration via organogenesis or somatic embryogenesis in sugarcane: Histological studies. Pak. J. Bot. 38(3): 631—636.
Murashige, T. 1974. Plant propagation through tis-sue culture. Ann. Rev. Plant Physiol. 25: 135—166.
Nasir, I.A., G.Z. Jahangir, Z. Qamar, Z. Rahman, and T. Husnain. 2011. Maintaining the regen-eration potential of sugarcane callus for longer span. African Journal of Agricultural Research. 6(1): 113—119.
Nuryani, I. 2006. Tanggapan pertumbuhan nilam (Pogostemon cablin Benth) terhadap jenis me-dia dasar dan penambahan benzyladenin secara in vitro. Skripsi. Universitas Lampung. Ban-dar Lampung.
Rival, A. dan G.K.A. Parveez. 2005. Elaeis guinen-sis Oil Palm. In: R.E. Litz (ed). Biotechnol-ogy of Fruit and Nut Crops. CABI Publishing. USA. p 113—143.
Shaheen, M.S. and M.S. Mirza. 1989. In vitro pro-duction of plants from sugarcane tissue. Jour-nal of Agric. Sci. 26: 302—312.
Siregar, L.A.M., C. Lai-Keng, dan B. Peng-Lim. 2010. Pengaruh kasein hidrolisat dan intensitas cahaya terhadap produksi biomassa dan alka-loid canthinone di dalam kultur suspensi sel pa-sak bumi (Eurycoma longifolia Jack). Makara Sains. 14(1): 12—21.
Supriyatdi, Dedi. 2010. Respons Eksplan Tebu (Sac -charum officinarum L.) Terhadap 2,4-D dan Kasein Hidrolisat Dalam Proses Induksi Kalus, Induksi Tunas, dan Pengakaran In Vitro. Tesis. Universitas Lampung. Bandar Lampung. Suryana, A., D. H. Goenadi, W. R. Susila,
Nahdo-din, dan H. Malihan. 2005. Prospek dan Arah Pengembangan Agribisnis Tebu. Badan Peneli-tian dan Pengembangan Pertanian Departemen Pertanian.
Trigiano, R.N. and D.J. Gray. 2010. Plant Tissue Culture, Development, and Biotechnology. CRC Press. Florida.
Yakub, M. 2011. Pabrik Gula Berkapasitas 10 Ribu Ton Dibangun di Lamongan. http: MediaIndo-nesia.com. Diakses pada tanggal 17 Juni 2011. Yusnita. 2003. Kultur Jaringan Cara Memperbanyak
Tanaman Secara Efisien. AgroMedia Pusta-ka. Jakarta.