BAB II
TINJAUAN PUSTAKA
2.1 Kaprolaktam
Kaprolaktam telah dikenal sejak abad ke-19. S.Gabriel dan T.A.Mass pertama kali mensintesis kaprolaktam pada tahun 1899 dengan proses siklis. O.Wallach mensintesis kaprolaktam dengan proses penyusunan Beckmann (Beckmann rearrangement) menggunakan senyawa sikloheksanon oksim. Produksi secara komersial meningkat mulai tahun 1938, ketika P.Schlack dari IG
Farbenindustrie memproduksi polimer siklis pertama dari proses polikondensasi kaprolaktam.
Sejak saat itu, kaprolaktam semakin dibutuhkan. Produksi skala industri meningkat drastis. Pada tahun 1989, produksi kaprolaktam dunia mencapai 2 x 106 ton dan pada tahun 1994 meningkat menjadi 2,2 x 106 ton ( Ullmann‟s, 2005).
Kaprolaktam (C6H11NO) atau dikenal dengan nama amino caproic lactam adalah senyawa kimia yang larut dalam air, toluena, sikloheksanol, sikloheksanon, metil etil keton, etil asetat, dan p-xilena. Kaprolaktam biasanya tersedia dalam bentuk bulat, serpihan ataupun kristal.
Kaprolaktam juga merupakan senyawa organik dengan kenampakan padatan yang memiliki titik leleh 69,30C dan titik didih 2700C serta bersifat higroskopis. Kaprolaktam merupakan salah satu produk industri petrokimia yang saat ini semakin dibutuhkan, khususnya dalam subsektor pertekstilan sebagai bahan baku nylon-6. Selain sebagai bahan baku nylon-6, kaprolaktam juga diperlukan dalam industri plastik, film, kulit imitasi, serat sintetis, plastisizer, dan cat mobil. Kegunaan lainnya sebagai ikatan silang pada poliurethane dan salah satu bahan baku untuk mensintesa asam amino lisin (Kirk-Othmer, 1967).
Mengingat banyaknya penggunaan produk kaprolaktam pada dunia industri, maka secara otomatis keperluannya akan semakin meningkat seiring dengan meningkatnya jumlah pemakaian produk dari industri-industri pengguna kaprolaktam (Nasmiarti, 2011).
2.2 Spesifikasi Bahan Baku dan Produk
2.2.1 Bahan Baku
A. Toluena ( C6H5CH3 ) Wujud : cair
Kenampakan : jernih tidak berwarna Bau : aromatis
Berat molekul : 92 gr/mol Titik didih : 1110C
Densitas : 0,876 gr / cm3 (250C, 1 atm) Viskositas : 0,548 mPa.s (cP) Panas penguapan : 33,59 kJ/mol Komposisi
Toluena : minimal 98% berat Benzena : maksimal 2% berat
(www.temarry.com)
B. Asam Nitrosilsulfur ( NOHSO4 )
Wujud : cair
Berat molekul : 127 gr/mol Warna : kekuning-kuningan Titik didih : 101,20C (1 atm) Specific Gravity : 1,890 – 1,895 Komposisi
Asam nitrosilsulfur : minimal 90% berat Air : maksimal 10% berat
(www.chemicalland21.com)
C. Hidrogen ( H2 ) Wujud : gas
Kenampakan : tidak berwarna Komposisi
H2 : minimal 90,52% mol
Ar : maksimal 2,16% mol N2 : maksimal 7,32% mol (www.airliquideindoneia.com) D. Udara Wujud : gas
Berat molekul : 29 gr/mol Komposisi Nitrogen : 79% mol Oksigen : 21% mol Partikulat : 1 mg/Nm3 (Perry&Green, 1999) E. Air (H2O) Wujud : cair
Berat molekul : 18 gr/mol Titik didih : 1000C (1 atm)
Densitas : 0,997 g/cm3 (250C, 1 atm) Titik beku : 00C
Latent heat of melting : 334 kJ/kg
Panas penguapan : 2,270 kJ/kg Temperatur kritis : 380 oC - 386 oC (www.engineeringtoolbox.com) 2.2.2 Bahan Pendukung A. Amonia (NH3)
Wujud : gas ( 250C, 1 atm) Berat molekul : 17 gr/mol Kenampakan : tak berwarna Bau : khas
Densitas ( 1 atm, 79oC ) : 0,817 gr / cm3
Komposisi NH3 : minimal 99,5% berat H2O : maksimal 0,5% berat (www.pupukkujang.com) B. Katalis Oleum ( H2S2O7 ) Wujud : cair-berasap
Kenampakan : jernih hingga kecoklatan Bau : khas
Berat molekul : 178 gr/mol
Densitas : 1,956 gr/cm3 (300C, 1 atm) 1,930 gr/cm3 (400C, 1 atm) Titik didih : 138oC Komposisi H2SO4 : 65% berat SO3 : 35% berat (www.alibaba.com) C. Katalis Paladium Wujud : padat Bentuk : serbuk
Kenampakan : putih keperakan Titik leleh : 15550C Densitas : 12,023 gr /cm3 (200C, 1 atm) Komposisi Paladium : 10% berat Charcoal : 90% berat (www.chemfinder.com)
D. Katalis Cobalt Naftenat
Wujud : padat Bentuk : serbuk
Kenampakan : perak Ukuran : diameter 0,25 mm Bau : khas Titik leleh : 14800C Densitas : 8,9 gr/cm3 (200C, 1 atm) Komposisi : 98% kobalt (www.alibaba.com) 2.2.3 Produk 2.2.3.1 Produk Utama Kaprolaktam ( NH(CH2)5CO ) Wujud : padat Bentuk : kristal Kenampakan : putih Berat molekul : 113 gr/mol Ukuran : 20-25 mesh Bau : khas
Titik leleh & titik didih : 690C & 2700C Densitas (cairan) : 0,9983 gr/cm3 (1000C) Viskositas : 8,82 mPa.s (800C)
Panas penguapan : 628 kJ/kg (1050C) Komposisi
Kaprolaktam : minimal 99,5% berat H2O : maksimal 0,3% berat Asam sulfat : maksiml 0,2% berat
(www.honeywell.com) 2.2.3.2 Produk Samping A. Amonium sulfat (NH4)2SO4 Wujud : padat Bentuk : kristal
Berat molekul : 132,14 gr/mol
Kenampakan : putih Bau : khas
Titik leleh : 2350C
Densitas : 1,769 kg / liter (200C, 1 atm) Komposisi
(NH4)2SO4 : minimal 98,5% berat H2O : maksimal 0,8% berat Asam sulfat : maksimal 0,7% berat
(www.wikipedia.com)
B. Benzaldehida (C6H5CHO) Wujud : cair
Berat molekul : 106 gr/mol Titik didih : 1790C (760 mm Hg) 112,50C (100 mm Hg)
Titik beku : -260C (-150F)
Specific Gravity : 1,046
Kelarutannya : 0,6% (benzaldehida dalam air) 1,5% (air dalam benzaldehida)
Panas penguapan : 42,13 kJ/mol Viskositas : 1,4 cp (250C) Tekanan uap : 10 mm Hg (620C) 60 mm Hg (99,60C) 100 mm Hg (112,50C) 400 mmHg (154,10C) (www.emeraldkalamachemical.com) 2.2.3.3 Produk Antara
A. Asam Benzoat (C6H5COOH)
Massa Molar : 122 gr/mol
Temperatur didih pada 1 atm : 249,2oC Densitas : Padat : 1,316 gr/cm3
Cair : 1,029 gr/cm3
Temperatur kritis : 751oK
Viskositas (130oC) : 1,26 mPa.s (cP) Panas penguapan pada 140oC : 534 J/g
pH pada larutan jenuh, 25oC : 2,8 (Kirk & Othmer, 1989)
B. Asam Sikloheksana Karbosilat / CHCA (C6H11COOH)
Berat molekul : 128 gr/mol
Densitas : 1,079 g/cm3 Titik lebur : 30-32℃
Titik didih : 233°C (760 mmHg) Indeks bias : 1,48
Kelarutan dalam air : 0,201 g/100 mL (15℃)
(www.chemicaldatabase.com)
C. Asam Sulfat (H2SO4) Wujud : cair
Berat molekul : 98 gr/mol Densitas : 1,76 gr/mol (1000C) Titik didih : 279,60C
Viskositas : 6 cP (800C)
Panas penguapan : 650 kJ/kg (279,60C) Kelarutan dalam air : sangat baik (Kirk & Othmer, 1989)
2.3 Proses Pembuatan Kaprolaktam
Kaprolaktam dapat dibuat dengan proses dan bahan baku yang berbeda-beda. Jenis proses dan bahan baku pembuatan kaprolaktam menentukan tahapan proses yang diperlukan dan biaya produksi yang harus dikeluarkan. Adapun beberapa metode produksi / proses pembuatan kaprolaktam ditunjukkan oleh Gambar 1 di bawah ini:
SikloheksanaFenolSikloheksanolSikloheksanonSikloheksanon oksimKaprolaktonToluenaAsam benzoatAsam sikloheksana karboksilatKaprolaktamMetode 1Metode IIMetode III
Gambar 2.1. Produksi Kaprolaktam dengan Berbagai Metode
Adapun perbedaan dari beberapa metode proses produksi kaprolaktam di atas adalah sebagai berikut.
a. Proses Menggunakan Sikloheksana
Proses ini terdiri atas 2 tahap di mana tahap pertama sikloheksana dioksidasi dalam campuran sikloheksanon / sikloheksanol lalu dihidrogenasi. Sikloheksanon yang dihasilkan diubah menjadi oksida dan laktam yang sama dengan proses fenol.
Katalis yang digunakan adalah seng yang merupakan logam. b. Proses Menggunakan Fenol
Prosesnya ada 3 tahap, di mana tahap pertama fenol dihidrogenasi menjadi sikloheksanol dengan suatu katalisator nikel, alkohol yang dibentuk dihidrogenasi kembali menjadi sikloheksanon, dan kemudian membentuk kaprolaktam dengan penyusunan Beckmann.
Katalis yang digunakan adalah natrium hidroksida (NaOH) yang merupakan senyawa basa. Melibatkan sikloheksanon sebagai bahan utama proses pembuatan kaprolaktam.
c. Proses Menggunakan Toluena
Tidak melibatkan sikloheksana sebagai bahan utama dalam pembuatan kaprolaktam. Ada 3 langkah yang harus ditempuh dalam pembuatan kaprolaktam :
1. Pembuatan asam benzoat melalui proses oksidasi toluena.
2. Proses hidrogenasi asam benzoat menjadi asam sikloheksana karboksilat. 3. Mengkonversi asam sikloheksana karboksilat menjadi kaprolaktam.
Berdasarkan jenis-jenis metode pembuatan kaprolaktam di atas, maka ada beberapa proses yang dikembangkan dalam rangka pembuatan kaprolaktam dalam skala pabrik komersial. Adapun beberapa proses yang telah dikembangkan dan digunakan sampai saat ini adalah sebagai berikut:
1. Allied Chemical Phenol Process
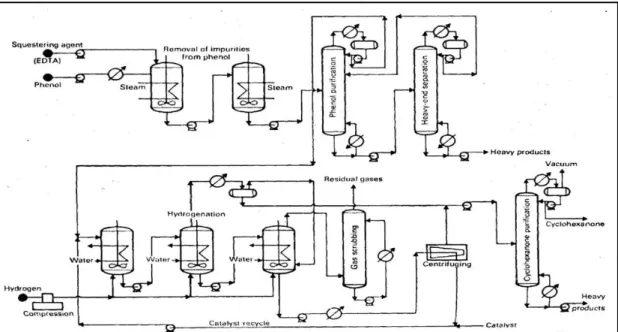
Pembuatan kaprolaktam dengan proses ini menggunakan bahan baku sikloheksanon dan fenol, dengan katalis paladium dan karbon. Proses ini digunakan oleh Allied Chemical Corporation di Amerika sejak tahun 1954. Pada proses ini fenol dihidrogenasi secara endotermis membentuk sikloheksanol dan sikloheksanon dalam jumlah kecil. Reaksi berlangsung pada 250°C-375°C dan tekanan 300-450 psig, dilakukan dalam reaktor seri dengan penambahan katalis paladium dan karbon. Efluen dari reaktor setelah mengalami filtrasi untuk pengembalian kembali katalis, dimasukkan pada menara destilasi untuk membuang fenol yang tidak bereaksi dengan cara mendaur ulang ke dalam reaktor. Campuran sikloheksanol dan sikloheksanon dipisahkan dengan cara distilasi. Sikloheksanol kemudian direaksikan dengan hidroksilamin sulfat dan amonia membentuk sikloheksanon oksim. Langkah berikutnya adalah proses pembentukan kaprolaktam sesuai dengan penyusunan Beckmann yaitu mereaksikan sikloheksanon oksim dengan oleum, yang kemudian dipisahkan dari reaksi dengan netraliser menggunakan larutan amonia dan larutan solvent. Kristal yang terbentuk kemudian dilelehkan serta dikeringkan dalam flash dryer. Hasil bawah ekstraktor berupa larutan amonium sulfat dan diproses lebih lanjut, sedangkan keluaran bawah solvent stripper diumpankan pada kristaliser
untuk kemudian diproses lebih lanjut menjadi produk akhir kaprolaktam. Adapun flowsheet pembuatan kaprolaktam ini ditunjukkan oleh Gambar 2 di bawah ini.
Gambar 2.2 Produksi Kaprolaktam dari Fenol dengan Allied Chemical Pheno Process
2. Toyo Rayon Photonitrosation
Pembuatan kaprolaktam dengan proses ini menggunakan bahan baku sikloheksana, amonia dengan katalis Pt-Rh. Proses ini dikembangkan oleh Toyo Rayon Co. dari Jepang. Proses
fotonisasi ini secara keseluruhan ditujukan untuk mengubah sikloheksana menjadi sikloheksanon oksim. Amonia dioksidasi dengan katalis Pt-Rh dalam sintesis asam nitrat normal, tetapi produk gas dari scrubber dengan asam sulfat menjadi nitrosilsulfat. HCl kemudian ditambahkan dalam larutan nitrosil sulfat membentuk gas nitrosilklorida dan asam sulfat. Sinar UV disini berfungsi sebagai penyuplai energi untuk reaksi nitrosil klorida menjadi sikloheksanon oksim hidroklorida, kemudian diubah menjadi kaprolaktam dengan penyusunan Beckmann, proses ini beroperasi pada kondisi operasi 1200C dan tekanan 1-2 atmosfir (Nasmiarti, 2011).
3. Proses Sosieta Nazionale Industria Applicazioni-Viscosa (Snia-Viscosa)
Pembuatan kaprolaktam dengan proses ini menggunakan bahan baku toluena dengan katalis cobalt, paladium dan oleum. Toluena dioksidasi dengan udara dalam fasa cair menggunakan katalis cobalt pada suhu 1600C-1700C dan tekanan 8-10 atm
dengan reaktor tunggal. Dilanjutkan dengan hidrogenasi asam benzoat menjadi asam sikloheksana karboksilat menggunakan katalis slurry paladium. Asam sikloheksana karboksilat selanjutnya direaksikan dengan asam nitrosil sulfat menghasilkan kaprolaktam sulfat yang kemudian dinetralisasi dengan amonia menghasilkan kaprolaktam dan produk samping amonium sulfat (Nasmiarti, 2011).
2.4 Pemilihan Proses
Pada pra perancangan pabrik pembuatan kaprolaktam, proses yang dipilih adalah Sosieta
Nasionale Industri Applicazioni – Viscosa (Snia-Viscosa). Adapun pemilihan proses ini dilakukan
adalah berdasarkan pertimbangan sebagai berikut.
- Konversinya lebih besar dibandingkan dengan proses lain.
- Bahan baku (toluena) yang digunakan lebih murah dibandingkan dengan bahan baku proses lain. - Tidak melibatkan senyawa sikloheksana sebagai bahan utama.
(Nasmiarti, 2011)
2.5 Deskripsi Proses Pembuatan Kaprolaktam
Pada tahun 1960, Sosieta Nasionale Industri Applicazioni – Viscosa (Snia-Viscosa) dari Italia menemukan cara alternatif dalam memproduksi kaprolaktam, yang memiliki kelebihan yaitu harga bahan baku toluena yang lebih murah dibandingkan dengan benzena yang merupakan bahan dasar pembuatan fenol dan sikloheksana. Pembuatan kaprolaktam dari bahan baku toluena dengan proses Snia-Viscosa didasarkan pada reaksi oksidasi toluena, hidrogenasi asam benzoat dan reaksi pembentukan kaprolaktam melalui reaksi nitrosasi dekarboksilasi dari cyclohexane carboxylic
acid.
Tahap pertama adalah reaksi oksidasi toluena dengan udara yang berlangsung pada fase cair-gas akan menghasilkan asam benzoat. Reaksi ini merupakan reaksi irreversibel eksotermis.
Selanjutnya pada tahap kedua asam benzoat yang terbentuk di hidrogenasi dengan gas hidrogen sehingga dihasilkan cyclohexane carboxylic acid (CHCA). Reaksi ini bersifat eksotermis irreversibel dan berlangsung pada fase cair-gas.
Pada tahap ketiga, kaprolaktam terbentuk dari hasil reaksi nitrosasi dekarboksilasi CHCA dengan asam nitrosilsulfur pada fase cair. Reaksi ini juga bersifat eksotermis irreversibel.
Berikut adalah persamaan reaksi pembentukan kaprolaktam dari toluena dengan proses Snia – Viscosa :
Reaksi oksidasi toluena akan menghasilkan asam benzoat menurut reaksi berikut:
Reaksi utama
C6H5CH3(l) + 3/2 O2(g) C6H5COOH(l) + H2O(l)
toluena asam benzoat
Reaksi samping
C6H5CH3(l) + O2(g) C6H5CHO(l) + H2O(l) benzaldehida
Reaksi hidrogenasi asam benzoat akan menghasilkan Cyclohexane Carboxylic Acid (CHCA)
menurut reaksi berikut :
C6H5COOH(l) + 3H2 (g) C6H11COOH (l)
asam benzoat hidrogen CHCA
Pembentukan kaprolaktam berdasarkan pada reaksi nitrosasi dekarboksilasi dari asam
sikloheksana karbosiklat atau cyclohexane carboxylic acid.
C6H11COOH (l) + NOHSO4 (l) C6H11ON.H2SO4 (l) + CO2 (g)
CHCA asam nitrosilsulfur kaprolaktam sulfat karbondioksida
Reaksi oksidasi toluena menjadi asam benzoat dilakukan di dalam bubbling reactor yang berlangsung pada kondisi isotermal 1600C dan tekanan 10 atm. Konversi toluena yang dihasilkan sebesar 30% dengan selektifitas asam benzoat sebesar 90%. Untuk mempercepat terjadinya reaksi oksidasi toluena menjadi asam benzoat digunakan katalis cobalt yang berbentuk serbuk.
Reaksi hidrogenasi asam benzoat menjadi CHCA juga dilakukan dalam bubbling reaktor yang berlangsung pada kondisi suhu 1700C dan tekanan 16 atm menggunakan katalis paladium dengan perbandingan mol asam benzoat dan hidrogen sesuai dengan koefisien reaksi yaitu 1: 3. Pada suhu 1700C dan tekanan 16 atm konversi mendekati sempurna (Chauvel dkk., 1989).
Reaksi nitrosasi CHCA menjadi kaprolaktam dilakukan dalam reaktor CSTR. Reaksi
berlangsung dalam fase cair pada suhu 800C dan tekanan 1 atm di mana perbandingan mol CHCA yang diberikan 25% berlebih dan NOHSO4 menjadi reaktan pembatas. CHCA dibuat berlebih dengan tujuan supaya reaktan pembatas tepat bereaksi sempurna. Pada suhu 800C dan tekanan 1 atm konversi yang diperoleh sebesar 50%. Pada reaksi nitrosasi, asam sikloheksana karbosiklat (CHCA) digunakan katalis berbentuk cair, yaitu oleum dengan komponen H2SO4 65% dan SO3 35% berat (Ullmann, 2005).
2.6 Langkah Proses
Proses pembuatan kaprolaktam dari toluena dengan menggunakan proses Snia – Viscosa terdiri dari 4 langkah proses, yaitu :
1. Penyiapan bahan baku 2. Pembentukan produk 3. Pemurnian produk 4. Penyimpanan produk
Berikut adalah penjelasan dari tiap langkah proses pembuatan kaprolaktam dari toluena dengan menggunakan proses Sosieta Nasionale Industri Applicazioni – Viscosa (Snia-Viscosa) :
1. Tahap Penyiapan Bahan Baku
Pembentukan Asam Benzoat
1. Mencampur toluena dari tangki penyimpan (TT-101) dengan sisa reaktan hasil pemisahan produk keluar menara destilasi 2 (T-101) pada mixer (M-101).
2. Memanaskan campuran dari suhu 300C sampai 1600C dengan menggunakan heater (E-101). 3. Memisahkan partikulat padat dari udara dengan melewatkan udara pada filter (P-101) 4. Mendinginkan udara tersebut dengan menggunakan cooler sampai 1600C (E-102)
5. Mereaksikan toluena dengan udara pada suhu 1600C dan tekanan 10 atm dalam bubbling
reactor (R-101)
6. Mempertahankan kondisi reaksi pada suhu 1600C dan tekanan 10 atm.
Bahan baku toluena dari tangki dicampur dengan sisa reaktan hasil pemisahan produk keluar menara destilasi 2 (T-102) di dalam mixer (M-101). Kemudian campuran pada kondisi kamar dialirkan ke dalam reaktor 1 (R-101) dengan menggunakan pompa sehingga tekanannya naik menjadi 10 atm. Katalis cobalt naftenat masuk ke dalam reaktor bersama-sama dengan aliran campuran.
Sebagai oksidator, udara dari lingkungan dipisahkan dari partikel padatnya dengan menggunakan filter (FG-101). Udara yang telah bersih tersebut dialirkan ke dalam reaktor 1 (R-101) dengan menggunakan kompresor (JC-101). Kemudian udara dilewatkan ke dalam pendingin (E-102) sehingga suhunya turun menjadi 1600C agar sesuai dengan kondisi reaksi.
Di dalam reaktor 1 (R-101) terjadi reaksi oksidasi toluena oleh oksigen dari udara menjadi asam benzoat. Pada reaksi ini terbentuk produk samping berupa benzaldehida dan air. Oleh karena reaksi tersebut merupakan reaksi eksotermis, maka akan dihasilkan sejumlah panas hasil reaksi. Untuk menjaga operasi reaktor 1 (R-101) pada kondisi isotermal maka panas yang timbul diserap dengan menggunakan air yang dilewatkan ke dalam koil.
Keluaran reaktor 1 (R-101) terdiri dari produk asam benzoat, katalis, sisa reaktan berupa toluena dan benzena, serta hasil samping yang berupa benzaldehida dan air. Katalis dipisahkan dengan menggunakan filter (P-101).
Pemisahan semua air dan benzena dari asam benzoat dan reaktan yang tidak bereaksi dilakukan dengan destilasi pada menara destilasi 1 (T-101). Produk atas keluaran menara destilasi 1(T-101) terdiri dari semua benzena, air dan sedikit toluena, sedangkan hasil bawahnya berupa toluena, benzaldehida, dan asam benzoat.
Uap keluar puncak menara destilasi 1 (T-101) diembunkan pada kondensor dan hasilnya
ditampung sementara di akumulator untuk kemudian diumpankan kembali ke menara destilasi 1 (T-101) sebagai refluks. Cairan keluar dasar menara destilasi 1 (T-101) yang terdiri dari toluena, benzaldehida, dan asam benzoat kemudian dipompa sehingga masuk menara destilasi 2 (T-102). Hasil atas dari menara destilasi 2 (T-102) terdiri dari semua toluena serta sedikit benzaldehida. Hasil atas puncak menara destilasi 2 (T-102) kemudian dikembalikan ke tangki pencampuran 1 (M-101).
Hasil bawah dari menara destilasi 2 (T-102) berupa asam benzoat dan benzaldehida dialirkan dengan menggunakan pompa menuju ke menara destilasi 3 (T-103). Hasil atas destilasi 3 (T-103) terdiri dari semua benzaldehida dan sedikit asam benzoat. Sedangkan hasil bawah terdiri dari asam benzoat. Asam benzoat kemudian dialirkan dengan menggunakan pompa menuju reaktor 2 (R-201) yang sebelumnya didinginkan di dalam pendingin (E-201) sampai suhu 1700C.
Pembentukan Cyclohexane Carboxylic Acid (CHCA) 1. Mendinginkan larutan asam benzoat sampai 1700C. 2. Memanaskan gas hidrogen sampai suhu 1700C.
3. Mereaksikan asam benzoat dengan gas hidrogen pada suhu 1700C dan tekanan 16 atm. 4. Mempertahankan kondisi reaksi pada suhu 1700C dan tekanan 16 atm.
Larutan asam benzoat dialirkan ke dalam reaktor 2 (R-201) dengan menggunakan pompa sehingga tekanannya naik menjadi 16 atm. Sebelum masuk ke dalam reaktor 2 (R-201) larutan tersebut didinginkan suhunya menjadi 1700C dengan cara dilewatkan ke dalam pendingin (E-201). Dengan demikian larutan asam benzoat siap untuk direaksikan dalam reaktor sesuai dengan kondisi operasi yang diinginkan.
Gas hidrogen dialirkan ke dalam reaktor dengan menggunakan kompresor sehingga tekanannya naik menjadi 16 atm. Kemudian dilewatkan ke dalam heater (E-202) sehingga suhunya naik menjadi 1700C agar sesuai dengan kondisi reaksi.
Reaksi hidrogenasi asam benzoat ini merupakan reaksi eksotermis maka akan dihasilkan sejumlah panas. Untuk menjaga operasi reaktor pada kondisi isotermal maka panas hasil reaksi tersebut diserap menggunakan pendingin yang dilewatkan dalam koil.
Keluaran reaktor 2 (R-201) terdiri dari produk cyclohexane carboxylic acid (CHCA) dan katalis paladium. Katalis dipisahkan dari produk dengan menggunakan filter (P-201), sedangkan CHCA diumpankan ke reaktor CSTR (R-301)
2. Tahap pembentukan produk
Pembentukan Kaprolaktam Tahap ini dimaksudkan untuk :
1. Mereaksikan CHCA, oleum dan asam nitrosilsulfur pada reaktor tangki berpengaduk (CSTR) pada suhu 800C dan tekanan 1 atm.
2. Mempertahankan suhu operasi reaktor pada suhu 800C dan tekanan 1 atm.
Bahan yang diperlukan untuk pembentukan kaprolaktam adalah CHCA, oleum dan asam nitrosilsulfur. CHCA sebagai produk reaktor kedua diumpankan ke dalam reaktor CSTR pada suhu 800C dan tekanan 1 atm. Oleum dari tangki (TT-301) dan asam nitrosilsulfur dari tangki (TT-302) dialirkan ke dalam reaktor dengan menggunakan pompa di mana masing-masing mengalami pemanasan terlebih dahulu di dalam heater (E-303) sebelum masuk ke reaktor hingga suhunya mencapai 800C.
Di dalam reaktor 3 (R-301) terjadi reaksi nitrosasi. Oleh karena reaksi tersebut merupakan reaksi eksotermis maka dihasilkan panas sehingga diperlukan pendingin berupa air yang dialirkan melalui jaket pendingin untuk menyerap panas hasil reaksi tersebut.
3. Tahap pemurnian produk
Tahapan ini dimaksudkan untuk :
1. Memisahkan produk kaprolaktam dari asam sulfat dan CHCA.
2. Menetralkan asam sulfat dengan amonia menjadi amonium sulfat dalam reaktor netralisasi (R-302).
Produk keluar dari reaktor 3 (R-301) dicampur dengan air di dalam tangki pencampur (M-301). Fungsi dari penambahan air adalah untuk melarutkan kaprolaktam. Kelarutan kaprolaktam dalam air sangat besar bila dibandingkan dengan kelarutan CHCA dalam air sehingga pemisahan produk dari CHCA yang tidak bereaksi dapat dilakukan.
Larutan keluar dari tangki pencampur pencampur (M-301 diumpankan ke dalam dekanter
(FL-301) untuk memisahkan CHCA dengan kaprolaktam sulfat dan air. Larutan terpisah menjadi 2 bagian di mana pada bagian atas terdiri dari CHCA dan pada bagian bawah terdiri dari
kaprolaktam sulfat yang larut dalam air. CHCA
yang terpisah kemudian diumpankan kembali ke dalam reaktor ketiga (R-301) sebagai recycle. Pemurnian kaprolaktam dilakukan dengan menggunakan amonia. Amonia akan mengikat sulfat yang ada dalam kaprolaktam sehingga akan dihasilkan produk samping berupa amonium sulfat. Pemisahan produk samping ini dilakukan dalam reaktor netralisasi (R-302) di mana akan dihasilkan kristal amonium sulfat.
Campuran kaprolaktam sulfat dan air dialirkan dengan pompa dan didinginkan dengan
menggunakan pendingin kemudian diumpankan ke dalam reaktor netralisasi / saturator kristaliser (R-302) Sementara itu, amonia cair dari tangki (TT-303) pada suhu 300C dan tekanan 11,6 atm diubah fasenya menjadi fase gas dengan menggunakan vaporiser (E-304) dan kemudian
diekspansi lalu dipanaskan menggunakan heater (E-306) dan selanjutnya diumpankan secara bersamaan dengan larutan kaprolaktam sulfat ke dalam reaktor netralisasi (R-302) untuk menetralkan kandungan asam sulfat pada kaprolaktam.
Produk keluar dari reaktor kristalisasi (R-302) dipisahkan antara kristal amonium sulfat yang terbentuk dan larutan kaprolaktam dengan menggunakan filter (P-301). Larutan kaprolaktam lalu diumpankan ke dalam evaporator (FE-301) untuk dipekatkan, selanjutnya diumpankan ke dalam
spray dryer (SR-301).
4. Penyimpanan produk
Kaprolaktam dalam bentuk butiran dari spray dryer (SR-301) masuk ke dalam belt conveyor (C-301) dan kemudian diangkut dengan bucket elevator (C-302) masuk ke dalam bin untuk disimpan sebelum masuk ke unit packing.