METODOLOGI PENELITIAN Waktu Dan Tempat Penelitian
Penelitian dilaksanakan mulai bulan Juni 2010 sampai dengan Februari 2011 bertempat di Laboratorium Kimia SEAFAST Center IPB dan Laboratorium Kimia Pangan Departemen Ilmu dan Teknologi Pangan (ITP), IPB .
Bahan Dan Alat
Bahan baku untuk sintesis monolaurin adalah asam lemak laurat teknis komersial, gliserol, enzim lipase Novozyme® 435 dari Novozymes A/S (Bagsvaerd, Denmark), standar monolaurin dari Sigma, heksan teknis, dan tert-butanol p.a (Sigma). Bahan kimia yang digunakan (NA2S2O3
Alat-alat yang digunakan dalam penellitian ini adalah rangkaian reaktor
packed bed yang dilengkapi dengan tangki stok, pompa peristaltik (BT 100-1 F),
waterbath (Stephen Haake, Germany) serta wadah penampung produk, serangkaian peralatan GC (Gas Chromatography) dengan detektor FID (Flame
Ionization Detector), GC-MS Pyrolisis, neraca analitik, Aw-meter (Shibaura
WA-360), pH meter, kertas saring dan peralatan gelas.
) 0.1N, larutan Wijs, larutan Alkohol 95%, indikator PP dan pati, Larutan NaOH 0.01N, larutan kloroform, Dimetil formamida (DMF), benzena, dan aquades.
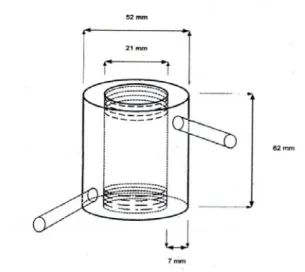
Reaktor packed bed yang digunakan dalam penelitian ini dibuat sesuai dengan disain pada Gambar 10. Reaktor dibuat dari bahan gelas dan dibuat berjaket untuk sirkulasi air dari waterbath, sehingga suhu reaktor dapat dipertahankan. Reaktor juga dilengkapi dengan filter pada bagian atas dan bawah untuk memisahkan antara enzim dan substrat. Tinggi reaktor 62 mm, diameter luar 52 mm, diameter dalam 21 mm dan volume kosong 16,5 mililiter. Volume kerja reaktor 15 mililiter setelah diisi enzim novozyme sebanyak 4,6 gram. Volume kerja reaktor ditentukan dengan cara menghitung waktu yang diperlukan oleh substrat dengan laju aliran tertentu untuk mengalir melalui reaktor packed bed yang berisi enzim novozyme. Hasil perkalian antara waktu untuk mengalir melalui reaktor dengan laju aliran substrat merupakan volume kerja reaktor.
Gambar 10 Desain reaktor
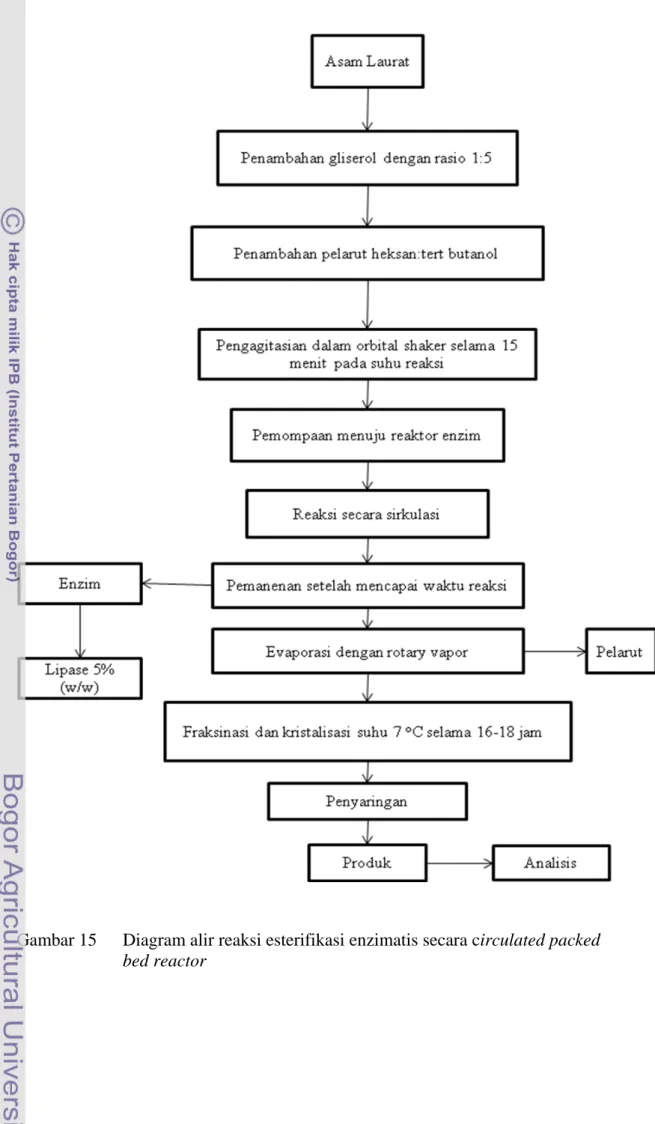
Skema proses produksi MAG secara circulated packed bed reactor dapat dilihat pada Gambar 12. Rangkaian alat esterifikasi enzimatis menggunakan reaktor packed bed dapat dilihat pada Gambar 11 dimana substrat dari wadah reaktan (B) dialirkan dengan laju tertentu ke dalam reaktor packed bed yang berisi enzim lipase (A) menggunakan pompa peristaltik(E). Produk yang dihasilkan ditampung dalam wadah produk (C).
Keterangan : A. Reaktor Enzim B. Wadah Reaktan C.Wadah Produk D. Waterbath
E. Pompa Peristaltik
Gambar 11 Rangkaian alat reaksi esterifikasi menggunakan Reaktor Packed
Bed (Soekopitojo, 2003)
Gambar 12 Skema alur reaksi esterifikasi enzimatis circulated packed bed
reactor
Metode Penelitian
Analisis Sifat Kimia Bahan Baku
Asam laurat dan enzim yang digunakan dalam proses esterifikasi dianalisis terlebih dahulu untuk menentukan kualitas bahan baku. Analisis yang dilakukan meliputi kadar air, asam lemak bebas (ALB), dan bilangan peroksida. Enzim dilakukan karakterisasi terlebih dahulu dengan dilakukan pengukuran pH dan Aw enzim.
Uji Coba Reaksi Sintesis Monolaurin Secara Batch
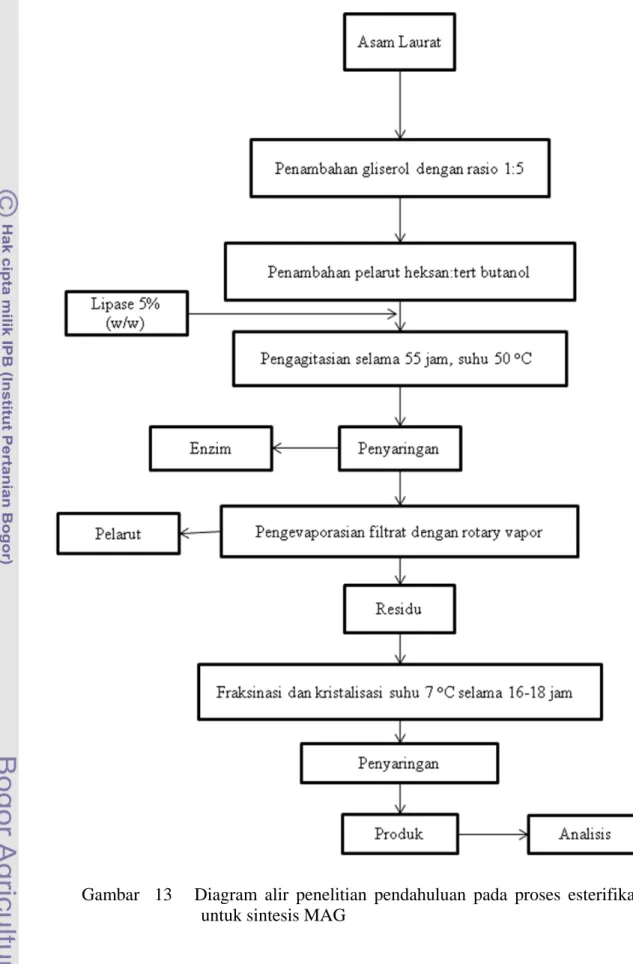
Uji coba hasil penelitian mengacu pada metode penelitian terdahulu. Proses esterifikasi dilakukan dengan mereaksikan substrat yaitu asam lemak laurat dan gliserol (Gambar 12). Asam lemak laurat dan gliserol direaksikan dalam tabung erlenmeyer sebanyak 1 : 5 (mol/mol substrat), ditambah campuran pelarut organik, kemudian diagitasi menggunakan orbital shaker dengan kecepatan 200 rpm. Reaksi dilakukan pada suhu 50o
Setelah suhu reaksi yang diinginkan dalam rotary shaker tercapai, ditambahkan enzim lipase dengan perbandingan 5% (w/w minyak). Reaksi dibiarkan berjalan hingga 55 jam. Kemudian produk dari enzim dipisahkan dengan cara disaring, kemudian filtrat disentrifuse untuk memisahkan dari pelarut. Setelah itu di fraksinasi 16-18 jam pada suhu 7
C.
o
C. Endapan yang merupakan produk hasil fraksinasi dipisahkan dengan cara penyaringan.
Gambar 13 Diagram alir penelitian pendahuluan pada proses esterifikasi untuk sintesis MAG
Optimasi dan Verifikasi Reaksi Esterifikasi untuk Sintesis Monoasilgliserol dalam Circulated Packed Bed Reactor
Konversi Reaksi Esterifikasi Proses Batch ke Circulated Packed Bed Reactor Sebelum dilakukan optimasi reaksi, terlebih dahulu dilakukan konversi dari proses batch ke proses circulated packed bed reactor. Hasil dari proses batch dipilih yang memiliki hasil dengan kadar MAG dan rendemen tertinggi, serta rasio substrat dan pelarut yang efektif untuk dilakukan proses secara circulated
packed bed reactor.
Optimasi Reaksi Esterifikasi Circulated Packed Bed Reactor
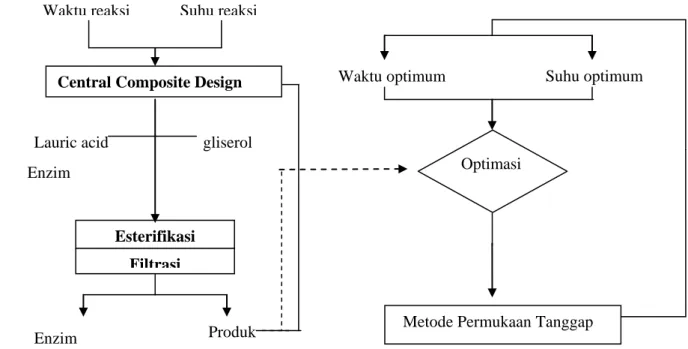
Pada tahap ini dilakukan penelitian untuk mencari kondisi optimum proses esterifikasi enzimatis secara circulated packed bed reactor yang dapat menghasilkan produk dengan kadar MAG tinggi. Diagram alir tahap optimasi dan proses reaksi esterifikasi dapat dilihat pada Gambar 14 dan 15. Rancangan percobaan yang digunakan pada tahap ini mengikuti rancangan Central
Composite Design (CCD) dari Respon Surface Methodology (RSM) dengan dua
variabel yaitu waktu dan suhu reaksi esterifikasi.
Penentuan titik tengah diambil dari reaksi circulated packed bed reactor yang menghasilkan kadar MAG dan rendemen terbaik serta dari referensi literatur. Sebagai contoh perlakuan dan kode perlakuan, serta rancangan percobaan masing-masing dapat dilihat pada Tabel 6 dan 7.
Gambar 14 Diagram alir proses optimasi sintesis monolaurin dengan metode circulated packed bed reactor
Tabel 6 Perlakuan dan kode perlakuan untuk reaksi esterifikasi
Perlakuan Kode perlakuan
-1,414 -1 0 1 1,414
Suhu 45 oC 46,5 oC 50oC 53,5 oC 55 oC
Waktu 1jam 1,3 jam 2 jam 2,7 jam 3 jam
Tabel 7 Rancangan percobaan dengan sistem pengkodean No Suhu ( C) Waktu Reaksi (jam)
1 -1 -1 2 1 -1 3 -1 1 4 1 1 5 -1,414 0 6 1,414 0 7 0 -1,414 8 0 1,414 9 0 0 10 0 0 11 0 0 12 0 0 13 0 0
Sumber : Cochran dan Cox (1962) Enzim
Enzim
Lauric acid gliserol
Produk
Optimasi
Central Composite Design
Waktu reaksi Suhu reaksi
Metode Permukaan Tanggap
Esterifikasi Filtrasi
Gambar 15 Diagram alir reaksi esterifikasi enzimatis secara circulated packed
Rancangan Percobaan
Rancangan percobaan yang digunakan adalah Central Composite Design. Model Respon Surface digunakan untuk melihat pengaruh perlakuan waktu dan suhu reaksi terhadap rendemen produk dan komposisi MAG dalam produk. Titik tengah perancangan penelitian diambil dari suhu dan waktu reaksi pada hasil penelitian pendahuluan.
Model Response Surface Methodology atau RSM adalah kumpulan teknik matematika dan statistik yang digunakan untuk membentuk model dan menganalisis masalah dalam suatu respon yang dipengaruhi oleh beberapa peubah dan bertujuan untuk mengoptimalisasi respon tersebut. RSM digunakan untuk mengetahui hubungan antara faktor percobaan dengan variabel respon. Berdasarkan hubungan tersebut dapat diperoleh nilai faktor percabaan yang akan menghasilkan nilai variabel respon yang dikehendaki. Seluruh perlakuan terdiri dari 13 set percobaan, dimana model umum rancangan percobaan yang digunakan adalah:
k k k -1,k
Y = β
o+
Σ
β
iX
i+
Σ
β
iiX
i 2+
Σ
β
i,jX
ii=1 i=1 i=1,j=2
Xj +
ε
Keterangan: Y = Respon Pengamatanβ
oβ
i = = Interceptβ
ii = Pengaruh linierβ
ij Pengaruh kuadratikXi = Kode untuk faktor ke-i = Pengaruh interaksi percobaan Xj = Kode untuk fakyor ke-j k = Jumlah faktor yang dicobakan
Verifikasi Kondisi Optimum Reaksi Esterifikasi Circulated packed bed reactor
Tahap verifikasi merupakan tahap pengujian terhadap kondisi proses optimum. Verifikasi dilakukan dengan maksud untuk memperbaiki tingkat keyakinan bahwa berdasarkan kondisi optimum yang diasumsikan, model yang dikembangkan dapat mewakili sistem yang sebenarnya. Verifikasi dilakukan dengan cara mengaplikasikan kondisi proses tersebut sebanyak lima kali ulangan, Tujuan verifikasi adalah melihat konsistensi produk yang dihasilkan berdasarkan pada nilai CV (Coeficeient Varians). Parameter yang dianalisis pada tahap verifikasi adalah komposisi MAG dan rendemen.
Uji Stabilitas Enzim Novozyme 435 pada Reaksi Esterifikasi Circulated packed bed reactor
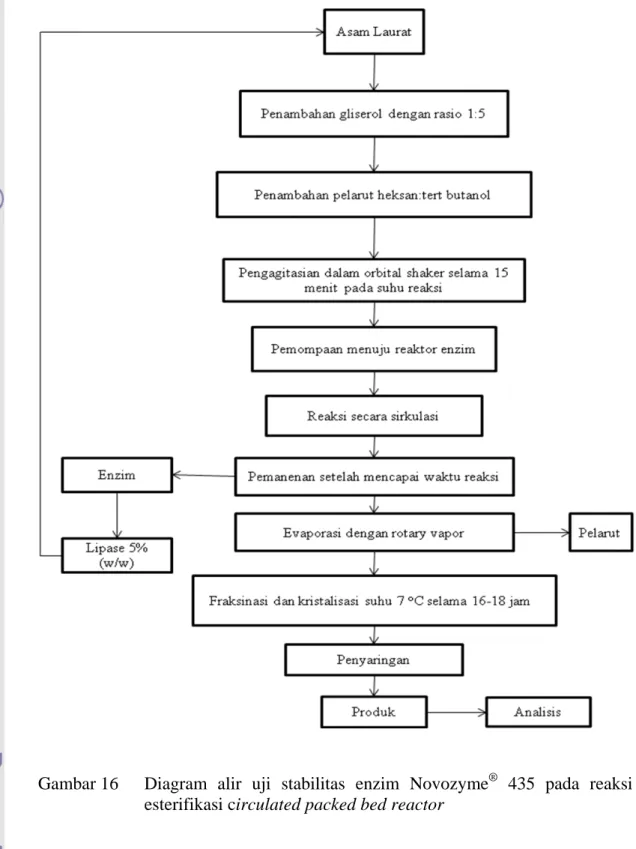
Uji stabilitas enzim dilakukan setelah didapatkan kondisi optimum proses esterifikasi yang telah diverifikasi. Enzim dipisahkan dari substrat reaksi, setelah itu dilakukan pencucian dengan pelarut ± 50 ml, dikering anginkan dan disimpan di refrigerator pada kondisi tertutup rapat jika tidak langsung digunakan, kemudian enzim digunakan kembali dalam reaksi dengan prosedur yang sama dan dilakukan berulang. Reaksi pengulangan dilakukan 10 kali dengan parameter yang dianalisa adalah komposisi MAG. Diagram alir uji stabilitas enzim dapat dilihat pada Gambar 16.
Gambar 16 Diagram alir uji stabilitas enzim Novozyme® 435 pada reaksi esterifikasi circulated packed bed reactor
Pengamatan
Bahan baku dan Produk MAG yang dianalisis merupakan produk hasil kondisi optimum proses dalam sistesis esterifikasi enzimatis MAG. Tujuan analisis ini adalah untuk mengetahui sifat fisik dan kimia bahan baku dan produk
MAG yang dihasikan. Analisis yang dilakukan meliputi bilangan Peroksida, kadar asam lemak bebas (ALB), Aw Enzim, pH enzim, analisis semi kuantitatif komposisi Gliserida dengan GC, Titik Leleh, dan analisis kuantitatif komposisi Gliserida produk dengan GC-MS Pyrolisis.
Analisis Kadar Air Dalam Minyak (AOAC,1995)
Sejumlah ± 5 g sampel dimasukkan ke dalam cawan yang telah diketahui beratnya. Kemudian cawan dimasukkan ke dalam oven bersuhu 100o
KA =
C hingga diperoleh berat yang konstan. Perhitungan kadar air dilakukan dengan menggunakan rumus : % 100 ) ( x c b a c− −
dengan: a = berat cawan dan sampel (g) b = berat cawan dan sampel akhir (g) c = berat sampel awal (g)
Analisis Bilangan Peroksida, Metode Titrimetri (AOAC, 1995)
Contoh minyak ditimbang seberat 5 gram dan dimasukkan ke dalam erlenmeyer tertutup dan diisi dengan gas N2. sampel ditambah dengan 55 ml kloroform dan distirer kemudian ditambah asam asetat glasial sebanyak 20 ml. Larutan KI jenuh ditambahkan sebanyak 0.5 ml kemudian ditutup dengan cepat, digoyang selama 1 menit. Sampel disimpan di tempat yang gelap selama 5 menit pada suhu 15oC sampai 25o
BP =
C. Setelah itu, sampel ditambahkan 30 ml air destilata. Larutan tersebut dititrasi dengan larutan sodium thiosulfat 0.01N dan digoyang dengan kuat. Larutan pati yang digunakan sebagai indikator ditambahkan ketika warna kuning larutan hampir hilang dan titrasi diteruskan hingga warna biru menghilang. Titrasi juga dilakukan terhadap blanko.
1000 ) ( x m xT Vb Vs−
Keterangan : BP = bilangan peroksida (meq O2
Vs = volume sodium thiosulfat untuk titrasi sampel (ml) /kg)
Vb = volume sodium thiosulfat untuk titrasi blangko (ml) T = konsentrasi sodium thiosulfat yang distandarisasi (N) m = massa sampel (g)
Analisis Kadar Asam Lemak Bebas (ALB) (AOAC, 1995)
Sampel ditimbang sebanyak 5 gram kemudian dilarutkan ke dalam 50 ml etanol (alkohol) 95%. Larutan ini kemudian ditrasi dengan NaOH 0,01N dengan indikator fenoftalein hingga terlihat warna merah muda selama 10 detik. Kadar asam lemak bebas dihitung dengan menggunakan rumus perhitungan :
Kadar Asam = m x M x T x V 10
Keterangan : V = volume (ml) KOH untuk titrasi T = normalitas larutan KOH M = berat molekul sampel
m = jumlah sampel yang digunakan
Pengukuran pH Enzim (Hariyadi, 1995)
Sebanyak 0.5 gram enzim disuspensikan dalam 15 ml air destilata. Campuran diaduk menggunakan magnetic stirer selama 2 menit dan diinkubasikan pada suhu kamar (±28 o
Pengukuran A
C) selama 30 menit. Selanjutnya dilakukanpengukuran menggunakan pH meter.
w
Pengukuran aktivitas air (A enzim (Hariyadi, 1995)
w) enzim dilakukan secara langsung menggunakan aw-meter Shibaura WA-60. Kalibrasi dilakukan garam NaCl dengan Aw= 0.7509. Sebanyak 1 gram sampel enzim diletakkan pada tempat sampel pada Aw-meter Shibaura WA-60. Selanjutnya Aw-meter ditutup dan ditunggu sampai angka hasil pengukuran pada Aw
Analisa Komposisi Gliserida MAG Dengan Kromatografi Gas (Modifikasi AOAC Official Method 993.18, 1995)
-meter konstan.
Sampel ditimbang teliti kurang lebih 0.2 mg dimasukkan dalam vial kemudian ditambahkan 0.2 ml BSTFA [bis(trimethylsilil)trifluoro acetamide] dan 0.1 ml TMCS (trimethylchlorsilane) dan 0.1 ml larutan standart internal n- tetradecana kemudian dikocok hati-hati dan dipanaskan pada suhu 70o C selama 30 menit setelah itu segera diinjeksikan ke kromatografi gas 1 μl. Dilakukan juga
seperti diatas untuk 0.1 ml larutan referensinya (MAG dan DAG) pada kondisi operasi yang sama, peak yang muncul diidentifikasi dengan membandingkan waktu retensi dari referensi. Larutan referensi dibuat dengan menimbang 0.2 mg referensi dilarutkan dalam piridin menggunakan labu takar 10 ml. Kromatografi gas yang digunakan dilengkapi dengan split injeksi atau kolom injeksi dan FID dengan operasi sebagai berikut: suhu kolom awal 50o C dinaikkan menjadi 180o C dengan kenaikan 15 o C/ menit kemudian dinaikkan lagi menjadi 230 o C dengan kenaikan 7 o C/menit dan dinaikkan lagi menjadi 380 o C, suhu detektor 390 o C, suhu injektor 390 o C, kecepatan gas pembawa 0.7 ml N2
Titik leleh (PORIM Test Method, 1995)
/menit, kecepatan aliran udara 450 ml/menit dan volume injeksi 1 μl.
Titik leleh didefinisikan sebagai suhu dimana sampel menjadi cair dengan sempurna. Produk mono dan diasilgliserol yang telah disaring dilelehkan dan dimasukkan ke dalam tabung kapiler (3 buah) setinggi 1 cm. Selanjutnya disimpan dalam refrigerator pada suhu 4-100C selama 16 jam. Ikatkan tabung kapiler pada termometer dan masukkan termometer tersebut ke dalam beaker
glass (600 ml) berisi air distilasi (sekitar 300 ml). Atur suhu air dalam beaker glass pada suhu 8 – 100C di bawah titik leleh sampel dan suhu air dipanaskan pelan-pelan (dengan kenaikkan 0.50C – 10
Kandungan gliserol bebas (AOCS Official Method Ca 5a-40, 1998)
C/menit) dengan pengadukan (magnetic
stirrer). Pemanasan dilanjutkan dan suhu diamati dari saat sampel meleleh sampai
sampel naik pada tanda batas atas. Titik leleh dihitung berdasarkan rata-rata suhu dari ketiga sampel yang diamati.
Sebanyak 5 g sampel ditimbang dalam gelas kimia 50 ml. Sampel dipindahkan ke dalam labu ukur 250 ml dengan penambahan pelarut kloroform sebanyak 22.5 ml. Sebanyak 125 ml air destilata ditambahkan ke dalam labu ukur kemudian labu ditutup. Campuran dalam labu dikocok dengan kuat selama kurang lebih 1 menit. Setelah dikocok, ditambahkan air destilata hingga tanda tera. Campuran didiamkan beberapa menit hingga terbentuk dua lapisan. Fase air yang berada bagian atas dipipet sebanyak 25 ml ke dalam erlenmeyer 250 ml,
kemudian ditambahkan asam periodat sebanyak 12.5 ml. Labu erlenmeyer dalam keadaan tertutup alumunium foil. Larutan KI 15% ditambahkan ke dalam labu kemudian didiamkan selama kurang lebih 1 menit. Ditambahkan sebanyak 100 ml air destilata ke dalam labu erlenmeyer. Campuran dititrasi dengan menggunakan larutan natrium tiosulfat 0.1 N hingga warna terbentuk warna kuning. Indikator pati ditambahkan sebanyak 2 ml kemudian dititrasi kembali hingga warna kompleks menghilang. Kandungan gliserol bebas dapat dihitung dengan rumus sebagai berikut
((B-S) x N x 2,302)/W
Keterangan : B – volume titrasi blanko (ml) N – konsentrasi sodium tiosulfat (N) S – volume titrasi sampel (ml) W – berat sampel (g)
Analisa Komposisi Gliserida MAG Dengan Kromatografi Gas- MS Pyrolisis (Modifikasi Ralph et al., 1991)
Sampel, 200-500 µg, dipirolisis dalam tabung kuarsa dalam 120 Pyroprobe (Chemical Data Systems) pada 600 oC (> 50o C / ms) selama 10 s menggunakan gas helium sebagai carrier dengan kecepatan linier 20 ml / menit. Sampel dibawa ke kolom DB-1 60 m X 0,25 mm (J & W Scientific) dipasang pada GC HP 5890 dalam mode splitless. Setting suhu di 80 oC selama 2 menit untuk menjebak dan fokus komponen volatil, kemudian diprogram pada suhu akhir 275 oC pada 4 OC / menit, dan waktu running lebih dari 60 min. Senyawa terselusi terdeteksi dengan Hewlett-Packard 5970 selektif massa detektor dikendalikan oleh HP UNIX stasiun data dan total ion kromatogram (TICS) terbentuk. Senyawa dielusi selama 2 jam