GUAR
ELIN VINA SETYOWATI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2008
GUAR
ELIN VINA SETYOWATI
Skripsi
sebagai salah satu syarat memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2008
ELIN VINA SETYOWATI. Stabilitas Obat Anti Peradangan Ketoprofen Tersalut Gel Kitosan-Gom Guar. Dibimbing oleh PURWANTININGSIH SUGITA, BUDI ARIFIN, dan BAMBANG SRIJANTO.
Gel kitosan yang dimodifikasi oleh hidrokoloid alami gom guar dengan glutaraldehida sebagai penaut silang berpotensi sebagai penyalut untuk digunakan dalam sistem pengantaran obat dalam bentuk mikrokapsul. Mekanisme pelepasan obat dari membran kitosan-gom guar telah dipelajari melalui uji difusi. Sementara laju pelepasan ketoprofen pada medium usus dan lambung telah dipelajari melalui uji disolusi. Sebagai sediaan obat yang baru, mikrokapsul ketoprofen ini perlu diuji stablitasnya. Tujuannya adalah untuk mengukur ketahanan penyalut selama penyimpanan dan penggunaan.
Sediaan obat dibuat dengan mencampurkan 228.60 ml larutan kitosan 1.75% (b/v), 38.10 ml larutan gom guar dengan ragam konsentrasi 0.35, 0.55, dan 0.75% (b/v), 7.62 ml glutaraldehida dengan ragam konsentrasi 3.0, 3.5, dan 4.0% (v/v), dengan 2 g ketoprofen yang dilarutkan di dalam etanol 96%. Campuran homogen yang diperoleh kemudian dikering semprot menjadi granul. Mikrokapsul yang optimum dalam menyalut ketoprofen dengan konsentrasi kitosan 1.75%, gom guar 0.35%, dan glutaraldehida 3.75% juga dibuat dan diuji stabilitasnya.
Uji stabilitas pada penelitian ini menggunakan uji dipercepat dalam climatic chamber dengan suhu (40 ± 2) °C dan kelembapan relatif (70 ± 5)% selama 3 bulan. Parameter yang diukur setiap minggu meliputi kadar air dengan moisture analyzer dan kadar ketoprofen dengan spektrofotometer ultraviolet pada panjang gelombang 254.6 nm. Kesepuluh formula menunjukkan nilai kadar air yang tinggi (>10%) dan berfluktuasi, sedangkan kadar ketoprofen terus menurun, mengikuti kinetika reaksi orde ke-nol. Mikrokapsul formula 7 (kitosan 1.75% [b/v], gom guar 0.75% [b/v], dan glutaraldehida 3% [v/v]) memiliki stabilitas paling baik. Persentase kadar ketoprofen yang masih tersalut setelah 12 minggu sebesar 86.78% (b/v), tetapan laju penguraian 0.3010 minggu-1, dan
ELIN VINA SETYOWATI. Stability of Antiinflamatory Ketoprofen Coated with Chitosan-Guar Gum Gel. Supervised by PURWANTININGSIH SUGITA, BUDI ARIFIN, and BAMBANG SRIJANTO.
Chitosan gel modified with guar gum natural hydrocolloid with glutaraldehyde as cross-linker are potential as coating agent to be used in drug delivery system in microcapsule form. Mechanism of drug release from chitosan-guar gum membrane has been studied by diffusion test, whereas release rate of ketoprofen in intestine and gastric medium has been studied by dissolution test. As a new drug preparation, the stability of this ketoprofen microcapsule need to be studied. The purpose is to measure the resistance of the coater during storage and use.
Drug preparations were made by mixing 228.60 ml 1.75% (w/v) chitosan solution, 38.10 ml of guar gum with concentration variation of 0.35, 0.55, and 0.75% (w/v); and 7.62 ml glutaraldehyde with concentration varied from 3.0, 3.5, and 4.0% (v/v), with 2 g of ketoprofen solubilized in 96% of ethanol. Homogenous mixture obtained was then spray-dried into granules. Optimum microcapsule for coating ketoprofen with chitosan, guar gum, and glutaraldehyde concentrations of 1.75% (w/v), 0.35% (w/v), and 3.75% (v/v) respectively, was also made and studied for its stability.
Stability was tested using accelerated test in climatic chamber under temperature (40 ± 2)°C and relative humidity (70 ± 5 )% for 3 months. The parameters were measured every week included moisture content by using moisture analyzer and ketoprofen content using ultraviolet spectrophotometer at wavelength of 254.6 nm. All ten formulas showed high (>10%) and fluctuating water contents and decreasing ketoprofen content, following a reaction kinetic of zero order. Microcapsule of formula 7 (1.75% [w/v] chitosan, 0.75% [w/v] guar gum, and 3.0% [v/v] glutaraldehyde) exhibited the best stability. The encapsulated ketoprofen content percentage still coated after the 12th week was 86.78%
Menyetujui, Pembimbing I,
Dr. Purwantiningsih Sugita, MS
NIP 131 779 513
Pembimbing II, Pembimbing III,
Budi Arifin, S.Si Ir. Bambang Srijanto NIP 132 321 568 NIP 680 003 303
Mengetahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor,
Dr. drh. Hasim, DEA
NIP 131 578 806
Bismillahirrahmanirrahim….
Segala puji hanya milik Allah Rabbul Izzati, syukur alhamdulillah penulis panjatkan ke hadirat Allah SWT atas rahmat dan hidayah-Nya sehingga karya ilmiah dengan judul ” Stabilitas Obat Anti Peradangan Ketoprofen Tersalut Gel Kitosan-Gom Guar” berhasil diselesaikan. Penelitian ini dilaksanakan sejak bulan April sampai November 2007 di Laboratorium Kimia Organik Departemen Kimia FMIPA IPB, Laboratorium Bersama Departemen Kimia FMIPA IPB, dan Laboratorium Farmasi dan Medika Pusat Penelitian Ilmu Pengetahuan dan Teknologi, Serpong.
Terima kasih penulis ucapkan kepada Dr. Purwantiningsih Sugita, MS, Budi Arifin, S.Si dan Ir.Bambang Srijanto selaku pembimbing yang senantiasa telah menyempatkan waktu untuk memberikan bimbingan, saran, dan ilmu pengetahuan kepada penulis. Terima kasih yang tak terhingga kepada Bapak, Ibu, Koko dan Mas Doni atas doa, cinta, kasih sayang, motivasi, kesabaran, dan perhatian, yang begitu besar selama ini. Penulis juga mengucapkan terimakasih kepada Pak Sabur, Ibu Yeni, Ibu Aah, Mas Heri, Mba Adew, dan Ibu Idah di Puspiptek serta seluruh staf Kimia atas sarana dan kemudahan yang telah diberikan. Selain itu penulis mengucapkan terima kasih kepada teman-teman seperjuangan di laboratorium organik (Dicky, Ichsan, Mba Dewi, Kak Budi, Bu Herdini, Mba Wati, Siti, Titik), Tim Mikrokapsul (Fitri, Debby, Mahdi, Feri, dan Yuyu), Iya, Nana, Iqoy dan warga Cidangiang 49 atas dukungan dan bantuannya, serta kepada teman-teman Kimia 40 atas dukungan dan kebersamaannya.
Pada kesempatan ini, penulis juga mengucapkan terima kasih kepada Direktur DP3M tahun 2007–2008 Direktorat Jenderal Pendidikan Tinggi Depdiknas melalui Hibah Bersaing XIV Dikti dan Hibah Penelitian Internal Departemen Kimia tahun 2006 sebagai sumber dana bagi penelitian ini.
Semoga karya ilmiah ini dapat bermanfaat.
Bogor, Februari 2008
Penulis dilahirkan di Malang pada tanggal 01 Maret 1985 sebagai anak pertama dari dua bersaudara dari ayah Sunarno dan ibu Winanti. Tahun 2003, Penulis lulus dari SMU Negeri I Gondanglegi, dan pada tahun yang sama lulus seleksi masuk Institut Pertanian Bogor melalui jalur Undangan Seleksi Masuk IPB pada Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, Penulis pernah menjadi asisten praktikum Kimia Fisika Departemen Ilmu Teknologi Pangan pada tahun ajaran 2006/2007dan Kimia Lingkungan Departemen Geofisika dan Meteorologi pada tahun ajaran 2007/2008. Selain itu, Penulis juga pernah menjadi staf pengajar Bimbingan Belajar Nurul Ilmi. Pada bulan Juli-Agustus 2006, Penulis melaksanakan Praktik Lapangan di Balai Penelitian Tanaman Obat dan Aromatik, BALITTRO, Bogor.
Halaman
DAFTAR TABEL………... viii
DAFTAR GAMBAR………... viii
DAFTAR LAMPIRAN………... ix
PENDAHULUAN………... 1
TINJAUAN PUSTAKA Gel Kitosan dan Modifikasinya….………... 1
Gom Guar………. 3
Ketoprofen……… 3
Mikroenkapsulasi………. 4
Metode Pengeringan Semprot (Spray Drying)... 4
Uji Stabilitas... 5
BAHAN DAN METODE Bahan dan Alat……….……… 5
Pembuatan Mikrokapsul………... 6
Uji Stabilitas ………...………. 6
Pencirian Mikrokapsul dengan SEM... 7
HASIL DAN PEMBAHASAN Pembuatan Mikrokapsul………... 7
Uji Stabilitas Mikrokapsul...………...………. 7
Pencirian Mikrokapsul dengan SEM... 10
SIMPULAN DAN SARAN Simpulan………... 11
Saran………... 11
DAFTAR PUSTAKA………. 11
Halaman
1 Spesifikasi kitosan niaga... 2
2 Formulasi mikrokapsul………. 6
3 Konsentrasi ketopofen dalam mikrokapsul kitosan-gom guar………. 8
4 Persamaan orde reaksi orde ke-0... 9
5 Penguraian kadar ketoprofen selama uji dipercepat 3 bulan... 10
DAFTAR GAMBAR
Halaman 1 Struktur kitosan... 22 Struktur hidrogel kitosan: (a) ikatan silang kitosan-kitosan, (b) jaringan polimer hibrida, (c) jaringan semi-IPN, dan (d) kitosan berikatan silang ionik... 2
3 Struktur gom guar... 3
4 Struktur ketoprofen... 4
5 Klasifikasi mikrokapsul menurut morfologi... 4
6 Perangkat alat pengeringan semprot... 6
7 Mikrokapsul tanpa dan dengan penambahan ketoprofen... 7
8 Foto SEM permukaan mikrokapsul tanpa penambahan ketoprofen... 7
9 Foto SEM permukaan mikrokapsul dengan penambahan ketoprofen... 7
10 Kurva kadar air formula 1 sampai 5... 8
11 Kurva kadar air formula 6 sampai 10... 8
Halaman
1 Diagram alir penelitian ………..……... 15
2 Penetapan kadar air dan kadar abu kitosan... 16
3 Kadar air dan abu kitosan………... 16
4 Spektrum FTIR dan penentuan derajat deasetilasi kitosan... 17
5 Penentuan bobot molekul kitosan... 18
6 Absorban larutan ketoprofen pada berbagai panjang gelombang... 19
7 Kurva standar larutan ketoprofen pada berbagai konsentrasi... 20
8 Data kadar air selama 3 bulan………... 21
9 Data kadar ketoprofen selama 3 bulan……….. 22
10 Penentuan orde raksi mikrokapsul hasil uji stabilitas... 23
PENDAHULUAN
Ketoprofen merupakan obat anti peradangan non-steroid yang bekerja menghambat sintesis prostaglandin. Ketoprofen sangat sukar larut dalam air, dan memiliki laju pelepasan obat yang cepat dalam tubuh. Penggunaan ketoprofen dalam dosis yang tinggi (>300 mg) dapat menyebabkan pendarahan pada lambung (AMA 1991). Salah satu cara untuk mengendalikan pelepasan obat tersebut ialah dengan membuat sediaan obat dalam bentuk mikrokapsul.
Mikroenkapsulasi merupakan salah satu cara penyalutan yang mudah dan sederhana untuk mengendalikan laju pelepasan senyawa yang disalutnya. Beberapa polimer turunan selulosa, seperti hidroksipropil metil selulosa dan etil selulosa telah digunakan dalam sediaan lepas terkendali, baik dalam bentuk matriks maupun mikrokapsul (Wade 1994 dalam Sutriyo et al. 2005). Kitosan memiliki struktur yang mirip selulosa juga telah dikembangkan.
Kitosan merupakan biopolimer yang sifatnya non-toksik, biokompatibel, dan biodegradabel. Selain itu, dalam suasana asam kitosan bersifat polikationik (Sutriyo et al. 2005) dan dapat membentuk hidrogel (Berger et al. 2004). Kitosan dalam bentuk gel atau lembaran telah digunakan sebagai penyalut obat anti-peradangan ketoprofen (Yamada et al. 2001) dan propanolol hidroklorida (Sutriyo et al. 2005). Namun, gel kitosan rapuh sehingga perlu dimodifikasi.
Perbaikan struktur gel kitosan telah banyak dilakukan, di antaranya dengan penambahan poli (vinil alkohol) (PVA) sebagai bahan saling tembus (interpenetrating agent) dan glutaraldehida sebagai penaut-silang. Penambahan kedua komponen tersebut dapat menurunkan waktu gelasi dan meningkatkan kekuatan mekanik gel (Wang et al. 2004). Modifikasi lain juga telah dilakukan dengan penambahan glutaraldehida dan hidrokoloid alami seperti gom guar (Sugita et al. 2006a), alginat (Sugita et al. 2006b), karboksimetil selulosa (Sugita et al. 2006c), dan gom xantan (Sugita et al. 2007a). Gel kitosan-gom guar telah diaplikasikan untuk menyalut ketoprofen (Sugita
et al. 2007b).
Gel kitosan dengan penambahan gom guar memiliki sifat reologi lebih baik dibandingkan dengan yang lainnya dan telah dioptimumkan untuk sistem pengantaran obat (Sugita et al. 2006a). Gom guar sendiri telah dimanfaatkan sebagai pembawa untuk memperbaiki sistem
pengantaran obat ke dalam usus besar untuk mengobati radang usus besar dan kanker usus besar (Kshirsagar 2000).
Kinerja membran gel kitosan-gom guar telah diuji oleh Nata et al. (2007) yang berupa uji difusi dan oleh Sugita et al. 2007b yang berupa uji disolusi. Uji disolusi dilakukan untuk mengetahui laju pelepasan ketoprofen tersalut gel kitosan-gom guar di dalam lambung dan usus, sedangkan uji difusi dilakukan untuk mengetahui mekanisme pelepasan obat dari membran gel tersebut. Menurut Sugita et al. (2007b), ketoprofen dilepaskan ketika matriks kitosan-gom guar bersentuhan dengan medium lambung dan usus, tetapi kinerja pelepasan pada medium usus lebih baik, yaitu dengan waktu paruh 15 menit. Pelepasan terjadi lewat mekanisme pembukaan pori, karena membran yang sudah diuji difusi memiliki lubang-lubang kecil yang dangkal yang tidak menembus membran (Nata et
al. 2007). Proses pembengkakan membran yang
disertai dengan pembukaan pori ini dapat membuat obat terlepas ketika mikrokapsul berinteraksi dengan cairan di dalam tubuh. Hasil kedua penelitian tersebut juga menunjukkan bahwa mikrokapsul kitosan-gom guar berpotensi sebagai sistem pengantaran obat.
Ketoprofen tersalut mikrokapsul kitosan-gom guar merupakan jenis sediaan obat yang baru. Karena itu, diperlukan uji kestabilan terhadap sediaan tersebut, untuk mengukur ketahanan penyalut selama penyimpanan dan penggunaan. Parameter stabilitas yang diukur meliputi kadar air dan kadar ketoprofen yang masih tersalut setelah 3 bulan penyimpanan, dan hasilnya digunakan untuk menentukan usia guna sediaan obat. Uji stabilitas diperlukan untuk menjamin keamanan dan khasiat obat selama penggunaan (Anonim 2005). Pengujian dilakukan menggunakan uji dipercepat selama 3 bulan (Agoes 2001). Parameter kinetika reaksi penguraian ketoprofen yang meliputi orde reaksi dan tetapan laju reaksi juga ditentukan dengan menggunakan metode grafis.
TINJAUAN PUSTAKA
Gel Kitosan dan Modifikasinya
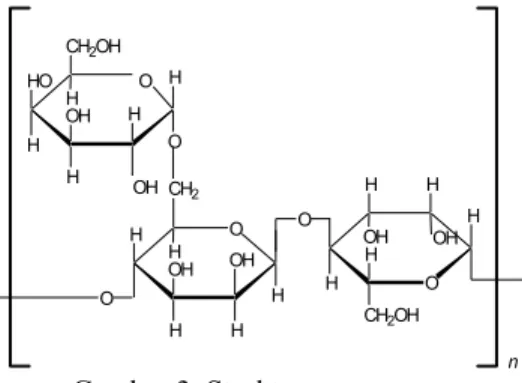
Kitosan merupakan biopolimer polikationik linear yang tersusun dari unit berulang 2-amino-2-deoksi-D-glukopiranosa yang terhubung oleh
ikatan β-(1,4) (Gambar 1). Kitosan memiliki rumus molekul (-C6H11NO4-)n dan merupakan
salah satu dari sedikit polimer alami yang berbentuk polielektrolit kationik dalam larutan asam organik (Hirano 1986 dalam Jamaludin 1994).
Gambar 1 Struktur kitosan.
Kitosan merupakan kitin yang terdeasetilasi dengan basa atau secara biokimiawi. Kitosan berbentuk padatan amorf dan larut dalam asam organik, tetapi tidak larut dalam air, alkohol, dan aseton. Dalam asam anorganik, seperti HCl dan HNO3, kitosan larut pada konsentrasi 1.1% (Muzi
dalam Jamaludin 1994). Mutu kitosan ditentukan dari nilai derajat deasetilasi (DD), kadar abu, kadar air, dan distribusi bobot molekul (BM)-nya. Tabel 1 menampilkan spesifikasi untuk kitosan niaga.
Tabel 1 Spesifikasi kitosan niaga*
Parameter Ciri Ukuran partikel Serpihan sampai bubuk
Kadar air ≤ 10%
Kadar abu ≤ 2%
Derajat deasetilasi ≥ 70%
Warna larutan Tidak berwarna
Viskositas (cps)
Rendah < 200
Medium 200–799
Tinggi 800–2000
Sangat tinggi > 2000
*Sumber: Anonim (1987) dalam Jamaludin (1994).
Larutan kitosan pada batas konsentrasi tertentu dalam asam asetat 1% dapat membentuk gel. Gel merupakan jejaring tiga dimensi yang terhubung antarmolekul atau partikel dan memerangkap sejumlah pelarut seperti spons. Gel terdiri atas serat-serat yang terbentuk dari molekul primer yang bergabung pada titik sambungan seperti ikatan hidrogen, interaksi hidrofobik, ikatan ionik, atau ikatan kovalen (Fennema 1976). Gel merupakan sistem semipadat berupa suspensi partikel anorganik
yang kecil atau molekul organik yang besar, yang terpenetrasi oleh suatu cairan. Sementara hidrogel merupakan gel yang dapat menahan air dalam strukturnya (Wang et al. 2004). Air yang terdapat dalam gel ini merupakan jenis air imbibisi, yaitu air yang masuk ke dalam suatu bahan dan menggembungkannya, tetapi bukan komponen penyusun bahan tersebut (Winarno 1997).
Hidrogel dibedakan menjadi hidrogel kimia dan fisika. Hidrogel kimia dibentuk dari reaksi yang tidak dapat balik, sedangkan hidrogel fisika dibentuk oleh reaksi yang dapat balik (Stevens 2001, Berger et al. 2004). Contoh hidrogel kimia adalah hidrogel kitosan. Ikatan-silang kovalen dalam hidrogel kitosan dapat dibedakan menjadi 4, yaitu ikatan silang kitosan-kitosan, jaringan polimer hibrida atau HPN (hybrid polymer
network), jaringan polimer saling-tembus
tanggung atau utuh (semi- atau full-IPN,
interpenetrating polymer network), dan kitosan
berikatan-silang ionik. Struktur hidrogel kitosan ditunjukkan pada Gambar 2.
Gambar 2 Struktur hidrogel kitosan: (a) ikatan silang kitosan-kitosan, (b) HPN, (c) jaringan semi-IPN, dan (d) kitosan berikatan silang ionik (Berger et al. 2004).
Gel kitosan memiliki bentuk yang rapuh, sehingga perlu dimodifikasi. Wang et al. (2004) melaporkan bahwa modifikasi gel kitosan dengan penambahan PVA sebagai agen saling tembus dan glutaraldehida sebagai penaut silang dapat menurunkan waktu gelasi dan meningkatkan kekuatan mekanik gel. Sementara itu, Cardenas
et al. (2004) melaporkan bahwa penambahan
alginat dapat memperbaiki struktur dasar makromolekul kitosan dengan cara pembentukkan ikatan silang pada proses gelasi sehingga strukturnya lebih kuat. Modifikasi lain O NH2 OH CH2OH O NH2 OH CH2OH O O O n
juga telah dilakukan dengan penambahan glutaraldehida dan hidrokoloid alami seperti gom guar (Sugita et al. 2006a), alginat (Sugita et al. 2006b dan Cardenas et al 2003), karboksimetil selulosa (Sugita et al. 2006c), dan gom xantan (Sugita et al. 2007a).
Sugita et al. (2006a) melaporkan bahwa gel kitosan-gom guar optimum berdasarkan optimalisasi dengan program Minitab Release 14, diperoleh dari larutan kitosan 2.5% (BM kitosan
4.30 × 103 g mol-1) dengan konsentrasi
glutaraldehida dan gom guar berturut-turut 4.86% (v/v) dan 0.33% (b/v). Sifat-sifat reologi kekuatan, titik pecah, ketegaran, pembengkakan, dan pengerutannya berturut-turut 553.356 g cm-2,
0.968 cm, 4.147 g cm-1, 4.0772 g, dan 1.2738 g.
Nata et al. (2007) melaporkan bahwa dalam uji difusi, model matematis fluks ketoprofen melalui membran kitosan-gom guar adalah J =
14.6207 + 0.165Cd − 0.398T – 0.2035h –
0.0007h2 − 0.0006C
dh − 0.007Th dengan nilai R2
= 98.4%. Labih jauh diperoleh bahwa membran tidak menunjukkan adanya pori sebelum diuji difusi, sementara setelah diuji difusi terbentuk lubang-lubang kecil dangkal yang tidak menembus membran. Proses pembengkakan membran yang disertai dengan pembukaan pori ini dapat membuat obat terlepas ketika mikrokapsul berinteraksi dengan cairan di dalam tubuh. Berdasarkan hasil uji disolusi yang dilakukan Sugita et al. (2007b), mikrokapsul optimum diperoleh saat konsentrasi gom guar dan glutaraldehida berturut-turut 0.35% (b/v) dan 3.75% (v/v) untuk konsentrasi kitosan 1.75%, yang dapat menyalut ketoprofen sebanyak 146.5086 mg. Disolusi ketoprofen dalam medium usus mengikuti kinetika reaksi orde ke-3 dengan nilai tetapan laju pelepasan ketoprofen, k dan waktu paruh, t1/2, rerata berturut-turut 1×10-5
l2mol-2menit-1 dan 15 menit. Gom Guar
Gom guar merupakan gom biji yang diperoleh dari tanaman Legominosae, Cyamopsis
tetragomolobus, dan Cyamopsis psoraloides yang
ditemukan di barat laut India dan Pakistan (Nussinovitch 1997). Komponen utamanya adalah galaktomanan. Galaktomanan memiliki rantai utama β-D-manopiranosil yang berikatan α-(1→4) dengan unit α-D-galaktopiranosil pada O-6. Struktur gom guar diperlihatkan pada Gambar 3. HO H H O H H OH CH2OH H O O O CH2 O H H CH2OH H H H OH O H H OH H H OHH n OH OH
Gambar 3 Struktur gom guar.
Pengolahan untuk mendapatkan gom guar meliputi pemisahan secara mekanik terhadap kulit biji, lalu lembaganya dibuang, dan endosperma yang mengandung gom digiling menjadi tepung halus. Gom guar tidak bermuatan sehingga tidak terpengaruh oleh pH dan sangat efektif dalam produk-produk asam. Interaksi gom guar tidak menghasilkan gel, tetapi hanya meningkatkan kekentalan, karena derajat substitusi rantai tulang punggungnya yang tinggi dapat mengurangi interaksi (Fardiaz 1989).Gom guar juga telah dimanfaatkan sebagai pembawa untuk memperbaiki sistem pengantaran obat ke dalam usus besar untuk mengobati radang usus besar dan kanker usus besar (Kshirsagar 2000).
Gom guar berfungsi sebagai bahan saling tembus (interpenetrating agent) yang diharapkan dapat menghasilkan sifat gel kitosan yang lebih baik. Sifat jaringan serta interaksi yang mengikat keseluruhan gel menentukan kekuatan, stabilitas, dan tekstur gel. Untuk memperkuat jaringan internal gel ini biasanya digunakan molekul lain sebagai pembentuk ikatan-silang, dalam penelitian ini digunakan glutaraldehida.
Ketoprofen
Asam 2-(3-benzoilfenil)propanoat, yang dikenal dengan nama dagang ketoprofen, merupakan obat anti peradangan nonsteroid dengan rumus molekul C16H14O3 dan berbobot
molekul 254.3 g mol-1. Zat ini berbentuk serbuk
hablur, putih atau hampir putih, tidak berbau, mudah larut dalam etanol, kloroform, dan eter, tetapi tidak larut dalam air, serta memiliki laju pelepasan yang cepat dalam tubuh. Suhu leburnya berkisar 93–96 °C (USP 2003). Struktur ketoprofen dapat dilihat pada Gambar 4.
C O CH CH3 COH O
Gambar 4 Struktur ketoprofen.
Ketoprofen merupakan zat dengan daya analgesik, anti-peradangan, dan antipiretik yang bekerja menghambat sintesis prostaglandin. Ketoprofen dieliminasi melalui ginjal. Dosis oral ketoprofen bagi penderita artritis rematoid dan osteoartritis adalah 75 mg, 3 kali sehari atau 50 mg, 4 kali sehari (AMA 1991).
Ketoprofen memiliki waktu paruh eliminasi dalam plasma darah sekitar 1.5−2 jam. Konsentrasi ketoprofen yang bertahan dalam plasma darah setelah 24 jam hanya sekitar 0.07 mg/L. Selain itu, ketoprofen dalam dosis yang tinggi (> 300 mg) dapat menyebabkan pendarahan pada lambung (AMA 1991). Oleh karena itu, ketoprofen perlu dimikroenkapsulasi untuk mengendalikan pelepasannya di dalam tubuh (Patil et al. 2005).
Mikroenkapsulasi
Mikroenkapsulasi adalah teknologi untuk menyalut atau melapisi suatu zat inti dengan lapisan dinding polimer sehingga menjadi partikel-partikel kecil berukuran mikro (seperseribu milimeter). Dengan adanya lapisan dinding polimer ini, zat inti akan terlindungi dari pengaruh lingkungan luar. Dalam bentuk yang sangat sederhana, mikrokapsul merupakan sebuah daerah (sphere) yang dikelilingi oleh dinding yang seragam. Bahan yang dibungkus di dalamnya disebut inti, fase internal, atau isi, sedangkan dindingnya kadang-kadang disebut kulit, penyalut, atau membran.
Mikroenkapsulasi merupakan salah satu upaya mengendalikan pelepasan senyawa aktif dalam obat. Kegunaan lain teknik ini adalah membuat bahan reaktif menjadi lebih aman dipegang, melindungi bahan yang peka terhadap lingkungannya, dan mengubah wujud bahan dari cair menjadi padat (Yoshizawa 2004).
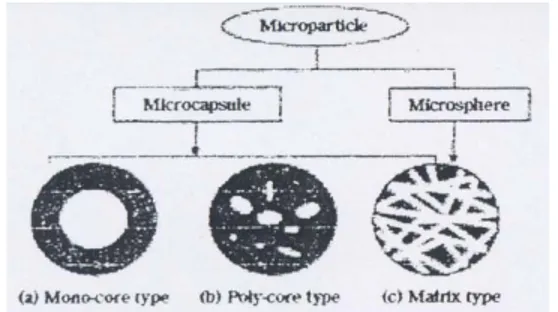
Secara umum, mikrokapsul dapat dibagi menjadi tiga kelompok, yaitu berinti tunggal, berinti banyak, dan tipe matriks (Gambar 5). Pengendalian sifat morfologi penting dan harus dilakukan dalam upaya menghasilkan mikrokapsul yang terbaik dengan sebagian besar
bergantung pada metode mikroenkapsulasi yang digunakan.
Gambar 5 Klasifikasi mikrokapsul menurut morfologi (Yoshizawa 2004). Mikroenkapsulasi dapat dilakukan secara fisika dan kimia. Metode fisika yang digunakan antara lain pan coating, pelapisan suspensi udara, piringan pemutar, dan pengeringan semprot (spray drying). Sementara metode kimia antara lain polimerisasi antarmuka, polimerisasi in-situ, polimerisasi matriks, penguapan pelarut, dan pemisahan fase. Dari berbagai metode di atas, metode pengeringan semprot paling mudah dan sederhana untuk mengkapsulasi suatu bahan karena larutan suspensi yang akan dimikroenkapsulasi cukup dimasukkan ke dalam alat pengering semprot dengan serbuk mikrokapsul sebagai produk (Oliveira et al. 2005).
Metode Pengeringan Semprot
Metode pengeringan semprot dapat dilakukan melalui beberapa tahapan, yaitu (1) produk yang berupa cairan didispersikan dalam penyemprot (sprayer), (2) kontak antara semprotan dan udara panas, (3) pengeringan hasil semprotan, serta (4) pemisahan antara produk kering (aliran serbuk bebas) dan udara (Oliveira et al. 2005). Beberapa keuntungan metode ini antara lain stabilitas serbuk yang dihasilkan tinggi, tekniknya dapat diandalkan dan terulangkan dengan mutu produk yang tinggi, biayanya efektif, tekniknya ramah lingkungan dan terhindar dari penggunaan pelarut organik, dapat dilakukan dalam satu tahap dan prosesnya berkelanjutan (continuous), serta merupakan metode yang fleksibel (dapat digunakan untuk enkapsulasi polimer-polimer yang berbeda dengan suhu berbeda). Selain itu, alat ini juga dapat digunakan untuk bahan yang tidak tahan panas atau titik didihnya rendah (Deymonaz et al. 1998).
Uji Stabilitas
Stabilitas didefinisikan sebagai kemampuan suatu produk untuk bertahan dalam batas waktu yang ditetapkan sepanjang periode penyimpanan dan penggunaan. Ada lima jenis stabilitas yang umum dikenal, yaitu stabilitas kimia, stabilitas fisika, stabilitas mikrobiologi, stabilitas terapi, dan stabilitas toksikologi. Stabil secara kimia berarti setiap zat mempertahankan keutuhan kimiawi dan potensi yang tertera pada etiket dalam batas yang dinyatakan pada spesifikasi. Stabilitas fisika berarti contoh mempertahankan sifat fisika awal termasuk penampilan, kesesuaian, keseragaman, disolusi, dan kemampuan untuk disuspensikan. Pada stabilitas mikrobiologi, sterilitas atau resistensi terhadap pertumbuhan mikrob dipertahankan sesuai dengan persyaratan yang dinyatakan. Sementara pada stabilitas terapi, efek terapi tidak berubah selama usia guna sediaan (Agoes 2001).
Parameter untuk uji stabilitas secara kimia meliputi penentuan persentase kadar ketoprofen yang masih tersalut, tetapan laju penguraian zat aktif (k), dan usia guna. Penentuan persentase kadar ketoprofen yang masih tersalut dilakukan untuk mengetahui efek kondisi penyimpanan terhadap kadar zat aktif dalam sediaan. Penentuan tetapan laju penguraian digunakan untuk mengetahui banyaknya zat aktif yang terurai dari penyalutnya selama periode penyimpanan. Sementara usia guna ditentukan untuk mengetahui keamanan dan khasiat obat selama penggunaan dan penyimpanan (Agoes 2001).
Uji stabilitas bertujuan menunjukkan mutu senyawa aktif atau jenis produk farmasi di bawah pengaruh faktor lingkungan, seperti suhu, kelembapan, dan pencahayaan. Suhu dan kelembapan udara sangat memengaruhi stabilitas obat dan dapat mengganggu sifat organoleptik, sifat fisiko-kimia, dan mikrobiologi obat. Pengaruh cahaya juga penting untuk mengetahui jenis kemasan yang akan digunakan dan cara penyimpanan obat yang sesuai (Agoes 2001). Uji stabilitas sangat diperlukan untuk semua sediaan farmasi. Alat yang digunakan untuk uji ini adalah
climatic chamber yang menyerupai oven, dan
digunakan untuk menyimpan sediaan farmasi yang diuji stabilitasnya. Pada alat ini suhu dan kelembapan dapat diatur sesuai dengan yang diinginkan.
Setiap sediaan obat harus diuji stabilitas untuk mengetahui usia gunanya. Berdasarkan
dokumen yang dibuat oleh International Conference on Hormonization (ICH), uji stabilitas untuk bahan aktif atau sediaan farmasi dapat dilakukan dalam jangka panjang atau dalam jangka waktu yang dipercepat. Uji jangka panjang dilakukan dalam waktu yang lama untuk memungkinkan terjadinya penguraian produk sesuai dengan rekomendasi kondisi penyimpanan. Uji jangka panjang dilakukan selama 12 bulan pada suhu (25±5) °C dan kelembapan relatif (RH) (60±5) %. Uji dengan jangka waktu yang dipercepat dilakukan untuk memperkirakan stabilitas produk dengan menyimpan sediaan obat di bawah kondisi yang dapat mempercepat penguraian, misalnya dengan menaikkan suhu. Selain itu, uji ini juga dilakukan untuk memenuhi syarat registrasi obat, sehingga dengan waktu yang lebih cepat dapat mempersingkat jadwal pengembangan produk. Uji ini digunakan untuk memperoleh petunjuk awal dari usia guna sediaan dan memungkinkan untuk menduga stabilitas produk pada suhu penyimpanan produk pada kondisi tertentu. Uji ini dilakukan selama 6 bulan pada suhu (40±5) °C dan RH (60±5) % atau selama 3 bulan pada suhu (45–50) °C dan RH 75 % (Agoes 2001).
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah kitosan niaga yang dibeli di CV Dinar Cikarang Bekasi dengan spesifikasi kadar air, kadar abu, DD, dan BM berturut-turut sebesar 10.80%, 0.53% 70.13%, dan 3090.45 g
mol-1, air suling, asam asetat teknis,
glutaraldehida, gom guar, kertas saring, Tween-80, etanol teknis, dan senyawa aktif ketoprofen yang diperoleh dari PT Kalbe Farma.
Alat-alat yang digunakan di antaranya alat-alat kaca, viskometer Ostwald, lempeng pemanas, oven J.P. SELECTA, pengaduk magnet, spektrofotometer inframerah transformasi fourier (FTIR) Bruker jenis Tentor 37, pelapis ion Au IB-2, mikroskop elektron susuran (SEM) JEOL JSM-5310LV, pengering semprot Buchi 190, climatic chamber, spektrofotometer ultraviolet (UV)-1700 PharmaSpec, dan moisture analyzer Precisa HA60. Analisis FTIR dilakukan di Pusat Studi Biofarmaka (PSB) IPB, uji stabilitas dilakukan
di Laboratorium Farmasi dan Medika Pusat Penelitian dan Teknologi (Puspiptek) Serpong, pembuatan mikrokapsul di Laboratorium Pilot
Plan PAU IPB, dan analisis SEM dilakukan di
Laboratorium Zoologi Lembaga Ilmu Pengetahuan Indonesia (LIPI) Cibinong.
Pembuatan Mikrokapsul
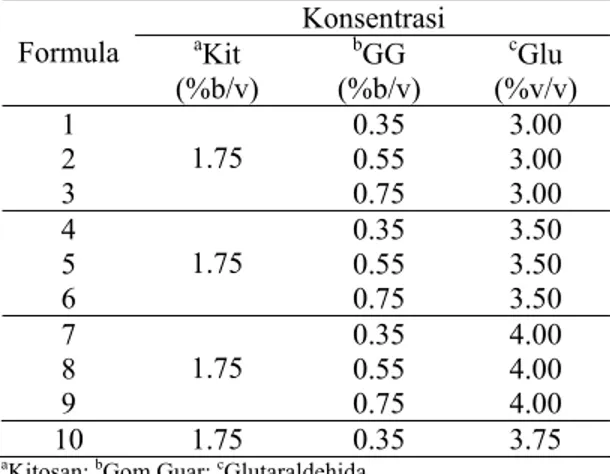
Diagram alir penelitian ini dapat dilihat secara garis besar pada Lampiran 1. Prosedur dan hasil pencirian kitosan ditunjukkan pada Lampiran 2–5 Sedangkan penentuan panjang gelombang maksimum dan kurva standar diberikan pada Lampiran 6 dan 7. Pembuatan mikrokapsul gel kitosan-gom guar menggunakan modifikasi dari metode Sugita et al. (2006a). Mula-mula dibuat larutan kitosan 1.75% (b/v) dalam asam asetat 1% (v/v). Sebanyak 228.6 ml larutan ini ditambahkan 38.1 ml larutan gom guar (gg) dengan ragam konsentrasi 0.35, 0.55, dan 0.75% (b/v) sambil diaduk dengan pengaduk magnet sampai homogen. Setelah itu, dilakukan penambahan 7.62 ml glutaraldehida (glu) sambil diaduk dengan ragam konsentrasi 3, 3.5, dan 4% (v/v). Mikrokapsul optimum juga dibuat dengan komposisi kitosan 1.75% (b/v), gom guar 0.35% (b/v), dan glutaraldehida 3.75% (v/v). Secara keseluruhan dibuat 10 formula mikrokapsul. Komposisi larutan kitosan, gom guar, dan glutaraldehida untuk masing-masing formula ditunjukkan pada Tabel 2.
Tabel 2 Formulasi mikrokapsul Konsentrasi Formula aKit (%b/v) bGG (%b/v) cGlu (%v/v) 1 0.35 3.00 2 0.55 3.00 3 1.75 0.75 3.00 4 0.35 3.50 5 0.55 3.50 6 1.75 0.75 3.50 7 0.35 4.00 8 0.55 4.00 9 1.75 0.75 4.00 10 1.75 0.35 3.75
aKitosan; bGom Guar; cGlutaraldehida
Masing-masing formula dicampurkan dengan 2 g obat ketoprofen yang dilarutkan dalam 250 ml etanol 96% untuk membuat suspensi dengan nisbah kitosan-ketoprofen 2:1, lalu ditambahkan 5 ml Tween-80 2%. Campuran kemudian diaduk
pada kecepatan skala 7 dengan pengaduk magnet selama 1 jam pada suhu kamar dan dibuat menjadi mikrokapsul dengan alat pengering semprot (Gambar 6) sampai berbentuk serbuk/butiran. Alat pengering semprot yang digunakan memiliki diameter lubang 1.5 mm dan di atur pada suhu inlet 170−185 °C, suhu outlet 65−95 °C, pompa dengan laju alir 60 rpm, dan tekanan semprot pada skala 2 bar.
Gambar 6 Perangkat alat pengering semprot.
Uji Stabilitas (Agoes 2001)
Setiap formula mikrokapsul dikemas ke dalam kapsul, 1 kapsul berisi sebanyak 100 mg. Mikrokapsul yang sudah dikemas dimasukkan ke dalam botol berwarna cokelat ukuran 100 ml sebanyak 12 botol untuk 12 minggu. Setiap botol tersebut diisi 20 kapsul, masing-masing 2 kapsul dari sepuluh ragam yang berbeda. Kemudian botol disimpan dalam climatic chamber pada suhu (40±2) °C dan RH (75±5) % selama 3 bulan.
Uji stabilitas mikrokapsul dilakukan secara kimia dan fisika. Pengujian secara kimia dilakukan dengan cara mengukur kadar ketoprofen. Sebanyak 1 kapsul diambil dari
climatic chamber untuk tiap varian dan
diekstraksi isinya dengan 45 mL etanol 96% selama 3 jam dengan penggantian pelarut setiap 1 jam (@15 mL). Konsentrasi ketoprofen yang terekstraksi ditentukan dengan menggunakan spektrofotometer UV pada panjang gelombang 254.6 nm. Pengambilan mikrokapsul dan ekstraksi dilakukan duplo untuk tiap varian. Sementara uji stabilitas secara fisika, yaitu pengukuran kadar air, dilakukan dengan menggunakan alat moisture analyzer. Mikrokapsul dari tiap varian (1 g) diukur kadar airnya setiap minggu. Berdasarkan kedua uji ini akan didapatkan data kadar air dan konsentrasi ketoprofen dalam mikrokapsul per minggu
selama periode 3 bulan, yang selanjutnya dipakai untuk menentukan stabilitas (usia guna) produk.
Pencirian Mikrokapsul dengan SEM
Mikrokapsul kosong dan salah satu mikrokapsul yang berisi ketoprofen (formula 3) dianalisis morfologi strukturnya menggunakan alat SEM. Analisis juga dilakukan terhadap mikrokapsul yang telah diuji stabilitasnya (formula 3 dan 7), untuk melihat perubahan morfologi permukaan mikrokapsul selama uji stabilitas.
HASIL DAN PEMBAHASAN
Pembuatan Mikrokapsul
Sebanyak 1L campuran kitosan-gom guar-glutaraldehida menghasilkan sekitar 2.5 g mikrokapsul berbentuk butiran atau granul halus yang kering dan rapuh dengan warna kuning kecokelatan (Gambar 7a). Larutan kitosan awal yang digunakan berwarna kuning, sehingga saat diubah menjadi bentuk butiran dengan bantuan panas yang tinggi pada alat pengering semprot, warnanya menjadi agak cokelat. Pencampuran dengan ketoprofen yang berwarna putih membuat warna mikrokapsul menjadi lebih pucat (Gambar 7b).
Gambar 7 Mikrokapsul tanpa (a) dan dengan penambahan ketoprofen (b).
Foto SEM mikrokapsul tanpa dan dengan ketoprofen (Gambar 8 dan 9) memperlihatkan bentuk yang bulat (sferis) dan tidak berlubang. Hal ini menunjukkan kehomogenan larutan mikrokapsul yang dibuat. Larutan mikrokapsul yang tidak homogen dapat memerangkap gelembung udara sehingga permukaan mikrokapsul akan tampak kisut dan berlubang. Ukuran mikrokapsul setelah penambahan ketoprofen berkisar 1 sampai 11 µm, lebih besar dibandingkan dengan sebelum penambahan ketoprofen (0.4–5 µm). Hal ini menunjukkan telah terisinya ruang kosong di dalam mikrokapsul oleh ketoprofen atau dengan kata lain proses enkapsulasi ketoprofen dengan kitosan-gom guar telah terjadi.
Gambar 8 Foto SEM permukaan mikrokapsul
tanpa penambahan ketoprofen pada perbesaran 2000×.
Gambar 9 Foto SEM permukaan mikrokapsul dengan penambahan ketoprofen pada perbesaran 2000×.
Uji Stabilitas Mikrokapsul
Uji stabilitas yang dilakukan dalam penelitian ini meliputi pengujian kadar air dan kadar ketoprofen. Uji kadar air dilakukan menggunakan moisture analyzer yang dapat secara langsung menunjukkan nilai kadar airnya. Kadar air untuk 10 formula (Lampiran 8) rata-b a 0.4-5µm 20 kV ×2.000 1.0-11µm ×2.000 20 kV
rata memiliki nilai yang tinggi dan berfluktuasi (Gambar 9 dan 10). Fluktuasi kadar air mikrokapsul ini terjadi karena ukuran partikel yang dihasilkan beragam sehingga banyaknya ketoprofen yang tersalut gel kitosan-gom guar tidak sama. Hal ini menyebabkan mikrokapsul yang dimasukkan dalam kapsul yang satu dengan kapsul yang lain dengan jumlah yang sama memiliki kadar air yang berbeda. Nilai kadar air suatu sediaan obat sebaiknya kurang dari 10% untuk mencegah tumbuhnya mikrob seperti
Staphylococcus aureus. Tingginya kadar air ini
diduga disebabkan karena sifat membran gel kitosan-gom guar yang higroskopis. Sugita et al. (2006a) melaporkan bahwa gom guar memiliki kemampuan yang tinggi dalam menyerap air. Hal ini juga didukung dengan salah satu sifat reologi gel tersebut, yaitu bahwa penambahan gom guar dapat menyebabkan pembengkakan gel. Pembengkakan ini terjadi karena gom guar dapat meningkatkan kemampuan gel untuk menarik air. Selain itu, adanya mikrob dapat meningkatkan lebih lanjut kadar air suatu sediaan obat (Agoes 2001).
Gambar 10 Kurva kadar air formula 1 sampai 5.
Gambar 11 Kurva kadar air formula 6 sampai 10.
Kadar ketoprofen (%b/b) yang tersalut oleh mikrokapsul gel kitosan-gom guar juga diukur setiap minggunya secara spektrofotometri. Kadar ketoprofen yang tersalut pada minggu ke-0 untuk setiap formula berkisar 24.45−33.02%. Nilai ini hampir sama dengan hasil penelitian Sugita et al. (2007b) yang berkisar 23.07–35.28% (Tabel 3).
Tabel 3 Konsentrasi ketoprofen dalam mikrokapsul kitosan-gom guar [Ketoprofen]
(%b/b)
Formula minggu
ke-0 minggu ke-12
[Ketoprofen] Sugita et al. (2007c) (%b/b) 1 26.58 22.28 35.28 2 26.57 18.63 28.97 3 29.25 19.11 25.20 4 26.42 19.86 30.42 5 26.29 20.76 32.72 6 33.02 22.95 28.47 7 26.93 23.17 34.93 8 27.94 22.58 31.92 9 24.45 20.69 23.07 10 28.51 22.01 29.30
Tabel 3 juga memperlihatkan bahwa setelah 3 bulan kadar ketoprofen menurun. Penurunan yang terjadi setiap minggunya diperlihatkan pada Lampiran 9, dan digunakan untuk penentuan orde reaksi penguraian ketoprofen. Penentuan orde dilakukan dengan metode grafis untuk orde ke-0, ke-1, ke-2, dan ke-3 yang persamaannya berturut-turut ialah
[ ] [ ]
Α t = Α0 −kt………...(1)[ ]
Α ln[ ]
Α t ln t = 0 −k …………...(2)[ ] [ ]
t Α 1 Α 1 0 t k + = …..….……...(3)[ ]
2[ ]
Α t 1 Α 2 1 2 0 2 t k + = ..……...(4)Nilai koefisien determinasi, R2 terbesar untuk
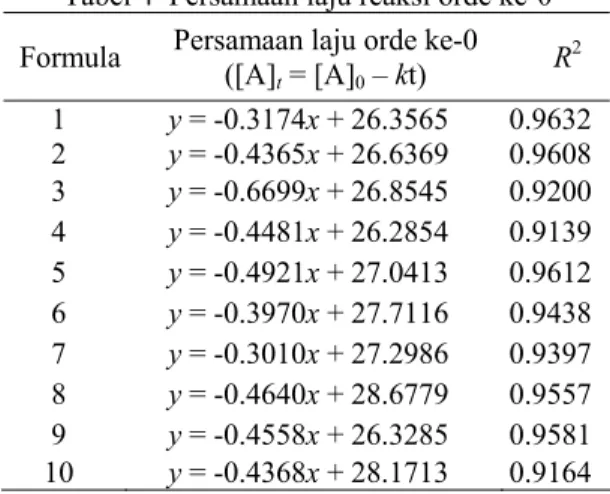
semua formula diperoleh pada orde ke-0 (Lampiran 10) dan persamaannya ditunjukkan pada Tabel 4.
Tabel 4 Persamaan laju reaksi orde ke-0 Formula Persamaan laju orde ke-0 ([A]
t = [A]0 – kt) R 2 1 y = -0.3174x + 26.3565 0.9632 2 y = -0.4365x + 26.6369 0.9608 3 y = -0.6699x + 26.8545 0.9200 4 y = -0.4481x + 26.2854 0.9139 5 y = -0.4921x + 27.0413 0.9612 6 y = -0.3970x + 27.7116 0.9438 7 y = -0.3010x + 27.2986 0.9397 8 y = -0.4640x + 28.6779 0.9557 9 y = -0.4558x + 26.3285 0.9581 10 y = -0.4368x + 28.1713 0.9164 Persentase kadar ketoprofen yang masih tersalut setelah 3 bulan (%[A]t) selanjutnya dapat
dihitung berdasarkan persamaan
%[A]t =
100
%
]
[
]
[
0×
Α
Α
t …………...(5) [A]t diperoleh dari persamaan-persamaan ordereaksi pada Tabel 4 dengan memasukkan t = 12
minggu, sedangkan [A]0 merupakan intersep
persamaan tersebut. Hasil perhitungan %[A]t
diberikan pada Tabel 5 dan kisaran nilainya 78– 87%, kecuali untuk formula 3 yang hanya sekitar 70%. Menurut Agoes (2001), obat dikatakan stabil jika kadar bahan aktif serendah-rendahnya 90% dari kadar awal. Meskipun persentase kadar ketoprofen yang masih tersalut dalam kesepuluh formula mikrokapsul kitosan-gom guar setelah 3 bulan menunjukkan nilai yang cukup besar, nilainya masih lebih rendah daripada batas minimum untuk uji stabilitas. Formula yang stabilitasnya terbaik ialah formula 7 (86.78%), diikuti berturut-turut oleh formula 1, 6, 10, 2, 8, 4 , 9, 5, dan formula 3 yang terendah (70.09%). Hasil ini tidak sejalan dengan peningkatan kadar air yang urutannya ialah formula 1 > 4 > 8 > 6 > 9 > 5 > 2 > 7 > 3 > 10. Menurut Agoes (2001), peningkatan kadar air suatu sediaan akan menurunkan kadar bahan aktif di dalamnya. Lebih jauh, Agoes (2001) mengatakan bahwa stabilitas sediaan obat termasuk baik jika laju penguraian zat aktifnya maksimum 3% per tahun atau setara dengan 0.06% per minggu. Sebagaimana ditunjukkan pada Tabel 5, nilai tetapan laju reaksi orde ke-0 (k) untuk seluruh formula lebih besar daripada batas nilai ini, yang
menegaskan kurang stabilnya penyalutan oleh membran gel kitosan-gom guar terhadap ketoprofen. Sejalan dengan nilai %[A]t yang
terbesar, formula 7 memiliki nilai k paling kecil, yaitu 0.3010 minggu-1.
Stabilitas yang rendah dari kesepuluh formula kemungkinan disebabkan oleh adanya air yang diserap oleh gom guar. Menurut Sugita
et al. (2006a), gom guar dapat menyebabkan
matriks mengembang, membentuk pori, dan memungkinkan terjadinya pelepasan ketoprofen dari matriks. Hal ini juga didukung oleh hasil eksperimen difusi yang dilakukan Nata et al. (2007) dengan membran yang sama yang menunjukkan bahwa matriks gel kitosan-gom guar akan membentuk pori ketika bersentuhan dengan cairan dan menyebabkan ketoprofen keluar dari penyalutnya. Namun, pori yang dihasilkan dalam penelitian ini tidak sebanyak ketika membran dalam kondisi eksperimen difusi, sehingga persentase ketoprofen yang tersalut masih cukup besar.
Hasil uji stabilitas selanjutnya digunakan untuk menentukan usia guna mikrokapsul. Batasan 90% ketoprofen yang tetap tersalut sebagai syarat stabilitas sediaan obat dijadikan dasar penentuan usia guna dari sediaan tersebut: Usia guna = k 0 [A] 0.1× …...……...(6) Hasil yang diperlihatkan pada Tabel 5 menunjukkan bahwa kesepuluh formula memiliki usia guna yang relatif pendek (< 1 tahun). Urutan dari formula dengan usia guna terpanjang adalah formula 7 (9.07 minggu), lalu formula 1, 6, 10, 2, 8, 4, 9, 5, dan 3 (4.01 minggu).
Berdasarkan ketiga parameter uji stabilitas, formula 7 menunjukkan stabilitas paling baik. Persentase kadar ketoprofen tersalut paling besar, tetapan laju penguraian paling kecil, dan usia gunanya paling panjang. Komposisi bahan penyalut formula 7 ialah kitosan 1.75% (b/v), gom guar 0.75% (b/v), dan glutaraldehida 3% (v/v). Sementara itu, persentase ketoprofen tersalut yang paling kecil, tetapan laju penguraian terbesar dan usia guna tersingkat ditunjukkan oleh formula 3, dengan komposisi kitosan 1.75% (b/v), gom guar 0.35% (b/v), dan glutaraldehida 4% (v/v).
Tabel 5 Penguraian kadar ketoprofen selamauji dipercepat 3 bulan Formula R2 Orde reaksi [A]0a (%b/b) [A]12b (%b/b) [A]Rc (%) [A]Td (%) ke (minggu-1) KAf (%) Usia guna (minggu) 1 0.9632 Orde-0 26.36 22.55 14.45 85.55 0.3174 20.77 8.3 2 0.9608 Orde-0 26.64 21.40 19.67 80.33 0.4365 19.50 6.1 3 0.9200 Orde-0 26.85 18.82 29.91 70.09 0.6699 19.29 4.01 4 0.9139 Orde-0 26.29 20.91 20.46 79.54 0.4481 20.69 5.87 5 0.9612 Orde-0 27.04 21.14 21.82 78.18 0.4921 19.51 5.49 6 0.9438 Orde-0 27.71 22.95 17.18 82.82 0.3970 20.56 6.98 7 0.9397 Orde-0 27.30 23.69 13.22 86.78 0.3010 19.33 9.07 8 0.9557 Orde-0 28.25 22.68 19.72 80.28 0.4640 20.58 6.09 9 0.9581 Orde-0 26.33 20.86 20.77 79.23 0.4558 19.90 5.78 10 0.9164 Orde-0 28.17 22.93 18.60 81.4 0.4368 18.48 6.45
aKadar awal ketoprofen; bKadar ketoprofen setelah 12 minggu; c% pelepasan ketoprofen setelah 12 minggu; d %Kadar ketoprofen
yang masih tersalut pada t = 12 minggu; elaju penguraian ketoprofen; fKadar Air
Pencirian Mikrokapsul dengan SEM
Hasil SEM mikrokapsul uji stabilitas formula 7 dan formula 3 ditunjukkan pada Gambar 13. Pada Gambar 13a tampak bahwa mikrokapsul memiliki ukuran yang lebih beragam, yaitu dengan diameter 1.25–23.01 µm. Mikrokapsul yang dihasilkan diduga berinti banyak, sehingga antara mikrokapsul yang satu dan yang lain dalam komposisi bahan penyalut yang sama memiliki jumlah inti yang berbeda. Hal ini menyebabkan jumlah ketoprofen yang tersalut berbeda-beda, sehingga dihasilkan ukuran mikrokapsul yang beragam. Gambar 13a, yang merupakan mikrokapsul dengan persentase penyalutan kadar ketoprofen paling besar, tetapan laju penguraian (k) paling kecil dan usia guna paling panjang (formula 7) memperlihatkan ukuran yang lebih besar. Ukuran yang besar menunjukkan bahwa mikrokapsul telah menyalut ketoprofen cukup banyak, sebagaimana hasil penelitian Sugita et al. (2007b) yang menyatakan bahwa mikrokapsul dengan penambahan ketoprofen (Gambar 9) berukuran lebih besar dibandingkan dengan yang tanpa penambahan ketoprofen (Gambar 8). Sementara itu, pada Gambar 13b, yang merupakan mikrokapsul dengan persentase penyalutan ketoprofen paling kecil, tetapan laju penguraian (k) ketoprofen paling besar, dan usia guna paling pendek
(formula 3) memperlihatkan diameter yang lebih kecil, yaitu 2.73–17.9 µm.
Bila dilihat dari komposisi bahan penyalut (kitosan, gom guar, dan glutaraldehida) formula 3 seharusnya memiliki persentase kadar ketoprofen yang lebih besar dibandingkan dengan formula 7. Penambahan lebih banyak glutaraldehida membuat ikatan silang kitosan-kitosan menjadi rapat, sedangkan penambahan gom guar dapat melemahkan ikatan tersebut. Kenyataannya dalam larutan kitosan yang sama, formula 3 yang memiliki kadar gom guar terendah dan glutaraldehida tertinggi, memiliki persentase kadar ketoprofen yang lebih kecil daripada formula 7 yang kadar gom guarnya tertinggi dan glutaraldehidanya terendah. Hal ini diduga karena membran kitosan-gom guar dari formula 3 terlalu rapat, sehingga distribusi ketoprofen ke dalam membran saat pembuatan mikrokapsul akan sulit terjadi. Akibatnya banyak ketoprofen yang masih berada di permukaan membran. Fenomena inilah yang menyebabkan ukuran mikrokapsul formula 3 lebih kecil daripada formula 7.
Hasil SEM untuk kedua formula juga menunjukkan ukuran mikrokapsul yang lebih besar dibandingkan dengan sebelum diuji stabilitasnya (Gambar 9 dengan diameter mikrokapsul 1.0−11 µm). Hal ini diduga disebabkan oleh tingginya kelembapan selama penyimpanan untuk uji stabilitas. Kelembapan yang tinggi menyebabkan pembengkakan
membran penyalut, sehingga diameter mikrokapsul akan semakin membesar.
Gambar 12 (a) Foto SEM permukaan mikrokapsul ketoprofen hasil uji stabilitas formula 7 dan (b) formula 3.
SIMPULAN DAN SARAN
Simpulan
Berdasarkan data uji stabilitas diperoleh bahwa formula yang menunjukkan stabilitas yang tinggi adalah formula 7 dengan komposisi gom guar dan glutaraldehida berturut-turut 0.75% (b/v), dan 3% (v/v) dalam kitosan 1.75% (b/v). Formula ini memiliki kadar ketoprofen tersalut sebesar 86.78%, tetapan laju pelepasan 0.3010 minggu-1, dan usia guna 9.07 minggu. Sementara
itu, formula yang menunjukkan stabilitas yang rendah adalah formula 3 dengan komposisi gom guar dan glutaraldehida berturut-turut 0.35% (b/v), dan 4% (v/v) dalam kitosan 1.75% (b/v). Formula ini memiliki kadar ketoprofen tersalut sebesar 70.09%, tetapan laju pelepasan 0.6699 minggu-1, dan usia guna 4.01 minggu. Hasil SEM
mikrokapsul sebelum uji stabilitas menunjukkan diameter berkisar 1.0–11 µm, sedangkan hasil SEM setelah uji stabilitas untuk formula 7
menunjukkan diameter berkisar 1.25–23.01 µm dan formula 3 berkisar 2.73–17.9 µm.
Saran
Diperlukan penelitian lebih lanjut untuk menyimpan sediaan mikrokapsul menggunakan
silica gel untuk mempertahankan nilai kadar air.
Agar didapat nilai kadar air yang tidak fluktuatif, kecepatan pengadukan saat pembuatan gel dan kecepatan saat penyemprotan dibuat sama untuk mendapatkan keseragaman ukuran mikrokapsul. Juga perlu dilakukan uji stabilitas dipercepat (3 bulan) pada suhu intermediet (suhu kamar), untuk melihat kestabilan yang lebih bagus. Setelah itu, perlu dilakukan pengujian lebih lanjut terhadap stabilitas mikrobiologi, stabilitas terapi, dan stabilitas toksikologi untuk melengkapi data uji stabilitas.
DAFTAR PUSTAKA
Agoes G. 2001. Studi Stabilitas Sediaan
Farmasi. Bandung: Teknologi Farmasi
Program Pasca Sarjana, Institut Teknologi Bandung.
[AMA] American Medical Association. 1991.
Drug Evaluations. Ed. ke-8.
[Anonim]. 2005. Spray dryer as a microfabrication process. Upperton Particle Technologies. http://wawen\situs\upperton [24 Okt 2005].
[AOAC] Association of Official Analytical Chemists. 1999. Official Methods of Analysis
of AOAC International. 5th Revision. Volume
2. Cunnif P, editor. Maryland: AOAC
International.
Berger J et al. 2004. Structure and interactions in covalently and ionically crosslinked chitosan hydrogels for biomedical applications. Eur J
Pharm and Biopharm 57:193-194
Cardenas A, Monal WA, Goycoolea FM, Ciapara IH, Peniche C. 2003. Diffusion through membranes of polyelectrolyte complex of chitosan and alginate. Macromol
Biosci 3:535-539.
a
b
20 kV 2000 x 1.25-23.01µm
Deymonaz C, Hobson M, Diaz D, Guidinger N.
1998. Spray drying.
http://www.wsu.edu/gmhyde/43_web_pages/ drying-web-pages98/spray-dry/ spray-drying-intro.htm [9 Jan 2006].
Fardiaz D. 1989. Hidrokoloid. Bogor: Pusat Antar Universitas Pangan dan Gizi, Institut Pertanian Bogor.
Fennema OR. 1976. Food Chemistry. Ed ke-2. New York and Basel: Marcel Dekker, inc. Jamaludin MA. 1994. Isolasi dan pencirian
kitosan limbah udang windu (Penaeus
monodon fabricus) dan afinitasnya terhadap
ion logam Pb2+, Cr6+, dan Ni2+ [skripsi]. Bogor:
Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Khan TA, Peh KK, Ch’ng HS. 2002. Reporting degree of deacetylation values of chitosan: The influence of analytical methods. J Pharm
Pharmaceut Sci 5:205-212.
Kshirsagar NA. 2000. Drug delivery system.
Indian J Pharmacol 32:54-61.
Nata F, Sugita P, Sjahriza A, Arifin B. 2007. Diffusion behavior of ketoprofen through chitosan-guar gum gel membranes.
Proceedings International Conference and Workshop on Basic and Applied Sciences
[6−7 Agustus 2007], in press.
Nussinovitch A. 1997. Hydrocolloid
Applications. Israel: Chapman and Hall.
Oliveira BF, Santana MHA, Re MI. 2005. Spray dried chitosan microsphere cross-linked with D,L-glyceraldehyde as a potential drug delivery system: Preparation and characterization. Brazilian J Chem Eng 22:353-360.
Patil PR, Praveen S, Rani RHS, Paradkar AR. 2005. Bioavailability assessment of ketoprofen incorporated in gelled self-emulsifying formulation: a technical note.
AAPS Pharm Sci Tech 6:E9-E13.
Stevens MP. 2001. Kimia Polimer. Sopyan I, Penerjemah. Jakarta: PT Pradnya Paramita. Terjemahan dari: Polymer Chemistry: An
Introduction.
Sugita P, Sjahriza A, Lestari SI. 2006a. Sintesis dan optimalisasi gel kitosan-gom guar. J
Natur 9:32-36.
Sugita P, Sjahriza A, Wahyono D. 2006b. Sintesis dan optimalisasi gel kitosan-alginat.
J Sains Teknol 8:133-137.
Sugita P, Sjahriza A, Rachmanita. 2006c. Sintesis dan optimalisasi gel kitosan-karboksimetil selulosa. Di dalam: Arifin B, Wukisari T, Gunawan S, Wahyuni WT,
editor. Prosiding Seminar Nasional
Himpunan Kimia Indonesia; Bogor, 12 Sep
2006. Bogor: Departemen Kimia FMIPA Institut Pertanian Bogor bekerja sama dengan Himpunan Kimia Indonesia Cabang Jawa Barat dan Banten. Hlm 380-386
Sugita P, Sjahriza A, Utomo DW. 2007a. Optimization synthesis chitosan-xanthan gum gel for metal adsorption. Proceedings 1st
International Conference on Chemical Science Yogyakarta-Indonesia, 24-26 Mei
2007.
Sugita P, Amelia F, Srijanto B, Arifin B, Wukirsari T. 2007b. Perilaku disolusi ketoprofen tersalut gel kitosan-gom guar.
JSChem, in press.
Sutriyo, Joshita D, Indah R. 2005. Perbandingan pelepasan propanolol hidroklorida dari matriks kitosan, etil selulosa, dan hidroksipropil metil selulosa. Maj Ilmu
Kefarmasian 2:145-153.
Tarbojevich M, Cosani A. 1996. Molecular weight determination of chitin and chitosan. Di dalam: Muzarelli RAA, Peter MG, editor.
Chitin Handbook. Ancona: European Chitin
Society 85-108.
[USP] United States Pharmacopoeia. 2003. US
Pharmacopeia 2003. Maryland: The United
States Pharmacopeial Convention.
Wang T, Turhan M, Gunasekaram S. 2004. Selected properties of pH-sensitive, biodegradable chitosan-poly(vinyl alcohol) hydrogel. Polym Int 53:911-918.
Winarno FG. 1997. Kimia Pangan dan Gizi. Jakarta: Gramedia.
Yamada T, Onishi H, Machida Y. 2001. In vitro and in vivo evaluation of sustained release chitosan-coated ketoprofen microparticles.
Yakugaku Zasshi 121:239-245.
Yoshizawa H. 2004. Trends in microencapsulation reseach. KONA 20. [terhubung berkala]. http.// www.kona.or.jp/search/22_023.pdf [22 Sep 2005].
Lampiran 1 Diagram alir penelitian ¾ Penelitian pendahuluan
¾ Penelitian utama
Pembuatan campuran kitosan-gom guar dengan konsentrasi kitosan tetap 1.75%, gom guar 0.35;
0.55; 0.75%, glutaraldehida 3; 3.5; 4% dan campuran kitosan 1.75%, gom guar 0.35%, glutaraldehida 3.75% (kondisi optimum Sugita et
al. [2007b])
Pembuatan Mikrokapsul (metode pengeringan semprot)
Pencirian morfologi mikrokapsul dengan SEM Ketoprofen 5 ml Tween-80 2 % Kadar Air (Moisture Analyzer) Produk Mikrokapsul Uji Stabilitas (Climatic Chamber) Kadar Ketoprofen (Spektrofotometer UV) Kitosan Kadar Air
(gravimetri) (gravimetri)Kadar Abu (FTIR metode garis dasar)Derajat Deasetilasi Bobot Molekul
Lampiran 2 Penetapan kadar air dan kadar abu kitosan (a) Penetapan kadar air (AOAC 1999)
Kadar air kitosan ditentukan dengan metode gravimetri. Sebanyak kira-kira 1.0000 g kitosan dimasukkan ke dalam cawan porselen yang telah diketahui bobotnya, kemudian cawan beserta isinya dimasukkan ke dalam oven pada suhu 105°C selama 3 jam atau sampai bobotnya konstan. Setelah itu, dimasukkan ke dalam desikator dan ditimbang. Pengeringan dan penimbangan diulang setiap jam sampai diperoleh bobot konstan. Kadar air kitin/kitosan dihitung dengan persamaan awal sampel bobot kering sampel bobot awal sampel bobot air Kadar = − × 100%
(b) Penetapan kadar abu (AOAC 1999)
Penetapan kadar abu kitosan juga dilakukan secara gravimetri. Cawan porselen dibersihkan dan dimasukkan ke dalam tanur untuk menghilangkan sisa-sisa kotoran yang menempel dalam cawan, kemudian didinginkan dalam eksikator dan ditimbang. Sebanyak kira-kira 0.5000 g kitin/kitosan dimasukkan ke dalam cawan tersebut dan dipanaskan sampai tidak berasap, kemudian dibakar dalam tanur pengabuan dengan suhu 600 °C sampai diperoleh abu berwarna putih. Setelah itu, cawan beserta isinya didinginkan dalam eksikator dan ditimbang. Kadar abu kitin/kitosan dihitung dengan persamaan
100% sampel bobot abu bobot abu Kadar = ×
Lampiran 3 Kadar air dan abu kitosan
Ulangan ke- Kadar air (%) Kadar abu (%) 1 10.71 0.44 2 10.90 0.53 3 10.78 0.62
Lampiran 4 Spektrum FTIR dan penentuan derajat deasetilasi kitosan (Khan et al. 2002)
Derajat deasetilasi kitosan ditentukan menggunakan FTIR. Kitosan yang diperoleh dibuat pelet dengan KBr 1%, kemudian dilakukan penyusuran pada bilangan gelombang antara 4000 dan 400 cm-1. Derajat deasetilasi ditentukan dengan metode garis dasar.
Puncak tertinggi dicatat dan diukur dari garis dasar yang dipilih. Nilai absorbans dapat dihitung dengan menggunakan rumus
P 0 P log
A=
P0 = % transmitans pada garis dasar
P = % transmitans pada puncak minimum
Kitin yang terdeasetilasi sempurna (100%) memiliki nilai A1655 = 1.33. Dengan membandingkan
absorbans pada bilangan gelombang 1655 cm-1 (serapan pita amida I) dengan absorbans pada
bilangan gelombang 3450 cm-1 (serapan gugus hidroksil), % derajat deasetilasi dapat dihitung
dengan persamaan % DD = 1 – 100% 1,33 1 3450 A 1655 A × ×
dengan: A1655 = absorbans pada bilangan gelombang 1655 cm-1 (serapan pita amida)
A3450 = absorbans pada bilangan gelombang 3450 cm-1 (serapan gugus hidroksil)
A1655 = log 2.6 11.0 = 0.6264 A3450 = log 0.4 15.1 = 1.5769 % DD = × − ) 33 . 1 1 5769 . 1 6264 . 0 ( 1 × 100 % = 70.13%
Lampiran 5 Penentuan bobot molekul kitosan (Tarbojevich & Cosani 1996)
Bobot molekul kitosan ditentukan dengan menggunakan metode viskometri Ostwald. Sebanyak kira-kira 0.1000 g kitosan dilarutkan dalam 100 mL asam asetat 0.5 M, kemudian diambil sebanyak 5 mL dan dimasukkan ke dalam viskometer untuk ditentukan waktu alirnya. Pengukuran juga dilakukan untuk beberapa konsentrasi kitosan lainnya
Waktu alir larutan kitosan
Konsentrasi Waktu alir (detik) Rata-rata ln(t/t0 -1)
0.00 65.90 65.80 65.80 65.70 0.02 81.30 81.33 -1.44385 81.20 81.50 0.05 99.40 99.80 -0.66026 100.30 99.70 0.07 126.10 126.47 -0.08117 126.70 126.60 0.09 129.40 129.17 -0.03763 129.10 129.00
Kemudian dibuat kurva hubungan antara lnηsp/c dengan c sehingga diperoleh persamaan:
lnηsp/c =ln [η] + k’ [η]2 c
x y a b
Kurva hubungan konsentrasi (%) dengan ln(t/t0 -1)
Bobot molekul kitosan dihitung dengan menggunakan persamaan Mark-Houwink: Viskositas relatif ηr = η/ηo ≅ t/to Viskositas spesifik ηsp =ηr -1 Viskositas intrinsik [η] = (ηsp/c)c=0 [η] = KMα dengan K = 3.5 x 10-4 mL/g α = 0.76 t = waktu alir zat t0 = waktu alir pelarut
η = viskositas zat
η0 = viskositas pelarut
M = bobot molekul zat
Kurva Penentuan Bobot Molekul
y = 22,87x - 1,8502 R2 = 0,9551 -2 -1,5 -1 -0,5 0 0,5 0,02 0,04 0,06 0,08 0,1 Konsentrasi (%) ln(t/to - 1)
Lanjutan lampiran 5
Dengan menggunakan mode regresi linear diperoleh persamaan: ηsp/c = [η]+k’[η]c sama dengan y = -1.8502 + 22.8699 x
Jadi ln[η] = 0.1572
untuk rumus [η] = KMa, maka 0.1572 = 3.5 × 10-4 × M0.76
sehingga diperoleh M = 3090.45 g/mol
Lampiran 6 Absorbans larutan ketoprofena pada berbagai panjang gelombang (λ)
Panjang Gelombang (nm) Absorbans
253.0 0.6898 253.2 0.6909 253.4 0.6923 253.6 0.6934 253.8 0.6941 254.0 0.6950 254.2 0.6957 254.4 0.6967 254.6b 0.6969 254.8 0.6969 255.0 0.6968 255.2 0.6959 255.4 0.6956 255.6 0.6951 255.8 0.6942 256.0 0.6936 Keterangan: a = konsentrasi 10 mg/L
b = panjang gelombang maksimum (λ maks)
Lampiran 7 Kurva standar larutan ketoprofen pada berbagai konsentrasi (λmaks = 254.6 nm) [Ketoprofen] (mg/l) Absorbans 1.0005 0.060 2.0010 0.125 3.0015 0.191 4.0020 0.270 5.0025 0.330 6.0030 0.395 7.0035 0.467 8.0040 0.537 9.0045 0.605 10.0050 0.691 11.0055 0.756 12.0060 0.820 13.0065 0.905 14.0070 0.954 15.0075 1.022 y = 0.069x - 0.014 R² = 0.999 0 0.2 0.4 0.6 0.8 1 1.2 0 5 10 15 20 A b sor b an s Konsentrasi Ketoprofen (mg/L)
Lampiran 8 Data kadar air selama 3 bulan
Formula Isi Ulangan Kadar Air (%) minggu ke-
0 1 2 3 4 5 6 7 8 9 10 11 12 Kit 1.75% 1 20.53 19.26 17.44 24.34 17.98 23.99 17.96 23.56 18.48 26.24 20.71 21.84 23.43 1 GG 0.35% 2 18.41 22 20.3 22.27 21.61 21.39 19.62 19.13 20.88 20.31 17.33 22.94 20.24 Glu 3% Rerata 19.47 20.63 18.87 23.305 19.795 22.69 18.79 21.345 19.68 23.275 19.02 22.39 21.835 Kit 1.75% 1 22.75 20.09 19.34 21.24 17.98 20.92 18.14 22.78 21.93 21.18 19.25 17.97 19.9 2 GG 0.35% 2 18.94 21.11 18.32 20.36 17.22 21.73 20.31 15.87 21.23 20.01 15.01 14.72 18.73 Glu 3.5% Rerata 20.845 20.6 18.83 20.8 17.6 21.325 19.225 19.325 21.58 20.595 17.13 16.345 19.315 Kit 1.75% 1 17.01 19.17 17.84 18.38 16.35 20.27 17.68 18.04 18.39 19.23 18.57 18.57 18.57 3 GG 0.35% 2 19.9 20.64 19.68 22.85 17.03 21.31 20.81 21.02 22.42 22.01 17.43 18.28 19.98 Glu 4% Rerata 18.455 19.905 18.76 20.615 16.69 20.79 19.245 19.53 20.405 20.62 18 18.425 19.275 Kit 1.75% 1 20.52 19.06 18.04 21.36 18.94 25.29 22.98 21.17 22.13 25.76 19.14 18.63 20.65 4 GG 0.55% 2 20.96 20.18 17.89 21.99 17.4 24.48 18.83 19.91 21.35 22.96 21.34 19.28 17.65 Glu 3% Rerata 20.74 19.62 17.965 21.675 18.17 24.885 20.905 20.54 21.74 24.36 20.24 18.955 19.15 Kit 1.75% 1 20.71 20.25 16.58 18.93 18.1 22.61 16.86 19.29 19.81 19.05 17.31 14.33 19.44 5 GG 0.55% 2 24.89 22.78 16.26 24.9 18.4 19.2 17.65 18.19 20.7 22.86 18.09 19.14 20.92 Glu 3.5% Rerata 22.8 21.515 16.42 21.915 18.25 20.905 17.255 18.74 20.255 20.955 17.7 16.735 20.18 Kit 1.75% 1 18.72 24.06 17.37 22 20.77 22.12 17.92 19.7 22.65 20.25 17.25 21.74 20.64 6 GG 0.55% 2 21.45 21.91 17.46 19.86 19.35 19.37 18.4 21.77 24.72 25.84 17.24 21.24 20.88 Glu 4% Rerata 20.085 22.985 17.415 20.93 20.06 20.745 18.16 20.735 23.685 23.045 17.245 21.49 20.76 Kit 1.75% 1 20.85 18.73 18.26 19.79 18.94 22.6 18.05 17.71 19.46 20.2 17.01 17.43 21.18 7 GG 0.75% 2 21.35 20.28 18.05 20.64 16.53 20.82 19.63 18.03 19.36 21.67 19.08 17.74 19.28 Glu 3% Rerata 21.1 19.505 18.155 20.215 17.735 21.71 18.84 17.87 19.41 20.935 18.045 17.585 20.23 Kit 1.75% 1 22.25 20.42 16.1 22.03 16.67 24.98 17.71 24.83 23.17 21.14 18.7 18.15 20.47 8 GG 0.75% 2 20.62 19.18 18.53 25.67 17.23 24.9 17.42 22.62 22.69 21.27 19.46 19.46 19.46 Glu 3.5% Rerata 21.435 19.8 17.315 23.85 16.95 24.94 17.565 23.725 22.93 21.205 19.08 18.805 19.965 Kit 1.75% 1 20.45 18.39 17.43 20.88 17.24 20.48 16.3 22.57 24.07 20.14 19.7 20.04 20.99 9 GG 0.75% 2 19.27 21.99 16.67 19.92 17.31 20.63 17.98 24.39 18.39 18.35 21.15 21.75 20.8 Glu 4% Rerata 19.86 20.19 17.05 20.4 17.275 20.555 17.14 23.48 21.23 19.245 20.425 20.895 20.895 Kit 1.75% 1 17.9 17.68 14.35 19.02 18.13 20.59 17.38 20.38 19.65 23.04 19.78 20.07 19.46 10 GG 0.35% 2 20.9 20.2 15.16 17.92 18.94 21.63 15.72 18.41 19.9 18.52 15.28 15.28 15.28 Glu 3.75% Rerata 19.4 18.94 14.755 18.47 18.535 21.11 16.55 19.395 19.775 20.78 17.53 17.675 17.37
Lampiran 9 Data kadar ketoprofen selama 3 bulan
Formula Isi Ulangan Kadar Ketoprofen (%b/v) minggu ke-
0 1 2 3 4 5 6 7 8 9 10 11 12 Kit 1.75% 1 27.02 25.72 25.35 24.44 26.92 23.1 24.66 22.47 24.97 25.19 22.01 21.5 21.84 1 GG 0.35% 2 26.14 25.64 25.49 26.32 23.28 26.76 25.12 25.69 22.93 22.37 23.95 24.16 22.72 Glu 3% Rerata 26.58 25.68 25.42 25.38 25.1 24.93 24.89 24.08 23.95 23.78 22.98 22.83 22.28 Kit 1.75% 1 25.15 34.11 27.91 26.01 24.68 22.61 24.07 23.93 23.44 21.98 23.64 22.73 21.7 2 GG 0.35% 2 27.99 21.75 23.85 25.27 24.71 25.75 23.83 23.04 22.65 24 22.07 19.91 15.55 Glu 3.5% Rerata 26.57 27.93 25.88 25.64 24.7 24.18 23.95 23.49 23.05 22.99 22.86 21.32 18.63 Kit 1.75% 1 24.87 24.59 23.81 24.69 22.81 21.59 21.86 20.55 20.86 20.63 18.1 13.58 20.86 3 GG 0.35% 2 33.62 24.97 29.21 24.89 25.97 25.48 23.99 26.39 21.58 20.93 19.48 24.42 17.35 Glu 4% Rerata 29.25 24.78 26.51 24.79 24.39 23.54 22.93 23.47 21.22 20.78 19.48 19 19.11 Kit 1.75% 1 28.19 26.33 24.14 19.89 24.3 26.32 22.76 24.59 23.57 23.17 22.04 23.63 22.62 4 GG 0.55% 2 24.65 25.07 24.76 29.49 24.6 22.72 25.44 22.94 22.22 22.64 21.25 19.05 17.09 Glu 3% Rerata 26.42 25.7 24.45 24.69 24.45 24.52 24.1 23.77 22.9 22.91 21.65 21.34 19.86 Kit 1.75% 1 25.15 26.76 29.1 27.54 23.06 23.91 24.22 21.44 25.21 23.74 21.59 22.72 24.37 5 GG 0.55% 2 27.43 27.54 24.04 23.8 26.37 24.71 24.26 25.21 21.44 21.52 22.87 21.12 17.14 Glu 3.5% Rerata 26.29 27.15 26.57 25.67 24.72 24.31 24.24 23.33 23.33 22.63 22.23 21.92 20.76 Kit 1.75% 1 39.75 24.4 25.61 25.42 25.89 30.13 23.55 26.11 24.7 22.36 21.87 23.78 25.35 6 GG 0.55% 2 26.29 32.41 27.35 28.42 26.87 23.66 27 23.61 24.8 25.16 24.81 23.84 20.55 Glu 4% Rerata 33.02 28.41 26.48 26.92 26.38 26.9 25.28 24.86 24.75 23.76 23.34 23.81 22.95 Kit 1.75% 1 27.02 27.59 25.37 27.44 25.54 26.33 24.64 27.25 28.05 25.4 23.7 24.29 24.02 7 GG 0.75% 2 26.84 26.49 27.41 25.37 26.89 25.71 27.09 23.44 22.7 24.68 25.06 23.09 22.32 Glu 3% Rerata 26.93 27.04 26.39 26.41 26.22 26.02 25.87 25.35 25.375 25.04 24.38 23.69 23.17 Kit 1.75% 1 28.47 27.41 20.52 24.07 26.81 27.09 26.75 25.49 26.42 25.82 24.91 22.31 23.56 8 GG 0.75% 2 27.41 28.89 30.72 31.72 27.83 26.26 25.99 24.99 23.36 23.36 22.94 25.26 21.59 Glu 3.5% Rerata 27.94 28.15 25.62 27.9 26.81 26.68 26.37 25.24 24.89 24.59 23.93 23.79 22.58 Kit 1.75% 1 26.87 27.05 26.05 24.76 26.87 25.73 25.27 25.6 23.99 25.09 23.78 21.12 22.07 9 GG 0.75% 2 22 23.13 25.82 25.78 22 21.57 21.84 21.46 21.27 20.34 19.29 21.3 19.31 Glu 4% Rerata 24.45 25.09 25.94 25.27 24.44 23.65 23.56 23.53 22.63 22.72 21.54 21.21 20.69 Kit 1.75% 1 29.6 27.41 31.23 29.54 19.89 27.01 27.87 26.91 26.35 24.87 25.63 24.02 26.14 10 GG 0.35% 2 27.41 26.59 23.51 21.27 29.49 24.86 22.93 24.3 23.07 33.62 23.96 22.53 17.88 Glu 3.75% Rerata 28.51 27 27.37 25.41 24.69 25.94 25.4 25.61 24.71 29.25 24.8 23.28 22.01
Lampiran 10 Penentuan orde reaksi penguraian ketoprofen dalam mikrokapsul hasil uji stabilitas (metode grafis) ¾ Formula 1 (Kitosan 1.75%, Gom Guar 0.35%, Glutaraldehida 3% dan zat aktif ketopofen)
Waktu % Ketoprofen rerata (b/b)
(minggu) [A]t (%) ln [A]t 1/[A]t 1/(2[A]t2)
0 26.58 3.2802 0.0376 0.0007 1 25.68 3.2457 0.0389 0.0008 2 25.42 3.2355 0.0393 0.0008 3 25.38 3.2340 0.0394 0.0008 4 25.10 3.2229 0.0398 0.0008 5 24.93 3.2161 0.0401 0.0008 6 24.89 3.2145 0.0402 0.0008 7 24.08 3.1814 0.0415 0.0009 8 23.95 3.1760 0.0418 0.0009 9 23.78 3.1688 0.0421 0.0009 10 22.98 3.1346 0.0435 0.0009 11 22.83 3.1281 0.0438 0.0010 12 22.28 3.1037 0.0449 0.0010
Kurva regresi untuk orde reaksi 0 Kurva regresi untuk orde reaksi 1
Kurva regresi untuk orde reaksi 2 Kurva regresi untuk orde reaksi 3
¾ Formula 2 (Kitosan 1.75%, Gom Guar 0.35%, Glutaraldehida 3.5% dan zat aktif ketopofen)
Waktu % Ketoprofen rerata (b/b)
(minggu) [A]t (%) ln [A]t 1/[A]t 1/(2[A]t2)
0 26.57 3.2798 0.0376 0.0007 2 25.88 3.2535 0.0386 0.0007 3 25.64 3.2442 0.0390 0.0008 4 24.70 3.2068 0.0405 0.0008 5 24.18 3.1855 0.0414 0.0009 6 23.95 3.1760 0.0418 0.0009 7 23.49 3.1565 0.0426 0.0009 8 23.05 3.1377 0.0434 0.0009 9 22.99 3.1351 0.0435 0.0009 10 22.86 3.1294 0.0437 0.0010 11 21.32 3.0596 0.0469 0.0011
Kurva regresi untuk orde reaksi 0 Kurva regresi untuk orde reaksi 1
Kurva regresi untuk orde reaksi 2 Kurva regresi untuk orde reaksi 3
¾ Formula 3 (Kitosan 1.75%, Gom Guar 0.35%, Glutaraldehida 4% dan zat aktif ketopofen)
Waktu % Ketoprofen rerata (b/b)
(minggu) [A]t (%) ln [A]t 1/[A]t 1/(2[A]t2)
1 24.78 3.2100 0.0404 0.0008 2 26.51 3.2775 0.0377 0.0007 3 24.79 3.2104 0.0403 0.0008 4 24.39 3.1942 0.0410 0.0008 5 23.54 3.1587 0.0425 0.0009 6 22.93 3.1324 0.0436 0.0010 7 23.47 3.1557 0.0426 0.0009 8 21.22 3.0549 0.0471 0.0011 9 20.78 3.0340 0.0481 0.0012 10 19.48 2.9694 0.0513 0.0013 11 19.00 2.9444 0.0526 0.0014 12 19.11 3.2100 0.0404 0.0008
Kurva regresi untuk orde reaksi 0 Kurva regresi untuk orde reaksi 1
Kurva regresi untuk orde reaksi 2 Kurva regresi untuk orde reaksi 3
¾ Formula 4 (Kitosan 1.75%, Gom Guar 0.55%, Glutaraldehida 3% dan zat aktif ketopofen) Waktu % Ketoprofen rerata (b/b)
(minggu) [A]t (%) ln [A]t 1/[A]t 1/(2[A]t2)
0 26.42 3.2741 0.0379 0.0007 1 25.70 3.2465 0.0389 0.0008 2 24.45 3.1966 0.0409 0.0008 3 24.69 3.2064 0.0405 0.0008 4 24.45 3.1966 0.0409 0.0008 5 24.52 3.1995 0.0408 0.0008 6 24.10 3.1822 0.0415 0.0009 7 23.77 3.1684 0.0421 0.0009 8 22.90 3.1311 0.0437 0.0010 9 22.91 3.1316 0.0436 0.0010 10 21.65 3.0750 0.0462 0.0011 11 21.34 3.2741 0.0379 0.0007 12 19.86 3.2465 0.0389 0.0008
Kurva regresi untuk orde reaksi 0 Kurva regresi untuk orde reaksi 1
Kurva regresi untuk orde reaksi 2 Kurva regresi untuk orde reaksi 3
¾ Formula 5 (Kitosan 1.75%, Gom Guar 0.55%, Glutaraldehida 3.5% dan zat aktif ketopofen)
Waktu % Ketoprofen rerata (b/b)
(minggu) [A]t (%) ln [A]t 1/[A]t 1/(2[A]t2)
0 26.29 3.2692 0.0380 0.0007 1 27.15 3.3014 0.0368 0.0007 2 26.57 3.2798 0.0376 0.0007 3 25.67 3.2453 0.0390 0.0008 4 24.72 3.2076 0.0405 0.0008 5 24.31 3.1909 0.0411 0.0008 6 24.24 3.1880 0.0413 0.0009 7 23.33 3.1497 0.0429 0.0009 8 23.33 3.1497 0.0429 0.0009 9 22.63 3.1193 0.0442 0.0010 10 22.23 3.1014 0.0450 0.0010 11 21.92 3.2692 0.0380 0.0007 12 20.76 3.3014 0.0368 0.0007
Kurva regresi untuk orde reaksi 0 Kurva regresi untuk orde reaksi 1
Kurva regresi untuk orde reaksi 2 Kurva regresi untuk orde reaksi 3
¾ Formula 6 (Kitosan 1.75%, Gom Guar 0.55%, Glutaraldehida 4% dan zat aktif ketopofen)
Waktu % Ketoprofen rerata (b/b)
(minggu) [A]t (%) ln [A]t 1/[A]t 1/(2[A]t2)
2 26.48 3.2764 0.0378 0.0007 3 26.92 3.2929 0.0371 0.0007 4 26.38 3.2726 0.0379 0.0007 6 25.28 3.2300 0.0396 0.0008 7 24.86 3.2133 0.0402 0.0008 8 24.75 3.2088 0.0404 0.0008 9 23.76 3.1680 0.0421 0.0009 10 23.34 3.1502 0.0428 0.0009 11 23.81 3.1701 0.0420 0.0009 12 22.95 3.1333 0.0436 0.0009
Kurva regresi untuk orde reaksi 0 Kurva regresi untuk orde reaksi 1
Kurva regresi untuk orde reaksi 2 Kurva regresi untuk orde reaksi 3


![Tabel 3 Konsentrasi ketoprofen dalam mikrokapsul kitosan-gom guar [Ketoprofen] (%b/b) Formula minggu ke-0 minggu ke-12 [Ketoprofen] Sugita et al](https://thumb-ap.123doks.com/thumbv2/123dok/4429864.2965843/18.918.172.452.563.753/konsentrasi-ketoprofen-mikrokapsul-kitosan-ketoprofen-formula-ketoprofen-sugita.webp)
![Tabel 5 Penguraian kadar ketoprofen selama uji dipercepat 3 bulan Formula R 2 Orde reaksi [A] 0 a (%b/b) [A] 12 b (%b/b) [A] R c (%) [A] T d(%) k e (minggu -1 ) KA f (%) Usia guna (minggu) 1 0.9632 Orde-0 26.36 22.55 14.4](https://thumb-ap.123doks.com/thumbv2/123dok/4429864.2965843/20.918.119.796.131.464/tabel-penguraian-ketoprofen-selama-dipercepat-formula-reaksi-minggu.webp)
