BAB I I
TINJAUAN PUSTAKA
A. Babat (Tripe)
Babat (Tripe) sesungguhnya adalah bagian dalam kulit lambung hewan (jeroan), yang sering juga disebut “handuk” karena bentuknya yang sangat mirip handuk ( Femina, 15/2009). Jeroan letaknya di dalam rongga dada dan perut, merupakan tempat mencerna dan menampung sisa-sisa makanan sehingga mengandung banyak bakteri (bkpausm.blogspot.com).
Dalam 100 gram babat mengandung : energi 113 kkal, protein 17,6 g, lemak 4 g, vitamin B1 0,1 mg, asam folat 5,7 mkg, kalsium 12 mg, besi 1 mg, seng 2 mg, fosfor 144 mg, kalium 90 mg, kolesterol 145 mg (Made, Astawan, 2009).
Babat banyak disukai oleh orang karena rasanya yang enak meskipun sebenarnya tidak layak dikonsumsi karena mengandung banyak purin dan sifatnya yang mudah membusuk. Dalam 100 gram babat mengandung kadar purin 470 mg (Cahanar dan Suhanda, 2006). Bila seseorang yang mempunyai asam urat disarankan kandungan purin dalam sehari-hari 100 – 150 mg. Babat yang sering beredar di pasaran dan yang sering diolah sebagai campuran makanan adalah babat sapi, dapat digunakan sebagai campuran untuk nasi goreng, nasi kebuli, bakso, dan campuran untuk gulai sapi.
B. Bahan Tambahan Pangan
Bahan Tambahan Pangan (BTP) adalah bahan atau campuran bahan yang secara alami bukan merupakan bagian dari bahan baku pangan, tetapi ditambahkan kedalam pangan untuk mempengaruhi sifat atau bentuk pangan. BTP atau ‘food additive’ yang digunakan harus mempunyai sifat dapat mempertahankan nilai gizi makanan tersebut, tidak mengurangi zat-zat essensial dalam makanan, dapat mempertahankan atau memperbaiki mutu makanan, dan menarik bagi konsumen. Dalam kehidupan sehari-hari BTP sudah umum digunakan namun sering terjadi kontroversi karena banyak produsen pangan yang menggunakan bahan tambahan yang berbahaya bagi kesehatan atau penggunaanya melebihi dari dosis yang diizinkan dalam industri (Mahmud, 2007).
BTP dapat berupa ekstrak bahan alami atau hasil sintesis kimia. Bahan yang berasal dari alam umumnya tidak berbahaya, sementara BTP sintetik mempunyai resiko terhadap kesehatan jika disalahgunakan pemakaianya. Bahan tambahan pangan yang dilarang oleh BPOM (Badan Pengawas Obat dan Makanan) diatur dalam Permenkes RI No.722 / Menkes / Per / IX / 88.
Macam-macam BTP sintetis yang diizinkan penggunaanya oleh BPOM menurut Permenkes RI No.722 / Menkes / Per / IX /88, antara lain :
1. Pewarna, yaitu BTP yang dapat memberi atau memperbaiki warna pada makanan. Contoh pewarna sintetis adalah Carmoisin (merah ungu), Eritrosin (merah muda), Tartrasin (kuning), Green S (hijau), Brown Ht (coklat), Brillian blue (biru).
2. Pemanis, yaitu BTP yang dapat memberikan rasa manis pada makanan. Contohnya adalah Sakarin, Siklamat dan Aspartam.
3. Pengawet, yaitu BTP yang dapat mencegah atau menghambat terjadinya fermentasi, pengasaman atau penguraian lain pada makanan yang disebabkan oleh pertumbuhan mikroba. Contohnya adalah Asam Asetat, Asam propionate, dan Asam benzoat.
4. Penyedap rasa atau penguat aroma, yaitu BTP yang dapat memberikan atau mempertegas rasa dan aroma. Contohnya Monosodium Glutamat (MSG). 5. Antioksidan yaitu BTP yang dapat menghambat atau mencegah proses oksidasi
lemak yang menyebabkan terjadinya ketengikan. Contohnya adalah TBHQ (Tertiary Butylhydroquinon).
Macam-macam BTP sintetis yang dilarang penggunaanya oleh BPOM menurut Permenkes RI No.722 / Menkes / Per / IX /88, antara lain :
1. Kalium klorat, nitrofurazon, dietilpilo karbonat, kloramfenikol, asam salisilat beserta garamnya, rhodamin B (pewarna merah), methanyl yellow (pewarna kuning), kalsium bromat dan minyak nabati yang dibrominasi.
2. Untuk pengawet dalam bahan tambahan pangan yang dilarang penggunaanya diantaranya Asam boraks (Boraks) dan Formalin (smallcrab.com).
C. Formalin 1. Definisi Formalin
Formalin adalah larutan yang tidak berwarna, baunya sangat menusuk dan memiliki sifat larut dalam air. Didalam formalin terkandung sekitar 37 persen
formaldehid dalam air, biasanya ditambah methanol hingga 15 persen sebagai pengawet. Formalin dikenal sebagai bahan desinfektan dan banyak digunakan dalam industri. Nama lain dari formalin adalah Formol, Methylene aldehyde, Paraforin, Morbicid, Oxomethane, Polyoxymethylene glycols, Methanal, Formoform, Superlysoform, Formaldehyde, Formalith (Made, Astawan, 2006).
Berat molekul formalin adalah 30,03 dengan rumus molekul HCOH, karena kecilnya molekul ini memudahkan absorbsi dan distribusinya ke dalam sel tubuh. Gugus karbonil yang dimilikinya sangat aktif dapat bereaksi dengan gugus –NH2 dari protein yang ada pada tubuh membentuk senyawa yang mengendap (Harmita, 2006). Menghilangkan kadar formalin dalam produk makanan tidak terlalu sulit cukup direbus, digoreng, dan direndam dalam air, maka formalin bisa luntur. Itu menyatakan bahwa karakterisitik formalin adalah mudah larut dalam air sampai dengan konsentrasi 55 persen. Formalin juga sangat reaktif dalam kondisi basa, selain itu titik didih formalin relatif rendah.
2. Penggunaan Formalin
Secara umum formalin mempunyai kegunaan sebagai pengawet mayat, pembasmi lalat dan serangga, bahan pembuatan sutra sintetis, zat pewarna, cermin, kaca, dan peledak. Dalam dunia fotografi biasanya digunakan untuk pengeras lapisan gelatin dan kertas, bahan pembuatan pupuk urea, bahan untuk pembuatan produk parfum, bahan pengawet produk kosmetika dan pengeras kuku, pencegah korosi untuk sumur minyak, bahan untuk isolasi busa, bahan perekat untuk produk kayu lapis (playwood). Dalam konsentrasi yang sangat kecil (< 1 persen) digunakan sebagai pengawet untuk berbagai barang konsumen seperti
pembersih barang rumah tangga, cairan pencuci piring, pelembut, perawatan sepatu, shampoo mobil, lilin, dan pembersih karpet (Made Astawan 2006).
3. Toksisitas Formalin
Toksik yang dihasilkan oleh bahan pengawet kimia formalin apabila masuk kedalam tubuh dapat bersifat karsinogenik atau menimbulkan penyakit kanker pada manusia. Bahaya jangka pendek (akut) apabila tubuh teracuni oleh formalin maka mulut, tenggorokan dan perut terasa terbakar, sakit pada saat menelan, mual, muntah, dan diare, kemungkinan terjadi pendarahan, sakit perut yang hebat, sakit kepala, hipotensi (tekanan darah rendah), kejang, tidak sadar hingga koma. Selain itu juga dapat terjadi iritasi saluran pernafasan, kerusakan hati, jantung, otak, limpa, pankreas, sistem susunan saraf pusat dan ginjal yang timbul dalam jangka panjang.
4. Tindakan Pencegahan dan Pertolongan Pertama Bila Terpapar Formalin
a. Untuk mencegah agar tidak terhirup gunakan alat pelindung pernafasan, seperti masker, kain, atau alat lainnya yang dapat mencegah kemungkinan masuknya formalin ke dalam hidung atau mulut.
b. Untuk mencegah agar tidak terkena mata gunakan pelindung mata atau kacamata pengaman yang tahan terhadap percikan dan sediakan kran air untuk mencuci mata di tempat kerja yang berguna apabila terjadi keadaan darurat. c. Hindari makan, minum dan merokok selama bekerja serta cuci tangan sebelum makan. Apabila diperlukan pertolongan intensif segera hubungi dokter atau dibawa ke rumah sakit.
5. Ciri-ciri Babat Berformalin dan Tanpa Formalin a. Ciri-ciri babat berformalin
Babat yang berformalin mempunyai beberapa ciri antara lain : babat berwarna cerah dan bersih, tekstur kenyal, tidak dihinggapi lalat, bau formalin menyengat, serta tidak rusak atau busuk sampai tiga hari dalam suhu kamar.
b. Ciri-ciri babat tanpa formalin
Babat yang bebas formalin memiliki ciri-ciri tekstur elastis, bau anyir dan banyak dihinggapi lalat (Widodo, 2009).
D. Penurunan kadar formalin pada bahan makanan
Formalin yang terkandung didalam bahan makanan tidak dapat dihilangkan 100 persen, tetapi dapat diturunkan. Penurunan kadar formalin dapat dilakukan dengan menggunakan air bersih mampu menurunkan kadar formalin sampai 61,25 persen pada ikan asin yang direndam selama 60 menit, air leri mampu menurunkan kadar formalin sampai 66,03 persen, air cuka 5 persen selama 15 menit mampu menurunkan kadar formalin sampai 98,53 persen, sedangkan pada air garam mampu menurunkan kadar formalin sampai 89,53 persen yang diterapkan pada ikan laut (Sukesi, 2007).
E. Air garam (Air mengandung NaCl)
Dalam ilmu kimia garam adalah senyawa ionik yang terdiri dari ion positif (kation) dan ion negatif (anion), sehingga membentuk senyawa netral (tanpa bermuatan). Garam terbentuk dari hasil reaksi asam dan basa. Komponen kation
dan anion ini dapat berupa senyawa anorganik seperti klorida (Cl−), dan bisa juga berupa senyawa organik asetat (CH3COO−) dan ion monoatomik seperti fluorida (F−) serta ion poliatomik seperti sulfat (SO42−). Natrium klorida (NaCl), bahan utama garam dapur adalah suatu garam. Misalnya natrium klorida dalam air merupakan larutan elektrolit, yaitu larutan yang dapat menghantarkan arus listrik. Selain itu pada air garam mampu menurunkan kadar formalin sampai 89,53 persen (Sukesi).
F. Metode-metode analisis formalin
1. Uji Kualitatif
a. Uji dengan Fenilhidrazina
Dipipet 1 ml hasil destilat dalam tabung reaksi, ditambahkan 2 tetes Fenilhdrazina hidroklorida, 1 tetes kalium haksasianoferat (III), dan 5 tetes HCl. Jika terjadi warna merah terang maka positif formalin (Farmakope Indonesia. Edisi ketiga, hal : 259).
b. Uji dengan Asam Kromatopat
Dipipet 5 ml larutan asam kromatopat 0,5% dalam H2SO4 60% dimasukkan dalam tabung reaksi, ditambahkan 1 ml larutan hasil destilat sambil diaduk. Tabung reaksi dimasukkan dalam penangas air yang mendidih selama 15 menit dan amati perubahan warna yang terjadi. Formalin positif ditunjukkan adanya warna ungu terang sampai ungu tua (Wisnu, Cahyadi, 2008).
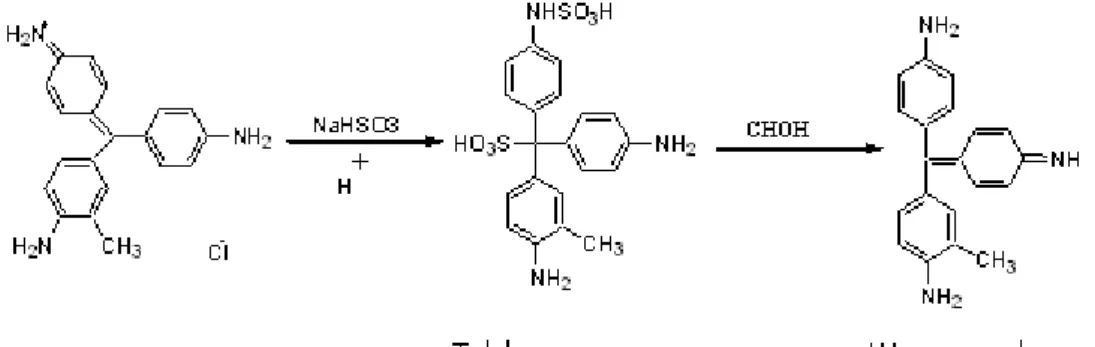
c. Uji dengan Larutan Schiff
Dipipet 1 ml hasil destilat dimasukkan dalam tabung reaksi, ditambahkan 1 ml H2SO4 1:1 (H2SO4 pekat) lewat dinding, kemudian ditambahkan 1 ml larutan schiff. Jika terbentuk warna ungu maka positif formalin (Farmakope Indonesia. Edisi ketiga, hal : 677).
Gambar 1. Reaksi Pembentukan Warna antara Formalin dan Pereaksi Schiff 2. Uji Kuantitatif
a. Dengan metode Asidialkalimetri
Dipipet 10,0 ml hasil destilat dimasukkan dalam erlenmeyer, kemudian ditambah 25 ml hidrogen peroksida encer dan 50 ml natrium hidroksida 0,1 N. Kemudian dipanaskan diatas penangas air hingga pembuihan berhenti, dan dititrasi dengan asam klorida 0,1 N menggunakan indikator larutan phenolphtalin. Dilakukan penetapan blanko, dipipet 50,0 ml NaOH 0,1 N, ditambah 2-3 tetes indikator phenolphtalin, dititrasi dengan HCl 0,1 N. Dimana 1 ml NaOH 0,1 N setara dengan 3,003 mg HCOH (Farmakope Indonesia. Edisi ketiga, hal : 677).
b. Dengan metode Spektrofotometri
Dipipet 5,0 ml destilat masukkan dalam labu ukur 50 ml, ditambahkan aquadest 45 ml kira-kira 5 ml sebelum tanda batas, kemudian ditambahkan 1 ml H2SO4 1:1 (H2SO4 pekat) lewat dinding, ditambahkan 1,0 ml larutan schiff, dan ditepatkan dengan aquadest sampai tanda batas, kemudian dibaca dengan spektrofotometer (Farmakope Indonesia. Edisi ketiga, hal : 677).
G. Spektrofotometer 1. Pengertian
Spektrofotometer adalah suatu alat instrument untuk mengukur transmisi atau absorben suatu sampel dengan cara melewatkan cahaya pada panjang gelombang tertentu pada suatu obyek kaca atau yang disebut kuvet. Sebagian dari cahaya tersebut akan diserap dan sisanya akan dilewatkan. Nilai absorbansi dari cahaya yang dilewatkan akan sebanding dengan konsentrasi larutan di dalam kuvet.
2. Jenis-jenis spektrofotometer
Ada tiga jenis spektrofotometer yang telah dikenal, yaitu : a. Single beam (berkas sinar tunggal) spektrofotometer
Spektrofotometer jenis ini banyak digunakan karena cukup murah dan memberikan hasil yang lebih akurat. Spektrofotometer ini terdiri hanya satu berkas sinar sehingga dalam praktek pengukuran sampel dan blangko atau standar harus dilakukan bergantian dengan ruang sel (ruang kuvet) yang sama.
b. Double beam (berkas sinar ganda) spektrofotometer
Spektrofotometer jenis ini biasa ditemui pada spektrofotomter yang telah memakai automatis absorbansi (A) sebagai fungsi panjang gelombang. Spektrofotometer jenis ini mempunyai dua berkas sinar sehingga dalam pengukuran absorbansi tidak perlu bergantian antara sampel dan blangko, tetapi dapat dilakukan secara paralel.
c. Gilford spektrofotometer
Spektrofotometer jenis ini banyak dipakai di laboratorium biokimia yang mampu membaca tiga absorbansi (A) sampel dalam satu kali kerja. Spektrofotometri jenis ini relatif lebih mahal dari spektrofotometri single beam dan double beam, karena memakai tiga berkas sinar dalam pengukuran absorbansi sampel.
3. Metode Analisis Spektrofotometri
Ada tiga teknik yang bisa digunakan untuk analisis secara spektrofotometri, yaitu a. Metode kurva kalibrasi
Dalam metode ini dibuat suatu baku seri larutan standar dengan berbagai konsentrasi selanjutnya absorbansi dari masing-masing larutan tersebut diukur dengan spektrofotometri. Kemudian dibuat grafik antar konsentrasi dengan absorbansi yang merupakan garis lurus melewati suatu titik.
A Absorbansi total Y : Absorbansi Y = bX + a X : Konsentrasi
a : Konstanta b : Koefisien
C standar = C sampel
Gambar 2. Metode kurva kalibrasi b. Metode standart tunggal
Metode ini sangat praktis karena menggunakan satu larutan standar yang telah diketahui konsentrasinya, selanjutnya absorbansi larutan standar dan absorbansi larutan sampel diukur dengan spektrofotometri.
Rumus perhitungan kadar sampel : Absorbansi sampel
x C standar x P sampel = ... Mg/L(ppm) Absorbansi baku
c. Metode Adisi Standar
Metode ini mampu meminimalisir kesalahan yang disebabkan oleh perbedaan kondisi lingkaran (matriks) sampel dan standar. Dalam metode ini dua atau lebih sejumlah volume tertentu dari sampel dipindahkan ke labu takar. Satu larutan diencerkan sampai volume tertentu dan diukur absorbansinya tanpa ditambah dengan larutan standar, sedangkan larutan yang lain sebelum diukur absorbansinya ditambahkan terlebih dahulu dengan sejumlah tertentu larutan standar dan diencerkan seperti pada larutan yang pertama.
4. Komponen Spektrofotometer
Komponen yang paling penting sekali dari suatu spektrofotometer yang secara skema sebagai berikut :
Gambar 3. Komponen Spektrofotometer Keterangan :
a. Sumber energi cahaya yang berkesinambungan yang meliputi daerah spectrum b. Monokromator, yakni suatu piranti yang menghubungkan dengan pita sempit
panjang gelombang dari spectrum lebar yang dipancarkan oleh sumber cahaya c. Wadah atau kuvet untuk sampel
d. Detektor, yang berupa transduser yang mengubah energi cahaya menjadi suatu isyarat listrik
e. Pengganda (amplifier) dan rangkaian yang berkaitan yang membuat isyarat listrik memadai untuk dibaca
f. Piranti baca (monitor), bertindak dalam menampilkan hasil yang diperoleh Detektor Sampel Monokromator Sumber Pengganda Piranti baca