1
BAB I
PENDAHULUAN
1.1 Latar Belakang
Tulang adalah satu-satunya jaringan tubuh yang mampu beregenerasi secara spontan dan menyusun kembali (remodelling) struktur mikro dan makronya, karena adanya interaksi antara proses osteogenic (pembentukan tulang) dan osteoclastic (resorbsi tulang) (Brighton, 1984). Tulang rahang baik rahang atas maupun rahang bawah merupakan sistem penopang wajah yang berfungsi selain sebagai pembentuk wajah, juga berfungsi untuk pengunyahan, penelanan, bicara dan tempat pertumbuhan gigi geligi sehingga mempengaruhi penampilan estetika seseorang.
Patah tulang adalah terputusnya (diskontinuitas) struktur tulang yang dapat disebabkan oleh trauma mekanis dari luar atau merupakan suatu kelainan patologis seperti osteoporosis (Brighton, 1984). Fraktur maksilofasial terletak di daerah yang memiliki anatomi spesifik, yaitu merupakan daerah tempat organ-organ penting seperti otak dan pusat persyarafan.
Penyebab kasus patah tulang rahang berbeda-beda di setiap negara. Di negara maju seperti Amerika dan Eropa menurut Gasner dkk. (2003), penyebab patah tulang wajah dan rahang adalah aktivitas sehari-hari dan olah raga (69%) serta kasus kekerasan (12%). Menurut Alvi dkk. (2003) dan Fischer dkk. (2003), penyebab terbesar patah tulang rahang bawah adalah perkelahian (41%) dengan
2
prosentase laki-laki 5 kali lebih banyak daripada wanita yang didominasi usia muda (20–30 th). Di kota-kota besar di Indonesia, kasus kecelakaan lalu lintas merupakan penyebab terbesar kasus patah tulang wajah dan rahang (maksilofasial) terutama rahang bawah/mandibula (Fauzi, 2010).
Prosedur tatalaksana patah tulang khususnya patah tulang wajah dan rahang telah mengalami perubahan yaitu dari operasi tertutup (close reduction) seperti fiksasi antar rahang (Inter Maxillary Fixation/IMF), menjadi operasi terbuka menggunakan fiksasi internal (open reduction and internal fixation/ORIF). Fiksasi patah tulang antar rahang (IMF) hanya menggunakan oklusi antar gigi rahang atas dan bawah sebagai acuan, sedangkan ORIF melakukan fiksasi patah tulang langsung pada tempat patah tulang sehingga didapat hasil fungsional dan estetik yang lebih bagus (Perry dan Booth, 2004; Suuronen dkk., 2007; Gerlach dkk., 2007).
Penggunaan alat fiksasi untuk mengkoreksi patah tulang wajah dan rahang serta tulang-tulang kecil seperti pada tangan (carpal, metacarpal dan phalange) dan kaki (tarsal, metatarsal dan phalange) telah menjadi prosedur rutin pada empat dekade terakhir dengan menggunakan alat yang kaku dan rigid, diawali dengan menggunakan plat dan sekrup (plate & screw) dari material logam (biometal) seperti titanium, titanium-alloy atau krom kobalt. Material logam titanium yang digunakan sebagai alat fiksasi patah tulang memiliki kekuatan dan kekakuan yang tinggi. Meskipun penggunaan material ini pada awalnya menunjukkan keberhasilan secara klinis (Van-Sickels dkk., 1986; Tulasne & Schendel, 1989; Mazzonetto dkk., 2004), tetapi kekuatan dan kekakuan yang
3
terlalu tinggi tersebut juga menyebabkan terjadinya stimulus mekanis pada tulang di bawahnya secara terus menerus (Tabel 1.1).
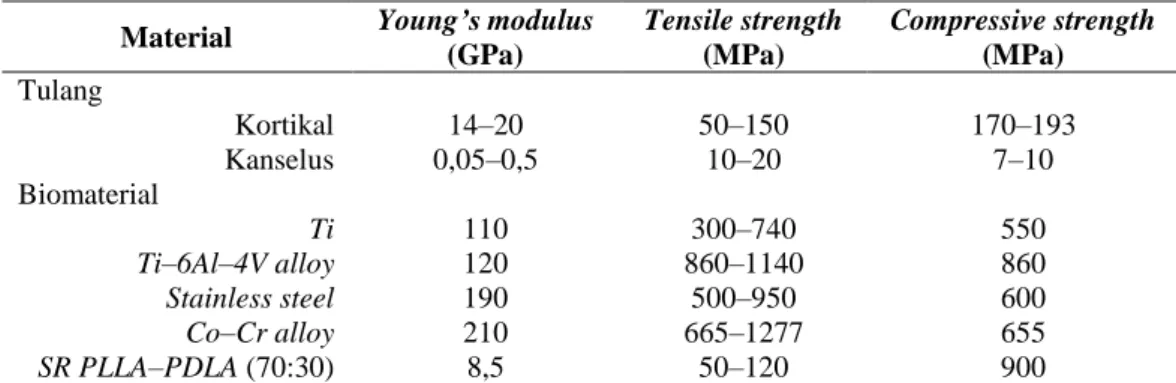
Tabel 1.1 Perbandingan karakteristik mekanis tulang dan biomaterial (Murugan dan
Ramakrishna, 2004)
Tabel 1.1 menunjukkan karakteristik mekanis material logam seperti titanium, titanium-alloy, stainless steel dan krom kobalt alloy yang terlalu tinggi bila dibandingkan dengan karakteristik mekanis tulang kortikal, sehingga menyebabkan atropi tulang di bawah plat dan selanjutnya menyebabkan gangguan pertumbuhan tulang terutama pada anak-anak (Kennady dkk., 1989; Brodke dkk., 2001). Kekurangan material logam lainnya adalah material ini secara visual dapat terlihat atau teraba (visibility or palpability), sekrup mudah longgar atau terlepas (loosening) dan sensitif terhadap dingin (cold hypersensitivity) (Suuronen, 1991; Bessho dkk., 1995; Jacobs dkk., 1998; Cilasun dkk., 2006). Material logam ini menyebabkan gangguan pencitraan (imaging) pada computed tomography scan (CT–Scan) atau magnetic resonance imaging (MRI), sehingga mengganggu interpretasi radiograf pada proses penyembuhan patah tulang. Material logam ini juga merupakan penghalang pada pasien yang membutuhkan terapi radiasi (Scher dkk., 1988; Mazzonetto dkk., 2004; Dhol dkk., 2008).
Material Young’s modulus (GPa) Tensile strength (MPa) Compressive strength (MPa) Tulang Kortikal 14–20 50–150 170–193 Kanselus 0,05–0,5 10–20 7–10 Biomaterial Ti 110 300–740 550 Ti–6Al–4V alloy 120 860–1140 860 Stainless steel 190 500–950 600 Co–Cr alloy SR PLLA–PDLA (70:30) 210 8,5 665–1277 50–120 655 900
4
Penelitian selanjutnya menunjukkan bahwa material logam titanium juga mempunyai beberapa kekurangan seperti adanya penyebaran ion-ion logam yang berakumulasi pada beberapa organ seperti kelenjar limfe regional (lymph nodes) (Schliephake dkk., 1993; Jorgenson dkk., 1997) dan sering menimbulkan reaksi alergi (Rosenberg dkk., 1993). Beberapa kekurangan tersebut menimbulkan perdebatan perlunya dilakukan operasi pengambilan kembali material fiksasi patah tulang, yang bila dilakukan akan menambah waktu perawatan dan pemulihan serta peningkatan jumlah biaya perawatan. Material fiksasi patah tulang yang bisa diserap tubuh (biodegradable) berkembang untuk mengatasi kekurangan material fiksasi dari titanium dan menghindari operasi sekunder tersebut.
Penggunaan material polimer biodegradabel sebagai alat fiksasi patah tulang masih menjadi perdebatan sampai sekarang. Penurunan stabilitas kekuatan mekanis yang terlalu cepat sebelum terjadinya penyembuhan tulang dan toksisitas yang tinggi akibat produk degradasi yang berlebihan yang disebabkan degradasi yang terlalu cepat, menyebabkan penggunaan material ini belum menjadi alternatif sebagai pengganti titanium (Bergsma dkk., 1993; Bostman, 1998; Kallela dkk., 2005).
Material fiksasi patah tulang yang bisa diserap tubuh seharusnya memiliki karakteristik antara lain cukup kaku (semi rigid), stabil dan dapat terdegradasi secara sempurna tanpa berbagai komplikasi. Selama proses degradasi, material ini harus tetap memiliki kekuatan yang cukup stabil sampai terjadinya penyembuhan tulang (Peltoniemi, 2000; Hasegawa dkk., 2006). Studi klinis menunjukkan
5
beberapa kekurangan penggunaan material fiksasi patah tulang yang bisa diserap tubuh seperti penurunan kekuatan mekanis dan terjadinya pembengkakan steril dalam jangka panjang (late aseptic swelling) (Bergsma dkk., 1993; Tegnander dkk., 1994; Bostman dkk., 1998; Kallela dkk., 2005), penyembuhan tulang yang tidak sempurna di bawah plat (Pihlajama dkk., 1992; Matsusue dkk., 1996) dan pergerakan plat (Donigian dkk., 1993; Bostman dkk., 1989; Ahl dkk., 1994).
Alat fiksasi patah tulang biodegradabel yang paling banyak digunakan di pembedahan tulang wajah dan rahang serta tulang-tulang kecil seperti pada tangan dan kaki berasal dari material polimer kristalin yaitu poly-L-lactic acid (PLLA). Material ini pada awalnya digunakan untuk penjahitan luka yang bisa diserap tubuh (bioresorbable suture material) seperti halnya polyglycolic acid (PGA), polydioxanone, polyglactin dan catgut, sehingga tidak perlu diambil kembali (Herrmann dkk., 1970). Alat fiksasi patah tulang biodegradabel dari material PLLA, seperti halnya titanium juga memiliki karakteristik mekanis yang tinggi dibandingkan tulang kortikal. Tabel 1.1 menunjukkan alat fiksasi patah tulang komersial dari material polimer yaitu SR PLLA–PDLA (70:30) memiliki modulus young sebesar 8,5 GPa, kekuatan tarik sebesar 50–120 MPa, kekuatan tekuk sebesar 275–400 MPa dan kekuatan tekan sebesar 900 MPa. Karakteristik mekanis yang tinggi tersebut tidak menyebabkan transfer tekanan pada tulang karena akan berkurang secara bertahap akibat proses degradasi (Mazzonetto dkk., 2004; Yerit dkk., 2005).
Penelitian selanjutnya menunjukkan bahwa SR PLLA–PDLA (70:30) bukan sebagai material fiksasi patah tulang yang ideal karena masih terjadi reaksi
6
benda asing akibat tingginya produk berupa kristal selama proses degradasi (Dawes dan Rushton, 1994; Kallela dkk., 1999). Monomer asam laktat (lactic acid) yang lepas selama degradasi menimbulkan reaksi lokal dan sistemik berupa respon seluler pada tempat implan (Wahl dan Czernuszka, 2006). Respon seluler yang terjadi akibat penurunan pH lokal memudahkan pelepasan prostaglandin (PGE2) oleh fibroblas dan makrofag, yang merupakan mediator kimia dan sebagai
penyebab resorbsi tulang (Dawes dan Rushton, 1994; Wahl dan Czernuszka, 2006). Untuk itu, merupakan suatu tantangan menggunakan material polimer biodegradabel lain yang memiliki karakteristik mekanis dan biokompatibilitas yang baik sebagai material fiksasi patah tulang yang bisa diserap tubuh, seperti Polivinil Alkohol (PVA).
Penggunaan Polivinil Alkohol (PVA) meningkat sebagai pengganti jaringan tubuh yang rusak akibat trauma atau penyakit, karena memiliki sifat fisikokemikal terutama sifat bio-tribological yang sangat baik. PVA menunjukkan keunggulan terhadap interaksi permukaan yaitu tahan terhadap gesekan (friction) dan keausan (wearness), serta memiliki permukaan yang licin (lubrication), sehingga dapat mencegah terjadinya erosi dan korosi (Zheng dkk., 1998; Stammen dkk., 2001; Suciu dkk., 2004). PVA merupakan material biodegradabel (Goodship dan Jacobs, 2005) dan memiliki biokompatibilitas yang sangat baik (Covert dkk., 2003; Kobayashi dkk., 2005). Material ini telah digunakan pada beberapa aplikasi biomedis seperti drug delivery, lensa kontak, graf tulang, penutup luka dan banyak digunakan untuk perbaikan jaringan lunak sendi lutut (articular cartilage) (Noguchi dkk., 1991; Pan dkk., 2007).
7
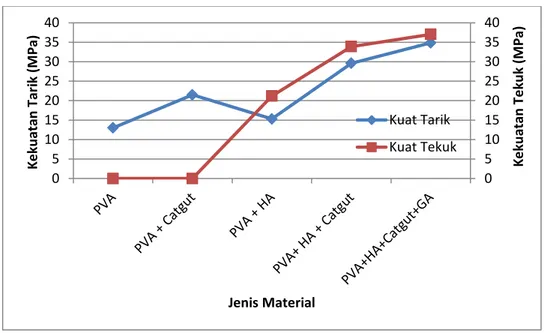
Penelitian pendahuluan menunjukkan bahwa polimer PVA memiliki kekuatan mekanis yang lemah sebagai material fiksasi patah tulang rahang yaitu memiliki rerata kekuatan tarik 13,01 MPa (Gambar 1.1). Dipandang perlu penambahan suatu material sebagai penguat untuk meningkatkan kekuatan mekanisnya.
Gambar 1.1 Rerata kekuatan mekanis pada uji pendahuluan
Material yang digunakan sebagai penguat (reinforcement) untuk meningkatkan kekuatan mekanis adalah catgut, yaitu benang untuk penjahitan luka yang bisa diserap tubuh (bioresorable suture). Catgut berasal dari kolagen usus (intestine) domba dan telah digunakan secara luas di bidang medis termasuk ortopedi untuk penutup jaringan yang dalam, sehingga tidak perlu diambil kembali. Material ini terdegradasi secara lengkap oleh enzim proteolitik dalam waktu 90 hari (Kruger, 1984). Catgut bila digunakan sebagai material penjahitan
0 5 10 15 20 25 30 35 40 0 5 10 15 20 25 30 35 40 K e ku atan Te ku k (M Pa) K e ku atan Tar ik (M Pa) Jenis Material Kuat Tarik Kuat Tekuk
8
luka, memiliki kekuatan tarik yang baik dan bertahan selama 7 hari. Penambahan lapisan krom (chromic acid salts) meningkatkan kekuatan tariknya dan bertahan lebih lama menjadi 21 hari (Mead, 1954). Belum diketahui stabilitas kekuatan tarik material ini bila digunakan untuk penguat pada komposit sebagai material fiksasi patah tulang.
Dari penelitian pendahuluan, penambahan penguat catgut dapat meningkatkan rerata kekuatan tarik polimer PVA yaitu dari 13,01 MPa menjadi 21,5 MPa (Gambar 1.1). PVA yang diperkuat catgut tidak memiliki ketebalan dan kekakuan sehingga tidak dapat dilakukan uji tekuk. Menurut Brydson (1999), ketebalan dan kekakuan polimer dapat ditingkatkan dengan penambahan beberapa zat tambahan (additive), salah satunya adalah penambahan filler. Pada penelitian ini, yang digunakan sebagai material pengisi (filler) adalah hidroksiapatit (HA) yaitu suatu material bioaktif dan osteokonduktif serta memiliki biokompatibilitas yang baik.
Komposit adalah kombinasi dua atau lebih material yang berbeda, memiliki ikatan yang cukup baik antara mereka (Vasiliev dan Morozov, 2001; Ramakrishna, dkk., 2004). Material komposit adalah material yang mengandung matrik yang berperan mengikat penguat (reinforcement) terus menerus dan memberikan bentuk sehingga menjadi lebih kuat dan kaku. Matrik merupakan struktur yang terlemah dari komposit, sebaliknya penguat merupakan struktur yang terkuat (Miracle dan Donaldson, 2001).
Hidroksiapatit [Ca10(PO4)6(OH)2] merupakan komponen anorganik utama
9
Hidroksiapatit merupakan material dengan kandungan utama kalsium dan fosfat, memiliki panjang partikel antara 102–106 nm dengan perbandingan rasio molar Ca dan P adalah 1,2–2 sehingga memiliki sifat yang stabil di dalam tubuh manusia (Specialia, 1971). Hidroksiapatit telah digunakan secara luas sebagai material bioaktif untuk regenerasi tulang, memiliki biokompatibilitas yang baik dengan jaringan keras, mampu melekat dengan tulang secara langsung, sangat osteokonduktif, tidak antigenik dan sitotoksik, karena secara komposisi kimia, biologis dan kristalnya mirip dengan tulang (Suchanek dan Yoshimura, 1998).
Hidroksiapatit memiliki kekuatan tekan yang baik tetapi tidak memiliki elastisitas yang baik karena kekuatan tariknya yang lemah (Booth dkk, 2007). Hidroksiapatit bersifat rapuh dan susah beradaptasi, sehingga sifat-sifat tersebut menyebabkan hidroksiapatit memiliki keterbatasan dalam aplikasinya yaitu hanya dapat digunakan untuk aplikasi yang mendapat tekanan yang rendah (Dewith dkk., 1981; Salyer dan Hall, 1995; Friedman dkk., 1998). Kerapuhan HA menyebabkan material ini tidak dapat digunakan tanpa dikompositkan dengan material lain untuk menggantikan tulang kortikal yang memiliki karakteristik mekanis yang lebih tinggi (Bonfield, 1984). HA sebagai keramik bioaktif, selain digunakan untuk meningkatkan diferensiasi serta pertumbuhan sel osteoblas, juga digunakan untuk mengisi cacat tulang pada operasi gigi dan tulang serta sebagai lapisan (coating) pada permukaan implan logam untuk meningkatkan integrasi implan dengan tulang host (Anusavice, 2003).
Sintesis hidroksiapatit dibuat dari berbagai sumber, baik dari sumber alami maupun sintesis secara kimia. HA yang diproduksi dari metode sintesis kimiawi
10
merupakan metode yang paling sering dipakai, karena merupakan metode yang bisa diandalkan untuk menghasilkan stokiometri HA tanpa adanya mineral seperti Na, Mg, K, F dan Cl (Herliansyah dkk., 2007). HA yang disintesis secara kimiawi membutuhkan material awal (reagen-reagen) yang mahal, menyebabkan harga yang relatif lebih tinggi daripada HA yang disintesis dari sumber alam.
Salah satu HA yang disintesis dari sumber alam (natural sources) adalah HA bovine yang disintesis dari tulang sapi yang tersedia melimpah di Indonesia. Material ini memiliki morfologi dan struktural yang sama dengan tulang manusia (Goren dkk., 2004). Penelitian oleh Herliansyah dkk. (2006), proses pemanasan (kalsinasi) serbuk tulang sapi pada temperatur ±900 oC akan langsung menghasilkan komposisi HA murni. HA kalsit dalam proses sinteringnya melalui reaksi hidrotermal, sebaliknya membutuhkan larutan diamonium hydrogen phosphate (DHP/(NH4)2HPO4) yang relatif mahal untuk mendapatkan bentuk HA
(Furuta dkk., 1998; Katsuki dkk., 1998).
Penelitian pendahuluan menunjukkan bahwa komposit PVA–HA bovine memiliki rerata kekuatan mekanis yang lemah sebagai material fiksasi patah tulang rahang yaitu rerata kekuatan tarik 15,3 MPa dan rerata kekuatan tekuk 21,2 MPa (Gambar 1.1). Selanjutnya dengan penambahan catgut sebagai penguat, kekuatan mekanis komposit PVA–HA bovine dapat ditingkatkan yaitu rerata kekuatan tarik 29,6 MPa dan rerata kekuatan tekuk 33,9 MPa (Gambar 1.1).
Metode lain untuk meningkatkan karakteristik mekanik dari komposit selain penambahan penguat (reinforcement) adalah dengan penambahan sejumlah agen crosslinker (Brydson, 1999). PVA sebagai hidrogel memiliki gugus hidroksil
11
atau amino dalam rantai utamanya, sehingga material yang sering digunakan sebagai crosslinker adalah glutaraldehid, asetaldehid dan formaldehid (Swieszkowski dkk., 2008). Penambahan glutaraldehid 1% (v/v) terhadap larutan PVA–HA bovine pada penelitian pendahuluan dapat meningkatkan rerata kekuatan tarik dari 29,6 MPa menjadi 34,85 MPa dan rerata kekuatan tekuk dari 33,9 MPa menjadi 37,04 MPa (Gambar 1.1).
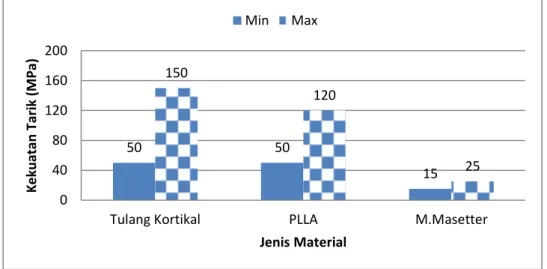
Kebutuhan kekuatan mekanis komposit PVA–HA bovine dengan penguat catgut dan glutaraldehid sebagai crosslinker untuk material fiksasi patah tulang rahang dan tulang-tulang kecil mengacu pada beberapa kondisi, yaitu kekuatan mekanis tulang kortikal (Murugan dan Ramakrishna, 2004), material fiksasi patah tulang komersial dari PLLA (Mazzonetto dkk., 2004) dan kekuatan otot pengunyahan (Wong dkk., 2010), seperti ditampilkan pada Gambar 1.2.
Gambar 1.2 Perbandingan kekuatan tarik antara tulang kortikal, PLLA dan m. masetter 50 50 15 150 120 25 0 40 80 120 160 200
Tulang Kortikal PLLA M.Masetter
K eku atan Tar ik (M P a) Jenis Material Min Max
12
Menurut Temenoff dan Mikos (2008), PVA merupakan polimer hidrofilik karena banyak mempunyai gugus OH dan polimerisasi terjadi dengan cara poliadisi. Selanjutnya menurut Temenoff dan Mikos (2008), mekanisme biodegradasi polimer dapat terjadi dalam dua cara, yaitu mekanisme pelarutan (swelling/dissolution) dan mekanisme pemotongan rantai (chain scission). Biodegradasi dengan cara pelarutan terjadi melalui penyerapan air ke dalam polimer yang menyebabkan adanya jarak antar makromolekul. Pada mekanisme ini, air berperan sebagai plastizer yang menyebabkan material polimer menjadi lebih lunak (ductile) yaitu terjadi pengurangan ikatan antara rantai sekunder. Kondisi ini menyebabkan penurunan kristalinitas polimer tersebut.
Material yang digunakan untuk pengujian biodegradasi adalah larutan PBS (phosphate–buffered saline) pH 7,4 (Pamula dkk., 2006; Annie dkk., 2008; Vaananen dkk., 2009; Tsuji dkk., 2011). PBS digunakan untuk pengujian biodegradasi karena dapat dilakukan pada polimer yang memiliki produk degradasi dalam lingkungan asam atau basa. Gugus buffer posfat berperan untuk mempertahankan pH tersebut. Osmolaritas dan konsentrasi ion dari larutan PBS berupa larutan isotonis yaitu sesuai dengan cairan tubuh manusia. PBS juga memiliki tingkat kristalisasi yang tinggi, sehingga kristalin mikro dapat dengan mudah dikontrol sehingga dapat dipertahankan kristalinitas yang sama (Cho dkk., 2000).
Menurut Temenoff dan Mikos (2008), indikator terjadinya degradasi adalah adanya perubahan warna, keretakan (crazes) dan penurunan kekuatan mekanis. Sedangkan menurut Laitinen dkk. (1992) dan Gijpferich (l994),
13
parameter yang digunakan untuk memonitor terjadinya biodegradasi selain penurunan berat molekul adalah menurunnya kekuatan mekanis.
Pengujian biodegradasi in vitro pada material komposit PVA–HA bovine dengan penguat catgut sebagai material fiksasi patah tulang rahang, sepengetahuan penulis belum pernah dilakukan. Pada penelitian ini, uji biodegradasi dilakukan dengan perendaman spesimen uji pada larutan PBS pH 7,4 pada temperatur 37 oC selama 30 dan 60 hari. Periode waktu yang digunakan tersebut didasarkan pada proses penyembuhan patah tulang yaitu terbentuknya kalus sekunder pada 20–60 hari (Weinman dan Sicher, 1955).
Biokompatibilitas didefinisikan sebagai kemampuan dari material untuk menimbulkan suatu respon yang baik jika material tersebut digunakan pada tubuh (Powers dan Sakaguchi, 2006). Biokompatibilitas menentukan apakah material tersebut dapat digunakan di dalam tubuh, di samping sifat fisikokimia, kemudahan proses, estetika dan harga yang terjangkau. Secara umum biokompatibilitas dapat diukur berdasarkan sitotoksisitas sistemik, setempat dan kemampuan menimbulkan alergi serta karsinogenik (Anusavice, 2003). Tujuan uji biokompatibilitas adalah untuk mengetahui interaksi antara material terhadap jaringan tubuh (Williams, 1990). Respon inflamasi ditunjukkan dengan peningkatan jumlah sel neutrofil terutama di bagian tepi dari jaringan yang mengalami reaksi toksisitas (Robbins dan Angell, 1976). Reaksi atau respon imun terjadi apabila terdapat penolakan terhadap material implan berupa reaksi hipersensitivitas (Roitt dkk., 1998).
14
1.2 Perumusan Masalah
a. Apakah perbandingan konsentrasi komposit Polivinil Alkohol (PVA)–HA bovine (60:40) fraksi berat dengan penguat catgut dan glutaraldehid sebagai crosslinker mempunyai kekuatan mekanis yang memadai untuk material fiksasi patah tulang rahang dan tulang-tulang kecil?
b. Apakah komposit Polivinil Alkohol (PVA)–HA bovine (60:40) fraksi berat dengan penguat catgut dan glutaraldehid sebagai crosslinker memiliki kekuatan mekanis yang stabil untuk material fiksasi patah tulang rahang dan tulang-tulang kecil setelah perendaman dalam larutan PBS pH 7,4 pada temperatur 37 oC selama 30 dan 60 hari?
c. Apakah komposit Polivinil Alkohol (PVA)–HA bovine dengan penguat catgut dan glutaraldehid sebagai crosslinker menimbulkan reaksi toksisitas pada hewan coba?
d. Apakah komposit Polivinil Alkohol (PVA)–HA bovine dengan penguat catgut dan glutaraldehid sebagai crosslinker menimbulkan reaksi hipersensitivitas pada hewan coba?
1.3 Tujuan Penelitian
1.3.1 Tujuan Umum:
Untuk mengetahui apakah komposit Polivinil Alkohol (PVA)–HA bovine dengan penguat catgut dan glutaraldehid sebagai crosslinker memiliki kekuatan mekanis yang memadai dan stabil untuk material fiksasi patah tulang rahang dan
15
tulang-tulang kecil serta memiliki biokompabilitas yang baik tanpa menimbulkan efek toksisitas dan hipersensitivitas pada hewan coba.
1.3.2 Tujuan Khusus:
a. Menentukan perbandingan konsentrasi komposit Polivinil Alkohol (PVA)– HA bovine fraksi berat dengan penguat catgut dan glutaraldehid sebagai crosslinker sehingga dapat memiliki kekuatan mekanis yang memadai untuk material fiksasi patah tulang rahang dan tulang-tulang kecil.
b. Mengkaji stabilitas kekuatan mekanis komposit Polivinil Alkohol (PVA)–HA bovine (60:40) fraksi berat dengan penguat catgut dan glutaraldehid sebagai crosslinker untuk material fiksasi patah tulang rahang dan tulang-tulang kecil setelah perendaman dalam larutan PBS pH 7,4 pada temperatur 37 oC selama 30 dan 60 hari.
c. Mengkaji pengaruh komposit Polivinil Alkohol (PVA)–HA bovine dengan penguat catgut dan glutaraldehid sebagai crosslinker terhadap timbulnya reaksi toksisitas pada hewan coba.
d. Mengkaji pengaruh komposit Polivinil Alkohol (PVA)–HA bovine dengan penguat catgut dan glutaraldehid sebagai crosslinker terhadap timbulnya reaksi hipersensitivitas pada hewan coba.
16
1.4 Keaslian dan Kedalaman Penelitian
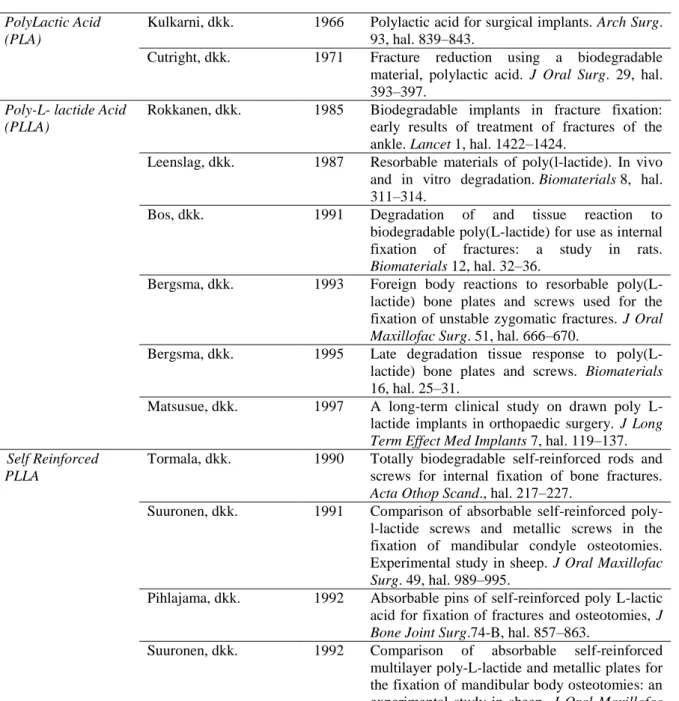
Penelitian tentang material fiksasi patah tulang yang bisa diserap tubuh (biodegradabel) telah banyak dilakukan, dengan menggunakan material polimer sintetis polylactide (Tabel 1.2).
Tabel 1.2 Matrik penelitian material fiksasi tulang yang bisa diserap tubuh
Material Peneliti Tahun Sumber
PolyLactic Acid (PLA)
Kulkarni, dkk. 1966 Polylactic acid for surgical implants. Arch Surg. 93, hal. 839–843.
Cutright, dkk. 1971 Fracture reduction using a biodegradable material, polylactic acid. J Oral Surg. 29, hal. 393–397.
Poly-L- lactide Acid (PLLA)
Rokkanen, dkk. 1985 Biodegradable implants in fracture fixation: early results of treatment of fractures of the ankle. Lancet 1, hal. 1422–1424.
Leenslag, dkk. 1.
1987 Resorbable materials of poly(l-lactide). In vivo and in vitro degradation. Biomaterials 8, hal. 311–314.
Bos, dkk. 1991 Degradation of and tissue reaction to biodegradable poly(L-lactide) for use as internal fixation of fractures: a study in rats. Biomaterials 12, hal. 32–36.
Bergsma, dkk. 1993 Foreign body reactions to resorbable poly(L-lactide) bone plates and screws used for the fixation of unstable zygomatic fractures. J Oral Maxillofac Surg. 51, hal. 666–670.
Bergsma, dkk. 1995 Late degradation tissue response to poly(L-lactide) bone plates and screws. Biomaterials 16, hal. 25–31.
Matsusue, dkk. 1997 A long-term clinical study on drawn poly L-lactide implants in orthopaedic surgery. J Long Term Effect Med Implants 7, hal. 119–137. Self Reinforced
PLLA
Tormala, dkk. 1990 1. Totally biodegradable self-reinforced rods and screws for internal fixation of bone fractures. Acta Othop Scand., hal. 217–227.
Suuronen, dkk. 1991 Comparison of absorbable self-reinforced poly-l-lactide screws and metallic screws in the fixation of mandibular condyle osteotomies. Experimental study in sheep. J Oral Maxillofac Surg. 49, hal. 989–995.
Pihlajama, dkk. 1992 1. Absorbable pins of self-reinforced poly L-lactic acid for fixation of fractures and osteotomies, J Bone Joint Surg.74-B, hal. 857–863.
Suuronen, dkk. 1992 Comparison of absorbable self-reinforced multilayer poly-L-lactide and metallic plates for the fixation of mandibular body osteotomies: an experimental study in sheep. J Oral Maxillofac
17
Surg. 50, hal. 255–262.
Suuronen, dkk. 1992 Sagittal split osteotomy fixed with biodegradable, self-reinforced poly-L-lactide screws. A pilot study in sheep. Int J Oral Maxillofac Surg. 21, hal. 303–308.
Suuronen, dkk. 1992 Comparison of shear strength of osteotomies fixed with absorbable self-reinforced poly-l-lactide and metallic screw. J Mater Sci Mater Med. 3, hal. 288–292.
SR-P(70L: 30DL)LA
Haers dan Sailer 1998 Biodegradable self-reinforced poly-L/DL lactide plate and screw in bimaxillary orthognathic surgery: short-term skeletal stability and material related failures. J Craniomaxillofac Surg. 26, hal. 363-372.
Kallela, dkk. 1999 Fixation of mandibular body osteotomies using biodegradable amorphous self-reinforced (70L:30DL) polylactide or metal lag screws: an experimental study in sheep. J Craniomaxillofac Surg. 27, hal. 124–133.
Yerit, dkk. 2002 Fixation of mandibular fractures with biodegradable plate and screw. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 94, hal. 294-300.
Mazzonetto, dkk 2004 A retrospective evaluation of rigid fixation in orthognathic surgery using a biodegradable self-reinforced (70L:30DL) polylactide. Int J Oral Maxillofac Surg. 33, hal. 664–669.
Yerit, dkk. 2005 Biodegradable fixation of mandibular fractures in children: stability and early results. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 100, hal. 17-24.
Wildemann, dkk. 2005 Short term in vivo biocompatibility testing of biodegradable poly(D,L-lactide)-growth factor coating for orthopaedic implants. Biomaterials 26(18), hal. 4035-4040.
Vaananen, dkk. 2009 Fixation properties of a biodegradable “free-form” osseosintesis plate with screw with cut-off screw heads: Biomechanical evaluation over 26 weeks. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 107, hal. 462–468
Penelitian terkini seperti ditunjukkan pada Tabel 1.2 bahwa material polimer sintetis yang digunakan sebagai material fiksasi patah tulang adalah komposit PLLA dan PDLA yaitu dalam bentuk self-reinforced (70L:30DL) polylactide. Penelitian oleh Kalela dkk. (1999); Wahl dan Czernuszka (2006), menunjukkan bahwa PLLA bukan sebagai material fiksasi patah tulang yang ideal
18
karena masih terjadi reaksi benda asing akibat tingginya produk berupa kristal dari PLLA selama proses degradasi, sehingga menyebabkan resorbsi tulang. Untuk itu, merupakan suatu tantangan menggunakan material polimer biodegradabel lain yang memiliki karakteristik mekanis dan biokompatibilitas yang baik sebagai material fiksasi patah tulang rahang yang bisa diserap tubuh, seperti Polivinil Alkohol (PVA).
Polivinil Alkohol (PVA) telah banyak digunakan dibidang medis sebagai drug delivery, lensa kontak, graf tulang, penutup luka, dan pengganti jaringan lunak sendi lutut (articular cartilage), yang semuanya tidak membutuhkan kekuatan mekanis yang tinggi. Penelitian penggunaan PVA dibidang medis ditampilkan pada Tabel 1.3.
Tabel 1.3 Aplikasi PVA dibidang medis
Material Peneliti Sumber Tahun Aplikasi
PVA Peppas dan Merrill
Development of semicrystalline poly(vinyl alcohol) hydrogels for biomedical application. J Biomed Mater Res. 11, hal. 423-434
1977 Jaringan sendi lutut
PVA Noguchi, dkk. Poly(vinyl alcohol) hydrogel as an artificial articular cartilage: evaluation of biocompatibility. Appl. Biomaterials 2(2), hal. 101–107
1991 Jaringan sendi lutut
PVA Kobayashi, dkk. Collagen immobilized PVA hydrogel-hydroxyapatite composites prepared by kneading methods as a material for peripheral cuff of artificial cornea. Materials Science and Engineering C 24, hal. 729–735 2004 Kornea buatan nanoHA- PVA Fenglan, X., Yubao, L., dan Xuejiang, W.,
Preparation and characterization of nano-hydroxyapatite/poly (vinyl alcohol) hydrogel biocomposite. Journal of Materials Science 39, hal. 5669–5672
2004 Jaringan sendi lutut
PVA-gel Pal, dkk. Preparation and characterization of polyvinyl alcohol–gelatin hydrogel membranes for biomedical applications. AAPS Pharm Sci Tech. 8(1), Article 21.
2007 Penutup luka dan drug delivery
19
PVA Pan, dkk. A study on the friction properties of poly(vinyl alcohol) hydrogel as articular cartilage against titanium alloy. Wear 262, hal. 1021–1025.
2007 Jaringan sendi lutut
nanoHA- PVA
Pan dan Xiong Study on compressive mechanical properties of nanohydroxyapatite reinforced poly(vinyl alcohol) gel composites as biomaterial, J Mater Sci: Mater Med. 20, hal. 1291–1297
2009 Jaringan sendi lutut
PVA/Gel/ HA
Tontowi, dkk. Effect of PVA Coating on Diametral Tensile Strength of Porous Block of Gelatine/Hydroxyapatite Composite, International Seminar of QIR, Denpasar, Bali.
2011 Graf tulang
Penelitian dengan menggunakan polimer Polivinil Alkohol (PVA) ini berbeda dari penelitian-penelitian pada Tabel 1.2 dan Tabel 1.3 tersebut di atas. Keterbaruan dan keaslian pada penelitian ini adalah:
a. Polivinil Alkohol (PVA) selama ini digunakan pada aplikasi yang tidak membutuhkan kekuatan mekanis yang tinggi. Pada penelitian ini dibutuhkan kekuatan mekanis yang tinggi sebagai material fiksasi patah tulang rahang dan tulang-tulang kecil. Kekuatan mekanis polimer PVA yang rendah tersebut dapat ditingkatkan dengan penambahan suatu material sebagai penguat (reinforcement).
b. Catgut yang selama ini digunakan sebagai material untuk penjahitan luka dalam yang bisa diserap tubuh (bioresorable suture), digunakan sebagai penguat (reinforcement) pada komposit PVA–HA bovine dengan tujuan untuk meningkatkan kekuatan mekanis.
c. Hidroksiapatit digunakan sebagai filler pada komposit yang bertujuan untuk meningkatkan kekakuan komposit. Hidroksiapatit disintesis dari tulang sapi, merupakan material lokal yang ketersediaannya melimpah di Indonesia.
20
Penggunaan material lokal yang relatif lebih murah dapat menghasilkan biaya produksi yang lebih murah dibandingkan dengan alat fiksasi patah tulang komersial.
d. Pada penelitian ini perbandingan konsentrasi polimer PVA dan HA (60:40) fraksi berat menunjukkan kekuatan mekanis yang optimal dibandingkan kelompok lainnya. Belum tercapainya kekuatan mekanis yang optimal menyebabkan aplikasi material komposit ini dibatasi pada kasus patah tulang dengan kekuatan mekanis yang tidak terlalu tinggi seperti patah tulang rahang dan tulang-tulang kecil seperti pada tangan dan kaki.
e. Penggunaan material sebagai alat fiksasi patah tulang yang seluruhnya bisa diserap tubuh (biodegradable), dapat mengatasi kekurangan material fiksasi dari titanium terutama untuk menghindari operasi sekunder. Pada penelitian ini dibatasi hanya sampai pembuatan spesimen uji. Diperlukan penataan catgut yang berbeda dan penambahan material lain sehubungan pembuatan prototipe berupa plate dan screw.
1.5 Manfaat Penelitian
Dari penelitian ini diharapkan dapat menghasilkan suatu material yang di samping dapat digunakan sebagai material fiksasi patah tulang rahang, dapat juga digunakan di bidang ortopedi sebagai material fiksasi patah tulang rahang dan tulang-tulang kecil seperti pada tangan (carpal, metacarpal dan phalange) dan kaki (tarsal, metatarsal dan phalange). Penggunaan material biodegradabel dapat bermanfaat bagi pasien yaitu tidak diperlukannya pembedahan tambahan untuk
21
pengambilan alat fiksasi patah tulang, yang dapat mengurangi total biaya perawatan. Penggunaan material yang biokompatibel, tidak menimbulkan reaksi toksisitas dan sensitivitas dan terjadi penyembuhan tulang yang lebih baik terutama pada anak-anak. Manfaat bagi klinisi adalah diagnosis pascaoperasi lebih mudah ditegakkan karena material ini tidak menyebabkan gangguan pencitraan (imaging) pada radiograf (MRI atau CT scan).