i
HUBUNGAN KUANTITATIF STRUKTUR-AKTIVITAS SENYAWA VINKADIFORMINA DAN TURUNANNYA SEBAGAI SENYAWA ANTIMALARIA BERDASARKAN PARAMETER TEORETIS HASIL PERHITUNGAN SEMIEMPIRIS PM3 (PARAMETERIZED MODEL 3)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh :
Nugraha Adi Hartantyo NIM : 038114134
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
ii
HUBUNGAN KUANTITATIF STRUKTUR-AKTIVITAS SENYAWA VINKADIFORMINA DAN TURUNANNYA SEBAGAI SENYAWA ANTIMALARIA BERDASARKAN PARAMETER TEORETIS HASIL PERHITUNGAN SEMIEMPIRIS PM3 (PARAMETERIZED MODEL 3)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh :
Nugraha Adi Hartantyo NIM : 038114134
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iii
HUBUNGAN KUANTITATIF STRUKTUR-AKTIVITAS SENYAWA VINKADIFORMINA DAN TURUNANNYA SEBAGAI SENYAWA ANTIMALARIA BERDASARKAN PARAMETER TEORETIS HASIL PERHITUNGAN SEMIEMPIRIS PM3 (PARAMETERIZED MODEL 3)
Oleh:
Nugraha Adi Hartantyo NIM : 038114134
Skripsi ini telah disetujui oleh
Pembimbing I
(Drs. Iqmal Tahir, M.Si.) tanggal ...
Pembimbing II
(Drs. Mulyono, Apt.)
v
Kupersembahkan karya ini untuk
Tuhan
yang Mengasihiku,Ibu-Bapakku,
ungkapan rasa hormat dan baktiku
Kakakku dan Kekasihku
serta
Almamaterku
Menjadi laki-laki adalah masalah kelahiran
Menjadi pria sejati adalah masalah pilihan
Segala sesuatu mungkin bagi orang yang percaya
Markus 9:23
vi PRAKATA
Puji syukur penulis panjatkan kepada Allah Yang Maha Kuasa, karena berkat rahmat dan kasih-Nya, penulis dapat menyelesaikan skripsi yang berjudul “Hubungan Kuantitatif Struktur-Aktivitas Senyawa Vinkadiformina dan Turunannya Sebagai Senyawa Antimalaria Berdasarkan Parameter Teoretis Hasil Perhitungan Semiempiris PM3 (Parameterized Model 3)”. Skripsi ini merupakan salah satu syarat untuk memperoleh gelar Sarjana Farmasi (S.Farm) di Fakultas Farmasi Universitas Sanata Dharma.
Penulis ingin mengucapkan terima kasih yang sebesar-besarnya kepada pihak-pihak yang telah terlibat dalam penyusunan skripsi ini, antara lain :
1. Fakultas Farmasi Universitas Sanata Dharma yang telah memberikan pendidikan dan pengajaran kepada penulis.
2. Bapak Drs. Iqmal Tahir, M.Si. selaku pembimbing utama yang telah memberikan bimbingan, kritik dan saran selama penyusunan skripsi ini.
3. Bapak Drs. Mulyono, Apt. selaku pembimbing pembantu yang berkenan memberikan bimbingan, pengarahan, kritik dan saran, serta diskusi-diskusi yang sangat memotivasi penulis.
4. Ibu Christine Patramurti, M.Si., Apt. selaku dosen penguji yang berkenan meluangkan waktu untuk menguji, memberikan kritik dan saran demi kesempurnaan skripsi ini.
vii
6. Bapak Enade Perdana Istyastono, S.F., Apt. selaku dosen yang turut membantu dan memberi masukan selama penelitian dan penyusunan skripsi. 7. Bapak Aman Soepardi dan Ibu Khatarina Sri Hardatyani tersayang, kedua
orang tua yang telah memberikan doa restu dan dukungan moral bagi penulis, sehingga penulis dapat menyelesaikan skripsi ini.
8. Mas Wied dan Pakde Bambang, kedua pakde beserta keluarganya yang telah memberikan doa restu dan dukungan bagi penulis, sehingga penulis dapat menyelesaikan skripsi ini.
9. Mba Mazi, Mas Ova, Mba Novi, dan Mba Ninin, kakak-kakak tercinta yang memberikan dukungan moral dan finansial selama penyusunan skripsi.
10. Tyas Ayu Puspita yang selalu menemani, memberi dukungan dengan setia, sabar, dan penuh kasih sehingga penulis dapat menyelesaikan skripsi ini. Terima kasih untuk semuanya.
11. Dominika Anny Yanuarti dan Ariyanto, teman-teman seperjuangan yang bersama-sama mengalami jatuh bangun selama proses penyusunan skripsi. Menjalani skripsi bersama kalian adalah pengalaman yang sangat berharga. 12. Teman-teman kelas C angkatan 2003 yang memberikan dorongan dan
semangat bagi penulis untuk menyelesaikan skripsi. Semoga kebersamaan dan persahabatan kita tidak akan lekang oleh waktu.
viii
14. Semua pihak yang tidak dapat penulis sebutkan satu per satu. Terima kasih atas bantuan dan dukungan yang telah diberikan, sehingga penulis dapat menyelesaikan skripsi ini.
Dengan segala kerendahan hati, penulis menyadari bahwa skripsi ini masih jauh dari sempurna, oleh karena itu penulis membuka diri terhadap kritik dan saran yang bersifat membangun. Penulis berharap, semoga skripsi ini dapat bermanfaat bagi perkembangan ilmu pengetahuan.
x INTISARI
Malaria telah dikenal sebagai salah satu penyebab kematian di daerah beriklim tropis, salah satunya adalah di Indonesia. Pengobatan pada orang yang terkena malaria telah banyak dilakukan, umumnya menggunakan berbagai jenis obat sintetik seperti klorokuin atau meflokuin, fenantrolin-1,10, turunan primakuin atau artemisinin. Untuk menanggulangi terjadinya resistensi dari obat-obat tersebut, maka perlu dilakukan pengembangan dan desain senyawa antimalaria baru, salah satunya dengan metode analisis Hubungan Kuantitatif Struktur-Aktivitas (HKSA). Penelitian ini bertujuan untuk mengetahui HKSA senyawa vinkadiformina dan turunannya yang telah diketahui memiliki aktivitas antimalaria yang dinyatakan dalam log 1/IC50. IC50 merupakan konsentrasi efektif
untuk menghambat pertumbuhan parasit malaria sebanyak 50%.
Penelitian ini menggunakan rancangan eksperimental kuasi. Sebagai variabel bebas digunakan deskriptor elektronik, sterik, dan hidrofobisitas yang berjumlah 17. Sebagai variabel tergantung digunakan aktivitas antimalaria dalam bentuk log 1/IC50. Data parameter teoretis diperoleh dengan perhitungan
semiempiris PM3 (Parameterized Model 3) menggunakan program komputer
HyperChem Pro ver.6.0.
Data parameter teoretis (deskriptor) diolah secara statistik menggunakan analisis regresi multivariat metode backward dengan program SPSS 11.0 for Windows. Analisis statistik yang dilakukan menghasilkan 7 model persamaan HKSA. Model persamaan 5 merupakan HKSA terbaik yang diperoleh berdasarkan kriteria statistik, yaitu :
Log 1/IC50 = 10,5159(qC1) - 32,2812(qC4) + 16,50897(qC5) + 5,614975(qC7) + 55,00465(qC9) + 0,95489(log P) - 0,3535(∂) + 0,01024(M) - 0,0388(µ) - 0,37543(ΔE) + 15,62413
Model persamaan tersebut dapat digunakan untuk memprediksikan aktivitas antimalaria senyawa-senyawa baru turunan vinkadiformina.
xi ABSTRACT
Malaria has been known as one of the causes of death in the tropical area, such as in Indonesia. Medication for people who suffered from malaria has been done. Generally, it used some of synthetic drugs such as chloroquin or mefloquin, phenanthrolyn-1,10, derivates of primaquin or arthemisinin. To overcome the resistance from those drugs, it needs to develop and design the new antimalarial substances using Quantitative Structure and Activity Relationship (QSAR) method for the example. The goal of this research is to know the quantitative relationship between structure and activity of vincadifformine and its derivatives based on log 1/IC50. IC50 is concentration that can inhibit 50% of the malaria
plasmodia’s growth.
This research uses quasi experimental design. Seventeen electronic, steric, and hydrophobicities descriptor were used as independent variabel. Antimalarial activity (log 1/IC50) was used as dependent variabel. Theoritical parameter data
were obtained by PM3 (Parameterized Model 3) semiempirical calculation from HyperChem Pro ver.6.0 computer programme.
Theoritical parameter data (descriptor) were analysed statistically using multivariate linear regression backward method by SPSS 11.0 for Windows programme. That statistic analysis results 7 QSAR equation models. The fifth equation model is the best quantitative relationship between structure and activity based on statistic criteria, with was represented i.e.
Log 1/IC50 = 10.5159(qC1) – 32.2812(qC4) + 16.50897(qC5) + 5.614975(qC7) + 55.00465(qC9) + 0.95489(log P) – 0.3535(∂) + 0.01024(M) – 0.0388(µ) – 0.37543(ΔE) + 15.62413
That equation model could be used to predict antimalarial activity of the new vincadifformine derivates.
xii DAFTAR ISI
HALAMAN SAMPUL ... i
HALAMAN JUDUL ... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN ... iv
HALAMAN PERSEMBAHAN ... v
PRAKATA... vi
PERNYATAAN KEASLIAN KARYA ... ix
INTISARI ... x
ABSTRACT... xi
DAFTAR ISI... xii
DAFTAR TABEL... xv
DAFTAR GAMBAR ... xvi
DAFTAR LAMPIRAN... xviii
DAFTAR SINGKATAN DAN ARTI LAMBANG ... xix
BAB I PENGANTAR... 1
A. Latar Belakang ... 1
B. Permasalahan ... 4
C. Manfaat Penelitian ... 4
D. Keaslian Penelitian... 5
E. Tujuan Penelitian ... 5
BAB II PENELAAHAN PUSTAKA ... 7
xiii
B. Pengelompokan Senyawa Antimalaria ... 10
C. Mekanisme Kerja Senyawa Antimalaria ... 23
D. Vinkadiformina ... 28
E. Hubungan Kuantitatif Struktur dan Aktivitas ... 29
F. Kimia Komputasi ... 31
G. Metode PM3... 33
H. Analisis Statistik ... 34
I. Keterangan Empiris ... 37
BAB III METODOLOGI PENELITIAN ... 39
A. Jenis dan Rancangan Penelitian ... 39
B. Variabel dan Definisi Variabel ... 39
C. Bahan dan Alat Penelitian... 40
1. Bahan ... 40
2. Alat... 43
D. Tata Cara Penelitian ... 43
1. Optimasi geometri struktur senyawa vinkadiformina dan turunannya dengan metode PM3 ... 43
2. Perhitungan sifat fisika kimia molekul senyawa vinkadiformina dan turunannya... 44
E. Analisa Data dan Hasil... 45
1. Analisis regresi multivariat ... 45
xiv
BAB IV HASIL DAN PEMBAHASAN ... 47
A. Optimasi Geometri Senyawa Vinkadiformina dan Turunannya dengan Metode PM3... 47
B. Perhitungan Sifat Fisika Kimia Senyawa Vinkadiformina dan Turunannya ... 50
C. Analisis Hubungan Kuantitatif Struktur Aktivitas Senyawa Vinkadiformina dan Turunannya ... 53
D. Makna Model Persamaan Terbaik ... 58
E. Strategi Rancangan Molekul Senyawa Antimalaria Baru Menggunakan Model Persamaan Terbaik... 64
BAB V KESIMPULAN DAN SARAN ... 73
A. Kesimpulan ... 73
B. Saran ... 73
DAFTAR PUSTAKA ... 74
LAMPIRAN... 77
xv
DAFTAR TABEL
I. Struktur senyawa vinkadiformina dan turunannya ... 41 II. Data aktivitas (log 1/IC50) senyawa vinkadiformina dan
turunannya ... 43 III. Deskriptor-deskriptor yang dihitung menggunakan metode PM3... 53 IV. Deskriptor-deskriptor yang terlibat di dalam model persamaan... 54 V. Nilai-nilai parameter statistik untuk mengeliminasi model persamaan .. 55 VI. Nilai aktivitas prediksi yang dihitung dengan model persamaan
5 dan dibandingkan dengan aktivitas eksperimen... 59
VII. Nilai koefisien dan nilai mutlak koefisien masing-masing
parameter pada persamaan 5 ... 60 VIII. Struktur senyawa hipotetik turunan vinkadiformina... 68 IX. Data aktivitas (log 1/IC50) senyawa hipotetik turunan vinkadiformina .. 70
X. Nilai log P senyawa hasil penelitian Mustofa, senyawa hipotetik
xvi
DAFTAR GAMBAR
1. Siklus perkembangan parasit malaria ... 8
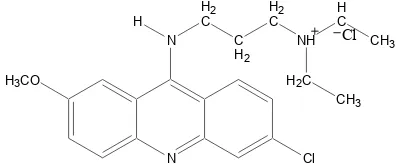
2. Struktur kuinakrin HCl ... 15
3. Struktur dasar senyawa 4-aminokuinolin... 16
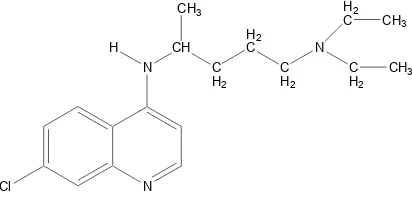
4. Struktur klorokuin ... 17
5. Struktur dasar senyawa 8-aminokuinolin... 17
6. Struktur primakuin ... 19
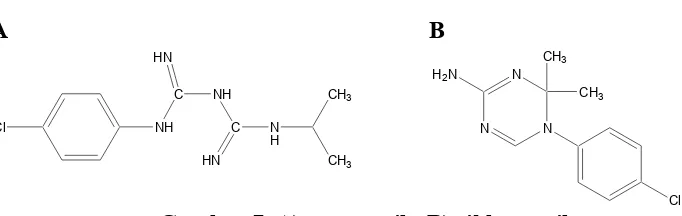
7. a. Struktur proguanil ... 19
b. Struktur sikloguanil... 19
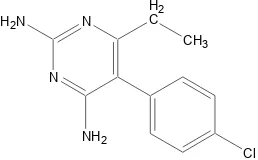
8. Struktur pirimetamin ... 20
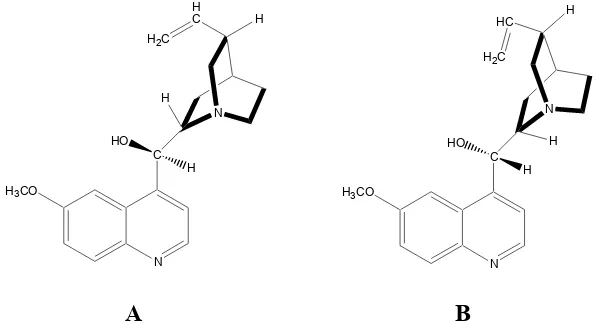
9. a. Struktur kuinin ... 21
b. Struktur kuinidin ... 21
10. a. Struktur sulfadoksin ... 22
b. Struktur dapson ... 22
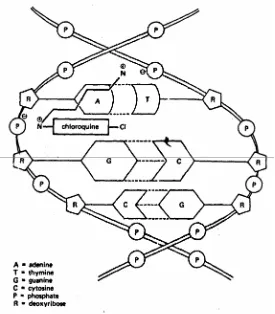
11. Mekanisme aksi klorokuin pada tingkat molekular ... 25
12. Struktur senyawa vinkadiformina ... 28
13. Struktur senyawa vinkadiformina dengan penomeran atom tidak mengikuti kaidah tatanama senyawa dan hanya digunakan untuk penelitian ini saja ... 40
xvii
optimasi geometri... 49
16. Model stick & ball senyawa vinkadiformina sesudah optimasi geometri... 50
17. Grafik PRESS pada persamaan 5... 59
18. Daerah sensitif senyawa turunan vinkadiformina... 61
19. a. Struktur indol ... 64
xviii
DAFTAR LAMPIRAN
1. Nilai-nilai parameter elektronik hasil perhitungan semiempiris PM3 ... 77 2. Nilai-nilai parameter sterik dan hidrofobik hasil perhitungan
semiempiris PM3 ... 78 3. Model summary hasil perhitungan metode backward menggunakan
SPSS 13.0 for Windows... 79 4. ANOVA hasil perhitungan metode backward menggunakan
SPSS 13.0 for Windows... 80 5. Koefisien hasil perhitungan metode backward menggunakan
SPSS 13.0 for Windows... 81 6. Nilai-nilai parameter elektronik, sterik dan hidrofobik hasil perhitungan
xix
DAFTAR SINGKATAN DAN ARTI LAMBANG 1. ADN: asam deoksiribonukleat
2. ARN: asam ribonukleat 3. AM1: Austin Model1
4. CNDO: Complete Neglect of Differential Overlap
5. EHOMO: Highest Occupied Molecular Orbitals Energy
6. ELUMO: Lowest Unoccupied Molecular Orbitals Energy
7. HKSA: Hubungan Kuantitatif Struktur Aktivitas 8. INDO: Intermediate Neglect of Differential Overlap
9. LFER: Linear Free Energy Relationship (hubungan energi bebas linear) 10. log1/IC50: - log konsentrasi yang dapat menghambat pertumbuhan
plasmodia sebesar 50%
11. log P: koefisien partisi obat dalam fase air dan fase lipid 12. M: Massa
13. MINDO: Modified Intermediate Neglect of Differential Overlap
14. MNDO: Modified Neglect of Diatomic Overlap
15. MR: Refraktivitas Molar
16. m: jumlah deskriptor dalam persamaan
17. NDDO: Neglect of Diatomic Differential Overlap
18. n: jumlah data
19. PM3: Parameterized Model3
20. PRESS: Predicted Residual Sum of Squares
21. qC: muatan bersih atom C 22. qN: muatan bersih atom N
23. QSAR: Quantitative Structure Activity Relationship
24. R: koefisien korelasi 25. R2: koefisien determinasi
26. SA: Surface Area (luas permukaan) 27. SE: Standard Error
28. Sig: Signifikansi 29. V: Volume Molekular
30. ZINDO: Zerner Intermediate Neglect of Differential Overlap
31. ΔE: selisih antara ELUMO dan EHOMO
32. µ: Momen Dipol
33. ∂: Polarisabilitas Molekular 34. 2D: dua dimensi
xx BAB I PENGANTAR
A. Latar Belakang
Malaria merupakan salah satu penyakit menular yang masih memerlukan perhatian khusus (Dewi, 2002). Peningkatan insiden malaria di beberapa daerah tertentu terutama di Indonesia Bagian Timur disebabkan antara lain: Plasmodium falciparum telah resisten terhadap beberapa obat antimalaria, ditemukannya P. vivax resisten klorokuin, dan belum tersedianya vaksin yang efektif (Taylor, 2004).
Resistensi dapat disebabkan karena pemakaian obat yang tidak tepat, sebagai contoh, penderita tidak menyelesaikan suatu rancangan pengobatan, dan pemakaian obat yang berlebihan atau tidak sesuai dosis yang telah ditetapkan. Di antara keempat spesies Plasmodia manusia, kasus malaria P. falciparum
tampaknya lebih dominan dan juga merupakan penyebab malaria berat yang banyak menimbulkan kematian. Di Indonesia dilaporkan terdapat fokus-fokus P. falciparum resisten terhadap klorokuin pada 26 propinsi, resisten terhadap sulfadoksin-pirimetamin pada 3 propinsi, dan resisten terhadap meflokuin pada dua propinsi (Tjitra, 1993).
Pengobatan malaria merupakan salah satu upaya dalam rangkaian kegiatan program pemberantasan. Keberhasilan pengobatan untuk penyembuhan maupun pencegahan tergantung apakah obat itu ideal, diminum secara teratur sesuai dengan jadwal pengobatan dan takaran yang telah ditetapkan. Obat antimalaria yang ideal adalah obat yang mempunyai efek terhadap semua jenis dan stadia
xxi
parasit, menyembuhkan infeksi akut maupun laten, cara pemakaian mudah, harganya terjangkau oleh seluruh lapisan penduduk dan mudah diperoleh, efek samping ringan dan toksisitas rendah. Sampai saat ini belum ada obat antimalaria yang ideal (Tjitra, 1993).
Pengembangan pengobatan malaria diperlukan untuk memperoleh obat yang ideal, mengatasi masalah resistensi, dan untuk membantu menanggulangi masalah malaria di dunia. Dasar pengembangan pengobatan malaria adalah dengan meningkatkan atau memperbaiki efikasi pengobatan malaria tanpa komplikasi yaitu dengan mengembangkan kombinasi atau regimen obat antimalaria yang tersedia di Indonesia atau dengan mempersiapkan obat antimalaria baru dan mencari obat antimalaria baru alternatif yang efektif sebagai obat penyelamat untuk pengobatan malaria dengan komplikasi (Taylor, 2004).
xxii
Pengembangan dan desain senyawa antimalaria baru dapat dilakukan dengan berbagai metode, salah satunya adalah analisis Hubungan Kuantitatif Struktur-Aktivitas (HKSA). Metode ini dapat mengurangi faktor trial and error
dalam sintesis obat baru, fokus pada sintesis obat baru serta mencapai efisiensi waktu dan biaya. Selain itu, kajian HKSA dapat memberikan informasi maksimum dari molekul obat baru dengan dana yang lebih sedikit (Foye, 1981).
Analisis HKSA vinkadiformina dan turunannnya telah dilakukan oleh Tahir dkk. (2005). Dalam penelitiannya, Tahir, dkk. menganalisis HKSA 16 senyawa vinkadiformina dan turunannya yang telah diuji aktivitasnya terhadap P. falciparum yang sensitif terhadap klorokuin (sel Nigerian), oleh Mustofa. Dengan metode semiempiris Austin Models 1 (AM1), Tahir, dkk. berhasil memperoleh model persamaan terbaik yang dapat menggambarkan hubungan kuantitatif struktur senyawa vinkadiformina dan turunannya dengan aktivitasnya sebagai antimalaria. Model persamaan yang diperoleh oleh Tahir, dkk. memperlihatkan bahwa parameter teoretis berupa parameter elektronik dan sterik memberikan pengaruh yang besar terhadap aktivitas antimalaria yaitu log 1/IC50. Log 1/IC50
menyatakan log konsentrasi yang dapat menghambat pertumbuhan plasmodia sebesar 50%.
xxiii
(PM3) yang diharapkan akan memberikan model persamaan terbaik yang menggambarkan hubungan kuantitatif struktur senyawa vinkadiformina dan turunannya melalui parameter teoretis yang meliputi parameter elektronik, sterik, dan hidrofobisitas, terhadap aktivitasnya sebagai antimalaria. Metode PM3 dipilih karena merupakan metode perbaikan dari metode sebelumnya yaitu Modified Neglect of Diatomic Overlap (MNDO) dan AM1 yang dapat memprediksikan sifat fisika kimia suatu senyawa dengan ketepatan yang lebih baik karena telah mengalami reparameterisasi. PM3 berbeda dari metode AM1 hanya pada nilai parameter yang digunakan. Metode PM3 digunakan untuk menghitung semua parameter secara bersamaan, dan melibatkan ratusan data dari basis set yang lebih banyak daripada metode lain. PM3 memiliki set parameter-parameter terbaik untuk data eksperimen.
B. Permasalahan
Dari latar belakang di atas muncul permasalahan sebagai berikut:
1. Bagaimana hubungan kuantitatif antara struktur dan aktivitas senyawa vinkadiformina dan turunannya sebagai senyawa antimalaria berdasarkan parameter teoretis hasil perhitungan semiempiris PM3?
xxiv
C. Manfaat Penelitian 1. Manfaat Teoretis
Penelitian ini diharapkan dapat memperkaya ilmu pengetahuan dalam kefarmasian, terutama dalam bidang kimia medisinal dan kimia komputasi.
2. Manfaat Praktis
Penelitian ini diharapkan dapat memberikan informasi mengenai hubungan antara struktur dan aktivitas senyawa vinkadiformina dan turunannya sehingga dapat dijadikan pedoman dalam penemuan senyawa antimalaria baru.
D. Keaslian Penelitian
Penelitian mengenai hubungan kuantitatif struktur-aktivitas senyawa vinkadiformina dan turunannya sebagai antimalaria telah dilakukan oleh Tahir dkk. (2005). Dalam penelitian ini digunakan 16 senyawa vinkadiformina dan turunannya beserta data IC50 yang sama dengan penelitian Tahir, dkk. (2005).
Pendekatan HKSA dilakukan menggunakan metode semiempiris PM3 dalam menghitung parameter teoretis struktur senyawa vinkadiformina dan turunannya hingga ditemukan model persamaan terbaik.
E. Tujuan Penelitian
xxv
xxvi BAB II
PENELAAHAN PUSTAKA
A. Malaria
Malaria merupakan infeksi yang penting dengan tanda-tanda khas yaitu demam, anemia, spelenomegali dan sering dengan komplikasi yang serius atau fatal. Disebabkan oleh protozoa dari genus Plasmodium yang termasuk kelas Sporozoa dan empat spesies yang umum ditemukan pada manusia, yaitu
Plasmodium vivax, P. malariae, P. falciparum,dan P. ovale (Yamaguchi, 1992). Malaria tersian, yang diakibatkan oleh P. vivax adalah bentuk penyakit malaria yang paling umum. Bentuk malaria tersian yang paling berat, disebut
tersian ganas, disebabkan oleh P. falciparum. Serangan oleh spesies-spesies ini lebih jarang dibandingkan dengan P. vivax. Malaria quartan, dengan tingkat keganasan menengah, disebabkan oleh serangan P. malariae. Malaria macam ini lebih jarang terjadi daripada tersian ganas. P. ovale mengakibatkan bentuk penyakit malaria yang jarang, yang disebut malaria tersian ovale. Malaria macam ini dalam banyak hal mirip dengan malaria tersian atau malaria P. vivax (Kier dan Roche, 1996).
xxvii
Gambar 1. Siklus perkembangan parasit malaria
(Siswandono dan Soekardjo, 1995) Siklus perkembangan parasit malaria dalam nyamuk Anopheles dan tubuh manusia serta tempat kerja obat antimalaria dapat dilihat pada gambar 1. Ketika nyamuk Anopheles betina (yang mengandung parasit malaria) menggigit manusia, akan keluar sporozoit dari kelenjar ludah nyamuk masuk ke dalam darah dan jaringan hati. Dalam siklus hidupnya parasit malaria membentuk stadium schizont jaringan dalam sel hati (stadium eksoeritrositik). Setelah sel hati pecah, akan
masuk melalui gigitan nyamuk
Oosit pecah Sporozoit pada kelenjar ludah
Sporozoit Schizont jaringan primer
Schizont jaringan sekunder/laten (P.vivax dan
P.ovale)
Schizont dikembangkan dalam sel hati Oosit tumbuh pada
dinding lambung
Merozoit masuk ke sel darah merah
masuk ke sel darah merah Merozoit
xxviii
keluar merozoit yang masuk ke eritrosit membentuk stadium schizont dalam eritrosit (stadium eritrositik). Di situ mulai terbentuk tropozoit muda sampai schizont tua atau matang sehingga eritrosit pecah dan keluar merozoit (Silalahi, 2004). Pada tahap terbentuknya schizont, pasien tidak mengalami gejala. Keadaan ini bertahan hingga schizont pecah, dan melepaskan kembali merozoit beserta pirogen ke dalam darah. Secara klinis, tahap ini ditandai dengan gejala menggigil (DiPalma, 1990). Sebagian besar merozoit masuk kembali ke eritrosit dan sebagian kecil membentuk gametosit jantan dan betina yang siap untuk diisap nyamuk malaria betina dan melanjutkan siklus hidupnya di tubuh nyamuk (stadium sporogoni) (Silalahi, 2004).
Di dalam lambung nyamuk, terjadi perkawinan antara sel gamet jantan (mikro gamet) dan sel gamet betina (makro gamet) yang disebut zigot (Silalahi, 2004). Zigot berkembang membentuk oosit (strukturnya bulat dan berada di dinding luar lambung). Oosit kemudian berkembang menjadi sporozoit dan dilepaskan ke dalam rongga perut nyamuk, lalu berpindah ke kelenjar ludah. Dari kelenjar ludah, sporozoit siap dipindahkan dan menginfeksi manusia yang digigit oleh nyamuk Anopheles betina (siklus berjalan kembali) (Williams dan Lemke, 2002).
xxix
menurun, misalnya akibat terlalu lelah, sibuk, stress atau perubahan iklim (musim hujan), hipnosoit dalam tubuhnya akan terangsang untuk melanjutkan siklus parasit dari sel hati ke eritrosit. Setelah eritrosit yang berparasit pecah, akan timbul kembali gejala penyakit. Misalnya 1–2 tahun sebelumnya pernah menderita P. Vivax / P. ovale dan sembuh setelah diobati, bila kemudian mengalami kelelahan atau stress, gejala malaria akan muncul kembali, sekalipun yang bersangkutan tidak digigit nyamuk Anopheles (Silalahi, 2004).
B. Pengelompokan Senyawa Antimalaria
Obat antimalaria adalah senyawa yang digunakan untuk pencegahan dan pengobatan malaria. Berdasarkan kerja utamanya, obat antimalaria dapat dibedakan dalam kelompok berikut: Skizontosida jaringan yang menghambat perkembangan bentuk eksoeritrositik, Skizontosida darah yang menekan perbanyakan parasit dalam eritrosit, Sporontosida yang mencegah pengembangan parasit dalam Anopheles (Mutschler, 1991). Menurut Siswandono dan Soekardjo (1995) terdapat kelompok antimalaria selain yang telah disebutkan di atas, yaitu: Skisontisida jaringan yang digunakan untuk kekambuhan, Gametositosida, dan Sporozoitosida.
xxx
1. Schizontisida jaringan untuk pencegahan kausal
Antimalaria kelompok ini menghancurkan bentuk jaringan primer plasmodia dan merozoit di hati, mulai dari tahap infeksi eritrositik, kemudian mencegah invasi eritrosit dan penyebaran infeksi ke nyamuk Anopheles. Contoh antimalaria kelompok ini adalah klorguanid, pirimetamin, dan primakuin (Siswandono dan Soekardjo, 1995). Klorguanid atau nama lainnya adalah proguanil, merupakan prototipe dari kelompok ini. Klorguanid telah digunakan secara luas untuk pencegahan kausal malaria yang disebabkan oleh
P. falciparum. Antimalaria ini mengalami masalah resistensi, namun tetap memberikan proteksi jika dikombinasikan dengan obat lain. Meskipun primakuin juga memiliki aktivitas terhadap P. falciparum, antimalaria ini memiliki potensi toksik yang tinggi dan digunakan untuk aplikasi klinis yang lain (Tracy dan Webster, 2001).
2. Schizontisida jaringan untuk mencegah kekambuhan
xxxi
3. Schizontisida darah untuk pengobatan klinis dan supresif
Menurut Korolkovas dan Burckhalter (1976), antimalaria dapat memberikan efek sebagai supresi atau pencegahan klinis, yaitu pencegahan dari gejala klinis dengan bekerja pada bentuk aseksual parasit dalam darah. Kerja ini dapat bersifat sementara atau permanen. Antimalaria kelompok ini bekerja terhadap merozoit pada fase eritrositik aseksual dari plasmodia malaria dan mengganggu schizogoni eritrositik ke bawah, sehingga serangan klinis tidak terjadi. Antimalaria ini juga digunakan dalam terapi penyembuhan supresif untuk eliminasi plasmodia secara lengkap. Kecuali primakuin, hampir semua antimalaria yang digunakan secara klinis dikembangkan aktivitasnya terhadap fase aseksual plasmodia. Berdasarkan masa kerjanya kelompok antimalaria ini dibagi menjadi dua, yaitu :
a. Schizontosida yang bekerja secara cepat
Contoh : amodiakuin, artemisinin, klorokuin, kuinin, kuinidin, meflokuin, dan atovaquon
b. Schizontosida yang bekerja secara lambat
Contoh : pirimetamin, klorguanid, sikloguanil pamoat, sulfonamida, dan sulfon
(Siswandono dan Soekardjo, 1995; Tracy dan Webster, 2001) 4. Gametositosida
xxxii
kuinin memiliki aktivitas gametosidal terhadap P. vivax, P. ovale, dan P. malariae, tetapi tidak untuk P. falciparum. Primakuin memiliki aktivitas gametosidal pada semua plasmodia termasuk P. falciparum (Kakkilaya, 2006).
5. Sporozoitosida
Antimalaria kelompok ini mampu membunuh sporozoit segera setelah masuk dalam darah sesudah gigitan nyamuk. Waktu antimalaria ini untuk bekerja sangat singkat oleh karena sporozoit secara cepat masuk ke sel hati sehingga banyak antimalaria kurang efektif terhadap bentu sporozoit tersebut. Contoh antimalaria kelompok ini adalah klorguanid, pirimetamin, dan primakuin (Siswandono dan Soekardjo, 1995).
6. Sporontosida
Antimalaria kelompok ini bekerja pada tubuh nyamuk malaria yang menginfeksi tuan rumah yaitu dengan mencegah pembentukan oosit dan sporozoit. Contoh : pirimetamin, klorguanid, dan primakuin (Siswandono dan Soekardjo, 1995).
Berdasarkan struktur kimianya, antimalaria dibagi menjadi 8 kelompok, yaitu turunan 9-aminoakridin, 4-aminokuinolin, 8-aminokuinolin, biguanida, diaminopiridin, kuinolinometanol, sulfonamida, dan sulfon.
1. Turunan 9-aminoakridin
xxxiii
antimalaria karena tersedia obat yang lebih aktif dengan toksisitas lebih rendah (Siswandono dan Soekardjo, 1995). Turunan 9-aminoakridin, melibatkan sistem cincin datar yang dimiliki oleh senyawa tersebut. Cincin datar yang dimiliki oleh turunan 9-aminoakridin adalah cincin akridin. Sistem cincin datar memungkinkan senyawa-senyawa tersebut dapat berinterkalasi di antara pasangan basa dobel heliks asam deoksiribonukleat (ADN) dan membentuk kompleks obat-ADN. Kompleks obat-ADN diperkuat dengan adanya ikatan rantai samping yaitu gugus amin tersier terprotonasi yang dapat berikatan secara ionik dengan gugus fosfat yang bermuatan negatif (Korolkovas dan Burckhalter, 1976). Dengan terbentuknya kompleks obat-ADN, maka transkripsi dan translasi ADN menjadi asam ribonukleat (ARN) akan terhambat. Hal ini akan mengurangi sintesis ADN dan ARN (DiPalma, 1990)
xxxiv
schizontosida darah yang bertindak sebagai basa lemah yang terkonsentrasi dalam vakuola makanan plasmodia yang bersuasana asam (Tracy dan Webster, 2001). Senyawa-senyawa ini kemudian mengalami protonasi, meningkatkan pH intravakuolar, dan terjebak di dalam vakuola makanan karena pori-pori membran vakuola juga bermuatan positif. Kondisi ini mempertahankan keberadaan senyawa-senyawa turunan 9-aminoakridin dalam hemoglobin penderita (Block, 2004). Dengan keberadaan senyawa-senyawa tersebut dalam hemoglobin penderita, maka aktivitas peroksidatif heme akan terhambat dan polimerisasi nonenzimatik heme menjadi hemozoin
akan terganggu (Tracy dan Webster, 2001). Keadaan ini akan membunuh plasmodia melalui perusakan oksidatif pada membran plasmodia dan/ atau sel darah merah, sehingga membran mengalami lisis (Block, 2004).
Turunan 9-aminoakridin bersifat sangat toksik dan telah banyak digantikan oleh senyawa-senyawa aminokuinolin. Toksisitasnya meliputi reaksi obat pada sistem saraf pusat, darah, dan reaksi obat yang fatal. Efek tokisknya meliputi kejang, reaksi psikotomimetik, anemia aplastik, dan dermatitis eksfoliatif (Kier dan Roche, 1996).
N Cl
xxxv 2. Turunan 4-aminokuinolin
Struktur dasar dari antimalaria turunan 4-aminokuinolin disajikan pada gambar 3.
Gambar 3. Struktur dasar senyawa 4-aminokuinolin
Turunan 4-aminokuinolin mempunyai aktivitas antimalaria yang lebih tinggi dibanding kuinin atau 9-aminoakridin.Karakteristik antimalaria turunan 4-aminokuinolin mempunyai sistem cincin kuinolin datar. Pada atom C nomor 4 terdapat gugus amin sekunder yang terikat oleh cincin kuinolin dan rantai samping. Pada atom C nomor 7 terdapat substituen Cl yang menunjukkan aktivitas yang optimal. Gugus amin tersier pada cincin kuinolin juga sangat penting berperan dalam aktivitasnya sebagai antimalaria. Contoh senyawa turunan 4-aminokuinolin adalah amodiakuin HCl, klorokuin fosfat, hidroksiklorokuin, dan sontokuin. Perbedaan struktur pada senyawa-senyawa turunan 4-aminokuinolin ini terdapat pada rantai samping yaitu R1 dan R2.
Dari turunan 4-aminokuinolin, klorokuin (gambar 4) menunjukkan aktivitas yang optimal (Siswandono dan Soekardjo, 1995).
xxxvi
Burckhalter, 1976), dan dapat mengikat dengan afinitas yang tinggi feriprotoporfirin IX membentuk kompleks koordinasi sehingga menyebabkan kerusakan dan lisisnya membran parasit malaria (Tracy dan Webster, 2001).
N
Gambar 4. Struktur klorokuin 3. 8-aminokuinolin
Turunan 8-aminokuinolin aktif terhadap bentuk eksoeritrositik plasmodia malaria yang disebabkan oleh P. vivax dan P. malariae. Mempunyai aktivitas gametositosida, tetapi tidak aktif terhadap bentuk plasmodia eritrositik. Turunan ini menimbulkan toksisitas lebih besar dibanding turunan 4-aminokuinolin (Siswandono dan Soekardjo, 1995). Struktur dasar dari antimalaria turunan 8-aminokuinolin disajikan pada gambar 5.
N
Gambar 5. Struktur dasar senyawa 8-aminokuinolin
xxxvii
atom C nomor 8. Pada atom C nomor 6 terdapat substituen metoksi yang menunjukkan aktivitas yang optimal meskipun batas keamanannya rendah, dan kemungkinan dapat diganti dengan gugus hidrogen atau hidroksi. Contoh senyawa turunan 8-aminokuinolin adalah primakuin, pamakuin, dan pentakuin (Siswandono dan Soekardjo, 1995).
Meskipun memiliki struktur yang mirip dengan kuinolinometanol, turunan 8-aminokuinolin memiliki mekanisme kerja yang berbeda. Primakuin bekerja dengan mengganggu mitokondria plasmodia (Block, 2004). Primakuin mengganggu transpor elektron, sehingga menyebabkan perusakan oksidatif pada sistem enzim mitokondrial. Proses ini mengakibatkan mitokondria plasmodia menggembung dan mengalami vakuolisasi. Dalam hal ini mitokondria penderita tidak terganggu. Primakuin juga menyerang bentuk seksual plasmodia dan membuat bentuk seksual ini tidak mengalami pematangan (DiPalma, 1990). Primakuin dapat diubah menjadi elektrofil yang bekerja sebagai mediator oksidasi-reduksi (Tracy dan Webster, 2001). Hal ini menyebabkan perusakan oksidatif pada elektron-kaya asam nukleat dalam gametosit. Dengan demikian primakuin dapat digunakan untuk mencegah penyebaran malaria (DiPalma, 1990).
xxxviii
Gambar 6. Struktur primakuin 4. Biguanida
Turunan biguanida merupakan schizontosida eksoeritrositik dan eritrositik terhadap P. falciparum dan P. vivax. Toksisitasnya relatif ringan. Turunan ini cepat menimbulkan kekebalan sehingga kurang populer sebagai antimlaria. Turunan biguanida mempunyai aktivitas antimalaria karena menghambat secara selektif enzim dihidrofolat reduktase yang mengkatalisis perubahan asam dihidrofolat menjadi asam tetrahidrofolat pada plasmodia. Penghambatan ini mempengaruhi biosintesis plasmodia terutama pembentukan basa purin, pirimidin, dan ADN. Meskipun turunan ini tidak bekerja secara selektif terhadap enzim plasmodia, tetapi dapat mengikat enzim dihidrofolat reduktase lebih kuat dibanding isoenzim pada penderita. Efek pemblokan ini tidak berbahaya bagi penderita karena asam folinat yang diperlukan dipasok dari luar melalui makanan (Siswandono dan Soekardjo, 1995).
A B
xxxix 5. Diaminopiridin
Turunan diaminopiridin merupakan schizontosida eksoeritrositik dan eritrositik terhadap P. Falciparum dan schizontosida eksoeritrositik terhadap
P. Vivax. Turunan ini juga sporontosida yang cukup efektif. Mekanisme kerja turunan diaminopiridin sama seperti turunan biguanida yaitu menghambat secara selektif enzim dihidrofolat reduktase yang mengkatalisis perubahan asam dihidrofolat menjadi asam tetrahidrofolat pada plasmodia (Siswandono dan Soekardjo, 1995).
Antimalaria yang merupakan turunan dari diaminopirimidin adalah pirimetamin (gambar 8) dan trimetoprim. Pirimetamin digunakan sebagai pencegahan malaria (Korolkovas dan Burckhalter,1976). Pirimetamin merupakan schizontosida darah lepas lambat yang memiliki efek in vivo yang mirip dengan proguanil. Pirimetamin memiliki potensi antimalaria yang lebih besar karena langsung bekerja pada plasmodia, dan waktu paruhnya lebih lama daripada sikloguanil, bentuk aktif proguanil. Berbeda dengan proguanil, pirimetamin tidak menunjukkan efektivitas yang berarti terhadap bentuk hepatik dari P. falciparum. Pada dosis terapetis, pirimetamin tidak dapat melakukan eradikasi terhadap jaringan sekunder P. vivax atau gametosit dari spesies P. malariae (Tracy dan Webster, 2001).
N N
H2N
Cl NH2
H2
C
CH3
xl 6. Turunan kuinolinometanol
Turunan kuinolinometanol terdapat pada tanaman Chinchona Sp., terutama pada bagian kulit kayu atau korteks. Korteks kina yang diperdagangkan mengandung alkaloid kuinin 5%, kuinidin 0,1%, sinkonin 0,3%, dan sinkonidin 0,4% (Siswandono dan Soekardjo, 1995). Bagian kuinolinometanol menjadi penting dalam obat-obat sintetik. Turunan kuinolinometanol bekerja pada merozoit eritrositik. Senyawa-senyawa ini tidak menyembuhkan secara tuntas, tetapi mengurangi gejala. Kuinin (gambar 9a) digunakan pada pengobatan malaria yang plasmodiumnya telah resisten terhadap zat-zat lain, misalnya klorokuin (Kier dan Roche, 1996). Stereoisomer kuinin yaitu kuinidin (gambar 9b), memiliki potensi yang lebih besar sebagai antimalaria, tetapi kuinidin juga lebih toksik. Kuinin bersifat mematikan terhadap semua bentuk schizont plasmodium dan gametosit P. vivax dan P. malariae tetapi tidak untuk gametosit P. falciparum. Sekarang, spektrum aktivitas kuinin terlalu sempit untuk penggunaan pencegahan malaria (Block, 2004).
xli
Turunan kuinolinometanol mempunyai mekanisme kerja berinterkalasi dengan ADN (Korolkovas dan Burckhalter, 1976), dan dapat mengikat dengan afinitas yang tinggi feriprotoporfirin IX membentuk kompleks koordinasi sehingga menyebabkan kerusakan dan lisisnya membran parasit malaria (Tracy dan Webster, 2001).
7. Turunan sulfonamida dan sulfon
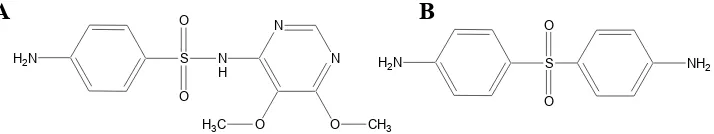
Turunan ini jarang digunakan dalam bentuk tunggal sebagai antimalaria, biasanya dikombinasi dengan pirimetamin dan digunakan untuk pengobatan infeksi P. falciparum yang sudah kebal terhadap klorokuin. Contoh turunan sulfonamida yang dapat digunakan sebagai antimalaria adalah sulfadoksin, sulfametoksipiridazin, sulfametopirazin, sulfisoksazol. Contoh sulfon yang digunakan sebagai antimalaria adalah asedapson dan dapson (Siswandono dan Soekardjo, 1995).
A B
Gambar 10. A) sulfadoksin ; B) dapson
xlii
C. Mekanisme Kerja Senyawa Antimalaria
Obat antimalaria sebagai senyawa yang digunakan untuk pencegahan dan pengobatan malaria dapat bekerja dengan mekanisme :
1. Berinteraksi dengan ADN
Turunan 9-aminoakridin, 4-aminokuinolin, 8-aminokuinolin dan kuinolinometanol menunjukkan efek schizontisid yang cepat dengan cara berinteraksi dengan ADN parasit. Turunan tersebut mempunyai sistem cincin datar yang dapat mengadakan interkalasi dengan pasangan basa dobel heliks ADN dan diperkuat melalui ikatan elektrostatik antara gugus amin tersier rantai samping dengan gugus fosfat ADN (Siswandono dan Soekardjo, 1995). Kompleks obat-ADN juga diperkuat dengan adanya ikatan hidrogen dengan molekul basa purin yaitu adenin (DiPalma, 1990). Perhitungan orbital molekul menunjukkan bahwa cincin aromatik planar dari turunan di atas, terutama bentuk terprotonasi, mempunyai nilai energi LUMO (Lowest Unoccupied Molecular Orbital) rendah sedang pasangan basa guanin dan sitosin mempunyai nilai energi HOMO (Highest Occupied Molecular Orbital) tinggi sehingga dengan mudah membentuk kompleks obat-ADN. Kuinin, dapat mengikat ADN melalui tiga jalur, yaitu:
a. Cincin kuinolin berinterkalasi diantara pasangan basa dobel heliks ADN, membentuk kompleks alih muatan.
xliii
c. Gugus kuinuklidin terproyeksi pada salah satu ADN, dan gugus amin alifatik tersier yang terprotonasi membentuk ikatan ion dengan gugus fosfat dobel heliks ADN yang bermuatan negatif.
Pembentukan kompleks akan menurunkan keefektifan ADN parasit untuk bekerja sebagai template enzim ADN dan ARN polimerase sehingga terjadi pemblokan sintesis ADN dan ARN (Siswandono dan Soekardjo, 1995).
Turunan aminokuinolin, membentuk kompleks dengan ADN melalui dua jalur, yaitu:
a. Gugus amin alifatik tersier rantai samping yang terprotonasi, membentuk ikatan ion dengan gugus fosfat dobel heliks ADN yang bermuatan negatif, melalui celah minor.
b. Alih muatan yang lebih khas atau interaksi hidrofob yang melibatkan cincin aromatik dan pasangan basa guanin-sitosin ADN.
Klorokuin dan amodiakuin, membentuk kompleks dengan ADN melalui dua jalur, yaitu:
a. Gugus amin alifatik tersier rantai samping yang terprotonasi membentuk ikatan ion dengan gugus fosfat dobel heliks ADN yang bermuatan negatif. b. Gugus 7-Cl dapat membentuk ikatan elektrostatik dengan gugus 2-amino
guanin yang bersifat khas.
2. Menghambat enzim dihidrofolat reduktase
xliv
pada parasit. Penghambatan ini mempengaruhi bioseintesis plasmodium terutama pembentukan basa purin, pirimidin dan ADN. Meskipun turunan ini tidak bekerja secara selektif terhadap enzim parasit, tetapi dapat mengikat enzim dihidrofolat reduktase plasmodia lebih kuat dibanding isoenzim pada hospes. Efek pemblokan ini tidak berbahaya bagi hospes karena asam folinat yang diperlukan dipasok dari luar melalui makanan.
xlv 3. Menghambat enzim dihidropteroat sintetase
Turunan sulfonamida dan sulfon bekerja sebagai antimalaria karena dapat menghambat secara selektif enzim dihidropteroat sintetase sehingga mencegah penggabungan asam p-aminobenzoat dengan asam dihidropteroat. Hambatan ini dapat menyebabkan kematian parasit.
4. Mengganggu mitokondria plasmodia
Turunan 8-aminokuinolin yaitu primakuin bekerja dengan mengganggu mitokondria plasmodia (Block, 2004). Primakuin mengganggu transpor elektron, sehingga menyebabkan perusakan oksidatif pada sistem enzim mitokondrial. Proses ini mengakibatkan mitokondria plasmodia menggembung dan mengalami vakuolisasi. Dalam hal ini mitokondria penderita tidak terganggu. Primakuin juga menyerang bentuk seksual plasmodia dan membuat bentuk seksual ini tidak mengalami pematangan (DiPalma, 1990). Primakuin dapat diubah menjadi elektrofil yang bekerja sebagai mediator oksidasi-reduksi (Tracy dan Webster, 2001). Hal ini menyebabkan perusakan oksidatif pada elektron asam nukleat dalam gametosit. Dengan demikian primakuin dapat digunakan untuk mencegah penyebaran malaria (DiPalma, 1990)
5. Menghambat sintesis protein
xlvi
6. Membentuk kompleks dengan feriprotoporfirin IX
Klorokuin, sinkonin, kuinidin, dan kuinin dapat mengikat dengan afinitas yang tinggi feriprotoporfirin IX membentuk kompleks koordinasi sehingga menyebabkan kerusakan dan lisisnya membran parasit malaria (Siswandono dan Soekardjo, 1995).
xlvii
penderita, maka aktivitas peroksidatif heme akan terhambat dan polimerisasi nonenzimatik heme menjadi hemozoin terganggu (Tracy dan Webster, 2001). Heme yang masih reaktif akan merusak membran plasmodia dan/ atau sel darah merah secara oksidatif, sehingga membran mengalami lisis (Block, 2004).
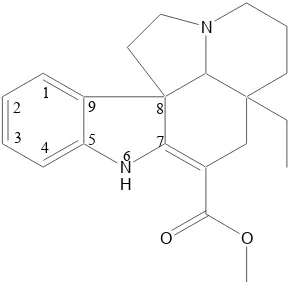
D. Vinkadiformina
N H
N
O O
1 2 3
4 5 6 7
8 9
Gambar 12. Struktur senyawa vinkadiformina
Senyawa vinkadiformina (gambar 12) merupakan hasil isolasi dari ekstrak tanaman Aspirdosperma pyrifolium dan A. megalocarpon yang merupakan tanaman tradisional sebagai obat antimalaria dari Amerika (Mustofa, 2001). Kuehne dkk. (1978) dalam jurnal mengenai studi biomimetik sintesis alkaloid memaparkan bahwa vinkadiformina dapat disintesis dari tetrahydro-β-carboline
xlviii
Vinkadiformina adalah salah satu indol alkaloid yang terkandung dalam tanaman Vinca minor L. Vinkadiformina bersifat hipotensif, kronotropik negatif, spasmolitik, hipoglikemik, dan simpatolitik (Anonim, 1996).
E. Hubungan Kuantitatif Struktur dan Aktivitas
Hubungan kuantitatif struktur kimia dan aktivitas biologis obat (HKSA) merupakan bagian penting rancangan obat, dalam usaha mendapatkan suatu obat baru dengan aktivitas yang lebih besar, keselektifan yang lebih tinggi, toksisitas atau efek samping sekecil mungkin dan kenyamanan yang lebih besar. Selain itu dengan menggunakan model HKSA, akan lebih banyak menghemat biaya atau lebih ekonomis, karena untuk mendapatkan obat baru dengan aktivitas yang dikehendaki, faktor coba-coba ditekan sekecil mungkin sehingga jalur sintesis menjadi lebih pendek (Siswandono dan Susilowati, 1998).
HKSA biologis tersebut dinyatakan dengan model matematis, sehingga sering disebut sebagai Hubungan Kuantitatif Struktur Aktivitas (HKSA) atau
xlix
Berdasarkan parameter yang digunakan, kajian HKSA digolongkan dalam tiga metode, yaitu : metode Hansch, metode Free-Wilson dan metode QSAR-3D atau CoMFA (Comparative Molecular Field Analysis) (Sudarmanto, 2002). Metode Hansch mengemukakan suatu konsep bahwa hubungan struktur kimia dengan aktivitas biologis (log 1/C) suatu turunan senyawa dapat dinyatakan secara kuantitatif melalui parameter-parameter sifat fisika kimia dari senyawa beupa parameter hidrofobik (π), elektronik (σ), dan sterik (Es) yang terdapat pada molekul. Model pendekatan ini disebut pula model hubungan energi bebas linear (linear free energy relationship = LFER) atau pendekatan ekstratermodinamik, yaitu suatu model matematik yang dikembangkan dari hubungan reaktivitas kimia dengan parameter substituen yang dikemukakan oleh Hammet pada tahun 1938 (Kubinyi, 1993). Aktivitas biologis umumnya berupa resiprok (log 1/C). Hal ini dikarenakan dengan menggunakan resiprok akan diperoleh hubungan yang valid. Yang terpenting, dengan menggunakan resiprok untuk aktivitas biologis akan diperoleh kemiringan garis regresi (slope) yang positif (Block, 2004).
l
mempengaruhi aktivitas, dan membuka jalan bagi optimisasi aktivitas biologis dalam satu seri senyawa (Davis, 1994).
F. Kimia Komputasi
Kimia komputasi merupakan disiplin ilmu yang baru. Hampir sama dengan disiplin ilmu kimia lainnya, kimia komputasi menggunakan sarana untuk mengetahui reaksi dan proses kimia dalam suatu sistem. Para ilmuwan menggunakan perangkat lunak komputer untuk mendapatkan informasi tentang proses kimia yang terjadi (Dearing, 1988).
Perkembangan eksperimen komputer mengubah secara substansial hubungan tradisional antara teori dan eksperimen. Simulasi komputer membutuhkan suatu metode yang akurat dalam memodelkan sistem yang dikaji. Simulasi sering dapat dilakukan dengan kondisi yang sangat mirip dengan eksperimen sehingga hasil perhitungan kimia komputasi dapat dibandingkan secara langsung dengan eksperimen. Metode kimia komputasi ini memungkinkan para kimiawan untuk melakukan penentuan struktur dan sifat suatu sistem kimia dengan cepat dengan mempelajari sifat molekul dan interaksi antar molekul (Pranowo, 2004).
li
reaksi, hubungan energi dan struktur, visualisasi molekul dan interaksi antar molekul (Pranowo, 2004).
HyperChem merupakan program yang dapat secara teliti digunakan untuk mengetahui struktur, stabilitas dan sifat molekul dengan menggunakan perhitungan mekanika molekular maupun mekanika kuantum. Dengan
HyperChem dapat dilakukan eksplorasi model energi permukaan potensial secara klasik atau kuantum dengan single point, optimasi geometri atau perhitungan dalam mencari keadaan transisi. Perhitungan single point dapat digunakan untuk menentukan energi molekul dari struktur yang telah ditentukan (tanpa proses optimasi). Perhitungan optimasi geometri menggunakan algoritma minimisasi energi untuk mendapatkan struktur yang paling stabil (Pranowo, 2004).
Program ini menyediakan metode sederhana untuk menghasilkan struktur molekul 3D dan terdapat 10 jenis metode semiempiris untuk mengoptimasi geometri suatu senyawa agar didapatkan struktur yang paling stabil. Perhitungan semiempirik dilakukan dari atom hidrogen sampai xenon, termasuk logam transisi. HyperChem menawarkan 10 metode molekul orbital semiempirik, dengan pilihan untuk senyawa organik dan senyawa-senyawa gugus utama, untuk senyawa-senyawa transisi dan untuk simulasi spektra. Kesepuluh metode semiempiris yang terdapat dalam program HyperChem adalah Extended Huckel
lii
initio yang dilengkapi dengan variasi himpunan basis yang dapat digunakan untuk menentukan sifat struktur molekul secara akurat (Pranowo, 2004).
G. Metode PM3
Perkembangan kimia komputasi, terutama dalam penerapan perhitungan kimia kuantum yang berlangsung dengan pesat memungkinkan untuk dilakukannya pemodelan molekul dan eksplorasi sifat fisika kimia suatu struktur molekul. Metode kimia kuantum yang sering digunakan dalam perhitungan senyawa organik adalah metode AM1 dan PM3. Sifat fisika kimia yang dihitung dengan metode kimia kuantum semiempirik tersebut dapat diterapkan dalam analisis HKSA menggunakan model Hansch. Berbagai penelitian tentang penggunaan deskriptor kimia kuantum dalam studi HKSA telah banyak dilaporkan, yang memberikan hasil dengan baik (Lee dkk., 1996, Tahir, 2000, Sudarmanto, 2002).
liii
Metode PM3 digunakan untuk menghitung semua parameter secara bersamaan, dan melibatkan ratusan data dari basis set yang lebih banyak daripada metode lain. PM3 memiliki set parameter-parameter terbaik untuk data eksperimen. Tetapi dalam prosesnya, masih diperlukan intervensi pengguna, dalam pemilihan data eksperimental. Metode ini diparameterisasi untuk beberapa unsur utama, terkhusus atom : H, Li, C, N, O, F, Mg, Al, Si, P, S, Cl, Zn, Ga, Ge, As, Se, Br, Cd, In, Sn, Sb, Te, I, Hg, Ti, Pb, Bi Po dan At. Jumlah logam transisi yang dapat dihitung dengan metode ini juga bertambah, dan melibatkan orbital d
(Jensen, 1999).
H. Analisis Statistik
Dalam penelitian, biasa digunakan model suatu hubungan fungsional antara peubah. Dengan model tersebut kelakuan sistem yang akan diteliti dapat dipahami, diterangkan, dikendalikan, dan kemudian diprediksikan. Prediksi memiliki arti yang khusus yaitu inter- atau ekstrapolasi (Sembiring, 2003).
liv
penyederhanaan dan abstraksi dari keadaan alam yang sesungguhnya. Dalam hal ini model akan selalu berbentuk fungsi dan regresi (Sembiring, 2003).
Salah satu metode statistik yang digunakan dalam analisis HKSA adalah metode korelasi. Metode ini mengidentifikasi hubungan kuantitatif antara x-deskriptor dan aktivitas biologis. Hansch pertama kali menggunakan multiple linear regression (regresi linear multivariat) sebagai metode statistik dalam HKSA dan metode ini masih digunakan sampai sekarang (Davis, 1994). Regresi linear multivariat hanya dibatasi untuk jumlah deskriptor kurang dari 20. Dalam metode ini dianggap bahwa semua deskriptor tidak berkorelasi satu sama lain dan semua deskriptor memiliki pengaruh yang penting terhadap aktivitas (Davis, 1994). Hal ini dikarenakan data yang digunakan adalah data percobaan laboratorium yang tidak lagi menggambarkan keadaan alamiah, tetapi telah dimanipulasi oleh peneliti (Sembiring, 2003).
Regresi linear untuk satu parameter fisika kimia dapat dinyatakan melalui persamaan sebagai berikut :
Y = aX + b (2) dimana, Y = aktivitas biologis ; X = parameter sifat fisika kimia ; a, b = koefisien Regresi linear untuk dua parameter sifat fisika kimia atau lebih dapat dinyatakan melalui persamaan sebagai berikut :
Y = aX1 + bX2 + cX3 + d (3)
dimana X1, X2, X3 = parameter – parameter sifat fisika kimia 1, 2, 3 (Siswandono
lv
Keabsahan persamaan yang diperoleh dan arti perbedaan parameter yang digunakan dalam hubungan struktur-aktivitas model Hansch dapat dilihat dengan beberapa kriteria statistik, antara lain :
1. Nilai R (koefisien korelasi)
Nilai R menunjukkan tingkat hubungan antara data aktivitas biologis dari pengamatan percobaan dengan data hasil perhitungan berdasarkan persamaan yang diperoleh dari analisis regresi. Koefisien korelasi bernilai mulai dari 0 sampai 1. Dalam penelitian HKSA dicoba dicapai suatu nilai R yang lebih besar dari 0,9, sebab semakin tinggi nilai R maka semakin baik hubungannya (Siswandono dan Soekardjo, 1995). Hubungan yang sangat kuat antara variabel bebas dan variabel tergantung sebenarnya telah tercapai pada nilai R antara 0,8 sampai dengan 1 (Anonim, 2006).
2. Nilai R2 (koefisien determinasi)
Nilai R2 menunjukkan berapa persen aktivitas biologis yang dapat dijelaskan hubungannya dengan parameter sifat fisika kimia yang digunakan. Misalnya suatu hubungan yang mempunyai nilai R = 0,990 berarti dapat menjelaskan (0,990)2 x 100% = 98% dari variasi antar data (Siswandono dan Soekardjo, 1995).
3. Nilai F
lvi
memenuhi syarat siginifikansi pada tingkat kepercayaan 95% adalah persamaan yang memiliki nilai Fhitung/Ftabel lebih besar dari 1 atau Fhitung lebih
besar daripada Ftabel (Yuliana, 2005).
4. Nilai Standard Error (SE)
Nilai SE merupakan simpangan baku yang menunjukkan nilai variasi kesalahan dalam percobaan (Siswandono dan Soekardjo, 1995).
5. Predicted Residual Sum of Square (PRESS)
Salah satu tujuan pembentukan model ialah untuk prediksi dan salah satu patokan prediksi yang baik ialah prediksi dengan nilai yang diprediksi sama atau hampir sama. Nilai PRESS merupakan selisih antara hasil prediksi dengan nilai yang diprediksi (eksperimen). Model yang baik adalah model yang menghasilkan PRESS yang kecil dalam kelompok parameter (Sembiring, 2003).
Menurut Hansch, aktivitas biologis dipengaruhi oleh parameter elektronik, sterik, dan hidrofobisitas dari suatu senyawa (Siswandono dan Soekardjo, 1995). Berdasarkan konsep ini, maka model persamaan terbaik juga ditentukan dari terpenuhinya ketiga parameter tersebut.
I. Keterangan Empiris
lvii
lviii BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini bertujuan untuk mencari hubungan antar variabel dengan cara menganalisis data yang telah dikumpulkan (Sastroasmoro dan Ismael, 1995). Hubungan yang dimaksud adalah hubungan antara struktur senyawa vinkadiformina dan turunannya dengan aktivitasnya sebagai antimalaria.
Jenis dan rancangan penelitian ini termasuk penelitian eksperimental kuasi. Pada penelitian ini digunakan data aktivitas antimalaria dari 16 sampel yang telah mengalami perlakuan pada penelitian sebelumnya yang dilakukan oleh Mustofa (2001). Senyawa vinkadiformina telah mengalami modifikasi struktur yang menghasilkan satu seri senyawa vinkadiformina dan turunannya dan diuji aktivitas antimalarianya. Dapat dikatakan data aktivitas yang diperoleh adalah data sekunder. Pemilihan 16 struktur senyawa vinkadiformina dan turunannya sebagai sampel tidak dilakukan secara acak, melainkan telah ditetapkan secara pasti.
B. Variabel dan Definisi Variabel 1. Variabel bebas
Variabel bebas dalam penelitian ini adalah deskriptor-deskriptor yang mewakili parameter Hansch. Parameter elektronik berupa momen dipol (μ),
Highest Occupied Molecular Orbitals Energy (EHOMO) dan Lowest Unoccupied
lix
Molecular Energy (ELUMO) yang diwakili oleh ΔE (ELUMO - EHOMO), dan muatan
bersih atom (q) pada atom C1 (qC1), C2 (qC2), C3 (qC3), C4 (qC4), C5 (qC5), N6
(qN6), C7 (qC7), C8 (qC8), C9 (qC9). Parameter sterik yang digunakan adalah luas
permukaan (SA), volume (V), polarisabilitas molekular (∂), refraktivitas molar (MR) dan massa (M). Parameter hidrofobisitas diwakili oleh log P.
N
Gambar 13. Struktur senyawa vinkadiformina dengan penomeran atom tidak mengikuti kaidah tatanama senyawa dan
hanya digunakan untuk penelitian ini saja
2. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah nilai log 1/IC50. Nilai ini
menggambarkan aktivitas senyawa vinkadiformina dan turunannya sebagai antimalaria yang didasarkan pada konsentrasi yang dapat menghambat pertumbuhan P. falciparum sebanyak 50%.
C. Bahan dan Alat Penelitian 1. Bahan penelitian
lx
Mustofa telah mensintesis dan menguji aktivitas antimalaria keenambelas senyawa tersebut terhadap P. falciparum yang tergolong sensitif terhadap senyawa klorokuin yaitu sel Nigerian, seperti tercantum dalam tabel I.
Tabel I. Struktur senyawa senyawa vinkadiformina dan turunannya No Struktur senyawa
No Struktur senyawa
i
No Struktur senyawa
ii
Tabel II. Data aktivitas (log 1/IC50) senyawa vinkadiformina dan turunannya No Senyawa log 1/IC50
1 Vinkadiformina -2,1455
2 Vinka-2 -1,5416
3 Vinka-3 -1,9274
4 Vinka-4 -1,1614
5 Vinka-5 -1,3784
6 Vinka-6 -2,3555
7 Vinka-7 -2,2363
8 Vinka-8 -1,3802
9 Vinka-9 -1,1399
10 Vinka-10 -1,3181 11 Vinka-11 -1,7973 12 Vinka-12 -1,4298 13 Vinka-13 -2,0535 14 Vinka-14 -2,0233 15 Vinka-15 -1,0253 16 Vinka-16 -2,0418
2. Alat penelitian
Penelitian ini menggunakan alat yang meliputi perangkat keras dan lunak. Perangkat keras berupa satu set komputer AMD Sempron 2200 1,49 GHz dengan kapasitas memori 512 MB yang mampu digunakan untuk melakukan perhitungan kimia komputasi. Perangkat lunak berupa paket program komputer HyperChem Pro ver.6.0 untuk melakukan perhitungan kimia kuantum. Perhitungan statistik dilakukan dengan program SPSS 11.0 for Windows.
D. Tata Cara Penelitian
iii
Langkah awal penelitian ini adalah dengan menggambar masing-masing senyawa vinkadiformina beserta turunannya yang terdapat dalam tabel 1 dalam bentuk dua dimensi (2D). Penggambaran dilakukan dengan paket program
HyperChem. Penambahan atom H dilakukan untuk melengkapi struktur dengan memilih menu [Build] [Add hydrogens]. Selanjutnya, struktur senyawa dalam bentuk 2D diubah menjadi 3D dengan memilih menu [Build] [Add H & Model Build]. Struktur 3D dioptimasi geometri menggunakan metode PM3 dengan algoritma Polak-Ribiere. Sebelum optimasi geometri dijalankan, perlu dilakukan pengaturan pada program HyperChem yaitu dengan memilih [Setup] [Semi-empirical] [PM3] [Option] [Convergence limit] 0,001 kkal/Å.mol [Iteration limit] 32767 [Accelerate convergence] [√]. Optimasi geometri dijalankan dengan memilih menu [Compute] [Geometry optimization] [Polak-Ribiere] [RMS Gradient of] 0,001 kkal/Å.mol or 500 maximum cycles [Screen refresh period] 1 cycles. Optimasi dihentikan setelah tercapai batas konvergensi yang telah ditetapkan yaitu 0,001 kkal/Å.mol. Struktur yang telah dioptimasi disimpan sebagai file.hin.
2. Perhitungan sifat fisika kimia senyawa vinkadiformina dan turunannya
iv
Perhitungan single point digunakan untuk memperoleh data nilai muatan bersih atom (qC1, qC2, qC3, qC4, qC5, qN6, qC7, qC8, qC9), momen dipol (μ).
Perhitungan ini diawali dengan memilih [File] [Start log], kemudian perhitungan
single point dilakukan dengan memilih menu [Compute] [Single point], lalu dipilih menu [File] [Stop log] untuk menghentikan pencatatan data. Data yang telah tercatat disimpan dalam bentuk file.log. Untuk memperoleh data nilai EHOMO
dan ELUMO dilakukan perhitungan orbitals setelah dilakukan perhitungan single point. Perhitungan orbitals dilakukan dengan memilih menu [Compute] [Single point] [Orbitals]. Data nilai polarisabilitas molekular (∂), luas permukaan (SA), volume (V), refraktivitas molar (MR), dan massa (M) diperoleh dengan perhitungan QSAR properties, yaitu dengan memilih menu [Compute] [QSAR properties] memilih variabel yang dinginkan [Compute].
E. Analisis Data dan Hasil 1. Analisis regresi multivariat
Analisis regresi multivariat dilakukan terhadap variabel bebas dan variabel tergantung untuk mengetahui HKSA senyawa vinkadiformina dan turunannya sebagai antimalaria. Metode yang digunakan dalam analisis regresi multivariat adalah metode backward yang diolah dengan SPSS 11.0 for Windows.Analisis ini menghasilkan suatu model persamaan matematis.
2. Analisis kriteria statistik model persamaan matematis
v
parameter Hansch, nilai R, nilai adjusted R2, nilai Fhitung/Ftabel, dan nilai SE.
Selanjutnya pemilihan model dilakukan berdasarkan parameter PRESS. Model persamaan terbaik adalah model persamaan yang mewakili ketiga parameter Hansch, memiliki nilai R > 0,8, memiliki nilai adjusted R2 yang tinggi, memiliki nilai Fhitung/Ftabel lebih dari 1, memiliki nilai SE rendah, dan memiliki nilai PRESS
vi BAB IV
HASIL DAN PEMBAHASAN
A. Optimasi Geometri Senyawa Vinkadiformina dan Turunannya dengan Metode PM3
Semua senyawa dalam seri senyawa vinkadiformina dan turunannya diperoleh dari Mustofa (2001). Senyawa yang diambil sebagai senyawa penuntun (lead compound) adalah senyawa vinkadiformina. Berikut merupakan gambar kerangka struktur senyawa vinkadiformina dan turunannya.
N
Gambar 14. Kerangka struktur senyawa vinkadiformina dan turunannya. Penomoran atom tidak mengikuti kaidah tatanama senyawa dan hanya digunakan untuk pemodelan pada penelitian ini.
Penelitian ini menggunakan perangkat lunak Hyperchem Pro ver. 6.0. yang digunakan dalam pemodelan struktur senyawa vinkadiformina dan turunannya dan perhitungan kimia komputasi untuk memperoleh data sifat fisika kimia molekul. Langkah awal yang dilakukan dalam penelitian ini adalah penggambaran struktur dua dimensi (2D) 16 senyawa vinkadiformina dan turunannya. Selanjutnya ditambah dengan atom hidrogen pada setiap atom untuk melengkapi struktur sebenarnya dan dibentuk menjadi struktur tiga dimensi (3D). Penggambaran struktur 3D dilakukan untuk menvisualisasikan struktur senyawa
vii
dalam ruang. Struktur senyawa haruslah spesifik dan berkesesuaian dengan reseptor. Struktur 3D ini diharapkan dapat menggambarkan struktur yang mendekati keadaan sebenarnya apabila terikat dengan reseptornya.
Sebelum dilakukan perhitungan sifat fisika kimia senyawa, 16 senyawa vinkadiformina dan turunannya dioptimasi geometri terlebih dahulu. Optimasi geometri merupakan suatu cara untuk menghitung tampilan struktur molekul yang mempunyai energi terendah dan gaya-gaya atomik terkecil. Optimasi geometri bertujuan untuk mendapatkan bentuk dan struktur molekul yang paling stabil dan mempunyai energi potensial paling rendah. Metode optimasi yang digunakan adalah metode Polak Ribiere hingga diperoleh konvergensi yang efisien. Pada proses optimasi geometri senyawa ini, ditentukan nilai limit konvergensi sebesar 0,001 kkal/Å.mol. Senyawa mengalami iterasi mencari bentuk konformasi yang stabil dengan energi potensial yang paling rendah dan mempunyai konvergensi 0,001 kkal/Å.mol. Konvergensi yang dimaksud disini adalah gradien antara perubahan energi dibagi perubahan posisi sampai mendekati 0,001 kkal/Å.mol. Apabila nilai gradien tersebut telah didapat, maka senyawa akan berhenti mengalami perubahan konformasi. Bentuk senyawa yang telah dioptimasi ini merupakan bentuk yang relatif stabil yaitu menggambarkan struktur dan jarak yang sebenarnya di alam.
viii
berlawanan akibat pengaruh induksi awan elektron pada atom maupun gugus tertentu.
Gambar 15 menunjukkan senyawa vinkadiformina sebelum mengalami optimasi geometri. Gambar 16 menunjukkan senyawa vinkadiformina sesudah mengalami optimasi geometri. Atom O yang membentuk sudut (X-Y-Z) pada senyawa sebelum dan sesudah optimasi mempunyai besar sudut yang berbeda. Pada senyawa vinkadiformina sesudah mengalami optimasi membentuk sudut yang lebih besar (118,634o) dibanding senyawa vinkadiformina sebelum mengalami optimasi (109,471o). Perubahan sudut ini menyebabkan terjadinya pelebaran jarak (r) antara atom di kiri dan atom di kanan O (X-Z) pada senyawa vinkadiformina sebelum mengalami optimasi dan senyawa vinkadiformina sesudah mengalami optimasi yaitu dari 2,278 Å menjadi 2,393 Å. Hal ini juga terjadi pada atom-atom lain yang berinteraksi satu sama lain.
Gambar 15. Model stick & ball senyawa vinkadiformina sebelum optimasi geometri
Atom N
Atom O Atom H
ix
Gambar 16. Model stick & ball senyawa vinkadiformina sesudah optimasi geometri
Perubahan energi juga terjadi akibat perubahan sudut dan jarak antar tiap atom tersebut. Nilai energi ini diperoleh dari perhitugan single point. Energi senyawa vinkadiformina sesudah mengalami optimasi lebih kecil (125,941 kkal/mol) dibanding energi senyawa vinkadiformina sebelum mengalami optimasi (259,916 kkal/mol). Dari senyawa hasil optimasi inilah akan dilakukan perhitungan kimia komputasi untuk memperoleh data sifat fisika kimia yang representatif.
B. Perhitungan Sifat Fisika Kimia Senyawa Vinkadiformina dan Turunannya
Dalam penelitian ini digunakan model pendekatan hubungan kuantitatif struktur-aktivitas Hansch. Hansch mengemukakan bahwa hubungan kuantitatif
Y Z
x
struktur kimia dengan aktivitas (log 1/IC50) suatu turunan senyawa dapat
dinyatakan secara kuantitatif melalui parameter-parameter sifat fisika kimia dari substituen yaitu parameter elektronik, sterik, dan hidrofobik (Siswandono dan Soekardjo, 1998). Perhitungan sifat fisika kimia ini dilakukan setelah 16 senyawa vinkadiformina dan turunannya dioptimasi geometri.
Parameter elektronik yang digunakan meliputi parameter elektronik yang bersifat atomik dan molekuler. Parameter elektronik atomik diwakili oleh muatan bersih atom (q) pada atom C1, C2, C3, C4, C5, N6, C7, C8, C9 yang didapat dari
perhitungan single point setelah proses optimasi geometri. Sedangkan Parameter elektronik molekuler diwakili oleh momen dipol dan ΔE (EHOMO - ELUMO).
Parameter elektronik tersebut saling berhubungan satu sama lain. Terutama dalam hal penentuan medan elektrostatik molekul obat untuk membentuk ikatan antara obat-reseptor baik pada awal kontak maupun selama kontak.
Penentuan EHOMO dan ELUMO sangat menentukan dalam proses reaksi
kimia, karena transisi elektron terluar merupakan salah satu faktor yang berperan dalam reaktivitas dalam kebanyakan reaksi kimia. EHOMO dikaitkan dengan
potensial ionisasi dan memberikan sifat kerentanan terhadap serangan elektrofil, dan ELUMO dikaitkan dengan afinitas elektron dan memberikan sifat kerentanan
terhadap serangan nukleofil (Karelson dkk, 1996). Energi dalam keadaan HOMO dan LUMO didapatkan dengan cara menentukan orbital molekul setelah proses optimasi geometri. Reaktivitas yang ditunjukkan lewat EHOMO dan ELUMO, dalam
penelitian ini diwakili oleh ΔE yang merupakan selisih antara ELUMO dan EHOMO.
xi
Momen dipol berhubungan dengan delokalisasi dengan elektron pada molekul sehingga akan terbentuk deferensiasi karakter elektrik masing-masing atom. Secara langsung momen dipol akan berhubungan dengan polarisabilitas dan koefisien partisi (log P). Nilai momen dipol dipengaruhi oleh jarak antar atom dalam suatu molekul, oleh karena itu pertimbangan dalam menentukan aktivitas prediksi optimal meliputi juga efek sterik dari senyawa obat tersebut.
Parameter sterik yaitu luas permukaan, volume, polarisabilitas, refraktivitas molar dan massa berpengaruh dalam menentukan ukuran molekul senyawa yang menentukan ikatan dengan reseptor. Perhitungan parameter ini diperoleh dari perhitungan QSAR properties.
Parameter lain yang digunakan yaitu parameter hidrofobik yang diwakili oleh koefisien partisi (log P) senyawa obat. Parameter log P merupakan perbandingan kelarutan senyawa dalam oktanol dan kelarutan dalam H2O yang
melambangkan kelarutan senyawa dalam media organik yang bersangkutan dengan proses masuknya obat menembus membran sel, dalam hal ini adalah sel Nigerian yang telah diinfeksi plasmodia dari P. falciparum. Perhitungan parameter ini diperoleh dari perhitungan QSAR properties.
xii
Tabel III. Deskriptor-deskriptor yang dihitung menggunakan metode PM3
Parameter Simbol Satuan
Parameter elektronik
Refraktivitas molar MR Å3
Volume molekular V Å3
Polarisabilitas molekular ∂ Å3
Massa M Sma
C. Analisis Hubungan Kuantitatif Struktur Aktivitas Senyawa Vinkadiformina dan Turunannya
Setelah mendapatkan data sifat fisika kimia senyawa, kemudian dilakukan pengolahan data dan analisis statistik menggunakan paket program SPSS 11.0. for Windows. Pengolahan data dilakukan dengan menggunakan regresi linear multivariat metode backward dengan variabel bebas adalah deskriptor-deskriptor elektronik, hidrofobik, dan sterik; dan sebagai variabel tergantung adalah log 1/IC50. Analisis regresi ini nantinya akan menghasilkan beberapa model