PROSIDING
SEMINAR GEOLOGI NUKLIR DAN SUMBERDAYA,-AtMBANG TAHUN 2004PUSAT PENGEIIJtBANGAN BAHAN GAl..IAN ,DAN GE<>L<:><3t NUKUR-BAXANi .J<:::Ik~<:::a. 22 s.&p4"~t:::>er 2C)C).41
PENENTUAN KONDISI DEKOMPOSISI OPTIMAL BIJIH URANIUM RIRANG KALAN
Erni RA, Susilaningtyas, Hafni LN, Sumarni, Widowati, Rusydi Pusat Pengembangan Bahan Galian Dan Geologi Nuklir-BATAN
Abstrak
PENENTUAN KONDISI DEKOMPOSISI OPTIMAL BIJIH URANIUM RIRANG KALAN. Bijih Uranium asal Rirang Kalimantan Barat yang diteliti adalah tipe monasit yang diambil dari lembah Rirang Atas, Tengah dan Sawah. Kandungan unsur dalam bijih Rirang mempunyai nilai ekonomis cukup potensial yaitu uranium (U) 8528,75 ppm .. unsur tanah jarang (RE203) 60,85 %, fosfat (P04) 32,84 % dan torium (Th) 861,5 ppm[1]. Berdasarkan hal terse but maka akan dilakukan penelitian pemisahan unsur-unsur dengan metoda basa. Tahap pertama dari metode basa adalah proses dekomposisi bijih yaitu untuk memisahkan
P043- dari ikatan monasit. Tujuan dari penelitian ini yaitu untuk mendapatkan kondisi optimal
pemisahan fosfat. Parameter yang diteliti meliputi perbandingan (berat) bijih terhadap NaOH dan air; ukuran bijih dan waktu dekomposisi dengan suhu yang ditetapkan ±140 DC. Hasil penelitian diperoleh kondisi optimal dekomposisi bijih uranium Rirang yaitu perbandingan (berat) B~ih : NaOH : Air
=
1 : 1,7 : 1,7 ; ukuran bijih minus 325 mesh; waktu dekomposisi 4 jam, P04 -±88,60 % dan unsur lain yang ikut terlarut dalam filtrat fosfat adalah U ±13,05 %,RE203±6,51 %, dan Th ±16,99 %.
Kata kunci : Dekomposisi, bijih Uranium Rirang, Kalan.
Abstract
DETERMINANT OPTIMUM CONDITIONS OF DECOMPOSIT10N URANIUM ORE FROM RIRANG KALAN. Uranium ore from Rirang, West Kalimantan was identified as monazite type ores: its picked from upper Rirang Valley, Middle and lower. Rirang ore contains some elements that have an economic value such as are uranium (U) 8528.75 ppm, RE20360.85 %, P04 32.84 % and Th 861.5 ppm[1]. Based on those facts, however, the experiment on separation of its potential elements has been carried out by using alkaline method. First of all is ore decomposition in order to separate P043- from monazites. This experiment was objected to find out the optimum condition phosphate separation. The experiment parameter of process would be identified as :weight ratio of are: NaOH : water, ore sizes, and time of decomposition with fixed temperature of about ±140 DC. The results exhibit that the optimum condition of decomposition of Rirang ore is weight ratio of : NaOH : Water = 1 : 1.7 : 1.7 , ore sizes is minus 325 mesh, time of decomposition is 4 hours, yielding the recovery of P043• ±88.60 % and another solved elements, e.g. U ±13.05 %,
RE203±6.51 %, and Th ±16.99 %.
Key words: Dekomposition, Rirang Uranium ores, Kalan.
PENDAHULUAN
Bijih uranium asal Kalimantan Sarat diklasifikasikan menjadi dua tipe, yaitu tipe monasit dan turmalin. Tipe monasit dengan kandungan monasit 40-90 %, uranium
0,1-2% dan P20S 20-30 %, sedangkan tipe turmalin mengandung turmalin 65-80 %, monasit 5 %, uranium 0,5-4,5 % dan P20S 3,21 %. Kedua tipe bijih tersebut dapat
PROS
IDI NG
SEMINARPUSAT PENGE •••••GEOLOGIBANGANNUKLIR DAN SUMBERDAYA TAM BANG TAHUN ~BAHAN GAt-tAN J~~~~~~~Idibedakan dengan mudah berdasarkan
kandungan monasit dan perbedaan
densitas (berat jenis), sedangkan
kandungan mineral mineral-mineralnya
relatif sarna yaitu uraninitlpitchblende,
molibdenit, pirit, i1menitdan ilmenorutil[1].
Untuk memisahkan unsur-unsur
tersebut diperlukan beberapa tahapan
proses yang dapat dilakukan dengan
metode asam maupun basa. Pada
penelitian ini menggunakan metode basa, dimana tahap pertama dari metode ini
adalah proses dekomposisi bijih. Pada
proses dekomposisi bijih uranium Rirang, ikatan fosfat pada mineral monasit akan terpecah sehingga uranium, unsur tanah
jarang dan toriurn terpisah dari fosfat
membentuk senyawa hidroksida yang tidak larut.
Tujuan dari penelitian untuk
mendapatkan fosfat sebanyak mungkin
dengan cara mencari kondisi optimal proses tersebut. Parameter yang akan diteliti pada tahap dekomposisi ini meliputi konsumsi reagen (NaOH), ukuran bijih dan waktu
dekomposisi, sedangkan suhunya
ditetapkan ±140 °C. Teori
Bijih uranium yang mengandung
monasit dapat didekomposisi dengan dua metode yaitu metode asam dan metode basa. Metode asam dengan menggunakan
H2S04 mempunyai kekurangan antara lain adalah suhu dalam proses sulit dikendalikan
karena terjadi pencampuran eksotermik
antara asam sulfat dan asam fosfat yang terbentuk. Bila suhu tertalu tinggi terbentuk torium fosfat yang sulit larut dan reaksi lambat karena hasil digesti akan melapjsi bijih yang belum terdigesti, sehingga bijih ini lama kelamaan sukar diaduk (terdigesti). Keuntungannya butir bijih yang diperlukan lebih kasar.
Metode basa dengan NaOH
mempunyai keuntungan antara lain
diperoleh hasil samping dalam bentuk
trinatrium fosfat yang dapat dipergunakan
sebagai bahan dasar pupuk kimia.
Kelebihan reagen (natrium hidroksida)
setelah kristalisasi fosfat dapat dipakai lagi. Kekurangannya adalah ukuran butir bijih yang diperlukan lebih halus.
Reaksi yang terjadi selama proses dekomposisi dengan metode basa adalah sebagai berikut
(U02h(P04h+6NaOH-3U02( OHh+ 2Na3P04
RE(P04)+3NaOH-RE(OHh+Na3P04
Th3(P04)4+12NaOH---.3Th(OH)4+4Na3P04 Uranium, torium dan unsur tanah jarang hidroksida yang terbentuk berada dalam
"slurry" yang dapat dipisahkan dari
trinatrium fosfat dengan penyaringan pada
kondisi tertentu. Kesempurnaan reaksi
PROSI DI NG
SEMINARPUSAT PENGEIVlBAN<3ANGEOLOGI NUKUR DAN SUMBERDAYABAHAN G-AL1AN DAN GeC>L<:::><3INUKUR-BATA~IJClI<c:rtCII •. 22TAMBANGSept...--b4!!!4'"TAHUN 200.4\2()C)4be rat bijih, NaOH dan air, suhu, waktu, dan ukuran bijih[2].
BAHAN, PERALATAN DAN TATA KERJA Bahan
Bijih Rirang (Kalimantan Barat), NaOH dan bahan kimia analisis.
Komposisi bijih uranium: U= 0,52 %, Th=O,02 %, RE203= 63,04 %, PO/-=25,55 %
Alat
Satu unit alat dekomposisi yang terdiri dari gelas kimia, batang pengaduk, motor pengaduk, pemanas listrik, pompa vakum, erlenmeyer, corong Buchner, timbangan, oven, termometer, botol semprot dan Spektrophotometer UV-VIS Shimadzu 2010PC.
Tata kerja
Siapkan satu unit alat dekomposisi yaitu gelas kimia dengan pengaduk bermotor, diletakkan diatas pemanas listrik. Dimasukkan air sebanyak 340 ml kedalam gelas kimia sambil diaduk dan dipanaskan sampai dengan suhu 40 aC, kemudian dimasukkan NaOH sebanyak yang diinginkan (divariasi), diaduk. Setelah suhu mencapai 60 aC, dimasukkan bijih sebanyak 200 gr, diaduk sampai dengan suhu 140°C. Setelah suhu 140 aC tercapai, campuran diaduk terus selama waktu yang diinginkan
(divariasi). Setelah dekomposisi bijih selesai, dilakukan pemisahan filtrat dan residu dengan penyaring vakum dalam keadaan panas. Selanjutnya dilakukan pencucian residu dengan air panas sejumlah 600 ml sampai dengan beberapa kali sehingga pH filtrat pencucian mencapai ±9,0. Residu hasil dekomposisi ini dikeringkan dalam oven selama waktu tertentu. Setelah kering ditimbang dan di "sampling" untuk diambil contohnya, dianalisis kadar U, RE203, Th dan P043- .
Perlakuan yang sama seperti tersebut diatas dilakukan terhadap bijih dengan ukuran yang berbeda (divariasi) dan juga parameter yang lainnya.
Metode Penelitian 1. Menyiapkan bijih
Bijih dihancurkan dan digerus, diayak dengan ayakan yang sesuai dengan ukuran butir yang dikehendaki yaitu minus 100, minus 200 dan minus 325 mesh
Masing-masing ukuran di "sampling", diambil contohnya untuk dianalisis kadar U, RE203, Th dan PO/-. Sebagai umpan
penelitian masing-masing ukuran bijih ditimbang dengan berat setiap kantong 200 gram.
2. Dekomposisi bijih
PROSI DI NG
SEMINARPUSAT PENGEflllBANGANGEOLOGI NUKLIR DAN SUMBEROAYA TAMBANGBAHAN GPALlAN DAN GE<>L<:><:P'NUKLIR-BATA':::1J<:Ikcw1'~ •.22 ~pt~bec"TAHUN 200412004Dilakukan dekomposisi dengan
memasukkan air 340 ml, sejumlah NaOH yang divariasi (1,4 ; 1,5 ; 1,7 ; 1,8 ; 2,0) kali jumlah bijih dan 200 gr bijih Rirang, diaduk pada suhu 140°C selama 4 jam.
Setelah itu campuran disaring, residu
dicuci dengan air panas sampai
dengan pH pencuci 9,0. Residu
dikeringkan dan diambil contoh untuk
dianalisis kadar U, RE203, Th dan
P043- . Data yang diperoleh dievaluasi antara jumlah perbandingan (berat) bijih : NaOH : air dengan rekoveri U,
RE203, Th dan P043- untuk menentukan konsumsi reagen yang optimal.
b Menentukan waktu dekomposisi Dilakukan dekomposisi dengan waktu yang divariasi (2, 3, 4, 5, 6) jam,
ukuran bijih minus 325 mesh,
perbandingan (berat) bijih, NaOH, air tertentu (kondisi optimal dari penelitian a) campuran ini diaduk pada suhu ±140 °c.
Setelah itu campuran disaring, residu
dicuci dengan air panas sampai
dengan pH pencuci 9,0. Residu
dikeringkan dan diambil contoh untuk
dianalisis kadar U, RE203, Th dan
P043-. Data yang diperoleh dievaluasi
antara waktu dekomposisi dengan
rekoveri U,RE203, Th dan P043- untuk
menentukan waktu dekomposisi yang optimal.
c Menentukan ukuran bijih
Dilakukan dekomposisi dengan
ukuran bijih yang divariasi (minus 100,
minus 200, minus 325 mesh),
perbandingan (berat) bijih : NaOH : air
= tertentu (kondisi optimal dari
penelitian a), waktu tertentu (kondisi optimal dari penelitian b). Campuran ini diaduk pada suhu ±140 °c. Setelah itu campuran disaring, residu dicuci dengan air panas sampai dengan pH pencuci 9,0. Residu dikeringkan dan diambil contoh untuk dianalisis kadar U, RE203, Th dan PO/-. Data yang diperoleh dievaluasi antara ukuran
bijih dengan rekoveri U, RE203, Th
dan P043- untuk menentukan ukuran
bijih yang optimal. d Uji coba kondisi optimal
Dilakukan uji coba kondisi optimal yang diperoleh sebanyak 2 kali percobaan
dekomposisi. Kondisi optimal yang
diperoleh adalah kondisi optimal dari
PROSI DI NG
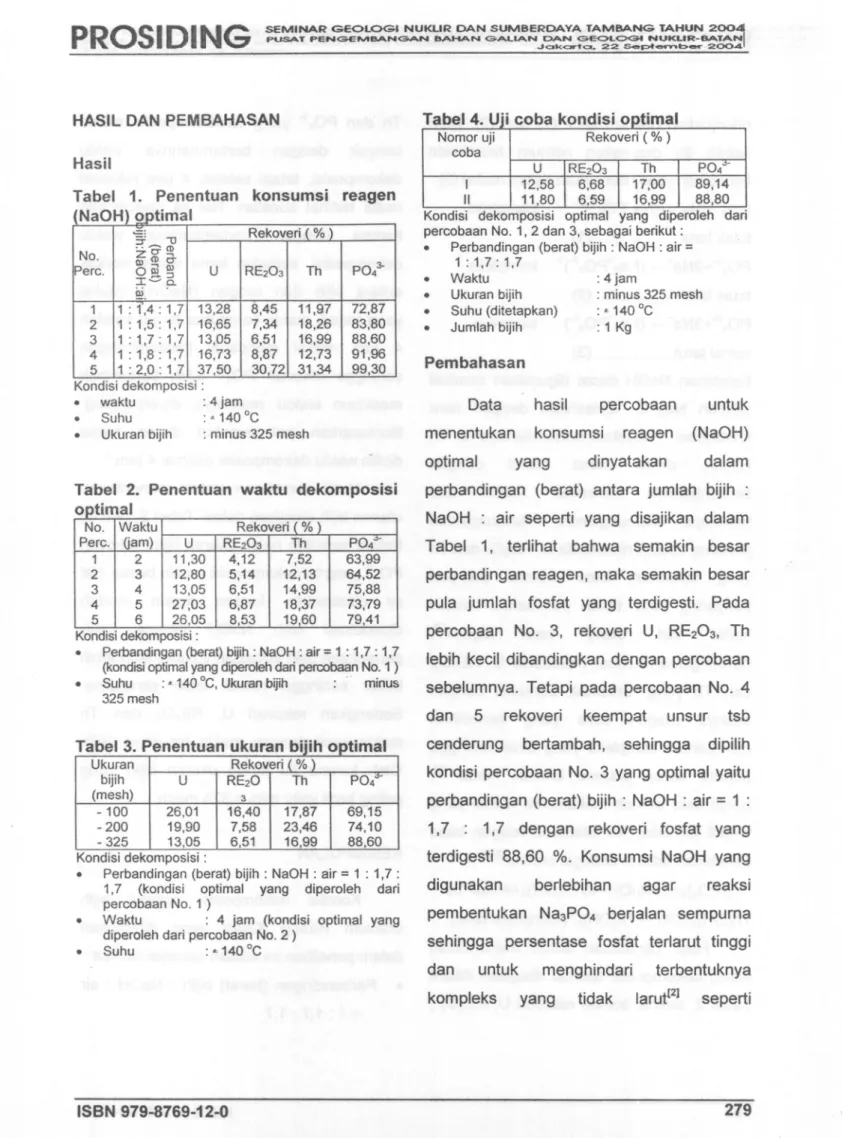
SEMINARpUSAT PENGE""BAN~GEOLOGI NUKUR DAN SUMBERDAYAbAHAN GALtAN ~ClkCW"OI. 22DAN GE<>L<::>Gt NUKUR-BATANTAMBANGs..e..pt~t:>4!M"'··2QC)4TAHUN 200~HASIL DAN PEMBAHASAN Tabel4. Uii coba kond" .
HasH
Tabel 1. Penentuan konsumsi reagen
Nomor uji Rekoveri (% )
coba U RE203Th P04"-I 12,58 6,68 17,0089,14 II 11,80 6,59 16,9988,80 NaOH) optimal '§: \J Rekoveri
(% )
•• - CD No. Q)C1>0- zo-..,Perc. RE203P043-oii3Q)ThU
I"::=: 5- 1 Qj . 1:1,4:1,7 13,2811,978,4572,87 2 1:1,5:1,7 16,6518,267,3483,80 3 1:1,7:1,7 13,0516,996,5188,60 4 1 : 1,8 : 1,712,738,8791,9616,73 5
1:2,0:1,7 37,5031,3430,7299,30 Kondisi dekomposisi optimal yang diperoleh dari percobaan No.1, 2 dan 3, sebagai berikut :
• Perbandingan (berat) bijih : NaOH : air= 1:1,7:1,7
• Waktu : 4 jam
• Ukuran bijih : minus 325 mesh • Suhu (ditetapkan) : • 140°e • Jumlah bijih : 1 Kg
Pembahasan
Tabel 2. Penentuan waktu dekomposisi timal
Kondisi dekomposisi : • waktu : 4 jam • Suhu : • 140°e
• Ukuran bijih : minus 325 mesh
Kondisi dekomposisi :
• Perbandingan (berat) bijih : NaOH : air=1 : 1,7 : 1,7 (kondisi optimal yang diperoleh dari percobaan No.1) • Suhu :. 140°e,Ukuran bijih . minus
325 mesh Ukuran Rekoveri (% ) bijih U RE20P04"""Th (mesh) 3 - 100 17,8716,4069,1526,01 - 200 19,90 7,58 23,4674,10 - 325 13,05 6,51 16,9988,60 untuk percobaan hasH Data
menentukan konsumsi reagen (NaOH)
optimal yang dinyatakan dalam
perbandingan (berat) antara jumlah bijih : NaOH : air seperti yang disajikan dalam
Tabel 1. terlihat bahwa semakin besar
perbandingan reagen, maka semakin besar pula jumlah fosfat yang terdigesti. Pada
percobaan No.3, rekoveri U. RE203• Th
lebih kecil dibandingkan dengan percobaan sebelumnya. Tetapi pada percobaan NO.4
dan 5 rekoveri keempat unsur tsb
cenderung bertambah, sehingga dipilih
kondisi percobaan No. 3 yang optimal yaitu
perbandingan (berat) bijih : NaOH : air= 1 :
1.7 : 1,7 dengan rekoveri fosfat yang
terdigesti 88,60 %. Konsumsi NaOH yang
digunakan berlebihan agar reaksi
pembentukan Na3P04 berjalan sempurna sehingga persentase fosfat terlarut tinggi
dan untuk menghindari terbentuknya
kompleks yang tidak larut[2] seperti
biiih ODf
k
t
-
-No. Waktu Rekoveri (% ) Perc. Gam)U RE203P04"""Th 1 2 11,304,127,5263,99 2 3 12,8012,135,1464,52 3 4 13,0514,996,5175,88 4 5 27,0318,376,8773,79 5 6 26,0519,608,5379,41 Kondisi dekomposisi :
• Perbandingan (berat) bijih : NaOH : air = 1 : 1,7 : 1,7 (kondisi optimal yang diperoleh dari percobaan No.1)
• Waktu : 4 jam (kondisi optimal yang diperoleh dari percobaan No.2)
• Suhu : • 140°e
PROSI DI NG
SEMINARPUSAT PEN~IVIBANGANGEOLOGI NUKLIR DAN SUMBERDAYA TAMBANGBAHAN G7A.L.IANDAN G7EC>Lc::><3I..JOII<.<::trt-CII.22 S-e-pt~be1'"NUKUR-BATA':'ITAHUN 2004\2004ditunjukkan dalam reaksi (1) dan (2). Oleh sebab itu digunakan natrium hidroksida berlebihan yang ditunjukkan dalam reaksi (3). P043-+Na+~(Na+P043-( kompleks tidak larut (1)
P043-+2Na+_ (Na/P043.)1' kompleks tidak larut (2)
P043'+3Na+~ (Na3+P043') senyawa netrallarut (3)
Kelebihan NaOH dapat digunakan kembali setelah Na3P04 dipisahkan dengan cara kristalisasi. Penyebab bertambahnya U, Th RE203, dalam tiltrat fosfat dengan bertambahnya konsumsi NaOH ada beberapa kemungkinan. Kemungkinan pertama adalah hidroksida U. RE203 dan Th yang terbentuk 101m;' melalui pori-pori. penyaring pada tahap pemisahan larutan fosfat dari "slurry" hasil digesti[2].
Kemungkinan kedua, hidroksida U, RE203, dan Th yang terbentuk bereaksi dengan adanya reagen basa yang berlebihan membentuk kompleks yang larut sehingga berada bersama-sama larutan fosfat [3]. Salah satu contoh mekanisme reaksi yang terjadi terhadap Th bilamana reagen basa
berlebihan adalah sebagai berikut[3][4] : Th3(P04)4+12NaOH~3Th(OH)4+4Na3P04 Th(OH)4+0H'- Th(OHh 5'(kompleks larut)
Hasil percobaan untuk menentukan waktu dekomposisi optimal disajikan dalam Tabel 2, terlihat bahwa rekoveri U, RE203 ,
Th dan P043. yang terdekomposisi makin banyak dengan bertambahnya waktu dekomposisi, tetapi setelah 4 jam rekoveri mulai terlihat konstan. Hal ini disebabkan karena dengan bertambahnya waktu dekomposisi, semakin lama waktu kontak antara bijih dan reagen (NaOH), reaksi yang terjadi makin sempurna tetapi setelah 4 jam reaksi mencapai kesetimbangan sehingga rekoveri P043' tidak bertambah meskipun waktu reaksinya diperpanjang. Berdasarkan hal tersebut diatas maka dipilih waktu dekomposisi optimal 4 jam.
Hasil percobaan untuk menentukan ukuran bijih disajikan dalam Tabel 3, terlihat bahwa semakin halus ukuran bijih, rekoveri P043- yang terdekomposisi makin besar. Hal ini disebabkan karena makin mudah dipenetrasi oleh NaOH karena rasio permukaan bijih terhadap volume jauh lebih besar sehingga reaksi lebih sempurna. Sedangkan rekoveri U, RE203 dan Th makin kecil dengan makin halusnya bijih. Oleh karena itu dipilih ukuran bijih yang paling kecil yaitu minus 325 mesh.
KESIMPULAN
Kondisi dekomposisi optimal bijih uranium Rirang Kalan yang ditentukan dalam penelitian ini adalah sebagai berikut : • Perbandingan (be rat) bijih : NaOH : air
PROSIDING
SEMINAR GEOLOGI NUKLIR DAN SUMBERDAYA TAMBANG TAHUN 2004PUSAT PENGE""BANGAN BAHAN GAl...IAN DAN GE<>L<::>Gt NUKUR-BATANI..JClkc:::w"fC::l•. 22 S<epternb<er 2004
•
•
Waktu"ThoriumProductionL., 2. CUTHBERT
= 4 jam
Technology", Addition
Wesley Ukuran bijih
Publishing Company, Inc., tahun 1958
= minus 325 mesh
3. COTTON, F.A,
WILKINSONG,
dengan suhu yang ditetapkan sebesar 140
°c
menghasilkan rekoveri P043- ±88,60 %dan unsur-unsur lain yang ikut terlarut adalah U ±13,05 %, RE203 ±6,51 %, dan Th ±16,99 %.
DAFT AR PUST AKA
1. BUSCH KLAUS, DJAWADI, AND SOEPRAPTO, "Investigation of Uranium Mineralization in the Rirang valey", West Kalimantan, Indonesia, tahun 1986.
Advanced Inorganic Chemistry", John Willey & Sons Inc., New York, tahun 1998.
4. CALLOW R.J, "The Industrial Chemistry of The Lanthanous, Ytrium and Uranium", Pergamon Press, tahun 1965.