7 BAB II
TINJAUAN PUSTAKA
Pada bab ini akan dikemukakan secara sistematis berbagai hal yang berkaitan dengan modifikasi bentonit menggunakan surfaktan kationik berbasis fatty imidazolinium. Pada sub bab pertama akan dijelaskan mengenai surfaktan; definisi surfaktan, tegangan permukaan dan antarmuka, sistem emulsi, klasifikasi surfaktan, cairan ionik sebagai salah satu kelompok dari surfaktan kationik, serta lebih spesifik lagi mengenai pengelompokan cairan ionik berbasis imidazolinium sebagai surfaktan kationik. Pada sub bab selanjutnya, akan diuraikan secara singkat mengenai bentonit; struktur, sifat, kapasitas pertukaran kation bentonit, dan pembentukan organobentonit. Pada sub bab berikutnya akan dikemukakan berbagai teori umum mengenai lumpur bor serta potensi pemanfaatan fatty imidazolinium sebagai pemodifikasi bentonit yang akan memberikan karakter termal yang baik ketika diaplikasikan pada lumpur pengeboran.
2.1 Surfaktan
2.1.1 Definisi Surfaktan
Surfaktan (surface active agent) merupakan senyawa organik ampifilik yang dalam molekulnya memiliki sedikitnya satu gugus hidrofilik (bagian kepala) dan satu gugus hidrofobik (bagian ekor). Molekul ini dapat melarutkan dua fasa cairan yang tidak dapat saling melarutkan menjadi larut, baik dalam pelarut organik maupun air (www.wikipedia.org).
Gambar 2.1 Molekul Surfaktan 2.1.2 Tegangan Permukaan dan Interface
Ketika ditambahkan ke dalam suatu cairan pada konsentrasi rendah, maka surfaktan dapat mengubah karakteristik tegangan permukaan dan interface (antar muka) cairan tersebut. Interface adalah bagian dimana dua fasa saling bertemu/ kontak (www.about.org).
Surfaktan mengurangi tegangan permukaan air dengan mengadsorbsinya pada interface cair-gas. Surfaktan pun mengurangi tegangan interfacial antara minyak dan air dengan mengadsorbsinya pada interface cair-cair. Banyak surfaktan juga dapat menyusun partikel-partikel larutan ke dalam agregat. Contoh dari bentuk agregat yang ada adalah vesikel dan misel (www.chemistry.co.nz).
2.1.3 Surfaktan dan Sistem Emulsi
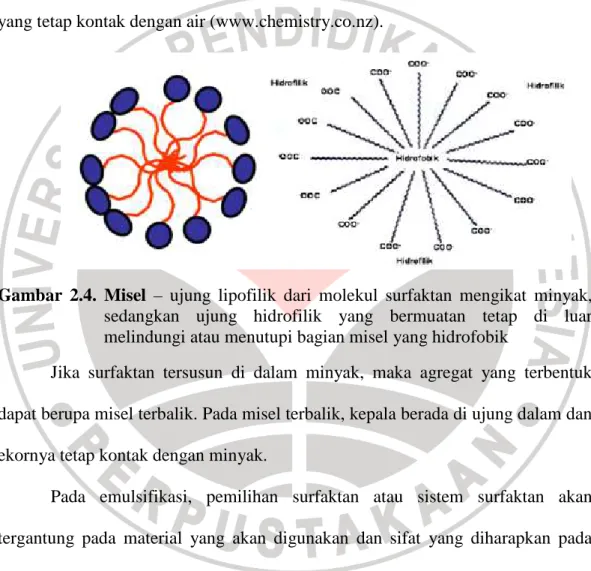
Konsentrasi dimana surfaktan mulai membentuk misel dikenal sebagai Konsentrasi Kritis Misel (critical micelle concentration) atau CMC. Saat misel terbentuk di dalam air, ekornya membentuk ujung dalam yang bisa menutupi tetesan minyak, dan bagian kepalanya yang polar/ ionik membentuk lapisan luar yang tetap kontak dengan air (www.chemistry.co.nz).
Gambar 2.4. Misel – ujung lipofilik dari molekul surfaktan mengikat minyak, sedangkan ujung hidrofilik yang bermuatan tetap di luar melindungi atau menutupi bagian misel yang hidrofobik
Jika surfaktan tersusun di dalam minyak, maka agregat yang terbentuk dapat berupa misel terbalik. Pada misel terbalik, kepala berada di ujung dalam dan ekornya tetap kontak dengan minyak.
Pada emulsifikasi, pemilihan surfaktan atau sistem surfaktan akan tergantung pada material yang akan digunakan dan sifat yang diharapkan pada produk akhir. Efek dari keberadaan surfaktan ini, kestabilan suspensinya sebanding dengan ukuran partikel dan kerapatan material tersuspensinya (www.chemistry.co.nz).
2.1.4 Klasifikasi Surfaktan
Surfaktan bisa diklasifikasikan berdasarkan gugus hidrofilik/ gugus muatan formal yang ada pada bagian kepalanya. Surfaktan non-ionik tidak memiliki gugus bermuatan pada bagian kepalanya. Bagian kepala dari surfaktan ionik tentunya membawa suatu gugus bermuatan. Jika muatannya negatif, maka surfaktannya lebih spesifik dengan sebutan surfaktan anionik. Sedangkan jika muatannya positif, maka disebut surfaktan kationik. Untuk surfaktan yang kepalanya memiliki dua gugus bermuatan yang berlawanan, maka surfaktan tersebut dikenal dengan istilah surfaktan zwitterionik.
2.1.5 Cairan Ionik
Cairan ionik adalah garam yang berwujud cair pada temperatur ruangan atau berada di bawah temperatur ruangan, bentuk lelehannya diisi keseluruhan ion (terdiri dari kation organik dan anion organik atau anorganik) (Mudzakir, 2006; Gordon, 2001 dan Davis, dkk., 2003).Sebagai spesi ionik (kation dan anion), cairan ionik tidak mengandung molekul netral tertentu, dan mempunyai titik leleh relatif rendah, terletak pada suhu < 100-150 oC, walaupun umumnya pada suhu kamar (Hagiwara, dkk., 2000).
Berbeda dengan garam cair (molten salts) yang biasanya mempunyai titik leleh dan viskositas tinggi juga sangat korosif, cairan ionik merupakan garam organik yang memiliki struktur asimetri tinggi yang dapat menghalangi pemadatan dan proses kristalisasi, umumnya berwujud cair pada suhu kamar, mempunyai viskositas relatif lebih rendah dan relatif tidak mempunyai sifat korosif (Brennecke, dkk., 2001; Toma, dkk., 2000). Seperti juga garam cair, cairan
ionik seluruhnya terdiri atas ion-ion (kation dan anion), tetapi mempunyai titik leleh yang relatif rendah, terletak pada suhu dibawah 100oC, walaupun umumnya pada suhu kamar (Fitzwater, dkk., 2005).
Cairan ionik mempunyai rentang cair yang sangat lebar; tidak menguap (non volatile); tidak terbakar (non flammable); stabilitas panas, kimia, dan elektrokimia yang tinggi (dalam bebarapa kasus mempunyai stabilitas termal sampai 400 °C); nilai tekanan uap yang dapat diabaikan; kemampuan melarutkan banyak senyawa organik dan anorganik; serta sifat kedapatlarutan (miscibility) yang beragam dengan pelarut air dan pelarut organik (Davis, dkk., 2003).
Aplikasi cairan ionik sangat luas diantaranya dalam bidang elektrokimia, bidang teknik, dan sintesis senyawa kimia. Pada bidang teknik proses, cairan ionik digunakan sebagai fluida teknik seperti sebagai cairan pengemban panas, pelumas, surfaktan dan kristal cair (Blake, dkk., 2002; Ye, dkk., 2001; Merrigan, dkk., 2000; Walid, dkk., 2004; Hollbrey, 1999; dan Gordon, 1998).
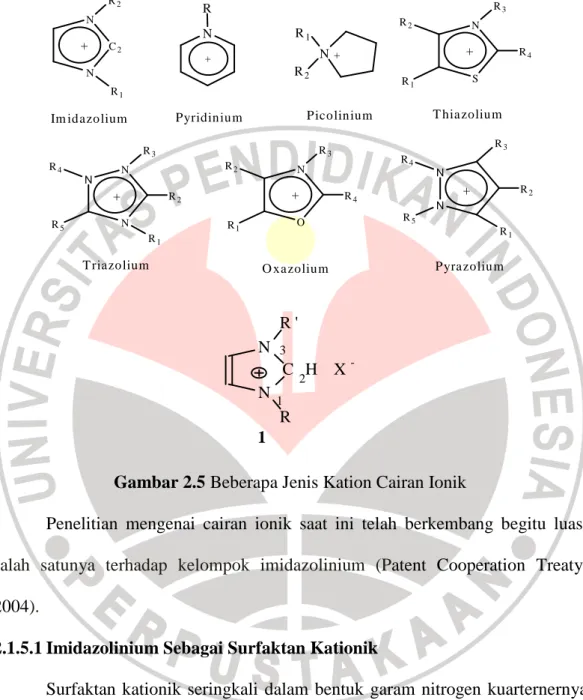
Sistem kation pada cairan ionik (dan kristal cair ionik) umumnya merupakan kation organik dengan sifat ruah, seperti N-alkilammonium, P-alkilposfonium, N-alkil-piridinium, S-alkilsulfonium, N-alkilpirolidinium, N,N-dialkilpirazolium dan N,N-dialkilimidazolium (Olivier, dkk., 2002).
N C2 N R2 R1 + [N RXH(4-X )]+ [SRXH(3-X )] [PRXH(4-X )]+ + N R + N R1 R2 + S N R3 R4 + R2 R1 N N N R3 R2 R4 R5 R1 O N R3 R4 + R2 R1 N N R3 R2 R4 R5 R1
A m onium Sulfonium Posfonium
Im idazolium Pyridinium Picolinium T hia zolium
T riazolium O xa zolium Pyra zolium
+ + N C H X -N R ' R 1 2 3 1
Gambar 2.5 Beberapa Jenis Kation Cairan Ionik
Penelitian mengenai cairan ionik saat ini telah berkembang begitu luas, salah satunya terhadap kelompok imidazolinium (Patent Cooperation Treaty, 2004).
2.1.5.1Imidazolinium Sebagai Surfaktan Kationik
Surfaktan kationik seringkali dalam bentuk garam nitrogen kuarternernya dan digunakan secara luas baik pada sistem aqueous maupun non-aqueous (Divya, et.al.,1976). Pada umumnya, surfaktan kationik diklasifikasikan ke dalam empat 4 kelas garam; garam fatty amine, garam fatty diamine, senyawa ammonium kuarterner, dan garam imidazolinium.
Senyawa imidazolin tersubstitusi memiliki kestabilan selama penyimpanan, viskositas, dispersibilitas, dan berbagai ragam aplikasi industri lainnya (Tyagi, et.al., 2007). Imidazolin kationik memiliki muatan positif pada inti imidazolin dan muatan elektrik pada molekul yang tidak terpengaruh oleh perubahan pH. Muatan positifnya akan tetap bertahan meski pada media asam, basa, maupun netral. Pada produk rumah tangga, surfaktan kationik ini sering diaplikasikan sebagai pelembut buatan, sabun, detergen, kondisioner rambut, dan perawatan rambut lainnya (Smith, 1976).
X- = Halida
R = C15-C17
Gambar 2.6 Struktur Imidazolinium
Surfaktan kationik imidazolinium dapat disintesis dari asam lemak dan trigliserida (Earl GW dkk dalam Tyagi, 2007).
2.2 Bentonit dan Organobentonit
Bentonit adalah batuan yang terbentuk dari lempung yang memiliki sifat plastis dan koloidal yang tinggi. Lempung tersebut tersusun dari monmorillonit sebagai komponen utama, suatu mineral lempung dari kolompok smektit, yang terbentuk melalui devitrifikasi abu vulkanis secara in situ. Selain monmorillonit, bentonit juga mengandung feldspar, kristobalit, dan kuarsa kristalin. Karakter utama bentonit adalah mampu membentuk gel thixotropic bersama air, suatu
kemampuan untuk menyerap air dalam jumlah yang sangat banyak, dan kapasitas tukar kation yang sangat tinggi. Sifat bentonit tersebut diperoleh dari struktur Kristal gugus smektit, dimana satu sublapis alumina oktahedral berada di antara dua sublapis silika tetrahedral. Variasi interstisi air dan kation yang dapat dipertukarkan pada ruang interlayer mempengaruhi sifat bentonit.
Dengan komposisi kimia secara umum (Mg,Ca)O.Al2O3.5SiO2. nH2O,bentonit berbeda dari clay lainnya karena hampir seluruhnya (75%) merupakan mineral monmorillonit. Monmorilonit digunakan secara luas di seluruh dunia sebagai drilling mud. Kebanyakan material dari jenis ini, secara umum dikenal sebagai bentonit. Bentonit tipe ini akan menghasilkan drilling mud yang dapat bekerja pada konsentrasi yang rendah, sekitar 5,5 sampai 7 persen dari berat mud, dengan hanya air saja, sebanding terhadap hasil dari 80 hingga lebih dari 100 barel mud per ton bentonit. Bentonit demikian berharga karena karakter permeabilitas cake-nya yang rendah, demikian halnya kelembutan yang diberikan terhadap filter cake tersebut.
Mineral monmorillonit terdiri dari partikel yang sangat kecil sehingga hanya dapat diketahui melalui studi mengunakan XRD (X-Ray Difraction). Struktur monmorillonit memiliki konfigurasi 2:1 yang terdiri dari dua silikon oksida tetrahedral dan satu aluminium oksida oktahedral. Pada tetrahedral, 4 atom oksigen berikatan dengan atom silikon di ujung struktur. Empat ikatan silikon terkadang disubtitusi oleh tiga ikatan aluminium. Pada oktahedral, atom aluminium berkoordinasi dengan enam atom oksigen atau gugus-gugus hidroksil yang berlokasi pada ujung oktahedron. Al3+dapat digantikan oleh Mg2+, Fe2+,
Zn2+, Ni+, Li+ dan kation lainnya. Substitusi isomorphous dari Al 3+ untuk Si 4+ pada tetrahedral dan Mg 2+ atau Zn 2+ untuk Al 3+ pada oktahedral menghasilkan muatan negatif pada permukaan clay, hal ini diimbangi dengan adsorpsi kation di lapisan interlayer (Alemdar, et. al., 2005).
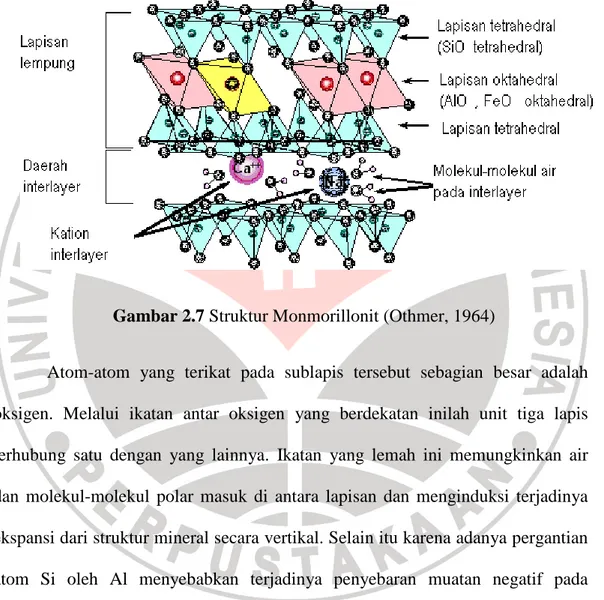
Gambar 2.7 Struktur Monmorillonit (Othmer, 1964)
Atom-atom yang terikat pada sublapis tersebut sebagian besar adalah oksigen. Melalui ikatan antar oksigen yang berdekatan inilah unit tiga lapis terhubung satu dengan yang lainnya. Ikatan yang lemah ini memungkinkan air dan molekul-molekul polar masuk di antara lapisan dan menginduksi terjadinya ekspansi dari struktur mineral secara vertikal. Selain itu karena adanya pergantian atom Si oleh Al menyebabkan terjadinya penyebaran muatan negatif pada permukaan bentonit. Bagian inilah yang disebut sisi aktif (active site) dari bentonit, dimana bagian ini dapat menyerap kation dari senyawa-senyawa organik atau dari ion-ion senyawa logam.
Perbedaan substitusi posisi kisi dan komposisi dasar menghasilkan jenis mineral lempung monmorillonit yang bervariasi. Antara lain monmorillonit (murni), nontronit, saponit, hektorit, saukonit, beidellit, volkhonskoit, pimelit, dan grifitit. Rumus molekul untuk monmorillonit secara umum adalah sebagai berikut: (M+ x·nH2O) (Al2–yMgx)Si4O10(OH)2, where M+ = Na+, K+, Mg2+, or Ca2+ (Brindley & Brown, 1980). Idealnya, x = 0.33.
Bentonit mempunyai berbagai kegunaan dikarenakan sifat koloidnya. Saat dicampur dengan air, material tersebut dapat mengalami pengembangan (swelling) secara signifikan. Di dalam air dan beberapa kondisi lingkungan yang organis, mineral ini pun dapat menghasilkan homogenitas yang baik serta plastisitas yang tinggi. Monmorilonit yang memiliki layer tipe smectite juga memiliki muatan permukaan yang negatif sehingga dapat memungkinkan pertukaran kation, seperti Na+ atau Ca2+.
Dispersi bentonit sensitif terhadap kation yang mudah dipertukarkan dan pH. Valensi kation yang dapat dipertukarkan, monovalen atau bivalen, memiliki pengaruh yang kuat terhadap sifat alirnya (Lagaly, 1994). Dalam hal pertukaran kation organik untuk ion-ion yang dapat dipertukarkan pada permukaan mineral, kation akan dilepaskan ke dalam larutan. Kation organik juga dapat masuk ke dalam reaksi pertukaran ion dengan kation-kation yang dapat ditukar di antara layer-layer-nya (Lagaly, 1994). Permukaan clay dapat dimodifikasi untuk membuat suatu organofilik yang kuat.
Organobentonit adalah bentonit yang menyerap molekul kation dari senyawa-senyawa organik. Selain itu bentonit yang dimodifikasi oleh senyawa organik dapat pula disebut sebagai organobentonit. Ada banyak pemanfaatan yang diperoleh dengan disintesisnya organobentonit. Pestisida dan makanan hewan merupakan sebagian kecil dari pemanfaatan organobentonit (Othmer, 1964).
Penambahan kation organik yang berasal dari garam organik dapat pula menghasilkan organobentonit yang memiliki sifat tertentu (Walid, dkk., 2003). Salah satu sifat yang merupakan suatu hal yang penting dalam pembentukan organobentonit adalah kestabilan termal yang dimiliki oleh garam organik. Dengan kestabilan termal yang dimiliki oleh garam organik yang selanjutnya digunakan untuk memodifikasi sifat bentonit, diharapkan akan terbentuk bentonit termodifikasi atau organobentonit yang memiliki kestabilan termal yang tinggi.
Salah satu sifat yang menarik dari bentonit adalah memiliki kemampuan menyerap kation tetentu yang selanjutnya diubah menjadi kation lain dengan menggunakan suatu pereaksi ion tertentu. Reaksi pertukaran kation ini terjadi pada bagian sisi dari unit struktur silika aluminat sehingga tidak merubah struktur mineral dari bentonit.
Pertukaran kation adalah reaksi reversibel dengan tranfer energi rendah dari ion antara fasa padat dan fasa cair. Metode pertukaran kation banyak digunakan pada proses-proses yang berkaitan dengan tanah, seperti pada pemisahan mineral tanah, adsorpsi nutrisi tanah, pemisahan senyawa elektrolit, dan untuk mempertahankan pH tanah.
Proses pertukaran kation menyebabkan terjadinya netralisasi dari muatan negatif koloid tanah melawan muatan kation. Kation berikatan dengan permukaan koloid melalui ikatan van der Waals. Gerakan kation pada permukaan koloid tidak terlalu kaku, tetapi karena ada energi panas yang mempengaruhi gerakan dan menyebabkan lebih mudah bergerak dai permukaannya, seperti gerakan belahan yang memberikan kombinasi khusus dari ion dan permukaan koloid. Ada dua tipe permukaan, pertama yang sukar terikat sehingga sulit terjadi pertukaran atau fixed cation dan yang kedua adalah tidak terlalu sukar untuk berikatan sehingga terjadi pertukaran kation.
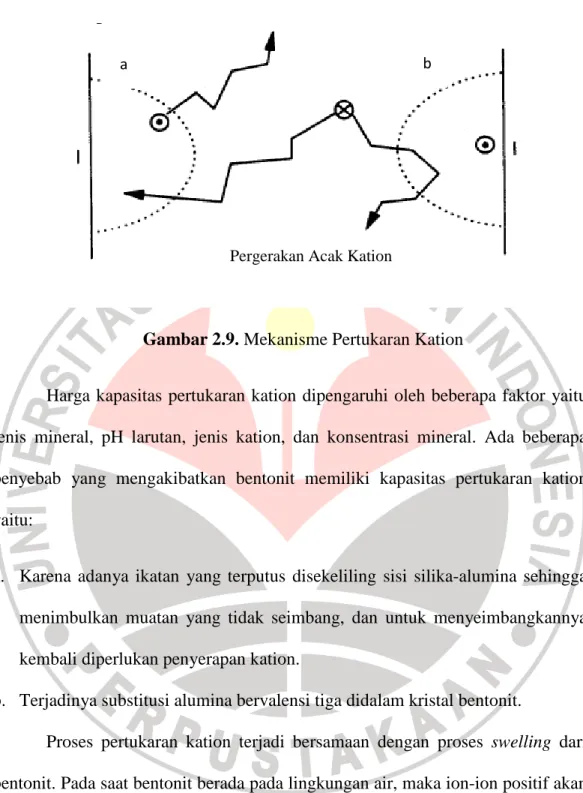
Pertukaran kation terjadi ketika ion ( ) berada dalam suatu larutan, kemudian bergerak daerah belahan kation pada permukaan ( ), sehingga terjadi proses pertukaran kation (Gambar 2.9a). Namun apabila ion yang ada pada permukaan terlalu sulit untuk mengalami pertukaran kation, maka pertukaran kation tidak akan terjadi (Gambar 2.9b).
Gambar 2.8. Kation yang Mengalami Pertukaran dan Tidak Mengalami Pertukaran
Tidak Terjadi Pertukaran (Gerakan Belahan Kecil)
Terjadi Pertukaran (Gerakan Belahan Besar)
Gambar 2.9. Mekanisme Pertukaran Kation
Harga kapasitas pertukaran kation dipengaruhi oleh beberapa faktor yaitu jenis mineral, pH larutan, jenis kation, dan konsentrasi mineral. Ada beberapa penyebab yang mengakibatkan bentonit memiliki kapasitas pertukaran kation yaitu:
a. Karena adanya ikatan yang terputus disekeliling sisi silika-alumina sehingga menimbulkan muatan yang tidak seimbang, dan untuk menyeimbangkannya kembali diperlukan penyerapan kation.
b. Terjadinya substitusi alumina bervalensi tiga didalam kristal bentonit.
Proses pertukaran kation terjadi bersamaan dengan proses swelling dari bentonit. Pada saat bentonit berada pada lingkungan air, maka ion-ion positif akan meninggalkan matrik bentonit. Karena molekul air bermuatan polar maka molekul air akan tertarik pada matrik bentonit dan kation yang terlepas dari bentonit. Apabila terjadi proses balik yaitu penarikan kation oleh bentonit, molekul air yang
Pergerakan Acak Kation
b a
bermuatan positif akan tertarik menuju bentonit. Sehingga terjadi proses mengembang dari bentonit yang lebih dikenal dengan istilah swelling.
2.3 Drilling Mud
Lumpur pengeboran (Drilling Mud) adalah suatu cairan yang terdiri dari campuran dari berbagai macam material yang dipakai pada waktu pengeboran. Dalam Luqman Arif, dkk (2001), secara umum lumpur pengeboran mempunyai empat komponen dasar, yaitu:
a. Komponen Cair
Komponen cair adalah suatu material yang diperlukan dalam pembuatan sistem lumpur (mud base) yang nantinya akan menentukan jenis sistem lumpur. Komponen cair dapat berupa air atau minyak. Air dapat pula dibagi menjadi dua yaitu air tawar dan air asin.
b. Komponen Padat Reaktif
Padatan ini bereaksi dengan sekelilingnya (sistem) membentuk koloid. Clay air tawar seperti bentonit menyerap air tawar dan membentuk lumpur. Jumlah barel lumpur yang dihasilkan dari satu ton clay agar viskositasnya 15 cp, disebut “yield”. Untuk bentonit yield-nya kira-kira 100 bbl/ton.
c. Komponen Padat Inert
Komponen Padat Non-Reaktif Komponen padat non-reaktif adalah komponen padat yang tidak bereaksi (inert) terhadap sistem lumpurnya atau komponen pemberat, seperti barit (BaSO4), galena (PbS) dan biji besi atau ore (Fe2O3).
d. Komponen Aditif/Pengontrol
Komponen aditif merupakan bagian dari sistem yang digunakan untuk mengontrol sifat-sifat lumpur bor. Bahan kimia tersebut pada umumnya digunakan untuk mengontrol: viskositas, filtration loss, pH, densitas.
2.3.1 Fungsi Lumpur Pengeboran
Fungsi utama lumpur pengeboran adalah mengangkat serbuk bor ke permukaan, mengontrol tekanan formasi, mendinginkan serta melumasi pahat dan
drill string, membersihkan dasar lubang bor, membantu dalam evaluasi formasi,
melindungi formasi produktif, dan membantu stabilitas formasi (Luqman Arif, dkk, 2001).
2.3.2 Sifat-Sifat Fisik Lumpur Pengeboran
Sifat fisik Lumpur yang terpenting yang dikontrol pada setiap operasi sumur migas dan panas bumi ada tiga, yaitu:
2.3.2.1Densitas
Pengontrolan densitas lumpur pada hakekatnya adalah mencegah blow out, dan kadang-kadang juga digunakan untuk menjaga stabilitas lubang bor. Lumpur yang terlalu berat dapat menyebabkan terjadinya lost circulation. Sedangkan, lumpur yang terlalu ringan dapat menyebabkan masuknya fluida formasi ke dalam lubang bor (kick ) dan jika tidak segera diatasi akan menyebabkan terjadinya semburan liar (blow out).
2.3.2.2 Reologi (sifat aliran)
Studi mengenai reologi atau sifat alir dari suatu suspensi merupakan suatu metoda penting untuk mengkarakterisasi interaksi partikel-partikel (Moore, J.H, dan Spencer, N.D., 2001). Pada tataran praktis, pengontrolan sifat-sifat reologi suspensi sangat krusial, dimana selama proses dan pada tahap aplikasi akhir, perilaku aliran biasanya harus berada di antara rentang spesifikasi yang cukup sempit.
Secara general, tegangan shear (gaya/ luas permukaan) koloidal suatu fluida Newtonian, τ sebanding dengan laju pemisahan (gradien kecepatan),
(2.1) Dispersi koloid seringkali menampakkan perilaku non-Newtonian, dimana perbandingan persamaan di atas tidak berlaku. Hal ini sangat penting bagi dispersi yang kental, yang cenderung sering digunakan. Persamaan (2.1) dapat digunakan untuk menentukan viskositas nyata, happ, pada laju pemisahan tertentu. Jika happ menurun seiring meningkatnya laju pemisahan, dispersi yang terjadi dapat dikatakan menipis (pseudoplastik). Tapi, jika meningkat, maka dapat dinyatakan sebagai menebal (dilatan).
Viskositas nyata juga bisa berubah sebagai fungsi waktu, pada penetapan laju pemisahan tetap, yang dihubungkan dengan pembentukan atau pemutusan jaringan partikel. Thixotropic dispersi menunjukkan penurunan happ seiring waktu. 2.3.2.2.1 Interaksi Partikel
Kebanyakan sifat dari suspensi koloidal, seperti kestabilannya, reologinya, dan perilaku fasa sangat berhubungan dengan interaksi diantara partikel-partikel
suspensi. Faktor-faktor yang paling banyak berkontribusi pada interaksi ini diantaranya:
2.3.2.2.2 Interaksi Van der Waals
Diantara dua atau lebih atom atau molekul, gaya van der Waals sangat berperan karena interaksi yang terjadi akibat fluktuasi medan elektromagnetik yang dihasilkan dari polarizabilitasnya. Demikian halnya, gaya van der Waals akan bekerja diantara dua partikel koloid pada suspensi.
2.3.2.2.3 Interaksi Elektrostatik
Pada pelarut polar, muatan elektrostatik biasanya memiliki kontribusi yang penting terhadap interaksi partikel.
2.3.2.2.3.1 Double Layer Bermuatan
Teori paling sederhana untuk menjelaskan double layer bermuatan, berasal dari teori Gouy–Chapman. Jika diasumsikan suatu larutan memiliki ion valensi z+ dan z-- pada medium dengan konstanta dielektrik є, ion-ion tersebut dapat diwakili oleh titik-titik muatan (tidak memiliki ukuran) dan diasumsikan bahwa ion-ion itu bergerak mengikuti pola Brownian.
Molekul yang berukuran terlalu panjang dan/ atau ruah akan mengalami penurunan distribusi ion ketika mendekati permukaan.
Permukaan pada pelarut polar, cenderung akan bermuatan melalui disosiasi gugus permukaan atau melalui adsorpsi ion-ion, menghasilkan rapat muatan σ. Di dekat pemukaan yang rata, besarnya potensial permukaan, Φ hanya akan bergantung pada jarak x dari permukaan.
2.3.2.2.3.2 Misel Yang Teradsorpsi
Pembentukan agregat surfaktan di permukaan dan bagaimana surfaktan tersebut tersusun ketika teragregasi di permukaan berhubungan dengan level atomik dan struktur mesoskala (geometri, bentuk, dan lain-lain).
Secara umum, adsorpsi surfaktan bermuatan akan meningkat, ketika diasumsikan bahwa muatan permukaan yang prevalen berlawanan dengan muatan kepala surfaktan. Asumsi ini paling banyak diterapkan pada adsorpsi surfaktan kationik berantai lurus pada permukaan bermuatan negatif (silika, logam, mineral, dan lain-lain).
Pengontrolan reologi diperlukan untuk mengangkat serbuk bor (cutting) pada saat pengeboran berlangsung. Dalam istilah teknis perminyakan, istilah “sifat aliran” (flow properties) dan “viskositas” digunakan untuk menggambarkan perilaku lumpur pengeboran dalam keadaan bergerak.
Viskositas fluida pengeboran merupakan fungsi dari beberapa faktor, yaitu:
a. Viskositas fasa cair
b. Volume padatan dalam lumpur
c. Volume fluida yang terdispersi (emulsi) d. Jumlah partikel per satuan lumpur e. Bentuk partikel padatan
f. Gaya tarik (atau gaya tolak) antara partikel-partikel padat, dan antara fasa padat dengan fasa fluida
Viskositas menunjukkan kekentalan lumpur dalam aliran, dan gel strength menunjukkan kekentalan lumpur dalam kondisi diam pada periode waktu tertentu. Secara ilmiah, viskositas adalah suatu konstanta antara shear stress dan shear rate untuk fluida Newtonian, seperti air, tetapi tidak berlaku untuk lumpur pengeboran. Untuk fluida pengeboran, perbandingan antara shear stress dan shear rate berkurang dengan naiknya shear rate.
Penggunaan utama plastic viscosity yang diukur dalam centipoises, adalah untuk menunjukkan pengaruh kandungan padatan terhadap kekentalan lumpur. Plastic viscosity diperoleh dengan mengurangkan dial reading 600 rpm dengan 300 rpm pada viscometer.
Besarnya plastic viscosity dipengaruhi oleh kandungan padatan, ukuran padatan, dan temperatur. Sukar mengatakan bahwa berat lumpur tertentu harus mempunyai viskositas tertentu juga, karena faktor ukuran padatan berpengaruh.
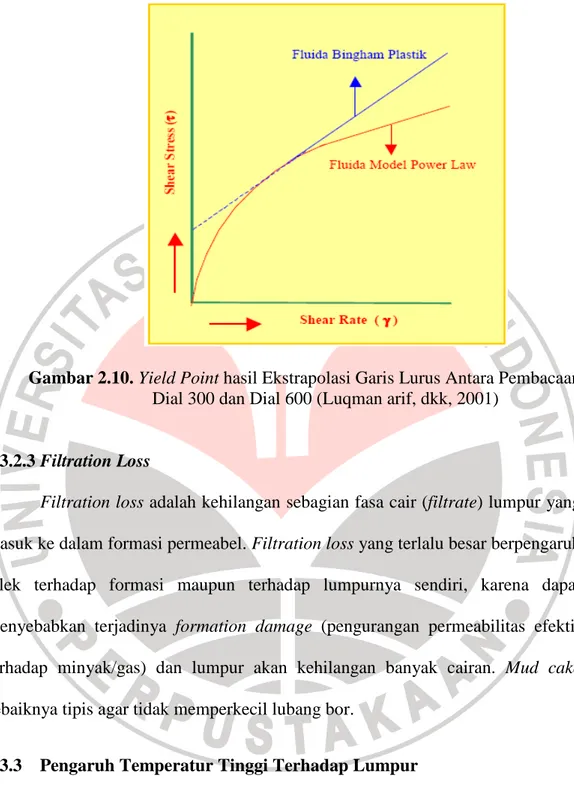
Yield point adalah merupakan suatu pseudometer, seperti ditunjukkan pada Gambar 2.10, yang diperoleh dengan ekstrapolasi garis lurus antara pembacaan di 300 rpm dan 600 rpm pada viscometer. Yield point ditentukan secara kuantitatif dengan pengurangan pembacaan 300 rpm dengan plastic viscosity.
Gel strength merupakan suatu harga yang menunjukkan kemampuan lumpur untuk menahan padatan-padatan. Faktor yang menyebabkan terbentuknya gel strength yaitu adanya gaya tarik menarik dari partikel-partikel atau plat-plat clay sewaktu tidak adanya sirkulasi lumpur. Fungsi gel strength dalam lumpur pengeboran adalah menahan cutting dan pasir dalam suspensi sewaktu sirkulasi lumpur dihentikan.
Gambar 2.10. Yield Point hasil Ekstrapolasi Garis Lurus Antara Pembacaan Dial 300 dan Dial 600 (Luqman arif, dkk, 2001)
2.3.2.3Filtration Loss
Filtration loss adalah kehilangan sebagian fasa cair (filtrate) lumpur yang masuk ke dalam formasi permeabel. Filtration loss yang terlalu besar berpengaruh jelek terhadap formasi maupun terhadap lumpurnya sendiri, karena dapat menyebabkan terjadinya formation damage (pengurangan permeabilitas efektif terhadap minyak/gas) dan lumpur akan kehilangan banyak cairan. Mud cake sebaiknya tipis agar tidak memperkecil lubang bor.
2.3.3 Pengaruh Temperatur Tinggi Terhadap Lumpur
Pada temperatur tinggi lumpur, sifat fisik lumpur yaitu sifat reologi dan filtration loss sulit untuk diprediksikan perubahannya. Hal ini disebabkan karena sifat-sifat tersebut sangat sensitif terhadap perubahan temperatur. Parameter dari
sifat reologi yang paling sensitif terhadap perubahan pembebanan temperatur adalah viskositas.
Ada beberapa faktor yang mempengaruhi viskositas lumpur pengeboran, diantaranya :
1) Interaksi mekanis antara padatan dan cairan 2) Interaksi elektris antara padatan-padatan dan 3) Shear rate
Pada umumnya fluida non-newtonian cenderung encer dengan adanya pengaruh shear, sebagai contoh, viskositas berkurang sebagai akibat naiknya shear rate. Perilaku fluida non-newtonian ini adalah karena interaksi padatan-padatan dalam lumpur. Interaksi padatan-padatan menyebabkan tahanan terhadap aliran gaya tarik elektrostatik dan refulsi pada permukaan padatan yang bermuatan listrik, atau dari tahanan mekanis terhadap aliran antara partikel dan fluida.
Perubahan viskositas plastis terhadap temperatur dan perubahan viskositas air terhadap temperatur mengindikasikan bahwa high-shear-rate viscosities ditentukan oleh interaksi mekanis antara padatan dan cairan. Hal ini berarti bahwa untuk meminimalkan viskositas pada high-shear-rate (seperti shear rate dibawah pahat), konsentrasi padatan dalam lumpur dan viskositas fraksi cairan di minimalkan.
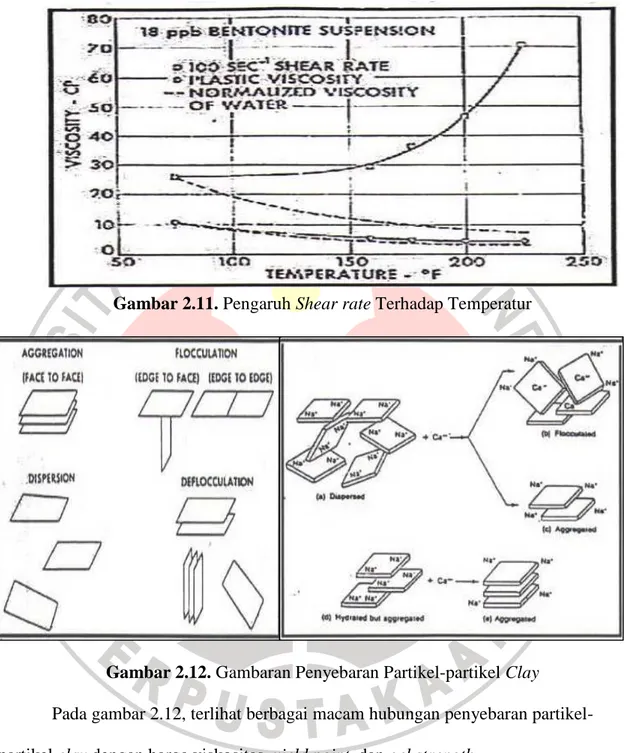
Gambar 2.11 juga menunjukkan bahwa viskositas shear rate rendah lebih besar dari viskositas pada viskositas pada shear rate yang lebih tinggi dan bahwa perbedaan ini menjadi lebih besar dengan bertambahnya temperatur. Suspensi menjadi lebih encer karena pengaruh shear dengan naiknya temperatur.
Gambar 2.11. Pengaruh Shear rate Terhadap Temperatur
Gambar 2.12. Gambaran Penyebaran Partikel-partikel Clay Pada gambar 2.12, terlihat berbagai macam hubungan penyebaran partikel-partikel clay dengan harga viskositas, yield point, dan gel strength.
2.3.3.1 Sistem dispersi
Keadaan dimana plat-plat clay tersebar merata karena gaya atraksi ternetralisir. Sistem penyebaran ini biasa dicapai dengan mengagitasikan bentonit ke dalam air tawar dengan menambahkan sedikit thinner. Thinner yang disebut
pula “protection colloid” akan melapisi plat-plat clay sehingga jumlah air yang terhidrasi menjadi lebih sedikit. Dengan cara ini akan didapatkan fasa kontiniu (air bebas) yang lebih banyak, oleh karenanya akan tercapai keadaan dispersi yang lebih stabil.
Sistem penyebaran ini memberikan ukuran partikel-partikel clay yang terkecil sehingga viskositas plastik sistem ini adalah yang tertinggi. Yield point cukup tinggi dan dengan ditambahkannya thinner akan menjadi lebih rendah. Gel strength rendah tapi progressive.
2.3.3.2 Sistem Flokulasi
Keadaan dimana partikel-partikel clay tersebar berupa kumpulan-kumpulan plat-plat yang saling terikat antara bidang permukaan dengan tepi atau tepi dengan tepi. Keadaan penyebaran ini bisa dicapai dengan menambahkan garam monovalen ke dalam sistem lumpur dispersi deflokulasi.
Sistem penyebaran ini kurang stabil, apabila dilakukan pengadukan system akan berubah menjadi dispersi deflokulasi. Viskositas plastis sistem flokulasi di bawah sistem dispersi deflokulasi. Yield point dan gel strength progressive tinggi karena adanya gaya atraksi antara plat-plat clay-nya.
2.3.3.3 Sistem agregasi
Sistem penyebaran partikel clay di dalam lumpur dimana plat-plat clay akan tersebar dalam kumpulan plat-plat clay yang terikat pada bidang-bidang permukaan dan antara tepi-tepinya, kumpulan plat-plat clay ini juga saling terikat, atau antara tepi dan bidang permukaan kumpulan plat-plat clay.
Sistem ini mempunyai luas pemukaan singgung partikel-partikel clay dengan fasa kontiniu yang terkecil, maka dari itu viskositas plastis sistem ini adalah yang terendah dari keempat sistem di atas. Karena adanya gaya atraksi yang kuat antara plat-plat clay maka yield point-nya menjadi tinggi (tertinggi dari keempat sistem), gel strength -nya tinggi tapi non-progressive.
2.3.3.4 Sistem deflokulasi
Dalam sistem ini plat-plat clay tersebar dalam kumpulan plat-plat terikat pada bidang permukaannya. Sistem ini biasa didapatkan dengan menambahkan garam-garam divalen kedalam sistem dispersi. Viskositas plastis sistem ini rendah karena luas bidang singgung plat clay dengan fasa kontiniunya kecil. Yield point rendah dan gel strength non-progressive rendah. Lumpur pengeboran harus mampu mengontrol problem-problem tersebut, sehingga lubang bor tetap terbuka dan proses pengeboran dapat terus dilanjutkan. Perencanaan sistem lumpur untuk menjaga stabilitas lubang bor sering digunakan sebagai basis untuk pemilihan jenis lumpur.
Clay pertama kali digunakan di dalam mud untuk mencegah hilangnya fluida mud itu sendiri. Namun, sebagian mud itu justeru hilang sebagai filternya meskipun cakenya menutupi formasi permeabelnya. Cake filter pada dinding lubang dapat meningkatkan ketebalan dengan bergantung pada banyak faktor, termasuk ketebalan cake yang telah terbentuk, viskositas fasa fluida dari mud (secara umum merupakan fungsi temperatur yang berlaku), diferensial tekanan pada cake, dan yang paling penting permeabilitas dari cake itu sendiri.
Permeabilitas dari cake bergantung pada sumber padatan pada mud, kondisi flokulasinya, dan peningkatan diferensial tekanan cake, beberapa cake diantaranya relatif dapat ditekan. Dalam hal kelemahan, jelas sekali pembentukan cake filter berlawanan dengan formasi permeabilitas serta dapat mereduksi diameter lubang. Pada skala laboratorium, dilakukan pengujian untuk menentukan apakah yang mungkin menjadi karakteristik paling penting dari drilling mud. Mud disaring dengan tekanan melalui kertas saring pada kondisi spesifik, baik waktu, temperatur, dan tekanan. Sehingga, hilangnya filtrat, laju perkembangan cake, dan sifat fisik dari cake dapat ditentukan. Metode untuk mengevaluasi data yang bervariasi pada prosedur pengujian diberikan pada publikasi Larsen (1938), Byck (1940), William dan Cannon (1939), Prokop dan lain-lain.
2.3.4 Fungsi clay di dalam mud
Sebagaimana telah diindikasikan, drilling mud yang biasa dan umum digunakan saat ini mengandung air yang telah ditambahkan ke dalam clay untuk meningkatkan luas permukaannya sehingga bisa menghasilkan viskositas beberapa kali lebih besar dibandingkan air. Demikian halnya, kekuatan untuk memecah yang bertambah. Dalam beberapa kasus utama, thixotropy juga ikut meningkat. Drilling mud tersebut merupakan fluida yang bersifat plastis di mana derajat keplastisitasannya meningkat seiring waktu akan tetapi menurun lagi setelah pengadukan.
Beberapa tahun lalu, telah ditemukan bahwa bentonit berkontribusi dalam mereduksi kerusakan yang diakibatkan korosi pada baja ketika menggunakan drilling mud (Speller, 1936; 1938). Clay sangat penting dalam emulsi lumpur
sebagai agen pengemulsi atau emulsifier. Selain itu, mineral ini juga merupakan bagian penting pada beberapa tipe drilling mud yang berbasis minyak.
Secara alami, semakin tinggi clay koloidalnya, khususnya yang mengandung bagian substansial mineral clay dari tipe swelling, maka semakin besar hasil yang diberikan.
2.3.5 Perlakuan kimia terhadap clay-mud
Beberapa tahun sebelumnya, pengeboran dengan sistem rotasi ini mencoba untuk memberikan perlakuan terhadap mud yang telah dipertebal dengan material-material yang telah ditemukan pada saat itu yang bermanfaat untuk digunakan sebagai campuran keramik, khususnya natrium hidroksida, natrium karbonat, dan natrium silikat. Sayangnya usaha tersebut menemui kegagalan. Saat ini, pereaksi kimia yang digunakan untuk tujuan ini dibagi kedalam dua kelompok besar: kompleks posfat anorganik, dan asam organik lemah yang secara umum memiliki bobot molekul besar yang berasal dari tumbuhan dan asam humik.
Senyawa organik yang telah terbukti paling banyak berguna dalam penipisan drilling-mud adalah yang berasal dari tumbuhan, dimana ekstrak quebracho adalah yang paling banyak digunakan. Sedangkan asam humik secara umum merupakan turunan dari lignit tertentu. Alasan digunakannya senyawa ini adalah karakternya yang baik pada pH alkalin, bahkan pada pH yang cukup tinggi dapat terionisasi sempurna sebagaimana asam yang diasumsikan.
Perlakuan terhadap drilling mud agar filtratnya memiliki efek swelling atau dislodging atau bahkan mungkin keduanya pada clay yang terbentuk serta pada partikel murni lainnya telah banyak memperoleh perhatian dari kalangan
ilmuwan dan khalayak industri beberapa tahun terakhir. Ekspedisi secara umum mendeduksi data dari clay-swelling atau data adhesi dari tipe von Buzagh untuk mensalinifikasi mud, khususnya dengan garam kation di- dan trivalen (Larsen, 1954).
2.3.6 Mud berbasis minyak
Upaya untuk menjaga agar seluruh air yang telah dimasukkan terpisah dari formasi lapisan minyak telah memicu perkembangan fluida pengeboran dengan memanfaatkan minyak dibanding air, sehingga disebut mud berbasis minyak (Oil based mud). Untuk bagian yang paling besar, fluida pengeboran tersebut tidak ditambahkan ke dalam clay, serta penggunaannya yang tidak umum sebagai “pembuat lubang” yang dibedakan dari pengeboran ke dalam formasi lapisan minyak. Rolshausen dan Bishkin (1937) mengajukan penggunaan bentonit secara bersama-sama di dalam mud berbasis minyak untuk mengambil air berlebih yang kinerjanya berlawanan selama pengeboran.
Yang paling menarik serta memainkan peran penting dari mud berbasis minyak dengan menggunakan clay monmorilonit yaitu material ini memiliki karakter swelling di dalam minyak sebagai suatu produk dari reaksi amina rantai panjang dan bentonit (Hauser, 1950). Sebagai contoh bentonit oleofilik, secara substansial dilapisi sepenuhnya oleh kation organik hidrofobik melalui suatu reaksi pertukaran basa yang berkaitan dengan kekuatan gel antara keduanya. Karena karakter yang cenderung merata, fluidanya menghilang menyisakan mud berbasis minyak, serta memungkinkan juga terjadi emulsifikasi air ke dalam mud selama penggunaan sebagai emulsi air-dalam-minyak yang stabil. Keuntungan
khusus lainnya adalah clay organofilik mempertahankan kemampuan gelling meski pada temperatur yang sangat tinggi, sehingga dapat menghindari berbagai kesulitan dan masalah yang dihadapi yang sering ditemui oleh tipe lain.
2.3.7 Cairan ionik fatty Imidazolinium sebagai surfaktan kationik pada drilling mud
Studi saat ini difokuskan pada modifikasi monmorilonit secara organik. Pada sistem ini, surfaktan kationik dengan rantai alkil panjang dapat terikat bagian ujungnya pada permukaan melalui interaksi gaya coulomb dengan layer permukaan yang bermuatan negatif (Hackett dkk., 1998 dalam Lee, 2005). Ketika sejumlah surfaktan kationik berlebih ditambahkan ke dalam larutan, adsorspi surfaktan akan terjadi melebihi kapasitas tukar kation (CEC) pada mineral clay (Lee, 2005). Surfaktan berlebih yang teradsorbsi melebihi CEC pada mineral clay ini dapat dijelaskan oleh interaksi van der Waals (Zhang dkk., 1993 dalam Lee, 2005).
Pemahaman tentang mekanisme adsorpsi surfaktan dan konformasi surfaktan pada permukaan mineral clay sangat krusial untuk memahami interaksi surfaktan yang teradsorbsi dengan senyawa organik dan anorganik dalam larutan serta untuk memprediksikan kestabilan surfaktan yang teradsorbsi. (Boyd, 2000).
Pada penambahan surfaktan kationik ke dalam dispersi mineral cair, surfaktan kationik mengganti kation interlayer yang asli. Penyusunan kation rantai panjang dalam ruang antar layer tergantung pada panjang rantai, muatan permukaan, dan jumlah yang teradsorbsi (Lee dan Kim, 2002a dalam Lee, 2005). Pertukaran ion anorganik yang dapat dipertukarkan oleh surfaktan kationik
menyebabkan flokulasi ketika jumlah yang teradsorbsi sama besar atau kurang dari CEC (Van Olphen, 1977; Xu dan Boyd, 1995; Janek dan Lagaly, 2003 dalam Lee, 2005).
Pada beberapa kasus, molekul terinterkalasi diketahui menyusun dirinya sendiri dalam suatu struktur yang teratur di dalam ruang antar layernya (Lagaly, 1994). Jika dibandingkan dengan material nanoporous atau mesoporous seperti zeolit, molekul-molekul berukuran besar dalam jumlah yang lebih banyak bisa diinterkalasikan ke dalam ruang antar layer, serta dapat mengatur dirinya sehingga dapat mengakomodasi molekul baru yang masuk (guest molecule) dengan meningkatkan jarak antar layernya (Lagaly, 1982; dalam Lagaly, 1994). ruang antarlayer bisa dimodifikasi dengan sejenis molekul (Jordan, 1949; Ogawa dan Kuroda, 1997; Klapyta dkk., 2001; Yui dkk., 2002; Imai dkk., 2003 dalam Lee, 2005). N C H X -N R CH3 1 2 3 2
Gambar 2.13. Struktur Garam 1-Alkil-3-Metil-Imidazolium 2
Pada garam 2 dengan gugus alkil R panjang akan teramati adanya fasa kristal cair (mesophase). Kestabilan mesophase secara cepat akan meningkat dengan meningkatnya panjang gugus R. Walaupun panjang minimum gugus R hingga mesophase teramati ternyata bergantung juga pada anion, tetapi nampaknya mulai gugus R dodesil hal ini dapat dipenuhi.
Tanpa pengecualian, garam 2 dengan gugus R relatif panjang akan menunjukkan fasa kristal cair smektit (smectic mesophases). Pada kondisi ini, molekul-molekul mengatur dirinya membentuk lapisan karena terjadinya interaksi elektrostatis antar konstituen pembentuk kristal cair ionik. Fasa nematik jarang ditemui pada sistem kristal cair ionik .
4 3 2 1 N C R X -N CH2-CH2-NH-C-R O CH3 N C R X -N R CH3 1 2 3 3
Gambar 2.14.Struktur Kation Imidazolium 3 dan Fatty imidazolinium4
Gugus amida primer tak tersubstitusi (-C(O)NH2) dikenal sebagai sinton pembentukan struktur supramolekular pada crystal engineering (Lee, dkk., 2005). Pembentukan kristal cair ionik supramolekular pada kation imidazolium 3 misalnya sebagian besar terstabilkan oleh interaksi ionik dan ikatan hidrogen lemah (interaksi sekunder) kation-anion. Masuknya gugus amida pada struktur kation 3 dapat memperkaya terbentuknya ikatan hidrogen lemah dan akan menstabilkan pembentukan kristal cair ionik supramolekular (Lee, dkk., 2005).
Dengan demikian dapat diduga bahwa dengan masuknya gugus amida pada struktur fatty imidazolinium4 juga akan mendorong kation mengatur dirinya (self-organize) membentuk pita polimer berikatan hidrogen (hydrogen bonded ribbon polymer). Hal ini akan menstabilkan pembentukan mesophase pada
rentang suhu yang cukup lebar. Dengan demikian, diasumsikan emulsi antara fatty imidazolinium dengan bentonit membentuk clay organofilik akan mampu mempertahankan kemampuan gelling meski pada temperatur yang sangat tinggi.