ANALISIS RESIDU ANTIBIOTIKA SPIRAMISIN
DALAM DAGING AYAM SECARA KHROMATOGRAFI
CAIR KINERJA TINGGI (KCKT)
YUNINGSIH danT.B. MURDIATIBalai Penelitian Veteriner, PO Box 151, Bogor 16114
ABSTRACT
Determination of Spiramycin Residue in Tissue by Liquid Chromatography with U.V.Detection
Spiramycin is commonly used in feed additive beside in treatment. Improper use of spiramycin can cause residue (resistance) and allergic reactions. In order to find out the extent of the residue content, it is necessary to carry out research by trying to develop effective and pricise analysis method for the spiramycin residue in tissue. An improved method has been developed for determination of spiramycin in tissue. After extraxction tissue with acetonitrile and isooctane, filtrate were applied to a SPE cartridge (C-18), then it were eluted with methanolic ammonium 0,1 M and analysed by High Performance Liquid Chromatography (HPLC) with UV detection at 232 nm, mobile phase : 0,01M NaHPO4: CH3CN= 77: 23, p.H= 2,5. The
recoveries of spiramycin are 96.29% and 108.33% in duplicates after adding spiramycin standards of 0.50 ug and 1,00 µg for each samples. The recovery result of this modified method is quite significant. A total of 36 samples from Sukabumi, Tangerang and Bogor were analysed for spiramycin residue by using developed method. The result show that 35 samples positive spiramycin, containing 0.0267- 0.6209 µg/g.. It’s conluded that 5 samples are above the Maximum Residue Limits (MRL spiramycin in tissue= 0.2 µg/g).
Key words: Spiramycin, tissue, SPE, HPLC
PENDAHULUAN
Aspek kesehatan masyarakat veteriner merupakan bagian yang sangat penting pada sistim perdagangan pada era globalisasi, termasuk adanya residu antibiotika dalam produk peternakan. Untuk mendukung program monitoring residu oleh pemerintah diperlukan metoda deteksi yang tervalidasi. Oleh karena itu perlu dikembangkan metoda uji spiramisin,suatu antibiotika golongan makrolida perlu dikembangkan.
Pemakaian obat-obatan terutama antibiotika yang terus menerus dan tidak memperhatikan waktu hentinya dalam industri peternakan maka akan menyebabkan residu antibiotika dalam produk hewani yang dihasilkan yang dapat menyebabkan reaksi alergi, resistensi dan kemungkinan keracunan.
Adanya residu antibiotika golongan tetras iklin dan penisilin telah banyak dilaporkan, akan tetapi residu antibiotika golongan makrolida belum banyak dilaporkan, kecuali dari luar negeri (CHAN et al., 1994; OKA et al., 1995). Padahal antibiotika golongan makrolida dipakai secara luas dalam industri peternakan. Sebagai contoh tilosin yaitu salah satu dari golongan makrolida yang lebih banyak dipasarkan karena mempunyai bahan aktif yang efektif dalam pencegahan dan pengobatan pada ayam termasuk meningkatkan produktivitasnya. (UNANDAR, 2000), begitu juga antibiotika golongan makrolida lain seperti
spiramisin. Maka upaya untuk mengetahui keberadaan residu antibiotika golongan makrolida ini, dicoba pengembangan metoda analisis residu golongan makrolida dalam produk ternak (daging ayam potong), kemudian disusul analisis residu pada daging ayam potong yang berasal dari lapangan, untuk mengetahui tingkat residunya.
MATERI DAN METODE
Penelitian dibagi dalam 2 tahap, yaitu:
Tahap 1: pengembangan metode deteksi residu spiramisin dalam daging ayam secara High Pressure Liquid Chromatography (HPLC) atau Khromatografi Cair Kinerja Tinggi (KCKT).
Tahap 2: penelitian lapang, yaitu menentukan kandungan residu spiramisin dalam daging ayam. Ayam berasal dari peternakan ayam broiler di Kabupaten Sukabumi, Kabupaten Tangerang dan Kabupaten Bogor dan ayam dari pasar tradisional di Kota Bogor.
Pengembangan metode deteksi residu spiramisin Pada prinsipnya analisis residu dibagi dalam 2 tahap, yaitu tahap ekstraksi tahap identifikasi
kuantifikasi dari hasil ekstraksi dengan mempergunakan alat KCKT. Metoda ekstraksi yang dikembangkan adalah metoda dari GAUGAIN et al. (1999), yaitu: ke dalam 5 gram sampel daging ayam ditambahkan 25 ml asetonitril dihomogenkan dengan alat homogeniser dan kocok selama 10 menit dengan alat vortex. Kemudian pisahkan larutan asetonitril dan tambahkan 10 ml isooktan dan kocok perlahan-lahan kemudian disentrifus. Hasil sentrifuse ada 2 lapisan: lapisan atas (isooktan) dibuang dan lapisan bawah (asetonitril) diambil 8 ml. Setelah itu lakukan pemurnian (clean up) dari lapisan bawah (8ml) tersebut dengan melalui cartridge (Sep-Pak C18) yang telah dikondisikan dengan 10 ml metanol disusul dengan 10 ml aquabides. Kemudian kolom Sep-Pak dielusi dengan 1,5 ml larutan 0,1 M metanol ammonium (7,708 g ammonium asetat dalam 1 L methanol) diikuti 1,5 ml larutan dipotasium hidrogen phosphate buffer (34,84 g dipotassium hidrogen fosfat dalam 1L aquabides). Hasil elusi dievaporasi dan siap disuntikan pada alat KCKT. Perhitungan konsentrasi pada khromatogram didasarkan pada luas area yang terbaca pada recorder.
Sistem KCKT
Ekstrak yang telah siap dilarutkan dahulu dalam larutan fase gerak sebelum disuntikan pada alat KCKT dengan mempergunakan kolom phase terbalik C-18 dan fase gerak campuran larutan NaH2PO4 0,01M: CH3CN= 77:23 pada p.H 2,5, kecepatan alir: 1,5 ml/menit panjang gelombang 232 nm dengan U.V detektor.
Validasi
Metode kemudian divalidasi yang meliputi:
- uji kesesuaian system - kalibrasi dan linearitas - limit deteksi
- uji perolehan kembali
Menentukan kandungan residu spiramisin dalam daging ayam
Sampel daging ayam yang dianalisis diperoleh dari peternakan ayam broiler di Kabupaten Sukabumi, Kabupaten Tangerang dan Kabupaten Bogor. Juga diambil sampel dari pasar tradisional di Bogor.
HASIL DAN PEMBAHASAN
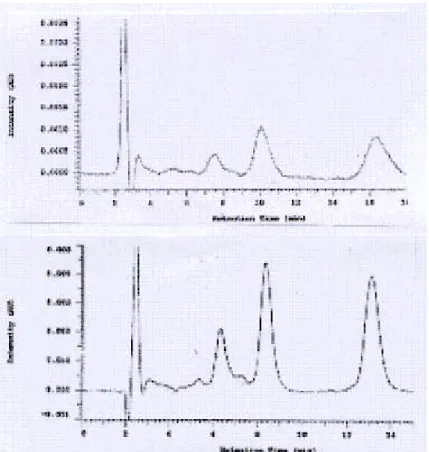
Spiramisin yang dipergunakan merupakan campuran Spiramisin I, II dan III, pada sistem KCKT terdeteksi pada menit 6.35 untuk Spiramisisn I, menit ke 8.41 untuk Spiramisin II dan menit ke 13.11 untuk Spiramisin III (Gambar 1.). Uji kesesuaian system dilakukan untuk mengetahui apakah alat, metode dan system KCKT yang digunakan dapat memberikan hasil yang baik. Uji dilakukan dengan cara melakukan penyuntikan ulang larutan standar paling sedikit 5 kali. Sistem KCKT dikatakan baik apabila simpangan baku < 2%. Dari uji kesesuaian system diperoleh nilai simpangan baku relatif berturut-turut 0,5463%, 0,3359% dan 0,4934% untuk Spiramisin I, Spiramisin II dan Spiramisin III (Tabel 1). Nilai ini memenuhi persyaratan F I IV dan USP XXV, yang menyatakan bahwa simpangan baku relatif harus < 2%. Dengan demikian dapat dikatakan bahwa system KCKT dapat dipergunakan.
Kalibrasi standar dilakukan dengan penyuntikan larutan standar dengan dosis bertingkat pada KCK, mulai dari konsentrasi 0,5 ppm hingga 10 ppm. Data yang diperoleh menunjukkan hubungan antara konsentrasi dan luas area di bawah peak sesuai dengan persamaan :
Y = 4395,8981 + 14056,2427 X, r = 0,9994
Sehingga dapat dikatakan adanya hubungan yang linear antara konsentrasi dan luas area di bawah peak.
Tabel 1: Uji kesesuaian system dari system KCKT untuk deteksi spiramisin
Luas area di bawah peak Injeksi pada KCKT ke
Spiramisin I Spiramisin II Spiramisin III
1 67238 148313 137005 2 67876 148600 136412 3 675632 147328 137328 4 67836 147293 137902 5 97031 148260 136250 Rata-rata 675026 148104 136979 Simpangan baku 368,7370 497,5364 675,8950
Gambar 1. Kromatogram spiramisin pada KCKT dengan mempergunakan kolom phase terbalik C-18 dan fase gerak campuran larutan NaH2PO4 0,01M : CH3CN= 77:23 , pH 2,5, dengan kecepatan aliran 1,5 ml/menit dan detector UV pada panjang gelombang 232 nm. Atas dan bawah adalah standar spiramisin dengan konsentrasi masing-masing 5 ppm dan 10 ppm
Uji batas deteksi dilakukan untuk mengetahui konsentrasi terendah dari standar yang dapat memberikan respon pada detector. Dari uji batas deteksi diperoleh bahwa konsentrasi 0,2 ppm dengan volume penyuntikan 20 ul, sehingga batas deteksi adalah 0,004 ug.
Uji perolehan kembali (recovery) dilakukan dengan menambahkan larutan standar pada contoh daging ayam, kemudian dilakukan pengujian sesuai dengan metoda yang telah dikembangkan, mulai dari ekstraksi hingga penyuntikan pada KCKT. Konsentrasi larutan standar yang ditambahkan adalah 0,5 ug/g dan 1,0 ug/g. Dengan dua kali ulangan, hasil perolehan kembali dapat dilihat pada Tabel 2.
Dengan perolehan kembali sebesar 96,29% dan 108,33% dapat dikatakan bahwa metoda cukup untuk digunakan menguji kandungan residu spiramisin dari daging ayam.
Kandungan residu spiramisin dalam daging ayam Sampel daging ayam yang diperoleh adalah 36 sampel yaitu 26 sampel diperoleh dari peternakan ayam dan 10 dari pasar tradisional. Sampel dari peternakan adalah 9 sampel dari Kabupaten Sukabumi, 9 sampel dari Kabupaten Tangerang, 8 sampel dari Kabupaten Bogor dan 10 sampel dari pasar tradisional yang ada di Bogor.
Hasil pemeriksaan residu spiramisin dalam sampel daging ayam dapat dilihat pada Tabel 3.
Berdasarkan hasil pemeriksaan residu spiramisisn ternyata menunjukkan bahwa 35 dari 36 sampel adalah positif mengandung spiramisin (97%) dan 1 sampel negatif (3%) Sedangkan 5 sampel mengandung spiramisin sudah melewati maksimum residu limit (MRL) yang diperbolehkan, yaitu kode B2 dan B6 (sampel dari Bogor), kode T6 (sampel dari Tangerang)
Tabel 2 : Hasil uji perolehan kembali spiramisin Ulangan Penambahan spiramisin (ug/g) Perolehan kembali (ug/g) Perolehan kembali (%) Rata-rata perolehan kembali (%) 1 0,50 0,553 110,68 96,29 2 0,50 0,445 81,91 1 1,00 1,244 124,24 108,33 2 1,00 0,922 92,20
Tabel 3. Kandungan spiramisin dalam sampel daging ayam yang berasal dari Kab. Sukabumi, Kab. Tangerang dan Kab. Bogor
dan pasar tradisional di Bogor
No. Kode sampel Kandungan spiramisin (ppm)
No. Kode sampel Kandungan spiramisin (ppm) Bogor Sukabumi 1 B1 0,0784 1 S1 0,1364 2 B2 0,5748 2 S2 0,1805 3 B3 0,0318 3 S3 0,0652 4 B4 0,0267 4 S4 0,0812 5 B5 0,0458 5 S5 0,1085 6 B6 0,6098 6 S6 0,0310 7 B7 Tt 7 S7 0,0893 8 B8 0,0349 8 S8 0,0304 9 S9 0,0175
Tangerang Pasar tradisional
1 T1 0,1389 1 PsB1 0,2014 2 T2 0,0923 2 PsB2 0,0694 3 T3 0,1078 3 PsB3 0,1414 4 T4 0,0822 4 PsB4 0,1168 5 T5 0,0565 5 PsB5 0,1414 6 T6 0,2670 6 PsB6 0,1280 7 T7 0,0893 7 PsB7 0,2286 8 T8 0,0625 8 PsB8 0,760 9 T9 0,1552 9 PsB9 0,0280 10 PsB10 0.0305
dan kode PsB1 dan PsB7 (sampel Pasar tradisional Bogor). Sesuai menurut EC Commission Decision 93/256/EEC menyatakan bahwa MRL untuk spiramisin dalam daging adalah 0,2 ug/g. Sedangkan menurut Standar Nasional Indonesia menyatakan bahwa MRL untuk spiramisin dalam daging adalah 0,1 ug/g. Kemungkinan adanya residu ini karena penambahan antbiotika kedalam pakan dan waktu henti (withdrawal time) dari jenis antibiotika tersebut belum selesai.
Hasil pemeriksaan spiramisin terhadap sampel lapang dan sampel pasar tradisional menunjukkan tidak jauh berbeda, hanya 2 sampel yang jauh di atas MRL (0,6098ug/g dan 0,5748 ug/g), yaitu sampel berasal dari peternakan di Bogor.
KESIMPULAN
Berdasarkan pengamatan hasil pemeriksaan dengan pengembangan (modifikasi) metoda residu antibiotika spiramisin terhadap keseluruhan sampel lapang, dapat diambil kesimpulan bahwa:
1. Rata-rata “recovery” dari modifikasi metoda tersebut masuk nilai kisaran uji validasi sehingga analisis residu spiramisin cukup baik.
2. 35 dari 36 sampel daging ayam mengandung positif spiramisin dan 5 sampel sudah melewati nilai BMR Sebagai saran sebaiknya tetap harus diperhatikan waktu pengobatan dan umur panen, sehingga waktu henti dari jenis antibiotika tersebut terkontrol sehingga
DAFTAR PUSTAKA
CHAN, W., G.C. GERHARDT dan C.D.C. SALISBURY. 1994. Determination of Tylosin and Tilmicosin Residues in Animal Tissues by Reversed Phase Liquid Chromatography.J. AOAC 77(2)331-333.
DAMME, K 1999. Natural enhancers could replace antibiotics in turkey feed. World Poultry. 15: 27-28.
DELEPIN, B., D.H. PESSEL dan P. SANDERS. 1996. Multiresidue Method for Confirmation of Macrolide Abtibitics in Bovine Muscle by Liquid Chromatography/Mass Spectrometry. J.AOAC. 79 (2) 397-404.
GAUGAIN, M.J. dan ANGER, B. 1999. Multiresidue Chromatographic Method for the Determination of Macrolide Residues in Muscle by High Performance Liquid Chromatography with UV Detection. J. AOAC. 82(5)1046-1053.
OKA, H, H. NAKAZAWA, K. HANADA dan J.D. MAC. NEIL. 1995. Chemical Analysis of Macrolide Antibiotics. Chemical Analysis for Agriculture. 165-205.
STANDAR NASIONAL INDONESIA. No. 01-6366-2000. Badan Standar Nasional Jakarta.
UNANDAR, T. 2000. Mengenal Aspek Ilmiah Tylosin. Infovet. Edisi 066. 35.