LAPORAN AKHIR PRAKTIKUM FARMASI FISIKA II LARUTAN
NAMA : Siti Sofiatul Jannah
NPM : 260110140116
HARI,TANGGAL PRAKTIKUM : Kamis, 26 MARET 2015
ASISTEN : 1. Novia Eka Putri
2. Rimba T
LABORATORIUM FARMASI FISIKA FAKULTAS FARMASI
UNIVERSITAS PADJADJARAN JATINANGOR
Abstrak
Tujuan dari percobaan ini adalah untuk mengetahui bagaimana hubungan antara presentase pelarut campur dengan konsentrasinya dan bagaimana penambahan zat pelarut dapat menaikkan kelarutan suatu zat. Larutan merupakan campuran dua zat atau lebih yang bersifat homogen dan sulit dipisahkan dengan proses kimia fisika biasa. Kelarutan merupakan kemampuan zat terlarut untuk dapat terlarut dalam pelarutnya. Sampel berupa asam salisilat dan asam benzoate yang mempunyai kelarutan yang rendah dalam pelarut air, sampel dilarutkan hingga jenuh dalam perbandingan presentase pelarut campur etanol dan air atau ditambahkan surfaktan, lalu dititrasi untuk diambil konsentrasinya dan dibuat grafik hubungan konsentrasi dan kelarutannya. Dari percobaan ini didapat bahwa kelarutan umumnya dapat meningkat seiring dengan penambahan pelarut campur yang sesuai dan penambahan zat lain seperti surfaktan.
Abstract
The purpose of this experiment is to know how the connection between the percentage of mixing solvent and the concentration of its solute, and to know how the adding process of other compounds can level up dissolution of substrates. Solute is a mix of two or more compounds which is homogeny and hard to be distracted by general physical process. Dissolution is the power of solute to be solved in its solvent. The samples are salicylic acid and benzoate acid which both have low dissolution trough water. Samples were solved until saturated in the percentage of mixing solvent ethanol and aquadest or be added by surfactant. Then, they were titrated to take its concentration and make the graphic. From this experiment, it can be concluded that generally, dissolution can be up straight trough the adding of right mixing solvent and the adding of other compunds such as surfactant.
I. Tujuan Percobaan
a. Membuat larutan natrium hidroksida (NaOH) yang dibakukan dengan larutan asam oksalat (H2C2O4) dengan indicator fenolftalein
b. Membuat pelarut campur dari air, etanol, gliserin dan propilenglikol
c. Menentukan kelarutan asam benzoate dan asam salisilat dari berbagai pelart campur
d. Membuat grafik hubungan konsentrasi dengan presentase pelarut campur
II. Prinsip Percobaan 1. Azas Le chatelier
Bila pada suatu system kesetimbangan diadakan aksi, maka system akan mengadakan reaksi sedemikian rupa sehingga pengaruh aksi itu menjadi sekecil-kecilnya (Ratna, 2009).
2. Kelarutan
Kelarutan digunakan untuk menyatakan jumlah maksimal suatu zat yang dapat larut dalam sejumlah tertentu larutan (Suyatno, 2006).
3. Titrasi Asam Basa
Titrasi merupakan salah satu metode untuk menentukan konsentrasi suatu larutan dengan cara mereaksikan seumlah volume larutan tersebut terhadap sejumlah volume larutan lain yang konsentrasinya sudah diketahui. Titrasi yang melibatkan reaksi asam basa diebut titrasi asam basa (Muchtaridi, 2009).
4. Like Dissolve Like
Suatu senyawa akan larut dalam senyawa yang mempunyai struktur kimia yang sama, polar dengan polar dan nonpolar dengan nonpolar (Arsyad, 2001).
5. Reaksi Netralisasi
Reaksi yang terjadi dengan pembentukan garam dan H2O netral (pH = 7,0), hasil reaksi antara H+ dari suatu asam dan OH- dari suatu basa (Sumardjo, 2006).
6. Pengenceran
Prosedur untuk penyiapan larutan yang kurang pekat dari larutan yang lebih pekat disebut pengenceran. Dalam melakukan pengenceran, perlu diingat bahwa penambahan lebih banyak pelarut ke dalam sejumlah tertentu larutan akan mengubah konsentrasi larutan tanpa mengubah jumlah mol zat terlarut yang terdapat dalam larutan (Chang, 2005).
7. Stoikiometri
Stoikiometri adalah penentuan perbandigan masa unsur-unsur pada senyawa dalam pembentukan senyawanya (Alfian, 2009).
III. Reaksi
(Harjadi, 1986)
IV. Teori Dasar
A. Larutan dan Kelarutan
Campuran homogen antara dua zat atau lebih dikenal sebagai larutan. Suatu campuran dikatakan homogen karena susunannya seragam sehingga tidak teramati adanya bagian-bagian yang berlalinan, bahkan dengan mikroskop optik.
Larutan (solution) terdiri atas zat pelarut (solvent) dan satu atau lebih zat terlarut (solute). Pelarut adalah medium tempat suatu zat lain melarut. Pelarut dikenal
sebagai zat pendispersi, yaitu tempat menyebarnya partikel-partikel zat terlarut. Zat terlarut adalah zat yang terdispersi di dalam pelarut. Perbedaan antara pelarut dan zat terlarut sebenarnya relatif. Suatu zat pada saat tertentu dapat berupa zat terlarut dan pada saat yang lain berupa zat pelarut. Larutan jenuh adalah larutan yang mengandung cukup banyak zat terlarut dengan jumlah maksimum. Pada larutan jenuh terdapat kesetimbangan antara partikel yang melarut dan partikel yang tidak melarut. Larutan yang mengandung zat terlarut dengan jumlah yang lebih sedikit dibandingkan dengan kemampuan pelarutnya disebut larutan tidak jenuh, sedangkan larutan yang mengandung zat terlarut lebih banyak dari kemampuan pelarutnya disebut larutan lewat jenuh (Sumarrdjo, 2009).
Kelarutan adalah kuantitas maksimal suatu zat kimia terlarut (solut) untuk dapat larut pada pelarut tertentu membentuk larutan homogen. Kelarutan suatu zat dasarnya sangat bergantung pada sifat fisika dan kimia solute dan pelarut pada suhu, tekanan, dan pH larutan. Secara luas kelarutan suatu zat pada pelarut tertentu merupakan suatu pengukuran konsentrasi kejenuhan dengan cara menambahkan sedikit demi sedikit solute pada pelarut sampai solute tersebut mengendap (tidak dapat larut lagi). Pengertian kelarutan sebaiknya tidak dikacaukan dengan kemampuan melarutkan atau mencairkan suatu zat, karena larutan dapat dibuat dengan mereaksikan suatu zat. Kelarutan tidak bergantung pada ukuran partikel atau factor kinetic lainnya, maupun waktu pelarutan (Nidaurrohmah dan Aliyah, 2013). B. Faktor-faktor yang Mempengaruhi Kelarutan
Kelarutan ini juga dipengaruhi dengan jenis pelarut dan jenis zat terlarut yang berdasarkan prinsip like dissolve like suatu campuran atau larutan yang memiliki sruktur kimia yang sama akan meningkatkan kelarutannya oleh karena itu jenis pelarut dan zat terlarut mempengaruhi tingkat kelarutan suatu zat. Kelarutan obat sebagian besar disebabkan oleh polaritas dari pelarut, yaitu oleh dipol momennya. Pelarut polar melarutkan zat terlarut ionik dan zat polar lain. Sesuai dengan itu, air
bercampur dengan alkohol dalam segala perbandingan dan melarutkan gula dan senyawa polihidroksi yang lain. Sedangkan pelarut non polar tidak dapat mengurangi gaya tarik-menarik antara ion-ion elektrolit kuat dan lemah,karena tetapan dielektrik pelarut yang rendah. Pelarut juga tidak dapat memecahkan ikatan kovalen dan elektrolit yang berionisasi lemah karena oelarut non polar termasuk dalam golongan pelarut aprotik. Dan bagian yang lain adalah pelarut semipolar, pelarut semipolar seperti keton dan alkohol dapat menginduksi suatu derajat polaritas tertentu dalam molekul pelarut non polar sehingga menjadi dapat larut dalam alkohol contohnya benzena yang mudah dapat dipolarisasikan. Kenyataannya senyawa semipolar dapat bertindak sebagai pelarut perantara yang dapat menyebabkan bercampurnya cairan polar dan nonpolar.(martin,2009)
Pada pengujian kelarutan terkadang dibutuhkan penambahan zat lain sebagai pembandingan, salah satu zat yang dijadikan pembanding yaitu kosolvent. Kosolven adalah suatu jenis pelarut yang dapat meningkatkan suatu kelarutan zat atau obat dalam sediaan cair,semi padat,dan sediaan transdermal. Contoh dari kosolvent adalah gliserin dan propilenglikol dengan penambahan zat ini maka kelarutan dari suatu zat akan meningkat. (widyaningsih,2009)
Faktor-faktor yang mempengaruhi kelarutan yaitu : 1. suhu
suhu mempengaruhi kelarutan suatu zat. Bayangkan dalam gedung bioskop yang banyak penonton sedang asyik menonton film dan tiba-tiba gedung tersbut terbakar,pasti keadaan tenang pasti akan saling berdesakkan dan menyebar. Demikian pula pada suhu tinggi partikel-partikel akan bergerak lebih cepat dibandingkan pada suhu rendah. Akibatnya kontak antara zat terlarut dengan pelarut menjadi lebih sering dan efektif. Hal ini menyebabkan zat terlarut menjadi lebih mudah larut pada suhu tinggi (azizah,2010)
2. pengadukan
3. semakin banyak jumlah yang pengadukan maka zat terlarut menjadi lebih mudah larut
4. luas permukaan sentuh zat
luas permukaan sentuh zat dapat diperbesar melalui proses pengadukan penggerusan secara mekanis
(azizah,2010) Bila ada 2 atau lebih zat yang tidak bereaksi dicampur maka campuran yang terjadi ada 3 kemungkinan, yaitu :
1. campuran kasar : campuran tanah dan pasir.gula dan garam,dsb 2. dispersi koloid : larutan tanah liat dan air , Fe(OH)3
3. larutan sejati : larutan gula dalam air,garam dalam air dan sebagainya tipe larutan dapat digunakan sesuai dengan keadaan terjadinya zat terlarut dan pelarut dan karena aada 3 wujud zat maka ada 9 kemungkinan sifat campuran homogen antara zat terlarut dan pelarut (Martin,1990)
V. Alat dan Bahan
a. Alat dan Gambar Alat
1. buret 2. Gelas kimia 3. Gelas ukur 4. Kertas saring
b. Bahan Percobaan 1. Air 2. Asam benzoate 3. Asam oksalat 4. Asam salisilat 5. Ethanol 6. Fenolftalein 7. Gliserin 8. NaOH 9. Propilenglikol VI. Prosedur
Pertama dilakukan terlebih dahulu pembakuan NaOH 0,1 N menggunakan larutan baku berupa asam oksalat 0,1 N dengan indicator PP. Setelah dilakukan pembakuan dibuat pelarut campur yang terdiri dari etanol,air,gliserin,dan propilenglikol dengan perbandingan yang berbeda-beda. Pelarut campur yang telah dibuat tadi dimasukkan serbuk asam salisilat dan asam benzoate diaduk lalu disaring, bagian filtratnya dibagi 2
menjadi 10 ml 10 ml lalu ditetesi PP dan dilakukan titrasi secara duplo. Lalu dihitung volume NaOH yang dibutuhkan sampai titrasi mencapai titik akhir lalu volume NaOH tersebut di masukkan kedalam perhitungan kelarutan dan didapatkan kelarutan dari asam salisilat dan benzoate.
VII. Data Pengamatan
a. Tabel Pembakuan NaOH
Perlakuan Hasil Gambar
Asam oksalat 0.1 N yang telah ditetesi PP dititrasi dengan NaOH secara triplo
Didapat konsentrasi NaOH 0.0983 N
Volume asam oksalat Volume NaOH
10 ml 10.3 ml 10 ml 10.5 ml 10 ml 9.8 ml Rata-rata = 10 ml 10.1667 ml
Perlakuan Hasil Gambar Timbang zat asam
benzoat dan asam salisilat
Didapat asam benzoat dan salisilat untuk dibuat larutan jenuh dalam pelarut campur Campurkan sampel
pelarut campur yang terdiri dari etanol,air, gliserin, dan
propilenglikol dengan rasio yang telah ditentukan, kemudian larutan dijenuhkan
Pelarut campur dengan sampel asam benzoat dan asam salisilat
Tabel 2 : perhitungan pearut campuran Bahan Uji No Pelarut
Kosolven
Pelarut Kosolven
Etanol Air Gliserin Propilenglikol Asam Salisilat dan Asam Benzoat 1. - 30 mL - - 2. - 28,5 mL - - 3. 1,5 mL 27 mL 3 mL - 4. - 27 mL - 3 mL
Bahan Uji No Pelarut Kosolven
Pelarut Kosolven
Etanol Air Gliserin Propilenglikol Asam
Salisilat
1. 3 mL 27 mL - -
dan Asam Benzoat
3. 3 mL 24 mL 3 mL -
4. 3 mL 24 mL - 3 mL
Bahan Uji No Pelarut Kosolven
Pelarut Kosolven
Etanol Air Gliserin Propilenglikol Asam Salisilat dan Asam Benzoat 1. 6 mL 24 mL - - 2. 7,5 mL 22,5 mL - - 3. 6 mL 21 mL 3 mL - 4. 6 mL 21 mL - 3 mL
Bahan Uji No Pelarut Kosolven
Pelarut Kosolven
Etanol Air Gliserin Propilenglikol Asam Salisilat dan Asam Benzoat 1. 9 mL 21 mL - - 2. 10,5 mL 19,5 mL - - 3. 9 mL 18 mL 3 mL - 4. 9 mL 18 mL - 3 mL c. Perhitungan kelarutan
Perlakuan Hasil Gambar
10 ml larutan dipipet untuk dilakukan titrasi diplo pada setiap pelarut campur, dan ditambahkan PP
10 ml zat dalam pelarut campur dalam erlenmeyer
Zat dalam perlarut campur dititrasi dengan NaOH untuk mengetahui kelarutan zat dalam pelarut campur
Didapatkan warna rosa pada larutan zat yang menunjukkan titik ekuivalen dan kelarutannya dapat dihitung Kelompok 1 Pelarut Campur Volume Larutan Asam Benzoat(Duplo) Volume
NaOH Kelarutan (gram/mL)
1. 10 mL 0,5 mL 0,6 2. 10 mL 0,075 mL 0,09 3. 10 mL 0,15 mL 0,18 4. 10 mL 1,5 mL 1,8 Kelarutan Rata-Rata 0,6675 Pelarut Campur Volume Larutan Asam Salisilat (Duplo) Volume
NaOH Kelarutan (gram/mL)
1. 10 mL 0,3 mL 0,4 2. 10 mL 0,05 mL 0,679 3. 10 mL 0,15 mL 0,204 4. 10 mL 0,25 mL 0,339 Kelarutan Rata-Rata 0,4055 Kelompok 2
Pelarut Campur Volume Larutan Asam Benzoat(Duplo) Volume
NaOH Kelarutan (gram/mL)
1. 10 mL 0,5 mL 0,6 2. 10 mL 0,75 mL 0,9 3. 10 mL 1,15 mL 1,38 4. 10 mL 1,35 mL 1,62 Kelarutan Rata-Rata 1,125 Pelarut Campur Volume Larutan Asam Salisilat (Duplo) Volume
NaOH Kelarutan (gram/mL)
1. 10 mL 1,35 mL 1,83 2. 10 mL 1,6 mL 2,17 3. 10 mL 0,7 mL 0,95 4. 10 mL 1,25 mL 1,69 Kelarutan Rata-Rata 1,66 Kelompok 3 Pelarut Campur Volume Larutan Asam Benzoat(Duplo) Volume
NaOH Kelarutan (gram/mL)
1. 10 mL 0,3 mL 0,36
2. 10 mL 0,45 mL 0,54
3. 10 mL 3,3 mL 3,96
4. 10 mL 2 mL 2,4
Pelarut Campur Volume Larutan Asam Salisilat (Duplo) Volume
NaOH Kelarutan (gram/mL)
1. 10 mL 1,3 mL 1,7 2. 10 mL 0,45 mL 0,54 3. 10 mL 0,3 mL 0,4 4. 10 mL 2 mL 2,4 Kelarutan Rata-Rata 1,26 Kelompok 4 Pelarut Campur Volume Larutan Asam Benzoat(Duplo) Volume
NaOH Kelarutan (gram/mL)
1. 10 mL 4,55 mL 5,46 2. 10 mL 2,7 mL 3,24 3. 10 mL 3,5 mL 4,2 4. 10 mL 1,75 mL 2,1 Kelarutan Rata-Rata 3,75
Perhitungan Kelarutan Asam Benzoat
Kelarutan = (Volume NaOH x N NaOH) x BE As. Benzoat 10 L 1. Kelarutan = 4,55 mL x 0,0983 N x 122,12 10 mL = 5,46 gram/mL 2. Kelarutan = 2,7 mL x 0,0983 N x 122,12 10 mL = 3,24 gram/mL
3. Kelarutan = 3,5 mL x 0,0983 N x 122,12 10 mL = 4,2 gram/mL 4. Kelarutan = 1,75 mL x 0,0983 N x 122,12 10 mL = 2,1 gram/mL Pelarut Campur Volume Larutan Asam Salisilat (Duplo) Volume
NaOH Kelarutan (gram/mL)
1. 10 mL 5,75 mL 7,8
2. 10 mL 2,35 mL 3,2
3. 10 mL 5,05 mL 6,9
4. 10 mL 3,75 mL 5,1
Kelarutan Rata-Rata 5,75
Perhitungan kelarutan asam salisilat
Kelarutan = (Volume NaOH x N NaOH) x BE As. Salisilat 10 L 1. Kelarutan = 5,75 mL x 0,0983 N x 138,12 10 mL = 7,8 gram/mL 2. Kelarutan = 2,35 mL x 0,0983 N x 138,12 10 mL = 3,2 gram/mL 3. Kelarutan = 5,05 mL x 0,0983 N x 138,12 10 mL
= 6,9 gram/mL
4. Kelarutan = 3,75 mL x 0,0983 N x 138,12 10 mL
= 5,1 gram/mL
VIII. Pembahasan
Percobaan kali ini dilakukan untuk mengetahui bagaimana hubungan antara konsentrasi dengan presentase pelarut campurnya. Zat-zat yang digunakan untuk membuat pelarut campur dalam praktikum ini di antaranya, air, etanol, gliseirn, dan propilenglikol. Secara teoritis, Senyawa polar (mempunyai kutub muatan) akan mudah larut dalam senyawa polar. Misalnya gula, NaCl, alkohol, dan semua asam merupakan senyawa polar. Senyawa non polar akan mudah larut dalam senyawa non polar (Sudarmo, 2004). Pada farmakope Indonesia IV dijelaskan bahwa asam salisilat merupakan serbuk hablur putih, sukar larut dalam air dan dalam benzene, mudah larut dalam etanol dan eter, larut dalam air mendidih dan agak sukar larut (Depkes RI, 1995). Sedangkan untuk asam benzoat, Asam benzoate memiliki bentuk serbuk kristal padat, tidak berwarna, tidak berbau, sedikit terlarut didalam air, tetapi larut dalam etanol dan sangat mudah larut dalam benzena dan aseton (WHO, 2000).
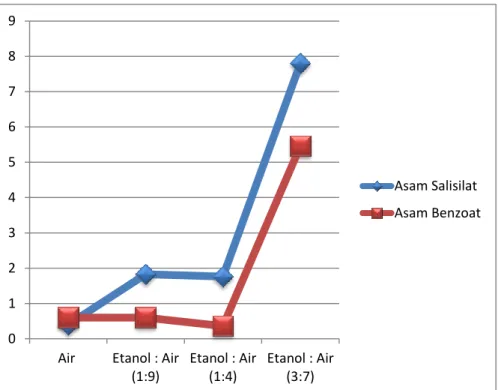
Grafik 1. Perbandingan Hubungan antara Kelarutan Asam Salisilat dan Asam Benzoat dengan Presentase Campuran Pelarut Etanol : Air
Dari grafik di atas, terlihat bahwa kelarutan baik asam salisilat dan asam benzoate naik dengan adanya pelarut campuran air dan etanol, lebih larut dalam pelarut tersebut dibandingkan pelarut air saja. Hal ini disebabkan karena struktur asam salisilat dan asam benzoat yang bersifat semipolar akan lebih larut dalam pelarut semipolar seperti etanol, hal ini sesuai dengan teori Like Dissolve Like.
Namun, penurunan kelarutan terjadi pada perbandingan pelarut etanol dan air (1 : 4) yang seharusnya tetap naik karena presntase etanolnya lebih banyak dari perbandingan yang pertama. Hal seperti ini dapat terjadi terlihat dari rentang yang jauh dari data ketiga menuju ke data empat yang menunjukan bahwa standar deviasinya cukup besar nilainya, standar deviasi dapat terjadi karena beberapa hal, di antaranya kesalahan dalam proses pelarutan, kesalahan titrasi dan kesalahan teknis seperti alat yang tidak disiapkan dengan baik.
Grafik 2. Perbandingan Hubungan antara Kelarutan Asam Salisilat dan Asam Benzoat dengan Presentase Campuran Pelarut Etanol : Air
0 1 2 3 4 5 6 7 8 9
Air Etanol : Air (1:9) Etanol : Air (1:4) Etanol : Air (3:7) Asam Salisilat Asam Benzoat
Pada data kedua, perbandingan pelarut antara etanol dan air lebih diperbesar, namun terlihat bahwa kedua data sampel sama-sama mengalami kenaikan kelarutan kecuali pada perbandingan 1:3, meskipun kenaikannya lebih sedikit daripada perbandingan yang pertama. Dari grafik 1 dan 2, dapat disimpulkan bahwa pada perbandingan pelarut etanol dan air tertentu, kelarutan zat asam salisilat dan asam benzoate turun jika presentase air lebih besar atau mempunyai perbandingan yang terlalu berdekatan dengan presentase etanolnya, meskipun campuran tersebut tetap dapat menaikkan kelarutan daripada pelarut air saja.
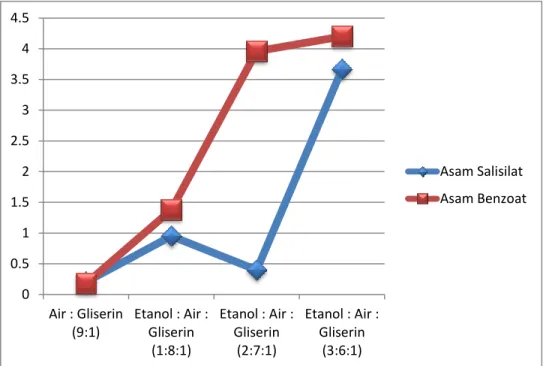
Grafik 3. Perbandingan Hubungan antara Kelarutan Asam Salisilat dan Asam Benzoat dengan Presentase Campuran Pelarut
Etanol : Air : Gliserin 0 0.5 1 1.5 2 2.5 3 3.5 Etanol : Air (1:19) Etanol : Air (3:17) Etanol : Air (1:3) Etanol : Air (3:7) Asam Salisilat Asam Benzoat
Pada perlakuan ketiga, data ditunjukkan oleh grafik 3 di atas. Presentase pelarut yang digunakan tetap etanol dan air, namun dengan ada penambahan gliserin di dalamnya. Terlihat dari data di atas, kelarutan zat meningkat cukup tinggi dengan penambahan gliserin ke dalam pelarut. Hal ini sesuai dengan fungsi gliserin sebagai kosolven ataupun surfaktan yang dapat menaikkan kelarutan. Namun, terdapat perbedaan data pada perbandingan ketiga, dimana asam benzoate tetap naik kelarutannya dan asam salisilat turun, perbedaan data ini bisa dipastikan terjadi karena kesalahan-kesalahan dalam percobaan seperti kesalahan dalam prosedur, kesalahan titrasi, ataupun saat kalibrasi alat yang baik.
Grafik 4. Perbandingan Hubungan antara Kelarutan Asam Salisilat dan Asam Benzoat dengan Presentase Campuran Pelarut
Etanol : Air : Propilenglikol 0 0.5 1 1.5 2 2.5 3 3.5 4 4.5 Air : Gliserin (9:1) Etanol : Air : Gliserin (1:8:1) Etanol : Air : Gliserin (2:7:1) Etanol : Air : Gliserin (3:6:1) Asam Salisilat Asam Benzoat
Kesulitan pengamatan data terjadi pada data keempat ini. Pada perlakuan ini, zat sampel dilarutkan ke dalam pelarut dengan perbandingan yang hamper sama namun dengan penambahan propilenglikol. Propilenglikol ini berfungsi sama halnya dengan gliserin, yaitu sebagai kosolven atau sebagai surfaktan untuk meningkatkan kelarutan. Fluktuasi yang terjadi dari hasil data di atas terjadi karena kesalahan pada saat melakukan prosedur seperti pelarutan yang tidak sampai jenuh, kurang ketelitian angka dalam membuat presentase pelarut, dan kesalahan teknis seperti alat-alat ang disiapkan dengan kurang baik. Namun pada dasarnya, propilenglikol, etanol dan air bersifat dapat menaikkan kelarutan zat.
0 1 2 3 4 5 6 Air : Propilenglikol (9:1) Etanol : Air : Propilenglikol (1:8:1) Etanol : Air : Propilenglikol (2:7:1) Etanol : Air : Propilenglikol (3:6:1) Asam Salisilat Asam Benzoat
IX. Kesimpulan
1. Larutan NaOH dapat dibuat dengan melarutkan padatan NaOH dalam aquades bebas CO2 yang kemudian dibakukan oleh asam oksalat dengan proses titrasi.
2. Pelarut campuran dapat dibuat jika masing-masing pelarut dapat tercampur dengan rata dan satu fase (homogen) sepert air, etanol, gliserin, dan propilenglikol.
3. Pelarut campuran pada umumnya dapat menaikkan kelarutan zat jika pelarut yang ditambahkan mempunyai struktur atau sifat yang sama dengan zat, dan juga dengan penambahan kosolven atau surfaktan.
DAFTAR PUSTAKA
Alfian,Zul.2009.Kimia Dasar.Medan:USU Press
Arsyad,N.2001.Kamus Kimia Anti dan Penjelasan Istilah.Jakarta:Gramedia
Azizah,Utiya.2010.faktor-faktor yang mempengaruhi kelarutan.Available online at www.chem-is-try.org/materi-kimia/kimia_dasar/asam_dan_basa/faktor-faktor-yang-mempengaruhi-kelarutan (diakses pada 29 Mret 2015)
Chang,Raymond.2005.Kimia Dasar.Jakarta:Erlangga
Martin,A.1990. Dasar-dasar Kimia Fisik dan Ilmu Farmasetika.Jakarta:UI Press
Martin,alfred.2009.farmasi fisik I.jakarta:UI Press
Muchtaridi.2007.Kimia 2.Jakarta:Yudhistira
Nidaurrohmah, N. dan Aliyah. 2013. Kelarutan. Available at
http://www.ilmukimia.org/2013/04/kelarutan.html [diakses 01 April 2015] Ratna.2009.Azas Le Chatelier. Available at
http://www.chem-is-try.org/materi_kimia/kimia-smk/kelas_x/azas-le-chatelier/. [Diakses pada tanggal 15 Maret 2015]
Sumardjo.2006.Pengantar Kimia.Jakarta:EGC
Suyatno.2006.Kimia.Jakarta:Grasindo