PREDIKSI TOKSISITAS SENYAWA PHOTOSENSITIZER TURUNAN CHLORIN DAN BACTERIOCHLORIN MENGGUNAKAN TOXTREE®
Dadan Suryasaputra1*
1Program Studi Farmasi, Fakultas Farmasi, Universitas Jenderal Achmad Yani, Cimahi *Corresponding author email: danfm97@gmail.com
ABSTRAK
Photosensitizer merupakan suatu kelompok senyawa yang digunakan dalam photodynamic therapy (PDT) untuk pengobatan kanker dan beberapa kondisi non-kanker. PDT didasarkan pada fotoaktivasi senyawa photosensitizer yang terakumulasi pada sel/jaringan target oleh cahaya pada panjang gelombang tertentu. Pengujian toksisitas diperlukan karena photosensitizer merupakan senyawa asing yang masuk ke dalam tubuh. Penelitian ini bertujuan untuk memprediksikan toksisitas senyawa photosensitizer sebelum fotoaktivasi. Prediksi toksisitas dilakukan terhadap 37 senyawa photosensitizer dari turunan chlorin dan bacteriochlorin menggunakan perangkat lunak Toxtree®. Hasil menunjukkan bahwa 20 senyawa dikategorikan
ke dalam kelas 9 (negative for nongenotoxic carsinogenicity) berdasarkan pada Benigni-Bossa rulebase serta didukung data ISSMIC, dimana terdapat setidaknya satu peringatan positif untuk mutagenisitas secara in vivo. Dari hasil pengujian potensi mutagenisitas dan karsinogenisitas terdapat dua senyawa yang bersifat mutagenik-karsinogenik. Dari hasil pengujian Developmental Toxicity Potency (DTP) diketahui bahwa 14 senyawa diprediksikan tidak bersifat toksik bagi reproduksi atau perkembangan embrio/janin, dan 23 senyawa dikategorikan sebagai berpotensi toksik, Maximum Tolerated Dose (MTD) senyawa photosensitizer antara 2,320 - 236,681 mg/kg BB, dan Low Observed Adverse Effect Level (LOAEL) antara 0,032 - 4,137 mg/kg BB.
Kata kunci : photosensitizer, toksisitas, Toxtree. ABSTRACT
Photosensitizer is a group of compounds that is recently used in photodynamic therapy (PDT) for cancer treatment and non-cancerous conditions. PDT is based on the photoactivation of photosensitizer which is accumulated in the targeted cell /tissue by light at specific wavelength. Toxicity test for photosensitizer is necessary due to its xenobiotic character for human. This study was conducted to predict the toxicity of compounds which are going to be used for photosensitizers. Prediction of toxicity was performed on 37 compounds of chlorine and bacteriochlorine derivatives using Toxtree software. Result showed that 20 compounds were categorized as class 9 (negative for nongenotoxic carsinogenicity) based on the Benigni-Bossa rulebase and supported by ISSMIC data, which stated at least one positive alert for mutagenicity in vivo by the micronucleus assay in rodents. Mutagenicity-carcinogenicity test showed that two compounds were potentially mutagent-carcinogent; whereas Developmental Toxicity Potency predicted that 14 compounds were categorized toxic for reproductive system or fetus and 23 were considered not toxic. The maximum tolerable dose (MTD) of photosensitizer ranged between 2.320 - 236.681 mg/kg body weight (laserphyrin), while the Low Observed Adverse Effect Level (LOAEL) was 0,032 – 4,137 mg/kg body weight.
PENDAHULUAN
Photosensitizer merupakan suatu kelompok senyawa yang banyak dipergunakan dalam Photodynamic therapy (PDT). Photodynamic therapy (PDT) merupakan teknik pengobatan terkini kanker dan beberapa kondisi non-kanker yang didasarkan pada fotoaktivasi senyawa photosensitizer yang terakumulasi pada sel / jaringan target (Tjahjono, 2006). Banyak senyawa photosensitizer untuk PDT merupakan senyawa turunan tetrapirol makrosiklik, seperti porfirin, klorin, bakterioklorin, dan ftalosianin (Djalil dkk, 2012).
Aktivasi senyawa photosensitizer dengan cahaya pada panjang gelombang tertentu akan menghasilkan spesi oksigen reaktif (reactive oxygen species, ROS) yang dapat merusak membran sel, mitokondria, atau lisosom yang mengakibatkan kematian sel (Tjahjono, 2006). Tahapan tersebut memungkinkan untuk menghindari toksisitas yang terkait terapi menggunakan photosensitizer sebelum diaktivasi. Akan tetapi pengujian toksisitas tetap diperlukan karena photosensitizer merupakan senyawa asing (xenobiotik) yang masuk ke dalam tubuh (Djalil dkk, 2012).
Profil dari photosensitizer yang ideal untuk digunakan dalam PDT harus memenuhi beberapa kriteria, yaitu (Sternberg dan David, 1998) :
a) mempunyai serapan radiasi elektromagnetik kuat di bagian merah dari
spektrum sinar tampak (> 650 nm)
b) menghasilkan energi triplet tinggi, dengan energi triplet lebih besar dari 94 kJmol-1
c) dapat menghasilkan kuantum oksigen singlet yang tinggi
d) memiliki toksisitas pra-aktivasi yang rendah
e) mempunyai selektivitas tinggi terhadap jaringan tumor vs jaringan sehat, terutama kulit
f) dapat diformulasi secara sederhana;
g) dapat disintesis dari bahan baku yang mudah tersedia, dan dengan mudah dapat diproduksi dalam skala besar.
Uji toksisitas secara eksperimental laboratorium membutuhkan tenaga, fasilitas,
waktu dan biaya mahal. Sebaliknya prediksi toksisitas dari model QSAR telah digunakan untuk mendukung hipotesis dan memprioritaskan studi eksperimental lebih lanjut (Djalil dkk, 2012). Dalam penelitan ini telah dilakukan prediksi toksisitas senyawa photosensitizer secara komputasi menggunakan perangkat lunak Toxtree dengan tujuan mengetahui toksisitas senyawa photosensitizer turunan klorin dan bakterioklorin pra-fotoaktivasi.
METODE
Perangkat lunak
Sistem Operasi : Windows® 7
Professional; Toxtree® 2.5.0, Chemsketch® 12.01.
Perangkat keras
ACPI x86 – based PC dengan platform Intel® Pentium® Core; Processor:
Dual-Core Processor T2080 - (1.83 GHz, 1MB L2 Cache, 533 MHz FSB); Memory : 2GB DDR2 667MHz RAM.
Prosedur :
Penelitian ini diawali dengan studi pendahuluan untuk menentukan senyawa photosensitizer yang akan diprediksikan toksisitasnya. Selanjutnya senyawa–senyawa tersebut digambarkan struktur 2D molekulnya menggunakan Chemsketch® 12.01 dan
dibuatkan notasi SMILES-nya. Senyawa yang diprediksikan toksisitasnya berasal dari penelitian sebelumnya (Ling, 1995, Frimayanti dkk, 2011, dan Djalil dkk, 2012)
Prediksi toksisitas in silico terhadap senyawa photosensitizer turunan klorin dan bakterioklorin dihitung menggunakan perangkat lunak Toxtree®. Senyawa uji (Tabel
2) diubah ke dalam notasi SMILES dan dijadikan sebagai masukkan data ke dalam perangkat lunak Toxtree.
Perangkat lunak Toxtree memprediksikan toksisitas berdasarkan penerapan decision tree untuk memperkirakan mutagenisitas dan karsinogenisitas didasarkan pada Benigni/Bossa rulebase, Structure Alerts untuk uji in vivo mikronukleus pada hewan pengerat (uji mutagenisitas secara in vivo pada tikus), toksisitas umum, toksisitas terhadap
perkembangan, serta mutagenisitas dan karsinogenisitas. Senyawa yang diprediksi dengan Toxtree dikelompokkan dalam kelas-kelas.
Penetapan kriteria pengujian toksisitas Kriteria pengujian toksisitas didasarkan pada protokol atau petunjuk pengujian yang dikeluarkan oleh ICH (Intenational Conference on Harmonisation) S9 : non-clinical evaluation for anticancer pharmaceutical, 2010, yang meliputi :
a. toksisitas umum mencakup MTD (Maximum Tolerated Dose), dan LOAEL (Low observed adverse effect level)
b. toksisitas terhadap reproduksi atau perkembangan janin (DTP = Developmental toxicity potency)
c. mutagenisitas d. karsinogenisitas
Tabel 1 Pembagian Kelas pada decision tree dengan metode Toxtree
Decison tree Kelas
Structure alerts untuk uji mikronukleus in vivo pada hewan pengerat
1
2
Setidaknya satu structural alert positif
untuk uji mikronukleus No alerts untuk uji mikronukleus Benigni/bossa rule base (untuk mutagenisitas dan karsinogenisitas) 1 2 3 4 5 6 7
Structure alerts untuk mutagenisitas dan karsinogenisitas
Structure alerts untuk non-genotoksik karsinogenisitas Potensial mutagen S. typhimurium TA100 berdasarkan QSAR Bukan mutagen S. typhimurium TA100 berdasarkan QSAR Potensial karsinogen berdasarkan QSAR Bukan karsinogen berdasarkan QSAR
Untuk penilaian lebih
8
9
10
baik, perhitungan QSAR dapat diterapkan Negatif genotoksik karsinogenisitas Negatif untuk nongenotoksik karsinogenisitas
Error ketika diterapkan decision tree
HASIL DAN PEMBAHASAN
Senyawa yang diprediksikan sebanyak 37 senyawa photosensitizer turunan klorin dan bakterioklorin (Tabel 2).
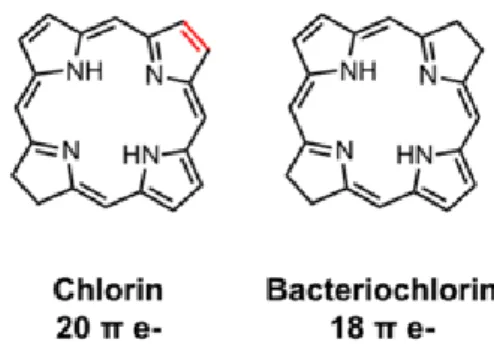
Gambar 1 : Struktur Chlorin dan Bacteriochlorin (Juse´lius, dkk, 2000)
Tabel 2 Senyawa photosensitizer yang diteliti Nama senyawa Nama senyawa hidroksi pheo a Pheo a metil ester G2 acid metil Klorofilon a Bphe a-OH rhodine g7
klorin e4 hirdroksi pheo b metil ester Bphe a metoksi G2 metil ester rhodoklorin metil Pheoforbid a purpurin 18 isoklorin e4
Pheoforbid B G2 aspartil deprotected piroPheoforbid a G2 aspartil protected Bakterioklorofil A Oktaetil purpurin purpurin 7 ftalosianin Klorin P6 G2 lisin deprotected klorin e6 Asp Klorin purpurin 18 metil ester purpurin lisin hidroksi pheo a metil ester Pha Asp
Pheo A G2 lisin protected NT1 purpurin Pha lys
G2 dimetil ester hidroksi pha lisin m-THPC
Hasil prediksi toksisitas
Prediksi toksisitas dilakukan untuk mengetahui potensi toksik suatu senyawa. PDT merupakan teknik pengobatan yang memerlukan kombinasi obat berupa senyawa photosensitizer dan cahaya untuk menghasilkan spesi oksigen reaktif yang akan menghancurkan sel kanker. Kedua bagian tersebut memungkinkan terhindarnya toksisitas sehubungan dengan obat yang digunakan, karena hanya photosensitizer yang telah diaktifkan cahaya yang sitotoksik.
Prediksi toksisitas umum yang mencakup MTD (Maximum Tolerated Dose), dan LOAEL (Low observed adverse effect level) dilakukan dengan perangkat lunak TOPKAT. Pengujian dilakukan terhadap seluruh senyawa yang terdapat pada Tabel 2. Pengujian untuk menentukan MTD dan LOAEL diperlukan untuk menentukan besarnya dosis yang dapat ditoleransi tanpa menimbulkan efek yang merugikan, yang akan diberikan selama uji pra-klinis dan uji klinis tahap I (ICH S9, 2010). Data prediksi MTD dan LOAEL ditampilkan pada Tabel 3.
Tabel 3. Low observed adverse effect level &
Maximum tolerate dose
Nama senyawa LOAEL
(mg/kg BB) MTD (mg/kg BB) hidroksi pheo a 0,032 12,855 G2 acid metil 0,055 33,649 Bphe a-OH 0,058 16,244 klorin e4 0,069 56,582 Bphe a 0,079 11,588 rhodoklorin 0,088 62,633 purpurin 18 0,093 23,194 Pheoforbid B 0,103 26,824 piroPheoforbid a 0,114 46,890 Bakterioklorofil A 0,119 2,320 purpurin 7 0,136 93,691 Klorin P6 0,138 89,662 klorin e6 0,144 84,461
purpurin 18 metil ester 0,158 5,140
hidroksi pheo a metil ester 0,163 6,608
Pheo A 0,185 9,509
NT1 purpurin 0,187 32,056
G2 dimetil ester 0,203 7,776
Pheo a metil ester 0,227 4,502
Klorofilon a 0,243 23,051
rhodine g7 0,250 96,347
hidroksi pheo b metil ester 0,289 7,379
metoksi G2 metil ester 0,290 5,649
metyl Pheoforbid a 0,308 8,502 isoklorin e4 0,383 79,401 G2 aspartil deprotected 0,405 69,037 G2 aspartil protected 0,497 10,988 Oktaetil purpurin 0,500 34,241 ftalosianin 0,587 52,836 G2 lisin deprotected 0,729 52,967 Asp Klorin 0,958 236,861 purpurin lisin 1,907 96,162 Pha Asp 2,430 104,999 G2 lisin protected 3,643 35,949 Pha lys 3,740 39,107
hidroksi pha lisin 3,809 51,560
m-THPC 4,137 99,931
Dari Tabel 3, dapat terlihat bahwa MTD terendah adalah 2,32 mg/kg BB untuk senyawa Bakterioklorofil A dan yang tertinggi 104,99 mg/kg BB untuk Pha asp.
LOAEL berkisar antara 0,032 – 4,137 mg/kg BB. Dosis LOAEL terendah ditunjukkan oleh hidroksi pheo a, sedangkan dosis LOAEL yang tertinggi ditunjukkan oleh m-THPC.
Selain prediksi toksikologi umum, TOPKAT dipergunakan juga untuk memprediksikan potensi toksisitas terhadap perkembangan (DTP). Hasil prediksi pengujian DTP dapat dilihat pada Tabel 4.
Tabel 4. Developmental Toxicity Potency (DTP) Nama senyawa DTP Prediction DTP Probability G2 aspartil deprotected Non-Toksik 0,453
ftalosianin Non-Toksik 0,464
Oktaetil purpurin Non-Toksik 0,470
NT1 purpurin Non-Toksik 0,471
Asp Klorin Non-Toksik 0,472
G2 aspartil protected Non-Toksik 0,473 Bakterioklorofil A Non-Toksik 0,481
Pha Asp Non-Toksik 0,482
Feoforbid B Non-Toksik 0,489
m-THPC Non-Toksik 0,489
hidroksi pheo a Non-Toksik 0,490
Bphe a Non-Toksik 0,492
purpurin lisin Non-Toksik 0,493
metil Feoforbid a Toksik 0,502
Pha lys Toksik 0,504
G2 lisin deprotected Toksik 0,508
G2 lisin protected Toksik 0,509
Bphe a-OH Toksik 0,509
klorin e4 Toksik 0,512
G2 acid metil Toksik 0,515
hidroksi pha lisin Toksik 0,517
purpurin 18 Toksik 0,521
rhodoklorin Toksik 0,522
pyroFeoforbid a Toksik 0,526
Pheo A Toksik 0,532
klorin e6 Toksik 0,534
metoksi G2 metil ester Toksik 0,534
rhodine g7 Toksik 0,535
purpurine 7 Toksik 0,535
isoklorin e4 Toksik 0,538
purpurin 18 metil ester Toksik 0,539
Klorin P6 Toksik 0,540
hidroksi pheo b metil ester
Toksik 0,546
Klorofilone a Toksik 0,546
G2 dimetil ester Toksik 0,549
Pheo a metil ester Toksik 0,553
hidroksi pheo a metil ester
Toksik 0,561
Dari Tabel 4 didapat bahwa 13 senyawa (35%) diprediksikan tidak bersifat toksik bagi reproduksi atau perkembangan embrio / janin, dan 24 (65%)
dikategorikan sebagai berpotensi toksik. Nilai probabilitas DTP antara 0,45 - 0,57 dimana nilai probabilitas > 0,495 diprediksikan sebagai toksik.
Gambar 2 : Distribusi Developmental toxicity potency
Prediksi mutagenisitas dan karsinogenisitas dilakukan dengan menggunakan perangkat lunak Toxtree dengan menerapkan suatu decision tree. Pembagian kelas pada masing-masing decision tree dipaparkan pada tabel 1. Hasil prediksi mutagenisitas dan karsinogenisitas dapat dilihat pada tabel 5.
Tabel 5. Prediksi mutagenisitas dan karsinogenisitas
(Toxtree-Benigni Bossa rule base & ISSMIC)
Nama senyawa Benigni/Bossa rulebase * (ISSMIC)** Klorofilon a 9 1 G2 acid metil 9 1 G2 dimetil ester 9 1 G2 lisin protected 9 1
hidroksi pha lisin 9 1
hidroksi pheo a 9 1
metoksi G2 metil ester 9 1
Pha Asp 9 1
Pha lys 9 1
purpurin 18 metil ester 9 1
purpurin 18 9 1 purpurin lisin 9 1 klorin e4 9 1 klorin e6 9 1 isoklorin e4 9 1 rhodoklorin 9 1 Klorin P6 9 1 purpurine 7 9 1 Bphe a 9 1 Bphe a-OH 9 1
G2 aspartil deprotected 1 & 9 1
G2 aspartil protected 1 & 9 1
hidroksi pheo a metil ester 1 & 9 1 hidroksi pheo b metil ester 1 & 9 1
Pheo a metil ester 1 & 9 1
Pheo A 1 & 9 1
pyroFeoforbid a 1 & 9 1
rhodine g7 1 & 9 1
aspartil klorin 1 & 9 1
Bakterioklorofil A 1 & 9 1
m-THPC 1 & 9 1
metil Feoforbid a 1 & 9 1
NT1 purpurin 1 & 9 1
Oktaetil purpurin 1 & 9 1
Feoforbid b 1 & 9 1
ftalosianin 1 & 9 1
* Benigni/Bossa rule base : 1 = alert for genotoxic carcinogenicity 9 = negative for nongenotoxic carsinogenicity ** alerts for micronucleus assay : 1 = setidaknya terdapat satu peringatan
positif untuk micronucleus assay
Dari prediksi dengan Benigni/Bossa rulebase, 20 senyawa dikategorikan masuk ke dalam kelas 9 (negative for nongenotoxic carsinogenicity), dan 17 senyawa termasuk kedalam kelas 1 & 9 (1: alert for genotoxic carcinogenicity), yang didukung pula dengan data dari ISSMIC dimana terdapat setidaknya satu peringatan positif untuk mutagenisitas secara in vivo.
Gambar 3 : Distribusi potensi mutagenisitas dan karsinogenisitas
Tabel 6 Prediksi Potensi Mutagenisitas & Karsinogenisitas Nama senyawa Mutagenisitas Karsinogenisitas Asp klorin Non-mutagen Non-Karsinogen Bakterioklorofil
a Non-mutagen Non-Karsinogen
Bphe a Non-mutagen Non-Karsinogen
Bphe a-OH Non-mutagen Non-Karsinogen Klorin e4 Non-mutagen Non-Karsinogen
Klorin e6 Non-mutagen Non-Karsinogen Klorin p6 Non-mutagen Non-Karsinogen Klorofilon a Non-mutagen Non-Karsinogen G2 acid metil Non-mutagen Non-Karsinogen G2 aspartil
deprotected Non-mutagen Non-Karsinogen
G2 aspartil
protected Non-mutagen Non-Karsinogen
G2 dimetil ester Non-mutagen Non-Karsinogen G2 lisin
deprotected Non-mutagen Non-Karsinogen
G2 lisin
protected Non-mutagen Non-Karsinogen
Hidroksi pha
lisin Non-mutagen Non-Karsinogen
Hidroksi pheo a Non-mutagen Non-Karsinogen Hidroksi pheo a
metil ester Non-mutagen Non-Karsinogen Hidroksi pheo b
metil ester Non-mutagen Non-Karsinogen Isoklorin e4 Non-mutagen Non-Karsinogen
m-THPC Mutagen Karsinogen
Metoksi g2 metil
ester Non-mutagen Non-Karsinogen
Metil Feoforbid
a Non-mutagen Non-Karsinogen NT1 purpurin Non-mutagen Non-Karsinogen Oktaetil
purpurin Non-mutagen Non-Karsinogen
Pha asp Non-mutagen Non-Karsinogen
Pha lys Non-mutagen Non-Karsinogen
Pheo a Non-mutagen Non-Karsinogen
Pheo a metil
ester Non-mutagen Non-Karsinogen
Feoforbid b Non-mutagen Non-Karsinogen
Ftalosianin Mutagen Karsinogen
Purpurin 18 Non-mutagen Non-Karsinogen Purpurin 18
metil ester Non-mutagen Non-Karsinogen Purpurin lisin Non-mutagen Non-Karsinogen Purpurine 7 Non-mutagen Non-Karsinogen PyroFeoforbid a Non-mutagen Non-Karsinogen Rhodine g7 Non-mutagen Non-Karsinogen Rhodoklorin Non-mutagen Non-Karsinogen
Dari Tabel 6 terlihat bahwa 35 senyawa dikategorikan sebagai mutagenik
non-karsinogenik dan dua senyawa dikategorikan mutagenik-karsinogenik, yaitu ftalosianin dan mTHPC.
KESIMPULAN
Dapat disimpulkan bahwa senyawa turunan klorin dan bakterioklorin diprediksi memiliki sifat toksik sehingga penggunaannya sebagai photosensitizer masih belum aman.
DAFTAR PUSTAKA
Allison, Ron R., Downie, G.H., Cuenca, R., Hu, Xin-Hua, Childs, C.J.H., dan Sibata, C.H. (2004) : Photosensitizer in Clinical PDT, Photodiagnosis and Photodynamic Therapy, 1, 27-42.
Benigni, R. (2005) : Structure-Activity Relationship Studies of Chemical Mutagens and Carcinogens: Mechanistic Investigations and Prediction Approaches, Chem. Rev., 105, 1767-1800.
Benigni, R., Bossa, C., dan Worth, A. (2010) : Structure Analysis and Predictive value of the Rodent in vivo Micronucleus Assay, Mutagenesis 25 (4), 335-341.
Benigni, R., Bossa, C., Jeliazkova, N., Netzeva, T., dan Worth, A. (2008) : The Benigni/Bossa Rulebase for Mutagenicity and Carcinogenicity – a Module of Toxtree, JRC Scientific and Technical Reports, EUR 23241 EN.
Calin, M.A dan Parasca, S.V., (2006) : Photodynamic therapy in Oncology, Journal of Optoelectronics and Advanced Materials, 8 (3), 1173-1179.
Dearden, John C., (2003) : In silico Prediction of Drug Toxicity, Journal of Computer-Aided Molecular Design, 17, 119-127.
Djalil, Asmiyenti D., Kartasasmita, R.E. Surantaatmaja, S.I., dan D.H.,Tjahjono, (2012) : Toxicity Prediction of Photosensitizer Bearing Carboxylic Acid Groups by ECOSAR and TOXTREE, Journal of Pharmacology and Toxicology
7 (5), 219-230.
Dourson, M.L. and Stara. J.F. (1983) : Regulatory Toxicology and Pharmacology.
3: 224-238.
Elsherbeny, E. dan Elfeky, S. (2004) : Basic Principles of Photosensitization, Biological & Medical Approaches.
Frimayanti, N., Li Y.M., Lee, H.B., Othman, R., Zain, S.M., dan Rahman, N.A. (2011) : Validation of Quantitative Structure-Activity Relationship (QSAR) Model for Photosensitizer Activity Prediction., Int. J. Mol. Sci., 12., 8626-8644; doi:10.3390/ijms12128626.
Anonim, ICH Harmonized Tripartite Guideline Topic S9 (2010) : Nonclinical Evaluation for Anticancer Pharmaceutical.
Ideaconsult Ltd, (2011) : Toxtree User Manual,http://ecb.jrc.ec.europa.eu/document s/qsar/qsar_tools/Toxtree_start_manual.pdf (diakses 20 Juli 2012).
Juse´lius, Jonas; Sundholm, Dage (2000). "The aromatic pathways of porphins, chlorins and bacteriochlorins". Physical Chemistry Chemical Physics 2 (10): 2145– 2151.
Moan, J dan Peng, Q, (2003) : An Outline of The History of PDT,1-4, dalam Hader, D.P., Jori, G., dan Patrice, T (editor), Photodynamic Therapy, Comprehensive Series in Photochemistry and Photobiology, p 286, The Royal Society of Chemistry.
Narang, Ajit S., Desai, Divyakant S. dan Mahato, Y., Lu. R.I. (editor) (2009) : Anticancer Drug Development, Unique Aspects of Pharmaceutical Development, Pharmaceutical Perspectives of Cancer Therapeutics, Springer Science Business Media, LLC, 45 – 92.
Schultz, T.W, J.W. Yarbrough, R.S. Hunter & A.O. Aptula., (2007), Verification of the Structural Alerts for Michael Acceptors., Chem. Res. Toxicol., 20, 1359-1363.
Sternberg, Ethan D. David, D. (1998) : Porphyrin-based Photosensitizer for Use in Photodynamic Theraphy, Tetrahedron report 54 (447), 4152-4161.
Tjahjono, D.H. (2006) : Porphyrin Structure-based Molecules for Photodynamic Therapy of Cancer, Acta Pharmaceutica Indonesia, XXXI (1), 1-12.
U.S. EPA, (1991) : Guidlines for Developmental Toxicity Risk Assessment, Federal Register, 56 (234), 63798-63826.
Venkatapathy, R., Moudgal, R., dan Bruce, R. M. (2004) : Assessment of the Oral Rat Chronic Lowest Observed Adverse Effect Level Model in TOPKAT, a QSAR Software Package for Toxicity Prediction, J. Chem. Inf. Comput. Sci., 44, 1623-1629.