PENYIAPAN RADIOFARMAKA TECHNETIUM-99M ANTI
CEA, PEMANFAATAN FOTOAKTIVASI UNTUK
MERE-DUKSI ANTI CEA
M. Yanis Musdja dan Stephen J. Mather
Pusat Pengembangan Radioisotop dan Radiofarmaka, Batan , Serpong
ABSTRAK
PENYIAPAN RADIOFARMAKA TECHNETIUM-99M ANTI CEA, PEMANFAATAN FOTOAKTIVASI UTNUK MERE-DUKSI ANTI CEA. Salah satu alasan utama tingginya angka kematian pasien kanker adalah disebabkan belum memadainya teknik untuk diagnosis kanker secara dini. Pada saat ini, salah satu cara yang terbaik untuk diagnos is kanker secara dini adalah dengan teknik Radioimmunosintigrafi. Dalam tulisan ini, kami melaporkan penyiapan sediaan Radiofarmaka untuk radioimmunosintigrafi kanker kolorektal dengan menggunakan antibodi monoklonal anti carcino-embrionik antigen (anti CEA) yang dilabel dengan Technetium-99m. Sebelum penandaan anti CEA dengan technetium-99m, anti CEA terlebih dahulu direduksi dengan penyinaran menggunakan sinar UV untuk memutuskan gugus sufidril dari anti CEA. Methilen difosfonat (MDP) digunakan seb agai agen chelat berfungsi ganda (bifunctional chelating agent) untuk penandaan anti CEA dengan technetium-99m. Faktor -faktor yang mempengaruhi penandaan dipelajari melalui penentuan kemurnian radiokimia hasil penandaan yang meliputi variasi waktu fotoaktivasi, konsentrasi reduktor Sn (II) fluorida sebagai agen pereduksi, konsentrasi dari pereaksi chelat MDP dan bahan utama anti CEA. Kemurnian radiokimia hasil penandaan ditentukan dengan menggunakan kromatografi lapis tipis cepat dan kromatografi cair kinerja tinggi. Hasil penandaan yang optimum didpatkan lebih besar dari 95% dicapai pada kondisi waktu foto aktivasi 30 menit, konsentasi SnF2 0.0034 mg, konsentrasi MDP 0,0625 mg dan konsentrasi anti CEA 1 mg. Sedangkan pengujian immunoreaktitas hasil penandaan pada antigen dilakukan dengan teknik ELISA yang dikembangkan oleh Durbin dengan kapabilitas pengikatan antigen sekitar 88%.
ABSTRACT
PREPARATION OF TECHNETIUM-99m ANTI CARCINO-EMBRYONIC ANTIGEN (CEA) AS RADIOPHARMACEUTICALS; THE APPLICATION OF A PHOTOACTIVATION FOR REDUCING AN ANTI CEA. One of the main reasons for the high mortality rate of cancer diseases is mostly caused by using the improper modality of the early diagnosis practices. However, a radioimmunoscintigraphic technique is wid ely used as a better alternative for the early diagnosis of several cancer diseases. In the present paper, we report the preparation of radioimmunoscintigraphic agents for the diagnosis of colorectal cancer through the
99mTc labeling of the monoclonal antibody of an anti carcino-embryonic antigen (Anti CEA). Prior to the
labeling, the sulphydril group in the antibody was broken off by reducing it using UV light. Methilenediphosphonate (MDP) was used as a bifunctional chelating agent. The labeling cond ition was studied by varying photoactivation time, the amount of tin (II) fluoride as a reducing agent, the amount of MDP and the amount of anti CEA. The labeling yield and radiochemical purity were determined by means of ITLC and HPLC. The immunoreaactivity test of 99mT c-anti CEA was performed using an ELISA method
developed by Durbin. Results show that the labeling yield 95% was achived at the photoactivation time of 30 Minutes, 0.0034 mg of SnF2, 0.0625 mg of MDP, and 1 mg of anti CEA . The immunoreactivity test showed
the value of 88%.
Kata kunci :
Kanker koloraktal , Radioimmunoscintigrafi, Antibodi monoklonal anti CEA, Tehcnetium-99m, Radiofarmasi. (Colorectal cancer , Radioimmunoscintigraphy, Monoclonal antibody anti CEA, Tehcnetium -99m, Radiopharmacy)
ada saat ini penyakit kanker merupakan penyakit penyebab kematian nomor tiga bagi penduduk Indonesia setelah penyakit infeksi dan penyakit kardiovaskular (5), menurut laporan berbagai sentra patologi di Indonesia lebih dari 70% penderita kanker tidak dapat disembuhkan dan akhirnya berakhir dengan kematian, sedangkan di negara -negara maju angka kematian penderita kanker bisa di tekan lebih kecil dari 40 % (5, 6). Penyebab tingginya kematian penderita kanker di Indon esia disamping sering terlambatnya pasien datang ke rumah sakit atau tempat pengobatan adalah kurang memadainya teknik untuk dapat mendeteksi kanker secara dini, sedangkan pengobatan kanker yang sudah berkembang pada tahap lanjut sangat sulit dan memerlukan biaya yang mahal. Menghindari faktor penyebab kanker adalah hal yang terbaik untuk mencegah terjadinya penyakit kanker, namun hal ini sangat sulit untuk dilakukan secara sempurna, karena sebagian besar penyebab dari penyakit kanker belum diketahui dengan pasti. Oleh karena itu strategi penang-gulangan penyakit kanker lebih ditekankan pada upaya deteksi kanker secara dini dan diikuti dengan pengobatan sedini mungkin pula. Salah satu cara yang terbaik untuk dapat melakukan diagnosis kanker secara dini adalah dengan menggunakan teknik radioimmunoscintigraphy (RIS), dan hampir 80% dari jenis kanker telah dapat dideteksi dengan teknik RIS (3, 11). Dengan teknik RIS ini melalui alat kamera gamma lokasi kanker dan penyebarannya dapat dilihat dengan jelas.
Ada beberapa keuntungan teknik RIS ini antara lain adalah: (3, 10)
1. Dapat mendeteksi lokasi dan tipe kanker
secara dini, sehingga terapi dapat dilakukan lebih awal dan pencegahan perkembangan kanker pada tahap lebih lanjut dapat dicegah atau dihambat.
2. Dapat mendeteksi efek pemakaian
kemoterapi terhadap kanker, sehingga dapat diperoleh informasi apakah kemoterapi dapat menghambat atau mematikan perkembangan sel-sel kanker atau tidak berpengaruh sama sekali.
3. Untuk memonitor perkembangan kanker
sebelum operasi dan pasca operasi Pada saat ini rumah-rumah sakit di Indonesia belum memanfaatkan teknik RIS ini untuk diagnosis kanker dan diharapkan dari hasil-hasil penelitian dalam negeri, bantuan IAEA atau negara yang telah menguasai sains dan teknologinya, teknik ini dalam waktu dekat dapat dimanfaatkan di Indonesia.
Radioisotop yang paling banyak digunakan dalam RIS adalah Technetium-99m, karena
Technetium-99m mempunyai banyak kelebihan bila dibandingkan dengan radioisotop lainnya, dian-taranya adalah mudah untuk didapatkan dan harganya lebih terjangkau, waktu paruhnya sekitar 6 jam tidak terlalu pendek untuk dapat melaksanakan diagnosis dengan baik dan tidak pula terlalu panjang untuk mencegah penerimaan dosis radiasi yang terlalu tinggi pada pasien. Disamping itu radiasi yang dibebaskan adalah gamma murni dengan energi sekitar 140 KeV. Pancaran energi ini disamping tidak begitu membahayakan bagi pasien juga sangat cocok untuk pencitraan kamera gamma SPECT.
Ada berbagai macam antibodi yang dapat digunakan unt uk RIS, salah satunya adalah anti CEA (carcinogen embrionic antigen). Bila anti CEA disenyawakan dengan radioisotop seperti tech --netium-99m , akan dapat dimanfaatkan untuk mendeteksi kanker kolorektal, kanker ovarium, kanker payudara dan kanker paru-paru dan yang paling spesifik adalah untuk kanker kolorektal (4, 9).
Berkaitan dengan uraian diatas, penelitian yang dilaporkan ini bertujuan untuk mendapatkan teknik dan metodologi dalam penyiapan radio
-farmaka 99mTc-anti CEA untuk deteksi dini kanker.
Diharapkan hasil penelitian ini dapat memberikan kontribusi pada upaya pencegahan dini penyakit kanker yang pada gilirannya dapat menurunkan angka kematian yang disebabkan oleh penyakit kanker.
TATA KERJA
Bahan dan alat
Antibodi monoklonal anti CEA (PR1A3) didapatkan dari the Hybridoma Development Unit, Imperial Cancer Research, Bartholomew’s Hospital, London. Kit radiofarmaka MDP (mengandung medronat 6,25 mg, timah (II) fluorida 0.34 mg dan asam p-aminobenzoat 2 mg) dan radioisotop Technetium-99m didapatkan dari Amersham. Instant
thin layer chromatography (ITLC) dibeli dari Gelman
Science Inc. Thin layer chroma-tography (silica gel,
F254) dibeli dari E-Merck. Kit ELISA dari
Immunomedics Inc, Ammonium hidroksida, aseton, salin, sodium hidroksida, asam klorida dan reagen-reagen kimia lainnya yang biasa digunakan di laboratorium dibeli dari Sigma Chemical Co dan E-Merck.
HPLC (Beckman 114M) digunakan untuk menentukan efisiensi penandaan , Gamma Counter (LKB Wallac Compu Gamma) untuk mengukur cacahan keradioaktifan, pH meter digunakan untuk mengukkur pH larutan , lampu UV (Rayonet RMR
3000 photochemical) digunakan untuk melakukan fotoaktivasi, UV-Vis Spektrofotometer untuk menentukan konsentrasi antibodi. Komputer yang telah di program untuk test ELISA dan RIA, serta peralatan umum lainnya yang biasa digunakan di laboratorium.
Prosedur Kerja
Pemeriksaan waktu efektif fotoaktiva-si.terhadap kemurnian radiokimia 99mTc -anti CEA
Disiapkan 6 buah vial steril, masing-masing mengandung anti CEA 0,5 mg dan 0,1 ml larutan kit MDP yang dibuat dengan menambahkan 2 ml larutan dapar fosfat salin (PBS) pH 7. Masing -masing vial disinari dengan sinar UV berturut-turut 0, 10, 15, 20, 40 menit dan 60 menit. Kemudian kedalam setiap vial ditambah dengan larutan technetium-99m sebanyak 0,1 ml dengan aktivitas sekitar 500 MBq dan masing-masing vial ditentukan kemurnian radiokimianya setelah 30 menit.
Pemeriksaan pengaruh konsentrasi MDP dan stannus fluorida terhadap kemurnian radiokimia
99m
Tc-anti CEA
Disiapkan 6 buah vial steril, masing-masing mengandung anti CEA 0,5 mg. Kedalam masing-masing vial berturut-turut ditambahkan 25, 50, 100,
150, 200 µl dan 250 µl larutan kit MDP dan kemudian
semua vial disinari dengan sinar UV selama 20 menit. Kemudian pada setiap vial ditambahkan larutan technetium-99m sebanyak 0,1 ml dengan aktivitas sekitar 500 MBq, lalu masing-masing vial ditentukan kemurnian radiokimianya setelah 30 menit.
Pemeriksaan pengaruh konsentrasi anti CEA terhadap kemurnian radiokimia 99mTc-anti CEA
Disiapkan 6 buah vial steril yang diisi dengan 1 ml larutan anti CEA yang diencerkan dengan larutan PBS pH 7 dengan konssentrasi berturut-turut 1,0, 0,5, 0,25, 0,125, 0,062 dan 0,031 mg anti CEA per ml, kedalam setiap vial ditambahkan 0,1 ml larutan kit MDP ( satu vial kit MDP ditambah 2 ml larutan PBS). Selanjutnya disinari selama 20 menit dengan sinar UV dan kedalam masing-masing vial ditambahkan 0,1 ml (500 MBq) larutan technetium-99m dan setelah 30 menit ditentukan kemurnian radiokimianya.
Pemeriksaan pengaruh waktu penyimpanan terhadap kemurnian radiokimia 99mTc-anti CEA
Anti CEA sebanyak 0,5 mg dalam larutan PBS ditambah 0,1 ml larutan kit MDP ( satu vial kit MDP dilarutkan dalam 2 ml larutan PBS) disinari dengan sinar UV dengan waktu fotoaktivasi 20 menit lalu ditambah 0,1 ml (500 MBq) larutan technetium-99m, kemudian setelah 0,5, 1, 2, 4, 8, 10, 20 dan 24 jam ditentukan kemurnian radiokimianya.
Pemeriksaan hasil Penandaan 99mTc-anti CEA
Pemeriksaan kemurnian radiokimia dan profil hasil penandaan dilakukan dengan dengan cara:
Menggunakan kromatografi ITLC-SG dengan fasa gerak salin, aseton dan ITLC -SG yang direndam dalam HSA 2,5 % kemudian dikromatografi dengan
fasa gerak larutan NH4OH :Metanol : Air (1 : 2 : 4).
Kromatogram kemudian dicacah menggunakan alat KLB Wallac Compu Gamma CS gamma counter.
Menggunakan HPLC. Penentuan profil hasil penandaan ditentukan dengan HPLC size exclusion menggunakan sebuah pompa Beckman 114M dengan suatu detektor 16 0 UV yang dihubungkan dengan alat Spectra -Physic SP4290. Sebagai fasa gerak digunakan 0,2M Natrium Posfat pH 7,0 yang dicampur dengan 2 mM EDTA dengan perbandingan volume 1 : 1.
Pemeriksaan Pembebasan Gugus Thiol
Jumlah gugus sulphidril antibodi yang dib ebaskan oleh penyinaran dengan lampu UV ditentukan dengan reagen Ellmans dengan cara
mencampur 50 µl larutan cuplikan dengan 50 µl
larutan asam 5,5’-dithio bis -(2-nitro-benzoat) 2mg/ml, kemudian dilarutkan hingga 1 ml dengan larutan dapar posfat 0,1M pH.8. Campuran diinkubasi pada temperatur ruangan selama 15 menit dan perubahan warna yang terbentuk diukur dengan menggunakan spektro -fotometer UV/Vis pada panjang gelombang 412 nm. Jumlah pembebasan gugus thiol yang dihasilkan dibandingkan dengan suatu standar kurva seri dari senyawa cystein yang dibuat dengan konsentasi 0,01 sampai 0,1 mM.
Uji Pengikatan Antibodi Terhadap Antigen
Untuk melaksanakan pengujian pengikatan antigen oleh antibodi dilakukan dengan menggunakan teknik ELISA yang dikem-bangka n oleh Durbin dengan nomor LS174T, dan dikerjakan oleh staf departemen immunologi , rumah sakit St. Bartholomew, London, yaitu dengan membandingkan aktivitas antara anti CEA yang
sudah ditandai dengan technetium-99m dengan aktivitas anti CEA sebelum penan daan. (3).
HASIL DAN PEMBAHASAN
Hal utama yang diharapkan dari penelitian ini adalah untuk mendapatkan kondisi optimum penandaan anti CEA dengan technetium-99m menggunakan teknik fotoaktivasi sinar UV untuk pemutusan gugus sulfida yang ada pada anti CEA , karena itu teknik yang digunakan untuk pengukuran
kemurnian radiokimia 99mTc-anti CEA merupakan hal
yang sangat penting Penggunaan fasa diam kertas fiber gelas ITLC-SG HSA 2,5% dengan fase gerak
larutan NH4OH :Metanol : Air (1 : 2 : 4), dapat
mengidentifikasi adanya spesi 99mTc Koloid yang
akan tertahan ditempat penotolan (Rf = 0,0),
sedangkan 99mTc–MDP-Ab dan 99mTc-MDP akan
naik keatas dengan Rf sekitar 0,4 – 0,6 dan 99mTcO4
-juga akan naik dengan Rf sekitar 1,0.
Penggunaan kertas fiber gelas ITLC-SG dengan fasa gerak larutan salin, membedakan spesi 99m
Tc-MDP-Ab dan 99mTc-koloid yang akan
tertinggal pada titik penotolan dengan 99m TcO4- dan
99m
Tc-MDP yang akan naik keatas dengan Rf 0,9-1,0.
Penggunaan kertas fiber gelas ITLC -SG dengan fasa gerak aseton membedakan spesi 99m
Tc-koloid dan 99mTcO4
yang akan tertinggal
dititik penotolan dengan 99mTc-MDP-Ab dan
99m
Tc-MDP yang akan naik keatas dengan Rf sekitar 0,8-1,0. ,(4, 10).
Dari beberapa faktor yang mempengaruhi kondisi optimum untuk penandaan didapatkan hasil sebagai berikut
Pengaruh waktu fotoaktivasi terhadap ke-murnian radiokimia 99mTc-anti CEA
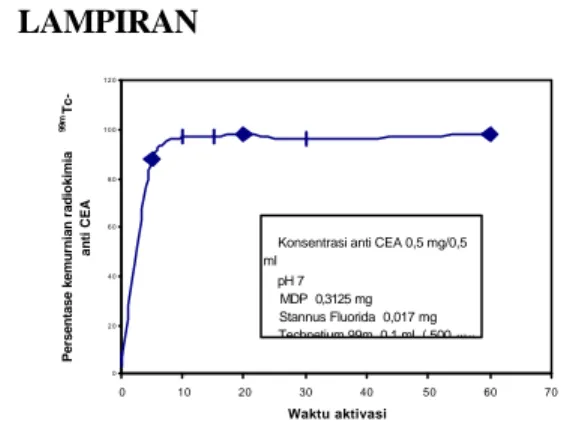
Variasi waktu fotoaktivasi yang dilakukan dari 0, 5, 10, 15, 20, 40 dan 60 menit, memberikan hasil kemurnian radiokimia sebagai berikut: Untuk waktu tanpa fotoaktivasi ( 0 menit ) didapatkan kemurnian radiokimia sekitar 6%, kemurnian radiokimia masih kecil karena belum ada pemutusan gugusan sulfidril yang disebabkan oleh pengaruh fotoaktivasi sinar UV sehingga technetium tidak dapat berikatan dengan anti CEA. Untuk waktu fotoaktivasi selama 5 menit terjadi peningkatan kemurnian radiokimia yang sangat tajam yaitu dengan kemurnian radiokimia sekitar 88%. Peningkatan kemurnian radiokimia yang sangat tajam ini terjadi karena pengaruh fotoaktivasi dari sinar UV yang menyebabkan pemutusan gugusan-gugusan sulfidril yang ada pada anti CEA. Untuk waktu 10
menit didapatkan kemurnian radiokimia sekitar 97 %. Untuk waktu penyinaran sampai 15 menit didapatkan kemurnian radiokimia sekitar 98 % dan untuk waktu penyinaran 20, 40 dan 60 menit didapatkan kemurnian radiokimia masih tinggi yaitu sekitar 98%. Untuk waktu penyinaran 20 sampai 60 menit tidak didapatkan perubahan kemunian radiokimia kemungkinan disebabkan telah terjadi pemutusan semua gugusan sulfidril yang mampu diputuskan oleh kekuatan sinar UV pada senyawa anti CEA sehinga pengaruh waktu fotoaktivasi tidak lagi mempengaruhi kemurnian radiokimia., sebagaimana ditunjukkan pada Gambar 1. Dari hal ini kelihatan bahwa untuk pemutusan gugusan sufidril dibutuhkan waktu optimal dan semakin banyak gugusan sulfidril yang putus semakin banyak
terbentuk senyawa 99mTc-anti CEA, karena 99mTc
hanya akan berikatan pada gugus sulfidril yang telah putus pada anti CEA.
Pengaruh konsentrasi timah (II) fluorida dan MDP terhadap kemurnian radiokimia 99mTc-anti CEA
Fungsi timah (II) fluorida yang ada dalam kit MDP adalah untuk mereduksi technetium dari valensi 7 menjadi valensi 5, dalam hal ini technetium valensi 5 akan dapat berikatan dengan anti CEA sedangkan technetium valensi 7 tidak berikatan dengan anti CEA. Karena itu jumlah konsentrasi timah (II) fluorida sangat mempe--ngaruhi terhadap
efisiensi penandaan radiofarmaka 99mTc-anti CEA
Pengaruh konsentrasi timah (II) fluorida terhadap
kemurnian radiokimia 99mTc-anti CEA ditunjukkan
pada Gambar 2. Dalam hal ini dengan konsentrasi
timah (II) fluorida sebesar 4,25 µg per mg antibodi
memberikan kemurnian radiokimia sekitar 13 % ,
untuk konsentrasi timah (II) fluorida 8,5 µg per mg
antibodi memberikan kemurnian radiokimia sekitar 33
%, sedangkan untuk konsentrasi 17 µg dan 25,5 µg
per mg antibodi didapatkan kemurnian radiokimia sekitar 98 %. Untuk konsentrasi timah (II) fluorida 34
µg per mg terjadi penururnan kemurnian radiokimia
manjadi sekitar 94% dan untuk konsentarasi timah
(II) fluorida 42,5 µg terjadi penurunan radiokimia
menjadi sekitar 88%. Penurunan kemurnian radiokimia terjadi pada konsentrasi timah (II) fluorida
34 µg dan 42,5 µg adalah disebabkan oleh pengaruh
jumlah mol 99mTc-MDP yang terbentuk lebih besar,
sedangkan jumlah mol 99mTc-MDP-anti CEA adalah
tetap. Pengaruh ini disebabkan radiofarmaka ini dibuat dengan menggunakan kit MDP, dalam hal ini bila jumlah timah (II) fluorida yang digunakan meningkat maka jumlah MDP yang digunakan juga akan meningkat.
Fungsi MDP dalam pembuatan radiofarmaka 99m
berfungsi ganda (bifunctional chelating agent) karena itu konsentrasi MDP akan sangat mempengaruhi efisiensi penandaan. Pengaru h konsentarasi MDP
terhadap kemurnian radiokimia 99mTc-anti CEA
adalah mirip dengan pengaruh konsentrasi timah (II)
fluorida terhadap kemurnian radiokimia 99mTc-anti
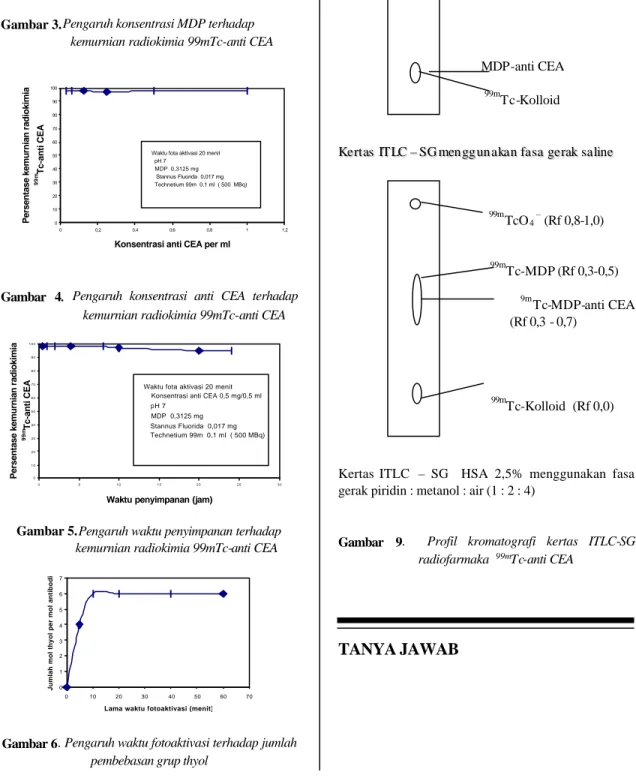
CEA, sebagaimana ditunjukkan pada Gambar 3, karena perbandingan antara timah (II) fluorid a dengan MDP dalam satu vial kit selalu tetap. Dalam
hal ini untuk konsentrasi MDP sebesar 13 µg per mg
antibodi didapatkan kemurnian radiokimia 99mTc-anti
CEA sekitar 13 % untuk konsentrasi MDP 156 µg per
mg antibodi didapatkan kemurnian radiokimia sekitar
33 %, untuk konsentrasi MDP 312,5 µg dan 468,75 µg
per mg antibodi didapatkan kemurnian radiokimianya
sekitar 98%. Untuk konsentrasi MDP 625 µg per mg
antibodi terjadi penurunan radiokimia menjadi 94%
dan untuk konsentrasi MDP 781,25 µg terjadi
penurunan kemurnia radiokimia yang cukup tajam yaitu sekitar 88 %. Untuk konsentrasi MDP
625 µg dan konsentrasi 781,25 µg per mg antibodi
terjadi penurunan kemurnian radiokimia 99mTc-anti
CEA adalah disebabkan jumlah mol 99mTc-MDP yang
terbentuk semakin besar sedangkan jumlah 99m
Tc-MDP-anti CEA tetap sebagaimana disebutkan diatas. Kemungkinan lain adalah disebabkan kenaikan timah (II) fluorida dan MDP sampai jumlah tertentu
akan mendorong pembentukan komplek 99mTc-anti
CEA, tetapi sampai pada batas tertentu kenaikan lebih lanjut akan menginhibisi pembentukan komplek 99m
Tc-anti CEA atau dapat memutus kembali ikatan 99m
Tc-anti CEA yang sudah terjadi.
Pengaruh konsentrasi anti CEA terhadap kemurnian radiokimia 99mTc-anti CEA
Untuk melihat pengaruh konsentrasi anti CEA
terhadap kemurnian radiokimia 99mTc-anti CEA
dibuat variasi konsentrasi anti CEA dengan pengenceran dalam larutan PBS pH 7 dengan konsentrasi berturut -turut 1,0 mg/ml, 0,5 mg/ml, 0,25 mg/ml, 0,125 mg/ml, 0,062mg/ml dan 0,0312mg/ml. Dalam hal ini didapatkan hampir tidak ada perubahan
kemurnian radiokimia 99mTc-anti CEA. Hal ini
menunjukkan bahwa jumlah konsentarasi anti CEA yang paling terkecil digunakan dalam percobaan ini yaitu sebesar 0,0312 mg/ml telah mencukupi untuk mengikat jumlah mol technetium-99m yang ada dalam 0,1 ml larutan technetium-99m yang digunakan. Sebagaimana ditunjukkan pada Gambar 4.
Pengaruh waktu penyimpanan terhadap kemurnian radiokimia 99mTc-anti CEA
Perubahan kemurnian radiokimia 99mTc-anti
CEA terhadap waktu penyimpanan diamati dari 0,5 jam, 1.0 jam, 2,0 jam, 4,0 jam 8,0 jam, 10jam , 20 jam dan 24 jam. Gambar 5 menunjukkan bahwa
radiofarmaka 99mTc-anti CEA masih tetap stabil
selama waktu penyimpanan sampai dengan 8 jam. Untuk waktu penyimpanan 10 jam terjadi sedikit penurunan kemurnian radiokima dan setelah waktu penyimpanan 20 jam dan 24 jam didapatkan penurunan kemurnian radiokimia berlanjut sampai mencapai sekitar 95%. Penurunan kemurnian radiokimia ini mungkin disebab kan stabilitas antibodi telah mulai rusak karena pengaruh efek sinar gamma yang dipancarkan oleh technetium-99m. Namun dengan batas ambang kemurnian radiokimia
yang minimal sebesar 95%, sediaan 99mTc-anti CEA
masih dapat digunakan setelah penyimpanan selama 3 - 4 kali waktu paruh tehcnetium-99m, apabila aktivitasnya masih mencukupi.
Pengaruh waktu fotoaktivasi terhadap jum-lah pembebasan grup thiol
Pengaruh waktu aktivasi terhadap jumlah pembebasan grup thiol dilakukan dengan meng -gunakan reagen Ellman dengan waktu fotoaktivasi 0, 5, 10, 20, 40 dan 60 menit. Dalam hal ini untuk waktu fotoaktivasi 0 menit atau tanpa foto aktivasi tidak didapatkan pembebasan grup thiol, untuk waktu fotoaktivasi 5 menit didapatkan pembebasan mol grup thiol sekitar 4 dan untuk fotoaktivasi 10, 20, 40 dan 60 menit didapatkan pembebasan grup mol thiol sekitar 6, untuk waktu fotoaktivasi dari 10 menit sampai dengan 60 menit tidak didapatkan jumlah peningkatan pembebasan mol thiol sebagaimana ditunjukan pada Gambar 6. Hal ini barangkali disebabkan pada waktu fotoaktivasi 10 menit semua grup thiol yang ada pada anti CEA telah diputuskan.. Dari pengukuran jumlah mol gugus thiol yang dibebaskan menggunakan reagen Ellman yang diakibatkan oleh pengaruh foto-aktivasi dengan sinar UV ini dapat dinyatakan bahwa sinar UV dapat memutuskan gugusan sulfidril yang ada pada anti CEA sebagaimana pemutusan gugusan sulfidril oleh zat-zat reduktor lainnya sseperti
2-mercaptoethanol dan ion Sn++ ( 10 ). Semakin banyak
pembebasan mol grup thiol berarti semakin banyak gugusan sulfidril yang diputuskan dan semakin banyak pula technetium-99m untuk dapat berikatan dengan gugusan sulfidril sehingga dari akibat ini akan meningkatkan kemurnian radiokimia komplek 99m
Tc-anti CEA.
Pemakaian cystein dalam percobaan ini untuk
penentuan pembebasan mol grup thiol yang ada pada anti CEA adalah karena satu mol cystein mengandung satu mol thiol. Dengan membuat kurva
standar cystein akan dapat dijadikan sebagai pembanding jumlah mol grup thiol yang dibebas kan pada anti CEA. Mol grup thiol yang dibebaskan bila direaksikan dengan reagen Ellman akan memberikan warna merah. Tingkat warna merah yang terbentuk bila diukur dengan alat spektrofotometer UV/VIS dapat digunakan untuk menentukan jumlah mol grup thiol yang dibebaskan pada anti CEA dengan membandingkannya dengan tingkat warna merah yang terbentuk pada pembebasan mol thiol pada cystein.
Pengujian jumlah pengikatan antigen oleh antibodi
Pengujian jumlah antigen yang diikat oleh antibodi dilakukan denga n menggunakan metode ELISA menggunakan fluorescence assay yang dikembangkan oleh Durbin ( 8 ). Jumlah pengikatan antigen yang diikat oleh anti CEA sebelum fotoaktivasi dianggap terjadi 100 %, kemudian dibandingkan dengan pengikatan antigen oleh anti
CEA setelah fotoaktivasi. Dalam hal ini 99mTc-anti
CEA yang diukur adalah 99mTc-anti CEA hasil
penandaan pada kondisi optimum, dengan waktu fotoaktivasi sekitar 20 menit , pH sekitar 7, konsentrasi anti CEA 0.5 mg, konsentrasi timah (II) fluorida 0,017 mg, ko nsentrasi MDP 0,03125 mg dan larutan Technetium-99m 0,1 ml dengan akti-vitas sekitar 500 MBq dengan volume total larutan 2 ml.
Didapatkan jumlah pengikatan antigen oleh 99m
Tc-anti CEA sekitar 88%. Penurunan jumlah pengikatan antigen oleh anti CEA setelah fotoaktivasi yang ditandai dengan technetium-99m dibandingkan sebelum fotoaktivasi kemungkinan disebabkan proses foaktiavasi tidak hanya memutuskan gugusan sulfidril ( yang dapat meningkatkan pembentukan 99m
Tc-anti CEA) tetapi juga merusak struktur aktif gugus antibodi yang dapat mengikat antigen , hal yang terakhir ini menyebabkan penurunan kemampuan untuk mengikat antigen. Kemudian kemungkinan lain adalah pengaruh radiasi sinar gamma yang dipancarkan oleh radioisotop technetium-99m juga dapat mengura ngi kemampuan anti CEA untuk dapat mengikat antigen.
Pemeriksaan hasil penandaan dengan HPLC
Profil hasil pemeriksaan 99mTc-anti CEA
dengan HPLC menggunakan detektor radioaktif dan detektor UV pada panjang gelombang 254 nm dapat dilihat pada Gambar 7 dan Gambar 8. Hasil peme-riksaan kemurnian radiokimia dengan menggunakan detektor radioaktif hampir sama dengan menggunakan kromatografi kertas ITLC-SG dalam fasa gerak saline dan kromatografi kertas ITLC -SG
HSA 2,5% dalam fasa gerak larutan NH4OH
:Metanol : Air (1 : 2 : 4), profil kromatografi kertas ITLC-SG yang dihasilkan ditunjukkan pada Gambar 9.
KESIMPULAN
Dari hasil penelitian yang telah disebutkan diatas dapat diambil kesimpulan :
1. Penandaan antibodi monoklonal anti CEA
dengan Technetium-99m bisa dilakukan dengan metode fotoaktivasi menggunakan sinar UV untuk pemutusan gugus sulfidril yang ada pada anti CEA dengan bantuan MDP yang berfungsi sebagai chelat berfungsi ganda (bifunctional chelating agent) dan Sn(II) fluorida yang berfungsi seba gai zat pereduksi technetium. Dari hasil penelitian ini didapatkan kemurnian
radiokimia 99mTc-anti CEA pada kondisi optimum
sekitar 98%, dengan waktu fotoaktivasi sekitar 20 menit , pH sekitar 7, konsentrasi anti CEA 0.5 mg, konsentrasi Sn(II)fluorida sekitar 0,017 mg atau 2 mg/ml, konsentrasi MDP 0,03125 mg dan larutan Technetium-99m 0,1 ml dengan aktivitas sekitar 500 MBq.
2. Sediaan Radiofarmasi 99mTc-anti CEA yang
disiapkan tidak memerlukan lagi pemurnian hasil penandaan, teknik penandaannya simpel dan hasil pengikatan antibodi-antigen setelah penandaan cukup tinggi yaitu sekitar 88%.
SARAN
.Teknik penyiapan radiofarmaka 99m
Tc-antiCEA ataupun penandaan antibodi lainnya dengan radioisotop yang dapat digunakan untuk melakukan diagnosis sebagian besar kanker secara dini, kiranya dapat diaplikasikan di Rumah Sakit-rumah sakit yang memiliki fasilitas kedokteran nuklir di Indonesia, karena hal ini akan bermanfaat banyak dalam menanggulangi panyakit kanker di Indonesia
UCAPAN TERIMA KASIH
Saya sangat berterima kasih kepada Dr. Stephen J Mather M..Pharm, Kepala Departemen Radiofarmasi dan Dr .K. Britton, Kepala Kedok-teran Nuklir, Rumah sakit St. Bartholomew’s, London, atas kesempatan yang dia berikan kepada saya untuk bekerja di Departemen Radiofarma si dan Departemen Kedokteran Nuklir selama 3 bulan. Terima kasih yang istimewa saya sampaikan kepada teman kerja saya Dr. J. Davis, karena berkat kerja samanya yang sangat kooperatif, semua pekerjaan saya di Rumah Sakit St. Bartholomew’s. London dapat berjalan
dengan sukses. Terima kasih juga saya sampaikan kepada Dr. Maria Stalteri dan Dr. Jane Sosabowski atas bantuannya dalam melaksanakan penelitian ini. Kepada Dr. Irene Wawra, Direktur Urusan Bantuan Penelitian dan Training, Badan teneaga Atom International, saya mengucapkan terima kasih, karena atas bantuan mereka semua pekerjaan saya dapat berjalan dengan lancar.
Penelitian ini dibiayai oleh Badan Tenaga Atom International (IAEA), dalam hal ini saya menyampaikan terima kasih banyak atas segala bantuan dan seleksi yang telah mereka lakukan sehingga penelitian ini dapat saya laksanakan dengan lancar.
DAFTAR PUSTAKA
1. Abrar Siddiqui., Syed M. Quadri et al., Tumor
Targeting and Pharmacokinatics of Unmodified and Modified (F(ab)2 Fragments of an Anti-CEA Murine
Monoclonal Antibody (Immu-14)., J. Nucl. Med.
Biol. Vol. 22, No. 4, 1995: 425-435,
2. Burchel J. Gendler., Gendler S., Taylor P. J., et
al., Development and Characterization of
Breast-cancer Reactive .Monoclonal .A.antibodies Directed to the Core Protein of the Human Milk Mucin.,
Cancer Res: No. 39: 1987: 317 – 328.
3. David M. Goldenberg., Steven M. Larson.,
Radioimmunodetection in Cancer Identification., J.
Nucl. Med. No. 33: 1992: 803-814.
4. Eckelman W.C., Paik C.H., Steigman J., Three
Aproaches to Radiolabelling with 99mTc., Nucl.
Med. Biol., No. 16: 1989: 171 –176.
5. Gani. W. Tambunan., Diagnosis dan Tatalaksana
Sepuluh Jenis Kanker Terbanyak di Indonesia., Editor Maylani Handojo., Penerbit buku
Kedokteran., EGC, 1995, halaman 1-19
6. Janet F. Eary., Robert W. Scroff et al., Successful
Imaging of Malignant Melanoma with Technetium-99m-Labeled Monoclonal Antibodies, J. Nucl.
Med. No. 30: 1989: 25-32.
7. John E., Thakur M. l., Wilder S., Alauddin M.
M., Eppstein A.L., Tectnetium-99M-Labeled
Monoclonal Antibodies: Influence of Technetium-99M Binding Sites., J. Nucl. Med. No. 35: 1994:
876-881.
8. Mather SJ. Ellison D. reduction-mediated
technetium-99m labelling of monoclonal antibodies . J. Nucl. Med No.31: 1990; 692-697.
9. Paik C.H., Phan Lan N.B., Hong J.J ., et al., The
Labelling of High Affinity Sites of Antibodies with Tc-99m. J. Nucl. Med. Biol : No. 12: 1985: 3-8.
10. Rhodes B.A., Direct Labelling of Protein with 99mTc. Nucl. Med. Boil., No. 18: 1991:: 667 – 676.
11. Sykes TR, Woo TK, Qi P, Baum RP, Noujaim AA, Photo labelling of proteins with technetium-99m (abstract) Nuclear Medicine Communication, No. 14: 1993; 909.
12. Thakur M.L., DeVulvio J., Richard M.D., Paik C.H., Technetium-99m Labellled Monoclonal
Antibodies: Evaluation of Reducing Agents., Nuc.
Med. Biol., No. 18: 1991: 227-234.
LAMPIRAN
0 2 0 4 0 6 0 8 0 1 0 0 1 2 0 0 10 20 30 40 50 60 70 Waktu aktivasiPersentase kemurnian radiokimia
99m
Tc-anti CEA Konsentrasi anti CEA 0,5 mg/0,5 ml
pH 7 MDP 0,3125 mg Stannus Fluorida 0,017 mg Technetium 99m 0,1 ml ( 500 MBq)
Gambar 1. Pengaruh Waktu Fotoaktivasi Terhadap
Kemurnian Radiokimia 99mTc-anti CEA
0 1 0 2 0 3 0 4 0 5 0 6 0 7 0 8 0 9 0 1 0 0 1 1 0 0 5 1 0 1 5 2 0 2 5 3 0 3 5 4 0 4 5
Microgram stannus fluorida per mg antibodi
Persentase kemurnian radiokimia
99m
Tc-anti CEA
Waktu fotoaktivasi 20 menit pH = 7 Anti CEA 0,5 mg/0,5 ml Technetium-99m 0,1 ml (500 MBq)
Gambar2. Pengaruh Konsentrasi Stannus Fluorida
Terhadap Kemurnian Radiokimia 99mTc-anti CEA
0 20 40 60 80 100 120 0 100 200 300 400 500 600 700 800 900
microgram MDP per mg antibodi
Persentase kemurnia radiokimia
99m
Tc-anti
CEA Waktu fota aktivasi 20 menit
Konsentrasi anti CEA 0,5 mg/0,5 ml pH 7
Technetium 99m 0,1 ml ( 500 MBq)
Gambar 3. Pengaruh konsentrasi MDP terhadap
kemurnian radiokimia 99mTc-anti CEA
0 10 20 30 40 50 60 70 80 90 100 0 0,2 0,4 0,6 0,8 1 1,2
Konsentrasi anti CEA per ml
Persentase kemurnian radiokimia
99m
Tc-anti CEA
Waktu fota aktivasi 20 menit
pH 7 MDP 0,3125 mg Stannus Fluorida 0,017 mg Technetium 99m 0,1 ml ( 500 MBq)
Gambar 4. Pengaruh konsentrasi anti CEA terhadap
kemurnian radiokimia 99mTc-anti CEA
0 1 0 2 0 3 0 4 0 5 0 6 0 7 0 8 0 9 0 1 0 0 0 5 1 0 1 5 2 0 2 5 3 0
Waktu penyimpanan (jam)
Persentase kemurnian radiokimia
99m
Tc-anti CEA
Waktu fota aktivasi 20 menit
Konsentrasi anti CEA 0,5 mg/0,5 ml pH 7
MDP 0,3125 mg Stannus Fluorida 0,017 mg Technetium 99m 0,1 ml ( 500 MBq)
Gambar 5. Pengaruh waktu penyimpanan terhadap
kemurnian radiokimia 99mTc-anti CEA
0 1 2 3 4 5 6 7 0 10 20 30 40 50 60 70
Lama waktu fotoaktivasi (menit)
Jumlah mol thyol per mol antibodi
Gambar 6. Pengaruh waktu fotoaktivasi terhadap jumlah
pembebasan grup thyol
99mTcO4 (Rf 0,8 –1,0) 99mTc- MDP (Rf 0,8 – 1,0) 99mTc- MDP-anti CEA 99mTc-Kolloid K KeerrttaassIITTLLCC––SSGGmmeenngggguunnaakkaannffaassaaggeerraakkssaalliinnee 99m TcO4 – (Rf 0,8-1,0) 99m Tc-MDP (Rf 0,3-0,5) 9m Tc-MDP-anti CEA (Rf 0,3 - 0,7) 99m Tc-Kolloid (Rf 0,0)
Kertas ITLC – SG HSA 2,5% menggunakan fasa gerak piridin : metanol : air (1 : 2 : 4)
Gambar 9. Profil kromatografi kertas ITLC-SG
radiofarmaka 99mTc-anti CEA
TANYA JAWAB
`