10 2.1 Tanaman Dewandaru
2.1.1 Klasifikasi Tanaman Dewandaru (Eugenia uniflora L)
Klasifikasi tanaman Dewandaru (Eugenia uniflora L.) dengan nama daerah Cereme asem (Melayu), Asem selong, belimbing londo, Dewandaru (Jawa) dalam sistematika tumbuhan (Hutapea, 1994), dapat dilihat pada Gambar 2.1 adalah :
Kingdom : Plantae
Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Dicotyledoneae Bangsa : Myrtales Suku : Myrtaceac Marga : Eugenia
Jenis : Eugenia uniflora L.
2.1.2 Buah Dewandaru
Buah dewandaru berupa buah buni bulat dengan diameter kurang lebih 1,5 cm dan berwarna merah, seperti pada Gambar 2.1 . Bijinya keras, berwarna coklat, dan kecil. Akar yang dimiliki berwarna coklat dan merupakan akar tunggang.
Gambar 2.1 Buah Dewandaru
Tanaman Dewandaru (Eugenia uniflora L.) berbentuk perdu yang tumbuh secara tahunan dengan tinggi lebih dari 5 meter. Batangnya tegak berkayu, berbentuk bulat dan berwarna coklat. Daun yang dimiliki berwarna hijau serta merupakan daun tunggal tersebar berbentuk lonjong dengan ujung runcing dan pangkal meruncing. Tepi daun rata, pertulangan menyirip dengan panjang lebih dari 5 cm dan lebar kurang lebih 4 cm. Tanaman ini memiliki bunga berbentuk tunggal berkelamin dua dengan daun pelindung yang kecil berwarna hijau. Kelopak bunga bertaju tiga sampai lima, benangsari yang dimiliki banyak dengan warna putih. Putik berbentuk silindris, mahkota bunga berbentuk kuku dan berwarna kuning (Hutapea, 1994).
2.1.3 Kegunaan Tanaman
Di Brasil buah Dewandaru sering digunakan sebagai antihipertensi dan pengobatan untuk gangguan pencernaan. Di beberapa daerah, digunakan sebagai diuretik, hipotensi, anti inflamasi, anti diare, dan antimikroba. Kandungan fitokimia pada spesies Eugenia mengungkapkan adanya flavonoid, tanin, terpenoid, dan minyak minyak esensial. Secara farmakologi, penelitian yang dilakukan dengan ekstrak buah dan senyawa telah terbukti memiliki efek anti inflamasi, analgesik dan antipiretik, antijamur, hipotensi, antihiperlipidemia, hipoglikemik, dan aktivitas antioksidan (Figueiroa, et al., 2013).
2.1.4 Kandungan Kimia Buah Dewandaru (Eugenia uniflora L)
Dewandaru mengandung senyawa flavonoid dan fenolik monoterpene (75,3%) ditemukan sebagai kandungan minyak atsiri tertinggi dalam buah Dewandaru. Senyawa lainnya yaitu transbeta-ocimene (36,2%), cis-ocimene (13,4%), isomenic beta-ocimene (15,4%), dan beta-pinene (10,3%). Kandungan terapeutik pada ekstrak daun seperti selina-1,3,7(11)-trien-8-one juga ditemukan pada ekstrak volatile buah. Hal itu menunjukkan kemungkinan buah bermanfaat terapeutik seperti layaknya ekstrak daun (Suhendi. et al. 2011).
Minyak esensial buah Dewandaru didapat melalui ektraksi dengan pelarut etil asetat dan dianalisis dengan gas chromatography-mass spectrometry (GC-MS). Terdeteksi senyawa monoterpen (75,3%), ditemukan pada sejumlah besar trans-β-ocimene (36,2%), cis-trans-β-ocimene (13,4%), isomer β-trans-β-ocimene (15,4%) dan β-pinene (10,3%), kandungan minyak menguap yang hampir sama dengan daun (Alessandra,
et al., 2006). Buah Dewandaru yang berwarna merah keunguan mempunyai
aktivitas antioksidan yang kuat karena terdapat kandungan total fenol dan antosianin yang tinggi (Bagetti, et al., 2011).
2.2 Antioksidan
Antioksidan adalah senyawa yang mempunyai struktur molekul yang dapat memberikan elektron kepada radikal bebas tanpa terganggu fungsinya dan dapat memutus reaksi berantai dari radikal bebas (Revolta, 2010). Antioksidan secara nyata mampu memperlambat atau menghambat oksidasi zat yang mudah teroksidasi meskipun dalam konsentrasi rendah (Halliwel, et al., 1998).
Antioksidan merupakan suatu senyawa yang dapat menyerap atau menetralisir radikal bebas sehingga mampu mencegah penyakit-penyakit degeneratif seperti kardiovaskuler, karsinogenesis dan penyakit lainnya. Senyawa antioksidan merupakan subtansi yang diperlukan untuk menetralisir radikal bebas terhadap sel normal, protein, dan lemak. Senyawa ini memiliki struktur molekul yang dapat memberikan elektron nya kepada molekul radikal bebas tanpa terganggu sama sekali fungsinya dan dapat memutus reaksi berantai dari radikal bebas (Murray, et al, 2009). Antioksidan dapat digolongkan menjadi antioksidan enzimatis dan non enzimatis. Antioksidan enzimatis disebut juga antioksidan primer atau antioksidan endogen, diantaranya SOD, GPx, dan Catalase. Antioksidan non enzimatis disebut juga antioksidan sekunder atau antioksidan eksogen, digolongkan sebagai yang larut dalam lemak seperti tokoferol, karotenoid, flavonoid, quinon, dan bilirubin, sementara yang larut dalam air seperti asam askorbat, asam urat, protein pengikat logam dan protein pengikat heme (Winarsi, 2007).
Butil Hidroksi Anisol (BHA), Butil Hidroksi Toluen (BHT), propel galat, tert-butil hidroksi quinon (TBHQ) merupakan antioksidan sintetik digunakan pada produk makanan (Prangdimurti,2007).
Studi epidemiologi menunjukkan bahwa adanya peningkatan konsumsi antioksidan alami yang terdapat dalam buah, sayur, bunga dan bagian-bagian lain dari tumbuhan dapat mencegah penyakit-penyakit akibat stres oksidatif seperti kanker, jantung, peradangan, ginjal dan hati (Yevgenia, et al., 2013).
Mikronutrien yang terkandung dalam tumbuhan seperti vitamin A, C, E, asam folat, karotenoid, antosianin dan polifenol memiliki kemampuan menangkap radikal bebas sehingga dapat dijadikan pengganti konsumsi antioksidan sintetis (Gill, et.al., 2002). Hal ini dibuktikan oleh Shafie (2011) bahwa vitamin E yang diberikan pada mencit secara oral dapat mencegah terjadinya penyakit periodontal. (Wrasiati, 2011) menyatakan bahwa ekstrak bunga kamboja cendana dapat meningkatkan aktivitas enzim SOD, GPx dan katalase. Zheng dan Wang (2009) menyatakan bahwa lebih dari 40 herbal tanaman obat di Cina mempunyai aktivitas antioksidan yang cukup tinggi dan dari 40 herbal tersebut mengandung senyawa fenol yang tinggi termasuk diantaranya kandungan flavonoidnya yang tinggi. Hasil penelitian You, et.al., (2010) menyatakan bahwa kandungan senyawa fenol dan aktivitas antioksidan 40 spesies tanaman obat di China dapat dipergunakan untuk mencegah terapi penyakit cardiovaskular dan cerebrovascular. Adanya gugus -OH pada tokoferol (Vit.E) dan senyawa fenol lainnya serta ikatan rangkap (>C=C<) pada β-karoten dapat menghambat dan menetralisir reaksi radikal bebas (Murray, et.al., 2009).
2.2.1 Enzim Antioksidan
Enzim antioksidan endogen atau antioksidan endogenous enzimatik adalah antioksidan yang diproduksi oleh tubuh manusia sebagai penangkal radikal bebas eksogen maupun radikal bebas endogen seperti superoksida dismutase (SOD), Glutation Peroksida (GPx) dan katalase (CAT). Antioksidan enzimatik disebut juga
antioksidan primer yaitu antioksidan yang berfungsi menangkap radikal bebas dan menghentikan pembentukan radikal bebas (Sadikin, 2002; Murray et.al., 2009).
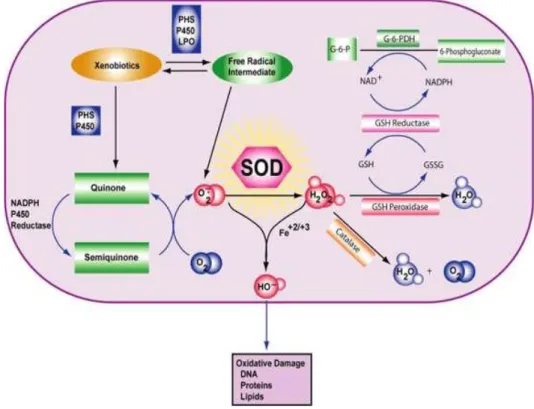
2.2.1.1 Super Oksida Dismutase (SOD)
Superoksida dismutase terdapat dalam semua organisme aerob, dan sebagian besar berada dalam tingkat intraseluler. Organisme aerob selalu membutuhkan oksigen untuk hidupnya, namun dalam setiap aktivitas nya dapat menimbulkan senyawa oksigen reaktif atau radikal bebas (Winarsi, 2007). Enzim antioksidan SOD merupakan kelompok enzim yang dapat ditemukan dalam sel (sitosol dan mitokondria) juga dalam plasma. SOD yang terdapat dalam sitoplasma ada dalam bentuk CuZn-SOD , mempunyai berat molekul 23.000 Dalton. Sedangkan dalam plasma berupa EC-SOD dengan berat molekul 135.000 dalton. Semua bentuk SOD tersebut mengkatalis perubahan anion superoxide menjadi
hydrogen peroxide (Marciniak et al., 2009) seperti reaksi:
2O2- + 2H+ SOD H2O2 + O2
Secara fisiologis tubuh menghasilkan senyawa radikal bebas melalui proses fosforilasi oksidatif. Selama proses ini, O2 akan tereduksi menjadi H2O dengan penambahan 4 elektron, sehingga terbentuk radikal anion superoksida dengan yang kemudian diubah menjadi hidrogen peroksida (H2O2) oleh enzim SOD. Proses fosforilasi dalam mitokondria menyebabkan satu molekul O2 tereduksi oleh 4 elektron bersama-sama ion H+ membentuk dua molekul H2O. Jika jumlah elektron yang mereduksi O2 kurang dari 4. proses fosforilasi berlangsung tidak sempurna
sehingga akan terbentuk senyawa radikal bebas (Mc. Cord and Fridovich, 2006; Goodsell, 2007; Murray, et.al., 2009).
Gambar 2.2 Peran SOD pada stres oksidatif (Zainuri dan Septelia, 2012) Kondisi hipoksia pada hewan coba menyebabkan terbentuk nya ROS seperti radikal super oksida (O2•), enzim MnSOD mengubah menjadi H2O2 dan katalase mengubah hidrogen peroksida menjadi air. Antioksidan endogen yang dapat menangkap dan menguraikan radikal bebas di dalam sel menjadi zat yang kurang reaktif, disajikan pada Gambar 2.2 (Zainuri and Septelia, 2012).
2.2.2 Antioksidan Non Enzimatis
Antioksidan non-enzimatis banyak ditemukan dalam sayuran dan buah-buahan. Komponen yang bersifat antioksidan dalam sayuran dan buah-buahan meliputi vitamin C, E, β-karoten, flavonoid, isoflavon, antosianin, katekin, dan
isokatekin (Kahkonen, et al., 1999), serta asam lipoat (Andreassen, et al.,2001). Klopotek, et.al. (2005) menyatakan bahwa kandungan vitamin C dan senyawa fenolik pada buah strawberi yang sudah mengalami pengolahan (prossesing) mengalami penurunan yang cukup signifikan. Hal ini mengakibatkan aktivitas antoksidan pada produk segar lebih tinggi dibandingkan dengan produk olahan. Penelitian yang dilakukan oleh Indriati, et.al. (2002) menyatakan bahwa buah jambu mete yang mengalami penundaan pengolahan mengakibatkan penurunan senyawa polifenol yang dapat menurunkan aktifitas antioksidannya.
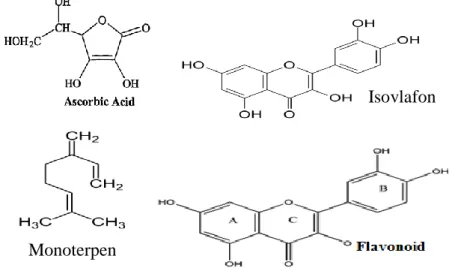
Gugus aktif yang umum berfungsi sebagai penangkap dan penghambat reaksi radikal bebas selanjutnya adalah gugus-gugus –OH dan ikatan rangka dua (>C=C<) Karena gugus-gugus ini dapat memberikan 1 molekul hidrogennya sehingga ROS menjadi stabil dan terbentuk radikal bebas baru yang kurang reaktif. Contoh senyawa antioksidan yang merupakan metabolit sekunder (senyawa fitokimia) dari tanaman dapat dilihat pada Gambar 2.3 (Winarsi, 2007).
Gambar 2.3 Berbagai senyawa antioksidan (Winarsi, 2007) Isovlafon
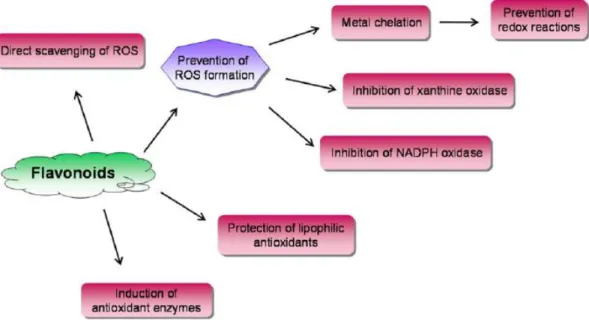
Flavonoid adalah sekelompok besar senyawa polifenol tanaman yang tersebar luas dalam berbagai bahan makanan dan dalam berbagai konsentrasi. Lebih dari 4000 jenis flavonoid telah teridentifikasi dan beberapa di antaranya berperan dalam pewarnaan bunga, buah dan daun. Flavonoid dapat memberikan efek antioksidan dengan cara mencegah terbentuknya ROS, langsung menangkap ROS, melindungi antioksidan lipofilik dan merangsang terjadinya peningkatan antioksidan enzimatik (Winarsi, 2007).
2.2.2.1 Flavonoid
Flavonoid adalah sekelompok besar senyawa polifenol tanaman tersebar luas dalam berbagai bahan makanan. Lebih dari 4000 jenis flavonoid telah diidentifikasi, dan beberapa diantaranya berperan dalam pewarnaan bunga, buah, dan daun (Winarsi, 2007). Flavonoid juga ditemukan dalam Dewandaru, wortel, jeruk, brokoli, kol, mentimun, bayam, tomat, merica, dan terung. Secara in vitro, senyawa flavonoid telah terbukti mempunyai efek biologis yang sangat kuat. Sebagai antioksidan, flavonoid dapat menghambat penggumpalan keping-keping sel darah, merangsang produksi nitrit oksida yang dapat melebarkan (relaksasi) pembuluh darah, dan dapat menghambat pertumbuhan sel kanker. Aktivitas antiperoksidatif flavonoid ditunjukkan melalui potensinya sebagai pengkelat Fe (Afanas, et al., 1989; Morel, et al., 1993).
Antioksidan senyawa fenol dan flavonoid dapat menghambat reaksi oksidasi lemak atau molekul lainnya dalam tubuh dengan cara menyerap,
menangkap dan menetralisir radikal bebas atau mendekomposisi peroksida (Zheng and Wang, 2009). Netralisir ini dilakukan dengan cara memberikan satu elektronnya pada saat reaksi inisiasi atau propagasi sehingga menjadi radikal yang kurang reaktif. Netralisasi dapat juga terjadi pada saat reaksi terminasi radikal menjadi senyawa-senyawa yang lebih stabil. Adanya hambatan ini menyebabkan reaksi-reaksi radikal bebas berakhir atau stress oksidatif tidak terjadi pada sel. Hal ini didukung oleh penelitian yang dilakukan (Praveen, et al., 2007; Aziatul, et al 2016) menyatakan bahwa kandungan senyawa fenol dan flavonoid pada ekstrak buah mengkudu mempunyai aktivitas antioksidan yang tinggi secara in vitro dan in vivo.
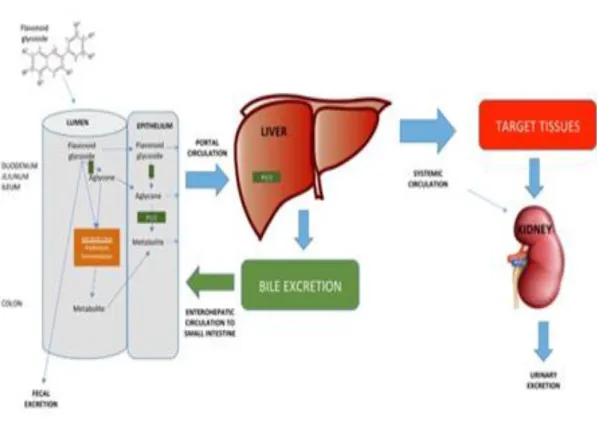
Farmakokinetik dan farmakodinamika flavonoid pada Gambar 2.4, Penyerapan flavonoid yang dibebaskan dari makanan tergantung pada sifat fisikokimia seperti ukuran molekul, konfigurasi, lipofilisitas, kelarutan, dan pKa. Flavonoid dapat diserap dari usus halus tergantung pada struktur flavonoid, yaitu apakah itu glikosida atau aglikon. Sebagian besar flavonoid, kecuali subkelas katekin, hadir dalam tumbuhan yang terikat pada gula sebagai β-glikosida . Aglikon dapat dengan mudah diserap oleh usus halus, sedangkan flavonoid glikosida harus diubah menjadi bentuk aglikon (Day, A.J., 2000; Cassidy and Anne., 2017). Absorbsi setelah pemberian oral dari 0 sampai lebih dari 50% dari dosis pemberian. Waktu paruh eliminasi pemberian intravena dan oral adalah 0,7 dan 2,4 jam (Graefe, et al., 1999).
Gambar 2.4 Metabolisme Flavonoid (Cassidy and Anne, 2017)
Setelah penyerapan, flavonoid terkonjugasi di hati dengan glukuronidasi, sulfasi, atau metilasi atau dimetabolisme menjadi senyawa fenolik yang lebih kecil (Bravo, L., 1998). Karena reaksi konjugasi ini, tidak ada aglikon flavonoid bebas yang dapat ditemukan dalam plasma atau urine, kecuali katekin. Bergantung pada sumber hayati bioavailabilitas flavonoid tertentu sangat nyata; Misalnya, penyerapan kuersetin dari bawang adalah empat kali lipat lebih besar dari pada apel atau the (Hollman, 2004). Flavonoid disekresikan dengan empedu di usus dan tidak dapat diserap dari usus halus terdegradasi di usus besar dengan mikroflora usus yang juga memecah struktur cincin flavonoid (Cassidy and Anne., 2017).
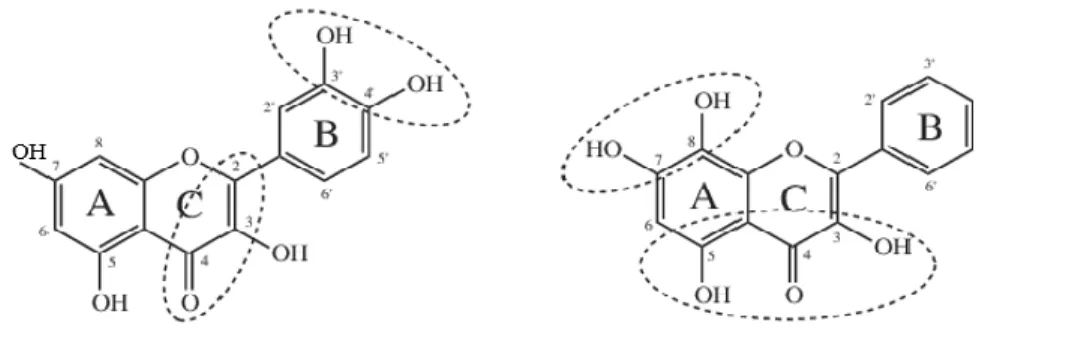
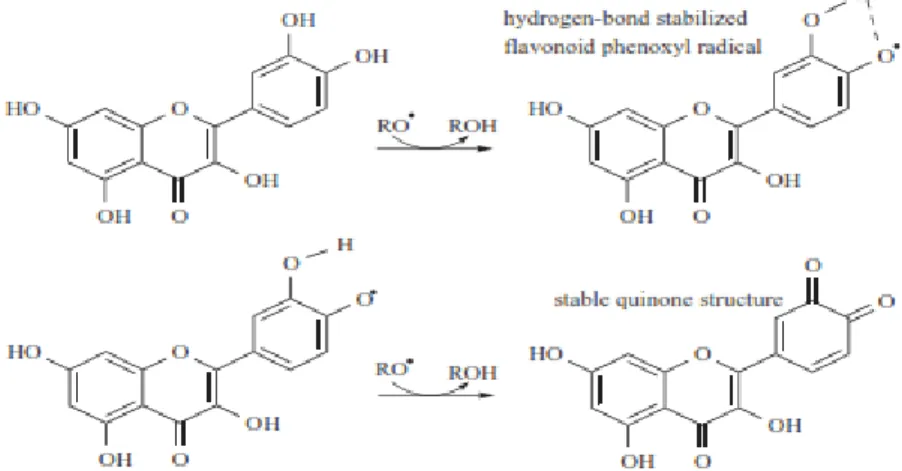
Flavonoid memiliki banyak sifat biokimia, namun sifat terbaik dari hampir setiap kelompok flavonoid adalah kemampuan mereka untuk bertindak sebagai antioksidan. Aktivitas antioksidan flavonoid tergantung pada pengaturan kelompok fungsional tentang struktur kimia. Konfigurasi, substitusi, dan jumlah gugus hidroksil secara substansial mempengaruhi beberapa mekanisme aktivitas antioksidan seperti penangkap radikal dan kemampuan kelat ion logam ( Kumar, S and Pandey, 2013). Konfigurasi cincin B hidroksil adalah penentu paling signifikan untuk penangkap ROS dan RNS karena menyumbangkan hidrogen dan elektron ke radikal hidroksil, peroksil, dan peroksinitrit, menstabilkannya dan membentuk flavonoid radikal yang relatif stabil (Cao, et al.,1997).Struktur hidroksil pada cincin B memberikan atom hidrogen membentuk flavonoid-radikal, dengan memperluas delokalisasi elektron sehingga lebih stabil. Kehadiran 3-OH dan 5-OH, keduanya memaksimalkan penangkapan dan penyerapan radikal bebas, seperti terlihat pada gambar 2.5 (Dragan, et al., 2007)
Mekanisme kerja antioksidan dapat mencakup (1) menekan pembentukan ROS baik dengan penghambatan enzim atau dengan mengkelat unsur-unsur yang terlibat dalam generasi radikal bebas; (2) menangkap ROS; dan (3) perlindungan pertahanan antioksidan (Halliwel, 1998; Mishra., A., et al., 2013). Sebagian besar mekanisme kerja flavonoid melibatkan mekanisme yang disebutkan di atas. Beberapa efek yang dimediasi oleh gabungan hasil aktivitas penangkapan radikal dan interaksi dengan fungsi enzim. Flavonoid menghambat enzim yang terlibat dalam pembentukan ROS, yaitu monooxygenase mikrosomal, glutathione S-transferase, suksinoksidase mitokondria, oksidase NADH (Brown, et al., 1998).
Flavonoid dapat memberikan efek antioksidan dengan cara mencegah terbentuknya ROS, langsung menangkap ROS, melindungi antioksidan lipofilik dan merangsang terjadinya peningkatan antioksidan enzimatik seperti yang disajikan dalam Gambar 2.6.(Akhlaghi, et al., 2009).
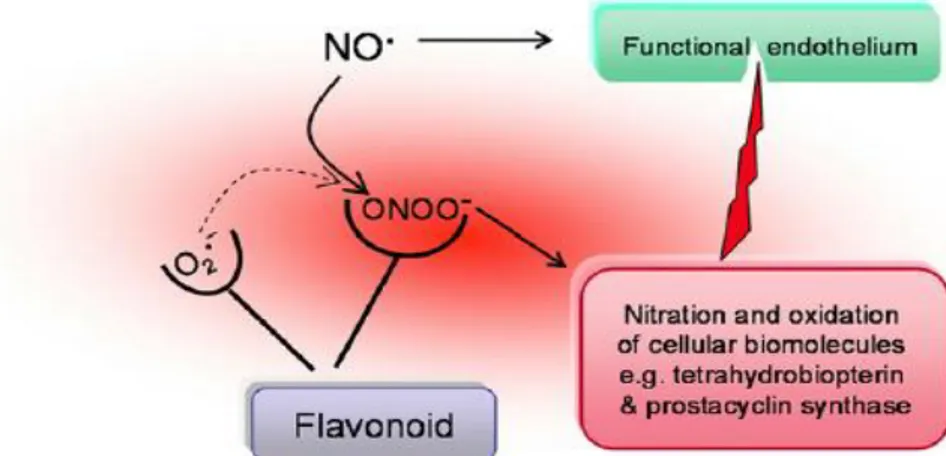
Flavonoid dapat menangkap secara langsung superoksida peroksinitrit. Proses penangkapan superoksida, flavonoid dapat meningkatkan bioavailabilitas NO dan menghambat pembentukan peroksinitrit yang merusak vacorelaxation
endothelium dan mengganggu endothelium, sehingga pada akhirnya menyebabkan
sirkulasi darah yang lebih baik dalam arteri koroner , seperti pada gambar 2.7 (Akhlaghi, et.al.,2009).
Gambar 2.7 Pengaruh Flavonoid terhadap radikal •NO (Akhlaghi, et al.,2009) Mekanisme flavonoid sebagai antioksidan dapat langsung menangkap radikal bebas, mengkelat ion logam dan menghambat enzim pembetukan radikal bebas (Dragan, et al., 2007, Kumar and Pandey, 2013) seperti yang disajikan pada Gambar 2.8.
Gambar 2.8 Mekanisme Flavonoid menangkap radikal bebas (Dragan, et al., 2007, Kumar and Pandey, 2013)
Gambar 2.9. Mekanisme Flavonoid mengkelat logam (Dragan, et al., 2007, Kumar and Pandey, 2013)
Flavonoid dapat memberikan efek antioksidan dengan cara mencegah terbentuknya ROS, langsung menangkap ROS, melindungi antioksidan lipofilik dan merangsang terjadinya peningkatan antioksidan enzimatik . Flavonoid dapat menangkap secara langsung superoksida dan peroksinitrit, Melalui penangkapan superosida, flavonoid dapat secara langsung dapat menangkap peroksinitrit yang merusak vascorelaxation endotelium dan mengganggu endotelium, sehingga pada akhirnya menyebabkan sirkulasi darah yang lebih baik dalam arteri koroner
(Akhlaghi, et al, 2009). Peningkatan antioksidan endogen oleh flavonoid telah terbukti dalam penelitian in vitro melalui peningkatan transkripsi Nrf2 yang meningkatkan ekspresi protein HO-1 (Maher and Hanneken, 2005). Peran flavonoid terhadap antioksidan endogen tergantung dari jenis flavonoid, Flavonoid dapat mengaktifkan ERK (extracelluler signal-regulated protein kinase), JNK (c-Jun N-terminal kinase) dan p38. Flavonoid meningkatkan ekspresi mRNA yang selanjutnya mengaktifkan Nrf2 sehingga terjadi peningkatan gen antioksidan endogen.
2.3 Malondihaldehide
Malondialdehid adalah senyawa organik dengan rumus CH2(CHO)2, struktur senyawa ini lebih komplek dari pada rumusnya, senyawa reaktif ini hasil alami dan penanda dari stress oksidatif. Malondialdehid merupakan senyawa yang sangat reaktif yang tidak biasanya diamati dalam bentuk murni. Di laboratorium dapat dihasilkan dengan hidrolisis dari 1,1,3,3-tetramethoxypropane, yang tersedia secara komersial. (Nair et al, 2008). Reaktif oksigen spesies mendegradasi lemak tak jenuh membentuk malondihaldehid. Senyawa ini merupakan aldehida reaktif dan merupakan salah satu dari banyak senyawa elektrofil reaktif yang menimbulkan stres toksik dalam sel dan bentuk protein kovalen yang disebut produk lipoxidation sebagai hasil akhir (Farmer dan Davoine, 2007). Produk aldehid ini digunakan penanda tingkat stress oksidatif dari suatu organisme (Del Rio et al., 2005). Malondialdehid bereaksi dengan deoxyadenosine dan deoxyguanosine dalam DNA, membentuk komplek DNA yang mutagenik. (Marnett, 1999). Analisis
malondihaldehid dan zat reaktif tiobarbiturat lain membentuk kondensasi yang setara dengan dua asam tiobarbiturat menghasilkan warna merah derivatif yang bisa diamati dengan spektrofotometer (Botsoglou,1994).
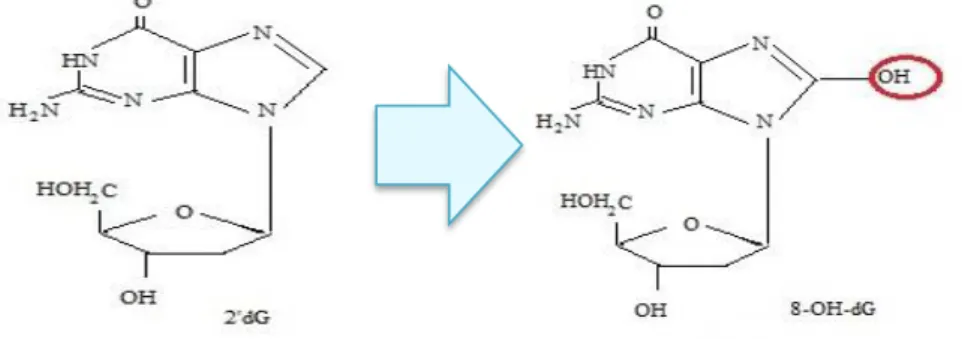
2.4 8OHdG
Delapan hidroksi-2-dioksiguanosin merupakan basa nukleosida yang telah dimodifikasi , pada umumnya 8-hidroksi-2-dioksiguanosin diketahui sebagai hasil samping dari kerusakan DNA yang diekskresi dalam serum DNA repair. Pada saluran kemih 8-OHdG dan analog nya 8-hidroksiguanin, dapat dikaitkan dengan penyakit degeneratif. Asosiasi ROS dan penggunaan 8-OHdG sebagai biomarker stress oksidatif telah diselidiki dalam berbagai penyakit termasuk kandungan kemih dan kanker prostat (Dorall, et al, 2012).
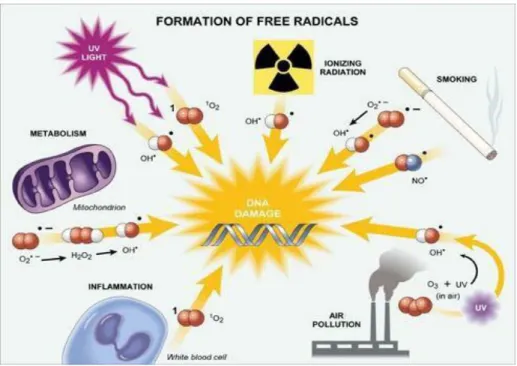
Gambar 2.10 Sumber radikal bebas yang menyerang DNA (Vasudevan and Sreekumari,2004)
Berdasarkan bukti eksperimental bahwa kerusakan oksidatif permanen terjadi pada lipid membran seluler, protein dan DNA. DNA mitokondria, 8-hidroksi-2-dioksiguanosin (8-OHdG) adalah salah satu bentuk dominan dari radikal bebas yang disebabkan lesi oksidatif, dan telah banyak digunakan sebagai biomarker untuk stress oksidatif dan karsinogenesis, Gambar 2.9 (Vasudevan and Sreekumari, 2004). Studi menunjukkan bahwa 8-OHdG adalah biomarker untuk penilaian resiko berbagai kanker dan penyakit degeneratif. Biomarker 8-OHdG atau 8-oxodG telah menjadi penanda penting untuk mengukur dampak kerusakan oksidatif endogen pada DNA dan sebagai faktor inisiasi dan promosi karsinogenesis dan juga digunakan untuk memperkirakan kerusakan DNA pada manusia setelah terpapar agen penyebab kanker, seperti asap tembakau, serat asbes, logam berat, dan hidrokarbon aromatik polisiklik (Cheng, et al., 2006).
Gambar 2.11 Mekanisme Reaksi Pembentukkan Senyawa 8-OHdG (Chabowska, et al., 2009)
Arsen mempunyai peran penting dalam penyebab kanker pada manusia, pada lingkungan industri. Terdapat sebuah hipotesis bahwa arsen memacu
terbentuk nya ROS yang berperan pembentukan 8-hidroksi deoksiguanosin, seperti pada Gambar 2.11 (Chabowska, et al., 2009)
2.5 F2 Isoprostan
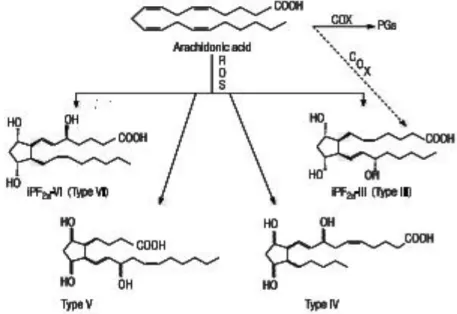
Morrow pada tahun 1990, menemukan substansi isoprostan dalam tubuh manusia yang menyerupai prostaglandin , yang kemudian dinamakan F2-isoprostane. F2-isoprostan merupakan suatu metabolit hasil peroksidasi asam arakhidonat oleh radikal bebas, melalui mekanisme yang di katalisir langsung oleh radikal bebas (free radical-calatyzed mechanism) dan tidak bergantung pada peranan enzim cyclooxygenase, disajikan pada Gambar 2.11 (Pilacik, et al.,2002). F2-IsoP ini memiliki struktur kimia yang cukup stabil, dibentuk pada tempat serangan dari radikal bebas, kemudian segera bersirkulasi dalam darah dan diekskresikan melalui urin (Cracowski, et al., 2003).
Gambar 2.12 Jalur Biosintesis Metabolisme Asam Arahidonat melalui Free
Dibandingkan dengan yang lainnya bentuk F2-IsoP merupakan yang paling banyak terdapat dalam plasma ( Fam and Morrow, 2003; Farooqui and Horrock, 2007). F2-IsoP mempunyai empat isomer, yaitu seri 5, 8, 12, dan 15. Seri 8 atau 8-isoprostan, merupakan isomer F2-IsoP yang paling banyak dihasilkan dan merupakan F2-IsoP yang paling banyak diteliti. Sifat dari molekul F2-Isoprostan yaitu stabil, kuat, dan dapat dideteksi melalui berbagai cairan tubuh seperti urin, plasma, atau cairan serebrospinal (Aschner and Milatovic, 2009). Hingga saat ini F2-IsoP,merupakan petanda yang dianggap sebagai petanda lipid peroksidasi in vivo yang paling baik, baik pada manusia maupun pada binatang, yang secara signifikan lebih akurat dan stabil daripada senyawa lainnya (Dalle-Donne, et al ., 2006). Pengukuran F2-IsoP sebagai marker stres oksidatif mempunyai beberapa keuntungan dibandingkan dengan metode lain karena F2-IsoP secara kimia stabil, hasil spesifik dari peroksidasi, terbentuk in vivo, terdeteksi pada jaringan dan cairan, naik secara substansial pada model binatang dengan jejas oksidan, tidak dipengaruhi oleh jumlah lemak dalam makanan dan sensitif terhadap dosis antioksidan (Montuschi et al., 2004).
2.6 Stres Oksidatif
Stres oksidatif merupakan suatu kondisi ketidakseimbangan antara produksi radikal bebas dengan antioksidan, di mana kadar radikal bebas lebih tinggi dibandingkan antioksidan. Kondisi tersebut dipengaruhi oleh faktor internal seperti genetik, umur, oksidasi fosforilasi, proses patofisiologi, dan faktor eksternal seperti
olahraga berlebih, asupan makanan, patogen, sinar ultraviolet, dan bahan kimia (Waris and Ahsan, 2006).
Faktor internal utama yang menimbulkan stres oksidatif adalah oksidasi fosforilasi akibat melakukan aktivitas fisik maksimal. Selama akvifitas fisik, terbentuk radikal bebas bersamaan dengan reaksi oksidasi fosforilasi untuk membentuk energi (ATP) dalam mitokondria. Dalam reaksi tersebut dibutuhkan oksigen di mana oksigen akan bereaksi dengan hidrogen untuk membentuk air, tetapi sejumlah oksigen dapat berubah menjadi radikal bebas (Marciniak, et al.,2009).
2.7 Aktivitas Fisik maksimal
Latihan fisik (exercise) dan aktivitas fisik (physical activity) sering digunakan secara tertukar, tetapi istilah ini bukan merupakan sinonim. Aktivitas fisik adalah setiap pergerakan tubuh yang dihasilkan oleh kontraksi dari otot rangka yang menyebabkan terjadinya penggunaan energi yang lebih tinggi dari pada saat istirahat. Sedangkan latihan fisik adalah bentuk dari aktivitas fisik yang didefinisikan sebagai pergerakan tubuh yang direncanakan , terstruktur, dan repetitif yang dilakukan untuk meningkatkan atau memelihara satu atau lebih dari komponen-komponen kebugaran fisik (physical fitnes). Physical fitnes secara khusus di definisikan sebagai sekumpulan karakteristik yang dimiliki atau dicapai oleh seseorang yang berhubungan dengan kemampuan untuk melakukan aktivitas fisik (Haskell, et al., 2007).
Pelatihan fisik merupakan suatu gerakan fisik atau aktivitas mental yang dilakukan secara sistematis dan berulang-ulang (repetitif) dalam jangka waktu (durasi) lama, dengan pembebanan yang meningkat secara progresif dan individual, yang bertujuan untuk memperbaiki sistim serta fungsi fisiologis tubuh agar pada waktu melakukan aktivitas olahraga dapat mencapai penampilan yang optimal (Nala, 2011). Kegiatan berolahraga dapat meningkatkan konsumsi oksigen (VO2), yang digunakan untuk menghasilkan energi berupa ATP, melalui proses fosforilasi oksidatif dalam mitokondria. Dalam proses ini oksigen akan tereduksi menjadi air, namun sekitar 4-5% oksigen akan berubah menjadi senyawa oksigen reaktif atau ROS yang terjadi pada rantai transport elektron pada membran dalam mitokondria (Sutarina & Edward, 2004). Aktivitas fisik yang berlebihan dapat meningkatkan konsumsi oksigen menjadi 100-200 kali lipat karena terjadi peningkatan metabolisme dalam tubuh. Hal ini disebabkan oleh kontraksi otot, yang dapat menyebabkan terjadinya peningkatan kebocoran elektron dari mitokhondria menjadi ROS (Reactive Oxygen Species) (Clarkson & Thomson, 2000 ; Sauza et al, 2005). Latihan fisik maksimal meningkatkan stres oksidatif di dalam darah dan otot berupa lipid peroksidasi berupa pentana, malondihaldehida, isoprostan, dan 8OHdG (Maria and Priscilla, et al., 2003)
Proses terjadinya peningkatan radikal bebas akibat latihan fisik berlebih disebabkan oleh (Miyazaki, et al., 2000) :
1. Selama latihan fisik berlebih, seluruh tubuh mengkonsumsi oksigen (VO2) menjadi 20 kali lebih besar dibandingkan pada saat istirahat. Bahkan di dalam
otot, peningkatan konsumsi oksigen dapat mencapai 100 - 200 kali lebih besar dibandingkan saat istirahat. Mitokondria adalah tempat utama pembentukan spesies oksigen reaktif (SOR) selama latihan melalui jalur transpor elektron. akibatnya akan terbentuk radikal bebas superoksid.
2. Radikal superoksida (O2^) secara cepat akan direduksi menjadi hidrogen peroksida (H2O2) oleh enzim superoksid dismutase dalam mitokondria.Bila molekul H2O2 bereaksi dengan logam transisi seperti Fe+ dan Cu+ (reaksi Fenton atau reaksi Haber-Wess) akan meningkatkan pembentukan radikal hidroksil (*OH) yang merupakan senyawa paling reaktif dan berbahaya. 3. Kondisi hipoksia relatif yang terjadi di dalam organ hati, ginjal dan usus
disebabkan redistribusi aliran darah ke otot yang bekerja. Keadaan ini akan menyebabkan aktivasi xantin oksidase dengan reduksi satu elektron oksigen sehingga akan meningkatkan pembentukan radikal superoksida (O2.). Pada aktivitas fisik berlebih akan mengaktifkan jalur xanthin oksidase ini. Konsentrasi hypoxanthin dan xanthin dalam darah meningkat setelah latihan yang intensif.
4. Neutrofil dan respon inflamasi
Neutrofil berperan penting dalam pertahanan jaringan dari invasi virus dan bakteri. Neutrofil akan bermigrasi pada tempat injuri yang ditarik oleh faktor kemotaktik yang dihasilkan oleh sel yang rusak dan melepaskan dua faktor utama selama fagositosis yaitu lysozim dan radikal superoksida (O2^). Lysosome memfasilitasi kerusakan protein sedangkan radikal superoksida (O2^) dihasilkan oleh myeloperoksidase dan NADPH oksidase.Walaupun respon inflamasi ini adalah mencegah infeksi bakteri dan virus,senyawa oksigen
reaktif (SOR) dan oksidan lainnya yang dilepaskan dari neutrofil juga dapat menyebabkan kerusakan sekunder seperti peroksidasi lipid.
2.8 Reaktif Oksigen Spesies (ROS)
Sering kali pengertian radikal bebas disamakan dengan oksidan karena keduanya memiliki kemiripan sifat yakni agresivitas untuk menarik elektron di sekelilingnya. Setiap radikal bebas adalah oksidan, tetapi tidak setiap oksidan adalah radikal bebas. Oksidan adalah senyawa penerima elektron atau suatu senyawa yang dapat menarik elektron (electron acceptor) seperti ion ferri yang berubah menjadi ferro (Fe 3+ + e ^ Fe 2+). Sedangkan, radikal bebas merupakan atom atau molekul yang mempunyai satu atau lebih elektron yang tidak berpasangan. Molekul ini sangat reaktif dan akan menyerang molekul stabil di dekatnya sehingga menjadi radikal bebas (Winarsi,2007). Dengan demikian maka radikal bebas akan memicu terjadinya reaksi berantai. Ada dua bentuk umum dari radikal bebas yaitu ROS dan reactive nitrogen species (RNS). Termasuk ROS di antaranya ion
superoxide (O2_•), hydrogen peroxide (H2O2), hydroxyl radical (OH•), dan peroxyl
radical (OOH•). Sementara RNS sering dianggap sebagai subklas dari ROS, di
antaranya nitic oxide (NO), nitrous oxide (N2O), peroxynitrite (NO3-), nitroxyl anion (HNO) dan peroxynitrous acid (HNO3-) (Marciniak, et al., 2009).
Reactive oxygen species dapat terbentuk sebagai produk samping selama
reaksi oksidasi fosforilasi dalam rantai transpor elektron pada mitokondria. Fosforilasi oksidatif bertujuan untuk membentuk energi dalam bentuk ATP. Pembentukan ATP tersebut membutuhkan O2, tetapi tidak semua O2 berikatan
dengan hidrogen untuk membentuk air, sekitar 4% - 5% berubah menjadi radikal bebas (Figueiredo et al., 2008; Marciniak et al., 2009). Dengan demikian, maka oksigen hanya mampu menerima elektron tahap demi tahap dan hanya satu elektron tiap tahapnya. Pemindahan elektron yang tidak sempurna tersebut mengakibatkan terbentuknya ROS (Winarsi, 2007). Elektron pertama mereduksi oksigen untuk membentuk anion superoxide, kemudian reduksi berikutnya membentuk hydrogen
peroxide dan hydroxyl radical, elektron terakhir mereduksi hydroxyl radical.
2.9 Radikal Bebas
Radikal bebas adalah molekul, atom atau gugus yang memiliki 1 atau lebih electron yang tidak berpasangan pada kulit terluarnya sehingga sangat reaktif dan radikal seperti misalnya radikal bebas turunan oksigen reaktif (Reactive Oxygen
Species). Radikal bebas cukup banyak jenisnya tapi yang keberadaannya paling
banyak dalam sistem biologis tubuh adalah radikal bebas turunan oksigen atau
reactive oxygen species (ROS) (Sadikin,2002 ; Murray, et.al.,2009).
Radikal-radikal bebas ini merupakan hasil pemecahan hemolitik dari ikatan kovalen suatu molekul atau pasangan elektron bebas suatu atom. ROS merupakan bagian dari hasil metabolisme sel normal atau sel yang terpapar zat-zat lain yang menyebabkan terjadinya inflamasi atau peradangan. ROS sebagian besar merupakan hasil dari respon fisiologis (ROS endogen) yaitu hasil metabolisme sel normal dan sebagian kecil merupakan hasil paparan dari luar tubuh (ROS eksogen)
yaitu oksigen reaktif yang berasal dari polutan lingkungan, radiasi, infeksi bakteri, jamur dan virus (Sadikin, 2002 ; Murray, et.al., 2009).
ROS terdiri dari superoksida (•O₂), hidroksil (•OH), peroksil (ROO•), hidrogen peroksida (H₂O₂), singlet oksigen (•O₂), oksida nitrit (NO•), peroksinitrit (ONOO•) dan asam hipoklorit (HOCl). Radikal bebas yang paling banyak terbentuk didalam tubuh adalah superoksida. Superoksida ini akan diubah menjadi hidrogen peroksida (H₂O₂). Hidrogen ini dalam tahap propagasi akan diubah menjadi radikal hidroksil (•OH). Radikal hidrosil inilah yang menyebabkan terjadinya peroksidasi lemak pada membran sel sehingga sel mengalami kerusakan, (Sadikin, 2002 ; Murray, et.al., 2009).
Radikal bebas dapat berada di dalam tubuh karena adanya hasil samping dari proses oksidasi dan pembakaran sel yang berlangsung pada waktu bernafas, metabolisme sel, olahraga yang berlebih, peradangan, dan terpapar polusi (asap kendaraan, asap rokok, makanan, logam berat, dan radiasi matahari). Radikal bebas akan bereaksi dengan molekul sel di sekitarnya untuk memperoleh pasangan elektron sehingga menjadi lebih stabil, tetapi molekul sel tubuh yang diambil elektronnya akan berubah menjadi radikal bebas. Reaksi ini akan berlangsung terus menerus dalam tubuh dan bila tidak dihentikan akan menimbulkan stress oksidatif yang menyebabkan suatu peradangan, kerusakan DNA atau sel dan berbagai penyakit seperti kanker, jantung, katarak, penuaan dini, serta penyakit degeneratif lainnya, seperti yang ditunjukkan dalam Gambar 2.12 (Akhlaghi, et al., 2009)
Gambar 2.12 Pengaruh ROS dan RNS terhadap kesehatan manusia (Akhlaghi, et.al., 2009)
Akibat begitu besarnya pengaruh radikal bebas terhadap kesehatan manusia maka tubuh memerlukan suatu asupan yang mengandung suatu senyawa yaitu antioksidan yang mampu menangkap dan menetralisir radikal bebas tersebut sehingga reaksi-reaksi lanjutan yang menyebabkan terjadinya stres oksidatif dapat berhenti dan kerusakan sel dapat dihindari atau indikasi suatu penyakit dapat dihentikan (Sibuea, 2003). Reaksi terminasi antioksidan biasanya menangkap radikal hidroksil (•OH) pada tahap reaksi peroksidasi lemak protein atau molekul lainnya pada membran sel normal sehingga kerusakan sel dapat dihindari (Sadikin, 2002 ; Murray, et.al., 2009)
Keberadaan radikal bebas tidak selamanya merugikan tubuh manusia akan tetapi ada juga yang mempunyai efek yang menguntungkan, seperti membantu destruksi sel-sel mikroorganisme, kanker dan proses pematangan sel-sel di dalam tubuh. Leukosit memproduksi radikal bebas untuk memusnahkan gingival, ligamen periodontal dan tulang alveolar dengan cara merusak DNA, menganggu produksi prostaglandin dan merangsang pembentukan sitokin proinflamasi seperti IL-6 dan
TNF-α. Akan tetapi produksi radikal bebas yang berlebihan dan produksi antioksidan yang tidak memadai dapat menyebabkan kerusakan sel-sel jaringan dan enzim-enzim. Kerusakan jaringan dapat terjadi akibat gangguan oksidatif yang disebabkan radikal bebas asam lemak atau dikenal sebagai peroksidasi lipid (Zheng dan Wang, 2009 ; Murray, et. al 2009).
Reaksi-reaksi radikal di dalam tubuh merupakan penyebab atau mendasari berbagai keadaan patologis suatu penyakit. Diantara senyawa-senyawa ROS, radikal hidroksil (•OH) merupakan radikal bebas yang yang paling reaktif atau berbahaya karena mempunyai tingkat reaktivitas sangat tinggi. Radikal hidroksil (•OH) dapat merusak tiga jenis senyawa yang penting mempertahankan ketahanan sel yaitu :
1. Asam lemak tak jenuh (PUFA) yang merupakan komponen penting fosfolipid penyusun membran sel.
2. DNA, yang merupakan piranti genetik dari sel
3. Protein, yang memegang berbagai peran penting seperti enzim, reseptor, antibodi, dan pembentukan matriks serta sitoskeleton (Fessenden and Fessenden, 1999 ; Sadikin, 2002 ; Murray ,et.al., 2009)
Regulasi jumlah radikal bebas secara normal dalam sistem biologis tubuh dilakukan oleh enzim-enzim antioksidan endogenous seperti enzim superoksida dismutase (SOD), katalase dan glutation peroksidase (GPx). Pengukuran radikal bebas di dalam tubuh sangat sulit dilakukan karena radikal bebas bereaksi sangat cepat sehingga seringkali dilakukan pengukuran tidak langsung melalui produk
turunannya seperti malondialdehida (MDA) dan 4-hidroksinonenal. Kedua senyawa tersebut sering digunakan untuk pengukuran reaksi radikal bebas lipid (Fessenden and Fessenden, 1999 ; Sadikin, 2002 ; Murray , et.al., 2009).
2.10 n-Butanol
n-Butanol atau n-butil alkohol atau normal butanol adalah alkohol primer dengan struktur 4-karbon, dan memiliki rumus kimia C4H9OH. Isomernya antara
lain isobutanol, 2-butanol, dan tert-butanol. Sifat kimia fisika, tak berwarna , bentuk cair, bau mirip amil alkohol , titik didih 117,70C, dapat campur dengan banyak pelarut organik seperti, sangat larut dalam aseton, dapat campur dengan etanol dan etil eter. Pada suhu 250C dapat larut 63200 mg/L air. (Haynes, W.M, 2014)
2.11 Kapasitas Antioksidan
Aktivitas antioksidan menggambarkan kemampuan suatu senyawa antioksidan untuk menghambat laju reaksi pembentukan radikal bebas. Penentuan kapasitas antioksidan secara invitro ditentukan secara spektroskopi UV-Vis. Eksplorasi senyawa fitokimia terutama senyawa bioaktif yang terdapat pada tanaman obat atau bukan tanaman obat secara terus menerus diteliti untuk mendapatkan senyawa antioksidan yang berfungsi menjaga kesehatan tubuh manusia dari serangan penyakit (Prakash, 2001).
Pengujian aktivitas antioksidan harus didasari atas efek farmakologis dari zat tersebut diantaranya adalah :
rekombinan
2. Menangkap ion logam yang diperlukan untuk tujuan katalisis reaksi oksidasi oleh radikal bebas seperti deferoksamin
3. Menangkap (scavenging) atau memutus reaksi rantai (chainbreaking) dari radikal bebas seperti vitamin C, E, β-karoten dan senyawa fenol (flavonoid)
4. Menghambat aktivitas enzim-enzim yang terlibat dalam pembentukan radkal bebas seperti allopurinol
2.11.1 Pengukuran Kapasitas Antioksidan secara in vitro
Beberapa metode pengukuran kapasitas antioksidan secara in vitro yang digunakan dewasa ini adalah beta karoten bleaching, 1,1 Dhifenyl-2-
Picrrylhydrazyl (DPPH Radical Scavenging) method, Thiobarbituric
Acid-Reactive-Subtances (TBARS) assay, Oxygen Radical Absorbance Capacity
(ORAC) assay, Total Radical-Trapping Antioxidant Parameter (TRAP) dan
Ferric Reducing/Antioxidant Power (FRAP) assay, Trolox Equivalent
Antioxidant Capacity (TEAC) method, Peroxyl Radical Scavenging (PSC) dan
Total Oxyradical Scavenging Capacity (TOCS) method dan Folin-Ciocalteau
Total Phenolic Assay dan lain-lain (Zou, et al., 2004).
Klopotek, et. Al., (2005) menyatakan bahwa metode FRAP assay dan TEAC assay yang digunakan untuk mengukur perubahan aktivitas antioksidan buah strawberi segar dan olahannya memberikan hasil yang tidak jauh berbeda. Penelitian yang dilakukan oleh Gill, et al. (2002) menghasilkan
bahwa aktivitas antioksidan pada buah plum menggunakan FRAP assay lebih tinggi (40.0 mg) sampai dengan 127.2 mg ekivalen vitamin C) dibandingkan pengukuran dengan DPPH Radical Scavenging Method (27.4 mg sampai dengan 61.1 mg ekivalen vitamin C). Penelitian lain juga menunjukkan bahwa analisis aktivitas antioksidan menggunakan Total Phenolic Assay dan FRAP assay memiliki hubungan positif yang sangat kuat (R2 = 94.8%) antara daun , batang, dan ekstrak buah tanaman Momordica charantia L (Kubola and Siriamornpun, 2008).
2.11.2 Pengukuran Akvititas Antioksidan secara invivo
Wolfe, et.al., (2007 ; 2008) menyatakan bahwa disamping analisis in vitro, perlu dilakukan pengukuran aktivitas antioksidan secara in vivo pada hewan coba yang selanjutnya diterapkan pada sukarelawan manusia agar didapatkan efikasi actual antioksidan tersebut di dalam tubuh.
Hewan coba yang biasa digunakan dalam menetukan aktivitas antioksidan secara in vivo adalah mencit dan tikus. Dalam penelitian ini peneliti menggunakan tikus sebagai hewan coba karena beberapa alasan dan beberapa penelitian sebelumnya yaitu (Ridwan, 2013) :
1. Keragaman dari subyek penelitian dan dapat diminimalisasi karena secara genetic hampir sama atau identik.
2. Variabel penelitian lebih mudah dikontrol, karena tikus ini secara genetik mirip, patuh dan secara cepat beradaptasi dengan lingkungannya sehingga mudah dikendalikan dari umur, jenis kelamin, berat badan,
kenyamanannya, kesehatan, makanan dan minuman.
3. Pemilihan jenis hewan dapat disesuaikan dengan kepekaan hewan terhadap materi penelitian yang dilakukan.
4. Biaya relatif murah karena harga tikus, makanan dan minuman relatif murah.
5. Mendapatkan informasi lebih mendalam dari penelitian yang dilakukan karena karakteristik genetic, biologi, kelengkapan organ, kebutuhan nutrisi, metabolisme biokimia dan perilaku sangat mirip dengan manusia sehingga kita dapat membuat sediaan biologi dari organ hewan yang digunakan.
6. Memperoleh data maksimum untuk keperluan penelitian simulasi. 7. Dapat digunakan untuk uji keamanan, diagnostik dan toksisitas.