*Corresponding author: Jurusan Kimia FMIPA UNSRAT, Jl. Kampus Unsrat, Manado, Indonesia 95115; Email address: wuntudenny@yahoo.com
Published by FMIPA UNSRAT (2015)
dapat diakses melalui http://ejournal.unsrat.ac.id/index.php/jmuo
Analisis
Beberapa
Asam
Organik
pada
Nira
Aren
Menggunakan HPLC Fasa Terbalik Kolom YMC Triart C
18Sitti R. Limo
a*, Julius S. Pontoh
a, Audy D. Wuntu
aa
Jurusan Kimia, FMIPA, Unsrat, Manado
K A T A K U N C I A B S T R A K Nira Aren
Asam Organik HPLC Fasa Terbalik
Metode HPLC fasa terbalik dengan kolom YMC Triart C18 dapat
digunakan untuk pemisahan dan perhitungan konsentrasi asam organik pada nira aren. Metode analisis HPLC ini dilakukan pada suhu kolom 400C
dan dideteksi pada panjang gelombang 210 nm dengan kalium dihidrogen fosfat (pH 2.8) sebagai fase gerak. Sampel yang diuji pada penelitian ini adalah nira aren yang diperoleh dari daerah kota Tomohon. Penentuan asam-asam organik dalam nira aren dilakukan menggunakan asam-asam standard asam malat, asam askorbat, asam laktat, asam asetat, asam sitrat, asam piroglutamat, dan asam fumarat. Ketujuh asam organik ini terdeteksi dalam sampel nira aren. Akan tetapi, keberadaan asam organik tersebut bergantung pada kondisi nira itu sendiri karena nira aren mudah mengalami fermentasi. Perhitungan konsentrasi asam organik pada nira aren menggunakan kurva standard dan diperoleh konsentrasi asam organik yang tertinggi dalam nira aren adalah asam malat yaitu 0.198 g/100mL untuk sampel A dan 0.774 g/100mL untuk sampel B.
K E Y W O R D S A B S T R A C T
Palm juice Organic acid
Reverse phase HPLC
Reverse phase HPLC method using YMC Triart C18 can used to
separating and calculating concentration of organic acid in palm juice. This method did on 40 0C column temperature and detected on wavelength
210 cm with potassium dihydrogen phosphate (pH 2.8) as a mobile phase. Sample which tested on this research is palm juice with getted from Tomohon city. Determining of organic acids on palm juice did used standard acids such as malic acid, ascorbic acid, lactic acid, acetic acid, citric acid, pyroglutamic acid and fumaric acid. This seventh organic acids was detected on the palm juice sample, but the presence of its organic acid was dependent on condition of the palm juice its self, because the palm juice can fermenting easily. Calculating of concentration of organic acid on palm juice used standard curve and getted the highest concentration of organic acid was malic acid that is 0.198 g/100 mL for sample A and 0.774 g/100 mL for sample B.
AVAILABLE ONLINE 10 Februari 2015
1. Pendahuluan
Asam organik adalah senyawa organik yang memiliki gugus karboksil (Theron dan Lues, 2010). Asam organik dapat diklasifikasikan berdasarkan tipe rantai karbon (alifatik, alisiklik, aromatik, atau heterosiklik), kejenuhan, substitusi, dan nomor gugus fungsinya (Gomis, 2000). Keasaman dari suatu senyawa organik ditentukan oleh nilai pKa dari senyawa tersebut. Semakin kecil nilai pKa dalam
senyawa organik, sehingga semakin tinggi tingkat keasamannya.
Nira aren dihasilkan dari tanaman aren dan merupakan salah satu produk yang popular di Indonesia. Nira sering dijadikan sebagai bahan baku dalam pembuatan gula aren dan minuman beralkohol (Itoh et al., 1982). Nira mudah mengalami fermentasi yang dapat meningkatkan kandungan asamnya (Marsigit, 2005).
HPLC (High Performance Liquid Chromatography) adalah metode analisis yang banyak dilaporkan untuk analisis asam organik. Teknik HPLC dibedakan atas fase normal (menggunakan pelarut nonpolar sebagai fase gerak), fase terbalik (menggunakan pelarut polar sebagai fase gerak) dan penukar ion (menggunakan gradient konsentrasi ion dalam fase geraknya). Analisis asam organik dalam buah-buahan telah dilaporkan oleh Nour et al. (2010) menggunakan HPLC fase terbalik dengn kolom C18
sebagai fase diam dengan larutan fosfat 50 mM sebagai fase gerak, juga telah dilaporkan oleh Ergonul dan Nergiz (2010) analisis buah zaitun dengan kolom penukar ion dan asam fosfat 0.1 %(w/v) sebagai fase gerak dan Itoh et al. (1982) melaporkan analisis asam organik pada nira aren menggunakan kromatografi penukar ion dengan asam fosfat 0.05% sebagai fase gerak. Namun demikian, Itoh et al. (1982) melakukan persiapan sampel yang lebih kompleks dengan mengekstraksi nira menggunakan metode soxlet.
2. Metode 2.1. Bahan dan Alat
Brix meter, HPLC merek Shimadzhu, UV-VIS detector SPD- 20A, pompa LC-20AD, oven kolom CTO- 20A, Kolom YMC Triart C18, pH meter, Alat-alat gelas
secara umum pyrex, Schott Duran, pipet, mikropipet, alumunium foil, botol serum, neraca elektrik, hot plate, magnetic stirrer, labu ukur 100 mL dan 1000 mL.
Nira aren yang diperoleh dari daerah kota Tomohon dengan waktu pengambilan Juli 2014 sebagai sampel A dan Oktober 2014 sebagai sampel B, kalium dihidrogen fosfat, akuades, asam fosfat, asam asetat 10 %, asam sitrat, asam askorbat, asam malat, asam laktat 10%, asam piroglutamat, asam fumarat, whatman membrane filter PTFE 0.2 µm dan membrane filter 0.45 µm.
2.2. Penyiapan sampel
Nira yang diperoleh dari kota tomohon dievaporasi pada suhu 100 0C hingga nilai brix
mencapai 22 0brix yang diukur menggunakan
brixmeter. Pembuatan sampel 22 0brix dilakukan
untuk mengawetkan nira. Nira yang dianalisis ada dua yaitu sampel A yang diperoleh dari daerah kota tomohon dengan waktu pengambilan Juli 2014 dan sampel B dengan waktu pengambilan Oktober 2014. 2.3. Pembuatan Kurva Standar Asam Organik Asam Malat
Disiapkan larutan stok asam malat konsentrasi 2% (dengan melarutkan asam malat sebanyak 2 g dalam 100 mL buffer fosfat). Selanjutnya disiapkan 3 buah botol vial, masing-masing diisi dengan asam stok sebanyak 0.1 mL, 0.25 mL dan 2.5 mL, selanjutnya ditambahkan dengan larutan fosfat hingga 5 mL dan disimpan pada suhu ± 4 0C selama
proses penelitian. Dari konsentrasi asam organik standar, dibuat kurva standar (Luas area vs konsentrasi).
Asam Laktat
Disiapkan larutan stok asam laktat konsentrasi 1% yaitu dengan menambahkan 10 mL asam laktat (10%) kedalam 90 mL bufer fosfat, selanjutnya disiapkan 3 buah botol vial, masing-masing diisi dengan asam stok sebanyak 0.2 mL, 1 mL, dan 2 mL, selanjutnya ditambahkan dengan larutan fosfat hingga 5 mL dan disimpan pada ± 4 0C selama proses
penelitian. Dari konsentrasi asam organik standar, dibuat kurva standar (Luas area vs konsentrasi). Asam Asetat
Disiapkan larutan stok asam asetat konsentrasi 1% yaitu dengan menambahkan 10 mL asam asetat (10%) kedalam 90 mL bufer selanjutnya disiapkan 3 buah botol vial, masing-masing diisi dengan asam stok sebanyak 0.5 mL, 1 mL, dan 2 mL, selanjutnya ditambahkan dengan larutan fosfat hingga 5 mL dan disimpan pada suhu ± 4 0C selama proses penelitian.
Dari konsentrasi asam organik standar, dibuat kurva standar (Luas area vs konsentrasi).
Asam Sitrat
Disiapkan larutan stok asam sitrat konsentrasi 0.1% (dengan melarutkan asam sitrat sebanyak 0.1 g dalam 100 mL buffer fosfat). Selanjutnya disiapkan 4 buah botol vial, masing-masing diisi dengan asam stok sebanyak 0.2 mL, 0.5mL, 1 mL, dan 3 mL, selanjtnya ditambahkan dengan larutan fosfat hingga 5 mL dan disimpan pada suhu ± 4 0C selama proses
penelitian. Dari konsentrasi asam organik standar, dibuat kurva standar (Luas area vs konsentrasi). Asam Piroglutamat
Disiapkan larutan stok asam Piroglutamat konsentrasi 0.1% (dengan melarutkan asam piroglutamat sebanyak 0.1 g dalam 100 mL buffer fosfat). Selanjutnya disiapkan 4 buah botol vial, masing-masing diisi dengan asam stok sebanyak 0.1 mL, 0.5mL, 1 mL, dan 2 mL, selanjutnya ditambahkan dengan larutan fosfat hingga 5 mL dan disimpan pada suhu ± 4 0C selama proses penelitian. Dari
konsentrasi asam organik standar, dibuat kurva standar (Luas area vs konsentrasi).
Asam Fumarat
Disiapkan larutan stok asam Fumarat konsentrasi 0.1% (dengan melarutkan asam Fumarat sebanyak 0.1 g dalam 100 mL buffer fosfat). Selanjutnya disiapkan 4 buah botol vial, masing-masing diisi dengan asam stok sebanyak 0.01 mL, 0.02mL, 0.1 mL, dan 0.2 mL, selanjutnya ditambahkan dengan larutan fosfat hingga 5 mL dan disimpan pada suhu ± 4 0C selama proses penelitian..
Dari konsentrasi asam organik standar, dibuat kurva standar (Luas area vs konsentrasi).
Asam askorbat
Disiapkan larutan stok Asam askorbat konsentrasi 0.4% (dengan melarutkan Vtamin C sebanyak 0.4 g dalam 100 mL buffer fosfat). Selanjutnya disiapkan 4 buah botol vial, masing-masing diisi dengan asam askorbat stok sebanyak 0.1 mL, 0.5 ml , 1 mL, dan 2.66 mL selanjutnya
ditambahkan dengan larutan fosfat hingga 4 mL dan disimpan pada suhu ± 4 0C selama proses penelitian.
Dari konsentrasi asam organik standar, dibuat kurva standar (Luas area vs konsentrasi).
2.4. Analisis HPLC (Nour et al., 2010)
Standar asam organik dan sampel nira aren dianalisis dengan kromatografi fasa terbalik menggunakan kolom YMC Triat C18 250 x 4.6 mm i.d ,
dan dibaca pada = 210 nm. Sebelum diinjeksi ke dalam HPLC, standar asam organik dan sampel disaring terlebih dahulu dengan membrane filter 0.2 µm.
Analisis ini dilakukan pada kondisi isokratik pada suhu 40 0C dengan menggunakan larutan fosfat 50
mM sebagai fasa gerak (melarutkan 6.8 g kalium dihidrogen fosfat dalam 900 mL air, nilai pH diatur dengan menambahkan asam fosfat hingga pH 2.8 menggunakan pH meter, lalu ditambahkan dengan air hingga 1000 mL), selanjutnya disaring dengan membrane filter 0.45 µm. Laju alir fasa gerak diatur 0.7 mL/menit. Sebelum dilakukan injeksi, alat harus distabilkan terlebih dahulu.
3. Hasil dan Pembahasan 3.1. Nilai Brix Nira Aren
Tabel 3 menampilkan nilai brix dari kedua sampel nira. Sebelum dianalisis, nira aren dievaporasi sehingga brix mencapai 22 0brix.
Pembuatan 22 0brix pada nira aren juga dilakukan
agar supaya puncak dalam kromatogram yang dihasilkan mudah terbaca.
3.2. Kromatografi Asam-Asam Organik Melalui Kolom YMC Triart C18
Kromatogram campuran asam-asam organik standar ditampilkan pada Gambar 11. Kromatogram
dari campuran asam-asam organik inilah yang digunakan untuk analisis beberapa senyawa organik dalam nira aren yang dilihat berdasarkan perbedaan waktu retensinya (tr).
Tabel 1 – Nilai brix nira aren
Nira Aren Brix awal Brix akhir Sampel A (Juli 2014) 13 0brix 22 0brix
Sampel B (Oktober 2014)
13 0brix 22 0brix
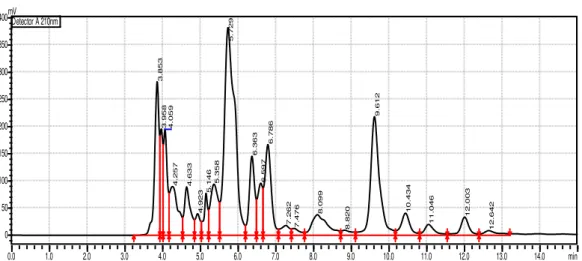
Campuran dari asam-asam organik standar ini dibuat dengan mencampurkan asam malat sebanyak 0.5 mL, asam laktat 1mL , asam asetat 1mL , asam sitrat 2mL , asam piroglutamat 1mL dan asam fumarat sebanyak 0.1mL. Perbedaan jumlah volume untuk pembuatan campuran asam standar ini diperhitungkan berdasarkan tinggi puncak yang diperoleh dari konsentrasi tertentu, tinggi puncak yang digunakan yaitu 200-500 mV, agar supaya diperoleh kromatogram campuran asam standar dengan tinggi puncak yang hampir sama (Gambar 1).
Dari Gambar 1 terlihat bahwa luas area dari asam fumarat sangat besar sekalipun konsentrasinya lebih kecil (0.1 mL) dari asam organik lainnya. Hal ini menunjukkan bahwa asam fumarat lebih sensitif dibandingkan asam organik lainnya. Sedangkan tingkat sensitifitas yang paling rendah adalah asam sitrat, yang menunjukkan luas area dan puncak yang lebih rendah, sedangkan konsentrasi yang digunakan lebih besar (2 mL) dibandingkan asam organik lainnya.
Gambar 1 – Kromatogram campuran asam organik standar
3.2. Analisis Asam-Asam Organik dalam Nira Aren Sampel A
Kromatogram dari sampel A ditampilkan pada Gambar 2 (ulangan 1) dan 3 (ulangan 2). Pada kedua kromatogram ini, terdapat beberapa puncak yang menunjukkan keberadaan asam organik yang dilihat berdasarkan waktu retensi dari asam-asam organik standar. Kromatogram sampel A1 (Gambar 2) menunjukkan kehadiran asam malat (tr 5.729), asam
askorbat (tr 6.597), asam laktat (tr 7.262), asam
asetat (tr 8.099), dan asam piroglutamat (tr 9.612).
Sedangkan untuk kromatogram sampel A2 (Gambar 3) terdeteksi asam malat (tr 5.949), asam askorbat (tr
6.681), asam laktat (tr 7.245), asam sitrat (tr 8.442),
asam piroglutamat (tr 9.672) dan asam fumarat (tr
10.129). . Selain itu, kromatogram pada sampel A juga terdapat beberapa peak yang masih berimpitan
Sample ID:1 0.0 1.0 2.0 3.0 4.0 5.0 6.0 7.0 8.0 9.0 10.0 11.0 12.0 13.0 14.0 min 0 250 500 750 1000 1250 1500 mV Detector A 210nm 5 .7 1 0 7 .3 1 2 8 .0 4 8 8 .4 7 4 9 .6 3 5 1 0 .0 9 4
yang menunjukkan metode yang digunakan belum optimal sehingga perlu dikembangkan lebih lanjut.
Perbedaan jenis puncak antar sampel A1 dan A2 mungkin disebabkan oleh perubahan yang terjadi
dalam sampel nira aren karena pengujian sampel A1 dan A2 dilakukan pada hari yang berbeda.
Gambar 2 ‒ Kromatogram sampel A1(ulangan 1)
Gambar 3 ‒ Kromatogram sampel A2 (ulangan 2)
3.3. Nira Aren Sampel B
Gambar 4 dan 5 menunjukkan kromatogram dari sampel B. Dapat dilihat berdasarkan asam organik standar yang ada, terdapat beberapa asam organik yang terdapat dalam sampel B dengan ulangan 1 dan 2. Sampel B1(ulangan 1) yaitu terdapat asam malat (tr 5.773), asam askorbat (tr 6.667), asam sitrat (tr
8.501) dan asam piroglutamat (tr 9.689). Sedangkan
asam organik yang terdeteksi pada sampel B2 (ulangan 2) yaitu asam malat (tr 5.758), asam laktat
(tr 7.183) dan asam Fumarat (tr 9.900). Perbedaan
kandungan asam organik pada kedua kromatogram sampel B tersebut mungkin disebabkan terjadi perubahan dalam sampel B2 (sedikit terfermentasi).
Pada kromatogram B1 (Gambar 4), asam askorbat terdeteksi pada waktu retensi 6.667 sedangkan waktu retensi untuk asam askorbat pada asam standar adalah 6.5. untuk itu dilakukan spike, dengan menambahkan asam askorbat kedalam sampel B1 dan diperoleh kromatogram yang
menunjukkan tinggi puncak meningkat pada menit ke 6.6, sehingga dapat dipastikan bahwa asam askorbat pada sampel B1 terdeteksi dengan tr 6.667.
Pada nira jenis ini (sampel B), asam malat adalah asam organik dalam nira yang memiliki puncak yang paling tinggi. Pada kromatogram sampel B juga terdapat beberapa puncak yang belum diketahui jenis senyawanya diantaranya adalah puncak dengan waktu retensi 3.843, 6.422, 9.181, dan 10.559 dan perlu juga dianalisis lebih lanjut menggunakan GCMS.
3.4. Konsentrasi asam organik dalam nira aren Konsentrasi asam organik yang terdapat dalam nira aren dihitung menggunakan kurva standar dari asam organik . Dilihat dari koefisien korelasi dari asam-asam organik yang dibuat, diperoleh kurva yang cukup linear. Konsentrasi asam organik yang terdapat dalam nira aren dapat dilihat pada Tabel 4. Dari kedua jenis nira aren yang dianalisis, diperoleh konsentrasi asam organik tertinggi adalah asam Sample ID:1 0.0 1.0 2.0 3.0 4.0 5.0 6.0 7.0 8.0 9.0 10.0 11.0 12.0 13.0 14.0 min 0 50 100 150 200 250 300 350 400mVDetector A 210nm 3 .8 5 3 3 .9 5 8 4 .0 5 9 4 .2 5 7 4 .6 3 3 4 .9 2 3 5.1 4 6 5 .3 5 8 5 .7 2 9 6 .3 6 3 6 .5 9 7 6 .7 8 6 7 .2 6 2 7 .4 7 6 8 .0 9 9 8 .8 2 0 9 .6 1 2 1 0 .4 3 4 1 1 .0 4 6 1 2 .0 0 3 1 2 .6 4 2 0.0 1.0 2.0 3.0 4.0 5.0 6.0 7.0 8.0 9.0 10.0 11.0 12.0 13.0 14.0 min 0 50 100 150 200 250 300mVDetector A 210nm 3 .8 4 4 4 .0 5 4 4 .4 4 8 4 .7 3 2 5 .2 7 2 5 .6 1 1 5 .9 4 9 6 .3 5 3 6 .6 8 1 6 .8 5 8 7 .2 4 5 8 .8 5 3 1 0 .5 7 9 1 1 .3 2 9
malat yaitu 0.198 g/100 mL untuk sampel A dan 0.774 g/100 mL untuk sampel B.
Perhitungan konsentrasi asam oganik dalam sampel yang dicantumkan dalam Tabel 4, hanya sebagian yang merupakan konsentrasi rata-rata darisampel ulangan 1 dan ulangan 2. Karena dari
kedua ulangan yang diuji menghasilkan kromatogram dengan jenis puncak yang sedikit berbeda karena perubahan yang terjadi pada nira selama proses penelitian.
Gambar 4 ‒ Kromatogram sampel B ulangan
Gambar 5 ‒ Kromatogram sampel B ulangan 2
Tabel 2 ‒ Konsentrasi beberapa asam organik dalam nira aren
Asam standar Sampel A (g/100mL) Sampel B (g/100mL)
Asam Malat 0.198 0.774 Asam askorbat 0.029 0.121 Asam Laktat 0.104 - Asam Asetat 0.002 - Asam Sitrat 0.0038 0.003 Asam Piroglutamat 0.0117 0.0097 Asam Fumarat - 0.29 4. Kesimpulan
Berdasarkan tujuh standar asam organik yang digunakan, semuanya terdeteksi dalam nira aren
menggunakan HPLC fase terbalik dengan kolom YMC Triart C18.
Konsentrasi asam organik dalam sampel A nira aren adalah 0.198 dan 0.774 g/100mL untuk asam malat, 0.029 dan 0.121 g/100mL untuk asam Sample ID:1 0.0 1.0 2.0 3.0 4.0 5.0 6.0 7.0 8.0 9.0 10.0 11.0 12.0 13.0 14.0 min 0 250 500 750 1000 mV Detector A 210nm 3 .8 4 3 3 .9 6 8 4 .6 1 0 5 .0 2 6 5 .7 7 3 6 .4 2 2 6 .6 6 7 7 .4 0 0 7 .5 6 8 8 .5 0 1 9 .1 8 1 9 .6 8 9 10.5 5 9 1 2 .3 4 1 1 2 .7 3 8
Sample Name:Nira Brix 22 Ulangan
0.0
1.0
2.0
3.0
4.0
5.0
6.0
7.0
8.0
9.0
10.0
11.0
12.0
13.0
14.0
min
0
250
500
750
1000
mV
Detector A 210nm
1 . 6 2 8 3 . 8 4 8 3 . 9 9 4 4 . 0 5 5 4 . 5 7 7 4 . 9 1 2 5 . 0 1 1 5 . 3 7 0 5 . 7 5 8 6 . 4 4 6 7 . 1 8 3 7 . 4 3 6 8 . 8 5 9 9 . 9 0 0 1 0 . 6 4 8 1 1 . 7 0 6 1 2 . 1 5 1 1 2 . 7 9 7 1 3 . 5 2 7 1 4 . 8 4 2askorbat, 0.104 g/100mL untuk asam laktat, 0.002 g/100mL untuk asam asetat, 0.0038 g/100mL dan 0.003 g/100mL untuk asam sitrat, 0.0117 g/100mL dan 0.0097 g/100mL untuk asam piroglutamat, dan 0.29 g/100mL untuk asam fumarat. Dan sampel B adalah 0.774 g/100mL untuk asam malat, 0.121 g/100mL untuk asam askorbat, 0.003 g/100mL untuk asam sitrat, 0.0097 g/100mL untuk asam piroglutamat, dan 0.29 g/100mL untuk asam fumarat.
Terdapat beberapa puncak yang belum teridentifikasi apakah sebagai senyawa organik atau bukan sehingga metode ini masih perlu dioptimalkan.
Daftar Pustaka
Agilent Technologies, Inc. 2014.Fundamentals of
Liquid Chromatography
(HPLC).http://polymer.ustc.
edu.cn/xwxx_20/xw/201109/P0201109062630 97048536.pdf#page=21&zoom=auto,-45,12 [1 Juni 2014 ]
Ardianingsih, R. 2009. Penggunaan High Performance Liquid Chromatography
(HPLC) dalam Proses Analisa Deteksi Ion. Berita Dirgantara. 10: 101- 104
Clark, J. 2007. Kromatografi Cair Kinerja Tinggi
(HPLC).
http://www.chem-is-try.org/materi_kimia/instrumen_analisis/kromato grafi1/kromatografi_cair_kinerja_tinggi_hplc/ [ 21 Mei 2014 ].
Day R. A. Jr., and Underwood A.L. 2001. Analisis Kimia Kuantitatif. Erlangga, Jakarta.
Ergonul, P. G., and C. Nergiz. 2010. Determination of Organic Acids in Olive Fruit by HPLC. Czech Journal Food Science.28: 202- 205
Fessenden, R. J., and J. S. Fessenden. 1986. Kimia Organik. Edisi ke-3. Erlangga, Jakarta.
Gomis, D. B. 2000. HPLC Analysis of Organic Acids. Di dalam : Nollet, L. M. L. (ed). Food Analysis by HPLC. CRC Press, New York
Haard, N. F., and G. W. Chism. 1996. Characteristics of Edible Plant Tissues. Di dalam: Fennema, O.R. Food Chemistry. CRC Press, New York
Itoh, T., C. H. Widjaja, A. Matsuyama, M. Z. Nasution, and J. Kumendong. 1982. Compositional Characteristics of Nira- Palm Juice of High Sugar Content from Palm Tree. Di dalam: Agricultural Production and Processing Tecnology. Proceeding of IPB-JICA International Synposium, Bogor.Hlm 233- 240.
Lempang, M. 2012. Pohon Aren dan Manfaat Produksinya.Info Teknis EBONI.9: 37- 54.
Marsigit, W. 2005.Penggunaan Bahan Tambahan pada Nira dan Mutu Gula Aren yang Dihasilkan di beberapa Sentra Produksi di Bengkulu.Jurnal Penelitian Universitas Bengkulu.11: 42- 48 Nour, V., I. Trandafir, and M. E. Ionica, 2010.HPLC
Organic Acid Analysis in Different Citrus Juices under Reversed Phase Condition.Notulae Botanicae Horti Agrobotanici Cluj-Napoca.1: 44- 48
Samudra, A. A. 2011. Strategi Pengembangan Agribisnis Aren ( Arengapinnata) di Kecamatan Mungka Kabupaten Lima Puluh Kota. Fakultas Pertanian Universitas Andalas, Padang.
Shepard, L. 2012. Relating Sensory and Chemical Properties to Consumer Acceptance of Sour Cream : Organic Acid [ thesis]. Faculty of North Carolina State University, North Carolina
Theron, M. M., and J. F. R. Lues. 2010. Organic Acids and Food Preservation. CRC Press, New York. Weikle, K. 2012. Determination of Citric Acid in Fruit
Juices Using HPLC. Concordia College Journal of Analytical Chemistry. 3: 57-62