DIKTAT KULIAH
BIOKIMIA
Oleh:
Eddy Sulistyowati, Apt., M.S.
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS NEGERI YOGYAKARTA
KATA PENGANTAR
Diktat kuliah ininmerupakan kumpulan hand out kuliah Biokimia yang telah dipergunakan sejak tahun 1992 hinga tahun 2009 dengan telah mengalami perbaikan dan penyempurnaan dengan mengambil dari berbagai sumber sebagai referensi.
Tentu saja masih belum sempurna, namun untuk kepentingan pendidikan Biokimia bagi mahasiswa kependidikan maupun non kependidikan dirasa telah cukup sebagai bekal awal dalam mempelajari Biokimia lanjut.
Harapan kami semoga diktat ini bermanfaat dan sumbang saran pembaca sangat diharapkan, dan penulis menerimanya dengan senang hati sehingga diktat ini akan lebih sempurna lagi.
Terimakasih kepada Mbak Indri Pahalaning W., S.Si., dan Mbak Murniagus W, S.Si. yang telah membantu terselesaikannya diktat ini.
KARBOHIDRAT
Karbohidrat = sakarida (yunani: gula)
Karbohidrat adalah polihidroksi aldehid/keton dan polimer-polimernya, mengandung C, H, O dan unsur-unsur lain N, P, S.
Klasifikasi karbohidrat 1. Monosakarida
Gula sederhana = monomer → unit tunggal
Rumus umum (CH2O)n , n: 3-10, C: 5-6
Umumnya terdapat di alam
Berdasar gugus keton/aldehid maka dibagi 2, yaitu aldosa dan ketosa Jumlah atom C-nya: 3 atom C disebut treosa aldotreosa
Ketotreosa
Semua monosakarida mempunyai satu atau lebih atom C asimetri
Struktur monosakarida mempunyai satu gugus aldehid (pada atom C no. 1)/keton (pada atom C no.2)
Contoh:
Glukosa, fruktosa
Mempunyai struktur terbuka
Mempunyai struktur tertutup (cincin)
HC O
Beberapa reaksi dari monosakarida
I. Reaksi transformasi enediol dari Lobry De Bruyn.
D. glukosa enediol D. mannosa
HC O
II. Reaksi mereduksi: adanya gugus aktiv C H O
dapat mereduksi ion logam sebagai dasar identifikasi kualitatif dan kuantitatif.
III. Reaksi pembentukan ozazon, bila direaksikan dengan fenil hidrazin.
HC O
D. glukosa D. glukosa Phenil hidrason hasil antara
HC N
CH2OH
D. fruktosa phenil hidrason
N NH C6H5
D. fruktosa phenil ozazon
H
Ozazon akan dihidrolisis oleh Hcl pekat → ozon
HC N
aldehid → ketosa.
HC O
V. Pembentukan asam gula, dengan oksidasi air brom akan terjadi 3 macam asam.
VI. Reaksi asam terhadap monosakarida
Pada umumnya monosakarida relatif stabil dalam asam encer pada pemanasan singkat tetapi untuk ketosa akan mengalami dekomposisi pada pemanasan yang lebih lama.
* Bila (A) diperbesar monosakarida akan mengalami dekomposisi. Contoh: hidroksi metil furfural
VII. Pembentukan glikosida.
Gula sederhana direaksikan dengan alkohol dengan katalisator Hcl. Pada atom C no. 1 ikat OR (hidroksil).
Contoh:
Glikosida saponin : gula + sapogenin Glikosida indican : glukosa + indoxyl Glikosida plorizin : glukosa + ploretin Contoh:
- metil - D. galakto piranosida
Monosakarida yang terdapat banyak di alam bersifat optik aktif.
Contoh paling sederhana gliseraldehida, terdapat 1 pusat khiral, sehingga dapat berbentuk 2 isomer optik yang berbeda. Aldoheksosa mempunyai 4 pusat khiral sehingga dapat berada dalam 2n = 24 = 16 stereo isomer yang berbeda.
Rumus konformasi tersebut dinamakan epimer.
Contoh:
D. glukosa dan D. manosa epimer pada atom C-2 D. glukosa dan D. galaktosa epimer pada atom C-4
CHO
2. Oligosakarida, terdiri beberapa monosakarida, antara lain: Disakarida
Contoh:
Sukrosa, maltosa, laktosa.
Kedua unit monosakarida digabungkan dengan ikatan kovalen yang disebut ikatan glikosida, yaitu gugus hidroksil pada salah satu gula bereaksi dengan karbon anomer pada gula kedua.
Ikatan glikosida segera terhidrolisa oleh asam encer, tetapi tahan terhadap basa, dihasilkan monosakarida bebas.
o Sukrosa
Dibentuk oleh tanaman (tebu, biet, buah-buahan). Merupakan gula paling manis daripada disakarida lain.
Terdiri dari monosakarida a-D. glukopiranosa dengan b-D.
O
Tidak dapat mereduksi, sehingga tidak dapat dioksidasikan Cu++, bila di
200º
kental seperti sirup disebut karamel.
o Maltosa
Disakarida paling sederhana mengandung 2 residu D. glukosa, dihubungkan oleh ikatan glikosida C1-4.
O
Merupakan disakarida pereduksi karena ada OH bebas. Diperoleh dari hasil pemecahan:
pati Amilase
Liur maltosa, bila masuk usus
Maltase
D. glukosa
o Laktosa
Terdapat dalam susu, merupakan gabungan b-D. galaktopiranosa dan b-D. glukopiranosa dengan ikatan 1,4.
O
Merupakan disakarida pereduksi karena terdapat OH bebas.
Dalam proses pencernaan dihidrolisis enzimatik oleh enzim laktase (dari sel mukosa usus) menjadi glukosa dan galaktosa.
Trisakarida : rafinosa (fru-glu-gal); gentianosa (fru-fru-glu). Tetrasakarida : skhiosa (gal-gal-glu-fru)
3. Polisakarida
monosakarida, sebagai unsur struktural dinding sel dan jaringan pengikat). Mengalami hidrolisa sempurna oleh asam/enzim spesifik, hasil: monosakarida. Jika polisakarida terdiri satu jenis unit monosakarida maka disebut homopolisakarida.
Jika polisakarida terdiri 2/lebih unit monosakarida maka disebut heteropolisakarida.
Contoh:
Homopolisakarida → D. glukosa saja → adalah pati.
Heteropolisakarida → 2 unit gula, berganti-ganti → hialuronat pada jaringan pengikat
Polisakarida penyimpan yang pati (pada tanaman) dan glikogen (pada hewan). Pati
Terdiri a amilosa dan amilopektin.
a amilosa merupakan rantai lurus dari D. glukosa dengan ikatan a. 1-4
Amilopektin merupakan rantai bercabang dengan ikatan a. 1-4 dan pada
percabangan dengan ikatan a. 1-6.
O
amilosa ikatan . 1-4
Non pereduksi
rantai utama O
1
6
Glikogen
Merupakan polisakarida utama pada sel hewan, terdiri D. glukosa bercabang dengan ikatan a. 1-4, seperti struktur amilopektin, tetapi
percabangan lebih banyak dan struktur lebih kompak. amilase
hidrolisis
Pati dan glikogen dalam saluran pencernaan mecah ikatan . 1-4 pada cabang luar
Terbentuk D. glukosa + maltosa + dekstrin glukosidase hidrolisis
mecah ikatan cabang . 1-6
Selulosa
Merupakan unsur strukturan ekstra sel pada dinding sel tumbuhan. Sifat: seperti serabut, liat, tidak larut dalam air.
Merupakan homopolisakarida linear tidak bercabang. Terdiri 10 000/lebih unit D. glukosa dengan ikatan b 1-4.
Gambar rantai paralel:
Contoh:
Kayu, katun, kertas.
Kulit udang, kepiting, insekta (polisakarida khitin) Terdiri N-asetil D-glukosamin dengan ikatan b 1-2.
O
OH
OH
NH CH2OH H
C O CH3
1
2
Pada bakteri dinding sel sebelah luar membran sel membentuk pembungkus
yang kuat.
Terdiri polisakarida bercabang diselingi polipeptida
N-asetil D. glukosiamin penta peptida residu glisin
membentuk peptidoglikan
LIPIDA
Adalah kelompok senyawa heterogen yang berkaitan, baik secara aktual maupun potensial dengan asam lemak
Lipid mempunyai sifat umum:
o Relatif tidak larut dalam air
o Larut dalam pelarut non polar: eter, kloroform, benzen
Yang termasuk dalam lipid adalah: lemak, minyak, lilin.
Lipid adalah unsur makanan penting karena nilai energinya yang tinggi, tetapi juga karena vitamin yang larut dalam lemak dan asam lemak esensial yang dikandung dalam lemak makanan alam.
Dalam tubuh lemak berfungsi sebagai sumber energi efisien, secara langsung dan secara potensial, bila disimpan dalam jaringan adiposa.
Kombinasi lemak dan protein (lipoprotein) merupakan unsur sel yang penting, terdapat dalam membran sel dan mitokondria dalam sitoplasma, berfungsi sebagai alat pengangkut lipid dalam darah.
Klasifikasi lipid dikemukakan oleh Bloor:
A. Lipid sederhana: ester asam lemak dengan bermacam alkohol. 1. Lemak dan minyak
Adalah ester asam lemak dengan gliserol. 2. Lilin (waxes)
Adalah ester asam lemak dengan alkohol mono-OH yang mempunyai berat molekul lebih besar.
B. Lipid campuran: ester asam lemak yang mengandung gugus tambahan selain alkohol dan asam lemak.
1. Fosfolipid
Adalah lipid yang mengandung residu asam fosfat sebagai tambahan asam lemak dan alkohol.
Mempunyai basa yang mengandung nitrogen. Contoh:
Pada fosfolipid yakni gliserofosfolipid, alkoholnya gliserol. 2. Glikolipid
Adalah campuran asam lemak dengan karbohidrat yang mengandung nitrogen tetapi tidak mengandung asam fosfat.
Contoh:
Glikosil diasil gliserol ~ terdapat dalam tanaman dan mikroorganisme. 3. Lipid campuran lain
Asam Lemak
Merupakan senyawa penyusun lipida.
Adalah asam karboksilat yang diperoleh dari hidrolisis ester.
Asam lemak terdapat di alam mengandung atom C genap dan merupakan derivat berantai lurus, dapat jenuh/tidak jenuh.
Jumlah atom karbon hampir semua genap dan panjang rantai 14-22. Jumlah asam lemak tak jenuh lebih banyak daripada asam lemak jenuh, dan pada umumnya ikatan ganda pada atom C ke-9 dan 10 dan ikatan ganda tambahan antara sesudah atom C no. 10 kearah gugus metil.
CH3 C C COOH
no 9
10
Bila ikatan ganda lebih dari 1 biasanya dibatasi 1 gugus metilena.
CH CH CH2 CH CH
Asam lemak jenuh, Cn H2n+2 O2, beberapa yang penting: asam palmitat, stearat,
laurat, miristat.
Asam lemak tak jenuh, Cn H2n O2, beberapa yang penting: asam oleat, asam
linoleat, asam linolenat, arachidonat.
Asam lemak tak jenuh di alam jumlah lebih besar daripada asam lemak jenuh. Sifat fisik asam lemak:
o Asam lemak dengan atom C > 4 tidak larut dalam air, tapi dalam pelarut
non polar.
Asam lemak dengan atom C < 4 dapat larut dalam air. Contohnya asam asetat, butirat.
o Asam lemak dalam suasana basa membentuk garam disebut saponus =
sabun. Untuk Na, K → sabun mudah larut di air dan berbusa; untuk alkali tanah, Ca, Mg → sabun tidak mudah larut dalam air dan tidak berbusa.
o Makin pendek atom C, titik cair rendah, makin banyak ikatan ganda, titik
cair rendah.
o Seperti asam karboksilat lain maka:
- mudah diesterkan
- mudah direduksi
- reaksi ikatan ganda → addisi halogen
hidrogenasi/penjenuhan,
isomerisasi/perubahan konformasi oksidasi
Halogenisasi dengan I2 sering dipergumakan sebagai analisa kuantitatif
menentukan derajad kejenuhan.
Peristiwa oksidasi dikenal dengan ransiditas = penengikan, adalah peristiwa dimana lemak mengalami dekomposisi disertai dengan bau tak enak dan merangsang.
C C HC CH2
OH
CH2
C O
Rantai pecah: lebih pendek
Sumber asam lemak jenuh:
1. Asam asetat Atom C 2 Hasil akhir fermentasi karbohidrat pada pemamah biak
2. Asam propionat Atom C 3 Idem no. 1
3. Asam butirat Atom C 4 Dalam jumlah kecil pada mentega dan idem no. 1
4. Asam valerat Atom C 5 Idem no. 3 5. Asam kaproat Atom C 6 Idem no. 3
6. Asam kaprilat Atom C 8 Terdapat dalam mentega - lemak nabati
7. Asam dekanoat (kaproat)
Atom C 10 Idem no. 6
8. Asam laurat Atom C 12 Pada minyak ikan paus, kelapa sawit, minyak kelapa
9. Asam miristat Atom C 14 Pada pala, kelapa sawit, minyak kelapa
10. Asam palmitat Atom C 16 Pada semua lemak hewan dan tumbuh-tumbuhan
11. Asam stearat Atom C 18 Idem no. 10
12. Asam arakidat Atom C 20 Pada minyak kacang tanah 13. Asam behenat Atom C 22 Pada biji-bijian
14. Asam lignoserat Atom C 24 Pada minyak kacang tanah, serebrosida
A. Lipida sederhana = lemak netral = lemak = (tri) asil gliserol = (tri) gliserida. Merupakan ester dari alkohol gliserol dengan (3 mol) asam lemak. Merupakan komponen utama dari lemak penyimpan/depot lemak. Berdasar jumlah asam lemak, ada 3 macam antara lain:
o Monoasil gliserol = monogliserida
H2C
HC
H2C
O C R
O
OH
o Diasil gliserol = digliserida
H2C
HC
H2C
O C R1
O
OH
O C R2
O
o triasil gliserol = trigliserida
H2C
HC H2C
O C R1
O
O C R2
O
O C R3
O
1. Lemak netral berdasar sifat fisika terdiri atas 2 golongan:
o Minyak → cair pada suhu kamar o Lemak → padat pada suhu kamar
* Sifat-sifat asil gliserol suhu cair lemak ditentukan oleh asam lemak → suhu cair
naik bila jumlah atom C dan rantai C makin besar.
o Lemak dari alam biasanya tersusun bermacam-macam asam lemak,
terutama:
Asam lemak jenuh : palmitat, stearat, laurat, miristat. Asam lemak tak jenuh : umumnya oleat.
o Penamaan tergantung asam lemaknya
Misal:
3 asam lemak sama : tri-oleil-glis (lemak tunggal).
3 asam lemak tidak sama : oleil-palmitil-stearil-glis (lemak campuran).
o Penetapan kuantitatif lemak didasarkan pada adanya ikatan-ikatan tak
jenuh
- Nilai saponifikasi
Adalah jumlah KOH yang dibutuhkan untuk mensaponifikasikan 1 gram lemak.
- Nilai iodium
2. Lilin = waxes
Adalah ester asam lemak dengan alkohol bukan gliserol. Lilin merupakan komponen utama dari lilin lebah, sebagai lapis penutup pada kulit, daun, bulu, buah dari tanaman derajad tinggi.
a. Beeswax lilin yang terdapat pada insecta.
Komponen utamanya adalah ester mirisil palmitat C15 H31 COOC 30 H61,
selain itu juga terdapat asam lemak bebas dengan atom C24-C34, juga
monohidroksi alkohol primer dengan atom C24-C34 dan parafin hidrokarbon
dengan atom C25-C31.
b. Carnauba wax lilin yang terdapat dalam tanaman (kutikula daun). Merupakan senyawa kompleks. Asam lemak dan alkohol (C26-C34) dan
parafin hodrokarbon C27.
c. Sperm oil dari ikan paus spermaceti sebagian besar terdiri setil palmitat. d. Lanolin minyak wol, merupakan pelindung dari serat-serat wol. Terdiri
dari campuran ester kholesterol (C27 H45 OH), lanosterol (C30 H49 OH),
agnosterol (C30 H47 OH).
B. Lemak Campuran 1. Fosfolipid = fosfatida
Adalah lipid yang mengandung fosfor yang terikat sebagai ester fosfat → dianggap sebagai derivat asam fosfatidat.
R1
Berikatan dengan senyawa nitrogen: kolin, serin, etanol amin. Fosfolipid ~ terdapat dalam sel tumbuhan/hewan.
Contoh:
Pada hewan di otak, telur, hati, ginjal, pankreas, jantung.
fosfolipid tidak larut dalam aseton, sehingga cara pemisahan dengan
ekstraksi: eter, semua lipis larut, kemudian ditambah aseton → fosfolipid.
R1 C O C
lesitin fosfatidil kolin
Jika:
Alkoholnya bukan gliserol → sphingosin
CH CH C CH CH3OH2
(CH2)12CH CH3
H
OH
NH2
1
2
Contoh:
Pada 1 sphingomielin adalah senyawa paling sederhana dan paling banyak dijumpai, yakni pada hampir semua membran sel terutama sel syaraf.
Strukturnya:
sphingosin - fosfokolin (2)
asam lignoserat (1)
N CH2 CH2 O
P O
HO
O
CH3 (CH2)22 C O OH (CH3)3
Contoh lain: serebrosida
2. Glikolipida
Banyak terdapat dalam tanaman. Strukturnya:
sphingosin - D. galaktosa (2)
PROTEIN
Protein merupakan polipeptida dengan berat molekul besar (paling kecil 8 000-10 000).
Protein dibagi menjadi 2 golongan:
Protein sederhana, hanya mengandung asam amino saja. Contoh: kolagen,protein kontraktil.
Protein kompleks, terdiri asam amino dan non asam amino. Contoh: hem, glikoprotein, lipoprotein.
Klasifikasi protein berdasar: I. Kelarutan
Sejak tahun 1907 sampai sekarang klasifikasi ini tetap digunakan (lihat tabel), tetapi batas antara kelas tidak jelas/tegas.
Pembagian dilihat dari:
Mudah/tidak larut dalam air
Mudah/tidak larut dalam asam/basa Mudah/tidak larut dalam larutan garam Mudah/tidak larut dalam etanol encer/absolut II. Bentuk
Berdasarkan bentuknya protein terdiri: 1. Protein fiber/fibrous/fibrosa.
Molekul bentuk fiber (serat) yang panjang/spiral panjang yang terikat satu dengan yang lain. Banyak terdapat dalam protein hewan, tidak larut dalam air, tahan terhadap enzim proteolitik.
a. Kolagen
Merupakan protein jaringan tubuh, tidak larut dalam air, tahan terhadap pemecahan enzim. Bila dipanaskan dalam air mendidih/asam encer/alkali encer akan menjadi gelatin yang lebih mudah larut dalam air dan mudah dipecah enzim.
Kurang lebih 30% dari protein total dalam hewan mamalia adalah kolagen. Kolagen mengandung hidroksi prolin, hidroksi lisin. Tidak terdapat unsur S, sehingga tidak mempunyai sistein, sistin, triptofan. b. Elastin
Adalah protein yang terdapat dalam urat darah, jaringan elastis (jaringan penghubung).
c. Keratin
2. Protein globular.
Molekul yang berbentuk bulat/lonjong. Rantai polipeptida lipatan dan berbelit. Mudah larut dalam air dan larutan garam dan asam dan basa dan alkohol.
a. Albumin
Terdapat dalam telur, serum darah.
Mudah larut dalam air, muda dikoagulasi bila dipanaskan, dapat diendapkan dengan penambahan (NH4)2 SO4 jenuh.
b. Globulin
Terdapat dalam protein hewani, nabati, terdiri atas glisin yang terkandung di dalamnya dan mudah larut dalam garam netral (Nacl). Dapat dikoagulasi dengan panas dan dapat diendapkan dengan (NH4)2
SO4 jenuh. Ovoglobulin dalam kuning telur diekstraksi dengan larutan
Nacl 5-10% dan diendapkan. c. Histon
Larut dalam air, asam, alkali, garam.
Dengan tidak segera koagulasi
III.Struktur 1. Primer
Menunjukan sekwensi residu-residu asam amino dalam rantai polipeptida yang saling diikat secara kovalen oleh ikatan peptida, dan posisi serta jumlah ikatan disulfida yang membentuk ikatan-ikatan silang di dalam rantai polipeptida/antara 2 rantai polipeptida.
Protein yang pertama kali diteliti dengan lengkap tentang struktur primernya adalah insulin-sapi (oleh F. Sanger 1950). Insulin adalah hormon hasil dari pankreas. Merupakan protein kecil dengan BM = 14 000 terdiri atas 2 rantai. Sanger dapat memisahkan 2 rantai tersebut, dimana rantai A: terdiri atas 21 residu asam amino, rantai B: terdiri atas 30 residu asam amino.
Antara 2 ikatan peptida terdapat 2 ikatan interpeptida di-sulfida, dan 1 ikatan intrapeptida di-sulfida.
2. Sekunder
Ditandai dengan adanya putaran-putaran/belokan dari rantai peptida. Dengan adanya putaran ini dapat terjadi interaksi di dalamnya karena sangat berdekatan, interaksi umumnya ikatan hidrogen yakni antara:
C O H N C
Dengan adanya interaksi maka struktur sekunder mantap dan lebih khas untuk tiap protein.
a heliks (konformasi a), timbul karena putaran dari rantai peptida. Yang
mula-mula ditemukan: protein panjang a keratin, tidak larut dalam air dan
tidak dapat dicernakan.
O
H O
H Dalam rambut dan wool terdiri 3-7 rantai dan membentuk heliks lagi
Ikatan hidrogen:
paralel dengan poros intrapeptida
Lempeng bergelombang (konformasi b)
NH2
COOH COOH
NH2
Ikatan hidrogen tegak lurus pada poros interpeptida
3. Tersier
PENDAHULUAN PROTEIN
Adalah senyawa organik yang terdapat pada kebanyakan sel hewan, merupakan 50% (kira-kira) dari berat sel kering.
Ditemukan di dalam semua sel dan bagian-bagian sel.
Mempunyai berbagai peranan biologis, karena protein merupakan instrumen molekuler yang mengekspresikan informasi genetik.
Semua protein baik berasal dari bakteri, bahkan kehidupan tinggi, dibangun dari rangkaian dasar yang sama yaitu asam amino, yang dikenal ada 20 macam yang berfungsi biologis (disebut juga asam amino baku).
Rangkaian asam amino disebut peptida, dihubungkan oleh ikatan kovalen. Sumber protein: daging, telur, dan lain-lain dalam tubuh manusia. Sedang dalam tumbuhan terdapat dalam biji-bijian palawija, juga buah-buahan.
Klasifikasi protein: protein sederhana dan protein majemuk. Protein sederhana terdiri dari unsur C, H, O, N.
Protein majemuk terdiri dari unsur pokok + gugus prostetik. Misal:
Nukleoprotein, prostetik : asam nukleat Lipoprotein, prostetik : lipida
Khromoprotein, prostetik : 2 warna Struktur umum asam amino
C H2N
COOH
R H
20 macam asam amino mempunyai ciri yang sama: gugus karboksil dan gugus amino diikat pada atom karbon yang sama, masing-masing berbeda pada rantai samping (gugus R) yang bervariasi dalam struktur, ukuran, muatan listrik dan kelarutan dalam air.
Misal:
Alanin Ala A ... non polar
Arigin Arg R ... polar bermuatan positif Asparagin Asn N ... polar
Asam aspartat
Asp D ... polar bermuatan positif
Sistein Cys C ... polar Glutamin Gln Q ... polar Asam
glutamat
Glu E ... polar
Glisin Gly G ... polar bermuatan negatif
Histidin His H
Isoleusin Ile I ... non polar
Leusin Leu L
Lisin Lys K ... polar bermuatan positif Metionin Met M ... non polar
ASAM AMINO DAN PEPTIDA
Makro molekul → dari sel hidup sebagai: struktural, biokatalisataor, hormon,
reseptor, genetik Protein Asam nukleat Polisakarida
Adalah biopolimer terdiri monomer asam amino, nukleotida, gula.
Protein → monomer asam amino → struktur 3 dimensi → asam amino berikatan →
rantai polipeptida.
Asam amino/Asam a amino
Di alam terdapat 300 jenis, yang terpenting 20 jenis sebagai monomer protein. Rumus:
Struktur asam amino pada pH fisiologis
R COOH R C
Ke 20 jenis asam amino aesensial dibedakan dalam 2 golingan:
I. Asam amino dengan gugus R non polar (Ala, Ile, Leu, Met, Phe, Pro, Trp, Val).
Penamaan asam amino mempergunakan singkatan 3 huruf dan lazim dipakai hingga saat ini (lihat tabel).
Selain 20 macam asam amino tersebut terdapat asam amino yang mempunyai fungsi esensial pada proses metabolisme (lihat tabel).
Reaksi kimia asam amino
o Adanya gugus karboksil dengan gugus amino menunjukkan reaksi sesuai
fungsi masing-masing (pembentukan garam, esterifikasi, asilasi).
o Beda asam amino satu dengan yang lain tidak berdasar pada gugus amino
dan gugus karboksil, tetapi dari R.
o Reaksi penunjuk umum untuk semua asam amino adalah ninhidrin →
warna biru sampai ungu, dan warna ini teramati secara kuantitatif (menyerap sinar pada 570 nm) dengan kolorimeter.
o Beberapa reaksi penting untuk asam amino tertentu.
No Reaksi Pereaksi Asam
Asam fosfomolibdo tungstat Tyr Biru
Peptida
Terdiri 2 atom lebih residu asam amino dengan ada 2 ikatan peptida.
Ikatan peptida: ikatan utama dalam protein dan merupakan reaksi terpenting, antara gugus amino dan karboksil dengan membebaskan 1 mol H2O.
Contoh:
Ikatan peptida berbentuk rantai panjang, sebagai ikatan utama.
Struktur peptida ditulis dengan residu asam amino n-terminal (a amino bebas) di
sebelah kiri, dengan residu c-terminal (a karboksil bebas) di sebelah kanan).
Contoh:
Penulisan rumus bangun polipeptida:
1. Gambarkan tulang punggung yang menghubungkan gugus a-NH2, a-COOH,
dan atom a-C. Letaknya berselang-seling, bentuk zig-zag.
Penamaan peptida dihitung jumlah asam aminonya, biasanya sampai 6 peptida. NH2 – Val – Cys – Ala – Phe – Arg – Try – COOH.
Sifat asam basa peptida hampir serupa dengan asam amino.
Gugus NH2 dari peptida dapat bereaksi secara kuantitatif dengan ninhidrin.
Reaksi lain yang khas untuk peptida adalah biuret dapat dilakukan pada senyawa yang mempunyai ikatan peptida minimal 2 ikatan peptida dengan Cu++ → ikatan kompleks dan terjadi warna biru ungu dapat diamati dengan kolorimetri.
Beberapa Pemisahan/isolasi peptida: Elektroforesis
Kromatografi kertas Kromatografi lapis tipis Kromatografi pertukaran ion
ENZIM
Tubuh merupakan laboratorium yang rumit karena di dalamnya terjadi reaksi kimia yang beraneka ragam. Antara lain pemecahan zat-zat yang terdapat dalam makanan, penggunaan hasil pemecahan ini untuk memperoleh energi, dan penggabungan kembali untuk membentuk persediaan makanan dalam tubuh, serta reaksi-reaksi kimia lain tidak mungkin dilakukan secara in vitro ( di laboratorium/luar tubuh). Semua proses tersebut dapat dilakukan dengan baik di dalam tubuh (in vivo) tanpa memerlukan suhu tinggi dan terjadi dalam tempo singkat, ini dikarenakan adanya katalis yang disebut enzim.
Proses peragian/fermentasi menurut Pasteur hanya dapat terjadi dengan adanya sel hidup yang mengandung enzim. Kemudian diubah oleh Buchner setelah terbukti bahwa cairan yang berasal dari ragi tanpa adanya sel hidup dapat menyebabkan terjadi fermentasi gula menjadi alkohol dan CO2. Tahun 1926 Sumner berhasil
isolasi urease dari kacang panjang. Enzim ini mengurai urea → CO2 + NH3.
Tata nama dan kekhususannya
Dalam tubuh manusia terjadi bermacam-macam proses biokimia dan tiap proses reaksi tertentu dibantu oleh enzim tertentu. Untuk membedakannya maka tiap enzim diberi nama. Secara umum setiap enzim dinamai menurut substratnya dengan penambahan kata akhiran ase dibelakangnya.
Contoh:
Urea → urease Arigin → ariginase
Enzim-enzim dengan fungsi sejenis diberi nama menurut fungsinya. Contoh:
Hidrolase → katalis reaksi hidrolisis
Enzim bekerja khas terhadap substrat tertentu, ini adalah ciri khas dari enzim. Contoh:
Enzim urease hanya bekerja terhadap urea sebagai substratnya.
Enzim esterase ini bekerja terhadap lebih dari 1 substrat ester-ester asam lemak, tetapi tidak dapat untuk substrat lain selain ester. Jadi tetap mempunyai kekhasan tertentu.
Suatu asam amino tertentu sebagai substrat mengalami reaksi berbeda dengan berbagai enzim.
CH R
NH2
COOH R CH2 NH2 CO2
C
R COOH C
C
R COOH NH3
O
O
OH
O
CH2 CH NH2
C O OH oksidase
dekarboksilase
transaminase
Walaupun ketiga reaksi tersebut berjalan namun tiap enzim hanya bekerja pada 1 jenis reaksi saja.
Fungsi dan cara kerja enzim
Enzim sebagai katalis untuk proses biokimia yang terjadi dalam sel maupun di luar sel. Enzim dapat mempercepat reaksi 108-1011 kali lebih cepat daripada reaksi tanpa enzim. Enzim sebagai katalis yaitu bekerja dengan menurunkan energi aktivasi suatu reaksi kimia sehingga reaksi berlangsung lebih mudah dan cepat.
Kompleks enzim-substrat
Agar berlangsung reaksi enzimatik maka harus terdapat kontak antara enzim-substrat, yang terjadi pada bagian aktiv dari enzim. Kontak dapat terjadi apabila bagian aktiv dari enzim mempunyai ruang yang tepat untuk menampung susbtrat yang sesuai. Substrat yang bentuk konformasinya tidak cocok dengan tempat aktiv enzim, tidak bisa dengan enzim, sehingga enzim tidak dapat berfungsi terhadap substrat. Hubungan antara enzim-substrat menyebabkan terjadinya kompleks enzim-substrat, sifatnya aktiv dan sementara, akan terurai lagi → hasil reaksi + enzim bebas.
S
S
S S
E E E
Bagian aktiv enzim, terbentuknya kompleks enzim substrat dan penguraiannya
AB
A + B energi aktivasi Tingkat
energi
Pada percobaan hidrolisis sukrosa menjadi glukosa dan fruktosa oleh enzim, ternyata bahwa pada konsentrasi sukrosa rendah kecepatan reaksi tergantung pada konsentrasi sukrosa (berbanding lurus). Akan tetapi pada konsentrasi tinggi ternyata kecepatan reaksi tidak lagi dipengaruhi oleh pertambahan konsentrasi (tidak berbanding lurus). Berarti enzim telah jenuh dengan substrat.
kecepatan reaksi
v
v maks orde zero
1/2 v maks
km [s] [sukrosa]
es atu
or d
orde camp
Grafik hubungan [sukrosa] dengan kecepata reaksi pada reaksi enzimatik
Mikhaelis dan Menten tahun 1913 mengajukan hipotesis bahwa dalam reaksi enzim terjadi lebih dahulu kompleks enzim-substrat yang kemudian memberikan hasil reaksi + enzim kembali.
E + S k1 k2 Es
k2
P + E
Mikhaelis dan Menten berkesimpulan bahwa kecepatan reaksi bergantung pada [ES], hingga dari penurunan persamaan dan kurva di atas diperoleh persamaan:
Vmaks =
[s]
Km+ [s] = Vmaks [s]
Km + [s]
V
V
V = Kecepatan reaksi enzimatik
Vmaks = Kecepatan maksimum pada [S] tidak terbatas [S] = Konsentrasi substrat mol/liter larutan
Km = Konstanta Mikhaelis
Dari rumus bila [S] > Km, maka V mendekati Vmaks. Reaksi mendekati orde zero.
V = ½ Vmaks maka Km2[S], berarti harga Km sama dengan konsentrasi substrat (mol/liter) yang menghasilkan kecepatan sebesar ½ Vmaks.
= Vmaks [s] Km + [s] V
1
V = Vmaks [s]
Km + [s]
=
Vmaks [s]
Km
Vmaks [s]
[s]
1
V = Vmaks
Km 1
[s]
1 Vmaks
Disebut persamaan Lineweaver-Burk
Bentuk kurva sebagai berikut:
1 V
Vmaks
Km
1 Km
1 Vmaks
1 [s]
Faktor-faktor yang mempengaruhi kerja enzim
Sangat erat hubungannya dengan sifat dari protein antara lain: 1. Konsentrasi substrat
2. Pengaruh pH
Perubahan pH langsung mempengaruhi sifat ion dari gugus amino dan gugus karboksilat sehingga mempengaruhi bagian aktiv dan konformasi enzim. pH yang ekstrem akan denaturasi protein enzim, sehingga enzim tidak aktiv lagi. pH dimana enzim bekerja optimal disebut dengan optimum enzim.
3. Pengaruh temperatur
Enzim bekerja sesuai temperatur tubuh dimana enzim bekerja pada temperatur tinggi (40º) denaturasi – hilang fungsi enzim.
4. Pengaruh aktivator dan gugus prostetik (F)
Kebanyakan enzim tidak berfungsi optimal karena tidak adanya zat kedua [aktivator] umum: ion logam, sehingga kecepatan reaksi enzimatik menjadi tergantung pada [aktivator].
(F)
Enzim bersifat protein majemuk terdiri dari:
protein = gugus apoenzim dan gugus prostetik = koenzim yang saling berikatan.
Ikatan antara apoenzim dan koenzim dapat kuat, kurang kuat. Umumnya koenzim
adalah vitamin (yang larut dalam air/umumnya vitamin B). 5. Pengaruh inhibitor
Inhibitor adalah zat yang efektif dalam jumlah kecil menghambat jalannya reaksi menjadi lebih lambat atau berhenti sama sekali. Berdasar mekanisme reaksi, inhibitor dibagi 3 golongan:
a. Kompetitiv inhibitor b. Non kompetitiv inhibitor c. Und kompetitiv inhibitor
Inhibitor enzim adalah senyawa yang dapat mengadakan kompetisi dengan substrat yang dapat mengikatkan diri dengan aktiv dari enzim.
a. Kompetitiv inhibitor
i. E + S ES E + P
ii. E + I EI
1 V
Vmaks Km
1 Km
1 Vmaks
1 [s] In 2 I
n 1
E
S I
kompetisi S dan I
Dengan kurva Lineweaver Burk:
* Km berubah, Vmaks tetap, 1/Vmaks, slope berubah Contoh:
Pada enzim suksinat dehidrogenase. Spesifik untuk suksinat. Senyawa-senyawa yang strukturnya mirip suksinat dapat sebagai inhibitor.
CH2 CH2
COOH COOH
suksinat
COOH
COOH CH2
COOH COOH
malat oksalat
b. Non kompetitiv inhibitor
[ES]
Dengan kurva Lineweaver-Burk:
* Km tetap, Vmaks berubah, slope berubah c. Und kompetitiv inhibitor
Adalah senyawa yang dapat mengikat kompleks enzim-substrat menjadi kompleks baru yang tidak dapat bersenyawa lagi, tempat ikatan belum diketahui. Ada pendapat: Inhibitor mol besar sehingga menutupi semua.
ES
Dengan kurva Lineweaver-Burk:
* Km tetap, Vmaks berubah, slope berubah
Struktur enzim
International Union of Biochemistry (IUB) telah mendasarkan penggolongan enzim pada 4 pokok:
1. Berdasar reaksi kimia, telah dikelompokkan menjadi 6 golongan besar enzim, masing-masing dikelompokkan dalam 4-13 sub-golongan.
2. Penamaan enzim dengan nama substrat ditambah –ase.
3. Informasi pelengkap ditempatkan di belakang nama enzim dalam kurung. Contoh:
Nad-oksido reduktase (decarboxylating). 4. Sistem kode angka sebanyak 4 angka (E.C)
Angka I : Jenis reaksi sebagai kelas Angka II : Sub-kelas
Angka III : Sub-sub-kelas
Angka IV : Untuk enzim spesifik Misal:
Berdasar ke-4 konsep tadi maka IUB mengklasifikasikan enzim ke dalam 6 golongan besar:
1. Oksidoreduktase
Enzim yang berfungsi dalam reaksi-reaksi oksidasi (dehidrogenase dan oksidase).
2. Transfarase
Enzim yang bekerja dalam reaksi-reaksi transfer gugus. 3. Hidrolase
Enzim yang bekerja pada hidrolisis ester, peptida, glikosa dan lain-lain. 4. Liase
Enzim yang menghilangkan gugus tertentu dari substrat dengan mekanisme yang lain dari hidrolisis, misal enzim untuk menarik air dari gugus alkohol sehingga terbentuk ikatan rangkap.
5. Isomerase
Enzim yang berfungsi merubah posisi optik dalam isomer. 6. Ligase
Enzim yang berfungsi sebagai katalis dalam reaksi penggabungan 2 mol dan pemutusan ikatan pirofosfat dalam ATP. Ikatan yang terbentuk adalah C – O, C – S, C – N, C – C.
Aktivitas spesifik adalah jumlah unit aktivitas enzim per miligram protein atau jumlah katalis per kilogram protein atau mol substrat/men/mg protein enzim. Angka pergantian (turnouder number) adalah angka yang menunjukkan jumlah molekul substrat yang ditransformasikan per satuan waktu oleh satu molekul enzim.
Aktivitas total adalah jumlah mol substrat yang diubah oleh enzim tersebut per menit per gram atau jumlah berat tertentu bahan yang digunakan untuk sampel enzim.
Mekanisme aksi enzim
Enzim mempunyai bagian/sisi aktif yang dapat mengikat substrat , ini terdiri residu asam amino tertentu, sengan ikatan peptida yang dapat mengadakan kontak dengan substrat. Ada beberapa teori:
1. Hipotesa Lock and Key (lubang kunci dan anak kunci) menurut Fischer 1913. 2. Induced fit theory
Pengikatan enzim dan substrat merubah konformasi enzim sehingga enzim baru dapat aktiv mengerjakan substrat.
Vitamin dan koenzim
Vitamin adalah senyawa organik tertentu yang merupakan faktor diit esensial yang diperlukan dalam jumlah kecil, untuk berlangsungnya metabolisme dan fungsi metabolisme tubuh.
Menurut Warburg (1932-1935) mengenai koenzim menunjukkan adanya hubungan antara struktur kimia dengan koenzim.
1. Nikotinamida (niasin) dan asam nikotinat
N
COOH
N
CONH2
Koenzim:
a. Nikotinamida adenin dinukleotida (NAD+).
b. Nikotinamida adenin dinukleotida fosfat (NADP+). Fungsi:
a. Sebagai dehidrogenase. Misal:
asam laktat
laktat dehidrogenase
asam piruvat
NAD+ NADH + H+
asam isositrat isositrat dehidrogenase ketoglutarat
NADP+ NADPH + H+ b. Sebagai pereduksi.
Misal:
FAD + NADH + H+→ FADH2 + NAD+
Kekurangan : Gejala penyakit pellagra ( dermatitis, diarhe, demensia). Sumber : Makanan kaya protein hewani, biji-bijian.
2. Riboflavin (Vitamin B2)
Sebagai koenzim FMN. Fungsi : Dehidrogenase. Misal :
suksinat suksinat dehidrogenase fumarat
FAD FADH2
Kekurangan : Terjadi cheilosis (kerak pada sudut mulut), keratosis lidah. Sumber : Susu, daging, telur, ikan, biji-bijian.
3. Biotin
Sebagai kofaktor terikat kuat pada protein enzim (BCCP). Fungsi : Karboksilasi dan transkarboksilasi.
Misal :
Kekurangan : Kulit bersisik, kurang selera makan (anoreksia), HB turun,
kolesterol naik, urat sakit. Sumber : Daging, kuning telur, biji-bijian. 4. Thiamin (Vitamin B1)
Sebagai koenzim TPP. Fungsi:
a. Dekarboksilasi asam a keto.
b. Oksidasi asam a keto.
c. Transketolasi. d. Fosfoketolasi.
Kekurangan : Beri-beri, muntah-muntah, diarhe, akibat alkoholisme. Sumber : Biji-bijian, daging, telur, susu, kacang-kacangan. 5. Vitamin B6 (Piridoksin, piridoksal, piridoksamin)
Sebagai koenzim: a. Piridoksal fosfat. b. Piridoksamin fosfat. Fungsi:
a. Transaminasi. b. Dekarboksilasi. c. Rasemasi. Misal:
asam glutamat + asam oksaloasetatglutamat aspartat transaminaseasam keto glutamat + asam aspartat
Kekurangan : Borok kulit, lemah, letih, lesu, nervous. Sumber : Protein hewani, biji-bijian, ubi-ubian. 6. Asam folat
Sebagai koenzim.
Fungsi : Reduksi, sumber H+, C pada sintesa CH3.
Kekurangan : Megaloblastik ademi, diarhe.
Sumber : Protein hewani, biji-bijian, sayur hijau. 7. Asam pantotenat
Sebagai koenzim : Koenzim A.
Fungsi : Pentransfer gugus asil.
CH2
R C O
OH
KoASH R CH2 C
O
S KoA H2O
Kekurangan : Selera makan berkurang, depresi mental, kram, insomnia,
gangguan pencernaan.
8. Vitamin C
Sebagai hidroksilasi (prolin, lisin), pereduksi kuat. Fungsi:
a. Pembentukan zat interseluler kolagen b. Pernafasan sel
c. Sintesa hormon steroid dari kolesterol.
Kekurangan : Skorbut, gusi berdarah, kulit mudah mengelupas, mudah luka,
mudah kena infeksi, pertumbuhan tulang pada bayi tidak normal.
Sumber : Sayuran hijau, buah berwarna. 9. Vitamin A
Sebagai pro vitamin A dalam tumbuhan.
Fungsi : Penting pada proses fotokimia dalam retina zat picmen dalam
mata rodopsin karena pengaruh cahaya → opsin + trans retinen.
Akan diubah: Trans vitamin A dalam darah. Dalam gelap diubah
kembali jadi rodopsin.
Kekurangan : Rabun senja, mempengaruhi pembentukan mukosa, esensial
untuk pertumbuhan tulang dan gigi.
Sumber : Minyak ikan, protein hewani, sayur hijau, buah berwarna. 10.Vitamin D
Fungsi:
a. Mengatur absorbsi Ca dan Fosfor dari pencernaan. b. Mengatur klasifikasi tulang dan gigi.
c. Membantu kelancaran transpor aktiv.
Kekurangan : Riketsia pada anak (tulang lunak, perubahan bentuk tulang, gigi
tumbuh terlambat).
Sumber : Minyak ikan, susu, sinar matahari pagi.
Mengubah provitamin D → D
11.Vitamin E Fungsi:
a. Sebagai antioksidan
b. Mengurangi oksidasi vitamin A c. Mengatur kesuburan dan reproduksi.
Kekurangan : Terjadi hemolisa sel darah hewan, anemia ringan, kemandulan
(pada hewan).
12.Vitamin K Fungsi:
a. Pembentukan protombin dan protein. b. Pembekuan darah.
c. Fosforilasi oksidatif dalam metabolisme sel.
ASAM NUKLEAT
Asam nukleat adalah senyawa organik makro molekul yang kompleks yang pegang peranan. Dalam sistem biologi asam nukleat bertugas sebagai penyimpanan dan transmisi informasi genetik serta menterjemahkan informasi ini untuk mensintesis dengan teliti protein-protein yang khas bagi sel individu.
Asam nukleat adalah pembawa informasi kebakaan (turunan) dari generasi.
Dalam semua organisme terdapat 2 jenis asam nukleat yakni DNA (deoksiribonukleat-asam) dan RNA (ribonukleat asam). Dna dan RNA merupakan polimer nukleotida.
Struktur asam nukleat
Asam nukleat terbentuk dari polimerisasi nukleotida-nukleotida. Nukleotida terbentuk dari nukleosida dan asam fosfat.
Sebuah nukleosida tersusun dari basa purin/pirimidin dengan sebuah molekul ribosa/deoksiribosa.
Asam nukleat
Nukleotida
Nukleosida Fosfat
Basa nitrogen Pentosa
Purin Pirimidin Ribosa Deoksiribosa
Nukleotida Nukleotida
Adenin Guanin
N
Adenin Guanin Purin
1 2
3 4 5
6
Sitosin Urasil Timin
Pirimidin
Sehingga senyawa yang terkandung dalam:
DNA: Pentosa adalah deoksiriboda
Basa N adalah adenin, guanin (purin) dan Fosfat sitosin, timin (pirimidin)
RNA: Pentosa adalah ribosa
Basa N adalah adenin, guanin (purin) Fosfat sitosin, urasil (pirimidin)
Dalam nukleosida (-glikosidik/C-1) dari ribosa terikat pada n-1 pirimidin atau n-9 basa purin.
Ribosa dengan basa purin/ pirimidin
ribonukleosida
Deoksiribosa dengan basa purin/ pirimidin
Ribonukleosida yang umum terdapat di alam adalah: rantai 4 nukleosida yang membentuk RNA.
C HN
N C C O
H2N N
N
O
OH CH2
O O
P O
OH
O CH2 O
OH
O P
O
OH
O CH2 O
OH
O P
O
OH
O CH2 O
OH
O P
O
OH
Guanosin
Guanin
Adenosin Adenin
Urasil
Uridin
Sitosin
Deoksiribonukleotida yang paling umum di alam: rantai 4 nukleosida yang membentuk DNA.
O
Sebuah nukleosida bila berikatan dengan fosfat akan membentuk nukleotida. Dari struktur kimianya dapat disebutkan bahwa nukleotida adalah ester fosfat dari nukleosida. Ikatan ester terbentuk anatara gugus OH C-5 ribosa dengan asam fosfat. Sehingga ester fosfat disebut juga nukleosida-5 fosfat atau 5-nukleotida. Nukleotida yang diturunkan dari adenosin disebut adenilat. Yang diturunkan dari guanosin disebut guanilat.
Basa Ribonukleosida Ribonukleotida Nama Menurut Struktur Kimia Adenin Adenosin Adenilat Adenosin mono fosfat (AMP) Guanin Guanosin Guanilat Guanosin mono fosfat (GMP) Urasil Uridin Uridilat Urisin mono fosfat (UMP) Sitosin Sitidin Sitidilat Sitidin mono fosfat (CMP)
Adenin Deoksiadenosin Deoksiadenilat Deoksi adenosin mono fosfat (dAMP)
Guanin (dGMP)
Timin (dTMP)
Sitosin (dCMP)
Asam Nukleat terbentuk dari polimerisasi nukleotida-nukleotida. Polimerisasi
Dua rantai polimer nukleotida dapat berikatan melalui ikatan hidrogen yang terbentuk antara basa-basa pada kedua rantai.
Ikatan hidrogen ini terbentuk antara atom-atom hidrogen dari sebuah basa rantai pertama dengan atom nitrogen dari basa pada rantai nukleotida lainnya, sehingga akibatnya terbentuk struktur heliks dari 2 rantai nukleotida.
Struktur heliks rangkap DNA
menurut Watson dan Crick A = Adenin
C = Sitosin G = Guanin T = Timin P = Pospat
DNA dan RNA mempunyai susunan kimia yang hampir bersamaan dengan hanya beberapa perbedaan:
No DNA RNA
1. Gula pentosa deoksiribosa. Gula pentosa ribosa. 2. Mempunyai asam fosfat yang
menghubungkan gula dari tiap nukleosida membentuk rantai nukleotida.
Idem.
3. Basa nitrogennya:
Purin : Adenin, Guanin Pirimidin: Sitosin, Timin
Basa nitrogennya:
Purin : Adenin, Guanin Pirimidin: Sitosin, Urasil 4. Mempunyai 4 nukleotida:
dAMP, dGMP, dCMP,dTMP
Mempunyai 4 nukleotida: AMP, CMP, GMP, UMP 5. Struktur terdiri 2 rantai
polimer nukleotida yang membentuk dobel heliks.
Struktur terdiri hanya 1 rantai polinukleotida.
6. DNA adalah materi genetik dan terdapat dalam
kromosom, nukleoplasma dan mitokondria.
RNA adalah pembawa informasi genetik dan berperan dalam sintesis protein. RNA terdapat dalam nukleous, nukleoplasma dan sitoplasma.
DNA mempunyai berat molekul sampai jutaan (7 juta) dengan struktur dobel heliks yang panjangnya mencapai 30 000 A dan lebar 15-20 A.
RNA terdapat dalam keadaan terlarut di dalam plasma dengan berat molekul rendah sekitar 100 nukleotida (contoh RNA untuk transfer alanin pada biosintesa protein). tRNA ini mempunyai struktur berlipat karena ada ikatan hidrogen antara sesama basa dalam 1 rantai molekul polinukleotida.
Nukleoprotein
Kebanyakan dari asam nukleat tidak terdapat bebas di dalam sel, biasanya asam nukleat diisolasi dari nukleoprotein, yakni gabungan asam nukleat dengan protein. Ikatan antara protein dengan asam nukleat mudah dilepaskan hanya dengan penambahan elektrolit/perubahan pH. Nukleoprotein berat molekul rendah, kaya arigin dan lisin. Contoh: Histon dan Protamin.
Virus
Merupakan nukleoprotein → asam nukleat berupa DNA dan RNA sehingga ada
virus RNA dan virus DNA, masing-masing mempunyai unit protein sehingga disebut nukleoprotein. Protein terletak di sebelah luar dan asam nukleat di sebelah dalam.
Contoh:
Virus mozaik tembakau (TMV)
Asam nukleatnya berupa rantai tunggal yang membentuk a heliks dan yang
bersifat infektif adalah asam nukleatnya.
Protein
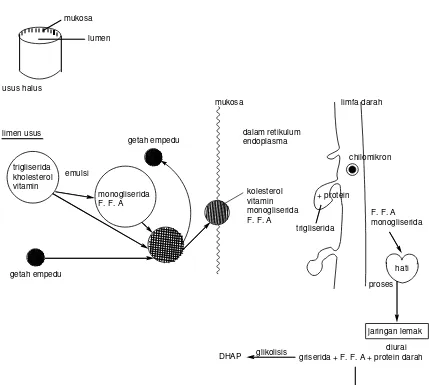
PENCERNAAN
Zat makanan:
Polimer masuk dalam tubuh diubah menjadi bentuk molekul dilakukan oleh organ (alat pencerna). Ukuran molekul akan diproses lebih lanjut untuk menghasilkan antara lain, tenaga, zat pembangun pertumbuhan dan lain-lain.
Bahan makan makro molekul
(karbohidrat, protein, lemak) Organ pencerna Molekul sederhana Absorpsi
Mulut
Kelenjar ludah
Hati
Lambung
Pankreas
Usus halus
Usus besar
Anus Usus buntu
Duodenum Kantung empedu
Esofagus
Saluran empedu Katup pilorus
X
Sel
11
12
1
2
3
4
5
6 7
8 9 10
1. Membran sel 2. Mitokondria 3. Lisosom
4. Retikulum endoplasmik 5. Sitoplasma
6. Inti 7. Plasma inti 8. Membran inti 9. Nukleous 10. Ribosoma 11. Golgi
Proses pencernaan Dalam mulut
Makanan → ukuran yang lebih kecil
luas permukaan bertambah kontak dengan enzim baik reaksi berjalan lebih cepat
Enzim ptialin dalam mulut yang membantu, dihasilkan oleh kelenjar ludah (glandula submaxilaris, glandula sublingualis, glandula parotis)
Komposisi ludah:
99,5 % zat cair dan 0,5 % zat padat pH ludah 6,35-6,85
Berat jenis ludah 1,003 Fungsi ludah:
o Membasahi makanan
o Pelumas dalam kerongkangan o Pemecah amilum, dekstrin
Enzim ptialin dalam mulut:
pH optimun 6,6, dibawah itu tidak aktiv, hanya mampu mengubah/memecah ikatan 1,4 pada amilum dan dekstrin. Enzim ini dalam lambung hanya mampu
bertahan 15’-30’. Dalam lambung
Terdapat cairan lambung: 99,4 % air dan 0,6 zat padat, dengan berat jenis = 1,001.
Enzim yang terdapat di lambung: Pepsin, lipase.
Cairan lambung mengandung: Hcl, Nacl, Kcl, fosfat, musin, enzim-enzim. Hcl berfungsi:
o Pendenaturasi protein
o Mengaktivkan pepsinogen → pepsin
o Merangsang sekretin yang terdapat dalam usus 12 jari.
o Mencegah fermentasi o Dan lain-lain
Pepsin berfungsi:
o Pemecah peptida → bentuk yang lebih sederhana o Mengumpulkan susu → pemecahan
Lipase berfungsi: Pemecah lemak
Renin berfungsi: (pada lambung bayi) penggumpal susu
Mukus/lendir berfungsi: Melindungi dinding lambung dari Hcl Dalam usus
Proses dilakukan oleh pankreas enzim, empedu, cairan usus. Cairan pankreas:
o Hasil dari sel dalam kelenjar pankreas o Terdiri 98,7 % cair dan 1,3 % padat. o pH 7,5-8,2
o Terdapat karbonat, enzim, tripsin, khimotripsin, karboksipeptidase, amilase,
Cairan usus:
o Hasil dari kelenjar-kelenjar mukosa usus
o Terdapat enzim karbohidrase, peptidase, nukleo-fosfatase, nukleosidase,
enterokinase yang berfungsi mengaktivkan tripsinogen → tripsin Empedu:
o Hasil dari sel hati, kuning-pahit, pH 7,0-8,5
o Terdiri zat padat 1-4 % dan zar organik: Asam empedu, bilirubin, kholesterol
o Merupakan tempat pembuangan sisa dari sel hati
o Asam empedu yang terdapat: asam kholat, asam deoksikholat yang
berfungsi:
Emulgator lemak Mengaktivkan lipase
METABOLISME SEL
Zat makanan → ukuran kecil → dalam sel.
Mengalami proses:
Anabolisme (membentuk molekul besar)
Katabolisme (energi dipecah → molekul kecil)
Dalam proses katabolisme maka energi dipakai untuk proses kimia sel dan fungsi tubuh. Proses yang berlangsung dalam sel dengan bantuan enzim.
Sitoplasma
Sintesis protein
Ribosom F.A.
Fat
F.A. Ac. CoA ATP
sRNA mRNA tRNA Inti
Purin Pirimidin Pentosa
Mitokondria
CO2 + H2O
G Gly
Hormon
A.A
F.A
Karbohidrat
Metabolisma pada mamalia:
Glikolisis : Oksidasi glukosa/glikogen menjadi piruvat dan laktat melalui
jalur EMP.
Enzim terdapat : Extra mitokondria.
Glikogenesis : Sintesis glikogen dari glukosa. Glikogenolisis : Pemecahan glikogen →
Proses di hati: Hasilnya glukosa
Proses di otot: Hasilnya piruvat dan laktat
Siklus Kreb’s : Suatu jalan bersama dari oksidasi karbohidrat, lipid,
(Siklus trikarboksilat) protein, melalui asetil Ko A dan akan dioksidasikan:
(Siklus asam sitrat) CO2 + H2O
(TCA/CAC)
HMS/DOP/PGOP/PPC : Suatu jalan/jalur lain dari oksidasi glukosa selain melalui
EMP/Kreb’s.
Glukoneogenesis : Pembentukan glukosa/glikogen dari zat-zat bukan
karbohidrat.
glukosa darah
glukosa-6-fosfat glikogen Hati
glikogen glukosa-6-fosfat Otot
piruvat
laktat
darah
laktat
piruvat
ALA NH3
ALA NH3 urea
Glikolisis
Semua enzim yang diperlukan untuk jalur EMP terdapat pada extra mitokondria, enzim-enzim tersebut bertanggung jawab terhadap perubahan glukosa menjadi piruvat dan laktat.
glikogen
glukosa-6-fosfat
fruktosa-6-fosfat
Mg++ ATP * ADP
fruktosa-1,6-difosfat dihidroksi asetofosfat gliseraldehid-3-fosfat
Mg++ ATP* ADP -D. glukosa
triosafosfat (DHAP + gliseraldehida-3-fosfat) 1,3 difosfogliserat
pi
Mg++
ATP ADP
3-fosfogliserat
2-fosfogliserat
Mg++ H 2O fosfoenolpiruvat
Mg++
ATP ADP
piruvat (enol)
piruvat (keto)
laktat
asetil Ko A
oksaloasetat
sitrat CO2 -keto glutamat
CO2 propionat
NAD+ NADH + H+
R 3 ATP
Jalur glikogenesis dan glikogenolisis
glikogen 1,4 dan 1,6 glucosil
pi
glukosa-1-fosfat
glukosa-6-fosfat
-D. glukosa
C 1,4-(glucosil unit)x
UDPG
METABOLISMA KARBOHIDRAT
Terdiri digesti dan absorpsi
Karbohidrat merupakan sumber kalori yang penting, umumnya yang dimakan poli dan oligo-sakarida, sedang monosakarida sedikit terdapat dalam makanan.
Makanan Mulut
(ptialin amilase)
Oesopagus Lambung (getah lambung, enzim proteolitik)
Tetap di usus halus menjadi monosa diserap villi monosa fosfat
kapiler darah vena
Hati metabolise Monosa lain Glukosa fosfat
Jadi monosa diaktivkan menjadi monosakarida fosfat (fosfat berenergi tinggi: pirofosfat) sehingga senyawa monosa menjadi lebih reaktiv.
mono
ATP ADP
monosa fosfat Proses berjalan katalitik
O glukosa- 6-fosfat glukosa- 1-fosfat
galaktosa galaktosa- 1-fosfat fruktosa-6-fosfat
ATP
Glikogenolisis
Pengubahan glikogen → glukosa dalam hati dan otot.
glukosa makanan
glikogen hati glukosa darah
(70-90 mg %)
glikogen otot
Proses: - glikogen
- glukosa-1-fosfat - glukosa-6-fosfat
glukosa-1-fosfat glukosa-6-fosfat glukosa + piruvat
1. fosforilase 2. fosfoglukomutase 3. fosfatase
1 2 3
Pengaturan glukosa darah tetap (hemeostatis): bahwa antara pengambilan dan pemberian adalah diatur oleh hormon insulin, hasil dari insula langer hans-pankreas, yang mengatur glikogenolisis dan glikogenesis dalam hati.
Glukosa darah diatas normal - glikogenolisis
- glikogenesis otot - absorbsi glukosa usus
hiperglikemia = diabetes melitus = glukosuria
hormon insulin berkurang menurunkan glukosa darah
Glukosa darah turun: - glikogenolisis - glikogenesis otot
Glikolisis
Emden Mayerhof Pathway, penguraian glikogen/gula → asam piruvat secara anaeraob.
Berlangsung dalam jaringan-jaringan aktiv-otot.
glikogen (poli -1,4-glukosa)
pi
asam fosfoenol piruvat (PEP)
1. fosforilase
2. fosfogluko mutase 3. fosfogluko isomerase 4. frukto kinase
5. aldolase
6. isomerase triosafosfat 7. dihidrogenase-3-fosfat 8. kinasefosfo gliserat 9. fosfoglisero mutase 10. enolase
Dalam otot asam piruvat akan diubah: Asam laktat
C COOH
asam piruvat CH3
O
dehidrogenase laktat NADH + H+ NAD+
HC COOH
asam laktat CH3
OH
Dalam ragi : Glikolisa → Etanol (fermentasi alkohol) Syarat : Larutan harus steril → Hasil manis
Larutan tidak steril → Hasil asam
C COOH
CH3 O
CO2 C
O H CH3
CH3 COOH
NADH + H+ NAD+
CH2OH
etanol CH3
2
3 1
Glikogenesis
Pembentukan glikogen dalam hati/otot.
Tahap: Fosforilasi, mutasi, pemanjangan rantai.
O 2. fosfogluko mutase 3. pirofosforilase UDPG 4. sintetase glikogen
rantai glikogen non reduktor
1 2
3
4
glukosa/glikogen 10 tahap
anaerob asam piruvat tahap 11
tahap 11 asam laktat
asetaldehid tahap 12 etanol Hasil glikolisis:
-Dibutuhkan 2 ATP (jika yang diubah glukosa) (jika glikogen: butuh 1 ATP) -Dibutuhkan 1 NADH untuk 3 atom C
-Dikeluarkan 2 NADH + 2H+ untuk 6 atom C -Dikeluarkan 2 ATP 2 untuk 6 atom C -Dikeluarkan 2 mol asam laktat
Siklus asam sitrat
= Siklus Krebs (penemu: Sir Hans Krebs)
Dasar: Glukosa → glukosa-6-fosfat → asam piruvat → asetil Ko A → siklus asam
asam ketoglutarat
C
suksinil koenzim A COOH
Berlangsung dalam mitokondria
Interaksi Metabolisme
Metabolisme berkangsung menurut urutan reaksi disebut jalur metabolik, berlaku untuk glukosa, asam amino, asam lemak yang saling berhubungan metabolit tertentu adalah asam piruvat, asetil koenzim A dan siklus asam sitrat.
Zat Makanan
Protein Karbohidrat Lemak
Asam Amino Glukosa Gliserol dan Asam Lemak Protein Tubuh Glikogen
Depot Lemak Asam Piruvat
Asetil KoA Zat antara Siklus Asam Sitrat
Siklus Asam Sitrat Transpor Elektron dan
Fosforilasi Oksidatif
H+
Efisiensi energi dari 1 mol glukosa bila diubah menjadi CO2 dan H2O dalam metabolisme (glikolisis → asam piruvat → asetil koenzim A → siklus asam sitrat)
akan dihasilkan ATP = 38.
Satu mol glukosa dalam glikolisis dan siklus asam sitrat akan menghasilkan: 10 mol NADH + H+, 2 FADH2, 2 ATP dan 2 GTP. Dalam proses transpor elektron dan
fosforilasioksidatif menghasilkan, antara lain:
NADH menghasilkan 3 mol ATP dan GTP + ADP ATP + GDP FADH2 menghasilkan 2 mol ATP
Enzim yang berperan adalah sitokrom a,b,c; koenzim Q dan FMN, sehingga 1 mol glukosa menghasilkan 34 ATP (dari NADH dan FADH2) + 2 ATP + 2 ATP = 38
ATP.
Lingkaran pentosa fosfat (LPP)
LPP juga dinamakan heksosa monofosfat shunt. Disebut cabang, karena glukosa →
glukosa-6-fosfat akan dipecah → fruktosa-6-fosfat melalui glikolisis, selain itu juga pecah melalui LPP dan dihasilkan pentosafosfat yang kemudian untuk biosintesis asam nukleat.
Selain itu LPP berfungsi untuk pembentukan NADPH + H+ ekstra mitokondrial yang akan dipakai sebagai sumber hidrogen pada biosintesis asam lemak.
LPP terdiri dari 2 tahap: Oksidasi dan pengembalian.
6 glukosa-6- fosfat + 12 NADP+ + 7 H2O 12 NADPH + 12 H+ + 6 CO2 + 2 pi 6 glukosa-6-fosfat
6 fosfat glukonat 6 NADP+
6 NADPH
6 NADP+ 6 NADPH
6 ribulosa-5-fosfat
2 silulosa-5-fosfat 2 ribosa-5-fosfat
2 gliseraldehida-3-fosfat 2 sedoheptotulosa-7-fosfat
2 fruktosa-6-fosfat 2 fruktosa-6-fosfat 4 fruktosa-6-fosfat
4 glukosa-6-fosfat 2 silulosa-5-fosfat
2 eritrosa-4-fosfat
2 gliseraldehida-3-fosfat
gliseraldehida-3-fosfat dihidroksiasetonfosfat
fruktosa difosfat pi fruktosa-6-fosfat
HUBUNGAN ANTAR METABOLISMA
KARBOHIDRAT-LEMAK-PROTEIN
karbohidrat glikogen
glukosa-1-fosfat
glukosa-6-fosfat
fruktosa difosfat
fosfo gliseraldehida
fosfo gliserat
fosfo piruvat
piruvat
asetil KoA=
oksaloasetat
malat fumarat
suksinat
ketoglutarat isositrat sitrat glukosa
glisin alanin serin
asetoasetat
leusin isoleusin tirosin fenil alanin treonin prolin,histidin
asam glutamat
arigin
ornitin asam lemak
gliserol
lemak
= protein
![Grafik hubungan [sukrosa] dengan kecepata reaksi pada reaksi enzimatik](https://thumb-ap.123doks.com/thumbv2/123dok/930895.730603/29.612.142.437.154.283/grafik-hubungan-sukrosa-kecepata-reaksi-reaksi-enzimatik.webp)