BAB II
TINJAUAN PUSTAKA
2.1 Uraian Hewan 2.1.1 Habitat Sponge
Sponge merupakan biota laut dari filum porifera yang hidup pada
ekosistem terumbu karang. Habitat sponge umumnya menempel pada pasir,
batu-batuan dan karang-karang mati (Amir dan Budiyanto, 1996). Sponge kelas
Demospongiae dari bangsa Haplosclerida seperti sponge marga Chalinula tersebar
di seluruh dunia, dari Indo-Pasifik sampai Karibia (Suparno, 2005). Sponge jenis
Chalinula sp terdapat di Indonesia salah satunya di daerah Sibolga, Tapanuli
Tengah provinsi Sumatera Utara. Sponge jenis Chalinula sp hidup pada
kedalaman 1-6 m dari permukaan laut (Ilan dan Loya, 1990).
2.1.2 Morfologi Sponge
Bentuk luar sponge sangat dipengaruhi oleh faktor lingkungannya. Sponge
yang berada pada lingkungan terbuka, berombak besar, dangkal dan terkena sinar
matahari cenderung berukuran pendek, merambat dan memiliki kisaran warna
yang gelap hingga terang seperti coklat, abu-abu, ungu, biru, jingga dan kuning.
Sponge yang hidup pada perairan yang lebih dalam, berarus tenang dan tidak
terkena sinar matahari pertumbuhannya cenderung tegak dan tinggi serta
warnanya pucat (Amir dan Budiyanto, 1996).
Sponge Chalinula sp dari bangsa Haplosclerida yang terdapat di daerah
Sibolga, Tapanuli Tengah provinsi Sumatera Utara memiliki bentuk tubuh
bercabang, berpori, konsistensi lunak dan berwarna ungu kecoklatan. Morfologi
sponge Chalinula sp ini hampir sama dengan morfologi sponge Chalinula molitba
Salvador yaitu memiliki bentuk tubuh bercabang, berpori tetapi berwarna ungu
menyala. Jenis sponge lainnya yang juga berasal dari bangsa Haplosclerida adalah
Haliclona Grant, 1836 yang diperoleh dari daerah Sulawesi. Sponge Haliclona
Grant memiliki bentuk tubuh bercabang, pipih, berpori, konsistensi lunak dan
berwarna jingga (Ilan dan Loya, 1990).
Di dalam tubuh sponge terdapat rongga yang disebut spongocoel. Pada
permukaan tubuh terdapat lubang-lubang atau pori-pori yang merupakan lubang
air masuk ke spongocoel, untuk akhirnya keluar melalui osculum (Suwignyo,
dkk., 2005).
Pada dasarnya dinding tubuh sponge terdiri atas tiga lapisan (Suwignyo,
dkk., 2005) yaitu:
1. Pinacocyte atau pinacoderm
Pinacocyte berfungsi untuk melindungi tubuh bagian dalam. Bagian sel
pinacocyte dapat berkontraksi atau berkerut sehingga seluruh tubuh hewan dapat
membesar dan mengecil.
2. Mesohyl atau Mesoglea
Mesohyl terdiri dari zat semacam agar (gelatinous protein matrix) dan
mengandung sel amebocyte. Sel amebocyte mempunyai banyak fungsi, antara lain
sebagai cadangan makanan, membuang partikel sisa metabolisme dan berperan
dalam proses reproduksi yaitu sebagai pembawa sperma menuju sel telur dalam
mesohyl.
3. Choanocyte
Choanocyte yang melapisi spongocoel. Bentuk choanocyte agak lonjong,
Berdasarkan sistem aliran air, bentuk tubuh porifera dibagi menjadi
tigatipe (Suwignyo, dkk., 2005)yaitu:
1. Asconoid
Asconoid merupakan bentuk yang paling primitif, menyerupai vas bunga.
Pori-pori atau lubang air masuk merupakan saluran yang berbentuk tabung,
memanjang dari permukaan tubuh sampai spongocoel keluar melalui osculum.
2. Syconoid
Dinding tubuh melipat secara horizontal sehingga potongan melintangnya
seperti jari-jari. Lipatan dalam menghasilkan sejumlah besar kantung yang dilapisi
coanocyte, sedangkan lipatan luar sebagai saluran air masuk.
3. Tipe Leuconoid
Tipe ini merupakan tipe saluran air yang rumit/kompleks, memiliki banyak
lipatan-lipatan membentuk rongga kecil sehingga menyebabkan bentuknya
menjadi tak beraturan, banyak terdapat choanocyte-choanocyte pada rongga.
Air masuk melalui pori yang bercabang-cabang dan keluar melalui osculum.
Tubuh sponge yang lunak dapat berdiri karena ditunjang oleh sejumlah
besar spikula kecil serta serat organik yang berfungsi sebagai kerangka. Spikula
berasal dari CaCO3 dan silikat. Bentuk spikula bermacam-macam, seperti
monaxon berbentuk seperti jarum, lurus atau melengkung, tetraxon berbentuk
empat percabangan, polyaxon berbentuk banyak percabangan dan berbentuk serat
atau benang-benang spongin (Suwignyo, dkk.,2005).
Sponge umumnya memilki satu atau lebih dari satu bentuk spikula, sehingga
perlu adanya pengamatan yang rinci tentang bentuk-bentuk mikroskopis dari
setiap spikula yang dikandungnya. Untuk pengujian spikula tertentu dapat
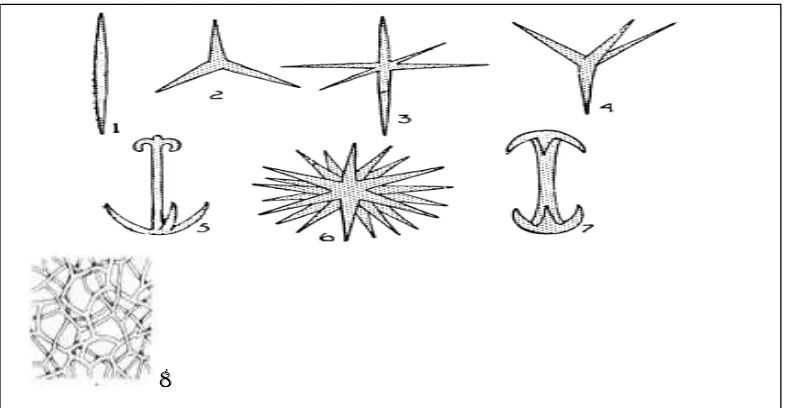
Tipe spikula dapat dilihat pada Gambar 2.1.
Gambar 2.1 Tipe spikula
Keterangan: 1 dan 7. Monaxon; 2. Triod; 3 dan 6. Polyaxon; 4. Tetraxon; 5. Anchor ; 8. Benang-benang spongin.
(Sumber: Amir dan Budiyanto, 1996).
Berdasarkan ukuran, spikula dibedakan menjadi mikrosklera yang
berukuran kecil dan megasklera yang berukuran empat sampai lima kali ukuran
mikrosklera (Suwignyo, dkk.,2005).
Megasklera berperan untuk membentuk tubuh sponge dan perkembangan
struktur internal. Mikrosklera berperan dalam membentuk kelompok antara
kumpulan megaklera yang tersebar pada permukaan atau membran internal.
Ukuran, bentuk dan susunan dari masing-masing spikula yang dikandung oleh
hewan sponge sangat berguna untuk menentukan klasifikasi, bentuk dan nama
dari megasklera dan mikrosklera (Amir dan Budiyanto, 1996).
2.1.3 Reproduksi Sponge
Reproduksi sponge dapat dilakukan secara aseksual dan seksual.
Reproduksi secara aseksual terjadi dengan cara pembentukan tunas atau gamul
(gammules). Gamul terbentuk dari sekumpulan archeocyte berisi cadangan
makanan dikelilingi amebocyte yang membentuklapisan luar yang keras berupa
cangkang yang mengandung spikula yang akan melakukan diferensiasi menjadi
beberapa tipe sel yang diperlukan untuk tumbuh menjadi sponge kecil (Suwignyo,
dkk., 2005).
Reproduksi secara seksual terjadi pada sponge yang hermaprodit maupun
gonokoris. Kebanyakan porifera adalah hermaprodit, namun sel telur dan sperma
diproduksi dalam waktu yang berbeda. Sperma dan sel telur dihasilkan oleh
amebocyte. Sperma keluar dari tubuh induk melalui osculum bersama dengan
aliran air dan masuk ke sponge lain melalui ostium juga bersama aliran air. Dalam
spongocoel, sperma akan masuk ke amebocyte. Sel amebocyte berfungsi sebagai
pembawa sperma menuju sel telur dalam mesohyl, kemudian sperma dan sel telur
akan melebur dan terjadilah pembuahan (fertilisasi). Perkembangan embrio
sampai menjadi larva berflagela masih di dalam mesohyl. Larva berflagela keluar
dari mesohyl dan bersama dengan aliran air keluar dari tubuh induk melalui
osculum. Larva berflagela berenang bebas lalu menempel pada substrat dan
berkembang menjadi sponge muda yang akhirnya tumbuh menjadi sponge dewasa
(Suwignyo, dkk., 2005). Reproduksi sponge jenis Chalinula sp terjadi secara
seksual yaitu hermaprodit (Ilan dan Loya, 1990).
2.1.4 Klasifikasi sponge
Filum Porifera yang dibagi dalam 3 kelas (Pechenik, 2005) yaitu:
1. Kelas Hexactinellida
Sponge ini dikenal sebagai sponge gelas, memiliki tipe aliran air syconoid.
Spikula terdiri dari silikat dan tidak mengandung spongin. Spikulanya berbentuk
bidang triaxon, dimana masing-masing bidang terdapat dua jari-jari. Sponge dari
2. Kelas Calcarea
Spikula sponge ini hanya tersusun dari kalsium karbonat dan tidak
mengandung spongin, memiliki tipe aliran air asconoid, syconoid dan leuconoid,
tetapi pada akhirnya hanya tipe aliran asconoid yang banyak ditemukan pada
sponge kelas calcarea. Sebagian besar dari kelas ini bentuknya kecil-kecil dan
berwarna keabu-abuan dan ada beberapa jenis yang berwarna kuning, pink atau
hijau. Beberapa jenis sponge ini yang umum adalah Sycon gelatinosum (berbentuk
silinder berwarna coklat muda).
3. Kelas Demospongiae
Demospongiae merupakan kelas terluas (setidaknya terdapat 80% dari
semua jenis sponge), memiliki tipe aliran air leuconoid. Spikula jenis sponge
kelas ini mengandung serat spongin atau silikat tetapi tidak mengandung kalsium
karbonat. Pada umumnya spikula berbentuk monoakson atau tetraxon.
2.1.5 Sistematika sponge Chalinula sp
Sistematikasponge Chalinula sp (Ilan dan Loya, 1990) sebagai berikut:
Kingdom : Animalia
Filum : Porifera
Kelas : Demospongiae
Ordo : Haplosclerida
Famili : Chalinidae
Genus : Chalinula
2.2 Metode Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut
sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut tertentu.
Beberapa metode ekstraksi dengan menggunakan pelarut (Depkes RI,
2000) yaitu:
A. Cara dingin
1. Maserasi
Maserasiadalah proses penyarian simplisia dengan cara perendaman
menggunakanpelarutdengan sesekali pengadukanpadatemperaturkamar.
Remaserasi berarti dilakukanpengulangan penambahan pelarut setelah dilakukan
penyaringanmaseratpertamadanseterusnya.
2. Perkolasi
Perkolasi adalah proses penyarian simplisia menggunakan alat perkolator
dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang
umumnya dilakukan pada temperatur kamar. Proses perkolasi terdiri dari tahap
pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya
(penetesan/penampungan ekstrak), terus-menerus sampai diperoleh perkolat.
B. Cara panas
1. Refluks
Refluksadalah proses penyariansimplisiadenganpelarut pada temperatur
titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif
konstan dengan adanya pendingin balik.
2. Digesti
Digesti adalah proses penyarian simplisia dengan pengadukankontinu pada
3. Sokletasi
Sokletasiadalah proses penyarian menggunakanpelarut yang selalubaru
yang umumnya dilakukandenganmenggunakanalatsokletsehingga terjadi ekstraksi
kontinudengan jumlah pelarutrelatif konstandenganadanyapendinginbalik.
4. Infudasi
Infudasiadalah proses penyarian denganpelarut air padatemperatur 90°C
selama 15 menit.
5. Dekoktasi
Dekoktasi adalah proses penyarian dengan pelarut air pada
temperatur90°C selama 30 menit.
2.3 Uraian Kimia 2.3.1 Alkaloid
Alkaloid adalah senyawa bersifat basa yang mengandung satu atau lebih
atom nitrogen yang terletak dalam sistem siklik yang mempunyai aktivitas
fisiologi yang dapat digunakan dalam bidang pengobatan. Alkaloid biasanya
tidak berwarna, sering sekali bersifat optis aktif, kebanyakan berbentuk kristal
tetapi hanya sedikit yang berupa cairan pada suhu kamar (Harborne, 1987).
Ada tiga pereaksi yang sering digunakan dalam pemeriksaan senyawa
kimia untuk mendeteksi golongan senyawa alkaloid sebagai pereaksi
pengendapan adalah pereaksi Mayer, Bouchardat dan Dragendorff (Depkes RI,
2.3.2 Glikosida
Glikosida adalah senyawa organik yang bila dihidrolisis menghasilkan
satu atau lebih gula yang disebut glikon dan bagian bukan gula yang disebut
aglikon. Gula yang paling sering dijumpai dalam glikosida adalah glukosa. Secara
kimia dan fisiologi, glikosida alam cenderung dibedakan berdasarkan bagian
aglikonnya (Robinson, 1995).
Menurut Farnsworth (1996), berdasarkan hubungan ikatan antara aglikon
dan glikon, glikosida dapat dibagi menjadi empat yaitu:
1. Tipe O-glikosida, ikatan antara bagian glikon dengan aglikon melalui atom O,
contoh: salicin.
2. Tipe S-glikosida, ikatan antara bagian glikon dengan aglikon melalui atom S,
contoh: sinigrin.
3. Tipe N-glikosida, ikatan antara bagian glikon dengan aglikon melalui atom N,
contoh: visin dan krotonosid.
4. Tipe C-glikosida, ikatan antara bagian glikon dengan aglikon melalui atom C,
contoh: aloin.
2.3.3 Saponin
Saponin adalah glikosida triterpenoid dan sterol (Harborne, 1987).
Saponin mula-mula diberi nama demikian karena sifatnya yang menyerupai sabun
(bahasa Latin sapo berarti sabun). Saponin merupakan senyawa aktif permukaan
yang kuat yang menimbulkan busa jika dikocok dalam air dan pada konsentrasi
yang rendah sering menyebabkan hemolisis sel darah merah, dalam larutan yang
sangat encer saponin sangat beracun untuk ikan. Beberapa saponin bekerja
sebagai antimikroba. Saponin merupakan senyawa berasa pahit dan
2.3.4 Steroid/Triterpenoid
Steroid adalah triterpen yang kerangka dasarnya sistem cincin
siklopentana perhidrofenantren. Senyawa steroid dahulu dianggap sebagai
senyawa satwa yaitu sebagai hormon kelamin, asam empedu dan lain-lain. Salah
satu estrogen hewan adalah esteron. Triterpenoid adalah senyawa yang kerangka
karbonnya berasal dari enam satuan isoprena dan secara biosintetis diturunkan
dari hidrokarbon C30 asiklik, yaitu skualen. Senyawa ini berstruktur siklik yang
relatif rumit, kebanyakan berupa alkohol, aldehida atau asam karboksilat. Mereka
berupa senyawa tanpa warna, berbentuk kristal, seringkali bertitik leleh tinggi dan
aktif optik. Triterpenoid dapat dibagi atas 4 golongan senyawa yaitu triterpen
sebenarnya, steroid, saponin dan glikosida jantung (Harborne, 1987).
Pembagian triterpenoid berdasarkan jumlah cincin yang terdapat pada
struktur molekulnya (Robinson, 1995) yaitu:
a. Triterpenoid asiklik, yaitu triterpenoid yang tidak mempunyai cincin tertutup
dalam cincin molekulnya, contoh: skualen.
b. Triterpenoid trisiklik, yaitu triterpenoid yang mempunyai tiga cincin tertutup
dalam cincin molekulnya, contoh: ambrein.
c. Triterpenoid tetrasiklik, yaitu triterpenoid yang mempunyai empat cincin
tertutup dalam cincin molekulnya, contoh: lanosterol.
d. Triterpenoid pentasiklik, yaitu triterpenoid yang mempunyai lima cincin
tertutup dalam cincin molekulnya, contoh: α –amirin.Struktur steroid dan
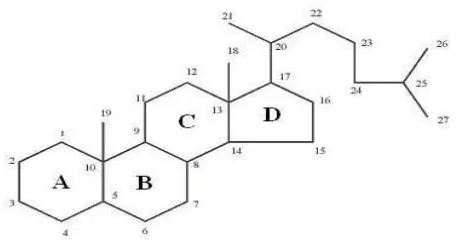
Gambar 2.2Struktur dasar steroid
(Sumber : Robinson, 1995)
2.4Kromatografi
Kromatografi adalah suatu proses pemisahan berdasarkan perbedaan
perpindahan dari komponen-komponen senyawa di antara dua fase yaitu fase
diam (dapat berupa zat cair atau zat padat) dan fase gerak (dapat berupa gas atau
zat cair). Kromatografi serapan dikenal jika fase diam berupa zat padat, jika zat
cair dikenal sebagai kromatografi partisi (Sastrohamidjojo, 1985). Semua
pemisahan dengan kromatografi tergantung pada kenyataan bahwa
senyawa-senyawa yang dipisahkan terdistribusi sendiri di antara fase gerak dan fase diam
dalam perbandingan yang sangat berbeda-beda dari satu senyawa terhadap
senyawa yang lain (Sastrohamidjojo, 1985).
2.4.1 Kromatografi lapis tipis
Kromatografi lapis tipis (KLT) merupakan bentuk kromatografi planar,
dimana fase diamnnya berupa lapisan yang seragam pada permukaan bidang datar
yang didukung oleh lempeng kaca, lempeng aluminium atau lempeng plastik
(Gandjar dan Rohman, 2007). Campuran yang akan dipisah berupa larutan yang
ditotolkan baik berupa bercak ataupun pita. Setelah plat atau lapisan dimasukkan
gerak), pemisahan terjadi selama perambatan kapiler (pengembangan).
Selanjutnya senyawa yang tidak berwarna harus ditampakkan (Stahl, 1985).
a. Penyerap/Fase diam KLT
Fase diam yang digunakan dalam KLT merupakan Penyerap berukuran
kecil dengan diameter partikel antara 10-30 µm. Semakin kecil ukuran rata-rata
partikel fase diam dan semakin sempit kisaran ukuran fase diam maka semakin
baik kinerja KLT. Penyerap yang paling sering digunakan adalah silika dan
serbuk selulosa (Gandjar dan Rohman, 2007).
b. Fase gerak pada KLT
Fase gerak yang digunakan pada KLT dapat dipilih dari pustaka, tetapi
lebih sering dengan mencoba-coba. Biasanya fase gerak yang digunakan berisi
dua campuran pelarut organik karena daya elusi campuran kedua pelarut ini dapat
mudah diatur sedemikian rupa sehingga pemisahan dapat terjadi secara optimal.
Fase gerak yang digunakan harus memiliki tingkat kemurnian yang tinggi
sehingga dapat memberikan pemisahan yang baik (Gandjar dan Rohman, 2007).
c. Harga Rf
Rf atau faktor retardasi didefinisikan sebagai perbandingan antara jarak
yang ditempuh solut dengan jarak yang ditempuh oleh fase gerak. Nilai Rf ini
terkait dengan faktor perlambatan dan nilai ini bukanlah suatu nilai fisika absolut
untuk suatu komponen, meskipun demikian dengan pengendalian kondisi KLT
secara hati-hati, nilai Rf dapat digunakan sebagai cara identifikasi untuk kualitatif.
Nilai maksimum Rf adalah 1 dan nilai minimumnya adalah 0 (Sastrohamidjojo,
1985).
Faktor-faktor yang mempengaruhi harga Rf yaitu struktur kimia dari
senyawa yang dipisahkan, sifat dari penyerap dan derajat aktifitasnya, tebal dan
keterataan dari lapisan penyerap, pelarut dan derajat kemurniannya, derajat
kejenuhan uap pengembang dalam bejana, teknik percobaan, jumlah cuplikan
yang digunakan, suhu dan kesetimbangan (Sastrohamidjojo, 1985).
2.4.2 Kromatografi lapis tipis preparatif
Kromatografi lapis tipis (KLT) preparatif merupakan salah satu
metodepemisahan dengan menggunakan peralatan sederhana. Ketebalan Penyerap
yangsering dipakai adalah 0,5-2 mm. Plat kromatografi biasanya berukuran 20 x
20 cm. Pembatasan ketebalan lapisan dan ukuran plat sudah tentu mengurangi
jumlah bahan yang dapat dipisahkan dengan KLT preparatif. Penyerapyang paling
umumdigunakan adalah silika gel. Penotolan cuplikan dilakukan dengan
melarutkancuplikan dalam sedikit pelarut.Cuplikan ditotolkan berupa pita dengan
jarak sesempit mungkin karena pemisahan tergantung pada lebar pita.Penotolan
dapat dilakukan dengan pipet tetapi lebih baik dengan penotol otomatis.
Pengembangan plat KLT preparatif dilakukan dalam bejana kaca yang dapat
menampung beberapa plat. Bejana dijaga tetap jenuh dengan pelarut pengembang
dengan bantuan kertas saring yang diletakkan berdiri disekeliling permukaan
bagian dalam bejana (Hostettmann, dkk., 1995).
2.4.3 KLT dua arah
KLT duaarahatau KLT
duadimensiinibertujuanuntukmeningkatkanresolusisampelketikakomponen-komponensolutmempunyaikarakteristikkimiayang hampirsama,
sangatberbedadapatdigunakansecaraberurutanpadasuatucampurantertentusehingga
memungkinkanuntukmelakukanpemisahananalit yang
mempunyaitingkatpolaritas yang hampirsama (Gandjar dan Rohman, 2007).
Cuplikan ditotolkan pada satu sudut lapisan yang berbentuk bujur sangkar
dan dikembangkan dengan satu sistem pelarut sehingga campuran terpisah
menurut jalur yang sejajar dengan salah satu sisi. Plat diangkat, dikeringkan,
diputar 90 derajat, lalu diletakkan di dalam sistem pelarut yang kedua sehingga
bercak yang terpisah pada pengembangan pertama terdapat di sepanjang bagian
bawah plat. Komponen yang terpisah (bercak) biasanya terdapat dimana saja pada
lapisan (Gritter, dkk., 1991).
2.5 Spektrofotometri
2.5.1 Spektrofotometri sinar ultraviolet (UV)
Spektrofotometri ultraviolet adalah pengukuran serapan cahaya di daerah
ultraviolet (200-400 nm) oleh suatu senyawa. Semua metode spektrofotometri
berdasarkan pada serapan sinar oleh senyawa yang ditentukan, sinar yang
digunakan adalah sinar monokromatis (Day dan Underwood, 2002).
Prinsip spektrofotometri ultraviolet adalah interaksi yang terjadi antara
energi yang berupa sinar monokromatis dari sumber sinar dengan materi yang
berupa molekul. Prinsip kerja spektrofotometri ultraviolet berdasarkan hukum
Lambert-Beer, bila cahaya/sinar monokromatis melalui suatu media (larutan),
maka sebagian cahaya tersebut diserap, sebagian dipantulkan dan sebagian lagi
dipancarkan ((Dachriyanus, 2004).
Spektrum ultraviolet adalah suatu gambaran yang menyatakan hubungan
(absorbansi).Sinar ultraviolet mempunyai panjang gelombang antara 200-400
nm.Serapan cahayaoleh molekul dalam daerah spektrum ultraviolet tergantung
pada
struktur elektronik dari molekul yang bersangkutan (Sastrohamidjojo, 1985).
Terdapat berbagai faktor yang mengatur pengukuran serapan (absorbansi)
UV (Gandjar dan Rohman, 2007) yaitu :
1. Adanya gugus-gugus penyerap (kromofor)
Kromofor merupakan semua gugus atau atom dalam senyawa organik
yang mampu menyerap sinar ultraviolet dan sinar tampak.
2. Pengaruh pelarut yang digunakan untuk melarutkan sampel
Spektrofotometer ultraviolet padaumumnya digunakanuntuk
(Sastrohamidjojo, 1991):
1. Menentukan jenis kromofor, ikatan rangkap terkonjugasi dan auksokrom dari
suatu senyawa organik.
2. Menjelaskan informasi dari struktur berdasarkan panjang gelombang
maksimum suatu senyawa.
3. Mampu menganalisis senyawa organik secara kuantitatif dengan menggunakan
hukum Lambert-Beer.
2.5.2 Spektrofotometri inframerah
Spektrofotometri inframerah pada umumnya digunakan untuk:
1. Menentukan gugus fungsi suatu senyawa organik
2. Mengetahui informasi struktur suatu senyawa organik dengan membandingkan
daerah sidik jarinya.
Prinsip kerja spektrofotometri inframerah yaitu interaksi energi dengan
pada rentang frekuensi 4000-200 cm-1(Khopkar, 1990). Bentuk spektrum
inframerah yang dihasilkan berupa grafik yang menunjukkan persentase
transmitan yang bervariasi pada setiap frekuensi radiasi inframerah. Satuan
frekuensi yang digunakan pada garis horizontal yang dinyatakan dalam bilangan
gelombang yang didefinisikan sebagai banyaknya gelombang dalam tiap satuan
panjang. Pengukuran pada spektrum inframerah dilakukan pada daerah cahaya
inframerah tengah (mid-infrared) yaitu pada panjang gelombang 2,5–50 �m atau
bilangan gelombang 4000–200 cm-1. Energi yang dihasilkan oleh radiasi ini akan
menyebabkan vibrasi atau getaran pada molekul. Pita absorpsi sinar inframerah
sangat khas dan spesifik untuk setiap tipe ikatan kimia atau gugus fungsi
(Dachriyanus, 2004).
Daerah spektra spektroskopi inframerah dibagi dalam tiga kisaran yaitu
inframerah dekat (12.500-4000 cm-1), inframerah tengah (4000-400 cm-1) dan
inframerah jauh (400-100 cm-1). Daerah inframerah tengah merupakan daerah
yang digunakan untuk penentuan gugus fungsi (Gandjar dan Rohman, 2007).
Identifikasi setiap ikatan yang khas dari setiap gugus fungsi merupakan
basis dari interpretasi spektrum inframerah. Ada beberapa syarat yang harus
dipenuhi dalam menginterpretasikan spektrum (Dachriyanus, 2004) yaitu:
1. Spektrum harus tajam dan jelas.
2. Spektrum harus berasal dari senyawa yang murni.
3. Spektrofotometer harus dikalibrasi sehingga akan menghasilakn pita atau
serapan pada bilangan gelombang yang tepat.
Sinar inframerah yang dilewatkan melalui cuplikan senyawa-senyawa
organik, maka sejumlah frekuensi diserap sedang frekuensi yang lain