FORMULASI SEDIAAN TABLET LIQUISOLID GLIBENKLAMID DENGAN PELARUT GLISERIN DAN AMILUM KENTANG SEBAGAI
CARRIER MATERIAL Buana Cahya Wijaya
NIM : 128114127 INTISARI
Glibenklamid merupakan obat antidiabetik oral golongan sulfonilurea yang digunakan untuk pengobatan diabetes melitus tipe II dan termasuk dalam Biopharmaceutics Classification System (BCS) 2 yang memiliki kelarutan rendah dalam air dan memiliki permeabilitas tinggi. Penelitian ini memformulasikan sediaan tablet liquisolid glibenklamid dengan menggunakan pelarut gliserin dan amilum kentang sebagai carrier material. Tujuan penelitian ini untuk mengetahui pengaruh pelarut gliserin dan amilum kentang sebagai carrier material terhadap sifat fisik dan profil disolusi pada tablet liquisolid glibenklamid serta mengetahui proporsi optimum campuran bahan pelarut gliserin dan amilum kentang sebagai carrier material dalam tablet liquisolid glibenklamid.
Pada penelitian ini menggunakan metode simplex lattice design untuk optimasi formula dengan perbandingan run gliserin : amilum kentang R1 (0%:100%), R2 (0%:100%), R3 (25%:75%), R4 (50%:50%), R5 (50%:50%), R6 (75%:25%), R7 (100%,0%), dan R8 (100%,0%). Pengujian sifat serbuk meliputi indeks kompresibilitas. Pengujian sifat fisik tablet meliputi keseragaman kandungan, kekerasan, waktu hancur, kerapuhan, dan disolusi. Analisis data dengan menggunakan Design Expert 9.0.
ABSTRACT
Glibenclamide is an oral antidiabetics drug used for the treatment of diabetes type II and include as Biopharmaceutics Classification System (BCS) II which has a low solubility in water and high permeability. This research is formulation liquisolid glibenclamide tablet dosage with glycerin solvent and potato starch as carrier material. This study aims to determine the effect of solvents glycerin and potato starch as carrier material on the physical properties and dissolution profile in liquisolid glibenclamide tablet as well as to get optimum proportions of glycerin solvent and potato starch as carrier material in glibenclamide liquisolid tablet.
This study uses the method of optimization models simplex lattice design with a comparison of each formula Run (R) glycerin : potato starch are R1 and R2 (0%: 100%), R3 (25%: 75%), R4 and R5 (50%: 50%), R6 (75% : 25%), R7 and R8 (100%, 0%). Powder evaluation includes compressibility index. Evaluation tablet includes tablet content uniformity, hardness, friability, disintegration time and dissolution.
Data evaluation and evaluation of tablet powder was analyzed by Design Expert 9.0. The results showed that glycerin significantly increase friability, percentage drug dissolution, also decrease tablet hardness and disintegration time of tablet with optimum mixture proportion glycerin : potato starch by an amount of 25 mg and 287 mg (100%: 0%).
FORMULASI SEDIAAN TABLET LIQUISOLID GLIBENKLAMID DENGAN PELARUT GLISERIN DAN AMILUM KENTANG SEBAGAI
CARRIER MATERIAL
Skripsi
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Diajukan oleh: Buana Cahya Wijaya
NIM : 128114127
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
FORMULASI SEDIAAN TABLET LIQUISOLID GLIBENKLAMID DENGAN PELARUT GLISERIN DAN AMILUM KENTANG SEBAGAI
CARRIER MATERIAL
Skripsi
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Diajukan oleh: Buana Cahya Wijaya
NIM : 128114127
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
vii PRAKATA
Puji syukur penulis kepada Tuhan yang Maha Esa karena atas kasih, berkat, dan penyertaan-Nya penulis dapat menyelesaikan skripsi yang berjudul “Formulasi Sediaan Tablet Liquislod Glibenklamid dengan Pelarut Gliserin dan
Amilum Kentang sebagai Carrier Material” dengan baik. Penulisan skripsi ini merupakan salah satu syarat untuk mendapatkan gelar Sarjana Farmasi (S.Farm.) di Fakultas Farmasi Universitas Sanata Dharma.
Selama menyelesaikan perkuliahan, penelitian, dan penulisan skripsi ini peneliti mendapatkan motivasi, kerja keras, pantang menyerah, kritik dan saran dari berbagai pihak. Oleh karena itu penulis ingin mengucapkan terima kasih kepada :
1. Ibu Aris Widyawati, M.Si., PhD., Apt., sebagai Dekan Fakultas Farmasi Universitas Sanata Dharma
2. Bapak Dr. Teuku Nanda Saifullah Sulaiman, M.Si., Apt. sebagi Dosen Pembimbing yang telah banyak memberikan waktu, bimbingan, kritik, dan saran mulai dari penulisan proposal, penelitian, hingga penulisan skripsi.
3. Ibu Wahyuning Setyani, M.Sc., Apt., sebagai dosen penguji yang telah memberikan waktu masukan, kritik dan saran kepada penulis. 4. Ibu Dr. Dewi Setyaningsih, M.Sc., Apt., sebagai dosen penguji yang
viii
5. dr. Fenty M.Kes., Sp.PK sebagai dosen pembimbing akademik atas pendampingannya selama perkuliahan.
6. Ibu Agustina Setiawati, M.Sc., Apt sebagai Kepala Penanggung Jawab Laboratorium Fakultas Farmasi Universitas Sanat Dharma Yogyakarta yang telah memberikan ijin dalam penggunaan fasilitas laboratorium untuk kepentingan penelitian ini.
7. Semua dosen-dosen Fakultas Farmasi Universitas Sanata Dharma Yogyakarta yang telah sabar dalam mendidik dan memberikan ilmu kepada penulis selama menempuh pendidikan di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
8. Bapak Musrifin, Bapak Agung, Mas Kunto, Bapak Parlan, Bapak Kayat dan segenap laboran dan staff karyawan, yang telah membantu selama penelitian berlangsung.
9. Adhi darma Wijaya, Debbie Lukito, Indra Cahya Wijaya dan Veronica Cahya Wijaya sebagai orang tua dan kakak yang selalu memberikan doa, semangat dan finansial sehingga penulis dapat menyelesaikan penelitian ini.
10.Teman skripsi seperjuangan Yudha Adi Prabowo dan Desion Sudi yang dapat bekerja sama dengan baik selama penelitian berlangsung. 11.Sahabat-sahabatku Bartolomeus Widiasta, Laurensius Danang
ix
Evelina Larisa, Lotmi Barasa, Vinsensia Septima yang selalu memberikan dukungan, semangat, motivasi, dan persahabatan yang paling berkesan sampai selamanya.
12.Grup “Change or Die” yang selalu memberikan dukungan semangat kepada penulis
13.Teman-teman FST B 2012 dan angkatan 2012 Fakultas Farmasi Universitas Sanata Dharma yang juga memberikan warna selama masa perkuliahan penulis.
14.Semua pihak yang tidak dapat penulis sebutkan satu persatu yang telah memberikan doa, bantuan, dan dukungan selama penelitian skripsi.
Penulis menyadari bahwa penyusun skripsi ini masih banyak kekurangan mengingat keterbatasan kemampuan serta pengalaman yang dimiliki. Oleh karena itu, kritik dan saran yang membangun sangat diperlukan oleh penulis untuk menyempurnakan skripsi ni. Semoga skripsi ini dapat bermanfaat bagi perkembangan ilmu pengetahuan.
Yogyakarta, 20 Juli 2016
xiv
2. Kekerasan tablet ... 41
3. Kerapuhan tablet ... 43
4. Waktu hancur tablet ... 44
D. Hasil uji Penetapan Kadar tablet ... 46
E. Hasil Uji Disolusi Tablet ... 47
1. Penentuan Panjang gelombang maksimum ... 47
2. Penentuan Persamaan Kurva baku ... 48
3. Uji Disolusi Obat ... 49
F. Penentuan Formula Optimum ... 52
BAB V. KESIMPULAN DAN SARAN ... 54
A. Kesimpulan ... 54
B. Saran ... 54
DAFTAR PUSTAKA ... 55
LAMPIRAN ... 60
xv
DAFTAR TABEL
Tabel I. Hubungan sudut diam dan sifat alir serbuk ... 12
Tabel II. Parameter indeks kompresibilitas, hausner ratio, dan kategori .. 14
Tabel III. Penggunaan uji keseragaman pada sediaan tablet ... 16
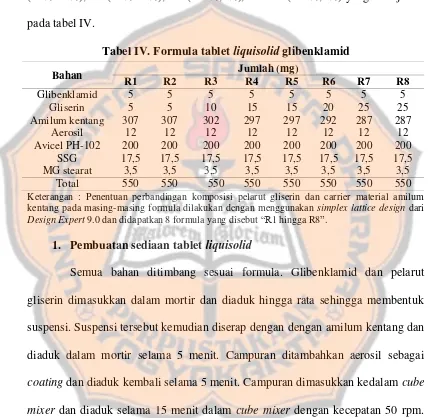
Tabel IV. Formula tablet liquisolid glibenklamid ... 28
Tabel V. Hasil uji homogenitas serbuk liquisolid ... 39
Tabel VI. Hasil penetapan kadar tablet liquisolid glibenklamid ... 46
Tabel VII. Pemberian nilai dan bobot pada respon ... 52
xvi
DAFTAR GAMBAR
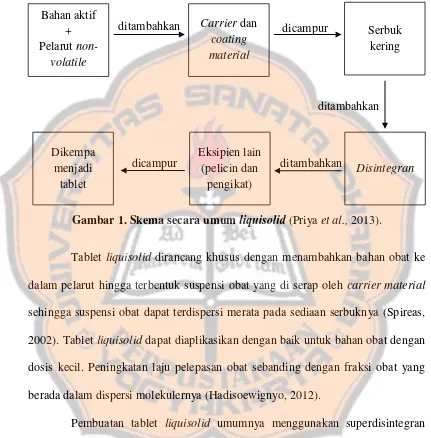
Gambar 1. Skema secara umum liquisolid ... 8
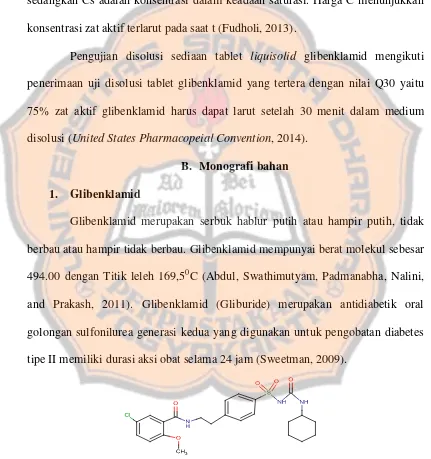
Gambar 2. Struktur kimia glibenklamid ... 18
Gambar 3. Struktur kimia gliserin ... 20
Gambar 4. Struktur kimia amilum kentang ... 20
Gambar 5. Model plot respon indeks kompresibilitas serbuk ... 36
Gambar 6. Spectrum graph glibenklamid dalam Methanol ... 37
Gambar 7. Kurva Baku Glibenklamid dalam metanol ... 38
Gambar 8. Model plot respon keseragaman kandungan tablet ... 40
Gambar 9. Model plot respon kekerasan tablet ... 42
Gambar 10. Model plot respon kerapuhan tablet ... 43
Gambar 11. Model plot respon waktu hancur tablet ... 45
Gambar 12. Spectrum graph glibenklamid dalam bufer fosfat pH 8,5 ... 47
Gambar 13. Kurva baku glibenklamid dalam bufer fosfat ... 48
Gambar 14.a Profil disolusi tablet liquisolid glibenklamid R1-R4 (n=6) ... 49
Gambar 14.b Profil disolusi tablet liquisolid glibenklamid R5-R8 (n=6) ... 50
Gambar 15. Model plot respon disolusi tablet ... 51
xvii
DAFTAR LAMPIRAN
Lampiran 1. Sertifikat Analisis (Certificate Of Analysis COA) ... 60
Lampiran 2. Hasil spektrofotometer UV glibenklamid ... 67
Lampiran 3. Data hasil uji sifat alir serbuk ... 69
Lampiran 4. Data hasil uji homogenitas campuran ... 70
Lampiran 5. Data hasil uji sifat fisik tablet ... 71
Lampiran 6. Data penetapan kadar tablet ... 77
Lampiran 7. Data hasil uji disolusi tablet ... 78
Lampiran 8. Perhitungan keseragaman kandungan ... 102
Lampiran 9. Perhitungan disolusi tablet ... 104
Lampiran 10. Data hasil kurva baku glibenklamid ... 106
Lampiran 11. Analisis statistik sifat alir, sifat fisik dan disolusi tablet liquisolid glibenklamid dengan Design Expert 9.0 dan formula optimum ... 109
Lampiran 12. Analisis statistik sediaan tablet liquisolid glibenklamid dengan menggunakan sofware R studio 3.23 ... 114
xviii INTISARI
Glibenklamid merupakan obat antidiabetik oral golongan sulfonilurea yang digunakan untuk pengobatan diabetes melitus tipe II dan termasuk dalam Biopharmaceutics Classification System (BCS) 2 yang memiliki kelarutan rendah dalam air dan memiliki permeabilitas tinggi. Penelitian ini memformulasikan sediaan tablet liquisolid glibenklamid dengan menggunakan pelarut gliserin dan amilum kentang sebagai carrier material. Tujuan penelitian ini untuk mengetahui pengaruh pelarut gliserin dan amilum kentang sebagai carrier material terhadap sifat fisik dan profil disolusi pada tablet liquisolid glibenklamid serta mengetahui proporsi optimum campuran bahan pelarut gliserin dan amilum kentang sebagai carrier material dalam tablet liquisolid glibenklamid.
Pada penelitian ini menggunakan metode simplex lattice design untuk optimasi formula dengan perbandingan run gliserin : amilum kentang R1 (0%:100%), R2 (0%:100%), R3 (25%:75%), R4 (50%:50%), R5 (50%:50%), R6 (75%:25%), R7 (100%,0%), dan R8 (100%,0%). Pengujian sifat serbuk meliputi indeks kompresibilitas. Pengujian sifat fisik tablet meliputi keseragaman kandungan, kekerasan, waktu hancur, kerapuhan, dan disolusi. Analisis data dengan menggunakan Design Expert 9.0.
xix ABSTRACT
Glibenclamide is an oral antidiabetics drug used for the treatment of diabetes type II and include as Biopharmaceutics Classification System (BCS) II which has a low solubility in water and high permeability. This research is formulation liquisolid glibenclamide tablet dosage with glycerin solvent and potato starch as carrier material. This study aims to determine the effect of solvents glycerin and potato starch as carrier material on the physical properties and dissolution profile in liquisolid glibenclamide tablet as well as to get optimum proportions of glycerin solvent and potato starch as carrier material in glibenclamide liquisolid tablet.
This study uses the method of optimization models simplex lattice design with a comparison of each formula Run (R) glycerin : potato starch are R1 and R2 (0%: 100%), R3 (25%: 75%), R4 and R5 (50%: 50%), R6 (75% : 25%), R7 and R8 (100%, 0%). Powder evaluation includes compressibility index. Evaluation tablet includes tablet content uniformity, hardness, friability, disintegration time and dissolution.
Data evaluation and evaluation of tablet powder was analyzed by Design Expert 9.0. The results showed that glycerin significantly increase friability, percentage drug dissolution, also decrease tablet hardness and disintegration time of tablet with optimum mixture proportion glycerin : potato starch by an amount of 25 mg and 287 mg (100%: 0%).
1 BAB I PENDAHULUAN
A.Latar Belakang
Glibenklamid adalah salah satu obat antidiabetik oral golongan sulfonilurea generasi kedua yang digunakan untuk pengobatan diabetes tipe II. Glibenklamid merupakan obat yang termasuk dalam Biopharmaceutics Classification System (BCS) 2 yang memiliki kelarutan yang rendah dalam air dan
memiliki permeabilitas tinggi (Sirisha, Sruthi, and Eswariah, 2012). Pada obat yang termasuk dalam BCS II, bioavailabilitas obat ditentukan dari kelarutan obat tersebut dalam cairan gastrointestinal (Savjani, Gajjar and Savjani, 2012), sehingga diperlukan teknik dalam formulasi untuk meningkatkan kelarutan obat, diantaranya pengecilan ukuran partikel (mikronisasi), penambahan surfaktan, pembuatan obat dalam bentuk garam, pembentukan kompleks, atau dengan pembuatan dispersi solid, dan Liquisolid (Hadisoewignyo, 2012).
non-volatile. Contoh pelarut yang biasa digunakan PEG, propilen glikol, tween,
gliserin, dimetil etil asetamida, polisorbat (Syed and Pavani, 2012). Syarat carrier material yaitu harus memiliki daya absorpsi yang tinggi sehingga dapat menyerap
suspensi obat. Contoh carrier material yaitu starch, cellulose dan laktosa (Kulkarni, Aloorkar, Mane and Gaja, 2010).
Pada penelitian ini digunakan pelarut berupa gliserin, bahan ini banyak digunakan sebagai bahan tambahan pada suatu formulasi untuk meningkatkan kelarutan obat yang sukar larut dalam air. Glibenklamid memiliki kelarutan dalam gliserin yang cukup tinggi dibandingkan beberapa pelarut lainnya yaitu sebesar 7,17 µg/mL (Singh et al., 2012). Gliserin diketahui telah berhasil digunakan untuk formulasi likuisolid dan dapat memperbaiki profil disolusi pada beberapa obat seperti Spironoloacton (Akbari et al., 2015), indometachin (Saeedi et al., 2011).
Formulasi sediaan tablet liquisolid glibenklamid dengan pelarut gliserin dan amilum kentang sebagai carrier material diharapkan mampu memberikan pengaruh terhadap sifat fisik dan persentase obat yang terdisolusi serta mendapatkan proporsi formula optimum sediaan tablet liquisolid glibenklamid.
B. Rumusan Masalah
Berdasarkan latar belakang yang telah dikemukakan sebelumnya, timbul beberapa masalah yang akan diteliti sebagai berikut:
1. Bagaimana pengaruh pelarut gliserin dan amilum kentang sebagai carrier material terhadap sifat fisik dan profil disolusi tablet liquisolid glibenklamid?
2. Berapa proporsi optimum campuran pelarut gliserin dan amilum kentang sebagai carrier material dalam tablet liquisolid glibenklamid?
C. Keaslian Penelitian
Telah dilakukan beberapa penelitian tentang formulasi sediaan tablet liquisolid glibenklamid dengan berbagai macam kombinasi pelarut dan carrier
material diantaranya PEG 400 dengan MCC oleh Sirisha (2012), propilen glikol
dengan Amilum kentang oleh Arun Kumar (2012), Synperonic PE/L44, dan Cremophor ELP dengan Amilum kentang oleh Javaheri (2014). Formulasi sediaan tablet Glibenklamid untuk meningkatkan kecepatan disolusi dengan teknik Liquisolid dengan kombinasi pelarut tween 80 dan carrier material dengan Amilum jagung oleh Sirisha (2012). Sejauh penelusuran peneliti, penelitian tentang “Formulasi Sediaan Tablet Liquisolid Glibenklamid dengan Pelarut
D. Manfaat Penelitian a. Manfaat teoritis
Penelitian ini diharapkan dapat memberikan manfaat bagi penelitian untuk pengembangan formulasi tablet liquisolid glibenklamid dengan pelarut gliserin dan amilum kentang sebagai carrier material.
b. Manfaat praktis
Penelitian ini diharapkan dapat memberikan informasi tentang sediaan tablet liquisolid gilbenklamid bagi masyarakat.
E. Tujuan Penelitian a) Tujuan umum
Mengetahui pengaruh pelarut gliserin dan amilum kentang sebagai carrier material terhadap sifat fisik dan profil disolusi tablet liquisolid glibenklamid.
b) Tujuan khusus
Mengetahui proporsi campuran pelarut gliserin dan amilum kentang sebagai carrier material terhadap sifat fisik dan profil disolusi tablet liquisolid
5 BAB II
TINJAUAN PUSTAKA
A. Tablet Liquisolid 1. Definisi liquisolid
Liquisolid merupakan suatu teknik pembuatan tablet untuk meningkatkan
laju disolusi obat yang diperkenalkan oleh Spires pada tahun 2002 (Spireas, 2002). Metode ini telah diketahui dapat meningkatkan luas permukaan obat dan persen obat terbasahi, liquisolid pada obat dengan kelarutan yang rendah dalam air diharapkan dapat meningkatkan pelepasan dan bioavailabilitas obat secara oral (Pavani, Noman dan Syed, 2013). Formulasi tablet liquisolid dapat diterapkan pada berbagai macam obat yang sukar larut air atau hampir tidak larut air dengan dosis obat yang kecil (kurang dari 100 mg) (Sinkar, Gondkar and Saudagar, 2015).
2. Keuntungan dan Kerugian dari Teknik Liquisolid
dibutuhkan penambahan pelarut, carrier material dan coating material dalam jumlah yang besar untuk mendapatkan sifat alir dan kompresibilitas baik sehingga dapat meningkatkan bobot tablet (Syed et al., 2012).
3. Komponen tablet liquisolid a. Pelarut non volatile
Pelarut non volatile merupakan bahan yang bertindak sebagai surfakatan untuk membantu kelarutan bahan aktif dalam air. Syarat pelarut dalam liquisolid bersifat inert, tidak menguap, memiliki titik didih tinggi, dapat melarutkan bahan aktif dan dapat terdispersi dalam sistem liquisolid. Contoh pelarut non–volatile yang dapat digunakan dalam formulasi tablet liquisolid antara lain PEG, propilen glikol, tween, gliserin, dimetil etil asetamida, polisorbat (Syed et al., 2012).
b. Carrier material
Carrier material merupakan bahan yang berfungsi sebagai penyerap
liquid medication dalam formulasi tablet liquisolid. Syarat carrier material yang
dapat digunakan dalam formulasi liquisolid antara lain memiliki pori dan daya serap yang mencukupi untuk menyerap liquid medication. Contoh carrier yang dapat digunakan dalam formulasi tablet liquisolid antara lain amilum, beberapa tingkatan microcrystalline cellulose dan laktosa. (Syed et al., 2012).
c. Coating material
Coating material merupakan bahan yang digunakan untuk melapisi
dan daya adsorpsi yang tinggi untuk menghasilkan serbuk yang kering dan memiliki laju alir yang baik. Coating material yang relatif sering digunakan dalam formulasi liquisolid adalah colloidal silicon dioxide (Aerosil®, Cab-O-Sil® M5) (Vraníková and Gajdziok, 2013).
d. Superdisintegran
Superdisintegran merupakan bahan yang digunakan untuk mempercepat waktu hancurnya tablet dalam medium air, dan dapat terdisintegrasi menjadi partikel penyusunnya sehingga akan meningkatkan kecepatan disolusi dan tercapainya bioavailabilitas yang diharapkan. Jenis bahan penghancur seperti pati dan jenis-jenis lainnya merupakan jenis bahan penghancur yang umumnya digunakan dan harganya relatif murah. Biasanya digunakan dengan konsentrasi 5-20% dari berat tablet (Lachman, Ziff and Spiro, 1994). Syarat-syarat bahan superdisintegran harus menghasilkan kehancuran yang cepat, memenuhi kompaktibilitas yang baik, ukuran partikel kecil,dan memiliki sifat alir yang baik (Debjit, Chiranjib, Krishnakanth, Pankaj, and Chandira, 2009). Superdisintegran memiliki daya mengembang yang sangat tinggi dan cepat pada medium air sehingga mampu mendesak penyusun tablet lainnya ke arah luar secara cepat yang akan menyebabkan tablet dapat segera hancur (Sulaiman, 2007).
4. Cara pembuatan sediaan tablet liquisolid
dicampur ditambahkan
ditambahkan
dicampur ditambahkan
coating material (Gubbi and Jarag, 2009). Berikut merupakan tahapan secara
umum pembuatan tablet liquisolid pada gambar 1.
ditamba
dicampur
Gambar 1. Skema secara umum liquisolid (Priya et al., 2013).
Tablet liquisolid dirancang khusus dengan menambahkan bahan obat ke dalam pelarut hingga terbentuk suspensi obat yang di serap oleh carrier material sehingga suspensi obat dapat terdispersi merata pada sediaan serbuknya (Spireas, 2002). Tablet liquisolid dapat diaplikasikan dengan baik untuk bahan obat dengan dosis kecil. Peningkatan laju pelepasan obat sebanding dengan fraksi obat yang berada dalam dispersi molekulernya (Hadisoewignyo, 2012).
Pembuatan tablet liquisolid umumnya menggunakan superdisintegran dan bahan pelicin. Superdisintegran dapat membuat tablet menjadi mudah untuk hancur sehingga dapat membuat tablet menjadi lebih cepat untuk terdisolusi. Bahan pelicin digunakan untuk memudahkan serbuk untuk mengalir sehingga dapat dikempa menjadi tablet (Hadisoewignyo, 2012).
5. Mekanisme meningkatnya pelepasan obat liquisolid a. Meningkatnya luas permukaan bahan obat
Ketika obat dalam sistem liquisolid larut dalam pelarut non-volatile, obat akan berada pada keadaan dispersi molekuler di dalam carrier. Hal ini menyebabkan luas permukaan obat menjadi besar sehingga pelepasan obat meningkat. Dalam tablet liquisolid, pelepasan obat akan menjadi cepat karena luas permukaan obat besar dibanding dengan partikel obat yang dibuat dengan metode cetak langsung yang memiliki luas permukaan yang kecil untuk obat yang sulit larut (Vraníková et al., 2013).
b. Meningkatnya kelarutan obat dalam air
Perlu diketahui bahwa sedikit jumlah pelarut non-volatile dalam liquisolid tidak ikut melarutkan bahan obat. Pada antar permukaan padat-cairan
(liquisolid tablet dan medium disolusi), sangat memungkinkan sedikit jumlah dari pelarut tersebut berdifusi keluar bersama dengan molekul obat dan bertindak sebagai ko-solven yang akan membantu meningkatkan kelarutan bahan obat dalam air (Lohithatsu et al., 2014).
c. Meningkatkan proses pembasahan
6. Model matematika tablet liquisolid
Suatu pendekatan matematika yang dinyatakan Spireas dalam formulasi liquisolid untuk menghitung jumlah non-volatile solvent, carrier material dan
coating material sehingga serbuk liquisolid memiliki kemampuan mengalir dan
kompresibilitas yang baik. Rasio eksipien (R) merupakan rasio dari jumlah carrier (Q) dan coating material (q), nilai R ditunjukan dengan persaaman (1)
R = ... (1)
Liquid load factor (Lf) merupakan rasio dari jumlah liquid medication (W) dan carrier material (Q). Nilai Lf ditunjukkan persamaan (2).
Lf = ... (2)
(Hadisoewignyo, 2012). Hubungan antara liquid load factor (Lf) dan nilai R ditunjukkan dengan persamaan (3) dan persamaan (4).
Lf = ɸ + φ (1/R) ... (3) Lf = Ψ+ϕ (1/R) ... (4) Nilai Ψ danϕ menyatakan jumlah maksimum pelarut non-volatile yang digunakan dan memiliki kompaktibilitas yang baik yang ditandai dengan kekerasan tablet yang mencukupi dan tanpa adanya cairan yang keluar pada saat pencetakan tablet (Abbas, Rasool, and Rajab, 2014 ).
7. Uji sifat alir serbuk liquisolid
Sifat alir serbuk sangat penting dalam memastikan proses pencampuran yang efisien serta menjaga keseragaman bobot tiap tablet saat dikempa. Sifat alir serbuk dipengaruhi oleh ukuran, bentuk partikel, bobot jenis, kelembapan yang menyebabkan adanya kohesif antar partikel. (Siregar, 2008). Metode-metode yang dapat digunakan dalam mengevaluasi sifat alir serbuk antara lain:
a. Sudut diam
menggunakan metode sudut jatuh. (Siregar, 2008). Hubungan sudut diam dan sifat alir serbuk ditunjukkan pada tabel I.
Tabel I. Hubungan sudut diam dan sifat alir serbuk Sudut diam (o) Sifat aliran
Kecepatan alir merupakan waktu yang dibutuhkan sejumlah serbuk untuk mengalir melalui suatu alat. Mudah tidaknya granul atau serbuk dipengaruhi oleh bentuk, luas permukaan, kerapatan, kelembaban granul.
Kecepatan alir serbuk =
c. Kerapatan serbuk ruahan
Kerapatan serbuk ruahan adalah perbandingan antara massa serbuk yang belum dimampatkan terhadap volume termasuk kontribusi volume pori antarpartikel. Kerapatan serbuk ruahan tergantung pada kepadatan partikel serbuk dan susunan partikel serbuk. Pengukuran dilakukan dengan menggunakan gelas ukur maka kerapatan serbuk ruahan dinyatakan dalam gram per mL (g/mL). Kerapatan serbuk ruahan, dapat dihitung dengan rumus:
M merupakan bobot serbuk dan Vo merupakan volume wadah dalam satuan mL (Depkes RI, 2014).
d. Kerapatan serbuk mampat
Kerapatan serbuk mampat adalah tingkatan dari kerapatan serbuk mampat yang diperoleh dengan cara mengetuk dengan secara mekanis gelas ukur atau bejana pengukur yang berisi serbuk. Kerapatan serbuk mampat, dapat dihitung dengan rumus :
... (7)
M merupakan bobot serbuk dan Vf merupakan volume setelah pengetukan. (Depkes RI, 2014). e. Hausner ratio
Hausner ratio merupakan angka yang berhubungan dengan kemampuan
alir dari serbuk, dan tidak bernilai mutlak untuk suatu bahan tertentu, tergantung dari metode yang digunakan untuk menentukannya (Arulkumaran and Padmapreetha, 2014).
Uji Hausner ratio dapat dinyatakan dengan rumus :
...(9)
Vo merupakan bobot volum sebelum dimampatkan dan Vf merupakan bobot volum setelah pengetukan (Depkes RI, 2014).
f. Indeks kompresibilitas
indeks pengetapan serbuk atau granul, semakin baik sifat alirnya. Sebaliknya, semakin besar indeks pengetapan serbuk atau granul, semakin buruk sifat alirnya (Sirisha et al., 2012). Uji ini dapat dinyatakan dengan rumus :
...(8)
(Depkes RI, 2014). Berikut merupakan paramater indeks kompresibilitas, hausner ratio dan kategori yang disajikan pada tabel II.
Tabel II. Parameter indeks kompresibilitas, hausner ratio, dan kategori Indeks kompresibilitas (%) Hausner ratio Kategori
< 10 1,00-1,11 Sangat Baik
11-15 1,12-1,18 Baik
16-20 1,19-1,25 Cukup Baik
21-25 1,26-1,34 Agak Baik
26-31 1,35-1,45 Buruk
32-37 1,46-1,59 Sangat Buruk
>38 > 1,60 Sangat Buruk Sekali
(Arulkumaran et al., 2014). g. Distribusi Ukuran Partikel
Ukuran dan distribusi ukuran partikel atau granul akan mempengaruhi bobot tablet, keseragaman bobot, waktu disintegrasi, kerapuhan (friabilitas) sifat alir, dan kinetika kecepatan pengeringan pada granulasi basah. Metode yang sering digunakan untuk mengukur ukuran partikel dan distribusi partikel adalah mikroskopi, pengayakan dan sedimentasi (Dewi, 2010).
h. Kandungan Lembab (Moisture Content)
mengetahui kelembaban suatu bahan padat adalah dengan perhitungan menggunakan data berdasarkan bobot keringnya. Angka hasil perhitungan ini dianggap sebagai kandungan lembab (MC/moisture content) (Sulaiman, 2007). Persamaan untuk menghitung moisture content yaitu:
...(10)
(Dewi, 2010). 8. Uji Mutu tablet liquisolid
a. Keseragaman bobot
Keseragaman bobot tablet menentukan dosis dari tiap tablet yang telah diproduksi. Keseragaman bobot dapat ditentukan berdasarkan penetapan kadar zat aktif pada contoh bets yang mewakili menggunakan metode analisis yang sesuai (Depkes RI, 2014). Variasi bobot tablet yang dikempa dipengaruhi oleh jumlah serbuk yang memenuhi die pada proses pengempaan tablet (Allen, Popovich, Ansel, 2014).
b. Keseragaman kandungan
Uji keseragaman kandungan berdasarkan pada penetapan kadar masing – masing kandungan zat aktif dalam satuan sediaan. Keseragaman kandungan untuk sediaan padat ditentukan dengan cara menetapkan kadar masing-masing 10 satuan menggunakan metode analisis yang sesuai dan kemudian dihitung nilai penerimaan. Perhitungan nilai penerimaan dengan rumus :
M merupakan nilai rujukan , merupakan rata-rata dari masing-masing kandungan (X1, X2,…Xn) yang dinyatakan dalam persentase, k merupakan konstanta penerimaan dan s merupakan simpangan baku sampel.
Berikut merupakan penggunaan uji keseragaman pada sediaan tablet yang disajikan pada tabel III.
Tabel III. Penggunaan uji keseragaman pada sediaan tablet
Bentuk sediaan Tipe Sub tipe Dosis dan perbandingan zat aktif Tablet ≥ 25 mg dan ≥ 25% < 25 mg atau < 25%
Tidak bersalut
Keragaman bobot Keseragaman kandungan Salut Selaput Keragaman bobot Keseragaman
kandungan
Tablet harus cukup kuat untuk mempertahankan bentuk selama mengalami perlakuan mekanik pada saat proses pengemasan, transportasi, hingga pada saat pemakaian (Arulkumaran et al., 2014). Kekerasan tablet merupakan parameter penting dalam pembuatan tablet karena dapat mempengaruhi proses disintegrasi dan disolusi tablet (Allen et al., 2014). Kekerasan tablet dipengaruhi oleh bobot bahan, kompatibilitas bahan, tekanan pengempaan, celah antara punch atas dan punch bawah pada saat pengempaan pengempaan (Siregar, 2008)
d. Kerapuhan tablet
akibat goncangan atau gesekan selama pengangkutan. Kerapuhan tablet dianggap cukup baik bila hasilnya kurang dari 1 % (Sulaiman, 2007).
e. Waktu hancur tablet
Waktu hancur tablet adalah waktu yang diperlukan tablet untuk pecah dan menjadi partikel-partikel penyusunnya, sehingga akan meningkatkan luas permukaan yang kontak dengan cairan dalam tubuh. Tekanan kompresi akan mempengaruhi waktu hancur tablet. Semakin besar tekanan kompresinya pada maka waktu hancur tablet makin lambat (Siregar, 2008). Waktu yang diperlukan untuk menghancurkan tablet tidak lebih dari 15 menit (Allen et al., 2014). Selain tekanan kompresi waktu hancur tablet juga dipengaruhi oleh pemilihan bahan pembuatan tablet (Aulton, 2007)
f. Disolusi tablet
Disolusi adalah proses melarutnya zat aktif (bahan obat) dalam sediaan obat ke dalam suatu medium. Pada umumnya medium yang digunakan berupa air. Disolusi merupakan proses kinetik, sehingga prosesnya diamati dari pengamatan terhadap jumlah zat aktif yang terlarut ke dalam medium sebagai fungsi waktu. Disolusi juga merupakan tahap penentu terjadinya absorpsi. Berdasarkan laju disolusi, dapat diperkirakan kecepatan absorbsi yang mempengaruhi mulai kerja, intensitas, dan lama kerja obat di dalam tubuh.Pada tahun 1897, Noyes dan Whitney mencoba menguantifikasikan jumlah obat yang terlarut melalui persamaan :
W merupakan berat zat aktif yang terlarut dalam medium selama waktu t, sehingga dW/dt adalah kecepatan disolusi zat aktif (gram/waktu). D adalah koefisien difusi zat yang terlarut dalam medium yang digunakan, S adalah luas kontak muka zat aktif- medium, h adalah tebal lapisan tipis (film-difusi), sedangkan Cs adalah konsentrasi dalam keadaan saturasi. Harga C menunjukkan konsentrasi zat aktif terlarut pada saat t (Fudholi, 2013).
Pengujian disolusi sediaan tablet liquisolid glibenklamid mengikuti penerimaan uji disolusi tablet glibenklamid yang tertera dengan nilai Q30 yaitu 75% zat aktif glibenklamid harus dapat larut setelah 30 menit dalam medium disolusi (United States Pharmacopeial Convention, 2014).
B. Monografi bahan 1. Glibenklamid
Glibenklamid merupakan serbuk hablur putih atau hampir putih, tidak berbau atau hampir tidak berbau. Glibenklamid mempunyai berat molekul sebesar 494.00 dengan Titik leleh 169,50C (Abdul, Swathimutyam, Padmanabha, Nalini, and Prakash, 2011). Glibenklamid (Gliburide) merupakan antidiabetik oral golongan sulfonilurea generasi kedua yang digunakan untuk pengobatan diabetes tipe II memiliki durasi aksi obat selama 24 jam (Sweetman, 2009).
Glibenklamid bekerja dengan menurunkan kadar glukosa dalam darah dengan merangsang sel β Langerhans pankreas untuk memproduksi insulin. Kanal
Ca terbuka dan ion Ca2+akan masuk sel β, merangsang granula yang berisi insulin dan akan terjadi sekresi insulin dengan jumlah yang ekuivalen dengan peptida-C. Dosis yang dianjurkan untuk DM tipe 2 adalah 2,5-5 mg setiap hari. Pada penggunaan dosis yang besar dapat menyebabkan hipoglikemia. Glibenklamid lebih efektif diminum 30 menit sebelum makan agar mencapai kadar optimal di plasma. Obat ini cepat diserap dalam saluran pencernaan, cukup diberikan satu kali sehari (Suherman, 2007).
Glibenklamid tidak larut dalam air, agak sukar larut dalam metilen klorida, sukar larut dalam etanol dan metanol (Sweetman, 2009). Glibenklamid termasuk salah satu obat yang masuk dalam golongan 2 dari Sistem Klasifikasi Biofarmasetika (BCS) yang memiliki kelarutan yang rendah dalam air dan memiliki permeabilitas yang tinggi (Sirisha et al., 2012). Glibenklamid memiliki serapan maksimum pada panjang gelombang 229,5 nm dalam metanol (Sudharshan and Bonde, 2009). Glibenklamid dalam medium disolusi buffer phosphate pH 8.5 memiliki panjang gelombang 204.5 nm (Gianotto, Arantes, Larra-Filho, Filho, and Fregonezi-Nery, 2007).
2. Gliserin
Gliserin merupakan pelarut non-volatile yang digunakan dalam pembuatan tablet liquisolid (Kulkarni et al., 2010). Gliserin memiliki sifat yang stabil pada suhu ruang, tidak toksik dan tidak mengiritasi (Alvarez-Nunez and Medina, 2004).
Gambar 3. Struktur kimia gliserin (Alvarez-Nunez and Medina, 2004). 3. Amilum Kentang
Amilum kentang atau pati kentang memiliki pemerian pemerian serbuk putih yang tidak berbau dan tidak berasa. Amilum kentang memiliki berat molekul 0,8-0,9 g/cm3. Amilum kentang mengandung amilosa sebesar 20-23%. Amilum praktis tidak larut dalam air dingin dan ethanol dan larut dalam air panas. Amilum kentang memiliki sifat yang stabil pada suhu ruang dan bersifat inert (Häusler, 2009).
Gambar 4. Struktur kimia amilum kentang (Häusler, 2009).
membentuk jembatan hidrofil sehingga apabila tablet kontak dengan air, air akan segerap diserap dengan cepat oleh tablet melalui jembatan hidrofil (Sulaiman, 2007).
Amilum baik digunakan sebagai pengisi dan penghancur dalam tablet karena memiliki daya kompak, dapat menyerap air dan dapat terdisintegrasi dengan baik saat pelepasan obat dalam medium air (Siregar, 2008). Amilum kentang dapat digunakan sebagai carrier sebagai peningkat bioavailabilitas obat dengan kelarutan yang rendah (Häusler, 2009).
4. HDK Wacker N20 (Aerosil)
Aerosil merupakan silikon dioksida murni yang diketahui dalam jumlah kecil dapat menyerap air yang cukup besar. Aerosil berbentuk serbuk keputih-putihan, ringan, tidak berbau, dan tidak berasa yang memiliki berat molekul sebesar 60,08 dan praktis tidak larut dalam pelarut organik, air, dan asam, kecuali asam hidrofluorat. Larut dalam larutan hangat hidroksida alkali. Aerosil dapat berfungsi sebagai glidant pada konsentrasi 0,1-0,5% (Hapgood, 2009).
5. Avicel PH 102
yang baik dan dapat meningkatkan waktu hancur (Sulaiman, 2007). Avicel PH-102 merupakan pengikat kering yang cukup efektif dalam pencampuran kering (Siregar, 2008). Avicel PH-102 memiliki ukuran partikel 100 μm, kadar airnya 3 -5%, dan bobot jenis 0,28 – 0,33 g/mL (Guy, 2009). Avicel juga dapat meningkatkan laju alir dan mengurangi variasi dari berat tablet (Ohwoavworhua, Adelakun and Okhamafe, 2009).
6. Sodium Starch Glycolate (SSG)
Sodium Starch Glycolate (SSG) Pemeriannya berupa serbuk putih, tidak
berbau, tidak berasa, dan mudah mengalir dan sangat higroskopis. SSG memiliki nama lain yaitu explotab®carboxymethyl starch, sodium salt, primojel®. Larut sebagian dalam etanol 95% dan praktis tidak larut dalam air. Sodium Starch Glycolate merupakan contoh superdisintegran yang dapat mengembang cepat
ketika kontak dengan medium air dan sering digunakan pada formulasi tablet liquisolid. SSG umum digunakan sebagai penghancur pada konsentrasi 2 hingga
8% (Young, 2009).
7. Magnesium Stearat
dapat menurunkan kekerasan, kecepatan disintegrasi, kecepatan disolusi serta dapat meningkatkan kerapuhan tablet (Allen and Luner, 2009).
C. Landasan teori
Liquisolid merupakan salah satu metode pembuatan tablet yang
digunakan untuk meningkatkan kecepatan disolusi obat yang sukar larut dalam air. Metode liquisolid memiliki komponen utama yaitu pelarut dan carrier material sangat mempengaruhi sifat fisik dan kecepatan disolusi tablet (Hadisoewignyo, 2012). Metode liquisolid memiliki komponen utama yaitu pelarut dan carrier material. Pelarut yang digunakan pada penelitian ini yaitu gliserin.
Penelitian yang dilakukan oleh Ghadi (2015) tentang formulasi tablet liquisolid spironolacton dengan pelarut gliserin, pada peningkatan proporsi gliserin memberikan respon penurunan kekerasan tablet, peningkatan persentase kerapuhan tablet dan peningkatan jumlah obat yang terdisolusi. Gliserin bersifat inert larut dalam air, bahan ini banyak digunakan sebagai bahan tambahan pada suatu formulasi untuk meningkatkan kelarutan obat yang sukar larut. Obat yang ditambahkan pelarut akan berada pada keadaan dispersi molekuler dan ketika campuran menjadi suspensi, obat akan berada dalam dispersi kasar. Pendispersian tersebut menyebabkan luas permukaan obat menjadi besar, menurunkan tetapan dielektrik obat, dan menurunkan sudut kontak sehingga terjadi peningkatan kelarutan obat.
Carrier material yang digunakan dalam penelitian ini adalah amilum
formulasi sediaan tablet untuk memiliki waktu hancur dengan baik dalam medium disolusi dan memiliki laju disolusi yang tinggi (Javadzadeh et al., 2007). Mekanisme aksi amilum adalah dengan aksi kapiler, deformasi dan pengembangan ketika kontak dengan air dengan suhu 37oC, air akan segerap diserap dengan cepat oleh tablet melalui jembatan hidrofil (Sulaiman, 2007). Penelitian yang dilakukan oleh Shyam (2014) tentang formulasi tablet liquisolid lovastatin dengan amilum kentang sebagai carrier material, pada peningkatan
proporsi amilum kentang memberikan respon peningkatan waktu hancur, peningkatan persentase obat yang tedisolusi, penurunan kekerasan tablet dan penurunan persentase kerapuhan.
D. Hipotesis
1. Peningkatan proporsi gliserin sebagai pelarut dapat meningkatkan persentase kerapuhan, meningkatkan persentase obat yang terdisolusi dan menurunkan kekerasan tablet. Peningkatan proporsi amilum kentang sebagai carrier material dapat meningkatkan waktu hancur, meningkatkan persentase obat
yang terdisolusi, menurunkan kekerasan tablet dan menurunkan persentase kerapuhan tablet.
25 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian yang dilakukan adalah eksperimental murni dengan melakukan percobaan pembuatan formulasi sediaan tablet liquisolid glibenklamid dengan menggunakan kombinasi pelarut gliserin dan amilum kentang sebagai carrier material. Penelitian ini dilakukan di Laboratorium Formulasi Teknologi Sediaan
Padat dan Laboratorium Farmasi Fisika Universitas Sanata Dharma. B. Variabel Penelitian
1. Variabel bebas dalam penelitian ini adalah perbandingan gliserin dan amilum kentang menggunakan simplex lattice design dengan R1 (0%:100%), R2 (0%:100%), R3 (25%:75%), R4 (50%:50%), R5 (50%:50%), R6 (75%:25%), R7 (100%,0%), dan R8 (100%,0%).
2. Variabel tergantung dalam penelitian ini adalah disolusi tablet liquisolid, sifat fisik serbuk liquisolid (indeks kompresibilitas), sifat fisik tablet liquisolid (keseragaman bobot, kekerasan, kerapuhan, waktu hancur).
3. Variabel pengacau terkendali dalam penelitian ini adalah lokasi pemesanan bahan yang dipakai, nomor ayakan, dan waktu pencampuran.
C. Definisi Operasional
1. Sifat fisik serbuk merupakan parameter untuk mengukur kualitas serbuk 2. Indeks kompresibilitas merupakan banyaknya ruang kosong pada campuran
serbuk yang akan berdampak pada pembuatan tablet.
3. Sifat fisik tablet merupakan parameter untuk mengukur kualitas dari tablet yang akan diproduksi. Parameter tersebut meliputi uji kekerasan,kerapuhan, waktu hancur, keseragaman bobot, dan disolusi tablet.
4. Keseragaman kandungan merupakan salah satu parameter yang menunjukkan setiap tablet yang dibuat memiliki kadar obat yang sama.
5. Kekerasan tablet merupakan salah satu parameter yang menunjukkan interaksi-interaksi antar komponennya seperti goncangan dan keretakan tablet.
6. Kerapuhan tablet merupakan salah satu parameter yang menunjukkan kekuatan tablet terhadap benturan mekanik saat pentabletan.
7. Waktu hancur tablet merupakan salah satu parameter yang menunjukkan waktu yang dibutuhkan tablet telah hancur sempurna.
8. Disolusi merupakan salah satu parameter yang menunjukkan kadar obat yang terlarut sempurna pada waktu tertentu.
D. Alat dan Bahan Penelitian 1. Alat
Hardness tester merk Pharmatest®, Volumenometer merk ERWEKASYM®, disintegran tester merk ATMI®, attrition tester merk ATMI®, timbangan analitik merk DeltaRange®, MELTTER AE260, mesin cetak tablet single punch KORSCH, statif, mortir dan stamper,alat uji disolusi tablet RC-6 D, Spektrofotometer UV SCHIMADZU, stopwatch, dan alat- alat gelas.
2. Bahan
E. Tata Cara Penelitian
Formula penelitian dibuat dengan perbandingan gliserin : amilum kentang R1 (0%:100%), R2 (0%:100%), R3 (25%:75%), R4 (50%:50%), R5 (50%:50%), R6 (75%:25%), R7 (100%,0%), dan R8 (100%,0%) yang ditunjukan pada tabel IV.
Tabel IV. Formula tablet liquisolid glibenklamid
Keterangan : Penentuan perbandingan komposisi pelarut gliserin dan carrier material amilum
kentang pada masing-masing formula dilakukan dengan menggunakan simplex lattice design dari
Design Expert 9.0 dan didapatkan 8 formula yang disebut “R1 hingga R8”.
1. Pembuatan sediaan tablet liquisolid
Semua bahan ditimbang sesuai formula. Glibenklamid dan pelarut gliserin dimasukkan dalam mortir dan diaduk hingga rata sehingga membentuk suspensi. Suspensi tersebut kemudian diserap dengan dengan amilum kentang dan diaduk dalam mortir selama 5 menit. Campuran ditambahkan aerosil sebagai coating dan diaduk kembali selama 5 menit. Campuran dimasukkan kedalam cube
mixer dan diaduk selama 15 menit dalam cube mixer dengan kecepatan 50 rpm.
Massa serbuk kering dikeluarkan dari cube mixer kemudian diayak dengan pengayak mesh nomer 16. Massa serbuk yang telah diayak kemudian dimasukkan ke dalam cube mixer dan ditambahkan Avicel PH-102, SSG dan Mg stearat yang sudah ditimbang. Massa sebuk lalu dicampur homogen selama 15 menit di dalam
cube mixer. Selanjutnya diuji sifat alir serbuk dan uji homogenitas serbuk. Serbuk
yang telah diuji, kemudian dikempa menjadi tablet. Tablet yang sudah dikempa dilakukan pengujian meliputi sifat fisik dan uji disolusi.
2. Uji mutu serbuk liquisolid a. Indeks kompresibilitas
Timbang seksama lebih kurang 100 g serbuk (M) dengan tingkat akurasi 0,1%, masukan dalam gelas ukur 250 mL tanpa pemampatan. Ratakan permukaan serbuk dengan hati-hati tanpa pemampatan jika perlu, dan bacalah volume (V0) 1. Pembuatan larutan induk
Larutan induk dibuat dengan cara menimbang seksama 100,0 mg glibenklamid kemudian dilarutkan dengan metanol hingga 100 mL (Sudharshan et al., 2009).
2. Penentuan panjang gelombang serapan maksimum
3. Pembuatan kurva baku
Larutan induk dibuat seri kadar dengan konsentrasi 3,98 µg/mL, 5,97 µg/mL, 7,96 µg/mL, 9,95 µg/mL, 11,94 µg/mL dan diencerkan dengan metanol. Setelah itu larutan dibaca dengan Spektrofotometer UV pada panjang gelombang serapan maksimum, Serapan yang didapat dari masing-masing pengenceran diplotkan dengan kadar dan dibuat kurva dengan persamaan garis dan regresi linier.
4. Homogenitas serbuk
Pengujian dilakukan dengan mengambil 10 titik sampel serbuk. Sampel ditimbang seksama masing-masing 88,0 mg kemudian ditambahkan metanol sampai 100 mL. Sampel kemudian disaring dengan menggunakan milipore. Serapan dibaca menggunakan spektrofotometer UV pada panjang gelombang 229,0 nm. Homogenitas serbuk harus memenuhi kriteria coefficient variation (CV) kurang dari 5 %.
3. Uji mutu tablet liquisolid a. Keseragaman kandungan
b. Uji kekerasan tablet
Sebanyak 20 tablet diletakkan satu per satu secara horizontal pada hardness tester, kemudian salah satu bagian dari mesin ini akan bergerak maju untuk menghancurkan tablet dan alat membaca ukuran tablet yang hancur.. Kemudian, hasilnya dihitung rata-ratanya (Anilkumar, Arun, Amol, Harinath, 2010).
c. Uji kerapuhan tablet
Sebanyak 20 tablet ditimbang secara bersamaan dan dicatat sebagai bobot awal. Seluruh tablet dimasukkan ke dalam attrition tester dengan kecepatan putar 25 rpm selama 4 menit. Tablet hasil atrition tester dibersihkan dari serbuk serbuk halus yang menempel dan ditimbang kembali. Nilai persen kerapuhan dapat dihitung dari selisih penimbangan awal dengan penimbangan akhir dibagi penimbangan awal dan dikalikan 100 persen (Arulkumaran et al., 2014).
d. Uji waktu hancur tablet
Enam tablet dipilih secara acak diletakkan di dalam tabung disintegran tester. Tabung dimasukkan kedalam bejana yang telah diisi air bersuhu 370C, tinggi air tidak kurang dari 15 cm sehingga tabung dapat turun naik dengan jarak 7,5 cm. Kemudian dicatat waktu hancur tablet. Tablet dikatakan hancur apabila ada bagian tablet ada yang tertinggal di atas kasa. Waktu hancur tablet dikatakan baik ≤ 15 menit (Depkes RI, 2014).
e. Penetapan kadar
tanda. Serapan diukur pada panjang gelombang maksimum metanol. Kadar diperoleh dengan memasukkan nilai serapan ke dalam kurva baku glibenklamid dalam metanol. Percobaan diulang sebanyak tiga kali tiap running dan dihitung rata-rata serta simpangan deviasi (SD).
f. Uji Disolusi
1. Pembuatan Larutan buffer phosphate pH 8,5
Larutan buffer phosphate pH 8,5 sebagai medium disolusi dibuat dengan cara menimbang sebanyak 6,8 gram monobasic potassium phosphat dan 1,99 gram NaOH kemudian ditambahkan akuadest ke dalam labu takar 1000 mL hingga batas tanda (United States Pharmacopeial Convention, 2014).
2. Pembuatan larutan induk
Larutan induk dibuat dengan cara menimbang seksama 67,0 mg glibenklamid kemudian ditimbang seksama lalu dilarutkan 40 mL metanol di dalam labu takar 500 mL. Sonifikasi selama 5 menit lalu ditambahkan medium disolusi hingga batas tanda (United States Pharmacopeial Convention, 2014).
3. Penentuan panjang gelombang maksimum
Larutan induk kemudian diambil 400 µl dan diencerkan dengan larutan buffer phosphate pH 8,5 hingga 10 mL. Larutan ini dimasukkan dalam kuvet dan
diamati absorbansi pada panjang gelombang 200 – 400 nm sehingga akan diketahui serapan maksimum.
4. Pembuatan kurva baku
dengan buffer phosphate pH 8,5. Setelah itu larutan dibaca dengan Spektrofotometer UV pada panjang gelombang serapan maksimum, Serapan yang didapat dari masing-masing pengenceran diplotkan dengan kadar dan dibuat kurva dengan persamaan garis dan regresi linier.
5. Uji disolusi tablet
Tablet dimasukkan ke dalam labu yang berisi larutan 0,05 M buffer phosphate pH 8,5 yang berfungsi sebagai media disolusi. Jarak pengaduk dayung dari dasar labu adalah 2,5 ± 0,2 cm dan pengaduk dayung diputar pada kecepatan 50 rpm. Suhu medium dijaga konstan 37 ± 0,5º C dengan volume media disolusi yang digunakan adalah 900 mL. Sampel obat yang terlepas ke medium diambil pada menit ke 0, 5, 10, 15, 30, dan 45 menit sebanyak 5 mL pada posisi yang telah ditentukan. Setiap kali pengambilan sampel diganti dengan volume yang sama (5,0 mL) dengan medium buffer phosphate. Serapan dari larutan uji ditetapkan kadarnya dengan spektrofotometer UV-VIS pada panjang gelombang maksimum.
F. Analisis Data
Data yang diperoleh dari percobaan adalah data indeks kompresibilitas, homogenitas serbuk, uji disolusi dan sifat fisik tablet meliputi keseragaman bobot, kekerasan, kerapuhan tablet, dan waktu hancur tablet.
Data sifat fisik yang diperoleh, dihitung rata-rata dan standar deviasi. Data sifat alir, sifat fisik, dan uji disolusi tablet dianalisis menggunakan Design Expert 9.0 sehingga didapatkan interaksi dari kedua komponen untuk
35 BAB IV
HASIL DAN PEMBAHASAN
A. Hasil Uji Sifat Alir Serbuk Liquisolid
Serbuk liquisolid yang dihasilkan diuji sifat alirnya untuk mengetahui kemampuan alir serbuk dalam mengisi ruang kompresi pada mesin pencetak tablet sehingga tablet yang dihasilkan memiliki keseragaman bobot yang baik. Pengujian sifat alir serbuk liquisolid dilakukan dengan metode indeks kompresibilitas.
1. Indeks Kompresibilitas
Indeks kompresibilitas merupakan kemampuan granul untuk berkurang/menurun volumenya setelah diberi tekanan tertentu (Sulaiman, 2007). Peningkatan nilai indeks kompresibilitas menunjukkan penurunan kemampuan alir serbuk, sedangkan penurunan nilai indeks kompresibilitas menunjukkan peningkatan kemampuan alir. Indeks kompresibilitas dipengaruhi oleh bentuk, kerapatan dan ukuran partikel (Sirisha et al., 2012).
Respon indeks kompresibilitas ditunjukkan pada persamaan 13.
Y= 3,50 X1 + 0,05 X2 - 0,01 X1X2 ... (13)
Keterangan :
X1 = Gliserin
Model plot respon indeks kompresibilitas ditunjukan pada gambar 5.
Keterangan:
Y = Respon indeks kompresibilitas A = Komponen gliserin
B = Komponen amilum kentang
= Design point
= Convidence interval
--- = Tolerance interval
menurunkan indeks kompresibilitas. Hasil indeks kompresibilitas serbuk pada tiap formula menunjukkan indeks kompresibilitas serbuk berada pada rentang 11,49%-13,79% sehingga dapat dikatakan serbuk memenuhi persyaratan indeks kompresibilitas yang baik yaitu berada pada rentang 11%-15% (Arulkumaran et al., 2014).
B. Hasil Uji Homogenitas Serbuk
Uji Homogenitas serbuk dilakukan untuk mengetahui apakah proses pencampuran serbuk yang dilakukan menghasilkan campuran yang homogen. Pengukuran dilakukan menggunakan working standar glibenklamid dalam metanol pada instrumen spektrofotometer UV untuk menentukan panjang gelombang maksimum. Hasil serapan maksimum terukur pada panjang gelombang 229 nm yang ditunjukan pada gambar 6.
Gambar 6. Spectrum graph glibenklamid dalam metanol (panjang gelombang vs absorbansi)
Menurut Bilal (2013) serapan glibenklamid dalam metanol berada pada panjang gelombang dalam kisaran 229,5 nm. Hal ini tidak berbeda jauh dari penelitian tersebut dalam penentuan absorbansi panjang gelombang dibandingkan dengan hasil yang didapat. Ada beberapa faktor yang mempengaruhi absorbansi
y = 0,0606x + 0,058 pengganggu (Gandjar and Rohman, 2009). Berikut kurva baku glibenklamid yang ditunjukkan pada gambar 7.
Gambar 7. Kurva baku glibenklamid dalam metanol (n=1)
Pengujian homogenitas serbuk dilakukan dengan mengambil 10 titik sampel pada bagian atas tengah dan bawah cube mixer dan diukur dengan instrumen spektofotometer UV. Hasil penetapan kadar tablet ditunjukan pada tabel V.
Tabel V. Hasil uji homogenitas serbuk liquisolid
Hasil uji homogenitas diperoleh kadar 96,39 ± 1,44 (%) dengan coefficient variation (CV) sebesar 1,49 %, sehingga serbuk yang dibuat dapat dikatakan sudah homogen karena memenuhi persyaratan uji homogenitas yaitu memiliki CV kurang dari 5% (Depkes RI, 2014).
Sample no Kadar glibenklamid (%)
C. Hasil Uji Mutu Fisik Tablet Liquisolid 1. Keseragaman Kandungan Tablet Liquisolid
Uji keseragaman kandungan bertujuan untuk mengetahui kandungan zat aktif tiap tablet liquisolid yang telah dikempa.
Respon keseragaman kandungan ditunjukkan pada persamaan 14. Y=2,230 X1 + 0,311 X2 - 0,007 X1X2 ... (14)
Keterangan :
X1 = Gliserin
X2 = Amilum kentang
Model plot respon keseragaman kandungan ditunjukan pada gambar 8.
Keterangan:
Y = Respon keseragaman kandungan A = Komponen gliserin
B = Komponen amilum kentang
= Design point
= Convidence interval
--- = Tolerance interval
Gambar 8. Model plot respon keseragaman kandungan tablet liquisolid Pada persamaan (14) dapat diketahui bahwa gliserin, amilum kentang dan interaksi gliserin dan amilum kentang memberikan pengaruh respon keseragaman kandungan. Persamaan tersebut memiliki nilai p-value pada lack of fit sebesar 0,3347 (p>0,05), sehingga dinyatakan persamaan tersebut dapat
menunjukkan penggunaan komponen gliserin meningkatkan kadar obat yang terbaca dengan nilai 2,30. Komponen gliserin memiliki pengaruh yang dominan terhadap peningkatan keseragaman kandungan, hal ini disebabkan penambahan gliserin akan mendispersikan glibenklamid menjadi partikel yang lebih kecil, sehingga berdampak pada peningkatan kelarutan glibenklamid dalam metanol. Nilai negatif menunjukkan interaksi amilum kentang dalam menurunkan kadar obat yang terbaca dengan nilai -0,007, hal ini disebabkan komponen amilum kentang memiliki mekanisme pelepasan obat dengan mengembang dalam air sehingga obat sulit untuk lepas. Hasil keseragaman kandungan tablet pada tiap formula menunjukkan kadar tiap tabletnya berada pada rentang 93,65-100,45 dengan nilai penerimaan 2,81-7,56% sehingga dapat dikatakan tablet memenuhi persyaratan keseragaman kandungan yaitu memiliki nilai penerimaan kurang dari 15% (Depkes RI, 2014).
2. Kekerasan Tablet Liquisolid
Kekerasan tablet merupakan parameter yang menggambarkan ketahanan tablet terhadap tekanan mekanik seperti goncangan, kikisan dan terjadi keretakan tablet selama pembungkusan, pengangkutan dan pemakaian. Kekerasan tablet dipengaruhi oleh bobot bahan, kemampuan alir serbuk, kompaktibilitas bahan, tekanan pengempaan, celah antara punch atas dan punch bawah pada saat pengempaan pengempaan.
Respon kekerasan tablet ditunjukkan pada persamaan 15.
Y= –47,83 X1 + 0,03 X2 + 0,24 X1X2 + 0,0003 X1X2(X1X2) ... (15)
Keterangan :
X1 = Gliserin
Model plot respon kekerasan tablet ditunjukan pada gambar 9.
Keterangan:
Y = Respon kekerasan tablet A = Komponen gliserin
B = Komponen amilum kentang
= Design point
= Convidence interval
--- = Tolerance interval
Gambar 9. Model plot respon kekerasan tablet liquisolid
Pada persamaan (15) dapat diketahui bahwa gliserin, amilum kentang dan interaksi gliserin dengan amilum kentang memberikan pengaruh respon kekerasan tablet. Persamaan tersebut memiliki nilai p-value pada lack of fit sebesar 0,41 (p>0,05), sehingga dinyatakan persamaan tersebut dapat menggambarkan eksperimental. Hasil p-value pada anova untuk persamaan (15) sebesar 0,0001 (p<0,05) maka dapat disimpulkan bahwa ada perbedaan signifikan sehingga penambahan tunggal maupun interaksi gliserin dan amilum kentang pengaruhnya besar terhadap kekerasan tablet liquisolid.
memiliki kekerasan tablet pada rentang 4,0–7,8 sehingga dapat dikatakan tablet memenuhi persyaratan kekerasan tablet yaitu antara 4 kg hingga 8 kg.
3. Kerapuhan Tablet Liquisolid
kerapuhan tablet merupakan parameter kecenderungan tablet untuk terkikis selama penanganan, pengemasan dan pendistribusian. Kerapuhan tablet dipengaruhi oleh bobot bahan, kelembaban, kompatibilitas bahan, tekanan pengempaan.
Respon kerapuhan tablet ditunjukkan pada persamaan 16.
Y= 5,23 X1 + 0,001 X2– 0,026 X1X2– 0,00003 X1X2(X1X2) ... (16)
Keterangan :
X1 = Gliserin
X2 = Amilum kentang
Model plot respon kerapuhan tablet ditunjukan pada gambar 10.
Keterangan:
Y = Respon kerapuhan tablet A = Komponen gliserin
B = Komponen amilum kentang
= Design point
= Convidence interval
--- = Tolerance interval
Gambar 10. Model plot respon kerapuhan tablet liquisolid
menggambarkan eksperimental. Nilai p-value pada anova untuk persamaan (16) sebesar 0,0001 (p<0,05) maka dapat disimpulkan bahwa ada perbedaan signifikan sehingga penambahan tunggal maupun interaksi gliserin dan amilum kentang pengaruhnya besar terhadap persentase kerapuhan tablet liquisolid.
Nilai positif pada persamaan (16) menunjukkan penggunaan komponen gliserin meningkatkan kerapuhan tablet dengan nilai 5,23 dan nilai negatif menunjukkan interaksi amilum kentang menurunkan kerapuhan tablet dengan nilai -0,026. Komponen gliserin memiliki pengaruh yang dominan terhadap peningkatan kerapuhan tablet, hal ini disebabkan gliserin yang dijerap oleh amilum menyebabkan serbuk menjadi lebih lembab dan menghasilkan tablet yang lebih rapuh. Hasil kerapuhan tablet pada tiap formula menunjukkan bahwa nilai kerapuhan tablet berada pada rentang 0,28–0,67 % sehingga dapat dikatakan tablet memenuhi persyaratan kerapuhan tablet yaitu memiliki nilai kerapuhan yang kurang dari 1 % (Sharma, 2010).
4. Waktu Hancur Tablet
Respon waktu hancur tablet ditunjukan pada persamaan 17.
Y= –0,480 X1 + 0,002 X2 + 0,002 X1X2 ... (17)
Keterangan :
X1 = Gliserin
X2 = Amilum kentang
Model plot respon waktu hancur tablet ditunjukan pada gambar 11.
Keterangan:
Y = Respon waktu hancur tablet A = Komponen gliserin
B = Komponen amilum kentang
= Design point
= Convidence interval
--- = Tolerance interval
Gambar 11. Model plot respon waktu hancur tablet liquisolid
Pada persamaan (17) dapat diketahui bahwa gliserin, amilum kentang dan interaksi gliserin dan amilum kentang memberikan pengaruh respon waktu hancur tablet. Persamaan (17) memiliki nilai p-value pada lack of fit sebesar 0,9199 (p>0,05), sehingga dinyatakan persamaan tersebut dapat menggambarkan eksperimental. Nilai p-value untuk anova pada persamaan (17) sebesar 0,0004 (p<0,05) maka dapat disimpulkan bahwa ada perbedaan signifikan sehingga penambahan tunggal maupun interaksi gliserin dan amilum kentang pengaruhnya besar terhadap waktu hancur tablet liquisolid.
nilai 0,002. Komponen gliserin memiliki pengaruh yang dominan dalam menurunkan waktu hancur, hal ini disebabkan gliserin yang lebih cenderung hidrofil dan larut dalam air sehingga dapat menurunkan waktu hancur tablet. Komponen amilum kentang memiliki pengaruh dalam meningkatkan waktu hancur, hal ini disebabkan amilum kentang yang memiliki mekanisme mengembang dalam air dan tidak larut dalam air, sehingga dapat meningkatkan waktu hancur tablet. Hasil waktu hancur tablet pada tiap formula menunjukkan bahwa waktu hancur tablet berada pada rentang 0,81-1,26 menit, sehingga dapat dikatakan tablet memenuhi persyaratan waktu hancur tablet yaitu kurang dari 15 menit (Depkes RI, 2014).
D. Hasil Uji Penetapan Kadar Tablet Liquisolid
Uji penetapan kadar dilakukan untuk mengetahui kadar glibenklamid dalam tablet untuk digunakan dalam perhitungan uji disolusi. Hasil penetapan kadar tablet ditunjukan pada tabel VI.
Tabel VI. Hasil penetapan kadar glibenklamid dalam tablet liquisolid Formula Kadar tablet glibenklamid
memenuhi persyaratan kadar tablet glibenklamid yang tidak kurang dari 90 % dan tidak lebih dari 110 % (United States Pharmacopeial Convention, 2014)
E. Hasil Uji Disolusi Tablet Liquisolid 1. Penentuan Panjang Gelombang Maksimum
Penentuan panjang gelombang maksimum dilakukan menggunakan working standar glibenklamid dalam buffer phosphate pada instrumen
spektrofotometer UV. Hasil serapan maksimum terukur pada panjang gelombang 204,5 nm yang ditunjukan pada gambar 12.
Gambar 12. Spectrum graph glibenklamid dalam buffer phosphate (panjang gelombang vs absorbansi)
Menurut Gianotto (2007) glibenklamid dalam medium buffer phosphate memberikan serapan yang besar pada panjang gelombang 204,5. Dengan demikian panjang gelombang 204,5 nm dapat digunakan sebagai panjang gelombang maksimum dalam penentuan kurva baku glibenklamid dalam medium buffer phosphate.
y = 0,0982x - 0,006 2. Penentuan Persamaan Kurva Baku
Hasil penentuan persamaan kurva baku pada panjang gelombang 204,5 nm ditunjukkan pada gambar 13.
0
Disolusi merupakan salah satu parameter yang menunjukkan kadar obat yang terlarut sempurna pada medium disolusi pada waktu tertentu. United State Pharmacope XXXVII mensyaratkan bahwa kelarutan tablet glibenklamid dalam waktu 30 menit harus larut tidak kurang dari 75% dengan menggunakan alat tipe II (tipe dayung) dalam medium buffer phosphate pH 8.5. Menurut Brian (2014) medium disolusi buffer phosphate dapat mensimulasikan tubuh pada pengujian disolusi dengan obat yang tergolong dalam asam lemah. Pada penelitian ini waktu uji disolusi selama 45 menit untuk melihat apakah pada waktu tersebut masih terjadi pelepasan zat aktif atau tidak. Hasil pengungkapan disolusi obat dengan melihat nilai Q30 yaitu persentase kadar obat terdisolusi dalam medium pada waktu 30 menit.
Berikut profil uji disolusi tablet liquisolid glibenklamid yang dinyatakan dalam grafik persentase (%) obat terdisolusi dengan waktu yang ditunjukkan pada gambar 14.a dan 14.b.
0
Respon disolusi tablet liquisolid ditunjukkan pada persamaan 18.
Y= 8,71 X1 + 0,26 X2 - 0,03 X1X2 ... (18)
Keterangan :
X1 = Gliserin
X2 = Amilum kentang
Model plot respon disolusi tablet ditunjukan pada gambar 15.
Keterangan:
Y = Respon disolusi tablet A = Komponen gliserin
B = Komponen amilum kentang
= Design point
= Convidence interval
--- = Tolerance interval
Gambar 15. Model plot respon disolusi tablet liquisolid
Pada persamaan (18) dapat diketahui bahwa gliserin, amilum kentang dan interaksi gliserin dan amilum kentang memberikan pengaruh respon disolusi tablet. Persamaan (18) memiliki nilai p-value pada lack of fit sebesar 0,7506 (p>0,05), sehingga dinyatakan persamaan tersebut dapat menggambarkan eksperimental. Nilai p-value untuk anova pada persamaan (18) yang diperoleh sebesar 0,0002 (p<0,05) maka dapat disimpulkan bahwa ada perbedaan signifikan antar formula sehingga penambahan tunggal maupun interaksi gliserin dan amilum kentang memberikan pengaruh yang besar terhadap disolusi tablet liquisolid.
Nilai positif pada persamaan (18) menunjukkan penggunaan komponen
disebabkan gliserin dapat meningkatkan pelepasan obat dengan mengecilkan ukuran partikel, meningkatkan persentase obat yang terbasahi dan bertindak sebagai ko-solven. Hasil negatif menunjukkan interaksi komponen gliserin dan amilum kentang menurunkan persentase obat yang terdisolusi, penurunan disolusi terjadi karena komponen gliserin sebagai pelarut dalam jumlah banyak akan membuat obat tetap berikatan dengan gliserin (Hadisoewignyo, 2012) dan komponen amilum kentang memiliki mekanisme pelepasan obat dengan mengembang dalam air sehingga sulit dalam pelepasan obatnya sehingga interaksi keduanya menyebabkan obat sulit untuk lepas dalam waktu tertentu.
F. Penentuan Formula Optimum
Formula optimum ditentukan dengan menggunakan Design Expert versi 9.0 yang diawali dengan menentukan parameter sifat fisik (keseragaman kandungan, kekerasan, kerapuhan, waktu hancur) dan disolusi tablet liquisolid. Liquisolid merupakan metode pembuatan sediaan tablet yang diciptakan untuk