1
Pengaruh Pajanan Benzena terhadap Timbulnya Leukemia Mieloid Akut
pada Pekerja yang Terpajan
Febyan, Arwi Wijaya, Michelle Linardi, Johannes Hudyono
Departemen Kedokteran Okupasi
Published: Buletin Asosiasi Fakultas Kedokteran Swasta Indonesia (AFKSI) Oktober-Maret 2015 Fakultas Kedokteran Universitas Kristen Krida Wacana
Jl. Arjuna Utara No.6 Jakarta Barat 11510 Telp. 021-56942061 Fax. 021 5631731
Abstract
Benzene is defined as a colorless, flammable, toxic liquid with a pleasant aromatic odor.
Exposure to benzene is highest in areas of heavy motor-vehicle traffic and around gasoline
filling-stations. Its chemical properties have led to its widespread use as a solvent in a
number of industrial applications, and occupational exposure to benzene has been
documented for workers in different production sectors i.e. production of chemicals,
pharmaceuticals, plastics, synthetic rubbers, paints, oil processing etc. Benzene can be toxic
by ingestion, inhalation, and absorption through the skin. In California, the acute Reference
Exposure Level (REL, 6 hr) for benzene is 1300 μg/m3, and the chronic Reference Exposure
Level (REL) is 60 μg/m3 (OEHHA, 1999a; 2000b). The acute and chronic REL values are
based on hematotoxicity among benzene-exposed workers. Benzene is the second
best-documented risk factor for the development of Acute Myeloid Leukemia (AML). Benzene
itself is not toxic. It must be metabolize by enzymes in the liver into metabolites that are
potentially toxic .Among these metabolites the most potent in inhibiting erythropoiesis are
tt-muconaldehyde and 1,4-benzoquinone. Biomolecular analysis demonstrating that benzene
metabolites inhibit the DNA decatenation activity of topoisomerase II . Due to the nature of
Topoisomerase II-dependent sulfhydryl and the ability of some metabolites of benzene to
modify sulfhydryl groups, inhibition of topoisomerase activity by benzene metabolites has
been declared as a mechanism for the development of AML.
Key words: benzene, AML, topoisomerase II, occupational exposure
Abstrak
2 pekerja di sektor produksi yang berbeda yaitu produksi bahan kimia, obat-obatan, plastik, karet sintetis, cat, pengolahan minyak dan lain-lainnya. Benzena dapat toksik bila tertelan, terinhalasi, dan terabsorpsi melalui kulit. Di California, the acute Reference Exposure Level (REL, 6 jam) untuk benzena adalah 1300 mg / m3, dan the chronic Reference Exposure Level (REL) adalah 60 ug / m3 (OEHHA, 1999a; 2000b). Nilai REL yang akut dan kronis didasarkan pada hematotoksisitas pada kalangan pekerja yang terpajan oleh benzena. Benzena merupakan faktor risiko kedua sebagai penyebab Leukemia Mieloid Akut (LMA). Benzena sendiri tidak toksik. Tetapi harus dimetabolisme oleh enzim di hati menjadi metabolit yang berpotensi toksik. Di antara metabolit ini yang paling kuat dalam menghambat eritropoiesis yaitu tt-muconaldehyde dan 1,4-benzoquinon. Analisis biomolekuler menunjukkan bahwa metabolit benzena dapat menghambat aktivitas decatenation DNA dari topoisomerase II. Karena sifat dari topoisomerase II bergantung terhadap sulfhidril dan kemampuan beberapa metabolit benzena untuk memodifikasi kelompok sulfhidril, penghambatan aktivitas topoisomerase oleh metabolit benzena dinyatakan sebagai mekanisme penyebab LMA.
Kata kunci: benzena, LMA, topoisomerase II, pajanan okupasi
Pendahuluan
Seiring dengan perkembangan jaman dan ilmu pengetahuan maka turut berkembang
pula dunia industri. Penggunaan bahan kimia dalam kehidupan sehari-hari, seperti di dunia
industri pun semakin banyak. Salah satu bahan kimia yang digunakan dan dihasilkan oleh
perindustrian adalah benzena, dalam penelitian pajanan benzena antara polisi lalu lintas di
Roma, para polisi ini karena profesinya, terpajan asap kendaraan ketika mengendalikan lalu
lintas, dan mereka juga dapat dianggap sebagai model untuk kasus pajanan terburuk untuk
penduduk perkotaan.1-2 Pada tahun 1928, Dolore dan Borgomano mempublikasi kasus
pertama benzena yang menginduksi penyakit leukemia. Kasus leukemia limfatik akut ini
diidentifikasi pada pekerja farmasi yang dianggap memiliki risiko yang tinggi karena pajanan
benzena yang tinggi.3 Benzena dan naftalena terukur di udara dan napas pada 326 personel
Angkatan Udara AS, yang diklasifikasi dalam kategori pajanan terendah, sedang, dan tinggi
untuk bahan bakar jet (JP-8).4 Benzena adalah penyebab paling umum toksisitas bahan kimia
pada pekerja di Cina. Menurut statistik resmi, lebih dari 60 persen dari semua kanker dari
penyakit akibat kerja disebabkan oleh benzena.2 Di kota industri Dongguan, 30 persen dari
semua penyakit akibat pajanan kerja didiagnosis karena toksisitas benzena.3 Mereka yang
3 Tingkat kematian toksisitas akut benzena adalah 21,7%.5 Environtment Protection Agency
(EPA) telah menetapkan tingkat maksimum kadar benzena dalam air minum pada 5 bagian
per miliar benzena pada air (5 ppb). Occupational Safety and Health Administration (OSHA)
telah menetapkan batas 1 bagian benzena per juta bagian udara di tempat kerja (1 ppm)
selama 8 jam shift dan 40 jam dalam seminggu.6 Diperkirakan 99 persen dari total pajanan
benzena jika terhirup di udara bebas, benzena cepat terdegradasi dalam beberapa jam sampai
beberapa hari. Tercemarnya air oleh benzena dapat terjadi karena tumpahan atau kebocoran
bensin, limbah industri, dan dari tempat penimbunan limbah. Benzena yang ada di
permukaan air dengan cepat menguap ke udara. Namun, benzena yang masuk tanah
didegradasi lebih lama.7
Benzena
Benzena didefinisikan sebagai, bahan yang mudah terbakar, cairan toksik berwarna dengan bau aromatik yang harum. Mendidih pada 80,1 ° C, dan membeku pada 5,5 ° C. Benzena adalah hidrokarbon dengan rumus molekul C6H6.8 Pajanan benzena tertinggi di daerah lalu lintas padat kendaraan bermotor dan sekitar tempat pengisian bensin.9 Benzena telah digunakan dalam berbagai jenis industri selama lebih dari satu abad, dan merupakan salah satu yang terbanyak digunakan pada industri kimia. Benzena adalah bahan kimia yang terbentuk melalui proses alam seperti gunung berapi dan kebakaran hutan, serta melalui proses industri. Dapat ditemukan pada tingkat yang rendah dalam minyak mentah, bensin, asap kendaraan, udara perkotaan, asap rokok, dan bahkan di beberapa makanan.10
4 panas, tekanan dan waktu geologi. Dengan demikian, benzena yang terdapat dalam bahan bakar fosil dapat menguap ke udara ketika digali dan khususnya, ketika dipanaskan dengan pembakaran.13 Benzena berperanan penting dalam industri kimia, dibuktikan dengan produksinya yang lebih dari 2 miliar galon per tahun di Amerika Serikat. Pekerja di sejumlah industri, termasuk penyulingan minyak bumi, perkapalan, pabrik karet, perbaikan mobil, dan pabrik sepatu, yang berpotensi terpajan benzena tingkat tinggi. Pencemaran benzena di kalangan masyarakat umum lebih rendah daripada kebanyakan pekerjaan yang terpajan, rokok, penggunaan bensin, dan emisi kendaraan bermotor.14 Banyak subyek penelitian lain yang terpajan zat (misalnya, asbes, asap industri karet, asap pengeboran, hidrokarbon aromatik polisiklik), kanker paru dan mesothelioma cenderung mencerminkan pajanan pada karsinogen ini.15 Benzena sendiri tidak toksik, tapi harus dimetabolisme terlebih dahulu oleh enzim di hati menjadi metabolit yang berpotensi toksik. Toksisitas utama yang adalah dari sel darah yang berubah di sumsum tulang.16 Benzena bersifat lipofilik karena lebih larut dalam lemak. Konsentrasi benzena sendiri 20 kali lipat dalam jaringan lemak, sumsum tulang dan urin dibandingkan dengan yang ditemukan dalam darah.17 Benzena pertama kali ditemukan dan diisolasi dari tambang batubara di tahun 1800an.18
Penilaian risiko kanker benzena diduga adanya hubungan kumulatif antara pajanan dan risiko, dalam konsentrasi bebas. Pandangan lain menyatakan konsentrasi di bawah nilai ambang batas (NAB) tidak menyebabkan toksisitas pada sumsum tulang dan dengan demikian tidak meningkatkan risiko leukemia.19
Transmisi benzena
5 Dosis dan durasi pajanan terhadap benzena
Konsentrasi benzena ditemukan biasanya lebih tinggi di udara dalam ruangan
daripada udara di luar ruangan.22 Di California, the Acute Reference Exposure Level (REL, 6
jam) untuk benzena adalah 1300 mg / m3, dan the chronic Reference Exposure Level (REL)
adalah 60 ug / m3 (OEHHA, 1999a; 2000b). Nilai REL yang akut dan kronis didasarkan pada
hematotoksisitas pada kalangan pekerja yang terpajan oleh benzena. Beberapa efek akut dan
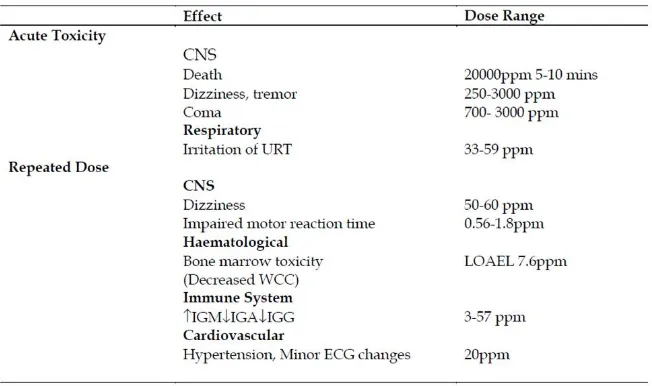
dosis berulang akibat pajanan benzena dapat dilihat tabel 1.
Tabel 1. Efek akut dan dosis berulang terhadap pajanan benzena.23
Data terbaru dari Pliofilm menunjukkan bahwa risiko leukemia secara signifikan
meningkat pada pajanan kumulatif> 50 ppm-tahun, sesuai dengan jangka panjang tingkat
pemajanan dalam pekerjaan> 1,25 ppm benzena dalam kehidupan kerja selama 40 tahun.13
Penelitian pada hewan telah menunjukkan bahwa tikus kecil lebih sensitif terhadap toksisitas
benzena daripada tikus besar. Collins dkk menemukan pajanan benzena sebesar 0,55 ppm
aman tanpa indikasi hematotoksisitas. Peningkatan insiden perubahan kromosom telah
dilaporkan pada pekerja yang terpajan 25-150 ppm benzena selama 1-25 tahun dibandingkan
dengan populasi umum.24 Beberapa penelitian pada hewan, telah menunjukkan secara
signifikan mengurangi jumlah limfosit pada tingkat pajanan benzena 10 ppm. Pekerja Cina
ditemukan telah menunjukkan tanda-tanda hematotoksisitas pada rata-rata tingkat pajanan
benzena di bawah 31 ppm (120) Kebanyakan prediksi risiko pajanan benzena telah
didasarkan pada pekerja karet yang terkena konsentrasi tinggi. Benzena merupakan penyebab
paling penting dari leukemia di Korea. Kerugian yang disebabkan oleh penyakit
hematopoietik yang berkaitan dengan benzena telah meningkat meskipun lingkungan kerja
6 Leukemia yang diinduksi oleh benzena adalah leukemia mieloid akut yang ditandai
dengan peningkatan jumlah sel morfologis menyerupai mieloblas. Konsentrasi minimum
yang penting yaitu 50-60 ppm benzena mungkin diperlukan untuk risiko leukemia di pekerja
plastik.24 Pajanan akut benzena dapat menimbulkan efek bius seperti: mengantuk,
kebingungan, tremor dan kehilangan kesadaran. Penggunaan alkohol meningkatkan efek
toksik. Benzena merupakan iritasi sedang pada mata dan bahan iritan pada kulit.26
Deteksi Benzena dalam Tubuh dan Monitoring Biologi
Beberapa tes dapat menunjukkan jika penderita telah terpajan benzena. Ada tes untuk
mengukur benzena dengan metode pernapasan. Tes ini harus dilakukan segera setelah
terpajan. Benzena juga dapat diukur dalam darah, namun karena benzena menghilang dengan
cepat dari darah, tes ini hanya berguna untuk pajanan yang baru saja terjadi.6 Metode analisis
standar terakhir untuk benzena di udara, air, tanah, makanan, asap, sampel biologis, produk
minyak bumi mengandalkan kromatografi gas (GC) dengan api atau deteksi foto ionisasi,
atau gas kromatografi-mass spectrometry (GC-MS) .13 Salah satu cara untuk menilai
kerusakan genetik adalah dengan mengukur mutasi pada gen-gen tertentu, seperti
glycophorin. Peningkatan kadar " gene-duplicating " mutasi GPA ditemukan pada pekerja
yang terpajan benzena. Metabolit awal benzena yaitu benzena oksida (BO), bereaksi dengan
residu cysteinyl dalam hemoglobin (Hb) dan albumin (Alb) untuk membentuk hasil ikatan
protein (BO-Hb dan BO-Alb), yang diduga menjadi biomarker tertentu pajanan benzena.27
Bois FY dkk menyatakan terdapat konsentrasi benzena di udara yang dihembuskan, di dalam
darah vena, dan fenol pada urin, dari tiga sukarelawan yang terpajan benzena dalam ruang
inhalasi selama 4 jam.28 Di dalam tubuh, benzena dimetabolisme menjadi produk yang
disebut metabolit. Metabolit tertentu dapat diukur dalam urin. Asam metabolit
S-phenylmercapturic dalam urin merupakan indikator yang sensitif terhadap pajanan benzena.
Namun, tes ini (monitoring biologi) harus dilakukan segera setelah terpajan benzena dan
bukan merupakan indikator utama untuk mengetahui seberapa banyak benzena yang telah
terpajan, karena metabolit mungkin terdapat dalam urin dari sumber yang lain.6
Leukemia Mieloid Akut
Kanker adalah pertumbuhan sel-sel abnormal yang tidak terkontrol dalam tubuh.
Kanker terjadi ketika pertumbuhan sel-sel dalam tubuh di luar kendali dan sel membelah
terlalu cepat.29 Istilah leukemia mengacu pada sekelompok penyakit dengan latar belakang
7 dengan transformasi maligna sel hematopoetik yang menghasilkan populasi leukemia yang
abnormal (clone) sel menekan produksi komponen darah normal seluler.12 Ada empat jenis
utama leukemia: leukemia akut limfatik (ALL), leukemia mieloid akut (LMA), leukemia
limfositik kronis (LLK), dan leukemia mieloid kronis (LMK).30LMA merupakan jenis
leukemia yang paling umum dari leukemia pada orang dewasa di Amerika Serikat, dan lebih
sering menimpa orang tua daripada orang muda. Faktor risiko untuk terjadinya LMA meliputi
pajanan benzena, dan pajanan radiasi, yang dapat menghasilkan 2 sampai 6 kali lipat
peningkatan risiko relatif.31 Leukemia mieloid akut (LMA) terjadi sebagai akibat dari
serangkaian perubahan genetik dalam sel prekursor hematopoietik. Perubahan ini mengubah
pertumbuhan dan diferensiasi hematopoietik yang abnormal sehingga terjadi akumulasi
sel-sel mieloid yang imatur di sumsum tulang dan darah tepi. 18
Ada banyak penyebab keganasan termasuk di antaranya benzena.29 Joseph T dkk
menyatakan bahwa ada bukti yang jelas dan konsisten tentang hubungan kasual antara
pajanan benzena dan leukemia mielogenous akut (LMA) atau leukemia akut non limfositik
(LANL), jenis leukemia yang dominan di antara pekerja benzena yang terpajan.18
Peningkatan risiko LMA khususnya setelah pajanan benzena telah diamati di beberapa
pekerja industry dari berbagai industri, dengan pajanan benzena jangka panjang.18 Oannis
Polychronakis menyatakan bahwa, penelitian yang berbeda telah menyebutkan sejumlah
faktor risiko potensial untuk leukemia mieloid akut, tetapi saat ini di antara pajanan radiasi
pengion, agen alkilating dan benzena, benzene merupakan yang paling berbahaya yang telah
terbukti berhubungan dengan leukemia mieloid akut,12 dan di antara bahan kimia yang
diketahui atau diduga penyebab leukemia (leukemogenik) adalah benzena. 32
Patogenesitas Leukemia Mieloid Akut (LMA) oleh Benzena
Risiko LMA yang diinduksi benzena pada manusia berdasarkan dosis metabolit
benzena yang mencapai sumsum tulang, efek benzena jangka pendek dapat berupa depresi
limfosit periferal dan depresi blastogenesis oleh mitogen pada B-lymfosit femoral pada tikus.
8
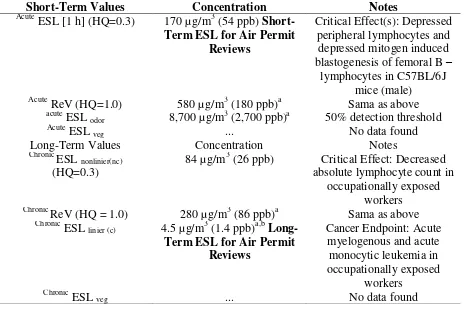
Tabel 2. Kadar Konsentrasi Benzena dalam Tubuh18
Short-Term Values Concentration Notes
84 µg/m3 (26 ppb) Critical Effect: Decreased absolute lymphocyte count in
Metabolisme primer benzena terjadi di hati oleh sitokrom P-450 2E1. 34 Sitokrom
P-450 2E1, mikrosomal epoksida hidrolase dan myeloperoxidase atau penurunan detoksifikasi
aktivitas enzim glutathione-S-transferase dan NAD (P) H: kuinon oxyreductase semuanya
secara individual telah dihubungkan dengan peningkatan kerentanan terhadap efek toksik
benzena.35 Kebanyakan benzena oksida spontan menjadi fenol (PH), yang baik diekskresikan
atau dimetabolisme lebih lanjut menjadi hidrokinon (HQ), 1,4-benzoquinon (BQ) dan
1,2,4-benzetriol (BT). Benzena oksida yang tersisa dihidrolisis untuk menghasilkan katekol (CAT)
dan 1,2 benzokuinon atau bereaksi dengan glutathione untuk menghasilkan S acid
-phenylmercapturic (S-PMA).36 Di antara metabolit ini yang paling poten dalam menghambat
eritropoiesis adalah 1,4-benzoquinon.37
Sasaran molekul kuinon dan oksigen radikal yang dihasilkan dari benzena yang paling
mungkin adalah tubulin, protein histon, topoisomerase II, dan protein DNA terkait lainnya.38
Martyn menyatakan bahwa benzena yang dimetabolisme di hati menjadi berbagai metabolit
didistribusi ke sumsum tulang dan mengakibatkan toksisitas.38 Di dalam sumsum tulang,
9 mieloperoksidase mungkin menjadi kunci bagi benzena sebagai zat karsinogenisitas. Untuk
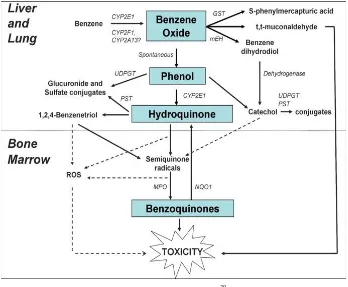
metabolisme benzena dari mulai hati sampai sumsum tulang , lihat gambar 1.
Gambar 1. Metabolisme Benzena39
Analisis biomolekuler menunjukkan bahwa metabolit benzena ini menghambat
aktivitas decatenation DNA dari topoisomerase II.34Aktivitas topoisomerase II tidak
dihambat oleh metabolit benzena pada konsentrasi kurang dari 500 ppm.13 Penghambatan
fungsi topoisomerase II ini dikaitkan dengan pajanan benzena in vivo pada tikus dan pajanan
HQ dan BQ in vitro. Bioaktivasi dari HQ ke BQ oleh peroksidase meningkatkan inhibisi
topoisomerase II dan BQ lebih kuat daripada HQ dalam sistem uji bebas sel. 39
DNA topoisomerase II merupakan enzim yang bertanggung jawab untuk modulasi
topologi DNA, yang sangat penting untuk replikasi DNA, kondensasi/dekondensasi
kromosom, dan segregrasi kromosomal saat mitosis.34 Karena sifat topoisomerase II yang
tergantung sulfhidril dan kemampuan beberapa metabolit benzena untuk memodifikasi
kelompok sulfhidril, penghambatan aktivitas topoisomerase oleh metabolit benzena telah
dinyatakan sebagai mekanisme penyebab LMA.13 Bila enzim topoisomerase II ini tidak
berfungsi dengan tepat maka akan terjadi penguraian DNA (DNA strand break, DSB) dan
penghapusan loop yang dapat merusak untai DNA. Kerusakan untai yang dihasilkan dari
tindakan ini memiliki potensi untuk menghasilkan penyimpangan rekombinasi mitosis
10 dapat menyebabkan penyimpangan kromosom dan mengganggu integritas genom sel.
Ketidakstabilan kromosom yang diinduksi oleh benzena metabolit, hidrokinon, dapat
berkontribusi sebagai penyebab LMA dengan meningkatnya jumlah lesi genetik dalam sel
hematopoietik.40 Sebuah studi pasien dengan terapi LMA mengidentifikasi korelasi yang erat
antara aktivitas inhibitor DNA-topoisomerase dan penyimpangan dalam kromosom 5, 7 dan
8 .13 Menurut Ronda K. Baker dkk pengamatan ini dapat dijelaskan, setidaknya dengan fakta
bahwa hidrokinon dan produk oksidasi utamanya, p-benzokuinon, adalah racun spindel kuat
yang mengganggu dinamika perakitan equilibrium mikrotubul dengan menghambat guanosin
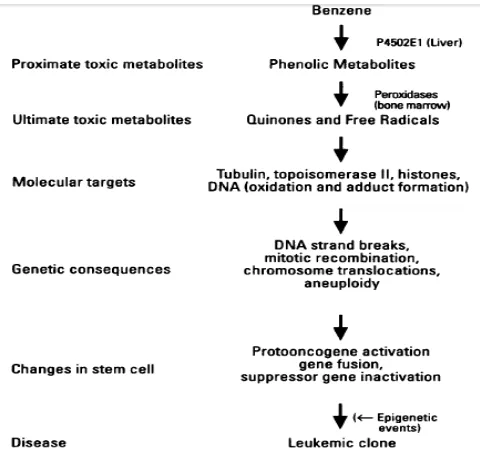
trifosfat (GTP) yang mengikat tubulin.34 Jika efek ini terjadi di stem sel atau sel progenitor
awal sel klon leukemia bisa menyebabkan aktivasi protoonkogen, fusi gen, dan inaktivasi
supresor gen. Lihat gambar 2.38
Martyn T. Smith juga menyatakan ada kemungkinan terjadi translokasi dan trisomi t
(8; 21) juga terlibat dalam pengembangan leukemia dari benzena. Mungkin ada sejumlah
jalur genetik benzene-induced leukemia, namun bukti yang dipelajari bahwa metabolit
benzena menghasilkan perubahan genetik yang faktor penyebab leukemia myeloid, yaitu t
(8; 21) dan aneuploidi kromosom 7, 8, dan 9.38
11
Kesimpulan
Berdasarkan data di atas, dapat disimpulkan bahwa benzena merupakan bahan yang
paling luas pengunaannya dalam berbagai industri dan dapat menyebabkan leukemia myeloid
akut (LMA) pada pekerja yang terpajan benzena dalam jangka waktu tertentu. Pajanan benzena tertinggi dapat di temukan pada daerah lalu lintas kendaraan bermotor dan sekitar tempat pengisian bahan bakar kendaraan. Melalui biomolekular analisis telah membuktikan bahwa metabolit benzena dapat menghambat eritropoesis dengan jalur inhibisi aktivitas decatenation DNA dari topoisomerase II. Aktivitas topoisomerase II tidak dihambat apabila konsentrasi metabolit benzena kurang dari 500 pm. Penghambatan aktivitas topoisomerase oleh metabolit benzena telah dinyatakan sebagai mekanisme untuk pembentukan LMA.
Daftar Pustaka
1. Galbraith D, Gross S.A, Paustenbach D. Benzene and human health: A historical review and appraisal of associations with various diseases. Informa Healthcare 10 Jul 2010; 40(2): 1-46
2. Crebelli R,Tomei F, Zijno A, et al. Exposure to benzene in urban workers: environmental and biological monitoring of traffic police in Rome. Occup Environ Med 2001; 58:165–71
3. Infante PF. Benzene: an historical perspective on the American and European occupational setting. Late lessons from early warnings: the precautionary principle 2000:38-50
4. Egeghy P.P, Cabalo L.H, Gibson R, Rappaport S.M. Benzene and naphthalene in air and breath as indicators of exposure to jet fuel. Occup Environ Med 2003; 60:969-76 5. Labour Action China. Toxic chemicals killing chinese workers: a critical analysis and
case studies of benzene poisoning in China. Labour Action China April 2014: 1-39 6. ATSDR Division of Toxicology and Environmental Medicine. Benzene. ATSDR
Atlanta, GA: U.S. Department of Public Health and Human Services, Public Health Service. Agustus 2007: 1-2
7. New Hampshire Departement of Environmental Service. Benzene: health information summary. New Hampshire Departement of Environmental Service 2013: 1-3
8. Zappala RA, Bisgaard LB, Smith. Benzene - A Primer for Defence Counsel. 2010: 1-4
12 10.American Bar Association Action of Litigation. Shoebotham J, Thompson, Knight, Houston.Recent developments in benzene litigation. American Bar Association 2013: 1-2
11.Richardson D.B. Temporal variation in the association between benzene and leukemia mortality. Environmental Health Perspectives March 2008; 116 (3): 370-4
12.Polychronakis I, Dounias G, Makropoulos V et al. Work related leukemia: systematic review. Journal of Occupational Medicine and Toxicology 2013;8:1-16.
13.Benzene. Priority existing chemical assessment report no.21. NICNAS. Australia Sep 2001:113
14.Smith M.T, Jones R.M, Smith A.H. Benzene exposure and risk of non-hodgkin lymphoma. Cancer Epidemiol Biomarkers Prev March 2007; 16(3): 385-91
15.Sorahan T, Kinlen L.J, Doll R. Cancer risks in a historical UK cohort of benzene exposed workers. Occup Environ Med 2005; 62: 231–6
16.Al-Faisal A.H.M, Hussein A.M, Kaleg A.R.A. Estimation of DNA damages, cytotoxicity and antioxidant status of heavy metals and benzene among petrol workers in Baghdad-Iraq. IJPS 2010; 6(1): 85-94.
17.Salim R.N. Analisis risiko kesehatan pajanan benzene pada karyawan di SPBU X pancoran mas Depok 2011:1-87.
18.Haney J.T. Benzene. Texas commission on environmental quality. 15 Okt 2007; 4-21
19.Collins J.J, Ireland B, Buckley C.F, Shepperly D. Lymphohaematopoeitic cancer mortality among workers with benzene exposure. Occup Environ Med. 2003; 60: 676 -9
20.Huff J. Benzene-induced cancers: Abridged history and occupational health impact. IJOEH. 2007; 13(2): 213-21
21.Kirkeleit J, Riise T, Gjertsen B.T, et al. Effects of benzene on human hematopoiesis. The open hematology Journal. 2008; 2: 87-102
22.Perbellini J.L, Faccini G.B, Pansini F, et al. Environmental and occupational exposure to benzene by analysis of breath and blood. Br J Ind Med. 1988; 45: 345-52).
23.Langley A, Gilbey M, Kennedy B. Benzene poisoning and lymphohaemopoietic malignancy. EPHC. 2003: 1-6
24.Khan H.A. Benzene’s toxicity: a consolidated short review of human and animal studies. Human & Experimental Toxicology 2007:1–9
13 2005; 49(3): 233–40
26.Exposure to Benzene: A major public health concern. WHO 2010:1-5
27.Smith M.T, Rothman N. Biomarkers in the molecular epidemiology of benzene -exposed workers. Taylor & Francis 2000;61:439-45
28.Bois F.Y, Jackson E.T, Pekari K, Smith M.T. Population toxicokinetics of benzene. Environmental health perspectives Dec 1996; 104(6):1405-11
29.Dhiman A, Hiremath S.K. , Pathak M et all. A Review article on anticancerous drugs in ayurveda and screened anticancer activity of medicinal plants, Int. J. Ayu. Alt. Med 2014; 2(4):54-60.
30.Farmers exposed to benzene in gasoline through multiple routes. National Institute for Farm Safety 14-18 Juni 2009:1-23.
31.Rathnasabapathy R. Management of acute myelogenous leukemia in the elderly. Lancet JE. the James P.Wilmot Cancer Center,University of Rochester Nov 2003;10(6): 469-77.
32.Miller RW. Epidemiology of leukemia epidemiology of leukemia. National Cancer Institute.37-41.
33.Lovern M.R, Turner M.J, Meyer M, et al. Identification of benzene oxide as a product of benzene metabolism by mouse, rat, and human liver microsomes. Oxford University Press. 1997; 18(9):1695-700.
34.Baker R.K, Kurz E.U, Pyatt D.W, et al.Benzene metabolites antagonize etoposide -stabilized cleavable complexes of DNAtopoisomerase IIa. Blood. 1 Agustus 2001; 98(3): 830-3.
35.Kirkeleit J, Riise T, Gjertsen B.T, et al. Effects of benzene on human hematopoiesis. The Open Hematology Journal 2008;2:87-102.
36.Smith M.T, Zhang L, McHale C.M, et al. Benzene, the exposome and future investigations of leukemia etiolog. NIH Public. Chem biol interact. 2011: 1-11.
37.Synder R. Leukemia and benzene. Int. J. Environ. Res. Public Health. 2012; 9: 2876 -93.
38.Smith M.T. Advances in understanding benzene health effects and susceptibility. Annu. Rev. Public Health. 2010;31:133–48.
39.Mchale C.M, Zhang L, Smith M.T. Current understanding of the mechanism of benzene-induced leukemia in humans: implications for risk assessment. Oxford University Press. 2011; 33(2): 240-52.