BAB II
TINJAUAN PUSTAKA
2.1 Tumbuhan Kol
2.1.1 Budidaya Tanaman Kol
Faktor utama dalam budidaya tanaman kol adalah temperatur iklim dan tempat penanaman. Kol dapat tumbuh baik pada daerah beriklim sejuk. Secara umum , temperatur yang terbaik untuk produksi tanaman kol berkisar pada temperatur 500 – 700 F. Kemudian musim yang cukup menguntungkan untuk budidaya jenis tanaman ini pada musim penghujan dan awal musim kemarau. Pengaruh iklim dengan daerah yang cukup air juga bisa menjanjikan untuk budidaya tanaman kol.
Kol tumbuh dalam beberapa varietas tanah. Secara umum tanaman untuk pangsa pasar dan pengiriman jarak jauh , ditanam dalam tanah yang agak berpasir. Untuk jenis penyimpanan dalam gudang , kol juga dapat tumbuh dengan baik pada kondisi tanah liat dan untuk industri , sebaiknya tanah diberikan sedikit asam agar varietas yang tumbuh nantinya tahan terhadap layu dan penyakit fungus yang serius.
Sebagimana yang dinyatakan sebelumnya , kol ditanam dengan pola pembesaran kuncup. Seperti tanaman komoditi yang lainnya ini merupakan kewajiban, pertumbuhan periode pertama komoditi yang lainnya ini merupakan kewajiban , pertumbuhan periode pertama harus pada pertumbuhan akar , daun dan batang. Dan periode berikutnya , difokuskan pada perkembangan organ yang dalam. Selama periode awal perkembangan kol yang menghasilkan banyak daun hijau dan kadang – kadang , daun – daun muda tersebut ada yang tumbuh dari dalam tanpa mengandung klorofil. Daun ini biasanya gemuk dan penuh dengan pati dan gula. Selama dalam tahap produksi harus difokuskan pada banyaknya daun yang dihasilkan.
Ada tiga tahap awal budidaya kol :
1. Menanam langsung benih kedalam tanah 2. Menanam langsung di aeral terbuka
Proses penanaman dapat dilakukan dengan cara manual ataupun mekanik. Secara umum penentuan jarak berpengaruh besar dalam kualitas dan kesuburan dari tanah itu sendiri. Biasanya pengaturan jarak rentang tanam diatur dari 12 – 18 inci dengan jarak lebar per tanaman 3,3 atau 4 kaki per bagian tanaman ( Muller HG, 1980 ).
2.1.2 Kandungan dan Manfaat Tumbuhan Kol
Kol merupakan jenis tumbuhan lunak , yang memerlukan proses penggemburan tanah dan pengairan yang cukup untuk menghasilkan jenis kol yang berkwalitet. Umumnya jenis sayuran kol yang merupakan produk andalan dalam proses niaga , mempunyai ciri khas dapat langsung dijadikan lalapan dengan adanya tanda – tanda dari daun pembungkus kol tersebut yang berwarna hijau tua.
Sedikit banyak tentang proses pembudidayaan kol , harus dilakukan dengan pengawasan yang ketat , dikarenakan tanaman kol ini rentan terhadap perubahan kelembapan dan cuaca ekstrim yang mendadak , yang tentu saja dapat mengurangi kualitas kol tersebut di pasaran dan juga zat – zat penting yang terkandung dalam kelopak daun kol ini.
Secara umum , sebuah kol segar mengandung air , protein , lemak , karbohidrat , serat , kalsium , fosfor , besi , besi , natrium , kalium , vitamin A , vitamin C , vitamin E , tiamin , riboflavin , nicotinamide , kalsium dan beta karoten.
Selain itu , kol mengandung senyawa sianohidroksibutena ( CHB ) , sulforafan dan iberin yang merangsang pembentukan glutation , suatu enzim yang bekerja dengan cara menguraikan dan membuang zat – zat beracun yang beredar didalam tubuh, Tingginya kandungan vitamin C dalam kol ini dapat mencegah timbulnya Scorbut ( scury ).
dalam sulfurnya juga berkhasiat menurunkan kadar kolesterol yang tinggi , penenang saraf dan pembangkit semangat.
Adapun kegunaan lain dari tumbuhan kol adalah sebagai berikut : 1. Pengobatan gatal akibat jamur candida ( candidiasis)
2. Menghilangkan jamur di kulit kepala , tangan dan kaki 3. Radang sendi
4. Melindungi tubuh dari sinar radiasi , seperti sinar X-ray , komputer , microwave dan televisi berwarna
5. Antidot pada pemabuk alkohol ( hangover ) , racun di hati 6. Menghilangkan keluhan prahaid ( premenstrual syndrom ) 7. Meningkatkan produksi ASI dan
8. Sulit buang air besar ( sembelit ) ( Edmond JB , 1957 ).
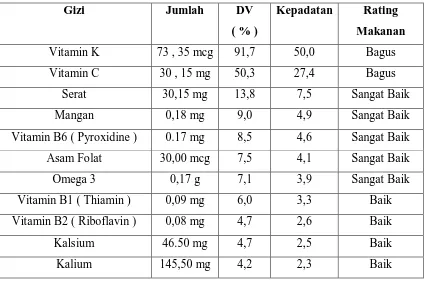
Berdasarkan data yang dihimpun oleh badan dunia WFO , jumlah kalori dan kandungan zat lain dalam kol , sangat menjanjikan komoditi kol dapat memenuhi asumsi nilai gzi dan nutrisi kebutuhan pangan dunia. Kalori yang dihasilkan dari 150 gram kol setelah direbus dalam 1 L air adalah 33 kalori dan nilai gizi terdapat pada tabel II.1 dibawah ini.
Tabel II.1 : Nilai gizi dalam 150 gram kol
Vitamin A 198,00 IU 4,0 2,2 Baik
Triptofan 0,01 g 3,1 1,7 Baik
Protein 1,53 g 3,1 1,7 Baik
Magnesium 12,00 mg 3.0 1,6 Baik
Berdasarkan data dari Badan Pangan Dunia ( WFO )
Rating Kesehatan Makanan Dunia Peraturan
Bagus DV >=75% atau Kepadatan >=7,6 dan DV.=10%
Sangat Baik DV>=50% atau Kepadatan>=3,4 dan DV>=5%
Baik DV>=25% atau Kepadatan>=1,5 dan DV>=2,5%
2.2 Vitamin C
2.2.1 Sejarah Umum Vitamin C
Vitamin merupakan suatu molekul organik yang sangat diperlukan tubuh untuk proses metabolisme dan pertumbuhan yang normal. Vitamin tidak dapat dihasilkan oleh tubuh manusia dalam jumlah yang cukup, oleh karena itu harus diperoleh dari bahan pangan yang dikonsumsi. Terkecuali pada vitamin D, yang dapat dibentuk dalam kulit jika kulit mendapat sinar matahari.
Dalam bahan pangan hanya terdapat vitamin dalam jumlah relatif sangat kecil, dan terdapat dalam bentuk yang berbeda-beda, diantaranya ada yang berbentuk provitamin atau calon vitamin (precursor) yang dapat diubah dalam tubuh menjadi vitamin yang aktif. Segera setelah diserap oleh tubuh provitamin akan mengalami perubahan kimia sehingga menjadi satu atau lebih bentuk yang aktif.
2.2.2 Sifat Vitamin C Sifat-sifat vitamin C adalah:
1.Vitamin C merupakan vitamin yang paling mudah rusak.
2.Vitamin C mudah teroksidasi dan proses tersebut dipercepat oleh panas, sinar, alkali, enzim, oksidator, serta oleh katalis tembaga dan besi.
Vitamin C dalam tubuh berguna dalam dalam pembentukan dan pemeliharaan zat perekat yang menghubungkan sel-sel dengan sel dari berbagai jaringan.
Kekurangan vitamin C dapat menyebabkan melemahnya dinding kapiler-kapiler darah sehingga mempermudah pedarahan. Kekurangan vitamin C juga dapat mengakibatkan perubahan susunan tulang dan tulang muda (kartilase), gusi berdarah,dan gigi.
Juga asam askorbin ini juga berpengaruh dalam pembentukan sel-sel darah dalam susunan tulang serta dalam pemeliharaan kadar haemoglobin yang normal. Penyakit skorbut, yang diakibatkan oleh kekurangan vitamin C adalah penyakit defisiensi yang paling lama dikenal. Sifat vitamin C mudah larut dalam air dan akan mudah rusak dengan pemanasan yang terlalu lama.
Berbagai faktor yang dapat mempengaruhi kadar vitamin C dalam makanan antara lain:
- Bahan makanan yang disimpan terlalu lama.
Vitamin C umumnya banyak sekali terdapat dalam bahan makanan, seperti buah-buahan yang masak. Cadangan vitamin C dalam tubuh dalam kelenjar adrenalin, kelenjar tumys dan lain-lain. Jumlah cadangan vitamin C ini tergantung pada jumlah vitamin C yang terdapat dalam makanan sehari-hari.
Oksidasi akan terhambat bila vitamin C dibiarkan dalam keadaan asam, atau pada suhu rendah. Vitamin C dapat terserap sangat cepat dari alat pencernaan kita masuk ke dalam saluran darah dan dibagikan ke seluruh jaringan tubuh. Kelenjer adrenalin mengandung vitamin C yang sangat tinggi.
Pada umumnya tubuh menyerap vitamin C sangat sedikit. Kelebihan vitamin C dari konsumsi makanan akan dibuang melalui air kemih. Karena itu bila seseorang mengkonsumsi vitamin C dalam jumlah besar (megadose), sebagian besar akan dibuang keluar, terutama bila orang tersebut biasa mengkonsumsi makanan bergizi tinggi. Tetapi sebaliknya, bila sebelumnya orang tersebut jelek keadaan gizinya, maka sebagian besar dari jumlah itu dapat ditahan oleh jaringan tubuh.
2.2.3 Akibat Kekurangan Vitamin C
Kekurangan vitamin C akan menyebabkan penyakit sariawan atau skorbut. Penyakit skorbut biasanya jarang terjadi pada bayi; bila terjadi pada anak-anak, biasanya pada usia setelah 6 bulan dan dibawah 12 bulan.
Gejala-gejala penyakit skorbut ialah terjadinya pelembekan tenunan kolagen, infeksi, dan demam. Juga timbul sakit, pelunakan, dan pembengkakan kaki bagian paha. Pada anak yang giginya telah keluar, gusi membengkak, empuk, dan terjadi pendarahan.
Penyakit sariawan yang akut dapat disembuhkan dalam beberapa waktu dengan pemberian 100 sampai 200 mg vitamin C per hari. Bila penyakit sudah kronik perlu diperlukan waktu lebih lama untuk penyembuhannya dan suplai vitamin C yang lebih.
2.2.4 Sumber Vitamin C
Sumber vitamin C sebagian besar berasal dari sayuran dan buah-buahan, terutama buah-buahan segar. Karena itu vitamin C sering disebut Fresh Food Vitamin. Buah yang masih mentah lebih banyak kandungan vitamin C-nya; semakin tua buah semakin berkurang kandungan vitamin C-nya.
Mengkonsumsi buah dalam keadaan segar jauh lebih baik dari buah yang sudah diolah. Pengolahan pada buah-buahan dengan menggunakan panas, akan mengakibatkan kerusakan pada vitamin C. Vitamin C mudah larut dalam air dan mudah rusak oleh oksidasi, panas, dan alkali. Karena itu agar vitamin C tidak banyak hilang, sebaiknya pengirisan dan penghancuran yang berlebihan dihindari.
Buah jeruk, baik yang dibekukan maupun yang dikalengkan merupakan sumber vitamin C yang tinggi. Demikian juga halnya berries, nenas, dan jambu. Beberapa buah tergolong buah yang tidak asam seperti pisang, apel, pear, dan peach rendah kandungan vitamin C-nya, apalagi bila produk tersebut dikalengkan.
Bayam, brokoli, cabe hijau, dan kubis juga merupakan sumber vitamin C yang baik, bahkan juga setelah dimasak
Sebaliknya beberapa jenis bahan pangan hewani seperti susu, telur, daging, ikan, dan unggas sedikit sekali kandungan vitamin C-nya.
Konsumsi bahan sayuran dan buah dalam keadaan segar, dapat menyediakan kebutuhan tubuh akan vitamin ini. Hanya saja terkadang kita sering kurang memperhatikan cara pengolahan bahan yang benar, sehingga vitamin C rusak dan terbuang percuma.
Saat proses merebus sayuran, guna mempertahankan kesegaran warna sering ditambahkan baking soda. Penambahan baking soda pada saat memasak sayuran, dapat merusak kandungan vitamin C pada sayuran. Oleh karena itu sebaiknya dalam pengolahan sayuran tidak menggunakan bahan tambahan yang dapat merusak kandungan zat gizi.
Kandungan vitamin C pada beberapa jenis sayuran: 1. Bayam dan tekokak : 80 mg / 100 g
2. Daun katuk : 239 mg / 100 g 3. Daun kelor : 220 mg / 100 g 4. Dan singkong : 275 mg / 100 g 5. Daun talas : 163 mg / 100 g 6. Daun lobak : 109 mg / 100 g 7. Daun melinjo : 182 mg / 100 g 8. Daun oyong : 150 mg / 100 g 9. Peterseli : 193 mg / 100 g
2.3. Titrasi Iodometri 2.3.1 Titrasi Redoks
Semula istilah oksidasi diterapkan pada reaksi suatu senyawa yang bergabung dengan oksigen dan istilah “reduksi” digunakan untuk menggambarkan reaksi dimana oksigen diambil dari suatu senyawa. Suatu reaksi redoks dapat terjadi apabila suatu pengoksidasian bercampur dengan zat yang dapat tereduksi. Dari percobaan masing-masing dapat ditentukan pereaksi dan hasil reaksi serta koefisiennya masing-masing-masing-masing.
Reduksi–oksidasi adalah proses perpindahan elektron dari suatu oksidator ke reduktor. Reaksi reduksi adalah reaksi penangkapan elektron atau reaksi terjadinya penurunan bilangan oksidasi. Sedangkan reaksi oksidasi adalah pelepasan elektron atau reaksi terjadinya kenaikan bilangan oksidasi. Jadi, reaksi redoks adalah reaksi penerimaan elektron dan pelepasan elektron atau reaksi penurunan dan kenaikan bilangan oksidasi.
Reaksi redoks secara umum dapat dituliskan sebagai berikut :
Ared + Boks - Aoks + Bred
Jika suatu logam dimasukkan ke dalam larutan yang mengandung ion logam lain, ada kemungkinan terjadi reaksi redoks, misalnya:
Ni(s) + Cu2+(l) Ni2+ + Cu(s)
Artinya logam Ni dioksidasi menjadi Ni2+ dan Cu2+ di reduksi menjadi logam Cu.
Demikian pula peristiwa redoks tersebut terjadi pada logam lain seperti besi. Sepotong besi yang tertutup lapisan air yang mengandung oksigen akan mengalami korosi.
Fe Fe2+ + 2e-
Dan reaksi yang terjadi pada karbon sebagai katoda yaitu :
½ O2 + H2O+ 2e- + 2OH- ( Day & Underwood 1981 ).
Ada beberapa cara untuk mencegah terjadinya korosi, salah satunya dengan menutup permukaan logam dengan zat lain agar tidak terjadi kontak langsung dengan lingkungan, seperti memberi cat, mengoleskan minyak atau oli, atau dengan cara melapisi logam dengan dengan logam lain yang lebih mudah teroksidasi, misalnya magnesium (Mg). Elektron yang dibutuhkan oleh oksigen diambil dari magnesium bukan dari logam yang dilindungi. Suatu proses reduksi dan oksidasi yang berlangsung secara spontan merupakan pengertian lain dari redoks. Dalam artian, selama berlangsungnya oksidasi, oksidatornya sendiri akan tereduksi pula. Begitu pula juga sebaliknya. Dengan demikian suatu proses oksidasi selalu disertai dengan proses reduksi dan sebaliknya. Redoks kadang-kadang juga sebagai perubahan kimia yang didalamnya terdapat peralihan elektron dari suatu proses atom atau molekul atau ion lain. Dalam proses-proses elektrokimia dalam sel-sel oksidasi (pada anoda) dan reduksi (pada katoda) juga terjadi. Sistem ini pun acap kali dikenal sebagai sistem redoks.
Kafein merupakan alkaloid dengan penamaan kimia 1, 3,7-trimetil xanthina. Dalam aktivitasnya secara faal, kafein berfungsi sebagai stimulat/perangsang. Kadar kafein dalam daun teh labih besar daripada di dalam biji kopi. Kadar kafein di dalam teh adalah sebesar 2-4%, sedangkan di dalam biji kopi hanya mencapai 0,5%.
Kafein terdapat pada teh, kopi, kola, mente dan coklat. Selain itu kafein juga dapat diperoleh dari sintesa kimia. Kadar kafein dalam teh lebih besar dari pada di dalam kopi. Kadar kafein di dalam teh 2-4%, sedangkan di dalam kopi hanya 0,5%. Kafein dapat bereaksi dengan iodium secara adisi, sehingga kadar kafein dapat diukur dengan larutan Iodium. Untuk reaksi adisi dengan kafein digunakan iodium berlebih, kelebihan iodium di analisa dengan titrasi redoks, yaitu penetapan kadar zat berdasarkan atas reaksi reduksi dan oksidasi.
I2 + 2e-2I
-2S2O32-S4O62- + 2e
-I2 + 2S2O32-2I- + S4O62
-Untuk mengetahui kadar kafein, maka terlebih dahulu teh diekstraksi dengan alkohol. Kemudian larutan yang mengandung kafein ini ditambahkan larutan iodium yang telah diketahui volume dan konsentrasinya. Kelebihan iodium setelah terjadi reaksi adisi di titrasi dengan larutan natrium thiosulfat (Na2S2O3), sehingga iodium yang teradisi oleh kafein dapat dihitung.
Kristal natrium thiosulfat dengan rumus kimianya Na2S2O3.5H2O, meskipun garam natrium thiosulfat mudah dperoleh dalam keadaan murni, tetapi oleh karena kandungan air krisatalnya tidak dapat diketahui dengan tepat sehingga larutannya tidak dapat digunakan sebagai larutan standar primer, artinya untuk menjadi larutan standar, larutan natrium thiosulfat harus distandarisasikan dahulu menggunakan larutan standar lain (primer) seperti K2Cr2O7, KIO3, Cu dan lain-lain. Penggunaan pelarut air yang tentunya masih mengandung CO2 yang dapat bebas, meskipun penguraiannya sangat lambat. Disamping hal tersebut, terjadinya penguraian juga disebabkan karena keaktifan bakteri Thiobacillus Thioparus.
Kalium dikromat merupakan pereaksi oksidasi yang cukup kuat, potensial standar dari reaksi :
Cr2O7 + 14 H+ + 6 e- 2Cr2- + 7 H2O
Akan tetapi ia tak sekuat permanganat atau ion Serium (IV). Keuntungannya adalah tidak mahal, sangat labil dalam larutan, dan dapat diperoleh dalam bentuk cukup murni untuk pembuatan larutan standar dengan menimbang langsung. Sering digunakan sebagai larutan standar primer untuk larutan natrium thiosulfat.
reaksi yang diharapkan terjadi dalam analisis. Titik ekuivalen pada titrasi redoks tercapai saat jumlah ekuivalen dari oksidator telah setara dengan jumlah ekuivalen dari reduktor. Bebrapa contoh dari titrasi redoks antara lain adalah titrasi permanganometri dan titrasi iodometri/iodimetri. Titrasi iodometri menggu nakan larutan iodium (I2) yang merupakan suatu oksidator sebagai larutan standar. Larutan iodium dengan konsentrasi tertentu dan jumlah berlebih ditambahkan ke dalam sampel, sehingga terjadi reaksi antara sampel dengan iodium. Selanjutnya sisa iodium yang berlebih dihiung dengan cara mentitrasinya dengan larutan standar yang berfungsi sebagai reduktor ( Anita F.P, 1973 ).
2.3.2 Iodometri
Metode titrasi langsung dinamakan iodimetri mengacu kepada titrasi dengan suatu larutan iod standar .Sedangkan metode titrasi tak langsung dinamakan iodometri adalah berkenaan dengan titrasi dari iod yang dibebaskan dalam reaksi kimia .Potensial reduksi normal dari sistem reversibel adalah 0,5345 volt.
I2 (solid) + 2e-↔ 2I
-Karena iod mudah larut dalam larutan iodida. Reaksi setengah sel itu lebih baik ditulis sebagai berikut :
I3- + 2e- ↔ I3
-Dan potensial reduksi standarnya adalah 0,5355 volt .Maka iod atau ion triiodida merupakan zat pengoksidasi yang jauh lebih lemah ketimbang kalium permangganat, kaliumdikhromat dan serium (IV) sulfat.
Dalam kebanyakan titrasi langsung dengan iod ,digunakan suatu larutan iod dalam kalium iodide, dan karena itu spesi reaktifnya adalah ion triiodida . Untuk tepatnya ,semua persamaan yang melibatkan reaksi-reaksi iod seharusnya ditulis dengan I3- dan bukan dengan I2 , misal :
akan lebih akurat dari pada :
I2 + 2S2O32-↔ 2I- + S4O6
2-Namun demi kesederhanaan, persamaan dalam buku ini biasanya lebih banyak ditulis dengan rumus-rumus iod molekuler dari pada ion triiodida( Day & Underwood 1981).
Zat-zat pereduksi yang kuat ( zat-zat dengan potensial yang jauh lebih rendah) ,seperti timah(II)klorida, asam sulfat, hydrogen sulfida , dan natrium tiosulfat bereaksi lengkap dan cepat dengan iod, bahkan dalam larutan asam . dengan zat oereduksi yang agak lemah ,misal arsen trivalent, atau stibium trivalent ,reaksi yang lengkap hanya akan terjadi bila larutan dijaga tetap netral atau sangat sedikit suasana asam.Pada kondisi ini potensial reduksi dari zat pereduksi adalah minimum , atau daya mereduksinya adalah maksimum.
Jika suatu zat pengoksidasi kuat diolah dalam larutan yang netral atau larutan yang asam ,dengan ion iodide yang sangat berlebih , yang terakhir bereaksi sebagai zat pereduksi,dan oksidan akan direduksi secara kuantitatif. Dalam hal-hal demikian , sejumlah iod yang ekuivalen akan dibebaskan ,lalu dititrasi dengan larutan standar suatu zat pereduksi, biasanya natrium tiosulfat.
Potensial reduk si normal dari system iod-iodida tak bergantung pada pH larutan , selama yang terakhir berada pH ± 8 , pada nilai-nilai yang lebih tinggi , iod bereaksi dengan ion hidroksida untuk membentuk iodida dan hipoiodit yang sangat tidak stabil, dimana hasil terakhir ini cepat sekali diubah menjadi iodat dan iodide oleh reaksi oksidasi dan reduksinya sendiri :
I2 + 2OH-↔ I- + H2O
3IO- ↔ 2I- +IO3
-Tembaga murni dapat digunakan sbagai standar primer untuk Iod dan natrium tiosulfat dan dianjurkan apabila tiosulfat harus digunakan untuk penetuan tembaga . potensial standar pasangan Cu (II) – Cu (I)
Adalah + 0,15 V dan dengan emikian iodium Eo = +0,53 V merupakan reaksi oksidasi yang lebih baik dari pada ion Cu (II) . Akan tetapi bila ion iodide ditambahkan pada suatu larutan Cu (II) ,maka suatu endapan CuI terbentuk.
2Cu2+ + 4 I- → 2 CuI (p) + I2
Reaksinya dipaksa berlangsung kekanan denagn pembentukan endapan dan juga dengan penambahan ion iodide berlabih ( Basset , 1994 ).
pH larutan harus dipertahankan oleh suatu system buffer, lebih baik antara 3 dan 4 . Pada harga pH lebih tinggi hidrolisa sebagian dari ion Cu (II) berlangsung dan reaksi denagn ion iodide adalah lambat.dalam larutan berasam tinggi oksidasi dengan katalis tembaga dari ion iodide terjadi dengan kecepatan yang cukup tinggi.
Jika anion (sepsert asetat) digunakan dalam buffer membentuk suatu kompleks cukup stabil dengan ion Cu (II) , reaksi antara ion Cu (II) dan ion iodide dapat dicegah untuk berlangsung secara lengkap. Jika iodium dihilangkan dengan titrasi dengan tiosulfat, kompleks Cu(II) berdisosiasi untuk membentuk ion Cu (II) lebih benyak , yang pada gilirannay bereaksi denagn iodide untuk membebaskan lebih banyak iodium . Ini menyebabkan suatu titik akhir yang terulang kembali.
Telah diketahui bahwa iodium ditahan karena adsorbsi pada permukaan endapan tembaga (II) iodide dan membuatnya berwarna abu-abu dari pada putih. Kecuali kalau iodium dihilangkan , maka titik akhir dicapai terlalu cepat dan dapat berulang jika iodium lambat dilapaskan dari permukaan ( Day & Underwood , 1981 ).
2.3.3 Iodometri Pada Sayuran Kol
Derajat kelarutan asam (atau derajat disosiasi asam, dilambangkan dengan pKa) dalam kimia digunakan sebagai ukuran kelarutan suatu asam (atau basa) dalam pelarut air dengan kondisi standar (1 atm dan 25°C). Nilai pKa didefinisikan sebagai "minus logaritma terhadap konsentrasi ion H+ dalam larutan". Definisi ini menyebabkan konsentrasi yang lebih tinggi memberikan nilai yang lebih rendah. Ukuran kelarutan diukur dari banyaknya ion H+ (dalam mol per liter larutan atau molar) terlarut. Air murni memiliki rumus kesetimbangan kelarutan: H2O <==> H+ + OH-.
Vitamin C atau asam askorbat mempunyai berat molekul 178 dengan rumus molekul C6H806. Dalam bentuk Kristal tidak berwarna, titik cair 190-1920C.bersifat larut dalam air sedikit larut dalam aseton atau alcohol yang mempunyai berat molukul rendah. Vitamin C sukar larut dalam kloroform, ether dan benzene. Vitamin C dengan logam akan membentuk garam. Sifat asam ditentukan oleh ionisasi enolgroup pada atom C nomor 3. Pada pH rendah vitamin C lebih stabil daripada pH tinggi. Vitamin C mudah teroksidasi lebih-lebih apabila terdapat katalisator Fe, Cu, enzim askorbat oksidase, sinar dan temperature yang tinggi. Larutan encer vitamin C pada pH kurang dari 7,5 masih stabil apabila tidak ada katalisator seperti diatas. Oksidasi vitamin C akan terbentuk asam dehidroasam askorbat.
Uji organoleptik didasarkan pada kegiatan penguji-penguji rasa (panelis) yang pekerjaannya mengamati, menguji, dan menilai secara organoleptik. Sensoris berasal dari kata “sense” yang berarti timbulnya rasa, dan timbulnya rasa selalu dihubungkan dengan panca indera. Leptis berarti menangkap atau menerima. Jadi pengujian sensoris atau organoleptik mempunyai pengertian dasar melakukan suatu kejadian yang melibatkan pengumpulan data-data, keterangan-keterangan atau catatan mekanis dengan tubuh jasmani sebagai penerima .
Reaksi percobaan adalah sebagai berikut :
Kadar vitamin C ditetapkan berdasarkan prinsip reduksi oksidasi yaitu dengan menggunakan titrasi iodimetri atau titrasi langsung. Dalam hal ini I2 atau iod adalah
sebagai titrant. Prinsip titrasi ini adalah analat atau contoh dioksidasi oleh I2 sehingga
I2 tereduksi menjadi ion iodida. I2 merupakan oksidator yang tidak terlalu kuat
sehingga hanya zat-zat yang merupakan reduktor yang cukup kuat yang dapat dititrasi. Indikator yang digunakan adalah amilum dengan perubahan warna dari tak berwarna menjadi biru.
Iod sebagai zat padat skar larut dalam air tetapi sangat mudah larut dalam larutan KI karena membentuk I3- sebagai berikut:
I2 + I- I3- ( Lee , FA 1975 )
Larutan iod dibuat dengan KI sebagai pelarut. Larutan iod ini bersifat tidak stabil sehingga perlu distandarisasi berulangkali terutama apabila akan dipakai sebagai titrant. Ketidakstabilan larutan iod disebabkan oleh penguapan iod, reaksi iod dengan karet, gabus dan bahan organic lain yang mungkin masuk dalam larutan lewat debu dan asap, serta disebabkan oleh oksidasi olleh udara pada pH rendah. Oksidasi ini dipercepat oeh cahaya dan panas. Maka hendaknya larutan ini disimpan pada tempat yang sejuk dengan botol berwarna gelap. Selain itu juga harus dihindarkan kontak dengan bahan organic maupun gas mereduksi seperti SO2 dan H2S. Bahan
Diencerkan dengan aquadest sampai tanda tera. Tujuan dari pengenceran ini adalah untuk mendapatkan konsentrasi analat yang sekecil mungkin. Dalam 5 g sampel buah atau sayur dimungkinkan terdapat banyak vitamin C dalam jumlah pekat sehingga perlu diencerkan lebih dahulu. Kocok agar larutan homogen. Pipet sebanyak 5 mL larutan sampel kedalam Erlenmeyer. Tambahkan 1 mL indikator amilum 1% kemudian dititrasi dengan larutan iodium 0,01 N ( Khopkar , 1994 ).
Vitamin C merupakan vitamin yang diperlukan oleh tubuh untuk meningkatkan sistem imunitas tubuh serta berfungsi sebagai antioksidan yang dapat menangkal senyawa radikal bebas penyebab penuaan serta munculnya sel-sel kanker.. Kebutuhan vitamin C yang tercukupi dapat menurunkan resiko terkena flu. Vitamin C mudah larut dalam air sehingga apabila terjadi kelebihan vitamin C akan dibuang melalui urin. Kebutuhan vitamin C setiap orang berbeda-beda tergantung pada daya tahan tubuhnya masing-masing.
Kekurangan vitamin ini dapat menyebabkan gusi berdarah, sariawan, nyeri otot atau gangguan syaraf. Kekurangan lebih lanjut mengakibatkan anemia, sering mengalami infeksi dan kulit kasar. Sementara kelebihan vitamin C dapat menyebabkan diare. Bila kelebihan vitamin C akibat penggunaan suplemen dalam waktu yang cukup lama dapat mengakibatkan batu ginjal, sedangkan bila kelebihan vitamin C yang berasal dari buah-buahan umumnya tidak menimbulkan efek samping.
Makanan yang mengandung vitamin C umumnya adalah buah-buahan dan sayuran. Buah yang mengandung vitamin C tidak selalu berwarna kuning, misalnya pada jambu biji yang merupakan buah dengan kandungan vitamin C paling tinggi yang dapat kita konsumsi. Bahkan, pada beberapa buah, kulitnya mengandung vitamin C lebih tinggi daripada buahnya. Misalnya pada kulit buah apel dan jeruk walaupun tidak semua kulit buah bisa dimakan.
timbulnya gas asam karbonat, hasil dari fermentasi kubis yang tidak dapat keluar dari perut.