BAB 2
TINJAUAN PUSTAKA
2.1. Myristica fragrans
Pala (Myristica fragrans) merupakan tumbuhan berupa pohon yang berasal dari kepulauan Banda, Maluku. Semenjak zaman eksplorasi Eropa Pala tersebar luas di daerah tropika lain seperti Mauritius dan Karibia (Grenada). Tumbuhan ini berumah dua (dioecious) sehingga dikenal pohon jantan dan pohon betina. Daunnya berbentuk elips langsing. Buahnya berbentuk lonjong seperti lemon, berwarna kuning, berdaging dan beraroma khas karena mengandung minyak atsiri pada daging buahnya. Bila masak, kulit dan daging buah membuka dan biji akan terlihat terbungkus fuli yang berwarna merah. Satu buah menghasilkan satu biji berwarna coklat. Anatomi tumbuhan Pala ditunjukkan pada Gambar 2.1.
a b
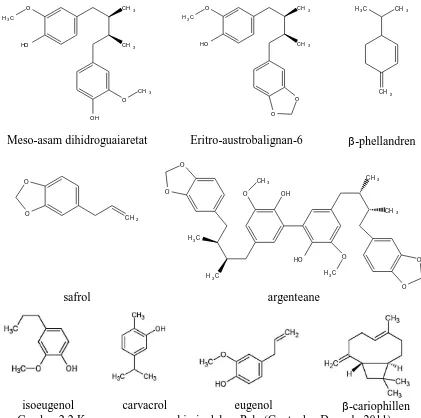
Gambar 2.1. Anatomi Tanaman Pala. Pohon Pala (a); Daun dan biji Pala (b) Bunga Pala mengandung senyawa lignan dan bersifat sebagai antioksidan dengan EC50 0,6 mg/mL (Chatterjee, 2007). Gopalarkishnan & Mathew, (1983)
bagian tumbuhan Pala seperti biji, buah, batang dan aril dapat dilihat pada Gambar
Meso-asam dihidroguaiaretat Eritro-austrobalignan-6 -phellandren
O
isoeugenol carvacrol eugenol -cariophillen
Klasifikasi ilmiah tanaman Pala yaitu Kerajaan : Plantae
Divisi : Magnoliophyta Kelas : Magnoliopsida Ordo : Magnoliales Famili : Myristicaceae Genus : Myristica
Spesies : M. fragrans Houtt
2.2. Senyawa Flavonoid
Senyawa flavonoid adalah senyawa polifenol yang mempunyai kerangka dasar karbon yang terdiri dari 15 atom karbon, dimana dua cincin benzen (C6) terikat pada
suatu rantai propan (C3) sehingga membentuk suatu susunan C6-C3-C6. Susunan ini
dapat menghasilkan 3 jenis struktur, yaitu 1,3-diarilpropana atau flavonoid, 1,2-diarilpropan atau isoflavonoid dan 1,1 1,2-diarilpropan atau neoflavonoid. Ketiga struktur kimia flavonoid dapat dilihat pada Gambar 2.3.
1 2 3
1 2 3
1 2 3
Flavonoid isoflavonoid neoflavonoid
Gambar 2.3. Struktur flavonoid
heterosiklik yang baru (cincin C) (Markham, 1988). Kerangka 2-fenilkroman dapat dilihat pada Gambar 2.4.
O
A C
B
1
4 2
3
Gambar 2.4. Kerangka 2-fenilkroman
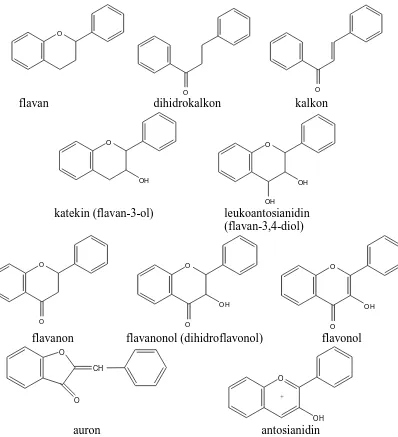
Senyawa heterosiklik pada tingkat oksidasi yang berbeda terdapat dalam kebanyakan tumbuhan. Berdasarkan tingkat oksidasi dari rantai propan dari sistem 1,3-diarilpropan, maka senyawa-senyawa flavonoid ini dibagi menjadi beberapa jenis. Kelompok senyawa kimia flavan dianggap sebagai senyawa induk dalam tatanama senyawa-senyawa turunan flavonoid karena mempunyai tingkat oksidasi terendah. Beberapa jenis flavonoid beserta struktur dasarnya dapat dilihat pada Gambar 2.5 (Markham, 1988).
Suatu jembatan oksigen yang melibatkan atom karbon sentral dari rantai C3
dalam alam, hanya terdapat dalam jumlah yang terbatas, dalam hal ini, cincin heterosiklis yang terbentuk adalah dari tipe furan, yaitu kerangka C15 dari 2-benzil
kumarin. Senyawa-senyawa auron misalnya termasuk dalam kelompok struktur ini. Selain sambungan atom karbon, senyawa flavonoid juga mempunyai pola oksigenasi dalam cincin benzennya. Substituen yang mungkin adalah –OCH3, -O-CH2-O- atau
0-glikosida. Sifat-sifat struktur yang lain adalah
O
O O
flavan dihidrokalkon kalkon
O
OH
O
OH OH
katekin (flavan-3-ol) leukoantosianidin (flavan-3,4-diol)
O
O
O
O
OH
O
O
OH
flavanon flavanonol (dihidroflavonol) flavonol
O
CH
O
O
OH +
auron antosianidin
OH
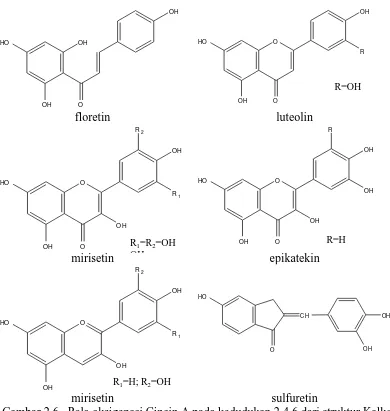
Gambar 2.6. Pola oksigenasi Cincin A pada kedudukan 2,4,6 dari struktur Kalkon b). Cincin B, kebanyakan mempunyai gugus fungsional oksigen berkedudukan para
atau dua oksigen berkedudukan para dan meta terhadap rantai C3 sentral, atau
tiga oksigen (satu para dan dua meta), seperti terlihat pada struktur senyawa diatas (Gambar 2.6). Senyawa yang mempunyai tiga gugus oksigen pada cincin B jarang dijumpai. Senyawa-senyawa dengan cincin B yang tidak teroksigenasi, atau
dengan substituen oksigen pada kedudukan orto juga jarang dijumpai (Leland et al., 2006).
Pada oksigenasi dari cincin A dan B seperti dikemukakan di atas, dimana cincin A mengikuti pola floroglusinol dan cincin B mengikuti pola katekol atau fenol dapat diterangkan oleh asal usul biogenetik (Achmad, 1986 dan Manitto 1992). Dalam tahap-tahap biosintesis awal, senyawa-senyawa flavonoid, kerangka C13 yang
dihasilkan, telah mempunyai substituen oksigen tertentu, kebanyakan sebagai gugus hidroksil pada kedudukan yang sesuai, sehubungan dengan pembentukan cincin A (jalur poliketida) dan dengan cincin B yang berasal dari shikimat (fenilalanin asam sinamat).
Setelah terjadi berbagai perubahan enzimatik, ketiga atom karbon sentral dari kerangka 1,3-diarilpropan dapat mempunyai berbagai gugus fungsional, misalnya hidroksil, ikatan rangkap karbonil dan sebagainya. Jadi keanekaragaman senyawa flavonoid, bukanlah disebabkan karena banyaknya variasi struktur, tetapi lebih disebabkan oleh berbagai tingkat hidroksilasi, alkoksilasi atau glikosilat. Dari penelusuran literatur, ditemukan beberapa jenis senyawa flavonoid. Adapun jenis-jenis flavonoid tersebut adalah :
1. Jenis kalkon 2. Jenis flavanon 3. Jenis flavon 4. Jenis flavonol 5. Jenis flavononol 6. Jenis auron
5. Jenis flavononol
Pola biosintesis flavonoid pertama kali disarankan oleh Birch. Menurut Birch, pada tahap-tahap pertama dari biosintesis flavonoid suatu unit C6-C3 berkombinasi
dengan tiga unit C2 menghasilkan unit C6-C3-(C2+C2+C2). Kerangka C15 yang
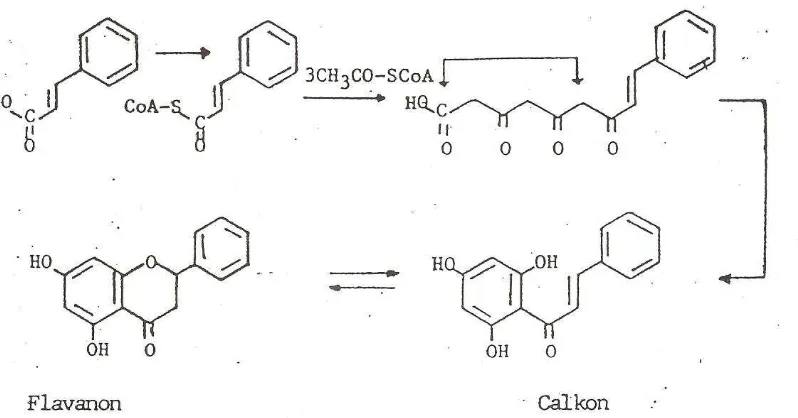
Adapun cincin A dari struktur flavonoid berasal dari jalur poliketida, yakni kondensasi dari tiga unit asetat atau malonat, sedangkan cincin B dan tiga atom karbon dari rantai propan berasal dari jalur fenilpropanoid (jalur shikimat). Dengan demikian, kerangka dasar karbon dari flavonoid dihasilkan dari kombinasi antara dua jalur biosintesis yang utama untuk cincin aromatik, yakni jalur shikimat dan jalur asetat-malonat. Selanjutnya, sebagai akibat dari berbagai perubahan, ketiga atom karbon dari rantai propan dapat menghasilkan berbagai gugus fungsi, seperti ikatan rangkap, gugus hidroksil, gugus karbonil, dan sebagainya. Reaksi biosintesis flavonoid ditunjukkan pada Gambar 2.7
Gambar 2.7. Reaksi biosintesis flavonoid (Dixon et al., 2002)
Menurut biosintesis ini pembentukan flavonoid dimulai dengan memperpanjang unit fenilpropanoid (C6-C3) yang berasal dari turunan sinamat seperti
Kalicin Antosianidin
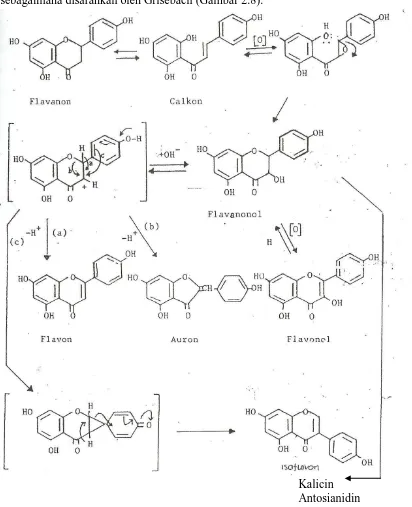
flavonoid lainnya. Adapun hubungan biogenetik antara berbagai jenis flavonoid, sebagaimana disarankan oleh Grisebach (Gambar 2.8).
Beberapa percobaan menggunakan senyawa bertanda, mendukung reaksi biosintesis di atas. Percobaan yang dilakukan oleh Grisebach menemukan bahwa calkon yang diberi bertanda dengan radioisotop 14C dan diberikan kepada tumbuhan tertentu, ternyata diinkorporasikan (digunakan) dalam berbagai senyawa flavonoid, seperti apigenin (suatu flavon), Quersetin (suatu flavonol), sianidin (suatu antosianidin) dan epikatekin (suatu katekin). Inkorporasi kalkon kedalam flavonoid juga ditunjukkan oleh percobaan-percobaan dengan penandaan rangkap. Misalnya kalkon yang bertanda pada cincin A dan pada posisi 2, bila diberikan kepada benih kubis merah, ternyata digunakan untuk menghasilkan sianidin radioaktif.
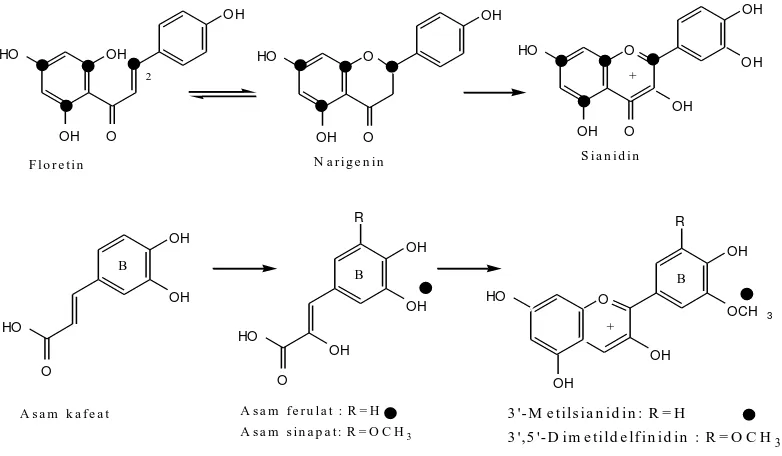
Suatu aspek lain dari biosintesis flavonoid yang telah diselidiki ialah saat daripada terjadinya oksigenasi pada cincin B. Percobaan menggunakan asam ferulat dan asam sinapat yang diberi bertanda dengan 14C pada gugus metoksil (-OCH3) dan
diberikan kepada tumbuhan. Petunia hibrida, menunjukkaan bahwa asam-asam ini diinkorporasikan ke dalam antosianidin yang dihasilkannya, dengan pola oksigenasi dari cincin B yang sebanding (Gambar 2.9).
OH
Hasil reaksi tersebut menjukkan bahwa oksigenasi cincin B dari struktur flavonoid terjadi pada tahap-tahap awal dari biosintesis flavonoid, yakni menggunakan turunan asam sinamat yang sesuai dan berasal dari fenilpropanoid yang ada.
2.3 Senyawa Antioksidan
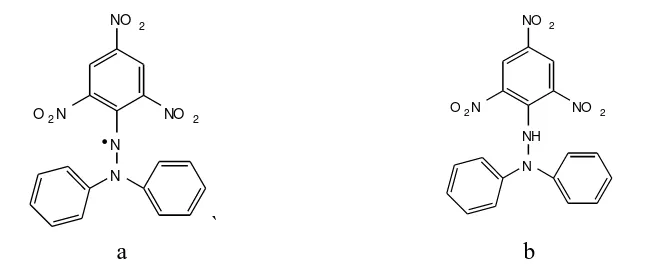
Antioksidan merupakan senyawa yang dapat menghambat laju oksidasi atau menetralisir radikal bebas, sehingga dianggap sebagai cancer preventive agent karena radikal bebas yang berlebihan dapat memicu terjadinya kanker (Yen dan Chen, 1995). Berbagai metode telah digunakan untuk mengukur kekuatan dari suatu antioksidan. Salah satu metode yang paling populer digunakan adalah metode peredaman radikal bebas dengan menggunakan reagen DPPH. Molekul DPPH dikarakterisasi sebagai radikal bebas yang stabil karena mekanisme delokalisasi elektron bebas oleh molekul yang mengalami resonansi radikal bebas dimana semakin banyak resonansi radikal bebas pada senyawa tersebut sehingga molekul ini tidak mengalami reaksi dimerisasi yang sering terjadi pada sebagian besar radikal bebas lainnnya. Delokalisasi juga memberikan efek warna ungu yang pada panjang gelombang 520 nm dalam pelarut metanol. Struktur DPPH ditunjukkan pada Gambar 2.10 (Molyneux 2004).
NO 2
Z* + AH Z H + A*
Dimana:
Z* = Radikal DPPH AH = Molekul donor
ZH = Bentuk tereduksi dari DPPH A* = Radikal bebas yang terbentuk
2.4. Senyawa Antimikroba
Senyawa antimikroba merupakan senyawa kimia yang dapat diperoleh dari beberapa spesies mikroorganisme dan tumbuh-tumbuhan. Komponen senyawa antimikroba tersebut pada konsentrasi rendah mampu menghambat atau mengganggu pertumbuhan mikroba sedangkan pada konsentrasi tinggi dapat membunuh mikroba. Senyawa antimikroba yang diperoleh dapat berupa minyak atsiri dan senyawa metabolit sekunder yang terkandung pada tumbuhan seperti terpenoid, steroid, alkaloid, dan flavonoid. Keadaan yang mempengaruhi kerja antimikroba ialah konsentrasi zat antimikroba, jumlah mikroorganisme, suhu, dan spesies (Pelczar, dan Chan, 1988). Mekanisme kerja senyawa antimikroba secara umum dapat menghambat atau membunuh mikroorganisme dengan beberapa cara yaitu merusak dinding sel, merubah permeabilitas sel, dan menghambat kerja enzim sehingga metabolisme sel terganggu atau matinya sel, serta menghambat sintesis asam nukleat dan protein (Fardiaz, 1989).
2.4.1. Escherichia coli
Escherichia coli adalah salah satu jenis spesies utama bakteri Gram negatif. Pada
pertumbuhannya sangat cepat dan mudah dalam penanganannya. Menurut Bergey dalam Capuccino (2001) klasifikasi E. coli adalah
Kingdom : Phylogenetica Divisi : Proteobacteria
Kelas : Gamma Proteobacteria Ordo : Enterobacteriales Famili : Enterobacteriaceae Genus : Escherichia
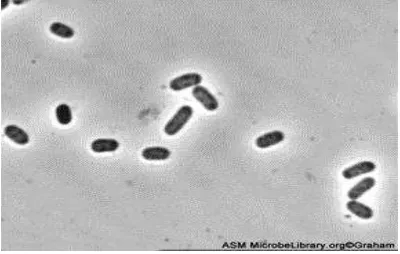
Species : Escherichia coli (Gambar 2.11)
Gambar 2.11 Escherichia coli
2.4.2. Staphylococcus aureus
Klasifikasi S. aureus menurut Bergey dalam Capuccino (2001) adalah : Kingdom : Monera
Divisio : Firmicutes Class : Bacilli Order : Bacillales
Family : Staphylococcaceae Genus : Staphylococcus
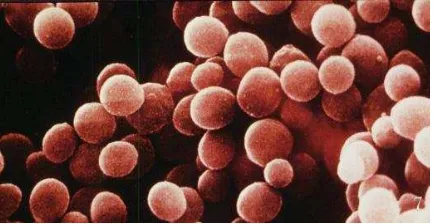
Gambar 2.12 Staphylococcus aureus
Staphylococcus aureus merupakan bakteri Gram positif, tidak bergerak, tidak
berspora dan mampu membentuk kapsul, berbentuk kokus dan tersusun seperti buah anggur sebagaimana terlihat pada Gambar 2.12. Ukuran Staphylococcus berbeda-beda tergantung pada media pertumbuhannya. Apabila ditumbuhkan pada media agar,
Staphylococcus memiliki diameter 0,5-1,0 mm dengan koloni berwarna kuning.
Dinding selnya mengandung asam teikoat, yaitu sekitar 40% dari berat kering dinding selnya. Asam teikoat adalah beberapa kelompok antigen dari Staphylococcus. Asam teikoat mengandung aglutinogen dan N-asetilglukosamin (Todard, 2002).
2.5. Senyawa Antifungi
Saat ini terdapat 1213 penelitian tentang senyawa antifungi, tetapi hanya ada beberapa saja yang terkait dengan tumbuhan. Pada tahun 2008 dilakukan penelitian terhadap senyawa antifungi Rubus ulmifolius. Minyak dari tumbuhan Biden pilosa
secara signifikan bersifat antibakteri dan jamur terhadap enam strain bakteri dan tiga strain jamur. Aktivitas daya hambat minyak bunga tumbuhan tersebut di dalam Gram negatif bakteri secara signifikan lebih tinggi dari Gram positif (Deba dkk, 2008). Aktivitas antifungi ekstrak air dan metanol dari tumbuhan cucumber Laut Mediterania, Holothuria polii, juga telah diteliti (Ismail, dkk, 2008) dan dilaporkan ekstrak tersebut secara signifikan aktif antifungi terhadap strain Aspergillus fumigatus
pada konsentrasi 150–300 μg/well. Senyawa kimia sesquiterpen lakton baru dari
bakteri dan delapan spesies jamur (Djeddi dkk, 2008). Total fenolik dari ekstrak aseton, etanol, metanol, butanol dan air biji Pala mempunyai aktivitas yang kuat terhadap jamur Aspergillus niger (Gupta et al, 2013). Salah satu jamur penyebab keputihan adalah Candida albicans.
Candida albicans merupakan jamur dimorfik karena kemampuannya untuk
tumbuh dalam dua bentuk yang berbeda yaitu sebagai sel tunas yang akan berkembang menjadi blastospora dan menghasilkan kecambah yang akan membentuk hifa semu. Perbedaan bentuk ini tergantung pada faktor eksternal yang mempengaruhinya. Sel ragi (blastospora) berbentuk bulat, lonjong atau bulat lonjong dengan ukuran 2-5 μ x 3-6 μ hingga 2-5,5 μ x 5-28 μ (Gambar 2.13).
Gambar 2.13. Morfologi Candida albicans
Candida albicans memperbanyak diri dengan membentuk tunas yang akan
terus memanjang membentuk hifa semu. Hifa semu terbentuk dengan banyak kelompok blastospora berbentuk bulat atau lonjong di sekitar septum. Pada beberapa
strain, blastospora berukuran besar, berbentuk bulat atau seperti botol, dalam jumlah
sedikit. Sel ini dapat berkembang menjadi klamidospora yang berdinding tebal dan bergaris tengah sekitar 8-12 μ.
biakan mempengaruhi besar kecil koloni. Warna koloni putih kekuningan dan berbau asam seperti aroma tape. Dalam medium cair seperti glucose yeast, extract pepton, C.
albicans tumbuh di dasar tabung. Klasifikasi dari Candida albicans adalah sebagai
barikut
Kingdom : Fungi Phylum : Ascomycota Subphylum : Saccharomycotina Class : Saccharomycetes Ordo : Saccharomycetales Family : Saccharomycetaceae Genus : Candida
Spesies : Candida albicans
2.6 Metode Pemisahan
Prinsip pemisahan adalah adanya perbedaan sifat fisik dan kimia dari senyawa yaitu kecendrungan dari molekul untuk melarut dalam cairan (kelarutan), kecenderungan molekul untuk menguap (keatsirian), kecenderungan molekul untuk melekat pada permukaan serbuk labus (adsorpsi, penyerapan).
2.6.1 Ekstraksi
Ekstraksi merupakan suatu teknik pemisahan yang biasa digunakan untuk memperoleh produk organik yang diinginkan. Selektivitas antara pelarut di dalam pelarut lainnya yang berbeda kepolarannya dalam melarutkan senyawa organik dan membentuk dua lapisan yang saling memisah (Khopkar, 1990).
2.6.2 Maserasi
berulang-ulang dan bila ampas dari hasil ekstraksi tidak berwarna, maka dianggap ekstraksi telah selesai. Ekstrak total dari sampel tumbuhan yang telah diekstraksi dapat diperoleh dengan cara pemekatan dengan menggunakan alat rotary evaporator
(Harborne, 1987).
2.7 Senyawa Metabolit Sekunder
Senyawa metabolit sekunder merupakan bahan yang dihasilkan oleh tumbuhan yang dapat digunakan antara lain sebagai bahan untuk melindungi dirinya, hormon penarik serangga dan lain-lain. Beberapa metabolit sekunder sering terjadi di dalam tumbuhan adalah alkaloid, flavonoid, steroid, poliketida dan lain-lain.
2.7.1 Alkaloid
Senyawa-senyawa yang mengandung atom N mempunyai sifat alkaloid dan sering digolongkan ke dalam golongan alkaloid, meskipun kerangka karbonnya menunjukkan bahwa senyawa ini turunan isoprenoid (Robinson, 1995). Umumnya alkaloid memilki kelarutan dan sifat lain yang berbeda-beda pada setiap jenisnya. Semua alkaloid mengandung paling sedikit satu atom N yang bersifat basa (Harborne, 1987).
Hampir semua alkaloid yang ditemukan di alam mempunyai keaktifan fisiologis tertentu, ada yang sangat beracun dan ada pula yang berguna untuk obat-obatan. Alkaloid dapat ditemukan dalam bagian tumbuhan seperti biji, daun, ranting, dan kulit kayu. Kadar alkaloid yang terkandung dalam jaringan tersebut sangat kecil, yaitu antara 1-10 % (Achmad, 1986). Adanya alkaloid diidentifikasi dengan pereaksi Mayer membentuk endapan putih, dengan pereaksi Dragendrof membentuk endapan kemerahan dan dengan pereaksi asam pikrat membentuk endapan kuning dan adanya asam tanat endapan coklat muda (Rusdi, 1988).
2.7.2 Flavonoid
terkonsentrasi dalam jaringan tertentu, misalnya antosianidin yaitu zat warna dari buah, bunga dan daun. Karena itu senyawa ini dianggap sebagai zat warna merah, ungu, biru dan sebagian kuning yang ditemukan dalam tumbuh-tumbuhan. Flavonoid mempunyai kerangka dasar karbon yang terdiri dari 15 atom karbon, mempunyai 2 cincin benzena (C6) yang terikat pada rantai propana (C3) sehingga membentuk suatu
susunan C6-C3-C6 (Achmad, 1986).
2.7.3 Terpenoid
Terpenoid adalah suatu senyawa kimia yang terdiri dari beberapa unit isoprene, mempunyai struktur siklik dengan satu arah atau lebih gugus fungsional berupa gugus hidroksil dan gugus karbonil (Rusdi, 1988). Terpenoid terdiri atas beberapa macam senyawa, mulai dari komponen minyak atsiri, yaitu monoterpen dan seskuiterpen (C10
dan C15) yang mudah menguap, diterpena (C20) yang lebih sukar menguap sampai ke
senyawa yang tidak menguap, yaitu triterpen dan sterol (C30). Pada umumnya
terpenoid larut dalam lemak dan terdapat di dalam sitoplasma sel tumbuhan. Biasanya terpenoid di ekstraksi dengan menggunakan eter minyak bumi, eter atau kloroform (Harborne, 1987).
2.7.4 Saponin
Saponin mula-mula diberi nama demikian karena sifatnya yang menyerupai sabun (bahasa lain sapo berarti sabun). Saponin adalah senyawa aktif yang menimbulkan busa jika dikocok dalam air dan pada konsentrasi yang rendah sering menyebabkan hemolisis sel darah merah. Saponin sangat beracun untuk ikan dalam konsentrasi rendah (Robinson, 1995).
2.8Kromatografi
pendeteksian senyawa metabolit sekunder dan dapat dijadikan sebagai patokan untuk proses pengerjaan berikutnya dalam menentukan struktur senyawa. Berbagai jenis kromatografi yang umum digunakan antara lain Kromatografi Lapis Tipis (KLT), Kromatografi Kolom, Kromatografi Cair dan Kromatografi Gas-Spektroskopi Massa (Darwis, 2000).
a. Kromatografi Lapis Tipis (KLT)
Merupakan salah satu metoda identifikasi awal untuk menentukan kemurnian senyawa yang ditemukan atau dapat menetukan jumlah senyawa dari ekstrak kasar senyawa metabolit sekunder. Cara ini sangat sederhana dan merupakan salah satu pendeteksian awal dari hasil isolasi.
b. Kromatografi Kolom
Digunakan untuk pemisahan campuran beberapa senyawa yang diperoleh dari isolasi tumbuhan. Dengan menggunakan fasa padat dan fasa cair maka fraksi-fraksi senyawa akan menghasilkan kemurnian yang cukup tinggi.
c. Kromatografi Cair
Lebih dikenal dengan HPLC (High Pressure Liquid Chromatography), yang diterjemahkan menjadi Kromatografi Cair Kinerja Tinggi. Hal yang menarik pada HPLC adalah kecepatan, ketelitian dan kemampuannya memisah-misahkan suatu campuran yang kompleks. Campuran yang dapat dipisah-pisahkan, meliputi molekul-molekul, senyawa-senyawa ionik, senyawa-senyawa yang tak stabil (yang jika diuapkan akan mengalami peruraian) dan juga senyawa-senyawa dengan massa rumus besar.
2.9Metode Penentuan Struktur Kimia
Untuk menentukan struktur kimia suatu senyawa dapat digunakan metode spektroskopi UV-Vis, Spektrofotometri Fourier Transform-Infra red (FT-IR),
Nuclear Magnetic Resonansce (NMR) atau Spektrometri Resonansi Magnetik Inti
(RMI) dan Mass Spectra atau Spektrometri Massa 1. Spektrofotometri UV-VIS
Pengukuran serapan dapat dilakukan pada daerah ultraviolet (panjang gelombang 190-380 nm) atau daerah cahaya tampak (panjang gelombang 380-780 nm). Semua molekul dapat mengabsorbsi radiasi dalam daerah UV-Vis karena mengandung elektron yang dapat dieksitasi ke tingkat energi yang lebih tinggi. Senyawa yang mengandung ikatan sigma (seperti pada ikatan tunggal C-C akan tereksitasi pada panjang gelombang sangat pendek dibawah 150 nm berada di luar daerah ukur spektrofotometer sehingga tidak akan menimbulkan serapan. Senyawa memiliki elektron phi (π) (mempunyai ikatan rangkap) dan mempunyai pasangan elektron bebas lebih mudah tereksitasi dan menyerap pada panjang gelombang yang lebih tinggi sehingga menimbulkan serapan pada spektrofotometer. Spektrofotometri digunakan untuk menganalisis struktur dan memberikan petunjuk adanya gugus kromofor, menetapkan kadar, menggunakan serapan maksimum dari kurva absorbsi, memeriksa kemurnian, memeriksa langsung konsentrasi analit, (Pare & Belanger, 1997)
2. Spektrofotometri Infrared (IR)
Daerah radiasi spektrofotometri IR berada pada bilangan panjang gelombang 12800-10 cm-1. Umumnya daerah radiasi IR terbagi dalam IR dekat (12800-4000 cm-1; 3,8-12 x 1014 Hz; 0,78-2,5 mikrometer), daerah IR tengah (4000-200cm-1; 3,8-12 x104 Hz, 2,5-50 mikrometer), daerah IR jauh (200-10 cm-1; 60-3 x 1011 Hz; 50-1000 mikrometer). Daerah yang paling banyak digunakan untuk berbagai keperluan praktis adalah 4000-690 cm-1 yang biasa disebut infra tengah (Khopkar, 1990)
a. Spektrofotometer IR dispersive, adalah spektrofotometri yang menggunakan monokromator untuk memisahkan frekuensi individu yang melewati sampel sehingga absorbsi dari masing-masing frekuensi dapat diukur.
b. Spektrofotometer Fourier-transform, adalah spektrofotometri yang dalam instrumennya tidak dipisahkan radiasinya, tetapi hampir semua panjang gelombang mencapai detektor secara bersamaan yang disebut Fourier-transform, yang digunakan untuk mengubah hasil spektrum IR menjadi khas. Yang digunakan sebagai pengganti monokromator adalah interferometer yang dapat memisahkan radiasi menjadi dua bagian dan menghubungkannya kembali sehingga variasi intensitas yang keluar dapat diukur sekali. Beberapa keuntungan spektrofotometer Fourier-transform dibandingkan dengan spektrofotometer dispersive adalah menghasilkan spektrum yang lebih cepat, resolusi yang lebih baik, dapat mengukur sampel dalam jumlah yang sangat sedikit (Silverstein, 2005) 3. Spektrometri Massa
Spektometri yang menggunakan penguraian senyawa organik dan perekaman pola fragmentasi menurut massanya. Uap cuplikan berdifusi ke dalam sistem spektrometer massa yang bertekanan rendah, kemudian diionkan dengan energi yang cukup untuk memutuskan ikatan kimia.
4. Spektrometri Nuclear Magnetic Resonansce (NMR) 1 Dimensi
Spektrometri Nuclear Magnetic Resonansce atau resonansi magnetik inti (RMI) merupakan metode yang sering dipakai dalam mempelajari struktur molekul. Untuk melengkapi bagian-bagian lain dari suatu molekul organik yang tidak diketahui (unknown) dapat digunakan RMI yang memberikan informasi yang berguna dalam penentuan struktur yaitu RMI 1 dimensi terdiri dari RMI proton (1H), RMI karbon (13C), DEPT (Distortionless Enhancement by Polarization Transfer). Prinsip RMI proton adalah inti atom hidrogen mempunyai sifat-sifat magnet, bila suatu senyawa mengandung hidrogen diletakkan dalam bidang magnet yang sangat kuat dan diradiasi menggunakan radiasi elektromagnetik maka inti atom hidrogen dari senyawa tersebut akan menyerap energi melalui suatu proses absorpsi yang dikenal dengan resonansi magnet.
Penyerapan gelombang pada fenomena RMI ataau NMR (Nuclear Magnetic
Resonance), terjadi bila inti menyerah terhadap medan magnet yang digunakan untuk
merubah arah orientasi spin. Spektrum RMI karbon dan DEPT memberikan informasi jenis atom karbon primer (CH3), sekunder (CH2) tersier (CH), dan kuarterner (C).
DEPT merupakan salah satu tipe spektra RMI karbon yang memberikan informasi jumlah karbon dari CH3, CH2, CH dan C yang diukur berdasarkan sudut pengukuran
RMI karbon. Hasil penelitian DEPT pada sudut 1350 menunjukkan bahwa sinyal karbon CH3 dan CH mengarah ke atas, sedangkan CH2 mengarah ke bawah, Untuk
mengetahui perbedaan CH3 dan CH dilakukan pengukuran pada sudut 900
(Silverstein, 2005).
5. Spektrometri Nuclear MagenticResonansce (NMR) 2 Dimensi
NMR dua dimensi merupakan spektrometri yang paling penting untuk memecahkan masalah struktur. NMR dua dimensi meliputi COSY (Correlation Spectroscopy), NOESY (Nuclear Overhauser Enhancement Spectroscopy) HSC (Heteronuclear Shift
Correlation) dan TOCSY (Total Correlation Spectroscopy).
simetris yang memiliki 1H-NMR yang mempunyai dua sumbu pergeseran kimia (F1 dan F2) (Gambar 2.14).
Gambar 2.14. Spektrum COSY
Spektrum COSY memiliki seperangkat diagonal puncak (lingkaran terbuka) serta puncak diagonal (lingkaran penuh). Puncak off-diagonal adalah sinyal penting karena ini terjadi pada posisi dimana ada kopling antara proton pada sumbu F1 dan satu pada sumbu F2. Dalam Gambar 2.14, sinyal off-diagonal menunjukkan bahwa
ada spin-kopling antara HC dan HD dan juga antara HB dan Hc tetapi proton berlabel
HA tidak memiliki mitra kopling (Field et al, 2008)
Gambar 2.15. Spektrum NOESY
Spektrum NOESY memiliki seperangkat puncak diagonal (lingkaran terbuka) serta puncak off diagonal (lingkaran penuh). Puncak off-diagonal terjadi pada posisi dimana sebuah proton pada sumbu F1 adalah dekat dalam ruang untuk satu lagi pada sumbu F2. Dalam Gambar 2.15 menunjukkan bahwa HA harus berada dekat dengan
HD dan HB harus berada dekat dengan HC. Dari analisis spektrum NOESY dapat
menentukan struktur tiga dimensi dari molekul atau bagian dari molekul. Spektrum NOESY sangat berguna untuk membangun stereokimia (misalnya konfigurasi cis / trans dari ikatan ganda atau persimpangan cincin) dari molekul di mana lebih dari satu stereoisomer yang mungkin ada.
Spektrum HSC tidak memiliki puncak diagonal. Puncak spektrum HSC terjadi pada posisi di mana proton dalam spektrum pada sumbu F2 digabungkan dengan karbon dalam spektrum pada sumbu F1. Dalam Gambar 2.16 menunjukkan HA dan
HB kopling dengan Cz, HC kopling dengan CY dan HD kopling dengan CX. Dalam
spektrum HSC, korelasi antara proton dalam spektrum 1H-NMR dan inti karbon dalam spektrum 13C dapat diperoleh.
Gambar 2.16. Spektrum HSC
Spektrum TOCSY berguna dalam mengidentifikasi semua proton yang memiliki sistem spin terisolasi. Seperti spektrum COSY dan NOESY, TOCSY juga mempunyai puncak diagonal pada frekuensi dari semua resonansi dalam spektrum. Eksperimen bergantung pada kopling spin-spin tapi bukan menunjukkan pasangan inti yang secara langsung digabungkan bersama-sama, TOCSY menunjukkan puncak lintas (off-diagonal peaks) untuk setiap inti yang merupakan bagian dari sistem spin bukan secara langsung digabungkan. Spektrum TOCSY simetris dengan diagonal dan memiliki 1H-NMR sebagai kedua sumbu pergeseran kimia (F1 dan F2) (Gambar 2.17).
dimana sebuah proton pada sumbu F1 mempunyai sistem spin yang sama sebagaimana dalam sumbu F2. Dari Gambar 2.17 dapat dilihat ada dua (HA1, HA2,
HA3) dan (HX1, HX2, HX3) yang terisolasi 3-sistem spin ditumpangkan dan cross peaks
jelas menunjukkan adanya resonansi yang dimiliki masing-masing sistem.
Gambar 2.17. Spektrum TOCSY
Spektrometri 2 D Heteronuclear Multiple Quantum Coherence (HMQC) berguna untuk melihat korelasi antara proton dengan karbon pada posisi geminal (1 ikatan) diastereotopik dalam struktur kimia (yang kadang-kadang sulit untuk membedakan secara tegas, bahkan pada COSY) karena hanya ini yang akan menghasilkan dua korelasi dengan karbon yang sama.