BAB II
TINJAUAN PUSTAKA
A. Deskripsi Teori 1. Aseton
Aseton merupakan keton yang paling sederhana, digunakan
sebagai pelarut polar dalam kebanyakan reaksi organik. Aseton dikenal juga
sebagai dimetil keton, 2-propanon, atau propan-2-on. Aseton adalah senyawa
berbentuk cairan yang tidak berwarna dan mudah terbakar, digunakan untuk
membuat plastik, serat, obat-obatan, dan senyawa-senyawa kimia lainnya. Selain
dimanufaktur secara industri, aseton juga dapat ditemukan secara alami, termasuk
pada tubuh manusia dalam kandungan kecil.
Aseton memiliki gugus karbonil yang mempunyai ikatan rangkap dua
karbon-oksigen terdiri atas satu ikatan σ dan satu ikatan π. Umumnya atom hidrogen yang terikat pada atom karbon sangat stabil dan sangat sukar diputuskan.
Namun lain halnya dengan atom hidrogen yang berada pada karbon (C) di
samping gugus karbonil yang disebut atom hidrogen alfa. Sebagai akibat
penarikan elektron oleh gugus karbonil, kerapatan elektron pada atom karbon alfa
semakin berkurang, maka ikatan karbon dan hidrogen alfa semakin melemah,
sehingga hidrogen alfa menjadi bersifat asam dan dapat mengakibatkan terjadinya
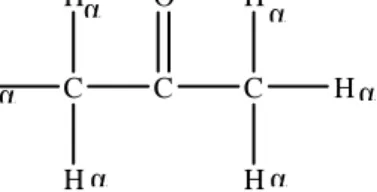
substitusi alfa (α). Substitusi α melibatkan penggantian atom H pada atom karbon α dengan elektrofil (Wade, L.G. 2006:1041-1063). Atom hidrogen alfa pada aseton dapat dilihat pada Gambar 1.
α α α α α α
Gambar 1. Atom hidrogen alfa pada aseton.
Aseton mempunyai atom hidrogen alfa bersifat asam, oleh karena itu dapat
terionisasi menghasilkan ion enolat. Ion enolat dapat berada dalam dua bentuk
yaitu bentuk keto dan bentuk enol yang disebut bentuk tautomerisasi. Tautomer
adalah isomer-isomer pada senyawa karbonil yang hanya dibedakan oleh
kedudukan ikatan rangkap dan yang disebabkan perpindahan letak atom hidrogen
alfa ke atom oksigen. Bentuk keto dan bentuk enol pada aseton dapat dilihat pada
Gambar 2.
H3C C CH2
O H
H3C C CH2
O H
Bentuk keto Bentuk enol
Gambar 2. Bentuk keto dan bentuk enol pada aseton.
Hidrogen alfa pada senyawa aseton dapat disubtitusi oleh karbokation
sehingga terjadi reaksi alkilasi. Reaksi alkilasi pada aseton terdapat pada Gambar
3. C H H C H C O H H H
AlCl3 H3C C CH2 O H + RX H3C C CH2 O R + HX
Gambar 3. Alkilasi pada aseton.
2. Senyawa 3-Hidroksibenzaldehida
Senyawa 3-Hidroksibenzaldehida dengan struktur seperti ditunjukkan
pada Gambar 4 merupakan senyawa turunan benzaldehida yang tersubstitusi
gugus hidroksi pada posisi meta pada cincin aromatik.
H O HO
Gambar 4. 3-hidroksibenzaldehida
Senyawa ini berbentuk kristal berwarna putih, memiliki titik leleh 100-103°C dan
titik didih 191°C dan larut dalam etanol pada suhu kamar.
Salah satu reaksi yang dapat dialami gugus karbonil pada benzaldehida
adalah reaksi kondensasi aldol silang dengan aseton menjadi benzalaseton seperti
H3C C O CH3+ C H O C CH3 O + H2O -OH
Gambar 5. Reaksi kondensasi aldol silang antara benzaldehida dengan aseton
3. Senyawa 4-(3-hidroksifenil)-3-buten-2-on
Senyawa 4-(3-hidroksifenil)-3-buten-2-on (Gambar 6) merupakan
senyawa turunan benzalaseton yang tersubstitusi gugus hidroksi pada cincin
aromatik. Senyawa turunan benzalaseton ini memiliki rumus molekul yang analog
dengan senyawa turunan asam sinamat (Gambar 7).
OH C CH3 O 2 1 3 4 1' 2' 3' 4' 5' 6'
Gambar 6. Struktur 4-(3-hidroksifenil)-3-buten-2-on
OH
C OR
O
Struktur 4-(3-hidroksifenil)-3-buten-2-on memiliki kemiripan dengan
turunan asam sinamat karena sama-sama memiliki senyawa karbonil tak jenuh α,β yang terkonjugasi dengan cincin benzena. Maka diharapkan senyawa tersebut juga
memiliki aktivitas sebagai tabir surya.
4. Senyawa Tabir Surya
Tabir surya adalah suatu senyawa yang digunakan untuk menyerap secara
efektif sinar matahari terutama daerah emisi gelombang UV sehingga dapat
mencegah gangguan pada kulit akibat pancaran secara langsung sinar UV tersebut
(Titik Taufikurohmah, 2008). Besarnya kemampuan suatu senyawa untuk
melindungi kulit dari sinar matahari dapat dilihat dari nilai SPF (Sun Protection
Factor) yaitu nilai pelindung terhadap UV yang dapat melindungi kulit terbakar
dari sinar matahari. SPF mengindikasikan berapa lama kita dapat berada di bawah
paparan sinar matahari langsung tanpa menyebabkan kulit terbakar. Perhitungan
SPF menurut Walter adalah SPF=10A
Senyawa tabir surya yang baik digunakan untuk melindungi kulit dari sinar
ultraviolet adalah senyawa yang memiliki kemampuan proteksi maksimal (ultra)
tetapi memiliki konsentrasi kecil sehingga tidak menimbulkan iritasi pada kulit.
Jenis proteksi ultra adalah senyawa yang memiliki nilai SPF di atas 15.
, dengan A adalah absorbansi tiap larutan
yang diukur menggunakan alat spektroskopi UV (Ike Yuliastuti dan Jumina,
2002).
Sinar ultraviolet dibagi menjadi tiga macam sesuai efek yang
= 100- 290 nm) mempunyai energi tertinggi dan berbahaya, namun tidak sampai
ke permukaan bumi karena terserap oleh lapisan termosfer. Sinar UV-B (λ = 290-320 nm) dengan energi yang relatif tinggi termasuk berbahaya sebab akan sampai
ke permukaan bumi walau hanya sebagian kecil saja. Meskipun UV-B hanya akan
terserap kulit sampai lapisan epidermis saja namun akan menyebabkan kulit
terbakar, efek penuaan dini dan kanker kulit. Sinar UV-A (λ = 320-400 nm) memiliki energi paling rendah, relatif tidak berbahaya namun mampu menembus
lapisan dermis kulit dan dalam waktu yang lama mengakibatkan efek merusak
pula seperti UV-B (Agus Dwiono, Jumina dan Iqmal Tahir, 2003 : 34)
Senyawa tabir surya yang banyak digunakan dalam industri kosmetika
adalah senyawa turunan alkil sinamat. Senyawa turunan alkil sinamat yang
populer adalah p-metoksi oktil sinamat. Berdasarkan struktur kimianya, ada dua
bagian pada senyawa tersebut yang dimungkinkan berperan penting yaitu bagian
rantai alkil dan bagian rantai benzil seperti pada Gambar 8.
.
OCH3
O
O R
Gambar 8. Struktur alkil parametoksisinamat
Berdasarkan struktur kimia senyawa tersebut maka terdapat bagian
benzena aromatik dan sisi alkil yang bersifat non polar. Efek perlindungan sinar
sisi alkil digunakan untuk kontribusi sifat non polar senyawa yang berakibat
senyawa tak larut dalam air (Ike Yuliastuti dan Jumina, 2002).
Kemampuan suatu senyawa tabir surya dalam melindungi kulit dari
paparan sinar UV identik dengan panjang gelombang serapan maksimum yaitu
panjang gelombang dengan intensitas absorpsi tertinggi atau maksimum. Hal
tersebut tergantung pada struktur elektronik dari setiap senyawa (Sastrohamidjojo,
1991).
5. Kondensasi Aldol silang
Reaksi kondensasi adalah suatu reaksi dimana dua molekul kecil
bergabung membentuk satu molekul besar dengan atau tanpa hilangnya suatu
molekul kecil (misalnya air). Kondensasi aldol adalah reaksi antar aldehida atau
antar keton yang sama menggunakan basa sebagai katalis. Syarat terjadinya reaksi
adalah tersedianya Hα pada karbonil yang terlibat dalam reaksi tersebut. Reaksi kondensasi aldol dalam beberapa kasus biasanya diikuti reaksi dehidrasi. Jika
aldehida tidak memiliki Hα, maka dimerisasi dengan kondensasi aldol tidak dapat terjadi, kondensasi dapat terjadi jika pada aldehida tersebut ditambahkan aldehida
atau keton yang mempunyai Hα. Kondensasi aldol melibatkan adisi nukleofilik sebuah enolat keton ke sebuah aldehida, membentuk hidroksi keton atau β-hidroksi aldehida dan diikuti dengan dehidrasi, menghasilkan sebuah enon
terkonjugasi (Wade, L.G. 2006:1041-1063).
Bila suatu aldehida yang memiliki atom Hα diolah dengan basa seperti NaOH dalam air, maka akan terbentuk ion enolat, yang kemudian dapat bereaksi
pada gugus karbonil dari molekul aldehida yang lain. Hasilnya ialah adisi satu
molekul aldehida ke molekul aldehida yang lain seperti pada Gambar 9.
2 CH3CH O 2 CH3CH OH CH2CH O Asetaldehida (suatu aldehida) 3-hidroksibutanal (suatu aldol) OH
-Gambar 9. Adisi satu molekul aldehida ke molekul aldehida yang lain.
Kondensasi aldol dengan menggunakan katalis basa akan membentuk ion enolat
(Gambar 10), yang kemudian akan terjadi serangan nukleofil oleh enolat pada
gugus karbonil lain yang terstabilisasi oleh resonansi (Gambar 11). Produk reaksi
ini adalah garam alkoksida, aldol akan terbentuk dan mengalami dehidrasi
menghasilkan senyawa karbonil tak jenuh (Gambar 12).
Reaksi dengan katalis basa :
C CH2 O H H + OH C CH2 O H C CH2 O H ion enolat + H2O
Gambar 10. Pembentukan ion enolat.
+ H C CH3 O H C CH3 O C H H HC O H O H H C CH3 O C H H HC O H + OH produk aldol C CH2 O H
H3O +
Gambar 12. Dehidrasi aldol.
Senyawa aldol (β-hidroksialdehida dan β-hidroksiketon) hasil dari reaksi adisi lebih mudah terdehidrasi karena ikatan rangkap dalam produk dehidrasi
berkonjugasi dengan gugus karbonil. Konjugasi meningkatkan kestabilan produk
dan oleh sebab itu senyawa karbonil tak jenuh α,β-aldehida atau keton mudah diperoleh sebagai produk kondensasi aldol (Bruice, P.Y., 2007 : 873).
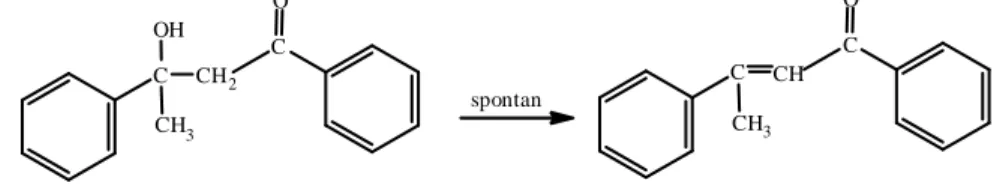
Bila dehidrasi menghasilkan suatu ikatan rangkap yang berkonjugasi
dengan cincin aromatik maka dehidrasi berlangsung spontan. Misalnya β-hidroksiketon yang dibentuk melalui adisi aldol dari asetofenon, karena ikatan
rangkap yang baru tidak hanya berkonjugasi dengan gugus karbonil tetapi juga
berkonjugasi dengan cincin aromatik, maka dehidrasi berlangsung spontan seperti
pada Gambar 13. Konjugasi dapat menstabilkan produk dehidrasi, maka relatif
lebih mudah diperoleh (Bruice, P.Y., 2007 : 873).
H2O H C CH3 O C H H HC O H produk aldol H C CH3 C H HC O
Reaksi : CH2 C CH3 OH C O CH C CH3 C O + H2O spontan
Gambar 13. Dehidrasi yang menghasilkan suatu ikatan rangkap terkonjugasi dengan cincin aromatik.
Suatu aldehida tanpa hidrogen α tidak dapat membentuk ion enolat dan dengan demikian tidak dapat berdimerisasi dalam suatu kondensasi aldol. Namun
jika aldehida semacam ini dicampur dengan senyawa lain yang memiliki hidrogen α maka kondensasi antara keduanya dapat terjadi. Reaksi inilah yang disebut aldol silang (cross aldol condensation). Suatu kondensasi aldol silang sangat berguna bila hanya satu senyawa karbonil yang memiliki hidrogen α, kalau tidak akan diperoleh produk campuran (R.J Fessenden & J.S. Fessenden, 1999 : 181).
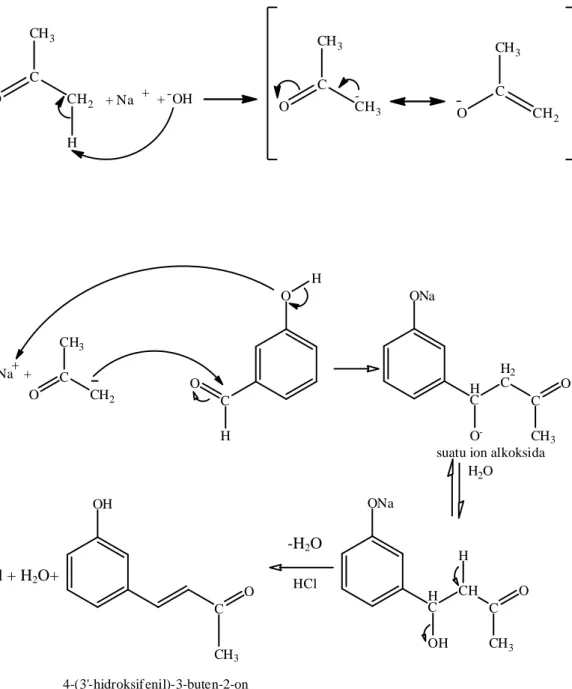
Mekanisme reaksi pembentukan senyawa
4-(3-hidroksifenil)-3-buten-2-on dari reaksi antara aset4-(3-hidroksifenil)-3-buten-2-on dengan 3-hidroksibenzaldehida ditunjukkan seperti
-H2O NaCl + H2O+ C CH3 O CH2 H + Na + + OH -C CH3 O CH- 3 C CH3 O CH2 -H2O H C ONa CH OH C O CH3 OH C O CH3 4-(3'-hidroksif enil)-3-buten-2-on HCl H CH3 C O CH2 O C O H H C ONa H2 C O -C O CH3
suatu ion alkoksida H
Na+
+ H+ +
Gambar 14. Mekanisme reaksi pembentukan 4-(3-hidroksifenil)-3-buten-2-on dengan katalis basa.
6. Teknik Rekristalisasi
Senyawa-senyawa organik yang berbentuk padat dari hasil isolasi maupun
dari hasil sintesis reaksi-reaksi organik umumnya jarang diperoleh dalam keadaan
murni. Senyawa tersebut biasanya terkontaminasi dengan sejumlah kecil dari
senyawa-senyawa lain yang dihasilkan selama reaksi berlangsung. Pemurnian
senyawa-senyawa yang berbentuk kristal yang tidak murni, lazimnya dilakukan
dengan jalan rekristalisasi dengan berbagai pelarut atau campuran pelarut.
Pemurnian zat-zat padat dengan jalan rekristalisasi didasarkan pada
kelarutannya di dalam pelarut tertentu atau campuran pelarut. Pada prinsipnya
pekerjaan rekristalisasi terdiri atas :
a. Melarutkan senyawa yang tidak murni (hasil sintesis atau isolasi) dalam
pelarut yang baik (sesuai) atau titik didihnya berdekatan.
b. Menyaring larutan yang masih dalam keadaan panas dari partikel-partikel
yang tidak larut.
c. Mendinginkan larutan panas sehingga zat terlarut menjadi kristal.
d. Memisahkan kristal dari larutan yang menyertainya.
Karakteristik dari pelarut yang umumnya digunakan untuk rekristalisasi
adalah :
a. Mempunyai daya melarutkan yang tinggi untuk senyawa yang akan
dimurnikan pada suhu yang relatif tinggi dan mempunyai daya melarutkan
yang rendah pada suhu kamar atau pada suhu yang lebih rendah.
b. Mampu melarutkan sedikit kotoran-kotoran (impurities).
d. Mudah dipisahkan dari kristal-kristal senyawa yang dimurnikan, atau
memiliki titik didih yang relatif rendah
e. Pelarut tidak bereaksi secara kimia dengan senyawa yang dimurnikan.
7. Kromatografi Lapis Tipis
Teknik kromatografi lapis tipis dikembangkan oleh Ismailoff dan
Schraibar pada tahun 1938. Adsorben dilapiskan pada lempeng kaca yang
bertindak sebagai penunjang fasa diam. Fasa bergerak akan menyerap sepanjang
fasa diam dan terbentuklah kromatogram. Ini dikenal juga sebagai kromatografi
kolom terbuka. Biasanya yang sering digunakan sebagai materi pelapisnya adalah
silika gel, bubuk selulosa, tanah diatome, dan kieselguhr (Hardjono
Sastrohamidjojo, 1991: 26-28). Pemilihan sistem pelarut dan komposisi lapisan
tipis ditentukan oleh prinsip kromatografi yang akan digunakan. Sampel
diteteskan pada salah satu bagian tepi plat kromatografi (0,01 – 10 µg zat).
Kromatografi lapis tipis digunakan untuk memisahkan
komponen-komponen atas dasar perbedaan adsorpsi atau partisi oleh fase diam dipisah
gerakan pelarut pengembang. Teknik Kromatografi Lapis Tipis (KLT)
dikembangkan oleh Egon Stahl dengan menghamparkan penyerap pada lempeng
gelas, sehingga merupakan lapisan tipis. KLT merupakan kromatografi serapan,
tetapi dapat juga merupakan kromatografi partisi karena bahan penyerap telah
dilapisi air dari udara. Sistem ini sangat popular karena banyak memberikan
yang singkat serta daya pisah cukup baik. Selain itu sampel yang dibutuhkan
sangat sedikit (Sudjadi, 1986 : 167).
Larutan cuplikan ditotolkan dengan pipet mikro atau injektor pada jarak
1-2 cm dari batas plat. Setelah pelarut dari noda menguap, plat siap untuk
dikembangkan dengan fasa gerak yang sesuai hingga jarak eluen/fasa gerak dari
batas plat mencapai 7-10 cm. Proses pengembangan dikerjakan dalam wadah
tertutup (chamber) yang diisi eluen yang sesuai dengan sampel. Chamber tersebut
dijenuhi dengan uap eluen agar dihasilkan pemisahan yang baik dan dapat ulang
(reproducible). Teknik pengembangan dapat dari bawah ke atas (ascending), dari
atas ke bawah (descending) atau mendatar. Jangan sampai terlalu lama
mencelupkan plat dalam bejana bila permukaan pelarut telah mencapai garis
akhir, karena oleh pengaruh difusi dan penguapan dapat menyebabkan
pemancaran dari noda-noda yang terpisah. Langkah berikutnya adalah
mengeringkan sisa eluen dalam lapisan tipis dengan didiamkan pada suhu kamar
beberapa saat. Noda pada lapisan tipis dapat diamati langsung untuk noda tampak.
Jika noda tidak tampak dapat dilihat dengan lampu UV pada panjang gelombang
pendek (254 nm) atau pada panjang gelombang (366 nm). Dapat juga dilihat
dengan menggunakan pereaksi semprot penimbul warna.
Pemilihan eluen yang tepat merupakan langkah yang sangat penting untuk
keberhasilan analisis dengan KLT. Pertimbangannya dapat menggunakan prinsip
“ like disolve like “.
Pemilihan eluen (fasa gerak) sebaiknya menggunakan campuran pelarut
serapan dari setiap komponen dari campuran pelarut. Jika komponen-komponen
yang mempunyai sifat polar yang tinggi (terutama air) dalam campuran akan
merubah sistem menjadi sistem partisi. Campuran yang baik memberikan
fasa-fasa bergerak yang mempunyai kekuatan bergerak sedang, tetapi sebaiknya
dicegah sejauh mungkin mencampur lebih dari dua komponen terutama karena
campuran yang lebih kompleks cepat mengalami perubahan-perubahan fasa-fasa
terhadap perubahan-perubahan suhu (Hardjono Sastrohamidjojo, 1991 : 28-36).
Setelah noda dikembangkan dan divisualisasikan, identitas noda
dinyatakan dengan harga Rf (Retordation Factor) yang didefinisikan sebagai rasio
jarak noda terhadap titik awal dibagi jarak eluen terhadap titik awal. Secara
matematis dapat ditulis:
Rf
h l
=
dengan l = jarak noda dari titik awal ke titik akhir setelah proses pengembangan
dan h = jarak eluen dari titik awal ke batas akhir eluen. Harga Rf berkisar antara
0-0,999. Faktor-faktor yang mempengaruhi gerakan noda dalam kromatografi
lapis tipis sehingga mempengaruhi harga Rf antara lain struktur kimia senyawa
yang dipisahkan, sifat penyerap, tebal dan kerapatan lapisan penyerap, pelarut
(fasa gerak), derajat kejenuhan, teknik pemisahan, jumlah cuplikan, dan suhu
(Hardjono Sastrohamidjojo, 1991 : 35-36).
Alat yang digunakan untuk mengetahui harga Rf secara langsung adalah
KLT Scanner. Alat ini akan memberikan data Rf dan luas area yang memberi data
Faktor-faktor yang mempengaruhi gerakan noda dalam KLT yang juga
mempengaruhi harga Rf (Hardjono Sastromidjoyo, 1991 : 35-36) adalah :
a. Struktur senyawa yang sedang dipisahkan.
b. Sifat adsorben dan derajat aktivitasnya. Perbedaan adsorben memberikan
perbedaan yang besar terhadap harga Rf.
c. Tebal dan kerataan lapisan adsorben.
d. Pelarut fasa gerak (dan tingkat kemurnianya).
e. Derajat kejenuhan dan uap dalam bejana pengembangan yang digunakan.
f. Teknik percobaan.
g. Jumlah cuplikan yang digunakan. Penetesan jumlah cuplikan yang
berlebihan memberikan tendensi penyebaran noda-noda dengan
kemungkinan terbentuknya ekor.
h. Suhu, untuk mencegah perubahan-perubahan dalam komposisi pelarut
yang disebabkan oleh penguapan-penguapan atau perubahan-perubahan
fasa.
8. Spektroskopi UV
Dasar spektroskopi UV adalah serapan cahaya. Serapan cahaya oleh
molekul dalam daerah spektrum UV tergantung pada struktur elektronik dari
molekul. Spektrum UV dari senyawa-senyawa organik berkaitan erat dengan
transisi-transisi diantara tingkatan tenaga elektronik, oleh sebab itu serapan radiasi
1991 : 11). Spektroskopi UV dapat digunakan untuk menentukan gugus kromofor
yang terdapat dalam suatu senyawa yang menyerap radiasi dalam daerah UV.
Serapan cahaya (energi) dalam daerah UV dari spektrum elektronik
mengakibatkan transisi elektronik, promosi elektron-elektron dari orbital keadaan
dasar berenergi rendah, ke orbital keadaan tereksitasi berenergi tinggi. Spektrum
UV terdiri dari pita serapan lebar pada daerah panjang gelombang yang lebar.
Panjang gelombang serapan biasanya dilaporkan sebagai λmaks
A = log
, yakni panjang
gelombang yang memberikan nilai serapan terbesar (Hardjono
Sastrohamidjojo,1991: 11). Serapan energi direkam sebagai absorbansi.
Absorbansi pada panjang gelombang tertentu didefinisikan sebagai :
I IO
Keterangan: A = absorbansi
Io = intensitas radiasi yang datang
I = intensitas radiasi yang diteruskan
Absorbansi suatu senyawa dengan panjang gelombang tertentu bertambah
dengan makin banyaknya molekul yang mengalami transisi. Panjang gelombang
tergantung pada kuat lemahnya elektron itu terikat pada molekul. Keuntungan
penggunaan spektroskopi UV yaitu gugus-gugus karakteristik dapat dikenal dalam
molekul-molekul yang sangat kompleks (Hardjono Sastrohamidjojo, 1991 : 12).
Panjang gelombang cahaya UV bergantung pada mudahnya promosi
(eksitasi) elektron. Molekul-molekul yang memerlukan lebih banyak energi untuk
promosi elektron (eksitasi) akan menyerap pada panjang gelombang lebih pendek.
Harga dasar enon asiklik : 215 nm
3 tambahan ikatan rangkap 3 x 30 : 90 nm
Komponen homodiena : 39 nm + λ maks terhitung : 344 nm OH C CH3 O
gelombang lebih panjang (R.J., Fessenden & J.S., Fessenden, 1999 : 437).
Umumnya penggunaan spektroskopi serapan pada senyawa-senyawa organik didasarkan pada transisi elektron n dan π ke excited state ke π*
Berdasarkan perumusan rumus empiris oleh Woodward-Fieser, λ karena
energi-energi yang diperlukan untuk proses-proses ini cukup rendah, yaitu pada daerah
spektrum (200-700 nm) (Sumar Hendayana, Asep K, AA Sumarna, Asep S,
1994:160).
maks secara teoritis dari senyawa 4-(3-hidroksifenil)-3-buten-2-on adalah:
Struktur 4-(3-hidroksifenil)-3-buten-2-on
Nilai panjang gelombang maksimum (λ maks) sebesar 344 nm menunjukkan potensi senyawa tabir surya UV-A.
9. Spektrofotometer FTIR
Spektrum IR digunakan untuk menentukan berbagai macam gugus fungsi
yang terkandung dalam suatu senyawa. Kegunaan dari spektroskopi inframerah
adalah untuk mengenal (elusidasi) struktur molekul, khususnya gugus fungsional
beserta lingkungannya. Hampir setiap senyawa yang memiliki ikatan kovalen baik
elektromagnetik dalam daerah spektrum IR. Sinar IR berada pada kisaran
gelombang elektromagnetik dengan panjang gelombang 0,5-1000 µm. Daerah
yang paling berguna untuk mengenal struktur suatu senyawa adalah pada daerah
1-25 µm atau 10.000 – 40.000 cm-1. Satuan yang lebih umum dipakai adalah
satuan frekuensi (cm
-Frekuensi inframerah biasanya dinyatakan dalam satuan bilangan
gelombang (wavenumber), yang didefinisikan sebagai banyaknya gelombang per
sentimeter. Instrumen biasa memindai (scan) pada kisaran sekitar 700 sampai
5000 cm
1), dan bukan satuan panjang gelombang. Serapan setiap tipe
ikatan (N-H, C-H, O-H, C-X, C=O, C-O, C-C, C=C, dan sebagainya) hanya
diperoleh dalam bagian-bagian kecil tertentu dari daerah vibrasi infra merah.
Kisaran serapan yang kecil dapat digunakan untuk menentukan setiap tipe ikatan.
-1
Spektrometer FTIR memiliki keuntungan yaitu dapat digunakan pada
semua frekuensi dari sumber cahaya secara simultan sehingga analisis dapat
dilakukan lebih cepat daripada menggunakan cara pemindaian, sensitifitas FTIR
lebih besar daripada cara dispersi disebabkan radiasi yang masuk ke sistem
detektor lebih banyak karena tanpa harus melalui celah (Palleros D. R, 2003 :
699-700).
. Kisaran frekuensi ini sama dengan energi sekitar 2 sampai 12
kkal/mol. Jumlah energi ini cukup untuk mempengaruhi getaran (vibrasi) ikatan
(gerakan seperti peregangan atau pembengkokan ikatan) tetapi sangat kurang
untuk memutus ikatan.
Spektra inframerah suatu senyawa dapat dengan mudah diperoleh dalam
sumber radiasi inframerah. Spektrometer secara otomatis membaca sejumlah
radiasi yang menembus sampel dengan kisaran frekuensi tertentu dan merekam
pada kertas berapa persen radiasi yang ditransmisikan. Radiasi yang diserap oleh
molekul muncul sebagai pita spektra.
Seberapa banyak frekuensi tertentu yang melewati senyawa tersebut
diukur sebagai persentase transmitansi (percentage transmittance). Persentase
transmitansi dengan nilai 100 berarti bahwa semua frekuensi dapat melewati
senyawa tersebut tanpa diserap sama sekali. Pada kenyataannya, itu tidak pernah
terjadi, selalu akan ada penyerapan, walaupun kecil, mungkin transmitansi sebesar
95% adalah yang terbaik yang bisa diperoleh.
Identifikasi pita absorpsi khas yang disebabkan oleh berbagai gugus fungsi
merupakan dasar penafsiran spektra inframerah. Delapan daerah terpenting dan
telah ditentukan dengan baik yang digunakan pada pemeriksaan pendahuluan
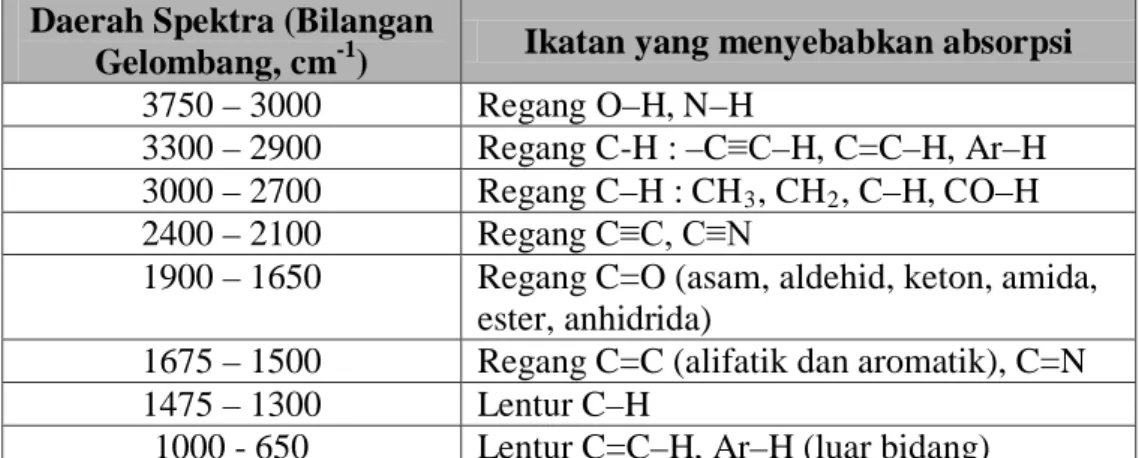
spektra tertera dalam Tabel 1 (Hardjono Sastrohamidjojo, 1991 : 82-85).
Tabel 1. Harga Dasar Serapan Ikatan Gugus Fungsi Daerah Spektra (Bilangan
Gelombang, cm-1) Ikatan yang menyebabkan absorpsi
3750 – 3000 Regang O–H, N–H
3300 – 2900 Regang C-H : –C≡C–H, C=C–H, Ar–H 3000 – 2700 Regang C–H : CH3, CH2, C–H, CO–H 2400 – 2100 Regang C≡C, C≡N
1900 – 1650 Regang C=O (asam, aldehid, keton, amida, ester, anhidrida)
1675 – 1500 Regang C=C (alifatik dan aromatik), C=N 1475 – 1300 Lentur C–H
Berdasarkan struktur dari senyawa 4-(3-hidroksifenil)-3-buten-2-on, maka
dapat diperkirakan kemungkinan gugus fungsi yang akan muncul dalam
spektroskopi infra merah diantaranya:
a. Adanya gugus karbonil C=O pada serapan 1900 – 1650 cm-1
b. Adanya gugus hidroksi memiliki serapan yang melebar pada daerah
3750-3000 cm
. Puncak ini
biasanya terkuat dengan lebar medium dalam spektrum dan serapan
tersebut sangat karakteristik.
-1
c. Adanya cincin aromatik memiliki serapan medium tinggi kuat pada
daerah 1675 – 1500 cm .
-1
d. Adanya ikatan rangkap C=C yang memiliki serapan pada daerah 1675–
1500 cm
.
-1
e. Adanya C-H alifatik pada daerah serapan kurang dari 3000 cm .
-1
, maupun
aromatik pada daerah serapan lebih dari 3000 cm-1
f. Adanya cincin disubtitusi meta pada daerah serapan 671 cm .
-1
dan satu
lagi dekat 780 cm-1.
10. Spektrofotometer 1
Spektroskopi Resonansi Magnet Inti memberikan gambaran mengenai
jenis atom, jumlah, maupun lingkungan atom hidrogen (
H-NMR
1
H NMR). Spektroskopi
NMR didasarkan pada penyerapan gelombang radio oleh inti-inti tertentu dalam
molekul organik, apabila molekul tersebut berada dalam medan magnet yang kuat
Interpretasi spektra 1H
a. jumlah sinyal, menunjukkan ada berapa macam perbedaan proton yang
terdapat dalam molekul
NMR harus memperhatikan hal-hal sebagai berikut:
b. kedudukan sinyal, ditunjukkan oleh geseran kimia (δ) ppm, menunjukkan jenis proton
c. intensitas sinyal atau harga integrasi masing-masing sinyal, perbandingan
harga integrasi menyatakan perbandingan jumlah proton
d. pemecahan (spliting), menerangkan tentang limgkungan dari sebuah
proton dengan proton lainnya yang berdekatan
Perbedaan frekuensi resonansi setiap proton dalam cuplikan diukur relatif
terhadap frekuensi resonansi dari proton-proton senyawa standar. Senyawa
standar yang umum digunakan yaitu tetrametilsilan (TMS). TMS dipilih karena
TMS memberikan puncak tunggal yang tajam dan kuat walaupun digunakan
konsentrasi yang rendah. Hal ini disebabkan duabelas proton pada TMS yang
ekuivalen. TMS bersifat inert, memiliki titik didih rendah sehingga mudah
diuapkan untuk memperoleh kembali cuplikan, dan TMS juga dapat larut dalam
kebanyakan pelarut organik (Kemp W, 1975: 83). Selain itu, proton-proton dari
gugus metil pada TMS jauh terlindungi bila dibandingkan dengan kebanyakan
senyawa-senyawa lain. Hal ini disebabkan silikon yang elektropositif mendorong
elektron ke gugus metil melalui efek induksi sehingga memberikan efek
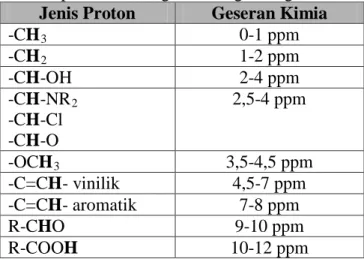
Tabel 2. Tipe Proton dengan Berbagai Pergeseran Kimia Jenis Proton Geseran Kimia
-CH3 0-1 ppm -CH2 1-2 ppm -CH-OH 2-4 ppm -CH-NR -CH-Cl 2 -CH-O 2,5-4 ppm -OCH3 3,5-4,5 ppm -C=CH- vinilik 4,5-7 ppm -C=CH- aromatik 7-8 ppm R-CHO 9-10 ppm R-COOH 10-12 ppm
Berdasarkan struktur dari senyawa 4-(3-hidroksifenil)-3-buten-2-on, maka
dapat diprediksikan kemungkinan gugus fungsi yang akan muncul dalam
spektroskopi 1
a. Adanya proton dari cincin aromatik akan ditunjukkan oleh puncak pada δ = 7 – 8 ppm, biasanya muncul dengan puncak tunggal.
H-NMR diantaranya:
b. Adanya proton dari primer jenuh –CH3
c. Adanya proton yang terikat pada atom C=C ditunjukkan oleh puncak pada δ = 5,0 – 6,5 ppm.
pada δ = 0 – 1 ppm.
d. Adanya proton dari –OH fenol akan ditunjukkan oleh puncak pada δ = 6 – 8 ppm.
B. Penelitian yang Relevan
Penelitian relevan yang mendukung penelitian ini adalah
1. Penelitian yang dilakukan oleh Fathul Arifin (2007) yang telah berhasil
mensintesis senyawa benzalaseton dan dibenzalaseton menghasilkan senyawa
dan panjang gelombang maksimum 328 nm untuk senyawa dibenzalaseton,
sehingga kedua senyawa tersebut memiliki potensi sebagai senyawa tabir
surya UV-A.
2. Penelitian yang dilakukan oleh Gunantyo Decky Wirawan (2008) yang telah
berhasil mensintesis senyawa 1,5-difenil-2,4-pentadien-1-on dengan panjang
gelombang maksimum 343 nm, sehingga senyawa tersebut memiliki potensi
sebagai senyawa tabir surya UV-A.
3. Penelitian yang dilakukan Sri Handayani (2009) yang telah berhasil
mensintesis senyawa dibenzalaseton asimetris dengan panjang gelombang
maksimum 350 nm, sehingga senyawa tersebut memiliki potensi sebagai
senyawa tabir surya UV-A.
C. Kerangka Berfikir
Senyawa 3-hidroksibenzaldehida merupakan senyawa turunan
benzaldehida yang tersubstitusi gugus hidroksi pada posisi meta. Senyawa ini
digunakan sebagai intermediet dalam sintesis organik. Pemanfaatan senyawa ini
dalam sintesis perlu dikembangkan, terutama untuk mensintesis suatu senyawa
baru yang diharapkan mempunyai banyak manfaat, salah satunya adalah
menghasilkan senyawa yang berpotensi sebagai tabir surya.
Senyawa 4-(3-hidroksifenil)-3-buten-2-on merupakan senyawa turunan
benzalaseton yang diperkirakan mempunyai aktivitas sebagai senyawa tabir surya,
karena senyawa ini mempunyai struktur yang mirip dengan senyawa turunan asam
yang banyak digunakan sebagai senyawa tabir surya. Hal ini juga diperkuat
dengan nilai panjang gelombang maksimum senyawa
4-(3-hidroksifenil)-3-buten-2-on sebesar 344 nm yang menunjukkan potensi senyawa tabir surya UV-A.
Senyawa ini disintesis dengan menggunakan reaktan
3-hidroksibenzaldehida dan aseton dengan katalis basa menggunakan reaksi
kondensasi aldol silang. Reaksi ini melibatkan ion enolat yang terbentuk dari
aseton yang akan bertindak sebagai nukleofil yang akan menyerang karbon karbonil senyawa aldehida aromatik menghasilkan senyawa β-hidroksi keton, yang selanjutnya mengalami dehidrasi menghasilkan senyawa α, β-keton tak jenuh 4-(3-hidroksifenil)-3-buten-2-on.