DAYA REDUKSI KAPANG A. Oligospora DAN Verticillium Spp.
TERHADAP LARVA
3H. contortus: STUDI PENDAHULUAN
(The Reduction Capacity of A. Oligospora and Verticillium spp. Molds
Against to H. Contortus Larvae
3: A Preliminary Study)
RIZA ZAINUDDIN AHMAD
Balai Penelitian Veteriner, PO Box 151, Bogor 16114
ABSTRACT
The in vitro reduction test of Arthrobotrys oligospora and Verticillium spp. local isolates of L3 H.
contortus were studied. The aim of this study is to show the ability of fungi to kill larvae. The tests were done
on 6 groups for spore treatments. The first to six treatment were: 5 x103 A. oligopora; 2.5 x 104 A. oligospora;
5 x 103 Verticillium spp; 2.5 x 104 Verticillium spp; 2.5 x 103 A.oligopora added 2.5 x 103 Verticillium spp,
and; 5 x 104 A. oligospora added 5 x 104 Verticillium spp., then each was placed in a glass containing 4567
epg and mixed with vermiculite. After inoculated for 7 days in the room temperature the number of larvae was counted. The results obtained from the control and six treatments were consecutively; 923; 265; 137; 684; 434; 276; 152. The best value is 137 with using A. oligospora molds to kill H. contortus larvae.
Key Words: A. oligospora, Verticillium spp., H. contortus larvae, reduction ABSTRAK
Uji reduksi secara in vitro kapang Arthrobotrys oligospora dan Verticillium spp. isolat lokal terhadap larva3 H. contortus bertujuan memperlihatkan daya reduksi kedua kapang tersebut dalam membunuh larva.
Penelitian ini dilakukan dengan cara memberi perlakuan terhadap 6 kelompok dengan dosis spora secara berurutan perlakuan I sampai dengan VI sebagai berikut: 5 x 103 A. oligospora; 2,5 x 104 A. oligospora; 5 x
103 Verticillium spp; 2,5 x 104 Verticillium spp; 2,5 x 103 A. oligospora ditambah 2,5 x 103 Verticillium spp,
dan; 5 x 104 A. oligospora ditambah 5 x 104 Verticillium spp. Setelah itu masing-masing diletakan pada gelas
yang berisi tinja mengandung EPG cacing: 4567 dan ditambahkan vermikulit. Setelah diinkubasi selama 7 hari dihitung larvanya. Hasil perhitungan larva yang diperoleh secara berurutan mulai kontrol sampai dengan perlakuan keenam adalah sbb: 923; 265; 137; 684; 434; 276; 152. Nilai terbaik adalah 137 dengan perlakuan memakai kapang A. oligospora untuk membunuh larva H. contortus.
Kata kunci: A. oligospora, Verticillium spp., larva H. contortus, reduksi
PENDAHULUAN
Kontrol biologis telah diterapkan sebagai strategi pengendalian parasit terpadu baik dalam peternakan konvensional dan organik dalam skala besar dan kecil (AHMAD, 1997;
AHMAD et al. 2002; LARSEN, 2000). Adapun pengendalian cacing H. contortus dengan memakai kontrol biologis merupakan salah satu pilihan, pilihan ini baik karena dapat dikombinasikan dengan cara lain dan bersifat aplikatip. Kapang nematofagus sudah diketahui mampu membunuh cacing nematoda, dan mekanismenya dilakukan dengan berbagai cara (PERSMARK, 1997). Kapang A. oligospora
dapat membunuh larva3 H. contortus dengan
cara membuat jerat, sedangkan kapang
Verticillium spp. dengan cara sebagai
endoparasit dan membunuh telur.
Adapun taksonomi A. oligospora menurut JACOBS (2002): Divisi: Eumycota, Kelas: Deuteromycetes, Ordo: Moniliale (Hyphomycetes), Famili: Moniliaceae, Sub famili: Hyalodidymae dan Genus: Arthrobotrys spp.
A. oligopora tumbuh saprofitik menyebar
dengan miselim vegetatif, memproduksi spora dengan perbanyakan aseksual. Banyak ditemui pada sampah organik, dan tanah. (GRONVOLD,
berdinding tipis dan kering. Sejumlah konidia berasal dari kelompok yang panjang dari koniafor yang tegak, tetapi beberapa konidia dapat bersifat dorman (khlamidospora) yang dihasilkan oleh miselium. dikarakterisasi dengan ciri-ciri membentuk jerat secara tak spontan, konidiafor bercabang membentuk jerat yang lengket lebih dari satu, konidia berumpun, bersepta berbentuk pyriform, berukuran bervariasi antara 22–32 µm x 12–20 µm (BARRON, 1977).
Adapun Verticillium spp. mempunyai taksonomi sebagai berikut menurut ANONIMOUS (2004), yaitu Superkingdom:
Eukaryota, Kingdom: Fungi, Filum: Ascomycota, Subfilum: Pezizomycotina, Kelas: Sordariomycetes, Ordo: Hypocreales, Famili: Hypocreales, Genus: Verticilium spp.
Verticillium spp termasuk kapang tanah
yang hidup kosmopolitan, sering ditemui sebagai kapang kontaminan dan isolat lokal telah berhasil ditemukan AHMAD dan
BERIAJAYA (1996). Secara mikroskopis terlihat
hifa memanjang, bersepta, mempunyai cabang, berkonidia. Menurut GILMAN (1959)
Verticillium spp. dapat digolongkan menjadi 9
spesies dan sejalan dengan kemajuan identifikasi spesies-spesies tersebut bertambah banyak, sampai saat ini beberapa VertilcillIum spp penting artinya sebagai kapang nematofagus yaitu Verticillium balanoides, V.
chlamydosporium. Adapun isolat Verticillium
spp yang dipakai pada penelitian ini identifikasi menurut GILMAN (1975) diduga
adalah tergolong V. tereteste.
Konidia-konidia Verticillium spp.
dihasilkan oleh ujung dari sel-sel konidiagenus yang panjang (phialid), muncul dalam lingkaran dari konidiafor yang memutari dari bangkai nematoda. Satu persatu atau sekelompok konidia melingkar sepanjang tangkainya. Beberapa spesies Verticillium spp. mempunyai konidiofor relatif pendek, kaku keras dan lebih atau sedikit tegak, sedangkan spesies lain konidianya panjang dan terkulai. Spora (phialokonidia) terkumpul dalam bola pada mulut dari phialid (BARRON, 2004).
Dibandingkan dengan konidia kapang pembuat perangkap, maka diameter konidia endoparasit lebih kecil dan tipis, juga mempunyai sifat
misalnya V. sphaerosporum yang mempunyai diameter berukuran 2,0–3,0 µm.
Kapang Verticillium spp. dapat sebagai endoparasit dan parasit telur, beberapa kapang diketahui sebagai parasit pada telur nematoda termasuk Verticillium alboatrum, V chlamydosporium, dan V. psalliosae.
Telur-telur cacing Ascaris lumbricoides dari babi dapat dipakai untuk menguji pengaruh kapang Verticillium
chlamydosporium dan Verticillium spp.
Kapang tersebut merusak dinding sel telur secara enzimatik dan kemudian menginfeksi telur (LYSEK dan KRAJEI, 1987: KUNERT,
1992).
Berbeda dengan kapang pemangsa, kapang endoparasit umumnya mempunyai hifa tidak berkembang, hanya membentuk tabung spora misalnya untuk cendawan berkelas yang lebih sederhana yaitu Oomycyetes (Catenaria spp.) yang bersifat parasit obligat pada inang, dan untuk lebih tinggi seperti Verticillium spp. mempunyai konidiafor, hifa dan bersifat saprofit.
Kedua kapang ini bila di kombinasikan di dalam membunuh cacing nematoda diduga akan memberikan hasil yang baik. Tujuan tulisan ini untuk memperlihatkan daya reduksi kapang-kapang tersebut terhadap cacing nematoda.
BAHAN DAN METODE
Penelitian pendahuluan ini dilakukan mulai bulan Januari sampai April 2004 di Balai Penelitian Veteriner, adapun isolat yang dipakai adalah isolat lokal hasil isolasi dan identifikasi dari penelitian sebelumnya. Sedangkan tinja yang berisi telur cacing H.
contortus diperoleh dari domba yang telah
diinfeksi murni oleh H. contortus. Uji dilakukan menurut MENDOZA et al. (1994) dengan sedikit modifikasi pada dosisnya.
Isolat-isolat yang dipakai adalah A.
oligospora dan Verticillium spp. Isolat tersebut
diperbanyak pada medium Corn Meal Agar (CMA) selama 2 minggu pada suhu kamar, setelah itu konidia dipanen dengan cara memberi aqudest secukupnya lalu dikerok dengan kaca penutup, hasil konidia dihitung
konidia yaitu tabung ke-1; 5 x 103 A.oligopora,
tabung ke-2; 2.5 x 104 A.oligospora, tabung
ke-3; 5 x 103 Verticillium spp, tabung ke-4; 2,5 x
104 Verticillium spp, tabung ke-5; 2,5 x 103
A.oligopora ditambah 2,5 x 103 Verticillium
spp, dan tabung ke-6; 5 x104 A.oligospora
ditambah 5 x 104 Verticillium spp. Selanjutnya
konidia tersebut akan diletakan pada tinja yang mengandung telur H. contortus.
Persiapan telur pada tinja dilakukan dalam waktu yang hampir bersamaan. Lima ekor domba dipakai setelah dibersihkan seluruh cacing yang menginfeksi dengan obat cacing lalu domba-domba tersebut diinfeksi murni oleh larva H. contortus. Setelah kira-kira 4 minggu telur pergram tinja (EPG) diukur kembali sampai mencapai (EPG) yang diinginkan bila belum tercapai direinfeksi kembali. Diperoleh rataan EPG untuk penelitian adalah: 4567.
Selanjutnya tinja masing-masing seberat 3 g yang mengandung cacing dibagi menjadi 7 kelompok. Satu kelompok sebagai kontrol dan lainnya diberi perlakuan 1 s/d 6 diberi konidia kapang yang telah dipanen. Tinja ditambahkan vermikulit dan konidia lalu diinkubasikan, dijaga kelembabannya dan setelah 1 minggu dipanen larvanya dengan metode WITHLOCK
(1949). Perlakuan tersebut dilakukan sebanyak 4 kali ulangan, hasil yang diperoleh dirata-ratakan.
HASIL DAN PEMBAHASAN
Adapun hasil yang diperoleh adalah sebagai pada Tabel 1.
Pada kontrol yang tidak diberi perlakuan ternyata larva yang menetas belum banyak dibanding dengan perhitungan EPGnya 4567 dan bila 3 g: 13701 sedangkan larva yang menetas (LPG) hanya 923 saja, dan bila 3 g: 1869. Keadaan ini diduga sangat dipengaruhi berbagai faktor seperti suhu, kelembaban, dan daya tetas. Bila suhu terlalu panas diatas normal 25–30oC, tidak lembab (kering) akan
mengurangi daya tetasnya. Namun bila dibandingkan dengan yang diberi perlakuan (P1, P2, P3, P4, P5 dan P6) maka larva yang menetas dari telur lebih tinggi.
Dari hasil yang didapat secara umum pemakaian kapang nematofagus pada tinja yang mengandung larva H. contortus memperlihatkan korelasi positif terhadap penurunan larva pada setiap perlakuan bila dibanding dengan kontrol. Pada perlakuan dengan kapang A.oligospora saja P1 (LPG; 265) dan P2 (LPG; 137)) dibandingkan dengan kombinasi antara kapang A.oligospora dan
Verticillium spp P5 (LPG; 276) dan P6 (LPG;
152) menunjukkan hasil yang tak jauh berbeda bila tidak diuji dengan alat bantu statistik.
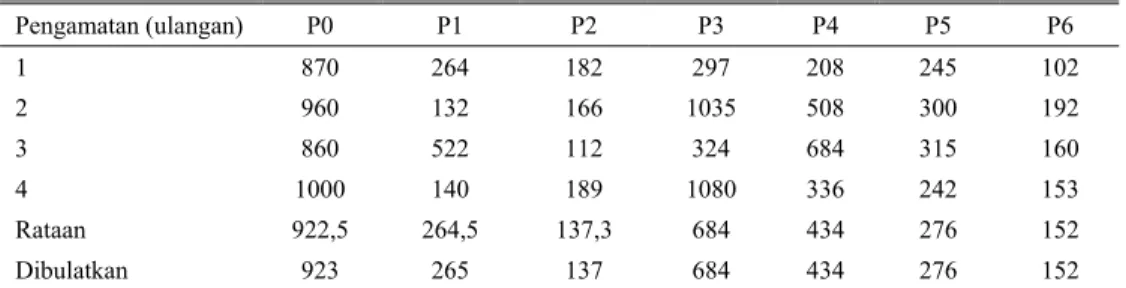
Tabel 1. Jumlah larva per gram tinja
Pengamatan (ulangan) P0 P1 P2 P3 P4 P5 P6 1 870 264 182 297 208 245 102 2 960 132 166 1035 508 300 192 3 860 522 112 324 684 315 160 4 1000 140 189 1080 336 242 153 Rataan 922,5 264,5 137,3 684 434 276 152 Dibulatkan 923 265 137 684 434 276 152
P0 : Kontrol, tanpa konidia
P1 : 5 x 103 konidia Arthrobotrys oligospora
P2 : 2,5 x 104 konidia Arthrobotrys oligospora
P3 : 5 x 103 konidia Verticillium spp.
P4 : 2,5 x 104 konidia Verticillium spp.
P5 : 2,5 x 103 konidia Arthrobotrys oligospora + 2,5. 103 konidia Verticillium spp.
Pada perlakuan 1 dan 2 kapang membunuh larva dengan cara memangsa memakai jerat sedangkan perlakuan 3 dan 4 memangsa telur dan sebagai endoparasit. Kombinasi dari keduanya pada perlakuan 5 dan 6. Hasil yang terbaik adalah perlakuan kedua dengan memakai kapang pembuat jerat. Alat bantu statistik tak digunakan untuk studi pendahuluan ini karena nilai hasil perhitungan larva sudah cukup terlihat bedanya antar perlakuan.
Pemakaian jerat lebih efektif dibanding dengan endoparasit maupun terhadap H.
contortus. Hal ini karena pertumbuhan kapang A. oligospora lebih cepat dibandingkan dengan Verticillium spp. pada media mengandung tinja
(LARSEN et al., 1994). Selain itu Verticillium
spp. yang diuji diduga tergolong endoparasit, sehingga kapang tersebut memerlukan waktu yang lebih lama untuk menginfeksi larva sebagai endoparasit, karena menghasilkan konidia (spora) terlebih dahulu lalu baru membunuh larva dibanding dengan A.
oligospora yang hifa vegetatif bagian tertentu
langsung membuat jerat pada larva. Adapun mekanismenya lebih jelas lagi sebagai berikut: Spora Verticillium spp. mempunyai ukuran kecil dengan ujung yang lengket untuk melekat pada kutikula nematoda. Pancangnya dipakai untuk menetrasi tubuh melalui epidermis dari inang, kemudian cendawan masuk tubuh hingga akhirnya mengisi inang dengan hifa. Selanjutnya cendawan memecah kembali dinding kulit dari nematoda yang mati untuk berproduksi.
Beberapa spesies Verticillium spp. adalah tergolong endoparasit nematoda. Mekanisme kapang endoparasit yaitu setelah spora tertelan larva, kemudian spora menempel pada saluran pencernaan dan mengambil nutrisi. Selanjutnya kapang tersebut berkembang biak dan akhirnya tumbuh keluar dengan cara menembus dinding kulit larva sehingga larva akhirnya mati, dan saat konidia endoparasit masuk dilakukan dengan cara model perlekatan yang sedikit mengalami modifikasi sesuai keadaan.
Peran penting dalam kontrol biologis lainnya sebagai parasit pada telur adalah kemampuan menyerang telur nematoda, ketika telur diletakan oleh nematoda betina, sebuah
selanjutnya tumbuh dengan cepat, berkembang dan mengambil nutrisi pada telur sehingga akhirnya telur tersebut mati.
Adapun mekanisme kapang A. oligospora di dalam membunuh larva adalah sebagai berikut; Kehadiran nematoda diinduksi oleh pembentukan organ perangkap (jerat) yang lengket dan kemudian tumbuh. Nemin dan kutikula yang terdapat pada larva H. contortus mempengaruhi pembentuk jaring (jerat) tersebut. Penangkapan nematoda melalui jaring hifa yang diikuti oleh penetrasi kutikula nematoda. Biasanya setelah pembentukan jerat memperangkap larva, kemudian terjadi infeksi gelembung dan masuk kedalam nematoda yang terperangkap. Dari infeksi gelembung tersebut, hifa tropik tumbuh keluar dan mengisi tubuh nematoda membentuk asimilasi hifa, segera setelah penetrasi pergerakan dari nematoda dihambat, dan sekreta nematotoksin yang dihasilkan membuat larva parasilis kemudian mati dan dicerna. (BARRON, 1977; PERSMARK
1997; JACOBS, 2004). Dari hasil yang diperoleh
pemakaian kombinasi spora pada tinja kurang baik dibanding dengan perlakuan satu macam spora yaitu A. oligospora, hal ini terjadi karena faktor-faktor pertumbuhan dan mekanisme seperti yang telah diuraikan di atas.
KESIMPULAN
Pemakaian A. oligospora sebagai kontrol biologis terhadap larva3 H. contortus secara in
vitro hasilnya lebih baik dibanding dengan Verticillium spp. ataupun kombinasi keduanya.
DAFTAR PUSTAKA
AHMAD, R.Z. 1997. Potensi kapang sebagai
pengendali biologi terhadap cacing. Majalah
Parasitologi Indonesia 10(2): 104−113. AHMAD, R.Z. dan BERIAJAYA. 1997. Isolasi
Verticillium spp. untuk dipakai sebagai kontrol
biologi cacing nematoda. Buletin Ipkhi Juli– Desember 1997, 7(2): 13−6.
AHMAD, R.Z.,BERIAJAYA danS. HASTIONO.2002.
Pengendalian infeksi cacing nematoda saluran pencernaan ruminansia kecil dengan kapang nematofagus. Wartazoa12(3): 121−126.
BARRON,G.L.1997.The nematode destroying fungi.
In: Tropic Mycobiology No.1. Canadian
Biological Publication Ltd. Guelph, Ontario, Canada.
BARRON, G.L. 2004.
http://www.uoguelph.ca/-gbarron/misc2003/verticill.htm.
GILMAN,J.C.1957.A Manual of soil fungi.2nd ed.
The Iowa State University Press, Ames, Iowa, Usa.
GRONVOLD, J., J. WOLSTRUP, P. NANSEN, S.A.
HENRIKSEN, M. LARSEN and J. BRESCIANI. 1993. Biological control of nematode parasites in cattle with nematode trapping fungi: a survey of danish studies. Vet. Parasitol. 48: 311−325.
GRONVOLD, J., P. NANSEN, S.A. HENRIKSEN, M.
LARSEN, J. WOLSTRUP, J. BRESCIANI, H. RAWAT and L.FRIBERT. 1996. Induction of
traps by ostertagia ostertagi larvae, chlamydospore production and growth rate in the nematode-trapping fungus duddingtonia flagrans. J. Helmintholog 70: 291−297. JACOBS PHILIP. 2004.
http://www.Biological-Research.Com/Philip-Jacobs%20bric/Ar-Olig. Htm.
KUNERT,J. 1992. On The Mechanism of Penetration
of Ovicidal Fungi Through Egg Shells of Parasitic Nematodes. Decomposition of Chitinous And Ascaroside Layers. Folia
Parasitologica; 39.
LARSEN, M., M.FAEDO,P.J. WALLER. 1994. The
Potential of nematophagous fungi to control the free-living stages of nematode parsites of sheep; survey for the presence of fungi in fresh faeces of grazing Livestock In Australia.
Vet. Parasitol. 53: 275−281.
LARSEN. 2000. Prospects for controlling animal
parasitic nematodes by predacious microfungi.
Parasitology. 120 S121−131
LYSEK, H. and D. KRAJEI. 1987. Penetration of ovicidal fungus verticillium chlamydosporium through the ascaris lumbricoides egg-shells.
Folia Parasitologica 34: 57−60.
PERSMARK, L. 1997. Dissertation Ecology of
Nematophagous Fungi in Agricultural Soils, Dept of Ecology Microbial Ecology, Lund University, Sweden.
MENDOZA DE-GIVES. P, VICTOR. M, VAZQUEZ
-PRATS. 1994. Reduction of haemonchus contortus infectve larvae by three nematophagous fungi in sheep faecal cultures.
Vet. Parasitol. 55: 197−203.
WHITLOCK, H.V.1948. Some modifications of mc master helmints egg counting technique and apparatus. J. Council.Sci. Industry Res. 21: 172−80.