i
Kinetic Study of Acid Hydrolysis of Amylose andAmylopectin From Acetylated Mocaf Flour
Oleh:
Nurlyana Puspitasari 652013016
TUGAS AKHIR
Diajukan kepada Program Studi Kimia Fakultas Sains dan Matematika guna memenuhi sebagian dari persyaratan untuk mencapai gelar Sarjana Sains
Program Studi Kimia Fakultas Sains dan Matematika Universitas Kristen Satya Wacana
Studi Kinetika Hidrolisis AsamAmilosa dan Amilopektin Pada Tepung Mocaf Terasetilasi
Kinetic Study of Acid Hydrolysis of Amylose andAmylopectin From Acetylated Mocaf Flour
Nurlyana Puspitasari*, Yohanes Martono ** , Cucun Alep Riyanto** *Mahasiswa Program Studi Kimia Fakultas Sains dan Matematika
**Dosen Program Studi Kimia Fakultas Sains dan Matematika Universitas Kristen Satya Wacana, Salatiga
Jl. Diponegoro No.52-60 Salatiga 50711 Jawa Tengah – Indonesia [email protected]
ABSTRACT
Acetylation is one of starch modification method that can increase the quality of the flour properties. The quality of the flour is influenced by the amylose and amylopectin content. The acid hydrolysis process of the starch can change the amylose and amylopectin content. The aim of this study was to determine the reaction kinetics of amylase and amylopectin on acetylated mocaf. Hydrolysis process was carried out using 0.1 M HCl with 5% and 10% acetylation concentration at 27˚C, 30˚C, 40˚C, and
50˚C. The amylose and amylopectin content were determined using UV-VIS spectrophotometry method. Reaction order and rate constant were determined using linear regression method. The energy activation of acetylated mocaf was determined using Arrhenius equation.
The results showed that the kinetics of the hydrolysis acetylated mocaf follow
pseudo zero order reaction. The highest reaction rate constant was achieved at 40˚C. The energy activation for amylose of 5%mocaf acetylation was +12,87755 kJ.mol-1.K-1 and +21,67543 kJ.mol-1.K-1for 10%, while energy activation of amylopectin from 5% and 10% acetylated mocaf were +34,32352 dan +14,42036 kJ.mol-1.K-1 respectively.
2
PENDAHULUAN
Pangan merupakan kebutuhan dasar yang paling penting bagi manusia untuk mempertahankan hidup.Persoalan pangan di Indonesia sekarang ini dihadapkan pada ketergantungan terhadap satu jenis tanaman pangan. Hal ini akan berdampak pada produk pangan dengan harga yang relatif kurang terjangkau sehingga akan mengancam ketahanan pangan nasional (Husodo, 2004).
Salah satu upaya untuk meningkatkan ketahanan dan kemandirian pangan yaitu melalui diversifikasi pangan. Diversifikasi pangan yaitu proses pengembangan produk pangan yang tidak bergantung pada satu jenis bahan saja, tetapi memanfaatkan berbagai macam bahan pangan secara optimal dan berkesinambungan (Suryana, 2009). Diversifikasi pangan berbasis tepung lebih mudah diterima masyarakat Indonesia karena tepung terigu dapat diolah menjadi bahan baku yang telah banyak digunakan dalam pembuatan roti, mie, kue, dan sebagainya. Salah satu sumber karbohidrat lokal yang dapat dimanfaatkan sebagai cadangan pangan untuk substitusi terigu dalam rangka mendukung ketahanan pangan nasional adalah ubi kayu atau singkong (Martono, 2016).
Mocaf sebagai produk unggulan hasil olahan ubi kayu diarahkan menjadi alternatifsumber pangan karbohidrat untuk mendampingi dan apabila dimungkinkan untuk mengganti konsumsi beras dan terigu.Penggunaan tepung mocaf sebagai bahan dasar pembuatan produk makanan tertentu seperti mie dan roti masih memiliki kekurangan yaitu pada daya kembang dan elastisitas tepung yang rendah sehingga penggunaan tepung mocaf untuk olahan pangan masih terbatas (Martono, 2016).
Peningkatan sifat fungsional dan karakteristik tepung mocaf dapat dilakukan dengan metode modifikasi pati dimana tepung mocaf mempunyai sifat – sifat yang diinginkan dan dapat memperluas penggunaanya dalam proses pengolahan pangan. Modifikasi pati ini dimaksudkan untuk merubah struktur molekul dari pati tersebut dengan cara merubah gugus hidroksilnya lewat suatu reaksi kimia (esterifikasi, asetilasi atau oksidasi) atau dengan mengganggu struktur asalnya (Fleche, 1985).
Proses hidrolisis asam terhadap pati membuat adanya perubahan pada kadar amilosa dan daya cerna (Wurzburg, 1995). Jumlah amilosa meningkat pada tahap awal proses hidrolisis asam. Proses hidrolisis asam akan memotong rantai amilopektin sehingga berat molekul (BM) lebih pendek (Wuttisela et al., 2007). Hidrolisis amilosa yang berkelanjutan diduga dapat memutus ikatan disakarida polimer amilosa dan menyebabkan monomer glukosa menjadi meningkat (Winarti dkk., 2014).
Berdasarkan penelitian-penelitian yang telah dilakukan,penelitian tentang derajat hidrolisis asam pada tepung mocaf terasetilasi belum pernah dilakukan sehingga penelitian ini akan mengkaji derajat hidrolisis asam tepung mocaf terasetilasi.Berdasarkan latar belakang di atas maka tujuan dari penelitian ini adalah sebagai berikut:
1. Menentukan parameter kinetika reaksi dan energi aktivasi tepung mocaf terasetilasi. 2. Melakukan identifikasi gugus fungsi MOCAF terasetilasi dengan menggunakan
spektrofotometer FTIR
METODE PENELITIAN
Bahan yang digunakan dalam penelitian ini adalah singkong yang diperoleh dari Pasar Blauran Salatiga. Air rendaman kedelai (ARK) diperoleh dari Pasar Bringin, Kabupaten Semarang. Bahan kimia yang diperlukan yaitu TCA (Tricholoroacetic acid), amilosa, amilopektin, I2, NaOH, HCl, Akuades, dan KI, Semua bahan yang digunakan
berderajat PA (Pro Analysis) diperoleh dari E – Merck, Germany.
Piranti yang digunakan yaitu grinder, ayakan80 mesh, centrifuge (EBA 21 Hettich Zentrifugen), drying cabinet, piranti gelas, neraca analitis dengan ketelitian 0,1 mg (Ohaus, PA214), spektrofotometer FTIR ABB MB 3000 (Clakuadeset Scientific, Northampton, UK), dan spektrofotometer UV- Vis (Optizen, 2120)
Preparasi Sampel
4
Fermentasi (Martono, 2016)
Sampel singkong yang telah dipotong-potong ditimbangseberat 200,00 g dan dimasukkan ke dalam wadah. Singkong dalam wadah dituangi air panas dengan suhu 60°C dan direndam selama 5 menit.Setelah selesai perendaman dengan air panas, air dibuang dan diganti dengan air rendaman kedelai dengan ratio 1:2 (w/v). Singkong difermentasi selama 12 jam.Setelah waktu fermentasi selesai, singkong dicuci dengan air bersih.
Uji keasaman Air Rendaman Kedelai (Jannah dkk., 2013)
Sejumlah20 mL air rendaman kedelai ditambah 1 mL indikator PP 0,1 % dititrasi dengan menggunakan NaOH 0,1 N hingga berwarna merah muda. Perhitungan kadar asam dilakukan dengan rumus :
Kadar asam = 𝑉1 𝑥𝑁𝑥𝐵
B = Berat molekul asam laktat (90)
Asetilasi Tepung Mocaf (Lawal etal., 2004)
Seberat50,00 g singkong ditambah dengan 125 mL akuades. Derajat pH larutan diatur menjadi 8 dengan NaOH 1,0 M dan dibiarkan selama 60 menit. Larutan kemudian ditambah dengan asam asetat glasial dengan konsentrasi yang berbeda yaitu 5 dan 10% (w/w) sedikit demi sedikit dan pH larutan diatur menjadi 8 dengan 1,0 M NaOH dan dibiarkan selama 60 menit. pH Larutan diatur menjadi 5,5 dengan 1,0 M HCl lalu singkong dicuci dengan air bersih. Mocaf dikeringkan dalam drying cabinet
pada suhu 40°C selama 24 jam.Singkong ditepungkan hingga halus dan disimpan dalam wadah tertutup.Tepung yang telah jadi disebut sebagai Mocaf terasetilasi.
Hidrolisis pati dengan asam (Chung et al., 2003 yang dimodifikasi)
dinetralkan dengan NaOH 1,0 M kemudian disentrifuge (2300 rpm)selama 15 menit lalu dikeringkan dalam drying cabinet pada 40°C.
Pengukuran kadar amilosa amilopektin (Martono dkk., 2016) Pembuatan Reagen (Amilosa dan Amilopektin)
Seberat 0,3 g iodin dan 1,2 g KI ditimbang dan dilarutkan kedalam 100 mL larutan HCl 0,01 M. Kemudian dilakukan pengenceran sebanyak 5 kali.
Pembuatan Kurva Standar Amilosa
Seberat 20,0 mg amilosa ditimbang dan dilarutkan kedalam 5 mL NaOH 1,0 M dan 5 mL aquades. Kemudian, larutan diambil 1 mL dan ditambahkan 5 mL HCl 1,0 M lalu digenapi dengan akuades hingga volume menjadi 50 mL. Selanjutnya, larutan amilosa diambil 5 mL dan ditambahkan dengan 2 mL larutan TCA (Tricholoroacetic acid) dan 2 mL larutan reagen I2-KI. Setelah itu, larutan diukur dengan
spektrofotometer UV-VIS dengan panjang gelombang 630 nm. Pembuatan Kurva Standar Amilopektin
Seberat 25,0 mg amilopektin ditimbang dan dilarutkan kedalam 5 mL NaOH 1 M dan 5 mL aquades. Kemudian, diambil 1 mL larutan dan ditambahkan5 mL HCl 1,0 M lalu digenapi dengan akuades hingga volume menjadi 50 mL. Selanjutnya, larutan amilopektin diambil 5 mL ditambahkan dengan 2 mL larutan TCA (Tricholoroacetic acid) dan 2 mL larutan reagen I2-KI. Setelah itu, larutan diukur dengan
spektrofotometer UV-VIS dengan panjang gelombang 533 nm. Pengukuran Sampel Kadar Amilosa
Seberat 20,0 mg sampel ditimbang dan dilarutkan kedalam 5 mL NaOH 1,0 M dan 5 mL aquades. Kemudian, diambil 1 mL larutan dan ditambahkan 5 mL HCl 1,0 M lalu digenapi dengan akuades hingga volume menjadi 50 mL. Selanjutnya, larutan sampel diambil 5 mL ditambahkan dengan 2 mL larutan TCA (Tricholoroacetic acid) dan 2 mL larutan reagen I2-KI. Setelah itu, larutan diukur dengan spektrofotometer
UV-VIS dengan panjang gelombang 630 nm. Pengukuran Sampel Kadar Amilopektin
6
sampel diambil 5 mL ditambahkan dengan 2 mL larutan TCA (Tricholoroacetic acid) dan 2 mL larutan reagen I2-KI. Setelah itu, larutan diukur dengan spektrofotometer
UV-VIS dengan panjang gelombang 533 nm. Kinetika Reaksi
Kinetika kimia mempelajari laju berlangsungnya reaksi kimia dan energi yang berhubungan dengan proses tersebut, serta mekanisme berlangsungnya reaksi. antara laju reaksi dengan konsentrasi reaktan dinyatakan dengan hukum laju. Dalam penurunan hukum laju dikenal istilah orde 'reaksi atau tingkat reaksi, yaitu bilangan pangkat yang menyatakan hubungan konsentrasi zat dengan laju reaksi. Harga orde reaksi hanya dapat ditentukan melalui eksperimen, sedangkan tahap penentu laju reaksi adalah reaksi yang paling lambat (Chang, 2005)
Reaksi orde nol v = k [A]O
Keterangan: Ao : konsentrasi saat t = 0 awal sebelum reaksi
At : konsentrasi saat t = t (reaksi berlangsung selama t berlangsung)
k : konstanta laju
T : temperatur (K)
A : faktor frekuensi tumbukan
Ea : energi aktivasi (kJ/mol)
R : konstanta gas (8,314 J/K.mol) (K)
Identifikasi Gugus Fungsi dengan Spektra FTIR (Martono dkk.,2016 yang dimodifikasi)
(HATR) pada suhu ruang (25°C).Spektra FTIR dari semua sampel dipindai dengan spektrofotometer FTIR ABB MB 3000 (Clakuadeset Scientific, Northampton, UK) yang dilengkapi dengan detektor Deuterated Triglycine Sulphate (DTGS) dan germanium beam splitter. Spektra FTIR sampel tepung dipindai pada bilangan gelombang 4000 – 650 cm-1 dengan resolusi 4 cm-1 dan jumlah pindaian sebanyak 32 kali. Semua spektra dikalibrasi dengan udara sebagai blanko.Setiap setelah pemindaian, FTIR dikalibrasi baru dengan udara sebagai blanko.Semua spektra direkam sebagai transmitan vs bilangan gelombang (cm-1) pada setiap titik data.
Analisa Data
Derajat hidrolisis tepung mocaf terasetilasi ditentukan berdasarkan parameter kinetika perubahan kadar amilosa, amilopektin dan gula pereduksi. Data hasil percobaan diplotkan dalam kurva orde reaksi 0, 1, dan 2 untuk menentukan orde reaksi. Nilai energi aktivasi (Ea) ditentukan berdasarkan persamaan Arrhenius.
HASIL DAN PEMBAHASAN Uji keasaman dan Fermentasi
Hasil kadar asam laktat yang diperoleh yaitu sebesar 1,90%. Hal ini menunjukkan bahwa pada Air Rendaman Kedelai (ARK) terkandung bakteri yang menghasilkan asam laktat yang dapat digunakan untuk fermentasi MOCAF. Selama proses fermentasi terjadi penghilangan komponen penimbul warna, seperti pigmen (khususnya pada ketela kuning), dan protein yang dapat menyebabkan warna coklat ketika pemanasan sehingga warna mocaf yang dihasilkan lebih putih jika dibandingkan dengan warna tepung singkong biasa (Martono, 2016).
Hidrolisis asam
Hidrolisis dilakukan di bawah suhu gelatinasi 52°C (Winarno, 2002). Hidrolisat pada tiap-tiap variasi dianalisa kadar amilosa dan amilopektinnya dengan menggunakan spektrofotometer UV-VIS. Berdasarkan besarnya absorbansi dapat dihitung konsentrasi amilosa dan amilopektin larutan hasil hidrolisis berdasarkan persamaan garis kurva baku amilosa dan amilopektin.
8
pati,molekul air membentuk ikatan hidrogen dengan amilosa dan amilopektin(McWilliams, 2001). Proses pertama yang terjadi adalah melelehnya bagiankristal dan membentuk suatu jaringan. Semakin tinggi energi panas, jaringankristal yang meleleh akan menjadi rusak dan melarutkan bagian amilosa danamilopektin. Kelarutan amilosa pada bagian kristal mengakibatkan bagian amorfmenjadi rusak tidak stabil (Belitz dan Grosch, 1999). Akibatnya ikatan hidrogendiantara amilosa dan amilopektin menjadi rusak.Kondisi di atas menyebabkan molekul air yang terus menerus masuk kedalam granula pati membuat ikatan hidrogen dengan amilosa maupunamilopektin pada bagian amorf maupun kristal granula pati menjadimembengkak dan ukuran granula meningkat sampaibatas tertentu (Hustiany, 2006).
Penentuan Parameter Kinetika Reaksi
Kinetika hidrolisis Mocaf terasetilasi ditinjau dari laju reaksi hidrolisis.Orde reaksi ditentukan secara regresi linear dengan menentukan model reaksi yang paling memberikan nilai koefisien determinasi regresi (R2) tertinggi dan error terendah.Nilai konstanta kecepatan reaksi dapat diperoleh dengan linearitas data konsentrasi terhadap waktu pada setiap variasi temperatur yang digunakan.Nilai konstanta kecepatan reaksi merupakan slope dari garis tersebut (Bej etal.,2008).Kinetika hidrolisis MOCAF terasetilasi mengikuti orde reaksi tertentu.Orde reaksi dapat ditentukan secara regresi linear.Hasil penelitian menunjukkan bahwa hidrolisispada MOCAF terasetilasi mengikuti orde 0 semu yang ditampilkan pada Tabel 1 dan Tabel 2.
Tabel.2 Perbandingan nilai R2 amilopektin terhadap berbagai Orde reaksi
Penambahan suhu reaksi meningkatkan kemampuan hidrolisis MOCAF terasetilasi sehingga laju degradasi amilosa dan amilopektin semakin besar, namun laju degradasi mulai menurun pada suhu 50˚C karena penambahan derajat asetilasi membuat konstanta MOCAF terasetilasi 10% lebih kecil dibandingkan mocaf terasetilasi 5%. Hal ini menunjukkan bahwa laju degradasi berjalan lebih lambat dengan adanya kenaikan derajat asetilasi. Laju degradasi amilosa amilopektin disajikan pada Tabel 3 dan Tabel 4.
Tabel 3. Nilai konstanta laju degradasi amilosa pada berbagai suhu dan konsentrasi asetilasi pada orde 0 semu.
Konsentrasi asetilasi
Konstanta laju reaksi (% b/b .menit-1)
27˚C 30˚C 40˚C 50˚C
5% 1,5 × 10-3 1,7 × 10-3 1,9 × 10-3 1,8 × 10-3
10% 1,4 × 10-3 1,5 × 10-3 2,0 × 10-3 1,9 × 10-3
Tabel 4. Nilai konstanta laju degradasi amilopektin pada berbagai suhu dan konsentrasi asetilasi pada orde 0 semu.
Konsentrasi asetilasi
Konstanta laju reaksi (% b/b.menit-1)
27˚C 30˚C 40˚C 50˚C
5% 3,8 × 10-3 5,3 × 10-3 7,0 × 10-3 5 × 10-3
10
Penentuan Nilai Energi Aktivasi (Ea)
Energi aktivasi (Ea) merupakan energi yang harus dimiliki oleh molekul sehingga mampu bereaksi. Penentuan nilai Ea untuk reaksi hidrolisis MOCAF terasetilasi dilakukan dengan menggunakan persamaan Arrhenius. Persamaan Arrhenius merupakan persamaan yang dapat digunakan untuk mengkuantitatifkan hubungan antara suhu reaksi dan Ea dengan konstanta laju reaksi (k). Persamaan Arrhenius ini dimodifikasi menjadi bentuk persamaan garis lurus (regresi linier) (Anugrahini dkk., 2013)
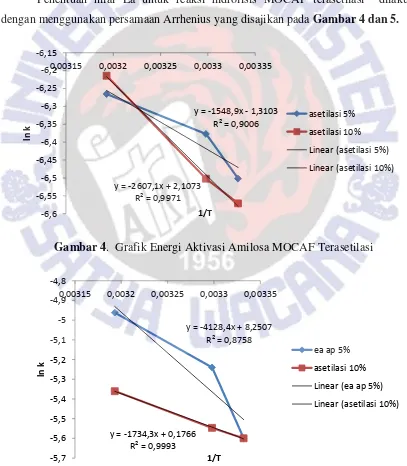
Penentuan nilai Ea untuk reaksi hidrolisis MOCAF terasetilasi dilakukan dengan menggunakan persamaan Arrhenius yang disajikan pada Gambar 4 dan 5.
Gambar 4. Grafik Energi Aktivasi Amilosa MOCAF Terasetilasi
Gambar 5. Grafik Energi Aktivasi Amilopektin MOCAF Terasetilasi
Nilai kemiringan (slope) dari persamaan garis lurus (regresi linier) kemudian digunakan untuk menghitung nilai Ea pada proses hidrolisis MOCAF terasetilasi. Nilai Ea dihasilkan dari perkalian antara slope dengan konstanta gas (R= 8,314 J.mol-1.K-1), sehingga diperoleh nilai Ea untuk reaksi hidrolisis amilosa dan amilopektin disajikan pada Tabel 5.
Tabel 5. Nilai energi aktivasi (Ea) reaksi hidrolisis MOCAF terasetilasi
Reaksi hidrolisis mocaf terasetilasi merupakan reaksi ini pemutusan rantai polimer pati menjadi unit-unit dekstrosa (C6H12O6). Pemutusan rantai polimer ini dapat
terjadi melalui beberapa cara misalnya secara enzimatis, kimiawi ataupun kombinasi keduanya (Muin dan Sari,2014).
Kadar Amilosa dan Amilopektin
12
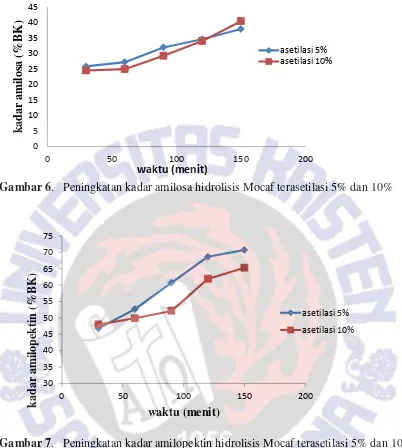
Gambar 6. Peningkatankadar amilosa hidrolisis Mocaf terasetilasi 5% dan 10%
Gambar 7. Peningkatan kadar amilopektin hidrolisis Mocaf terasetilasi 5% dan 10% Hasil penelitian menunjukkan kadar amilosa dan amilopektin meningkat sejalan dengan lamanya waktu hidrolisisdimanaini sejalan dengan penelitian Winarti dkk.,(2014) pada pati garut.Penambahan waktu hidrolisis mampu meningkatkan kadar amilosa dan amilopektin yang didapat karena dengan adanya tambahan waktu maka terjadinya kontak antara reaktan yang mengakibatkan hidrolisis dari reaktan menjadi produk akan semakin sering terjadi (Mastuti dan Setyawardhani, 2010). Hidrolisis pati dengan asam akan lebih mudah memutus rantai pada bagian amorf daripada kristalin karena daerah amorf tersusun lebih renggang sedangkan daerah kristalin lebih rapat.
Bagian amorf yang tersusun atas titik percabangan (ikatan α-D-1,6) dari amilopektin mudah mengalami hidrolisis oleh asam (Wurzburg, 1989). Terputusnya titik
percabangan dari rantai molekul amilopektin (fraksi bercabang) pada daerah amorf mengakibatkan meningkatnya fraksi linear pati (amilosa) rantai pendek (Faridah dkk., 2011).
Analisa FT-IR
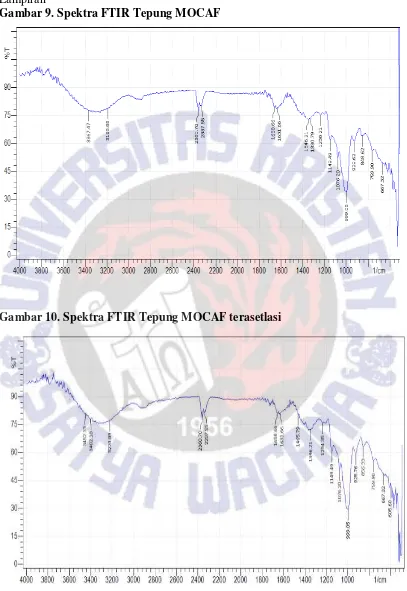
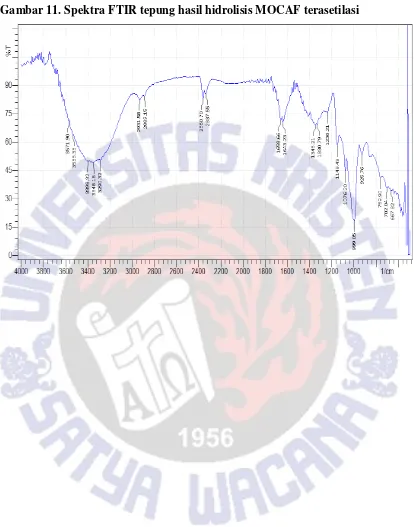
Spektra FTIR dari tepung MOCAF, MOCAF terasetilasi dan tepung MOCAF terasetilasi hasil hidrolisis disajikan pada Lampiran Gambar 9, 10, dan 11. Pada ketiga spektra, terlihat beberapa puncak gugus fungsiyang merupakan karakteristik dari pati, misalnya saja gugus fungsi O-H (stretchingatau pita uluran) antara 3000-3600 cm-1, C-H stretchingantara 2700-3300 cm-1, O-H(bending atau pita tekukan) antara 1200-1500 cm-1, C-H bending antara 1300-1500cm-1, dan C=O, C-Cstretchingantara 800-1300 cm
-1
(Muljana et al., 2010; Shogren,2003; Xu et al., 2004).
Adapun bilangan gelombang dan gugus fungsi beserta senyawa pada setiap sampel tepung berdasarkan hasil pemindaian spektra FTIR dapat dilihat pada Tabel 6
.Tabel 6. Hasil pemindaian spektra IR menunjukan adanya perubahan intensitas peak
dalam setiap perlakuan.
Sampel Bilangan gelombang (cm-1 ) Gugus Fungsi
MOCAF 3193,88 O−H
Berdasarkan hasilpenelitian tentang studi kinetika hidrolisis asam amilosa dan amilopektin tepung MOCAF terasetilasi dapat disimpulkan bahwa:
1. Kinetika reaksi hidrolisis MOCAF terasetilasi mengikuti orde nol semu. Kecepatan hidrolisis amilosa dan amilopektin akan meningkat seiring dengan peningkatan suhu reaksi dengan konstanta lajutertinggi pada suhu 40˚C.
14
hidrolisis mocaf terasetilasi 5% dan 10% berturut-turut adalah 34,32352 dan 14,42036 kJ.mol-1.K-1.
3. Pemindaian FTIR (Fourier Transform Infra Red) pada sampel tepung menunjukkan adanya gugus fungsi dominan yaitu C=O , C-O-C, dan O-H
SARAN
Berdasarkan penelitian yang sudah dilakukan, untuk penelitian selanjutnya perlu dilakukan penelitian mengenai daya cerna tepung MOCAF terasetilasi secara enzimatis. UCAPAN TERIMAKASIH
Kami mengucapkan terimakasih kepada Universitas Kristen Satya Wacana yang telah membiayai pembelian standar amilosa dan amilopektin.
DAFTAR PUSTAKA
Anugrahini, S.F.A., Ismuyanto, B., Indahyanti, S. 2013. Kinetika Reaksi Hidrolisis Pati Biji Durian (Durio zibethinus Murr.) Menjadi Glukosa Dengan Variasi Temperatur Dan Waktu. Kimia Student Journal. 2 (1): 344-351.
Belitz, H. D. and Grosch, W. 1999. Food Chemistry. Second Edition. Berlin: Springer Verlagg.
Bello-Perez, L.A., Agama-Acevedo, E., Zamudio-Flores, P. B., Mendez-Montealvo, G., andRodriguez-Ambriz, S. 2010. Effect of Low and High Acetylation Degree In The Morphological, Physicochemical And Structural Characteristics Of Barley Starch. Journal ofFood Science and Technology. 43(9): 1434- 1440.
Bej, B., Basu, R.K., and Ash,S.N. 2008. Kinetic Studies on Acid Catalysed Hydrolysis of starch. Journal of Scientific & Industrial Reasearch. 67: 295 – 298
Chang, R. 2005 .Kimia Dasar: Konsep-Konsep Inti Jilid1. Jakarta: Erlangga.
Chung, J., Jeong, Y.H., and Lima, T.S. 2003. Effects of Acid Hydrolysis And Defatting On Crystallinity And Pasting Properties Of Freeze-Thawed High Amylose Corn Starch. Journal of Carbohydrate Polymers. 54: 449–455.
Faridah, D.N., Fardiaz. D., Andarwulan, N., danSunarti, T.C. 2011. Perubahan Struktur Pati Garut (Maranta Arundinaceae) sebagai Akibat Modifikasi Hidrolisis Asam, Pemotongan Titik Percabangan Dan Siklus Pemanasan-Pendinginan.
Fleche, G. 1985.Chemical Modification and Degradation of Starchin G.M.A. Van Beynum dan J.A. Roels, ed. Starch conversion technology.London: Applied Science Pub.
Husodo, S.Y., 2004. Pertanian Mandiri. Jakarta : Penerbar Swadaya.
Hustiany, R. 2006. Modifikasi Asilasi dan Suksinilasi Pati Tapioka Sebagai Bahan Enkapsulasi Komponen Flavor. DISERTASI. Bogor: Institut Pertanian Bogor. Jannah, M. A., Legowo, M. A., Pramono, B. Y. 2013. Total Bakteri Asam Laktat, pH,
Keasaman, Citarasa dan Kesukaan Yogurt Drink dengan Penambahan Ekstrak Buah Belimbing. Jurnal Aplikasi Teknologi Pangan. 3(2): 7-11
Lawal, O.S., Adebowale, K.O., and Oderinde, R.A. 2004. Functional Properties Of Amylopectin And Amylose Fractions Isolated From Bambarra Groundnut (Voandzeia Subterranean) Starch. African Journal of Biotechnology. 3: 399-404. Martono, Y., Danriani, L.D., dan Hartini., S. 2016. Pengaruh Fermentasi Terhadap
Kandungan Protein Dan Asam Amino Pada Tepung Gaplek Yang Difortifikasi Tepung Kedelai (Glycine max (L)). Agritech.36: 56-63.
Martono, Y. 2016. Proses Produksi Tepung Mocaf Terasetilasi sebagai Pengganti Tepung Terigu.Hibah Penelitian Perseorangan/ Kelompok Wajib. Salatiga: Universitas Kristen Satya Wacana
Mastuti, E. dan Setyawardhani,D.A. 2010. Pengaruh Variasi Temperature dan Konsentrasi Katalis Pada Kinetika Reaksi Hidrolisis Tepung Kulit Ketela Pohon. Ekuilibrium. 9(1): 23 – 27.
McWilliams M. 2001. Foods Experimental Perspective Starch. New Jersey:Prentice Hall.
Muin, R., Lestari, D., dan Sari, T.W. 2014. Pengaruh Konsentrasi Asam Sulfat Dan Waktu Fermentasi Terhadap Kadar Bioetanol Yang Dihasilkan Dari Biji Alpukat Roosdiana Muin*, Dwi Lestari, Tri Wulan Sari Jurnal Teknik Kimia 4 :20 Muljana, H., Picchioni, F., Heeres, H.J.,and Janssen, L. 2010. Green starchconversions:
Studies on starch acetylation in densified CO2. Carbohydrate Polymers. 82:
653-662
Parker, R. 2003.Introduction to Food Science. United States of America: Delmar, Thomson Learning
Shogren, R.L. 2003. Rapid preparation of starch esters by high temperature/pressure reaction. Carbohydrate Polymers.52: 319-326
16
Suryana, A. 2009.Tantangan dan Kebijakan Ketahanan Pangan Dalam Pemberdayaan Masyarakat Untuk Mencapai Ketahanan Pangan Dan Pemulihan Ekonomi (ed). Jakarta: Pusat Studi Kebijakan Pangan dan Gizi Agrindo Aneka Consult.
Triyani, P., Ishartani M., danRahadian, A. 2013. Kajian Karakteristik Fisikokimia Tepung Labu Kuning (Cucurbita Moschata) Termodifikasi Dengan Variasi Lama Perendaman Dan Konsentrasi Asam Asetat.Jurnal Teknosains Pangan. 1-10
Winarno, F.G. 2002.Kimia Pangan dan Gizi.Jakarta: PT. Gramedia Pustaka Utama. Wurzburg, O. B. 1995. Starch, Modified Starch And Dextrin.Proceeding Of Seminar In
Products Of The Corn Refining Industry. 223– 32
Winarti, C., Richana, N., Mangunwidajay, D., dan Sunarti, C.T. 2014. Pengaruh Lama Hidrolisis Asam Terhadap Karakteristik Fisiko-Kimia Pati. Jurnal Teknologi Industri Pertanian. 24(3): 218-225
Wuttisela, K., Shobsngob, S., Triampo, W., and Triampo, D. 2007. Amylase and Amylopectin Simple DeterminationIn Acid Hydrolyzed Tapioca Starch. Journal of Chemical Society. 53(3): 1665-1667
Lampiran
Gambar 9. Spektra FTIR Tepung MOCAF
18