Laporan Sintesis Organik dan Anorganik
Reaksi Esterifikasi
Pembuatan Senyawa Metil Ester
Pembimbing : Iwan Ridwan, ST., MT.
Praktikan :
Kelompok VIII
Yuliana Nur Amanah 161411061
Yurike Dwiayu Rahmaningsih 161411062
Yuzvan Fauzi Darmawan D. 161411063
Zayyin Kamil Biliman 161411064
Kelas IB - TK
Tanggal Praktikum : 18 Mei 2017
Tanggal Penyerahan Laporan : 26 Mei 2017
JURUSAN TEKNIK KIMIA
Laporan Sintesis Senyawa Organik
I. Tujuan Percobaan :
1. Membuat senyawa metil ester.
2. Mengerti bahwa laju reaksi esterifkasi dipengaruhi oleh faktor-faktor antara
lain, suhu, konsentrasi, katalis, dan waktu.
3. Melakukan pengujian terhadap produk metil ester sesuai dengan persyaratan
mutu biodiesel Indonesia SNI-04-7182-2006.
II. Dasar Teori : A. Esterifikasi
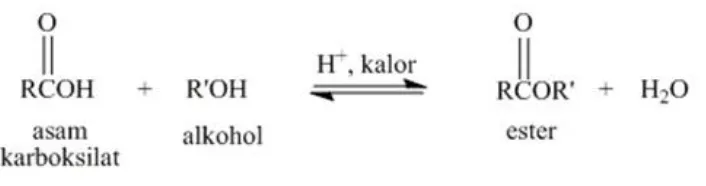
Reaksi esterifikasi adalah reaksi pembentukan ester dengan cara merefluks
sebuah asam karboksilat bersama sebuah alkohol dengan katalis asam. Asam yang
digunakan sebagai katalis biasanya adalah asam sulfat. Pembentukan ester melalui
asilasi langsung asam karboksilat terhadap alkohol, seperti pada esterifikasi
Fischer lebih disukai ketimbang asilasi dengan anhidrida asam ( atom yang
rendah) atau asil klorida (sensitif terhadap kelembapan). Kelemahan utama asilasi
langsung adalah konstanta kesetimbangan kimia yang rendah. Hal ini harus diatasi
dengan menambahkan banyak asam karboksilat, dan pemisahan air yang menjadi
hasil reaksi. Pemisahan air dilakukan melalui distilasi Dean-Strak atau
penggunaan saringan molekul.
Ester adalah campuran organik dengan simbol R’ yang menggantikan suatu atom hidrogen atau lebih. Ester juga dibentuk dengan asam yang tidak tersusun teratur; sebagai contoh, dimetil sulfat yang juga disebut “asam belerang, dimethyl ester” (Anonim, 2006).
Esterifikasi adalah reaksi pengubahan dari suatu asam karboksilat dan
alkohol menjadi suatu ester dengan menggunakan katalis asam. Reaksi ini juga
sering disebut esterifikasi Fischer. Ester adalah suatu senyawa yang mengandung
gugus -COOR dengan R dapat berbentuk alkil maupun aril. Suatu ester dapat
dibentuk dengan reaksi esterifikasi berkatalis asam. Reaksi esterifikasi merupakan
Gambar 1. Reaksi esterifikasi merupakan reaksi dapat balik (reversible).
Laju esterifikasi suatu asam karboksilat bergantung terutama pada halangan
sterik dalam alkohol dan asam karboksilatnya. Kuat asam dari asam karboksilat
hanya memainkan peranan kecil dalam pembentukan ester. Untuk alasan sterik,
urutan reaktivitas alkohol untuk reaksi esterifikasi adalah metanol > alkohol 1º >
alkohol 2º > alkohol 3º.
Variabel yang berpengaruh pada reaksi esterifikasi yaitu:
1. Suhu
Hal ini di karenakan sifat dari reaksi eksotermis, dan suhu dapat
mempengaruhi harga konstanta kecepatan reaksi.
2. Perbandingan zat pereaksi
Dikarenakan sifatnya yang reversible,maka salah satu perekatan harus di
buat berlebih agar optimal saat pembentukan ester.
3. Pencampuran
Dengan adanya pengadukan pada saat pencampuran,molekul-molekul
pereaktan dapat mengalami tumbukan yang lebih sering sehingga reaksi
dapat berjalan secara optimal.
4. Katalis
Adanya katalisator dalam reaksi dapat mempercepat jalannya suatu reaksi.
Kereakifan dari katalis bergantung dari jenis dan konsentrasi yang
digunakan.
5. Waktu reaksi
Jika waktu bereaksi lama maka kesempatan molekul-molekul pertumbukan
a. Sifat Laju Reaksi Esterifikasi
Laju reaksi esterifikasi sangat dipengaruhi oleh struktur molekul reaktan
dan radikal yang terbentuk dalam senyawa antara. Data tentang laju reaksi serta
mekanismenya disusun berdasarkan karakter kinetiknya, sedangkan data tentang
perkembangan reaksi dinyatakan sebagai konstanta kesetimbangan. Secara umum
laju reaksi esterifikasi mempunyai sifat sebagai berikut.
1. Alkohol primer bereaksi paling cepat, disusul alkohol sekunder, dan paling
lambat alkohol tersier.
2. Ikatan rangkap memperlambat reaksi.
3. Asam aromatik (benzoat dan p-toluat) bereaksi lambat, tetapi mempunyai
batas konversi yang tinggi.
4. Makin panjang rantai alkohol, cenderung mempercepat reaksi atau tidak
terlalu berpengaruh terhadap laju reaksi.
b. Penggolongan Proses Esterifikasi
Sistem pemroses yang dirancang untuk menyelesaikan reaksi esterifikasi
dikehendaki untuk sedapat mungkin mencapai 100%. Oleh karena itu reaksi
esterifikasi merupakan kesetimbangan, maka konversi sempurna tidak mungkin
tercapai, dan sesuai informasi yang ada konversi yang dapat dicapai hanya sampai
98%. Nilai konversi yang tinggi dapat dicapai dengan ekses reaktan yang besar.
Proses esterifikasi secara umum harus diketahui untuk dapat mendorong
konversi sebesar mungkin. Secara umum ada tiga golongan proses, dan
penggolongan ini bergantung kepada volatilitas ester, yaitu :
1. Golongan 1
Dengan ester yang sangat mudah menguap, seperti metil format, metil
asetat, dan etil format, titik didih ester lebih rendah daripada alkohol, oleh karena
itu ester segera dapat dihilangkan dari campuran reaksi. Produksi metil asetat
dengan metode distilasi Bachaus merupakan sebuah contoh dari golongan ini.
Metanol dan asam asetat diumpankan ke dalam kolom distilasi dan ester segera
terakumulasi di dasar tangki dan selanjutnya dibuang. Ester dan alkohol
dipisahkan lebih lanjut dalam kolom distilasi yang kedua.
2. Golongan 2
Ester dengan kemampuan menguap sebaiknya dipisahkan dengan cara
menghilangkan air yang terbentuk secara distilasi. Dalam beberapa hal, campuran
terner dari alkohol, air dan ester dapat terbentuk. Kelompok ini layak untuk
dipisahkan lebih lanjut: dengan etil asetat, semua bagian ester dipindahkan
sebagai campuran uap dengan alkohol dan sebagian air, sedangkan sisa air akan
terakumulasi dalam sistem. Dengan butil asetat, semua bagian air dipindahkan ke
bagian atas dengan sedikit bagian dari ester dan alkohol, sedangkan sisa ester
terakumulasi dalam sistem.
3. Golongan 3
Dengan ester yang mempunyai volatilitas rendah, beberapa kemungkinan
timbul. Dalam hal butil dan amil alkohol, air dipisahkan sebagai campuran biner
dengan alkohol. Contoh proses untuk tipe seperti ini adalah pembuatan dibutil
ftalat. Untuk menghasilkan ester dari alkohol yang lebih pendek (metil, etil,
propil) dibutuhkan penambahan hidrokarbon seperti benzena dan toluena untuk
memperbesar air yang terdistilasi.dengan alkohol bertitik didih tinggi (benzil,
furfuril, b-feniletil) suatu cairan tambahan selalu diperlukan untuk menghilangkan
kandungan air dari campuran.
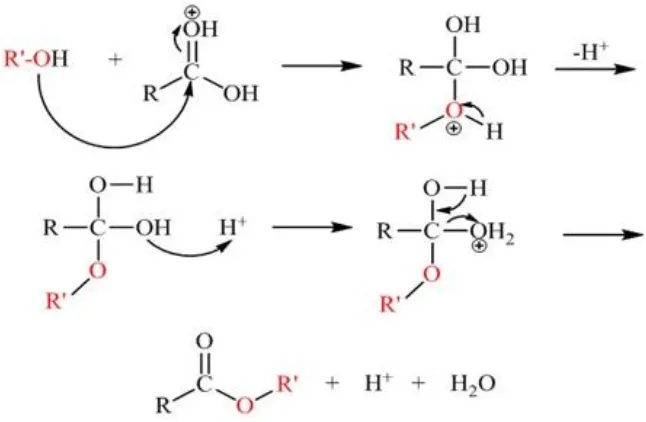
c. Mekanisme Reaksi Esterifikasi
Seperti banyak reaksi aldehida dan keton, esterifikasi asam karboksilat
berlangsung melalui serangkaian tahap protonasi dan deprotonasi. Oksigen
karbonil diprotonasi, alkohol nukleofilik menyerang karbon positif, dan eliminasi
Gambar 2. Mekanisme Reaksi Esterifikasi
Perhatikan bahwa dalam reaksi esterifikasi, ikatan yang terputus adalah
ikatan C-O asam karboksilat dan bukan -OH dari asam atau ikatan C-O dari
alkohol.
Reaksi esterifikasi bersifat reversibel. Untuk memperoleh rendemen tinggi
dari ester, kesetimbangan harus digeser ke arah sisi ester. Satu teknik untuk
mencapainya adalah menggunakan salah satu zat pereaksi yang murah secara
berlebihan. Teknik lain yaitu membuang salah satu produk dalam campuran reaksi
(misalnya dengan destilasi air secara azeotropik).
Dengan bertambahnya halangan sterik dalam zat antara, laju pembentukan
ester akan menurun. Rendemen esternya pun berkurang. Alasannya ialah karena
esterifikasi itu merupkan suatu reaksi yang bersifat dapat balik dan spesies yang
kurang terintangi (pereaksi) akan lebih disukai. Jika suatu ester yang meruah
(bulky) harus dibuat, maka lebih baik digunakan jalur sintesis lain, seperti reaksi
antara alkohol dengan suatu anhidrida asam atau klorida asam, yang lebih reaktif
daripada asam karboksilat dan dapat bereaksi secara tak dapat balik.
Ester fenil umumnya tidak dibuat dengan secara langsung dari fenol dan
asam karboksilat karena kesetimbangan cenderung bergeser ke sisi pereaksi
daripada produk. Ester fenil dapat diperoleh dengan menggunakan derivat asam
Reaksi esterifikasi Fischer adalah reaksi pembentukan ester dengan cara
merefluks sebuah asam karboksilat bersama sebuah alkohol dengan katalis asam.
Asam yang digunakan sebagai katalis biasanya adalah asam sulfat atau asam
Lewis seperti skandium (III) triflat.
Pembentukan ester melalui asilasi langsung asam karboksilat terhadap
alkohol, seperti pada esterifikasi Fischer lebih disukai ketimbang asilasi dengan
anhidrida asam (ekonomi atom yang rendah) atau asil klorida (sensitif terhadap
kelembapan). Kelemahan utama asilasi langsung adalah konstanta kesetimbangan
kimia yang rendah. Hal ini harus diatasi dengan menambahkan banyak asam
karboksilat, dan pemisahan air yang menjadi hasil reaksi. Pemisahan air dilakukan
melalui distilasi Dean-Stark atau penggunaan saringan molekul.
Mekanisme reaksi esterifikasi Fischer terdiri dari beberapa langkah:
1. Transfer proton dari katalis asam ke atom oksigen karbonil, sehingga
meningkatkan elektrofilisitas dari atom karbon karbonil.
2. Atom karbon karbonil kemudian diserang oleh atom oksigen dari alkohol,
yang bersifat nukleofilik sehingga terbentuk ion oksonium.
3. Terjadi pelepasan proton dari gugus hidroksil milik alkohol, menghasilkan
kompleks teraktivasi.
4. Protonasi terhadap salah satu gugus hidroksil, yang diikuti oleh pelepasan
molekul air menghasilkan ester.
d. Contoh Reaksi Esterifikasi
Contoh reaksi esterifikasi adalah reaksi antara asam asetat dan etanol
membentuk etil asetat. Reaksinya adalah :
Pembuatan Ester
1. Pembuatan ester dari alkohol dan asil klorida (klorida asam)
Jika kita menambahkan sebuah asil klorida kedalam sebuah alkohol,
maka reaksi yang terjadi cukup progresif (bahkan berlangsung hebat)
pada suhu kamar menghasilkan sebuah ester dan awan-awan dari asap
Sebagai contoh, jika kita menambahkan etanol klorida kedalam etanol,
maka akan terbentuk banyak hidrogen klorida bersama dengan ester cair
etil etanoat.
2. Pembuatan ester dari alkohol dan anhidrida asam
Reaksi-reaksi dengan anhidrida asam berlangsung lebih lambat
dibanding reaksi-reaksi yang serupa dengan asil klorida, dan biasanya
campuran reaksi yang terbentuk perlu dipanaskan.
Contoh etanol yang bereaksi dengan anhidrida etanoat sebagai sebuah
reaksi sederhana yang melibatkan sebuah alkohol.
Reaksi berlangsung lambat pada suhu kamar (atau lebih cepat pada
pemanasan). Tidak ada perubahan yang bisa diamati pada cairan yang
tidak berwarna, tetapi sebuah campuran etil etanoat dan asam etanoat
terbentuk.
3. Pembuatan ester dari asam karboksilat dan alkohol
Ester dihasilkan apabila asam karboksilat dipanaskan bersama alkohol
dengan bantuan katalis asam. Katalis ini biasanya adalah asam sulfat
pekat. Terkadang juga digunakan gas hidrogen klorida kering, tetapi
katalis-katalis ini cenderung melibatkan ester-ester aromatic (yakni
ester yang mengandung sebuah cincin benzen).
e. Kegunaan Ester
a. Sebagai pelarut, butil asetat (pelarut dalam industri cat).
b. Sebagai zat wangi dan untuk esterifikasi fenol sintesis aspirin
c. Berperan pada saat pembuatan biodiesel
B. Metil Ester
Metil ester merupakan ester asam lemak yang dibuat melalui proses
esterifikasi dari asam lemak dengan methanol. Pembuatan metal ester ada empat
macam cara, yaitu pencampuran dan penggunaan langsung, mikroemulsi, pirolisis
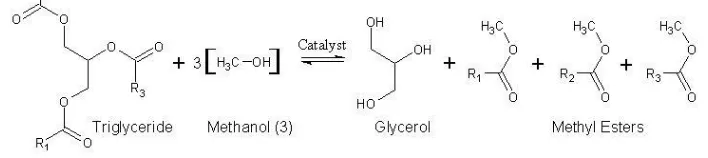
(thermal cracking), dan transesterifikasi. Namun, yang sering digunakan untuk
trigliserida (lemak atau minyak) dengan methanol untuk menghasilkan metil ester
dan gliserol.
Gambar 3. Rekasi Pembentukan Metil Ester
Metil ester dapat diperoleh dari hasil pengolahan bermacam-macam minyak
nabati, misalnya di jerman diperoleh dari minyak rapessed, di Eropa diperoleh
dari minyak biji bunga mataharprni dan minyak rapessed, di prancis dari itali
diperoleh dari minyak biji bunga matahari, di Amerika Serikat dan Brazil
diperoleh dari minyak kedelai, di Malaysia diperoleh dari minyak kelapa sawit,
dan di Indonesia diperoleh dari minyak kelapa sawit, minyak jarak pagar, minyak
kelapa, dan minyak kedelai (2,3,4). Selain minyak-minyak tersebut, minyak
safflower, minyak linsedd, dan minyak zaitun juga dapat digunakan dalam
pembuatan senyawa metal ester (4,5). Pada pengolahan minyak nabati di atas juga
di hasilkan gliserol sebagai hasil sampingnya.
Metil ester merupakan bahan baku dalam pembuatan biodiesel atau emollen
dalam produk kosmetika, sedangkan gliserol dapat digunakan sebagai bahan baku
dalam berbagai aplikasi industri seperti kosmetika, sabun, dan farmasi. Gliserol
yang diperoleh sebagai hasil samping pengolahan minyak nabati ini bukanlah
gliserol murni, melainkan gliserol mentah (crude glycerol), biasanya memiliki
kemurnian kira-kira 95%.
Minyak jelantah merupakan minyak nabati yang telah mengalami degradasi
kimia dan/atau mengandung akumulasi kontaminan-kontaminan di dalamnya.
Minyak ini dapat didaur ulang menjadi metil ester dengan reaksi transesterifikasi,
sehingga minyak jelantah yang sebelumnya merupakan limbah yang berbahaya
jika langsung dibuang ke lingkungan dapat menjadi suatu produk yang
mempunyai nilai ekonomis dan juga dapat mengurangi jumlah limbah minyak
metil ester adalah dapat direduksinya biaya operasional, karena harga minyak
jelantah pasti lebih murah daripada minyak bersih atau minyak baru.
Kekurangannya adalah komposisi asam lemak yang terkandung di dalam minyak
dapat berubah akibat pemanasan dan terikat dengan bahan makanan yang
digunakan pada proses penggorengan.
Senyawa metil ester dapat digunakan sebagai zat tambahan pada suatu
formulasi kosmetika, salah satu contohnya yaitu caprylic atau caprylic
triglyceride yang telah digunakan dalam formulasi kosmetika sebagai emolien.
Oleh karena itu, tidak menutup kemungkinan bahwa senyawa metil ester lainnya
juga dapat digunakan sebagai zat tambahan, baik sebagai emolien maupun fungsi
lainnya.
Metil ester yang diperoleh dari reaksi transesterifikasi dapat dimurnikan dan
ditetapkan kadarnya. Ada tiga metode analisis untuk menetapkan kadar metil ester
yaitu kromatografi gas, kromatografi cair kinerja tinggi, dan kromatografi lapis
tipis.
C. Reaksi Transesterifikasi dengan Katalis
Biodiesel dibuat melalui proses kimia yang disebut transesterifikasi.
Pembutan biodesel relatif sederhana dan mudah dikuasai dengan produk berupa
Fatty Acid Metyl Ester (FAME) yang melalui proses Transesterifikasi. Proses
Transesterifikasi adalah proses pertukaran antara gugus alkyl dari trigliserida
dengan gugus alkil dari Methanol (alcohol), sehingga terbentuk FAME dan
gliserin
Proses ini menghasilkan dua produk yaitu metil esters
(biodiesel)/mono-alkyl esters dan gliserin yang merupakan produk samping. Bahan baku utama
untuk pembuatan biodiesel antara lain minyak nabati, lemak hewani, lemak
bekas/lemak daur ulang.
Sedangkan sebagai bahan baku penunjang yaitu alkohol. Pada pembuatan
biodiesel dibutuhkan katalis untuk prosesesterifikasi. Produk biodiesel tergantung
pendahuluan dari bahan baku tersebut.Alkohol yang digunakan sebagai pereaksi
untuk minyak nabati adalah methanol, namun dapat pula digunakan ethanol,
isopropanol atau butyl, tetapi perlu diperhatikan juga kandungan air dalam alcohol
tersebut. Bila kandungan air tinggi akan mempengaruhi hasil biodiesel
kualitasnya rendah, karena kandungan sabun, ALB dan trigiserida tinggi.
Disamping itu hasil biodiesel juga dipengaruhi oleh tingginya suhu operasi
proses produksi, lamanya waktu pencampuran atau kecepatan pencampuran
alkohol. Katalisator dibutuhkan pula guna meningkatkan daya larut pada saat
reaksi berlangsung, umumnya katalis yang digunakan bersifat basa kuat yaitu
NaOH atau KOH atau natrium metoksida. Katalis yang akan dipilih tergantung
minyak nabati yang digunakan, apabila digunakan minyak mentah dengan
kandungan ALB kurang dari 2 %, disamping terbentuk sabun dan juga gliserin.
Katalis tersebut pada umumnya sangat higroskopis dan bereaksi membentuk
larutan kimia yang akan dihancurkan oleh reaktan alkohol. Jika banyak air yang
diserap oleh katalis maka kerja katalis kurang baik sehingga produk biodiesel
kurang baik. Setelah reaksi selesai, katalis harus di netralkan dengan penambahan
asam mineral kuat. Setelah biodiesel dicuci proses netralisasi juga dapat dilakukan
dengan penambahan air pencuci, HCl juga dapat dipakai untuk proses netralisasi
katalis basa, bila digunakan asam phosphate akan menghasil pupuk phosphat
(K3PO4).
Uji analisis yang dapat dilakukan adalah :
a. Uji Indeks Bias
Sin i
=
ɳ
2 = V1 Sin rɳ
1 V2b. Uji FFA
% FFA = mL KOH × N × Mr asam lemak × 100% Berat Sampel × 1000
c. Uji Konversi
d. Uji Massa jenis
ρ = m V
e. Uji Viskositas
Fs = 6 × 𝜋 ×
ɳ
× r × V
maksIII. Mekanisme Reaksi : A. Kondisi Operasi
Suhu : 60 - 65 °C
Rasio Bahan terhadap Reagen : Asam Oleat : Methanol = 4 : 1
Kecepatan Pengadukan : 125 – 150 rpm
Waktu Reaksi : 90 menit
B. Stoikiometri Reaksi
- Mol Asam Oleaat
m Asam Oleat = 0,895 g/mL × 100 mL
= 89,5 g
n Asam Oleat = m Asam Oleat =
89,5 g
= 0,3168 mol Mr Asam Oleat 282,5 g/mol
- Mol Metanol
m Metanol = 0,792 g/mL × 25 mL
= 19,8 g
n Metanol = m Metanol =
19,8 g
= 0,6188 mol Mr Metanol 32 g/mol
C18H34O2 + CH3OH → C19H36O2 + H2O mula-mula 0,3168 0,6188
reaksi 0,3168 0,3168
IV. Alat dan Bahan :
Alat : Bahan :
1. Reaktor
2. Penangas Air
3. Kondesnsor
4. Tabung CaCl2 5. Termometer
6. Motor pengaduk
7. Pengaduk Gelas
8. Selang Silikon 75 cm
9. Erlenmeyer 250 mL
10.Buret 50 mL
11.Pipet Ukur 5 dan 10 mL
12.Gelas Kimia 100, 250, dan 500 mL
13.Gelas Ukur 25, 50, dan 100 mL
14.Batang Pengaduk
15.Tabung Reaksi
16.Rak Tabung
17.Pipet Tetes
1. Asam Oleat
2. THF (tetrahidrofuran)
3. Metanol
4. Asam Sulfat pekat
5. KOH Alkoholis
6. Alkohol Netral
7. Phenolpthalein
V. Prosedur Kerja
Rangkai alat proses esterifikasi.
Maukan ke dalam reaktor Asam Oleat 100 mL dan 90 menit. Jaga suhu pada 60
°C.
Nyalakan penangas hingga suhu mencapai 60 °C.
Tambahkan H2SO4 sebanyak 3 mL.
Ambil 5 mL campuran sebagai sampel ke 0. 3. Tambahkan 3 tetes
indikator PP titrasi dengan KOH alkoholis. 4. Catat volume yang
tertera pada buret.
Setiap 15 menit, ambil sampel sebanyak 3 mL. lakukan uji indeks bias dan
FFA.
Matikan alat dan rapikan peralatan.
Lakukan perhitungan % FFA dan XA (konversi asam
lemak).
VI. Data Pengamatan : A. Perhitungan % FFA
% FFA = mL KOH × N × Mr asam lemak × 100% Berat Sampel × 1000
Konsentrasi KOH Alkoholis = 0,5 N
45 menit
B. Perhitungan Angka Asam
Bil Asam = (mL KOH sampel– mL KOH blanko) × NKOH × Mr KOH Berat Sampel
Konsentrasi KOH Alkoholis = 0,5 N
Volume Pentiter Blanko = 0,5 mL
15 menit
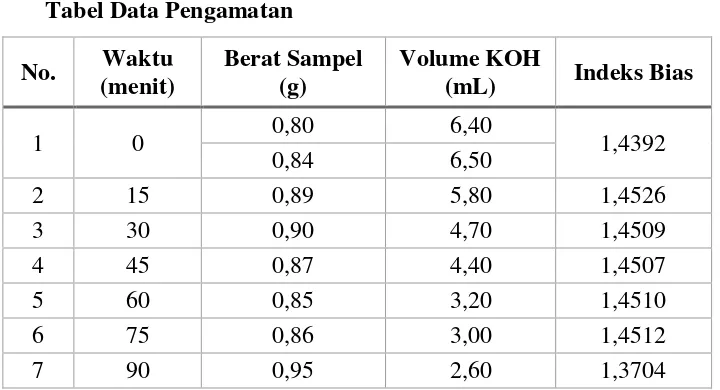
Tabel Hasil Pengolahan Data
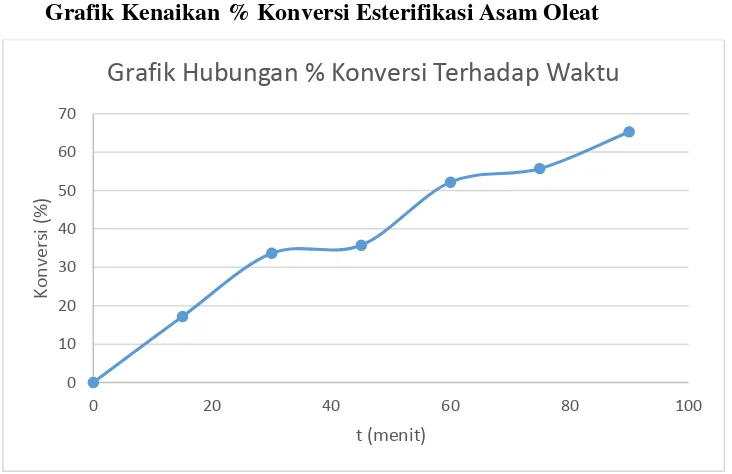
Grafik Kenaikan % Konversi Esterifikasi Asam Oleat
VIII. Keselamatan Kerja :
1. Gunakan Alat Pelindung Diri (APD) seperti jas laboraturium, sarung tangan,
masker dan safety googles.
2. Baca dan pahami job sheets, prosedur praktikum dan MSDS dari bahan – bahan yang digunakan.
3. Ikuti peraturan yang berada di laboraturium.
4. Bila terjadi kecelakaan dalam praktikum, jangan panik dan segera
mendapatkan pertolongan medis.
MSDS (Material Safety Data Sheet) A. Tetrahidrofuran (THF)
a. Sifat Fisika dan Kimia
Bentuk Fisik : Cairan
Titik Leleh : -108.3°C
Temperatur Kritis : 267°C
Specific Gravity : 0.8892 (Air = 1)
Tekanan Uap : 19.3 kPa (@ 20°C)
Densitas Uap : 2.5 (Udara = 1)
Kelarutan : Mudah larut dalam dietil eter, aseton. Larut
sebagian dalam air dingin.Kelarutan dalam air
sebesar 30%. Dapat dicampur dengan alkohol,
keton, ester, hidrokarbon dan eter.
b. Identifikasi Bahaya
Apabila mengenai kulit dan mata dapat menyebabkan iritasi.
Apabila terhirup dapat menyulitkan pernafasan dan apabila tertelan akan
menyebabkan keracunan.
c. Penanganan
Kontak Mata : Periksa dan lepaskan semua lensa kontak, bilas
mata dengan air mengalir minimal 15 menit, air
dingin dapat digunakan. Dapatkan penanganan
medis
Kontak Kulit : Bilas kulit dengan air mengalir. Tutupi kulit
yang teriritasi dengan obat merah. Lepaskan
pakaian yang terkontaminasi. Segera dapatkan
pertolongan medis.
Terhirup : Hirup udara segar, jika tak bernafas, berikan
alat bantu pernafasan dan jika sulit bernafas
berikan oksigen. Dapatkan pertolongan medis
Tertelan : Jangan memberikan apapun untuk dikonsumsi
kecuali dari pihak medis. Jangan berikan
apapun apabila korban dalam kondisi tidak
sadar. Apabila tertelan dalam kuantitas yang
B. Asam Sulfat
a. Sifat Fisika dan Kimia
Bentuk Fisik : Cairan
Bau : Tak berbau
Rasa : Asam Kuat
Berat Molekul : 98.08 g/mol
Warna : Tak Berwarna
PH : Asam
Titik Didih : 270°C
Titik Leleh : -35°C
Temperatur Kritis : -
Specific Gravity : 1.84 (Air = 1)
Tekanan Uap : -
Densitas Uap : 3.4 (Udara = 1)
Kelarutan : Mudah larut dalam air dingin dan etanol.
b. Identifikasi Bahaya
Sangat berbahaya jika terkena kulit (korosif, iritasi), tekena mata
(iritasi, korosif), tertelan dan terhitup. Uapnya dapat menyebabkan
menyebabkan kerusakan membrane mata, mulut dan jalur alat
pernafasan. Kontak kulit dapat meimbulkan luka bakar. Terhirup dari
uapnya dapat menyebabkan iritasi dalam alat pernafasan.
c. Penanganan
Kontak Mata : Periksa dan lepaskan semua lensa kontak, bilas
mata dengan air mengalir minimal 15 menit, air
dingin dapat digunakan. Dapatkan penanganan
medis
Kontak Kulit : Bilas kulit dengan air mengalir. Tutupi kulit
yang teriritasi dengan obat merah. Lepaskan
pakaian yang terkontaminasi. Apabila terkena
desinfektan dan berikan krim antibakteri.
Segera dapatkan pertolongan medis.
Terhirup : Dapatkan udara segar, berikan alat bantu
pernafasan, berikan oksigen jika sulit bernafas
dan dapatkan pertolongan medis.
Tertelan : Jangan memberikan apapun untuk dikonsumsi
kecuali dari pihak medis. Jangan berikan
apapun apabila korban dalam kondisi tidak
sadar. Apabila tertelan dalam kuantitas yang
banyak, segera panggil dokter.
C. Asam Oleat
a. Sifat Fisika dan Kimia
Bentuk Fisik : Cairan
Bau : Berbau seperti minyak kelapa
Rasa : -
Berat Molekul : 282.47 g/mol
Warna : Kuning Terang
PH : -
Titik Didih : 286.11°C
Titik Leleh : 16.3°C
Temperatur Kritis : -
Specific Gravity : 0.895 (Air = 1)
Tekanan Uap : -
Densitas Uap : 9.7 (Udara = 1)
Kelarutan : Larut dalam methanol, dietil eter, aseton. Tak
larut dalam air dingin. Larut dalam alkohol,
sebgian besar pelarut organik, benzene,
alkohol, karbon tetraklorida.
b. Identifikasi Bahaya
c. Penanganan
Kontak Mata : Periksa dan lepaskan semua lensa kontak, bilas
mata dengan air mengalir minimal 15 menit, air
dingin dapat digunakan. Dapatkan penanganan
medis
Kontak Kulit : Bilas kulit dengan air mengalir. Tutupi kulit
yang teriritasi dengan obat merah. Lepaskan
pakaian yang terkontaminasi. Segera dapatkan
pertolongan medis.
Terhirup : Hirup udara segar, jika tak bernafas, berikan
alat bantu pernafasan dan jika sulit bernafas
berikan oksigen. Dapatkan pertolongan medis
Tertelan : Jangan memberikan apapun untuk dikonsumsi
kecuali dari pihak medis. Jangan berikan
apapun apabila korban dalam kondisi tidak
sadar. Apabila tertelan dalam kuantitas yang
banyak, segera panggil dokter.
D. Kalium Hidroksida
a. Sifat Fisika dan Kimia
Bentuk Fisik : Padat (Butiran Padat)
Bau : Tak Berbau
Rasa : -
Berat Molekul : 56.11 g/mol
Warna : Putih
PH : 13 (Standar)
Titik Didih : 1384°C (Decomposition temperature)
Titik Leleh : 380°C
Temperatur Kritis : -
Specific Gravity : 2.044 (Air = 1)
Tekanan Uap : -
Kelarutan : Mudah larut dalam air dingin, air panas. Tak
larut dalam dietil eter.
b. Identifikasi Bahaya
Sangat berbahaya jika terkena kontak dengan kulit (korosif, iritasi),
dengan mata (iritasi, korosif), terirup dan tertelan. Jika terkena mata
dapat menyebabkan kerusakan kornea mata dan kebutaan. Bahan yang
terkena mata dapat dicirikan dengan mata merah, berair dan gatal.
Terkena kulit dapat menyebakan rasa panas dan peradangan. Jika
terhirup dapat menyebabkan iritasi dalam alat pernafasan yang dapat
dicirikan dari rasa terbakar, bersin dam batuk. Terhirup dalam jumlah
yang berlebih dapat menyebabkan kerusakan paru – paru dan kematian.
c. Penanganan
Kontak Mata : Periksa dan lepaskan semua lensa kontak, bilas
mata dengan air mengalir minimal 15 menit, air
dingin dapat digunakan. Dapatkan penanganan
medis
Kontak Kulit : Bilas kulit dengan air mengalir. Tutupi kulit
yang teriritasi dengan obat merah. Lepaskan
pakaian yang terkontaminasi. Apabila terkena
dampak yang serius, basuhlah dengan sabun
desinfektan dan berikan krim antibakteri.
Segera dapatkan pertolongan medis.
Terhirup : Hirup udara segar, jika tak bernafas, berikan
alat bantu pernafasan dan jika sulit bernafas
berikan oksigen. Dapatkan pertolongan medis
Tertelan : Jangan memberikan apapun untuk dikonsumsi
kecuali dari pihak medis. Jangan berikan
apapun apabila korban dalam kondisi tidak
sadar. Apabila tertelan dalam kuantitas yang
E. Metanol
a. Sifat Fisika dan Kimia
Bentuk Fisik : Cairan
Bau : Alkohol
Rasa : -
Berat Molekul : 32.04 g/mol
Warna : Tak Berwarna
PH : -
Titik Didih : 64.5°C
Titik Leleh : -97.8°C
Temperatur Kritis : 240°C
Specific Gravity : 0.7915 (Air = 1)
Tekanan Uap : 12.3 kPa (@ 20°C)
Densitas Uap : 1.11 (Udara = 1)
Kelarutan : Mudah larut dalam air dingin, air panas
b. Identifikasi Bahaya
Apabila mengenai kulit dan mata dapat menyebabkan iritasi.
Apabila terhirup dapat menyulitkan pernafasan dan apabila tertelan akan
menyebabkan keracunan. Paparan berlebih dapat menyebabkan
kematian.
c. Penanganan
Kontak Mata : Periksa dan lepaskan semua lensa kontak, bilas
mata dengan air mengalir minimal 15 menit, air
dingin dapat digunakan. Dapatkan penanganan
medis
Kontak Kulit : Bilas kulit dengan air mengalir. Tutupi kulit
yang teriritasi dengan obat merah. Lepaskan
pakaian yang terkontaminasi. Apabila terkena
dampak yang serius, basuhlah dengan sabun
desinfektan dan berikan krim antibakteri.
Terhirup : Hirup udara segar, jika tak bernafas, berikan
alat bantu pernafasan dan jika sulit bernafas
berikan oksigen. Dapatkan pertolongan medis
Tertelan : Jangan memberikan apapun untuk dikonsumsi
kecuali dari pihak medis. Jangan berikan
apapun apabila korban dalam kondisi tidak
sadar. Dapatkan pertolongan medis
F. Alkohol (Etanol)
a. Sifat Fisika dan Kimia
Bentuk Fisik : Cairan
Bau : Alkohol
Rasa : Tajam, Panas
Berat Molekul : 46.07 g/mol
Warna : Tak Berwarna
PH : -
Titik Didih : 78.5°C
Titik Leleh : -114.1°C
Temperatur Kritis : 243°C
Specific Gravity : 0.789 (Air = 1)
Tekanan Uap : 5.7 kPa (@ 20°C)
Densitas Uap : 1.59 (Udara = 1)
Kelarutan : Mudah larut dalam air dingin, air panas. Larut
dalam methanol, dietil eter, aseton.
b. Identifikasi Bahaya
Apabila mengenai kulit dan mata dapat menyebabkan iritasi. Tidak
korosif untuk mata dan kulit.
c. Penanganan
Kontak Mata : Periksa dan lepaskan semua lensa kontak, bilas
dingin dapat digunakan. Dapatkan penanganan
medis
Kontak Kulit : Bilas kulit dengan air mengalir. Tutupi kulit
yang teriritasi dengan obat merah. Lepaskan
pakaian yang terkontaminasi. Apabila terkena
dampak yang serius, basuhlah dengan sabun
desinfektan dan berikan krim antibakteri.
Segera dapatkan pertolongan medis.
Terhirup : Hirup udara segar, jika tak bernafas, berikan
alat bantu pernafasan dan jika sulit bernafas
berikan oksigen. Dapatkan pertolongan medis
Tertelan : Jangan memberikan apapun untuk dikonsumsi
kecuali dari pihak medis. Jangan berikan
apapun apabila korban dalam kondisi tidak
sadar. Dapatkan pertolongan medis
IX. Pembahasan : A. Yuliana Nur Amanah
Pada praktikum reaksi esterifikasi dilakukan pembuatan senyawa metil
ester. Raksi Esterifikasi adalah reaksi pembentukan ester dengan cara merefluks
asam karboksilat bersama sebuah alkohol dengan katalis asam. Pada proses ini
digunakan bahan baku Asam Oleat dan reagen methanol dengan perbandingan 4
: 1 dan menggunakan katalis asam yaitu asam sulfat pekat sebanyak 3% dari
jumlah bahan baku.
Pada proses tersebut digunakan THF (Tetrahidrofuran) yang merupakan
senyawa eter berfungsi untuk melarutkan asam oleat dan methanol. Katalis asam
sulfat berfungsi untuk mempercepat reaksi dan menurunkan kondisi operasi
dengan menurukan energi aktivasi, karena reaksi transesterifikasi tanpa katalis
baru akan terjadi pada suhu 250 °C.
Pengadukan sangat berpengaruh terhadap reaksi ini karena reaksi ini
membuat campuran reaksi yang maksimal. Pengadukan dilakukan dengan
kecepatan 125-150 rpm.
Selama proses reaksi berlangsung dilakukan pengambilan sampel setiap 15
menit, dari sampel tersebut kemudian dilakukan analisis FFA dan indeks bias.
Analis FFA secara berkala dilakukan untuk mengetahui perubahan nilai asam
lemak bebas yang terkandung didalam sistem tersebut.
Nilai FFA berkurang dengan bertambahnya waktu reaksi, karena semakin
lama semakin banyak asam lemak bebas yang bereaksi dengan methanol
membentuk metil ester. Nilai indeks bias di dalam sistem setelah dilakukan proses
esterifiskasi yaitu pada pengambilan sampel ke 15 menit, indeks bias yang didapat
sebesar 1,4526. Nilai tersebut sudah sesuai dengan indeks metil ester secara
teoritis yaitu 1,45.
Dari tabel hasil pengolahan data dapat dilihat bahwa nilai FFA semakin
berkurang dan % konversi semakin tinggi. Selisih % konversi paling tinggi terjadi
pada 15 menit pertama reaksi berlangsung. Semakin lama waktu reaksi semakin
banyak produk yang dihasilkan, hingga didapat kondisi
B. Yurike Dwiayu Rahmaningsih
Praktikum kali ini ditujukan untuk membuat metil ester dari bahan asam
oleat dan reagen metanol dengan perbandingan 4 : 1 (asam oleat 100 mL &
metanol 25 mL) serta katalis H2SO4 pekat sebanyak 3% (3 mL) dari volume asam oleat. Selain itu ditambahkan juga 1 mL Tetrahidrofuran ketika asam oleat dan
metanol sudah dicampurkan ke dalam reaktor. Campuran tersebut dipanaskan
selama 90 menit pada suhu 60°C. Sebelum dipanaskan, diambil 5 mL dari
campuran asam oleat dan methanol untuk diuji indeks bias dan FFA nya sebagai
sampel ke-0. Begitu juga setelah dipanaskan, diambil sampel ke 1, 2, 3, 4, 5, 6
masing masing sebanyak 5 mL untuk diuji indeks bias dan FFA nya setiap 15
menit sekali. Pengujian FFA dilakukan dengan cara menimbang 1 mL dari
sampel, ditambah 25 mL alkohol netral, dan dititrasi dengan KOH alkoholis. Dari
pengolahan data dan grafik yang dibuat dapat dikatakan bahwa semakin lama
waktu pengadukan dan pemanasan maka Bilangan asam dan %FFA nya semakin
oleat/minyak yang bereaksi dengan meanol dan terkonversi menjadi metil ester.
Hal ini dapat diperjelas dengan angka rata rata indeks bias sekitar 1,4371 yang
masuk ke dalam range indeks bias metil ester 1,435 – 1,450 .
C. Yuzvan Fauzi Darmawan D.
Pada praktikum kali ini, dilakukan percobaan pembuatan senyawa metil
ester dengan metode esterifikasi yaitu suatu rekasi antara asam karboksilat dengan
alcohol. Pada praktikum esterifikasi ini menggunakan senyawa asam oleat dengan
methanol.
Pada percobaan ini proses dilakukan dengan menggunakan penangas air
untuk menjaga suhu agar konstan dan tidak terlalu panas karena suhu yang
dibutuhkan dapat dicapai dengan penangas air. Pemanasan dan pengadukan
dilakukan selama 90 menit setelah suhu operasi tercapai. pada sintesis ini
ditambahkan THF yang berfungsi sebagai pelarut anatara asam oleat dengan
methanol dan digunakan asam sulfat pekat sebagai katalis. Katalis berfungsi untuk
mempercepat reaksi.
Dilakukan uji FFA dan indeks bias pada sampel yang diambil dari reaktor
secara berkala, yaitu setiap 15 menit selama 90 menit. Perlakuan ini dilakukan
dengan tujuan untuk mengetahui perubahan FFA dan indeks bias selama proses
berlangsung. Dapat diamati bahwa FFA berkurang dengan bertambahnya waktu
reaksi. Hal ini menunjukan asam lemak bebas didalam proses berkurang dan telah
bereaksi menjadi metil ester.
FFA yang didapat dari proses tersebut antara lain, pada t = 0 menit sebesar
110,96; pada t = 15 menit sebesar 91,89%; pada t = 30 menit sebesar 73,63%;
pada t = 45 menit sebesar 71,31%; pada t = 60 menit sebesar 53,08%; pada t =
75 menit sebesar 49,19%; dan pada t = 90 menit sebesar 38,59%. Sedangkan,
nilai indeks bias selama proses tersebut antara lain, pada t = 0 menit sebesar
1,4392; pada t = 15 menit sebesar 1,4526; pada t = 30 menit sebesar 1,4509; pada
t = 45 menit sebesar 1,4507; pada t = 60 menit sebesar 1,4510; pada t = 75 menit
D. Zayyin Kamil Biliman
Pada praktikum esterifikasi kali ini digunakan asam oleat sebagai bahan
baku dengan agent methanol. Metil dari methanol digunakan untuk disubstitusi
dengan H+ dari asam oleat sehingga didapatkan produk Metil Oleat dan H2O.
Perbandingan yang digunakan antara bahan baku (asam oleat) dengan agent
(metanol) adalah sebesar 4:1 dengan volume asam oleat yang digunakan sebanyak
100ml. Berdasarkan perbandingan tersebut maka methanol yang digunkan
sebanyak 25ml. Katalis yang digunakan pada praktikum kali ini adalah asam
sulfat. Asam sulfat ini berfungsi untuk menurunkan suhu reaksi dan meningkatkan
konversi metil oleat yang terbentuk. Asam sulfat yang digunakan sebanyak 3%
volume asam oleat atau sebanyak 3ml. Persamaan reaksi dari praktikum
esterifikasi adalah:
H2SO4
Asam Oleat (C18H34O2) + Metanol (CH3OH) → Metil Oleat (C19H36O2) + H2O Tetrahidrofuran digunakan dalam praktikum esterifikasi ini sebagai pelarut
dari asam oleat. Tetrahidrofuran yang digunakan adalah sebanyak 1ml. Faktor – faktor yang mempengaruhi esterifikasi adalah cepat lambatnya pengadukan, suhu
reaksi, banyaknya bahan baku dan agent yang digunakan serta banyaknya katalis.
Dari praktimkum esterifikasi didapatlah konversi metil oleat yang terbentuk
berdasarkan rentang waktu berikut. Pada t = 0 menit saat suhu reaksi ±60oC dan belum dimasukkannya asam sulfat kedalam reactor besarnya konversi sebesar 0%,
setelah sampel pada t = 0 menit diambil selanjutnya asam sulfat dimasukkan
kedalam reaktor. Kemudian pada t = 15 menit konversi yang didapat dari reaksi
terebut adalah sebesar 17,19%. Pada saat t = 30 menit konversi yang didapat
adalah sebesar 33,64%. Pada saat t = 45 menit konversi yang didapat sebesar
35,73%. Kemudian saat t = 60 menit konversi yang didapat sebesar 52,16%. Pada
t = 75 menit, konversi yang didapat adalah sebesar 55,67% dan pada rentang
waktu terakhir yaitu pada t = 90 menit konnversi dari metil oleat yang terbentuk
Berdasarkan hasil praktikum tersebut, rentang waktu antara 0 – 15 menit merupakan rentang waktu yang paling efektif dalam reaksi ini dibanding rentang
waktu yang lain karena konversi yang didapatkan adalah 17,19%. Jika dibanding
dengan rentang waktu antara 15 – 30 menit sebesar 33,64% - 17,19% = 16,45%. Sementara jika dibandingkan dengan rentang waktu 45 -60 menit dengan konversi
yang didapat sebesar 52,16% - 35,73% = 16,43%. Suhu reaksi angat berpengaruh
dalam proses ini. Berdasarkan referensi, suhu reaksi yang seharusnya adalah 60oC namun saat kami melakukan praktikum suhu reaksi yang digunakan adalah
sebesar 65oC karena suhu uap yang kami hitung suhunya. Dilebihkannya suhu 5oC dari suhu yang seharusnya dikarenakan detektor thermometer yang tidak dapat
menyentuh campuran dan dikhawatirkan akan membentur pengaduk yang
berputar apabila thermometer mengukur suhu campuran tersebut, atas dasar itulah
maka suhu uap yang diukur. Terjadinya perbedaan suhu antara uap dengan suhu
campuran yang bereaksi kami asumsikan sebesar 5oC karena suhu uap lebih kecil dari suhu reaksi sehingga dari asumsi tersebut apabila suhu uap 65oC maka suhu campuran lebih kurang sebesar 60oC. Atas dasar tersebut belum tepatnya suhu reaksi yang optimum mempengaruhi hasil konversi metil oleat yang terbentuk.
X. Kesimpulan :
Dari praktikum pembuatan senyawa metil ester dengan reaksi esterifikasi,
didapat :
- Reaksi yang terjadi pada pembuatan metil ester adalah reaksi
transesterifikasi.
- Semakin lama waktu pemanasan dan pengadukan nilai FFA semakin kecil
sementara % Konversi semakin besar, hal ini menunjukan semakin banyak
asam oleat yang terkonversi menjadi metil ester.
- % Konversi pada akhir proses adalah 65,22%.
XI. Daftar Pustaka :
No Name. No Date. http://www.suryadi.webege.com/web_d cuments/_presentasi -ayndri.pdf. Diakses 21 Mei 2017.
No Name. No Date. http://Students.chem.itb.ac.id/organic/kimia%20karbon.pdf. Diakses 21 Mei 2017.
Ria, Mesriah. 2016. “Reaksi Esterifikasi”. http://www.matadunia.id/2016/05/reak si-esterifikasi.html. Diakses 21 Mei 2017.
Lampiran
A. Foto Praktikum
Rangkaian Alat Proses Esterifikasi
Titik Akhir Titrasi FFA
B. Baku Mutu Biodiesel SNI-04-7182-2006