202
MAKALAH
PARALEL
PARALEL C
ISBN :978-602-73159-8
SINTESIS DAN KARAKTERISASI SENYAWA 4-ADIPOILBIS (1-
FENIL-3-METIL-5-PIRAZOLON) UNTUK DIGUNAKAN SEBAGAI
IONOFOR PADA ELEKTRODA SELEKTIF ION ND(III) DENGAN
MEMBRAN PTFE SEBAGAI PENDUKUNG
Husain Sosidi
1, Buchari
2, Indra Noviandri
21
Jurusan Kimia, Fakultas MIPA, Universitas Tadulako, Palu, Sulawesi Tengah, Indonesia
2
Jurusan Kimia, Fakultas MIPA, Institut Teknologi Bandung, Bandung Jawa Barat, Indonesia
1Chemistry Program, Faculty of Mathematic and Sains, Tadulako University, Central Sulawesi,
Indonesia
2Chemistry Program, Faculty of Mathematic and Sains, Technology Institute of Bandung, West
Java, Indonesia
*Untuk korespondensi: e-mail: husainasfah.chem@gmail.com
ABSTRAK
Telah berhasil disintesis dan dikarakterisasi senyawa 4-adipoilbis(1-fenitl-3-metil-5- pirazolon) (H2AdBP) untuk digunakan sebagai ionofor pada elektroda selektif ion Nd(III) (ESI- Nd) dengan membran PTFE sebagai pendukung. Sebelum digunakan membran PTFE terlebih dahulu direndam dalam larutan ionofor kloroform 1,5% selama 24 jam. Kinerja elektroda yang dipelajari adalah pengaruh pH dan konsentrasi larutan KCl sebagai penyangga kekuatan ion (ISA) terhadap beda potensial ESI H2AdBP-Nd. Variasi pH larutan diatur pada rentang 1 hingga 10 dengan menggunakan larutan HCl dan NaOH, sedangkan konsentrasi KCl divariasi antara 10-1 hingga 10-3 M. Rentang konsentrasi Nd3+ adalah antara 10-2 hingga 10-6 M. Penentuan potensial elektroda terbaik diperoleh pada pH 5 dengan konsentrasi ISA KCl 10-3 M, sensitivitas sebesar 20,52 ±0,2 mV/dekade dan waktu respon kurang dari 30 detik.
Kata kunci: H2AdBP, Elektroda Selektif Ion, Neodimium
ABSTRACT
The compound 4-adipoilbis(1-fenitl-3-methyl-5-pyrazolone) (H2AdBP) has been synthesized and characterized to be used as ionophores in ion-selective electrode Nd (III) (ESI- Nd) with a PTFE membrane as a support. Before use PTFE membranes are soaked in a solution of 1.5% chloroform ionophore for 24 hours. Electrode performance is studied the influence of pH and concentration of KCl as a buffer solution ionic strength (ISA) against potential difference H2AdBP ESI-Nd. Variations in pH of the solution is set in the range of 1 to 10 using HCl and NaOH, where as KCl concentration varied between 10 -1
M to 10-3M. Nd3+ concentration range is between 10-2 M to 10-6 M. Determining the best electrode potential obtained at pH 5 with a concentration of 10-3 M KCl as ISA, a sensitivity of 20.52 ± 0.2 mV / decade and a response time of less than 30 seconds.
203
SEMINAR NASIONAL KIMIA DAN PENDIDIKAN KIMIA IX (SN-KPK IX)
ISBN: 978-602-73159-8
PENDAHULUAN
Senyawa turunan pirazolon dapat disintesis dengan menggunakan berbagai jenis pereaksi seperti benzoil klorida [1], sebakoil klorida dan adipoil klorida [2]. Senyawa turunan pirazolon seperti 4adipoilbis (1-fenil-3-metilpirazolon) (H2AdBP) merupakan ligan yang telah banyak digunakan sebagai ekstraktan pada pemisahan ion LTJ secara ekstraksi pelarut dan secara solvent impregnated resin (SIR) Dari keberhasilan ligan tersebut pada memisahkan ion LTJ secara ekstraksi pelarut, maka perlu dipelajari kinerjanya pada metode potensiometri sebagai elektroda selektif ion (ESI) LTJ dengan membran polimer sintetik sebagai pendukung [3,5].
Dalam penelitian ini ESI-LTJ dengan senyawa turunan pirazolon sebagai ionofornya akan digunakan untuk mendeteksi ion logam Nd(III) dengan cara mensintesis ligan H2AdBP yang akan digunakan sebagai ionofor, mempelajari transport ion Nd(III) melalui membran berpendukung dengan H2AdBP sebagai ionofor, membuat sistem membran ESINd(III) menggunakan H2AdBP yang bagi penentuan Nd(III) secara potensiometrik dan mempelajari beberapa hal yang mempengaruhi terhadap kinerja ESI-Nd dalam berbagai komposisi analit [4].
Pada penelitian ini membran bagi keperluan pembuatan ESI-Nd(III) dibatasi dengan metode perendaman membran PTFE sebagai pendukung dalam larutan ionofor. Penguasaan metode sintesis senyawa H2AdBP yang dapat digunakan sebagai ionofor dan ekstraktan bagi
keperluan pemisahan ion LTJ, mendapatkan metode analisis secara potensiometri bagi penentuan ion Nd(III) yang memiliki akurasi, keberulangan, sensitivitas yang tinggi, mudah dalam pelaksanaan, rendah biaya dan dapat digunakan dilapangan. Senyawa H2AdBP disintesis dari 1-fenil-3-metil-5-pirazolon dengan 4-adipoil klorida dengan katalis kalsium hidroksida (Ca(OH)2) dalam pelarut dioksan.
Gambar 1. Struktur senyawa 4–adipoilbis (1-fenil-3-metil-5-pirazolon) (H2AdBP)
Elektroda bermembran selektif ion atau lebih dikenal dengan elektroda selektif ion (ESI) merupakan sensor elektrokimia yang digunakan untuk menentukan atkivitas atau konsentrasi ion berdasarkan pengukuran potensial membran [5,10]. Potensial membran tersebut berhubungan langsung dengan aktivitas atau konsentrasi ion melalui antarmuka membran sensitif saat ESI bersentuhan langsung dengan larutan ion target. Selain berfungsi sebagai sensor ionik, ESI juga mengukur aktivitasnya [6,8,9]. Sebagai contoh pengukuran ion Nd(III) secara potensiometrik menggunakan ESI-Nd mengandung dua elektroda pembanding yaitu internal dan eksternal. Sifat penting ESI seperti sensitivitas, linieritas respon, limit deteksi dan selektivitas terhadap ion lain serta waktu respon.
204
Sosidi, Sintesis dan Karakterisasi...ISBN: 978-602-73159-8
Ag/AgCl│KCl, Nd(III) ║ membran ESI-Nd║Nd (analit) │KCl (xM) │AgCl/Ag Elektroda pkerja Elektroda pembanding
Gambar 2. Notasi sel Elektroda Bermembran Selektif Ion-Nd
METODE PENELITIAN
Peralatan yang akan digunakan dalam penelitian ini antara lain peralatan sintesis ionofor melting point apparatus, spektrofotometer IR, NMR dan massa. pH meter, potensiometer, elektroda kerja dan elektroda pembanding Ag/AgCl beberapa jenis peralatan gelas lain.
Bahan yang akan digunakan untuk untuk sintesis H2AdBP seperti 1-fenil-3metil-5-pirazolon (PMP), adipoil klorida, dioksan sebagai pelarut, kalsium hidroksida (CaOH)2) sebagai katalis, membran politetrafluoroetilen (PTFE), garam Nd2O3, kawat Pt, kawat perak sebagai bahan elektroda Ag/AgCl, NaOH, HNO3, KCl, NaCl, HCl, aqua DM, aquades dan kertas saring Whatman 40. tabung teflon sebagai badan ESI-Nd.
Prosedur
Sebanyak 4,3820 gram PMP dilarutkan dalam dioksan 30 mL kemudian dimasukkan ke dalam labu. Pasang pada rangkaian refluks dan panaskan pada suhu 45 0C selama 20 menit. Tambahkan Ca(OH)2 sebanyak 5,0410 gram dan dioksan 20 mL, naikkan suhu menjadi 50 0C selama 30 menit. sebanyak 1,8 mL adipoil klorida dimasukkan tetes demi tetes sambil menaikkan suhu dari 50 0C sampai 120 0C, aduk selama 5 jam pada suhu 1200C. Setelah 5 jam dinginkan labu dengan melepaskan dari rangkaian refluks, setelah dingin tambahkan 200 mL HCl 2M dan
kocok selama 10 menit hingga terbentuk kristal. Kristal disaring dengan penyaring Buchner dan Whatman 40. Kristal coklat dicuci dengan aqua DM sampai netral. Keringkan padatan pada suhu 70 0C dengan oven dan karakterisasi dengan titik leleh, IR dan 1H NMR. Ionofor yang telah disintesis dan dikarakterisasi dilarutkan dengan kloroform dalam gelas kimia 50 mL. Membran PTFE direndam dalam larutan tersebut selama 24 jam dan setelah itu membran ditempelkan pada ujung elektroda tabung dengan menggunakan lem. Elektroda Ag/AgCl dibuat sebagai elektroda kerja dan sebagai elektroda pembanding. Elektroda Ag/AgCl yang digunakan sebagai elektroda kerja dimasukkan kedalam badan elektroda tipe tabung dari teflon yang telah dipasang membran yang mengandung ionofor. Elektroda pembanding Ag/AgCl dalam badan elektroda gelas dipasang paralel dengan elektroda kerja dan pengukuran diap dilakukan. Larutan stok Nd3+ 0,1M dibuat dengan melarutkan garam Nd2O3 dalam HNO3 dan aquades dengan perbandingan 1:1 sehingga diperoleh 100 mL larutan Nd3+ dengan konsentrasi 0,1M sebagai larutan sediaan (stock). Sebanyak 5 mL dari larutan sedian dipipet ke dalam labu takar 50 mL kemudian diencerkan sampai tanda dan diperoleh larutan Nd3+ 10-2M. Selanjutnya dibuat larutan yang sama dengan konsentrasi 10-2M sampai 10-6M dengan menggunakan larutan buffer (ISA) KCl sebagai pengencer.
205
SEMINAR NASIONAL KIMIA DAN PENDIDIKAN KIMIA IX (SN-KPK IX)
ISBN: 978-602-73159-8
3+
Sederetan larutan ini kemudian diukur beda potensialnya masing-masing dengan potensiometer Methrohm 692. Penentuan nilai beda potensial elektroda dilakukan sesuan dengan persamaan Nernst seperti berikut [7]. ENd = potensial lerutan Nd K = tetapan (intersep) R = tetapan T = Kelvin F = tetapan Faraday n = muatan ion
2,303 RT= Slop (sensitifitas elektroda) nF
HASIL DAN PEMBAHASAN
Hasil sintesis yang diperoleh merupakan serbuk yang berwarna kunig muda. Rendemen yang diperoleh 71%. Reaksi sintesis yang berlangsung pada suhu antara 500C sampai 1200C diperoleh seperti Gambar 2 dan stoikiometri reaksi pada Gambar 3 berikut
Gambar 3. Serbuk senyawa 4– adipoilbis(1fenil-3-metil-5-pirazolon) hasil
sintesis
Gambar 4. Stoikiometri reaksi senyawa 4–adipoilbis(1-fenil-3-metil-5-pirazolon) hasil sintesis Hasil karakterisasi yang dilakukan
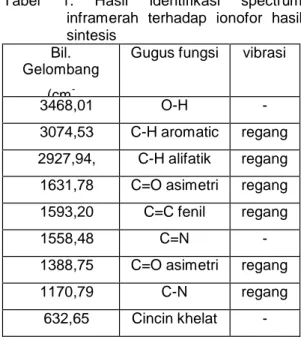
terhadap serbuk yang diperoleh dengan penentuan titik leleh dari H2AdBP adalah 1910C – 1940C yang mendekati titik leleh menurut literatur yaitu 1920C (Uzoukwu, 1998). Hasil elusidasi IR menunjukkan adanya ikatan C-H aromatis, CH2 alifatik, C=C fenil, cincin pirazolon, -CH3, C=O, C-N dan daerah sidik jari seperti pada pada tabel 1. Elusidasi spektrum 1H NMR pada Tabel 2 dan elusidasi spektrum 13C NMR dapat dilihat pada Tabel 3 berikut
Tabel 1. Hasil identifikasi spectrum inframerah terhadap ionofor hasil sintesis Bil. Gelombang (cm -1 )
Gugus fungsi vibrasi
3468,01 O-H -
3074,53 C-H aromatic regang 2927,94, C-H alifatik regang 1631,78 C=O asimetri regang 1593,20 C=C fenil regang
1558,48 C=N -
1388,75 C=O asimetri regang
1170,79 C-N regang
206
Sosidi, Sintesis dan Karakterisasi...ISBN: 978-602-73159-8
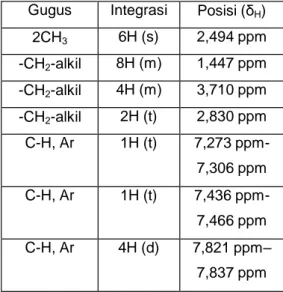
Tabel 2. Elusidasi struktur H2AdBP berdasarkan spectrum 1H NMR Gugus Integrasi Posisi (δH)
2CH3 6H (s) 2,494 ppm -CH2-alkil 8H (m) 1,447 ppm -CH2-alkil 4H (m) 3,710 ppm -CH2-alkil 2H (t) 2,830 ppm C-H, Ar 1H (t) 7,273 ppm- 7,306 ppm C-H, Ar 1H (t) 7,436 ppm- 7,466 ppm C-H, Ar 4H (d) 7,821 ppm– 7,837 ppm
Tabel 3.Elusidasi struktur H2AdBP berdasarkan spectrum 13C NMR Atom C Posisi δC 1 15,81 ppm 2 147,31 ppm 3 137,20 ppm 4 196,96 ppm 5 160,32 ppm 6,10 120,72 ppm 7,9 129,08 ppm 8 126,62 ppm 11 137,20 ppm 12,15 38,90 ppm 13,14 23,88 ppm
Pembuatan elektroda membrane H2AdBP ESI-Nd
Elektroda selektif ion Nd(III) (ESI-Nd) tipe tabung dibuat dari pipa Teflon dengan panjang 8 cm dan diameter 1,5 cm yang dilubangi dengan bor dengan diameter lubang 0,5 cm. Badan elektroda tipe tabung ini dibagi menjadi 3 yaitu tutup atas, badan utama dan tutup bawah. Pada ujung bawah diberi membrane sintesis dari PTFE yang
telah diimpregnasi (direndam) dalam larutan ionofor dengan spesifikasi diameter pori 0,2 μm, ketebalan 125 μm dan diameter 2 cm. Elektroda Ag/AgCl sepanjang 7 cm dipasang dalam badan elektroda dan 2 cm berada pada bagian luar yang disumbat dengan karet. Gambar elektroda selektif ion-Nd dapat dilihat seperti berikut.
Gambar 5. Konstruksi badan elektroda ESI H2AdBP-Nd
Pengaruh pH terhadap potensial ESI-Nd
Sederetan larutan Nd(III) dengan konsentrasi tetap 10-3M dengan variasi pH antara 1 sampai 10 yang diatur dengan menggunakan larutan asam dan basa. Larutan dengan pH tertentu diukur beda potensialnya dengan potensiometer menggunakan elektroda Ag/AgCl sebagai elektroda kerja dan elektroda pembanding. Kondisi pH optimal ini dicari untuk digunakan pada pengukuran beda potensial larutan agar nilai potensial larutan yang diperoleh optimal pada kondisi yang tidak mengendap. Oleh karena penentuan beda potensial elektroda banyak dipengaruhi oleh kondisi keasaman dan kekuatan ion dalam larutan, maka dilakukan optimasi pH larutan
207
SEMINAR NASIONAL KIMIA DAN PENDIDIKAN KIMIA IX (SN-KPK IX)
ISBN: 978-602-73159-8
analit untuk mengetahui pada pH berapa larutan dapat menghasilkan beda potensial yang baik dan masih memenuhi persamaan Nernts. Pada penelitian ini pengaturan pH dilakukan pada rentang 1 sampai 6 karena
larutan Nd(III) akan sangat mudah mengendap dalam suasana pH > 6. Hasil analisis beda potensial berdasarkan pH dapat dilihat pada Tabel 4 berikut
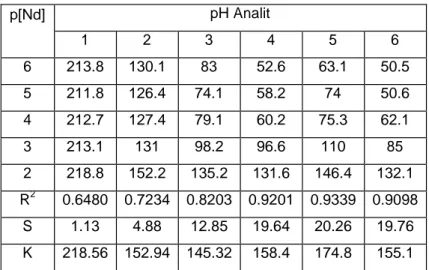
Tabel 4. Hasil analisis beda potensial ESI-Nd berdasarkan pH larutan
p[Nd] pH Analit 1 2 3 4 5 6 6 213.8 130.1 83 52.6 63.1 50.5 5 211.8 126.4 74.1 58.2 74 50.6 4 212.7 127.4 79.1 60.2 75.3 62.1 3 213.1 131 98.2 96.6 110 85 2 218.8 152.2 135.2 131.6 146.4 132.1 R2 0.6480 0.7234 0.8203 0.9201 0.9339 0.9098 S 1.13 4.88 12.85 19.64 20.26 19.76 K 218.56 152.94 145.32 158.4 174.8 155.1
Berdasarkan Tabel 4 diatas nampak bahwa beda potensial ESI-Nd menunjukkan sinsitivitas (S) elektroda meningkat dengan semakin naiknya keasaman (pH 5) kemudian turun kembali pada pH 6. Oleh karena itu pH 5 dianggap paling baik karena memiliki nilai koefisien korelasi ( R ) dan intersep yang terbaik masing-masing 0,9339 dan 174,8. Hal ini disebabkan karena pada pH 6 larutan mulai berubah menjadi keruh yang disebabkan oleh terjadinya endapan dari Nd3+ menjadi Nd(OH)3 sehingga ion Nd3+ sudah berkurang dalam larutan pada pH > 6. .
Pengaruh konsentrasi ISA terhadap beda potensial ESI H2AdBP-Nd
Kekuatan dan kestabilan ion dalam larutan ditentukan oleh adanya ion penyangga. Ion penyangga dalam analit disebut juga
sebagai ionic strength adjuste (ISA) yang berfungsi menstabilkan kekuatan ion dalam larutan. ISA adalah larutan ionik yang digunakan untuk menjaga agar analit tidak mengalami perubahan dalam larutan seperti pengendapan, oksidasi atau reduksi serta perubahan lainnya yang dapat menyebabkan terganggunnya harga potensial. Pada penelitian ini larutan ISA yang digunakan adalah larutan KCl dengan konsentrasi 10-4M sampai 10-1M. hasil penentuan beda potensial ESI-Nd pada larutan analit dengan kondisi pH 5 pada beberapa konsentrasi ISA dapat dilihat pada Tabel 5 berikut.
208
Sosidi, Sintesis dan Karakterisasi...ISBN: 978-602-73159-8
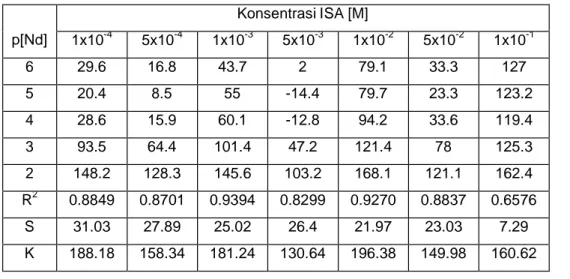
Tabel 5. Beda potensial ESI-H2AdBP-Nd dalam larutan ISA KCl
p[Nd] Konsentrasi ISA [M] 1x10-4 5x10-4 1x10-3 5x10-3 1x10-2 5x10-2 1x10-1 6 29.6 16.8 43.7 2 79.1 33.3 127 5 20.4 8.5 55 -14.4 79.7 23.3 123.2 4 28.6 15.9 60.1 -12.8 94.2 33.6 119.4 3 93.5 64.4 101.4 47.2 121.4 78 125.3 2 148.2 128.3 145.6 103.2 168.1 121.1 162.4 R2 0.8849 0.8701 0.9394 0.8299 0.9270 0.8837 0.6576 S 31.03 27.89 25.02 26.4 21.97 23.03 7.29 K 188.18 158.34 181.24 130.64 196.38 149.98 160.62
Dari Tabel 5 di atas diketahui bahwa konsentrasi ISA yang memberikan beda potensial yang baik adalah pada konsentrasi 10-3M. Hal ini dapat dilihat dari koefisien korelasi (R2) yang paling baik (0,9394) dan sensitivitas yang mendekati nilai ideal (25 mV/dekade) meskipun upper Nernstian (> 19,7 mV/dekade) dengan waktu respon 27 detik.
KESIMPULAN
Berdasarkan hasil yang telah diperoleh pada penelitian dapat dijelaskan bahwa kondisi pengukuran beda potensial elektroda selektif ion Nd(III) bermembran dengan menggunakan ionofor H2AdBP adalah pada pH 5 dengan menggunakan larutan penyangga (ISA) KCl dengan konsentrasi 10-3M. sensitivitas pengukuran yang diperoleh 20,26 mV/decade dengan waktu respon elektroda 27 detik (< 30 s).
UCAPAN TERIMA KASIH
Sebagai penghargaan yang tak terhingga kepada bapak Prof. Dr. Buchari
dan bapak Dr. Indra Noviandri dan Kementrian Riset dan Teknologi dan Pendidikan Tinggi serta Rektor Universitas Tadulako kami ucapkan terima kasih atas segala bantuan, bimbingan dan dana yang telah diberikan sampai penelitian ini selesai.
DAFTAR RUJUKAN
[1] Jensen B.S., 1959, The Synthesis of 1Phenyl-3-methyl-4-acylpyrazolone-5, Acta Chemica Scandinavica, 13.(8) pp. 1668-1670.
[2] Uzoukwu, B.A. and Okeke, S.I.1998,
Synthesis and spectroscopic studies of 4-Adipoyl- bis(1-phenyl-3-methyl pyrazolone-5 as a bis-(1,3-dioxane) J. Noth. Sci. Coun. 26.(3) pp. 229-233.
[3] Ganjali, M.R.,dan Pourjavid, M.R., 2006,
One Decade of Research on Ion Selective Electrodes in Iran (19962006)
J. Iran Chem. Soc. 4.(1) 1-29
[4] Gupta V.K., and Sharma R.A., 2009,
Comparative Studies of Neodymium(III) Selective PVC Membrane Sensors, Analytica Chimica Acta, (647) 66-71. [5] Zamani, H.A.,and Meghdadi ,S., 2011,
Neodymium(III)–PVC membrane sensor based on a new four dentate ionophore, Materials Science and Engineering: C 31, 588–592
209
SEMINAR NASIONAL KIMIA DAN PENDIDIKAN KIMIA IX (SN-KPK IX)
ISBN: 978-602-73159-8
[6] Atikah, 2004. Fenomena Transpor Ion Nitrat pada Eslektroda Selektif Ion Tipe Kawat Terlapis Membran Polivinil Klorida dengan Aliquot 336-Nitrat , Disertasi Program Pasca Sarjana Institut Teknologi Bandung
[7] Evans A., 1991, Potentiometry and Ion Selective Electrodes, John Wilet and Sons, London
[8] Zamani H.A., and Sahebnasagh S., 2013, Application of 1,2dimaleimidobenzene as a neutral ionophore in construction of a highly selective neodymium(III) liquid membrane electrode, Int. J. Electrochem. Sci. (8) 2722-2733.
[9] Chandra, S. and Sing, D.R., 2009,
Polymeric membrane neodymium(III) selective electrode based on
11,13diaza-4,7,12-trioxo- 2(3),8(9)dibenzoyl-cyclotetridecane-1,11-diene (DATODBCTD) Materials Science and Engineering A. 502.107-110
[10] Beena S., and Krishnapillai G.K, 2016,
PVC Membrane Sensor for Nd (III) Based on N1, N2-Bis (Salicylidine) Butane-1, 4 –Diamine, International Journal of Advanced Research in Chemical Science (IJARCS) Volume 3, Issue 2, pp 30-37