TUGAS PROSES INDUSTRI KIMIA POLISTIRENA
DISUSUN OLEH: KELOMPOK 7
Eko Noviariyono 21030112120003 Muqsit Bramantiya 21030112140142 Tommy Aji Susilo 21030112130082 Yuniar Luthfia L 21030112130091
JURUSAN TEKNIK KIMIA FAKULTAS TEKNIK UNIVERSITAS DIPONEGORO
ii KATA PENGANTAR
Puji syukur dipanjatkan kehadirat Tuhan Yang Maha Esa, atas limpahan rahmat, hidayat, karunia-Nya sehingga (kelompok 7) dapat menyelesaikan pembuatan Makalah Proses Industri Kimia yang berjudul “ POLISTIRENA” dengan baik.
Sedang proses studi pustaka dan penyusunan makalah ini, didapat bantuan dari berbagai pihak. Untuk itu diucapkan terima kasih kepada :
1. Ir. Slamet Priyanto, MS selaku dosen Proses Industri Kimia Jurusan Teknik Kimia Fakultas Teknik Universitas Diponegoro Semarang yang telah memberikan bimbingan dan pengarahan dalam pembuatan makalah ini.
2. Orang tua yang telah memberikan dorongan, semangat, fasilitas yang memadai untuk menyelesaikan makalah ini.
3. Semua pihak yang telah membantu secara langsung maupun tidak langsung selama penyusunan makalah ini.
Dalam penyusunan makalah ini, disadari masih banyak kekurangan. Oleh sebab itu saran dan kritik yang membangun dari para pembaca akan sangat berguna bagi perbaikan dan penyempurnaan makalah ini.
Semarang, 16 September 2013
iii DAFTAR ISI
HALAMAN JUDUL ... i
KATA PENGANTAR ... ii
DAFTAR ISI ... iii
BAB I PENDAHULUAN 1.1. Latar Belakang ... 1
1.2. Rumusan Masalah ... 1
1.3. Tujuan ... 1
BAB II TINJAUAN PUSTAKA 2.1. Definisi Polistirena... 2
2.2. Sejarah Polistirena ... 2
2.3. Sifat Polistirena ... 3
2.4. Kebutuhan Polistirena di Indonesia ... 4
2.5. Kapasitas Pabrik yang Telah Ada ... 5
2.6. Peluang Produk Polistirena di Indonesia ... 6
2.7. Lokasi Pendirian Pabrik Polistirena ... 7
2.8. Manfaat Polistirena ... 8
2.9. Reaksi Pembentukan Polistirena ... 10
2.10. Produksi Polistirena ... 11
2.11. Flowsheet Produksi Polistirena ... 16
2.12. Tinjauan Termodinamika ... 17
2.13. Tinjauan Kinetika... 20
BAB III PENUTUP 3.1. Kesimpulan ... 26
3.2. Saran ... 26
1 BAB I
PENDAHULUAN 1.1.Latar Belakang
Polistirena pertama kali diperkenalkan oleh Ostromislensky dari
Naugatuck Chemical Company pada tahun 1925. Pada saat yang hampir bersamaan I.C. Farbenindustrie juga mengembangkan polistirena yang berhasil dikomersialkan di Eropa. Pengembangan produk dan proses polistirena juga dikembangkan oleh Dow Chemical Company dan pertama kali dikomersialkan di Amerika Serikat pada tahun 1944.
Produk polistirena yang pertama kali diproduksi untuk dikomersialkan adalah homopolimer stirena yang juga dikenal sebagai polistirena kristal. Polistirena kristal ini juga dikenal sebagai General Purpose Polystyrene (GPP), yang lebih tahan panas daripada produk polimer thermoplastik lainnya. Perkembangan lebih lanjut dari polistirena ini adalah Expanable Polystyrene (EP). Produk polistirena lain yang tak kalah pentingnya adalah polistirena dengan modifikasi karet atau High Impact Polystyrene (HIP). Produk HIP ini bersifat tidak tembus cahaya, lebih keras dan lebih mudah dalam pembuatannya dibandingkan dengan produk polimer thermoplastik lainnya.
Polystyrene ( IUPAC Poly (1-phenylethane- 1,2-diyl)), disingkat berikut ISO Standard PS, adalah sebuah aromatik polimer yang dibuat dari aromatik monomer styrene, cairan hidrokarbon yang secara komersial diproduksi dari minyak bumi oleh di industri kimia. Polistirena adalah salah satu dari banyak digunakan sebagian besar jenis plastic .
Kegunaan dari polistirena ini cukup luas, antara lain untuk isolasi atau bahan pelapis pada kawat/kabel, peralatan rumah tangga dari plastik, botol,
furniture, mainan anak-anak, bagian dari refrigerasi, radio, televisi, AC, bahan pembuat kontainer, tempat baterai dan sebagainya. ( U.S. Patent, 1983).
Karena penggunaan polistirena sangat luas, maka disusunlah makalah ini untuk mengaji tentang karakteristik, cara pembuatan, kebutuhan, dan potensi pasar dari produk polistirena.
2 1.2.Rumusan Masalah
1. Apa rumus molekul dan rumus bangun polistirena? 2. Bagaimana sifat fisika dan kimia polistirena? 3. Berapa kebutuhan polistirena di pasar? 4. Bagaimana peluang pasar polistirena? 5. Apa manfaat polistirena?
6. Bagaimana reaksi pembentukan polistirena? 7. Bagaimana proses produksi polistirena?
1.3.Tujuan Penulisan
1. Mengetahui karakteristik dari polistirena
2. Mengetahui cara pembuatan dan reaksi pembentukan polistirena 3. Mengetahui potensi pasar dari polistirena
4. Mengetahui kondisi operasi optimal dan konversi maksimal pembuatan polistirena
5. Mengetahui reaktor dan diagram alir pembentukan polistirena BAB II
TINJAUAN PUSTAKA
2.1.Definisi Polistirena
Polistirena adalah sebuah polimer dengan monomer stirena, sebuah hidrokarbon cair yang dibuat secara komersial dari minyak bumi. Polimer ini merupakan plastik yang kuatdan murah, yang merupakan salah satu polimer golongan vinil (Storbl 2007).
Polistirena biasanya bersifat termoplastik padat pada suhu ruang, dan mencair padasuhu yang lebih tinggi. Secara struktur, polistirena merupakan rantai panjanghidrokarbon dengan gugus fenil yang berdekatan dengan setiap atom karbon (Storbl2007).
3 2.2.Sifat Polistirena
a. Rumus Molekul
Susunan kimiawi dari polistiren adalah hidrokarbon rantai panjang dengan setiap karbon lain yang terhubung ke kelompok fenil (nama yang diberikan kepada cincin aromatik benzena , ketika terikat untuk substituen karbon kompleks). Rumus kimia Polystyrene adalah (C8 H8) n,
itu berisi unsur-unsur kimia karbon dan hidrogen b. Rumus Bangun
c. Sifat Fisik
Sifat Fisis Polistirena
Kepadatan 1,05 g / cm 3
Kepadatan EPS 16-640 kg / m 3 Konstanta dielektrik 2.4-2.7
Listrik konduktivitas (s) 10 -16 S / m
Thermal konduktivitas (k) 0,08 W / (m ° K) Young’s modulus (E) 3000-3600 Mpa Kekuatan tarik (t) 46-60 Mpa
Perpanjangan putus 3-4%
Notch test 2-5 Kj / m 2
Suhu transisi gelas 95 ° C
Melting point 240 ° C
Vicat B 90 ° C [6]
4 Panas spesifik (c) 1,3 Kj / (kg K ·)
Penyerapan air (ASTM) 0.03-0.1
(http://bilangapax.blogspot.com/2011/02/polistirena.html)
d. Sifat Kimia
Inert : tidak bereaksi dengan kebanyakan substans
Larut dalam beberapa pelarut organic, terutama yang mengandung aseton
Perubahan ikatan rangkap karbon ke ikatan tunggal kurang reaktif Sangat mudah terbakar dengan bara api berwarna kuning
Pada oksidasi sempurna, hanya menghasilkan karbon dioksida dan uap air.
Fleksibel dan mudah dibentuk padatan karena kekuatan Van der Waal yang kuat, yang ada antara rantai hidrokarbon yang panjang.
2.3.Kebutuhan Polistirena di Indonesia
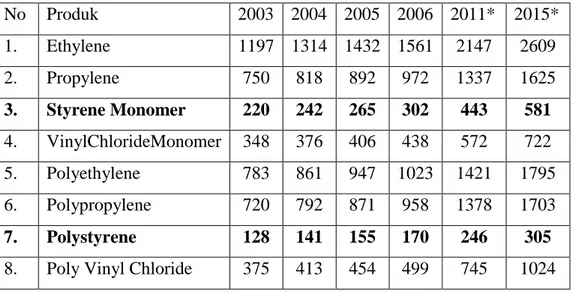
Perkembangan akan kebutuhan polistirena di Indonesia untuk beberapa tahun mendatang, diperkirakan akan mengalami peningkatan. Hal ini dapat dilihat pada tabel 1.4.1. Data kebutuhan monomer dan polimer di Indonesia berikut ini.
Tabel 1.4.1. Kebutuhan monomer dan polimer di Indonesia (1000 Ton/Thn) No Produk 2003 2004 2005 2006 2011* 2015* 1. Ethylene 1197 1314 1432 1561 2147 2609 2. Propylene 750 818 892 972 1337 1625 3. Styrene Monomer 220 242 265 302 443 581 4. VinylChlorideMonomer 348 376 406 438 572 722 5. Polyethylene 783 861 947 1023 1421 1795 6. Polypropylene 720 792 871 958 1378 1703 7. Polystyrene 128 141 155 170 246 305
5 (Ministry of Industry Republic of Indonesia, 2007) Tingginya kebutuhan polistirena di Indonesia berdampak pada jumlah impor polistirena yang terus meningkat tiap tahunnya.
Tabel 1.4.2. Data Impor Polistirena di Indonesia Tahun Kapasitas(Ton) 2002 6.182,44 2003 6.928,98 2004 7.393,503 2005 6.446,801 2006 5.532,667
(Sumber BPS Import tahun 2002-2006)
2.4.Kapasitas Pabrik yang Telah Ada
Dari produksi pabrik polistiren yang telah berdiri di Indonesia yaitu PT Polychem Lindo Inc, PT Pasific Indomas Plastik, dan PT Royal Chemical, perusahaan ini mulai berproduksi pada tahun 1985 dengan kapasitas produksi 21.500 ton per tahun. PT Pacific Indomas Plastic Indonesia, mulai beroperasi pada tahun 1993 berlokasi di Merak, memiliki kapasitas produksi 30.000 ton per tahun.
(www.businessenvironment.wordpress.com)
Tabel 1.5.1. Data Produksi Polistirena di Dunia
No Perusahaan Lokasi Kapasitas(Ton/th) 1. American Polymer USA 48.081
2. Chevron USA 21.724
3. Dow Chemical USA 171.458 4. Huntsman Chemical USA 181.437
5. BASF China 572.000
6. NOVA chemical China 413.000
6 8. Eni Chemical China 126.000
9. Taiwan Heqiao China 448.000
http://etd.eprints.ums.ac.id/3456/1/D500040017.pdf
2.5.Peluang Produk Polistirena di Indonesia
Dari data permintaan salah satu industri pembuatan sterofoam masa lalu untuk ketiga produk merupakan data yang akan digunakan untuk meramalkan jumlah permintaan pada masa yang akan datang. Data permintaan B-foam diperoleh dari laporan bulananan hasil penjualan dari bulan Januari 2010 sampai dengan Desember 2010. Untuk lebih jelas datanya dapat dilihat pada tabel di bawah ini.
Tabel 1.6.1. Data Permintaan B-foam Periode Januari 2010 – Desember 2010 PT. Beton Elemenindo Putra
No Periode WEB (Balok) WES (Lembaran) WEP (Pipa) 1 Januari 2010 527 19060 240 2 Februari 2010 318 24509 300 3 Maret 2010 388 23272 185 4 April 2010 321 27985 30 5 Mei 2010 367 25515 100 6 Juni 2010 432 30121 571 7 Juli 2010 382 34628 0 8 Agustus 2010 354 29628 15 9 September 2010 244 32569 1132 10 Oktober 2010 574 29057 20 11 November 2010 509 35645 237 12 Desember 2010 543 33286 0 Total 4959 345275 2830 http://elib.unikom.ac.id/files/disk1/532/jbptunikompp-gdl-rizkyrachm-26569-6-babiv.pdf
7 Dari data di atas menunjukan bahwa jumlah permintaan untuk sterofoam setiap bulan semakin meningkat. Hal tersebut meramalkan bahwa kebutuhan sterofoam pada masa yang akan datang akan semakin meningkat dan menunjukan masih ada peluang untuk mendirikan pabrik polistirena.
2.6.Lokasi Pendirian Pabrik Polistirena
Pemilihan lokasi pabrik merupakan hal yang sangat penting dalam perancangan suatu pabrik, karena hal ini menyangkut kelangsungan dan keberhasilannya, baik dari segi ekonomi maupun segi teknisnya. Pabrik polistirena ini direncanakan akan dibangun di daerah Merak, Jawa Barat dengan pertimbangan-pertimbangan di bawah ini :
1. Bahan Baku.
Bahan baku Ethylbenzene tersedia di daerah Merak, sehingga jarak yang dekat dengan sumber bahan baku akan menekan biaya transportasi dan memudahkan penyediaannya.
2. Pasar
Pabrik yang mempergunakan styrene sebagai bahan baku dan Jakarta sebagai pusat pasar jaraknya cukup dekat dengan Merak. Hal ini akan memudahkan dalam pemasaran produk styrene maupun polistirena.
3. Utilitas
Air sebagai salah satu kebutuhan proses tersedia dalam jumlah yang memadai di daerah Merak yang cukup dekat dengan pantai. Juga kebutuhan energi listrik tersedia dengan cukup dengan dibangunnya PLTU di Jawa Barat. Hal ini akan menunjang kelancaran operasional pabrik sehari-hari.
4. Transportasi
Tersedianya jalan tol Jakarta – Merak dan pelabuhan Tanjung Priok akan melancarkan pemasaran produk baik untuk pasar dalam negeri maupun untuk orientasi ekspor.
8 5. Tenaga Kerja
Kebutuhan tenaga kerja baik tenaga maupun pekerja biasa akan terpenuhi dengan banyaknya tenaga kerja di sekitar Merak maupun kota Jakarta.
6. Proses Produksi
Dalam proses produksi polistirena terjadi kehilangan berat bahan, tetapi karena kehilangan berat relatif kecil maka Merak yang dekat pasar dan sumber bahan baku tetap menguntungkan secara ekonomis.
7. Limbah dan Pengembangan Pabrik
Letak pabrik yang tidak berada di kota besar akan memudahkan dalam pengolahan limbahnya maupun dalam usaha perluasan pabrik khususnya dalam penyediaan tanah lokasi.
8. Pemerintah
Kebijakan pemerintah untuk menjadikan Merak, dan sekitarnya sebagai kawasan industri akan memudahkan dalam hal perijinan dan pengembangan pabrik.
2.7.Manfaat Polistirena
Polystyrene merupakan senyawa berbentuk Kristal bening yang mempunyai sifat elektris yang baik, derajat kekerasan yang tinggi, tahan terhadap panas, mudah dalam pewarnaan, permukaan yang halus dan low toxity.
Karena sifat-sifat seperti di atas maka polystyrene banyak digunakan sebagai:
9 b. Sebagai bahan isolator
c. Sebagai furniture
d. Sebagai bahan pengepakan
e. Peralatan rumah tangga, dll
10 1. Tahap Inisiasi
Proses inisiasi adalah proses pembentukan radikal bebas dari inisiator. (Billmayer, 1970). Reaksi inisiasi dipicu oleh Benzoyl peroxide yang ketika dipanaskan pada suhu 900 akan terpecah menjadi radikal carboxyl yang segera terdekomposisi menjadi radikal phenyl
Sebuah Radikal Phenyl akan masuk pada Styrene yang akan membentuk radikal Benzylic. Reaksi ini memulai pertumbuhan rantai polimer
2. Tahap Propagansi
Proses propagasi adalah proses pertumbuhan polimer sebagai akibat dari penggabungan monomer-monomer ke dalam rantai radikal aktif (Billmayer, 1970).
11 Proses propagasi dilanjutkan dengan proses terminasi yang merupakan proses penghentian propagasi (Billmayer, 1970).
Rantai ini akan terus memanjang dengan adisi ratusan hingga puluhan ribu unit styrene. Reaksi berantai iniakan berhenti ketika monomer habis.
2.9.Produksi Polistirena
1. Polimerisasi bulk (larutan)
Dalam industri umunya, polimerisasi bulk (larutan) disebut polimerisasi massa. Sebagian besar polistirena yang diproduksi sekarang ini menggunakan proses ini. Pada proses ini menggunakan sejumlah
solvent yang biasanya adalah monomer stirena itu sendiri dan Etil Benzena. Ada 2 jenis polimerisasi bulk, yaitu :
Polimerisasi bulk batch
Beberapa produsen polistirena masih menggunakan proses ini, dimana proses ini terdiri dari unit polimerisasi yang didalamnya terdapat tangki polimerisasi berpengaduk dengan konversi di atas 80%. Larutan polimer kemudian dipompa ke bagian finishing untuk devolatilisasi ataupun proses polimerisasi akhir dan grinding. ( U.S. Patent, 1983)
Polimerisasi bulk continuous
Proses ini merupakan proses pembuatan polistirena yang paling banyak digunakan. Ada beberapa jenis desain dimana beberapa diantaranya sudah mendapatkan lisensi. Secara umum proses ini terdiri dari satu atau lebih reaktor tangki berpengaduk (CSTR). CSTR ini biasanya diikuti oleh satu atau lebih reaktor yang didesain untuk menangani larutan yang kental (viskositas tinggi). Reaktor ini didesain untuk memindahkan panas baik secara langsung melalui koil maupun pendingin uap. Dengan menggunakan proses ini, konversi monomer stirena menjadi
12 polistirena dapat mencapai lebih dari 85% berat. Polimerisasi diikuti terjadinya devolatilisasi yang terus menerus. Devolatilisasi ini dapat terjadi melalui preheating dan vacuum flash chambers,
devoitizing extruders atau peralatan yang sesuai. Tingkat volatilitas dari 500 ppm stirena atau kurang dapat tercapai dengan peralatan khusus, meskipun polistirena yang umum dikomersialkan mempunyai tingkat volatilitas sekitar 2000 ppm stirena. ( U.S. Patent, 1983)
2. Polimerisasi Suspensi
Polimerisasi suspensi adalah sistem batch yang sangat popular untuk tahapan khusus pembuatan polistirena. Proses ini dapat digunakan untuk memproduksi kristal maupun HIP. Untuk memperoduksi HIP, stirena dan larutan karet diolah dengan bulk polymerized melalui fase
inverse. Kemudian disuspensikan ke dalam air untuk mendapatkan
suspense air dan minyak dengan menggunakan sabun atau zat pesuspensi. Kemudian butiran suspense ini dipolimerisasi lagi sampai selesai dengan menggunakan inisiator dan pemanasan bertahap. Fase air digunakan sebagai heat sink dan media perpindahan panas terhadap jaket yang dikontrol suhunya.
3. Polimerisasi Emulsi
Polimerisasi emulsi biasanya digunakan pada proses kopolimerisasi stirena dengan monomer atau polimer lain. Proses ini merupakan metode komersial yang jarang digunakan untuk memproduksi polistirena kristal atau HIP. Proses ini mempunyai persamaan dengan proses polimerisasi suspense kecuali bahwa butiran monomer yang digunakan dalam polimerisasi emulsi ini dalam ukuran mikroskopis. Air digunakan sebagai carrier dengan agen pengemulsi untuk memberikan partikel yang sangat kecil dan aktalis untuk mempercepat kecepatan reaksi.(Meyer,1984).
13 1. Polimerisasi bulk -bulk batch -bulk continous Prosesnya mudah. Kemurnian Produk. Alat-alat sederhana. Produk yang dihasilkan
lebih seragam.
Kemurnian produk tinggi. Pengontrolan suhu lebih
mudah. Sangat eksotermis. Waktu pengerjaan lama. Membutuhkan pengadukan dan alat recycle. 2. Polimerisasi Suspensi
Tidak ada kesulitan dengan panas polimerisasi. Ketel untuk proses
polimerisasi sederhana. Volatilitas dapat
dikurangi sampai pada tingkat yang rendah dengan pemilihan katalis dan suhu yang tepat.
Dimungkinkan adanya
kontaminasi dari air dengan agen penstabil.
3. Polimerisasi Emulsi
Prosesnya cepat dan tidak ada kesulitan dengan panas polimeriasi. Beberapa proses
polimerisasi yang tidak mungkin dilakukan dengan teknik lain tapi dengan mudah dilakukan dengan proses ini. Dapat diterapkan untuk
polimeriasi secara
Dimungkinkan terjadinya kontaminasi polimer dengan air dan agen pengemulsi. Berat molekul polimer tinggi untuk proses pembentukan yang cepat dengan
14
kontinyu. menggunakan
injeksi. Berdasarkan hasil pengamatan kelebihan dan kekurangan proses pembuatan High Impact Polystyrene diatas, maka pada pra rancangan pembuatan
High Impact Polystyrene ini digunakan proses bulk continuous.
Proses pembuatan High Impact Polystyrene secara berkelanjutan dilakukan dengan beberapa tahap proses, yaitu :
1. Tahap penyiapan bahan baku a. Stirena
Stirena monomer sebagai bahan baku utama disimpan dalam bentuk cair dalam tangki penyimpan (T-01) pada suhu 30Oc dan tekanan 1 atm, dialirkan ke dalam mixer 1 (M-01) untuk dicampur dengan arus recycle dengan menggunakan pompa sentrifugal P-01 dan selanjutnya dialirkan ke mixer 2 (M-02) yang sebelumnya dipanaskan terlebih dahulu oleh pemanas HE-01.
b. Etil Benzena
Etil Benzena sebagai pelarut disimpan dalam bentuk cair dalam tangki penyimpan (T-02) pada suhu 30Oc dan tekanan 1 atm, dialirkan ke mixer 1(M-01) dengan menggunakan pompa sentrifugal P-02 dan selanjutnya bersama stirena dan arus recycle dialirkan ke mixer 2 (M-02) yang sebelumnya dipanaskan terlebih dahulu oleh pemanas HE-01. c. Cis 1-4 polibutadiena
Cis 1-4 polibutadiena yang disimpan dalam bentuk padat dalam gudang (G-01) pada suhu 30Oc dan 1 atm, diangkut dengan menggunakan bucket elevator BE-01 menuju Hammer mill HM-01 untuk direduksi ukurannya dari 2,5 cm menjadi 10 μm, kemudian polibutadiena yang tidak memenuhi syarat dan yang melebihi ukuran dipisahkan di screner SC-01. Polibutadiena yang memenuhi syarat dikirim ke mixer 2 (M-02) dengan menggunakan belt conveyor BC-01, sedangkan yang melebihi ukuran akan menjadi limbah. Di mixer 2 (M-02) yang dilengkapi dengan pengaduk, polibutadiena dicampur dengan
15 bahan baku lainnya. Supaya polibutadiena terlarut sempurna, maka mixer 2 (M-02) dioperasikan pada suhu 105Oc dan tekanan 1 atm dengan waktu tinggal 4,5 jam. (US Patent,1983)
2. Tahap reaksi
Campuran stirena monomer, Etil Benzena, Polibutadiena dan inisiator Benzoil Peroksida dimasukkan ke dalam reaktor (R-01) yang berupa tangki berpengaduk. Reaksi yang terjadi adalah reaksi eksotermis sehingga diperlukan pendingin dengan menggunakan jaket pendingin. Sebagai pendingin digunakan air yang masuk pada suhu 30oC dan keluar pada suhu 45oC. Kondisi operasi dalam reaktor dipertahankan pada suhu 137oC dan tekanan 1 atm selama 7,6 jam untuk mencapai konversi sebesar 85% (US Patent,1976).
3. Tahap akhir
Produk yang keluar dari reaktor berbentuk slurry dengan menggunakan pompa sentrifugal P-05 dialirkan ke devolatilizer yang dioperasikan pada suhu 150oC dan tekanan vacuum 0,5 atm untuk memisahkan sisa pereaktan dengan produk High Impact Polystyrene
berdasarkan titik didihnya. Sisa pereaktan yang berupa Stirena monomer, Etil Benzena dikondensasikan di kondensor (C-01) dan hasil kondensasi direcycle kembali sebagai bahan baku.
Produk High Impact Polystyrene yang telah terpisah dari sisa pereaktan dengan suhu 150oC didinginkan terlebih dahulu di cooler (C-02) sampai suhu 30oC. Kemudian dimasukkan ke Rotary Dryer (RD) untuk dikeringkan dengan efisiensi 72%. Selanjutnya dalam pellet mill (PM) strand dipotong menjadi bentuk pellet, kemudian HIP akan di teruskan ke
screner (SC-02) untuk mendapatkan keseragaman ukuran dan selanjutnya HIP akan dimasukkan ke dalam unit pengantongan pada gudang (G–03).
16 a. GPPS Flowsheet
b. EPS Flowsheet
c. HIPS Flowsheet
17 Untuk menentukan sifat reaksi apakah berjalan secara eksotermis atau endotermis, maka perlu pembuktian dengan menggunakan panas pembentukan standar (ΔH°f) pada tekanan 1 atm dan suhu 298,15 K dari reaktan dan produk.
C6H5CH2CH3C6H5CHCH2+H2
ΔH°freaksi = ΔH°fproduk - ΔH°freaktor
ΔH°f C6H5CHCH2 = -69.87 kJ/mol
ΔH°f H2 = 0 kJ/mol
ΔH°fC6H5CH2CH3 = -12.5 kJ/mol
ΔH°freaksi = ΔH°fproduk - ΔH°freaktor
= (-69.87+0) – (-12.5) ΔH°freaksi = -57.37 kJ/mol
Dari perhitungan ΔH°f reaksi di atas, maka dapat disimpulkan bahwa
reaksi pembentukan stirena bersifat eksotermis.
Reaksi bersifat dapat balik (reversibel) atau searah (irreversibel) dapat ditentukan secara termodinamika, yaitu berdasarkan persamaanVan’t Hoff = (2.1) Dengan, = -RT ln K (2.2) Sehingga, = (2.3)
Jika ΔH° merupakan perubahan enthalpy standar (panas reaksi) dan dapat diasumsikan konstan terhadap suhu, maka persamaan (2.3) dapat diintegralkan menjadi :
ln = - ( - ) (2.4)
data data energi Gibbs (Gibbs heat of formation) Fe2O3
-69.87 Stirena EtilBenzen
18 ΔG°fC6H5CHCH2 = -67.4 kJ/mol
ΔG°fH2 =0 kJ/mol
ΔG°fC6H5CH2CH3 = 130.7 kJ/mol
ΔGReaksi = ∑ΔG298 produk - ∑ΔG298 reaktan
ΔG°f total =(-67.4+0) – (130.7)
= -198.1 kJ/mol
Konstanta kesetimbangan reaksi standart pada suhu 298,15 K dapat dihitung, dengan: RT G K exp K K mol kJ mol kJ K o o 15 , 298 314 . 8 1 . 198 exp
0.0799
exp K 0832 . 1 KHarga K yang sangat besar menunjukkan menunjukkan bahwa reaksi pembentukan polistirena bersifat searah (irreversibel).
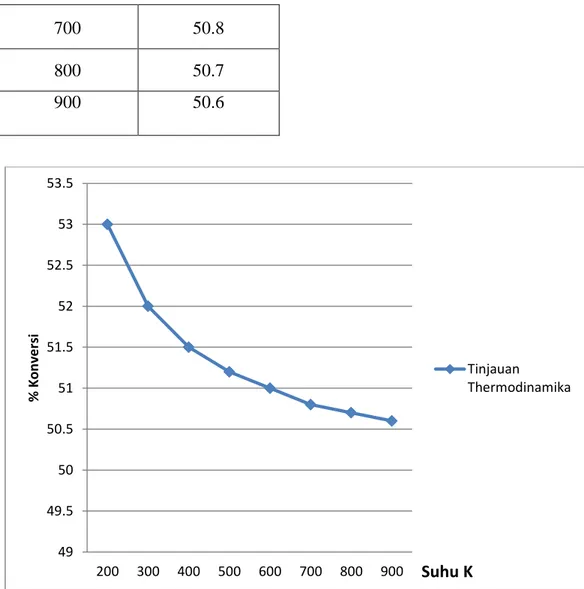
Berikut ini grafik hubungan suhu vs % konversi yang diperoleh dalam tinjauan termodinamika:
Grafik keseimbangan konversi pada tinjauan thermodinamika didapat dari persamaan berikut :
19 Contoh Perhitungan Tinjauan Termodinamika :
Rumus ∆G = -RT ln K lnK= x = 1. ln K = K = 1.1265 x = = 0.53 2. ln K= K = 1.0827 x = = 0.52 3. ln K= K = 1.0613 x = = 0.515
Grafik II.1. Grafik Hubungan Suhu dan % Konversi (Termodinamika)
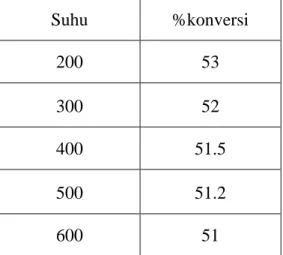
Suhu %konversi 200 53 300 52 400 51.5 500 51.2 600 51
20
700 50.8
800 50.7
900 50.6
Grafik II.1. Grafik Hubungan Suhu dan % Konversi (Termodinamika)
2.13. Tinjauan Kinetika
Tinjauan Kinetika Reaksi
Secara umum derajat kelangsungan reaksi ditentukan oleh konstanta kecepatan reaksi (k), orde reaksi dan konsentrasi reaktan.
Persamaan kecepatan reaksi pembentukan polistirena adalah sebagai berikut :
kc =
(ref. Westerterp)
Pada T = 137°C
kc = konstanta kecepatan reaksi 49 49.5 50 50.5 51 51.5 52 52.5 53 53.5 200 300 400 500 600 700 800 900 % Kon ve rsi Tinjauan Thermodinamika Suhu K
21 kb = konstanta Boltzman = 2,04666 kal/mol
h = konstanta Planck = 9,8204391 x kal.s /gmol K = probabilitas reaksi, asumsi =1
G = energi bebas Gibbs = -42750 kkal/mol k = 3,126 x 10 10 m3/kgmol.detik
untuk reaksi yang bersifat eksotermis, maka kenaikan suhu akan menaikkan kecepatan reaksi. Dari segi termodinamika, temperatur tertinggi yang dipilih mempertimbangkan pembentukan produk kristal yang terjadi.
Dengan menggunakan persamaan Arhenius :
Dimana :
k = konstanta kecepatan reaksi A = factor frekuensi gas ideal R = konstanta gas ideal T = suhu absolute
Dalam hubungan ini:
= 6189.9
T = 410°K
k = konstanta kecepatan reaksi (lt/kmol dt)
k pada temperature operasi 410°K adalah sebesar 9.3.10-4 lt/kmol dt
Dari persamaan di atas, maka untuk mempercepat reaksi perlu dilakukan usaha-usaha untuk memperbesar harga k, yaitu dengan jalan memperbesar harga A dan T, serta memperkecil harga E.
22 Reaksi pembentukan polistirena adalah reaksi reversibel orde satu, jadi persamaan yang digunakan untuk mencari konversi adalah:
(Reff: Levenspiel, 1999)
Contoh Perhitungan Grafik Tinjauan Kinetika : Dari rumus k = A -ln(1-XA)=kt t = 27360 detik 1. k = 0.122444 e-6189/200 k = 4.433 x 10-15 -ln(1-XA)=kt (1-XA)=0.999 XA= 1.213 x 10-10 2. k = 0.122444 e-6189/300 k = 1.34 x 10-10 -ln(1-XA)=kt (1-XA)=0.999963 XA= 3.67 x 10-6 3. k = 0.122444 e-6189/400 k = 2.329 x 10-8 -ln(1-XA)=kt (1-XA)=0.99936 XA= 6.37 x 10-4
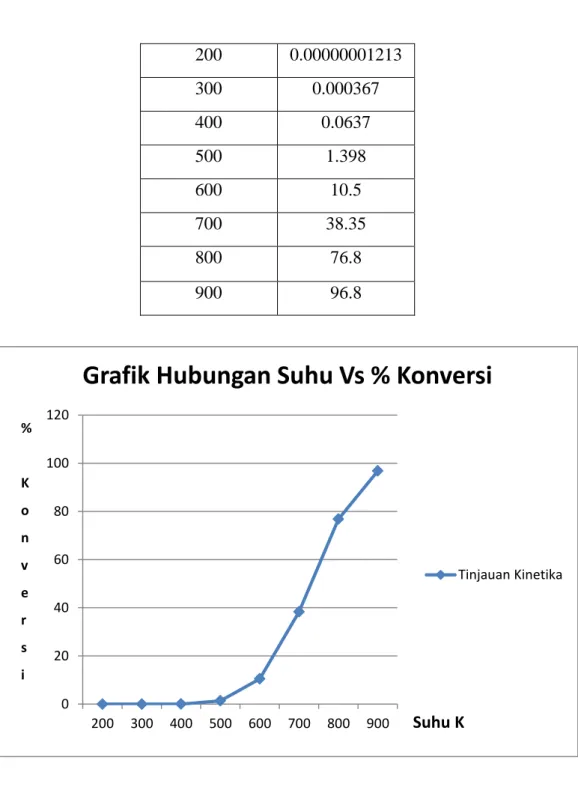
Berikut ini grafik hubungan suhu vs % konversi yang diperoleh dalam tinjauan kinetika:
Tabel II.2. Hubungan Suhu dan % Konversi (Kinetika) Suhu %Konversi
23 200 0.00000001213 300 0.000367 400 0.0637 500 1.398 600 10.5 700 38.35 800 76.8 900 96.8
Grafik II.2. Grafik Hubungan Suhu dan % Konversi (Kinetika) Faktor yang mempengaruhi kecepatan reaksi :
1. Suhu
Bila suhu dinaikkan maka kecepatan reaksi akan meningkat. Akibatnya reaksi akan berjalan dengan cepat.
2. Katalis 0 20 40 60 80 100 120 200 300 400 500 600 700 800 900
Grafik Hubungan Suhu Vs % Konversi
Tinjauan Kinetika Suhu K % K o n v e r s i
24 Katalis dapat menurunkan energy aktivasi (E). Dengan berkurangnya energy aktivasi maka harga K akan naik sehingga laju kecepatan reaksi akan bertambah cepat pula.
Tjukup Marnoto dan Endang Sulistyowati Pengembangan Teknologi Kimia untuk Pengolahan Sumber Daya Alam Indonesia Teknik Kimia, Fak Teknologi Industri, UPN “Veteran” Yogyakarta.
Grafik Konversi VS Suhu untuk Kondisi Optimum
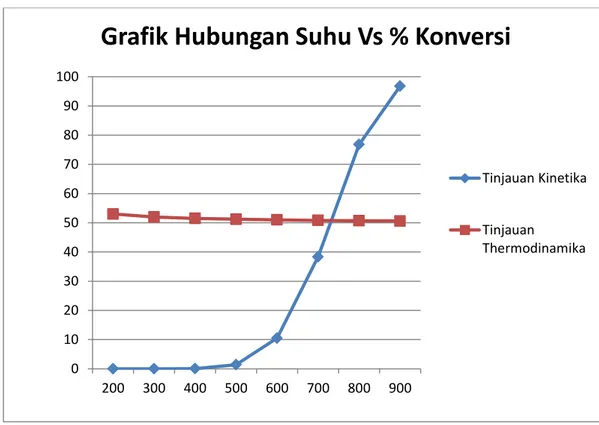
Pada saat komposisi keseimbangan, perubahan konversi terhadaptemperatur pada suatu reaksi dapat ditinjau secara dua aspek, yaitu melalui tinjauan thermodinamika dan tinjauan kinetika. Hubungan antara temperatur dan konversi dalam reaksi pembentukan polistirena dalam tinjauan thermodinamika dan kinetika ditunjukkan pada data berikut :
Grafik II.3. Grafik Hubungan Suhu dan % Konversi (Kondisi Optimum)
Dari hasil perhitungan yang ditinjau dari tinjauan thermodinamika dan kinetika diperoleh titik suhu optimum, yaitu pada suhu 720 K dengan
0 10 20 30 40 50 60 70 80 90 100 200 300 400 500 600 700 800 900
Grafik Hubungan Suhu Vs % Konversi
Tinjauan Kinetika
Tinjauan
25 konversi 50.78%. sedangkan produksi polistiren pada pabrik suhu yang dibutuhkan hanya 410 K dengan konversi 85%.
Penyimpangan terjadi karena proses produksi hanya membutuhkan waktu 1 jam. Seharusnya produksi polistirena membutuhkan waktu yang maksimal agar terjadi reaksi sempurna, mengingat agar cepat mendapatkan produk polistirena dan segera dipasarkan. Apabila menunggu sampai waktu maksimum, maka dibutuhkan waktu yang sangat lama. Selain itu, reaksi pembentukan polistirena merupakan eksotermis yang menghasilkan panas. Reaksi ini terjadi pada suhu 410 K. Apabila reaksi terjadi pada suhu yang sangat tinggi maka, sangat berbahaya dan produk yang dihasilkan kurang maksimal.
Untuk meningkatkan konversi bisa diatasi dengan menggunakan katalis Fe2O3. Katalis ini akan mengurangi energi aktivasi dan
meningkatkan kecepatan reaksi pembentukan polistirena.
26 BAB III
PENUTUP 3.1.Kesimpulan
Polystyrene adalah sebuah aromatik polimer yang dibuat dari aromatik monomer styrene, cairan hidrokarbon yang secara komersial diproduksi dari minyak bumi oleh di industri kimia.
Polystyrene merupakan senyawa berbentuk Kristal bening yang mempunyai sifat elektris yang baik, derajat kekerasan yang tinggi, tahan terhadap panas, mudah dalam pewarnaan, permukaan yang halus dan low toxity.
Polystyrene dibuat melalui beberapa tahapan reaksi, yaitu tahapan inisiasi, tahapan propagasi, dan tahapan terminasi. Sedangkan contoh proses produksinya adalah bulk-batch, bulk-continuous, polimerisasi suspensi, dan polimerisasi eemulsi.
Berdasarkan analisa data yang telah diperoleh, maka disimpulkan bahwa potensi pasar dari produk polistrena di Indonesia masih luas karena setiap tahun permintaan produk polistirena semakin meningkat.
3.2.Saran
a. Saran Untuk Produsen
Pendirian pabrik polistirena semakin cepat semakin baik, karena ke kebutuhan dalam negeri akan polystirena semakin tahun semakin tinggi
b. Saran Untuk Konsumen
Hindari pengunaan polistirena berlebih karena dapat mencemari lingkungan
Hindari penggunaan polistirena sebagai tempat makanan dengan suhu tinggi karena dapat terjadi kontaminasi pada makanan oleh polistirena.
c. Saran Untuk bidang IPTEK
Diharapkan ditemukannya bahan baku pengganti untuk sterofoam yang lebih ramah lingkungan dan lebih mudah terurai oleh alam.
27 DAFTAR PUSTAKA
Levenspiel, O. 1957. “Chemical Reaction Engineering”. New York: Mc Graw Hill Book Co.
Perry, R.H. and Green, D.W., 1997, Perry’s Chemical Engineers’ Handbook, 7th ed., Mc. Graw-Hill Book Company, New York.
Smith,J.M., H.C.Van Ness., M.M.Abbott. 2001. “Introduction to Chemical Engineering Thermodynamics” sixth ed. Singapore : Mc Graw Hill Book http://bilangapax.blogspot.com/2011/02/polistirena.html http://elib.unikom.ac.id/files/disk1/532/jbptunikompp-gdl-rizkyrachm-26569-6 babiv.pdf http://serbamurni.blogspot.com/2012/02/contoh-laporan-cstr-continuous-stirred.html selvyfransisca.files.wordpress.com/2011/07/makalah-asam-asetat.docx Wikipedia.com/polystyrene.html