INTERAKSI HASIL ANALISIS VEGETASI PADANG
PENGGEMBALAAN DAN INFESTASI CACING PADA
DOMBA DI KABUPATEN MAJALENGKA, JAWA BARAT
ELLY WIDYAS NINGSIH
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
BOGOR 2014
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul Interaksi Hasil Analisis Vegetasi Padang Penggembalaan dan Infestasi Cacing pada Domba di Kabupaten Majalengka, Jawa Barat adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, April 2014
Elly Widyas Ningsih
ABSTRAK
ELLY WIDYAS NINGSIH. Interaksi Hasil Analisis Vegetasi Padang Penggembalaan dan Infestasi Cacing pada Domba di Kabupaten Majalengka, Jawa Barat. Dibimbing oleh ACHMAD FARAJALLAH dan SULISTIJORINI.
Infestasi cacing parasit saluran pencernaan menyebabkan pertumbuhan domba terhambat. Faktor yang mempengaruhi infestasi cacing salah satunya adalah jenis pakan hijauan di lahan penggembalaan. Tujuan dari penelitian ini adalah untuk mempelajari interaksi keanekaragaman jenis tumbuhan dan keanekaragaman jenis cacing pada domba di padang penggembalaan domba Kabupaten Majalengka, Jawa Barat; serta membandingkan metode preparasi sampel feses. Analisis vegetasi dilakukan dengan menggunakan metode purposive
random sampling. Domba yang digembalakan pada lokasi tersebut diambil
fesesnya. Feses dipreparasi menggunakan metode pengapungan dan sedimentasi. Keanekaragaman jenis cacing dan nilai FEC pada domba berbeda antar lokasi penggembalaan. Domba yang digembalakan di areal persawahan pasca panen memiliki keanekaragaman jenis cacing dan nilai FEC yang lebih rendah dibanding domba yang digembalakan di kebun tebu. Pada lokasi yang terdapat tumbuhan yang diduga mengandung senyawa antelmintik, diperoleh nilai FEC yang lebih rendah. Metode pengapungan spesifik untuk spesies cacing Moniezia, sedangkan metode sedimentasi spesifik untuk cacing Bunostomum sp.
Kata kunci: FEC, keanekaragaman jenis cacing, pengapungan, sedimentasi
ABSTRACT
ELLY WIDYAS NINGSIH. Interaction Between Vegetation Analysis of Grassland and Worm Infestation of Sheep in Kabupaten Majalengka, West Java. Supervised by ACHMAD FARAJALLAH and SULISTIJORINI.
The gastrointestinal worm can inhibit the growing rate of sheep. Worm infestation on gastrointestinal of sheep influenced by vegetation composition of grassland when the sheep were kept in pastoral system. The aim of this research is to learn interaction between grassland’s plant composition and gastrointestinal worm diversity within sheep in Kabupaten Majalengka, West Java; and learn methods to determine the presence of worm eggs in faecal sample. Vegetation composition were analyzed using purposive random sampling method. Feces was taken from sheep that it was grazing on the location of grassland. Feces was prepared using floating method and sedimentation method. Worm diversity and FEC in sheep were different between locations. The sheep were grazing on post-harvested rice field has worm diversity and FEC lower than grazing on cane plantation. At locations with plants suspected to contain anthelmintic compound were found lower FEC. The floating method is spesific method to species
Moniezia, whereas the sedimentation method spesific to Bunostomum sp.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Biologi
INTERAKSI HASIL ANALISIS VEGETASI PADANG
PENGGEMBALAAN DAN INFESTASI CACING PADA
DOMBA DI KABUPATEN MAJALENGKA, JAWA BARAT
ELLY WIDYAS NINGSIH
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
BOGOR 2014
Judul Skripsi: Interaksi Hasil Analisis Vegetasi Padang Penggembalaan dan Infestasi Cacing pada Domba di Kabupaten Majalengka, Jawa Barat
Nama : Elly Widyas Ningsih NIM : G34100114
Disetujui oleh
Dr Ir Achmad Farajallah, MSi Pembimbing I
Dr Ir Sulistijorini, MSi Pembimbing II
Diketahui oleh
Dr Ir Iman Rusmana, MSi Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yesus Kristus atas berkat dan penyertaan-Nya sehingga karya ilmiah ini berhasil diselesaikan. Penelitian ini berjudul Interaksi Hasil Analisis Vegetasi Padang Penggembalaan dan Infestasi Cacing pada Domba di Kabupaten Majalengka, Jawa Barat. Penelitian dilaksanakan sejak bulan Oktober 2013 sampai Maret 2014 di padang penggembalaan domba di Kecamatan Jati Tujuh, Kabupaten Majalengka, Jawa Barat dan bagian Fungsi Hayati dan Perilaku Hewan Departemen Biologi, FMIPA IPB.
Terima kasih penulis ucapkan kepada Bapak Dr Ir Achmad Farajallah, MSi dan Ibu Dr Ir Sulistijorini, MSi selaku dosen pembimbing, dan Ibu Dr Ir Yohana C. Sulistyaningsih, MSi selaku dosen penguji skripsi atas bimbingan, saran, dan ilmu yang bermanfaat selama melaksanakan penelitian dan penulisan karya ilmiah. Terima kasih penulis ucapkan kepada Kak Wildan, Kak Silvi, Kak Wahyudin, Wahyu, Bapak Mansur, Bapak Wamin, Bapak Sur, dan Bapak Cahim yang telah membantu selama pengumpulan data. Terima kasih juga penulis ucapkan kepada Bapak Cita dan keluarga atas bantuan tempat tinggal selama penelitian. Di samping itu, terima kasih penulis ucapkan kepada ayah, ibu, serta seluruh keluarga, atas segala doa dan kasih sayangnya, serta teman-teman terbaik saya Mita, Agnes, Amel, Christyne, Irene, Ibeth, Sabeth, Carin dan seluruh teman-teman Biologi angkatan 47 atas dukungan, doa, semangat, dan kebersamaannya.
Semoga karya ilmiah ini dapat memberikan informasi yang berguna dan bermanfaat bagi perkembangan ilmu pengetahuan.
Bogor, April 2014
DAFTAR ISI
DAFTAR TABEL vi DAFTAR GAMBAR vi DAFTAR LAMPIRAN vi PENDAHULUAN 1 Latar Belakang 1 Tujuan Penelitian 1 METODE 2Waktu dan Tempat 2
Metode Penelitian 2
Analisis Vegetasi 2
Pengambilan Sampel Feses 3
Preparasi Sampel Feses 3
Identifikasi Telur Cacing 3
Analisis Vegetasi dan FEC 3
HASIL DAN PEMBAHASAN 3
Analisis Vegetasi 3
Faecal Egg Count 5
Perbandingan Metode Pengapungan dengan Metode Sedimentasi 5
Analisis Vegetasi dan FEC 7
SIMPULAN 11
DAFTAR PUSTAKA 11
LAMPIRAN 13
DAFTAR TABEL
1 Data jenis tumbuhan yang ditemukan di lima lokasi penggembalaan 4 2 Data jenis dan jumlah cacing yang menginfeksi domba di lima lokasi
penggembalaan 5
3 Pengelompokan cacing parasit domba 5
DAFTAR GAMBAR
1 Peta lokasi penggembalaan domba 2
2 Perbandingan jenis telur yang dapat diamati menggunakan metode
pengapungan dan sedimentasi 6
3.1 Kerapatan relatif spesies tumbuhan dan rataan FEC di lokasi A 7 3.2 Kerapatan relatif spesies tumbuhan dan rataan FEC di lokasi B 8 3.3 Kerapatan relatif spesies tumbuhan dan rataan FEC di lokasi C 8 3.4 Kerapatan relatif spesies tumbuhan dan rataan FEC di lokasi D 9 3.5 Kerapatan relatif spesies tumbuhan dan rataan FEC di lokasi E 9
DAFTAR LAMPIRAN
1 Data iklim makro Kecamatan Jatitujuh 13
2 Kerapatan dan frekuensi relatif jenis tumbuhan di setiap lokasi 14
3 Data sampel domba dan lokasi penggembalaan 15
4 Data jenis dan jumlah cacing yang mengifeksi domba 16 5 Gambar telur cacing yang ditemukan menginfeksi domba 17 6 Gambar cacing dewasa yang ditemukan menginfeksi domba 18
PENDAHULUAN
Latar BelakangSebagaimana ternak lainnya di daerah tropis basah, dalam saluran pencernaan domba bisa ditemukan beragam jenis cacing. Cacing yang ada di saluran pencernaan domba dianggap parasit dan umumnya tergolong ke dalam kelas Nematoda, Cestoda, dan Trematoda. Siklus hidup cacing Nematoda pada ruminansia bersifat langsung, tidak membutuhkan inang antara, sedangkan pada Cestoda dan Trematoda umumnya memerlukan inang antara (Levine 1990). Cacing parasit saluran pencernaan bisa menghambat pertumbuhan domba dan pada kondisi tertentu akan menyebabkan kematian. Cacing masuk ke dalam tubuh domba melalui dua cara, masuk bersama dengan pakan dan aktif menembus kulit domba. Cacing dewasa hidup dalam saluran pencernaan yang kemudian apabila bertelur, telur-telur tersebut akan dikeluarkan bersama dengan feses. Pada kondisi yang sesuai, telur akan berkembang menjadi larva, yang dapat melalui inang antara terlebih dahulu maupun langsung menjadi larva infektif dan menempel pada rumput dan termakan oleh domba.
Keberadaan cacing parasit dapat diketahui melalui pemeriksaan telur cacing yang ada di feses. Beberapa jenis cacing parasit pada domba adalah Capillaria sp.,
Trichuris sp., Strongyloides papillosus, Skrajabinema sp., Dicrocoelium dendriticum, Nematodirus sp., Fasciola hepatica, Protostrongylus sp., Dictyocaulus filaria, Moniezia expansa, Thysanosoma actinoides, dan Muellerius capillaris (Zajac dan Conboy 2012). Menurut Morley dan Donald (1977), faktor
yang mempengaruhi tinggi rendahnya infestasi cacing pada domba antara lain jenis pakan hijauan di lahan penggembalaan. Selain itu, domba yang digembalakan terus-menerus pada suatu lahan. Hal ini disebabkan rumput di tempat penggembalaan terkontaminasi oleh telur cacing yang menetas menjadi larva infektif (Batubara 2005). Domba di peternakan rakyat Kecamatan Jatitujuh, Kabupaten Majalengka, Jawa Barat, dipelihara dengan cara digembalakan. Pada musim kemarau, domba biasanya digembalakan di sawah, sedangkan apabila musim tanam padi tiba, domba digembalakan di areal kebun tebu. Ternak domba yang digembalakan di wilayah tersebut hanya mengkonsumsi pakan hijauan alami.
Menurut Fachrul (2007), masyarakat tumbuhan yang terbentuk oleh berbagai populasi jenis tumbuhan dalam satu wilayah atau ekosistem disebut vegetasi. Penduduk setempat di beberapa daerah mempercayai beberapa jenis tumbuhan memiliki khasiat mengobati penyakit cacingan (antelmintik) pada ternak (Ishtiaq et al. 2006). Beberapa jenis tumbuhan diketahui mengandung senyawa antelmintik (Chengaiah et al. 2009; Cordeiro dan Kaliwal 2012; Mahato
et al. 2014; Niezen et al. 2002; Priyanka et al. 2010, Shaik et al. 2006)
Tujuan Penelitian
Penelitian ini bertujuan mempelajari interaksi keanekaragaman jenis tumbuhan dan keanekaragaman jenis cacing pada domba di padang penggembalaan domba Kecamatan Jatitujuh, Kabupaten Majalengka, Jawa Barat; serta membandingkan metode preparasi sampel feses.
2
METODE
Waktu dan TempatPenelitian dilaksanakan pada bulan Oktober 2013 sampai dengan bulan Maret 2014 di padang penggembalaan domba di Kecamatan Jatitujuh, Kabupaten Majalengka dan bagian Fungsi Hayati dan Perilaku Hewan Departemen Biologi, FMIPA IPB.
Metode Penelitian Analisis Vegetasi
Analisis vegetasi dilakukan di lima lokasi, yaitu lokasi A, B, C, D, dan E (Gambar 1). Lokasi A, B, C merupakan areal persawahan pasca panen, sedangkan lokasi D dan E merupakan areal perkebunan tebu. Lokasi A dan B diamati pada bulan Oktober, lokasi C diamati pada bulan November, lokasi D diamati pada bulan Desember, dan lokasi E diamati pada bulan Februari. Analisis vegetasi dilakukan dengan menggunakan metode purposive random sampling. Plot berukuran 2 x 2 meter dibuat sebanyak minimal 6 plot di 5 lokasi. Plot tersebut ditentukan dengan mengikuti jelajah domba selama kurang lebih 1 jam. Setiap plot dilakukan inventarisasi jenis dan jumlah tumbuhan, kemudian dihitung kerapatan dan frekuensi relatifnya. Tumbuhan yang diperoleh diidentifikasi berdasarkan Kostermans et al. (1987) dan Van Steenis (1988). Kerapatan dan frekuensi relatif dihitung menggunakan rumus:
Data lingkungan yang direkam menggunakan alat pengukur cuaca tipe AW002 meliputi suhu, curah hujan, kelembaban, dan kecepatan angin.
3
Pengambilan Sampel Feses
Feses diambil dari domba yang digembalakan pada lokasi yang diamati. Feses diambil dengan cara faecal swapped from anus, yaitu diambil langsung dari anus. Kisaran umur domba ditentukan dengan metode judging dan bertanya kepada penggembala, sedangkan jenis kelamin diketahui dengan mengamati secara langsung.
Preparasi Sampel Feses
Sampel feses dipreparasi dengan dua cara, yaitu dengan metode pengapungan menggunakan larutan garam jenuh dan sedimentasi formalin-etil asetat.
Pengapungan. Sebanyak 2 gram feses digerus dan ditambahkan garam jenuh sebanyak 60 mL, dihomogenisasi, dan didiamkan selama 5 menit. Cairan yang berada di permukaan diambil menggunakan pipet tetes dan diletakkan di atas gelas objek (modifikasi McMaster) (Whitlock 1948) lalu diamati menggunakan mikroskop.
Sedimentasi. Sebanyak 10 mL formalin 10% ditambahkan pada 1 gram feses, kemudian diaduk sampai homogen. Campuran kemudian disaring dengan kain kasa dan dimasukkan ke dalam tabung sentrifuge hingga volume mencapai 7 mL. Lalu ditambahkan etil asetat sebanyak 3 mL dan disentrifuge selama 1 menit dengan kecepatan 2700 rpm. Supernatan dipindahkan ke dalam tabung sentrifuge yang lain dan disentrifuge selama 1 menit dengan kecepatan 1000 rpm. Bagian sedimen diambil dan diletakkan di atas gelas objek, lalu diamati menggunakan mikroskop.
Identifikasi Telur Cacing
Telur yang diperoleh diidentifikasi berdasarkan Zajac dan Conboy (2012), Mönnig dan Phill (1947), dan Soulsby (1982). Telur cacing yang ada di feses dihitung untuk mengetahui tingkat infeksi cacing (FEC, Faecal Egg Count). Domba tergolong infeksi ringan apabila jumlah telur cacing berkisar 0-499 telur/gram; sedang 500-2000 telur/gram; dan berat diatas 2000 telur/gram (Tarazona 1986).
Analisis Vegetasi terhadap FEC
Kerapatan relatif spesies tumbuhan dibandingkan dengan rataan FEC di setiap lokasi.
HASIL DAN PEMBAHASAN
Analisis VegetasiBerdasarkan hasil analisis vegetasi di lima lokasi, diperoleh jenis tumbuhan sebanyak 46 jenis. Keanekaragaman jenis tumbuhan paling rendah dijumpai pada lokasi A (8 jenis), sedangkan keanekaragaman yang paling tinggi terdapat pada lokasi B (21 jenis) (Tabel 1). Data iklim makro Kecamatan Jatitujuh disajikan
4
pada Lampiran 1. Nilai kerapatan dan frekuensi relatif spesies tumbuhan di setiap lokasi disajikan pada Lampiran 2.
Tabel 1 Data jenis tumbuhan yang ditemukan di lima lokasi penggembalaan
No Spesies tumbuhan Lokasi
A B C D E 1 Alternanthera nodiflora 2 Ammannia baccifera 3 Bergia ammannioides 4 Brachiaria reptans 5 Centella asiatica 6 Chrozophora rottleri 7 Cyperus difformis 8 Cyperus iria 9 Dactyloctenium aegyptium 10 Dichondra repens 11 Digitaria ciliaris 12 Echinochloa colonum 13 Eleusine indica 14 Eriochloa polystachya 15 Fimbristylis miliaceae 16 Fimbristylis sp. 17 Glinus lotoides 18 Heliotropium indicum 19 Houstonia longifolia 20 Hydrolea zeylanica 21 Leptochloa chinensis 22 Ludwigia hyssopifolia 23 Ludwigia peruviana 24 Ludwigia sp. 25 Marsilea crenata 26 Oryza sativa 27 Panicum repens 28 Paspalum sp. 29 Phyllanthus debilis 30 Phyllanthus urinaria 31 Poaceae 1 32 Rhynchosia minima 33 Richardia brasiliensis 34 Saccharum officinarum 35 Sp. 1 36 Sp. 2 37 Sp. 3 38 Sp. 4 39 Sp. 5 40 Sp. 6 41 Sp. 7 42 Sp. 8 43 Sphaeranthus africanus 44 Sphaeranthus indicus 45 Sutera cordata 46 Zea mays
5 Faecal Egg Count
Didapati 9 spesies cacing yang menginfeksi domba (Tabel 2). Pengelompokan jenis cacing tersebut dapat dilihat pada Tabel 3. Spesies
Oesophagostomum spp. ditemukan di setiap lokasi penggembalaan. Jumlah telur
cacing paling tinggi dijumpai pada domba yang digembalakan di lokasi C. Data sampel domba dapat dilihat pada Lampiran 3. Berdasarkan nilai FEC, diketahui sebanyak 87,9% domba terinfeksi ringan; 9,1% domba terinfeksi sedang; dan 3% domba terinfeksi berat (Lampiran 4). Gambar telur cacing yang diperoleh dapat dilihat pada Lampiran 5.
Tabel 2 Data jenis dan jumlah cacing yang menginfeksi domba di lima lokasi penggembalaan
Lokasi Jumlah
domba
Metode pengapungan Metode sedimentasi
Spesies cacing Rataan FEC (telur/g) Spesies cacing Rataan FEC (telur/g) A 5 Moniezia benedeni 6 Skrjabinema ovis 10
Moniezia expansa 6 Haemonchus contortus 10
Trichostrongylus spp. 6 Oesophagostomum spp. 60
Skrjabinema ovis 6 Strongyloides pappilosus 30
Strongyloides pappilosus 6 Trichostrongylus spp. 30 B 7 Schistosoma sp. 4 Oesophagostomum spp. 14 Strongyloides pappilosus 13 Oesophagostomum spp. 4 C 8 Oesophagostomum spp. 300 Oesophagostomum spp. 13 Trichostrongylus spp. 38 Trichostrongylus spp. 13 Haemonchus contortus 38 D 5 Oesophagostomum spp. 132 Schistosoma sp. 10 Trichostrongylus spp. 42 Strongyloides pappilosus 6
E 8 Haemonchus contortus 45 Bunostomum sp. 6
Oesophagostomum spp. 120 Oesophagostomum spp. 13
Trichostrongylus spp. 75 Trichostrongylus spp. 6
Schistosoma sp. 6
Tabel 3 Pengelompokan cacing parasit domba
Kelas Famili Spesies
Nematoda Ancylostomatidae Bunostomum sp.
Oxyuridae Skrjabinema ovis
Strongylidae Oesophagostomum spp.
Strongyloididae Strongyloides pappilosus
Trichostrongylidae Haemonchus contortus, Trichostrongylus spp.
Cestoda Anoplopcephalidae Moniezia benedeni, Moniezia expansa
Trematoda Schistosomatidae Schistosoma sp.
Perbandingan Metode Pengapungan dengan Metode Sedimentasi
Jenis cacing ditemukan lebih banyak pada sampel yang menggunakan metode pengapungan daripada metode sedimentasi (Gambar 3). Hal ini tidak sesuai dengan yang dikatakan Baker et al. (2007), bahwa metode sedimentasi
6
Metode sedimentasi Metode pengapungan
secara umum dapat digunakan untuk memperoleh jenis cacing yang lebih banyak dibanding metode pengapungan. Menurut Southwell et al. (2008) metode pengapungan menggunakan larutan garam jenuh dapat digunakan untuk mengamati Trichostrongylus, H. contortus, Teladorsagia, Cooperia, Bunostomum,
Oesophagostomum, Chabertia, Nematodirus, Moniezia, dan Trichuris.
Gambar 2 Perbandingan jenis telur yang dapat diamati menggunakan metode pengapungan dan sedimentasi
Pada metode pengapungan, larutan yang digunakan bersifat hipertonik. Pada pengamatan yang terlalu lama, larutan hipertonik tersebut dapat menaikan tekanan osmotik. Larutan flotasi yang bersifat hipertonik tersebut akan membuat bentuk telur terdistorsi, misal mengkerut karena kehilangan air. Selain itu, waktu penyimpanan yang lama sebelum dipreparasi dapat menyebabkan telur menjadi rusak (Baker et al. 2007). Kedua hal tersebut mungkin yang meyebabkan telur cacing Bunostomum tidak ditemukan pada metode pengapungan.
Metode sedimentasi memiliki tahapan pekerjaan yang lebih banyak. Tahap penyaringan dan pembuangan supernatan merupakan tahapan yang penting. Telur cacing Moniezia yang ditemukan pada metode pengapungan tidak ditemukan pada metode pengendapan. Hal tersebut mungkin disebabkan telur menempel pada kotoran saat proses penyaringan, terbuang bersama supernatan, atau terhalangi oleh debris saat pengamatan. Menurut Baker et al. (2007), salah satu kelemahan metode sedimentasi adalah adanya debris berukuran besar yang menghalangi pengamatan.
Berdasarkan dari banyaknya telur cacing maupun jenis cacing yang ditemukan, metode pengapungan menggunakan larutan garam jenuh jauh lebih baik daripada metode sedimentasi. Hal ini dikarenakan metode sedimentasi memiliki tahapan pekerjaan yang lebih banyak. Tahap penyaringan dan pembuangan supernatan merupakan tahapan yang penting yang memerlukan kecermatan, agar telur tidak menempel pada kotoran ataupun terbuang bersama supernatan. Strongyloides pappilosus Oesophagostomum spp. Trichostrongylus spp. Moniezia benedeni Bunostomum sp. Schistosoma sp. Skrjabinema ovis Moniezia expansa Haemonchus contortus
7 Ker ap atan r elatif ( %) R ataa n FEC ( telu r/g ) Spesies tumbuhan Spesies cacing Analisis Vegetasi dan FEC
Kelima lokasi penggembalaan yang dianalisis memiliki kerapatan dan jenis tumbuhan yang berbeda. Jenis dan jumlah cacing yang ditemukan pada saluran pencernaan domba, berbeda antar lokasi. Kerapatan relatif spesies tumbuhan dan rataan FEC di setiap lokasi digambarkan dalam bentuk diagram batang (Gambar 2.1-2.5).
Gambar 3.1 Kerapatan relatif spesies tumbuhan dan rataan FEC di lokasi A
0 10 20 30 40 50 60 70 0 10 20 30 40 50 60 70 80 90 100
8 Ker ap atan r elatif ( %) Ker ap atan r elatif ( %) R ataa n FEC ( telu r/g ) R ataa n FEC ( telu r/g ) Spesies tumbuhan Spesies tumbuhan Spesies cacing Spesies cacing
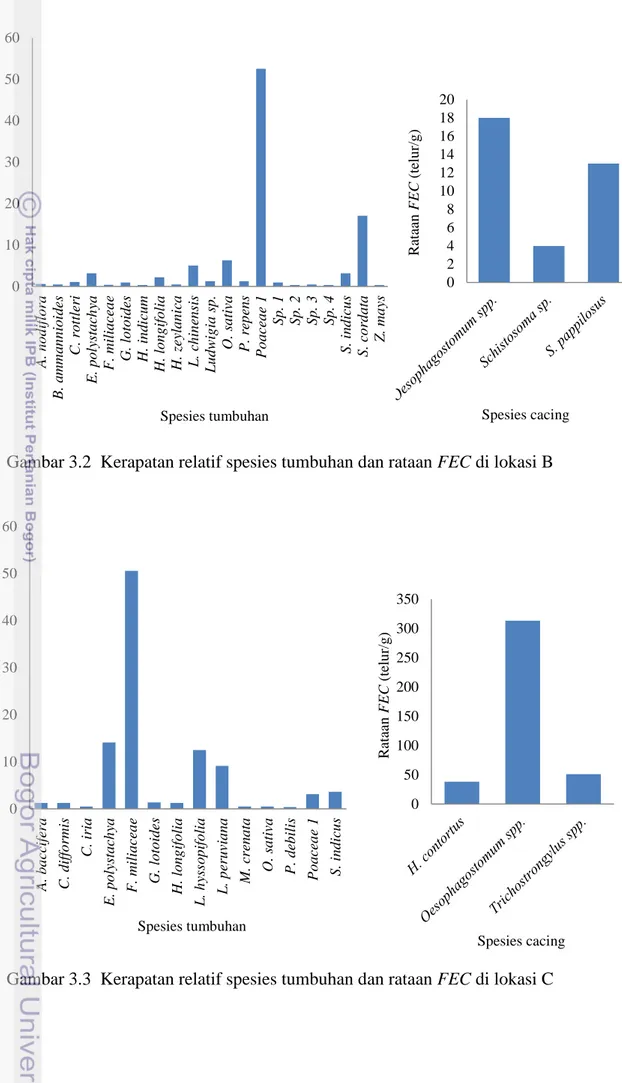
Gambar 3.2 Kerapatan relatif spesies tumbuhan dan rataan FEC di lokasi B
Gambar 3.3 Kerapatan relatif spesies tumbuhan dan rataan FEC di lokasi C
0 10 20 30 40 50 60 A . n o d iflo ra B . a mm a n n io id es C . ro ttler i E. p o lys ta ch ya F . milia ce a e G. lo to id es H. in d icu m H. lo n g ifo lia H. z ey la n ica L. ch in en sis Lu d w ig ia s p . O. s a tiva P . rep en s Po a cea e 1 S p . 1 S p . 2 S p . 3 S p . 4 S . in d icu s S . co rd a ta Z. ma ys 0 2 4 6 8 10 12 14 16 18 20 0 10 20 30 40 50 60 A . b a cc ifer a C . d iffo rmis C . ir ia E . p o lys ta ch ya F . milia ce a e G . lo to ides H. lo n g ifo lia L. h yss o p ifo lia L. p eru via n a M. cr en a ta O. s a tiva P . d eb ilis P o a ce a e 1 S . in d icu s 0 50 100 150 200 250 300 350
9 Ker ap atan r elatif ( %) Ker ap atan r elatif ( %) R ataa n FEC ( telu r/g ) R ataa n FEC ( telu r/g ) Spesies tumbuhan Spesies tumbuhan Spesies cacing Spesies cacing
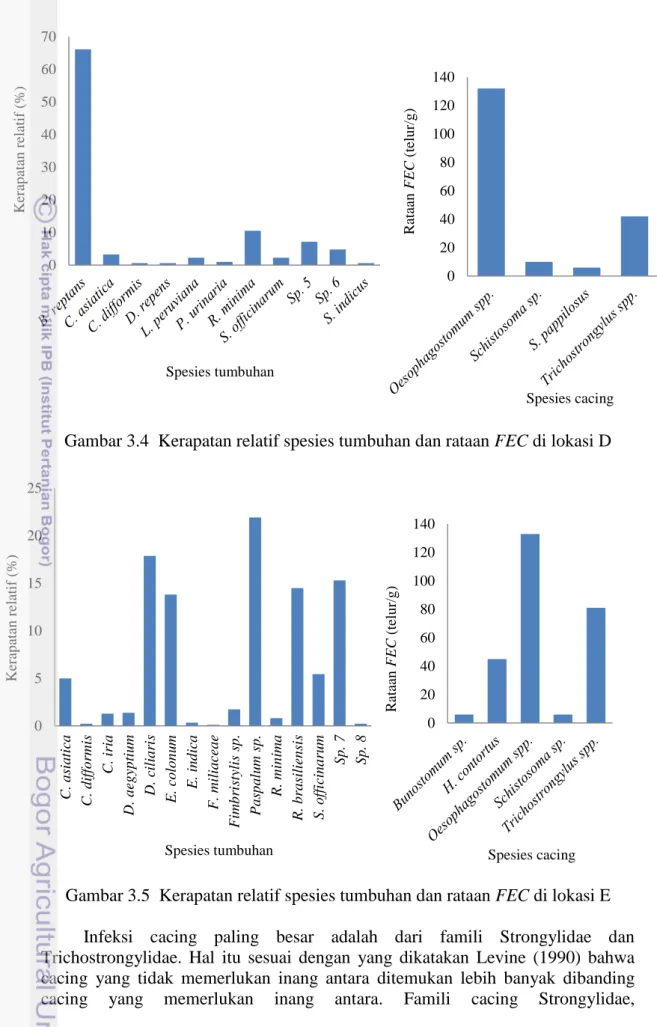
Gambar 3.4 Kerapatan relatif spesies tumbuhan dan rataan FEC di lokasi D
Gambar 3.5 Kerapatan relatif spesies tumbuhan dan rataan FEC di lokasi E Infeksi cacing paling besar adalah dari famili Strongylidae dan Trichostrongylidae. Hal itu sesuai dengan yang dikatakan Levine (1990) bahwa cacing yang tidak memerlukan inang antara ditemukan lebih banyak dibanding cacing yang memerlukan inang antara. Famili cacing Strongylidae,
0 10 20 30 40 50 60 70 0 20 40 60 80 100 120 140 0 20 40 60 80 100 120 140 0 5 10 15 20 25 C . a si a ti ca C . d iffo rmis C . ir ia D . a eg yp ti u m D. cilia ri s E . co lo n u m E . in d ica F . milia ce a e F im b ri sty li s sp . P a sp a lu m sp . R . min ima R . b ra silien si s S . o ff icin a ru m S p . 7 S p . 8
10
Trichostrongylidae, Strongyloididae, Oxyuridae, dan Ancylostomatidae tergolong ke dalam kelas Nematoda yang umumnya tidak memerlukan inang antara, sedangkan Schistosomatidae masuk ke dalam kelas Trematoda yang memerlukan inang antara berupa siput dan Anoplopcephalidae tergolong dalam kelas Cestoda yang memerlukan inang antara berupa tungau.
Keanekaragaman jenis cacing dan nilai FEC pada domba yang digembalakan, berbeda antar lokasi. Spesies cacing paling banyak ditemukan pada domba yang digembalakan di lokasi A. Jenis tumbuhan yang paling banyak dijumpai pada lokasi ini adalah Poaceae, sedangkan jenis cacing yang paling banyak menginfeksi domba adalah Oesophagostomum spp. Spesies cacing M.
expansa, M. benedeni, dan S. ovis hanya ditemukan pada lokasi A. Keberadaan
cacing Moniezia ini diduga karena pada lokasi A terdapat tungau yang merupakan inang antara cacing tersebut. Pada lokasi B, jenis tumbuhan yang paling banyak ditemukan adalah Poaceae. Pada lokasi ini keanekaragaman tumbuhannya paling tinggi, sedangkan kenanekaragaman cacingnya paling rendah. Jumlah telur cacing paling banyak dijumpai domba yang digembalakan di lokasi C yang didominasi oleh tumbuhan F. miliaceae. Lokasi D didominasi oleh tumbuhan B. reptans dengan jenis cacing yang ditemukan sebanyak empat jenis. Lokasi E didominasi oleh beberapa jenis tumbuhan dengan jenis cacing yang ditemukan sebanyak lima jenis. Spesies cacing Bunostomum sp. hanya ditemukan pada domba yang digembalakan di lokasi E.
Domba yang digembalakan di areal persawahan (lokasi A, B, dan C) umumnya memiliki keanekaragaman jenis cacing dan nilai FEC yang lebih rendah dibanding domba yang digembalakan di kebun tebu. Hal tersebut diduga karena domba digembalakan di sawah selama musim kemarau. Menurut Gordon (1948), musim kemarau merupakan masa yang sulit untuk perkembangan larva cacing, karena memiliki curah hujan dan kelembaban yang rendah. Peningkatan curah hujan dan kelembaban dapat meningkatkan nilai FEC. Domba yang digembalakan di lokasi E memiliki keanekaragaman jenis cacing dan nilai FEC yang lebih tinggi dibanding domba yang digembalakan di lokasi D. Hal tersebut karena domba digembalakan di lokasi E pada bulan Februari, dimana curah hujan dan kelembabannya lebih tinggi dibanding domba yang digembalakan di lokasi D pada bulan Desember.
Selain faktor diatas, faktor lain yang diduga mempengaruhi nilai FEC adalah adanya tumbuhan yang berpotensi antelmintik di lokasi penggembalaan. Pada lokasi penggembalaan diketahui terdapat tiga jenis tumbuhan yang memiliki potensi antelmintik. Ketiganya adalah Chrozophora rottleri, Heliotropium
indicum, dan Rhynchosia minima (Cordeiro dan Kaliwal 2012; Mahato et al.
2014; dan Priyanka et al. 2010). Ditemukan adanya tumbuhan C. rottleri dan H.
indicum pada lokasi B. Keberadaan tumbuhan tersebut diduga menjadi penyebab
rata-rata FEC pada lokasi B paling rendah. Sedangkan pada lokasi C, tidak didapati ketiga jenis tumbuhan yang mengandung senyawa antelmintik tersebut, sehingga diduga mengakibatkan rata-rata FEC di lokasi C paling tinggi dibanding lokasi lain. Lokasi A, D, dan E masing-masing didapati satu jenis tumbuhan yang mengandung senyawa antelmintik, sehingga rata-rata FEC tidak terlalu tinggi. Potensi antelmintik pada Chrozophora rottleri berasal dari ekstrak air pada daun (Patil et al. 2010). Menurut Mahato et al. (2014), Heliotropium indicum mengandung senyawa metanol yang memiliki potensi antelmintik. Aktivitas
11 antelmintik pada Rhynchosia minima diduga karena mengandung komponen aktif flavonoid, tanin, dan terpenoid (Cordeiro dan Kaliwal 2012).
SIMPULAN
Keanekaragaman jenis cacing dan nilai FEC pada domba, berbeda antar lokasi penggembalaan. Domba yang digembalakan di areal sawah pasca panen umumnya memiliki keanekaragaman jenis cacing dan nilai FEC yang lebih rendah dibanding domba yang digembalakan di kebun tebu. Pada lokasi yang terdapat tumbuhan yang diduga mengandung senyawa antelmintik, diperoleh nilai
FEC yang lebih rendah. Metode pengapungan garam jenuh dapat digunakan untuk
mengamati jumlah telur yang lebih banyak dibanding metode sedimentasi formalin-etil asetat. Metode pengapungan garam jenuh spesifik untuk jenis cacing
Moniezia benedeni dan Moniezia expansa, sedangkan metode sedimentasi
formalin-etil asetat spesifik untuk jenis cacing Bunostomum sp.
DAFTAR PUSTAKA
Baker DG, Baker RA, Ballweber LR, Berger DMP, Bowman DD, Byford RL, Cartner SC, Cogswell F, Craig ME, Craig TM, Fournie JW et al. 2007.
Flynn’s Parasites of Laboratory Animals. Ed ke-2. Iowa (US): Blackwell.
Batubara A. 2005. Pengaruh waktu rotasi gembala pada rumput Brachiaria
brizantha terhadap tingkat infestasi cacing Haemonchus contortus pada
ternak domba. Prosiding Seminar Nasional Teknologi Peternakan dan
Veteriner; 2004 Ags 4-5; Bogor, Indonesia. Bogor (ID): Pusat Penelitian
dan Pengembangan Peternakan. 354-359.
Chengaiah B, Kumar KM, Alagusundaram M, Sasikala C, Chetty CM. 2009. In-vitro anthelmintic activity of roots of Acalypha indica Linn. Int J
PharmTech Res. 1(4):1499-1502.
Cordeiro MC, Kaliwal BB. 2012. Antihelmintic activity of stem bark extract of
Bridelia retusa Spreng. IJABPT. 3(4):15-19.
Fachrul MF. 2007. Metode Sampling Bioekologi. Jakarta (ID): Bumi Aksara. Gordon MM. 1948. The epidemiology of parasitic diseases, with special reference
to studies with special nematode parasites of sheep. Austral Vet J. 24(2):17-45.
Ishtiaq M, Khan MA, Hanif W. 2006. Ethno veterinary medicinal uses of plants from Samahni Valley Dist. Bhimber, (Azad Kashmir) Pakistan. Asian J
Plant Sci. 5(2):390-396.
Kostermans AJGH, Soerjani M, Utomo IH, Wirjahardja S, Megia R, Laumonier EKW, Dekker RJ, Eussen JHH, Pons TL, Veenstra H. 1987. Weeds of Rice
in Indonesia. Jakarta (ID): Balai Pustaka.
Levine ND. 1990. Buku Pelajaran Parasitologi Veteriner. Ashadi G, penerjemah; Wardiarto, editor. Yogyakarta (ID): Gadjah Mada Univ Pr. Terjemahan dari:
12
Mahato K, Kakoti BB, Borah S, Kumar M. 2014. Evaluation of in-vitro anthelmintic activity of Heliotropium indicum Linn. leaves in Indian adult earthworm. Asian Pac J Trop Dis. 4(Suppl 4):S259-S262.
Mönnig HO, Phil BA. 1947. Veterinary Helminthology and Entomology. Ed ke-3. Baltimore (US): Williams & Wilkins.
Morley FHW, Donald AD. 1977. Farm management and systems of helminth control. Vet Parasitol. 6:105-134.
Niezen JH, Charleston WAG, Robertson HA, Shelton D, Waghorn GC, Green R. 2002. The effect of feeding sulla (Hedysarum coronarium) or lucerne (Medicago sativa) on lamb parasite burdens and development of immunity to gastrointestinal nematodes. Vet Parasitol. 105:229-245.
Priyanka P, Patel JK, Kulkarni PS, Patel MU, Bhavsar CJ, Patel JA. 2010. In vitro anthelmintic activity of various herbal plants extracts against Pheritima
posthuma. IJPP. 29(3):234-237.
Shaik SA, Terrill TH, Miller JE, Kouakou B, Kannan G, Kaplan RM, Burke JM, Mosjidis JA. 2006. Sericea lespedeza hay as a natural deworming agent against gastrointestinal nematode infection in goats. Vet Parasitol. 139(1-3):150-157.
Soulsby EJL. 1982. Helminths, Arthropods, and Protozoa of Domesticated
Animals. Ed ke-7. London (GB): Bailliere Tindall.
Southwell J, Fisk C, Sallur N. 2008. Internal Parasite Control in Sheep: reference
manual. Armidale (AU): Sheep CRC.
Tarazona JM. 1986. A method for interpretation of parasite egg count of faeces of sheep. Vet Parasitol. 22(1):113-119.
Van Steenis CGGJ. 1998. Flora: untuk sekolah di Indonesia. Surjowinoto M, penerjemah. Jakarta (ID): Pradnya Paramita Pr.
Whitlock HV. 1948. Some modifications of the McMaster helminth egg counting technique and apparatus. J Counc Sci Ind Res. 21:177-180.
Zajac AM, Conboy GA. 2012. Veterinary Clinical Parasitology. Ed ke-8. Oxford (GB): J Wiley.
13
LAMPIRAN
Lampiran 1 Data iklim makro Kecamatan Jatitujuh
Parameter October November December
Indoor humidity (%) 64,8 71,8 83,3 Indoor temperature (°C) 29,4 28,4 27,1 Outdoor humidity (%) 70,4 76 86,3 Outdoor temperature (°C) 28,9 28,2 27,1 Absolute pressure (mmHg) 755,5 753,8 753,9 Wind (m/s) 2,7 2,3 1,7 Gust (m/s) 3,5 3 2,4 Relative pressure (mmHg) 761 759,3 759,4 Dewpoint (°C) 22,6 23,1 24,4 Windchill (°C) 28,7 27,9 26,9 Hour rainfall (mm) 0,2 0,2 0,2 24 hour rainfall (mm) 5,4 4,2 5,3 Week rainfall (mm) 36,7 23,2 36,7 Month rainfall (mm) 43,6 115,9 153,1 Total rainfall (mm) 43,6 140,9 290,3 Wind level (bft) 2,1 1,8 1,5 Gust level (bft) 2,5 2,2 1,9
14
Lampiran 2 Kerapatan dan frekuensi relatif jenis tumbuhan di setiap lokasi Lokasi Spesies tumbuhan KR
(%) FR
(%) Lokasi Spesies tumbuhan
KR (%)
FR (%)
A Ammannia baccifera 1,44 17,86 D Brachiaria reptans 68,12 19,38
Chrozophora rottleri 0,61 10,71 Centella asiatica 3,23 16,13
Glinus lotoides 0,68 3,57 Cyperus difformis 0,28 3,22
Oryza sativa 6,40 17,86 Dichondra repens 0,28 6,45
Poaceae 1 86,75 17,86 Ludwigia peruviana 2,25 6,45
Sp. 1 0,06 3,57 Phyllanthus urinaria 0,84 3,22
Sphaeranthus africanus 0,61 10,71 Rhynchosia minima 10,53 16,13
Sphaeranthus indicus 3,45 17,86 Saccharum officinarum 2,25 16,13
B Alternanthera nodiflora 0,63 3,23 Sp. 5 7,16 6,45
Bergia ammannioides 0,47 1,61 Sp. 6 4,78 3,22
Chrozophora rottleri 1,11 4,84 Sphaeranthus indicus 0,28 3,22
Eriochloa polystachya 3,16 6,45 E Centella asiatica 4,99 10,17
Fimbristylis miliaceae 0,32 1,61 Cyperus difformis 0,23 1,70
Glinus lotoides 0,95 6,45 Cyperus iria 1,28 5,08
Heliotropium indicum 0,16 1,61 Dactyloctenium aegyptium 1,39 6,77
Houstonia longifolia 2,21 6,45 Digitaria ciliaris 17,87 10,17
Hydrolea zeylanica 0,47 4,85 Echinochloa colonum 13,81 10,17
Leptochloa chinensis 5,06 3,23 Eleusine indica 0,35 3,39
Ludwigia sp. 1,26 3,23 Fimbristylis miliaceae 0,12 1,70
Oryza sativa 6,32 6,45 Fimbristylis sp. 1,74 6,78
Panicum repens 1,26 6,45 Paspalum sp. 21,92 10,17
Poaceae 1 54,50 11,29 Rhynchosia minima 0,81 1,70
Sp. 1 0,95 6,45 Richardia brasiliensis 14,50 10,17 Sp. 2 0,16 1,61 Saccharum officinarum 5,45 10,17 Sp. 3 0,47 3,23 Sp. 7 15,31 8,47 Sp. 4 0,16 1,61 Sp. 8 0,23 3,39 Sphaeranthus indicus 3,16 6,45 Sutera cordata 17,06 11,29 Zea mays 0,16 1,61 C Ammannia baccifera 1,25 10,00 Cyperus difformis 1,25 6,60 Cyperus iria 0,50 3,40 Eriochloa polystachya 14,11 3,40 Fimbristylis miliaceae 50,56 16,60 Glinus lotoides 1,37 6,60 Houstonia longifolia 1,25 6,60 Ludwigia hyssopifolia 12,48 16,60 Ludwigia peruviana 9,11 10,00 Marsilea crenata 0,50 3,40 Oryza sativa 0,50 3,40 Phyllanthus debilis 0,38 3,40 Poaceae 1 3,12 3,40 Sphaeranthus indicus 3,62 6,60
15 Lampiran 3 Data sampel domba dan lokasi penggembalaan
Lokasi penggembalaan Sampel domba Umur (bulan) Jenis Kelamin Lokasi penggembalaan Sampel domba Umur (bulan) Jenis Kelamin A Sr 1 3 ♂ D Wm 1 8 ♂ Sr 2 24 ♀ Wm 2 3 ♀ Sr 3 5 ♀ Wm 3 8 ♀ Sr 4 24 ♀ Wm 4 7 ♂ Sr 5 5 ♂ Wm 5 7 ♀ B Mn 1 9 ♂ E Wm 6 6 ♀ Mn 2 24 ♀ Wm 7 24 ♀ Mn 3 7 ♀ Wm 8 1,5 ♂ Mn 4 7 ♂ Wm 9 1,5 ♂ Mn 5 7 ♀ Wm 10 12 ♀ Mn 6 60 ♀ Wm 11 7 ♀ Mn 7 18 ♀ Wm 12 2 ♂ C Mn 8 8 ♂ Wm 13 24 ♀ Mn 9 84 ♀ Mn 10 11 ♂ Mn 11 18 ♀ Mn 12 10 ♀ Mn 13 18 ♀ Mn 14 6 ♀ Mn 15 8 ♀
16
Lampiran 4 Data jenis dan jumlah cacing yang mengifeksi domba Sampel
Domba
Metode Pengapungan Metode Sedimentasi
Spesies FEC (telur/g) Spesies FEC (telur/g) Sr 1 - - - - Sr 2 - - Skrjabinema ovis 50 Sr 3 Moniezia benedeni 30 - - Moniezia expansa 30 Trichostrongylus spp. 30 Sr 4 - - Haemonchus contortus 50 Oesophagostomum spp. 300 Strongyloides pappilosus 100 Trichostrongylus spp. 150
Sr 5 Skrjabinema ovis 30 Strongyloides pappilosus 50
Strongyloides pappilosus 30 Mn 1 Schistosoma sp. 30 Oesophagostomum spp. 100 Mn 2 Strongyloides pappilosus 30 - - Mn 3 - - - - Mn 4 Strongyloides pappilosus 30 - - Mn 5 Oesophagostomum spp. 30 - - Mn 6 Strongyloides pappilosus 30 - - Mn 7 - - - - Mn 8 Oesophagostomum spp. 150 - - Trichostrongylus spp. 30 Mn 9 Haemonchus contortus 30 - - Mn 10 Oesophagostomum spp. 30 - - Mn 11 - - - - Mn 12 Oesophagostomum spp. 90 - - Trichostrongylus spp. 90
Mn 13 Haemonchus contortus 150 Oesophagostomum spp. 50
Oesophagostomum spp. 1860
Trichostrongylus spp. 150 Trichostrongylus spp. 100
Mn 14 Haemonchus contortus 120 Oesophagostomum spp. 50
Oesophagostomum spp. 180 Mn 15 Oesophagostomum spp. 90 - - Trichostrongylus spp. 30 Wm 1 Oesophagostomum spp. 270 - - Trichostrongylus spp. 90 Wm 2 Oesophagostomum spp. 60 - - Trichstrongylus spp. 30 Wm 3 Oesophagostomum spp. 90 - - Wm 4 Oesophagostomum spp. 60 Schistosoma sp. 50 Trichostrongylus spp. 90 Wm 5 Oesophagostomum spp. 180 - - Strongyloides pappilosus 30
Wm 6 Haemonchus contortus 210 Bunostomum sp. 50
Oesophagostomum spp. 450 Oesophagostomum spp. 100 Trichostrongylus spp. 300 Trichostrongylus spp. 50 Wm 7 Haemonchus contortus 120 - - Oesophagostomum spp. 240 Trichostrongylus spp. 180 Wm 8 - - - - Wm 9 Haemonchus contortus 30 - - Oesophagostomum spp. 60 Trichostrongylus spp. 30 Wm 10 Oesophagostomum spp. 120 Schistosoma sp. 50 Trichostrongylus spp. 60 Wm 11 - - - - Wm 12 Oesophagostomum spp. 90 - - Trichostrongylus spp. 30 Wm 13 - - - -
17 Lampiran 5 Gambar telur cacing yang ditemukan menginfeksi domba
Bunostomum sp. Haemonchus contortus Schistosoma sp.
Trichostrongylus sp. Oseophagostomum sp. Strongyloides pappilosus
18
Lampiran 6 Gambar cacing dewasa yang menginfeksi domba
Oesophagostomum spp. Haemonchus contortus Trichostrongylus spp. Strongyloides sp. Moniezia sp. Schistosoma sp.
19
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 10 Juni 1992. Penulis merupakan putri ketiga dari empat bersaudara, dari pasangan Bapak Homat Syukur dan Ibu Marsini. Penulis lulus dari SMA Negeri 112 Jakarta pada tahun 2010 dan melanjutkan pendidikan S1 di Departemen Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor melalui jalur Seleksi Nasional Masuk Perguruan Tinggi Negeri (SNMPTN).
Semasa studi penulis pernah menjadi penyaji makalah Seminar Nasional MIPA (Semirata) tahun 2014, asisten praktikum mata kuliah Biologi Dasar tahun 2013-2014, Botani Umum dan Struktur Hewan tahun 2014. Penulis melaksanakan Studi Lapangan tahun 2012 di di Taman Nasional Gunung Gede Pangrango dan kawasan Kebun Raya Cibodas, Jawa Barat dengan judul Diversitas Serangga di Kebun Raya Cibodas dan Taman Nasional Gunung Gede Pangrango, yang dibimbing oleh Dr Tri Atmowidi, MSi. Penulis melaksanakan kegiatan Praktik Lapangan tahun 2013 di PT Indofood Sukses Makmur Tbk. Bogasari Flour Mills Jakarta dengan judul Proses Pengolahan dan Analisis Mutu Tepung Terigu di PT Indofood Sukses Makmur Tbk. Bogasari Flour Mills, yang dibimbing oleh Dr Ir Nisa Rachmania Mubarik, MSi.