Isolasi, Enumerasi dan
dari Hutan Li
RAMDAN1
Balai Penelitian dan P Jln. Perintis Kemerdeka
Email: ramda
Hutan Lalindu merupakan berfungsi untuk mengatur tata wilayah hutan lindung ini menye salah satu mikroba tanah potensia nutrisi bagi tanaman, khususny enumerasi, dan karakterisasi bakt pada wilayah ini. Pengambilan sa tiap plot di areal hutan lindung y Sebanyak 1 kg tanah diambil pada dan selanjutnya dibawa ke labora areal Hutan Lindung Alami (HL) Terbakar (HT), yaitu 4,4 x 105 c kelompok Rhizobium dan 2 lainn serta tidak mampu tumbuh pada optimum pertumbuhan bervariasi Kata Kunci: Enumerasi, Hutan Li PENDAHULUAN
Berdasarkan Undang-Unda Tahun 1999 tentang Kehuta lindung merupakan kawasan mempunyai fungsi pokok perlindungan sistem penyangga untuk mengatur tata air, menc mengendalikan erosi, mencegah laut, dan memelihara kesubur (Kementerian Kehutanan, 2014 menunjang kegiatan pemba Indonesia, pemerintah membua dengan mengubah kawasan hut lahan yang diperuntukkan untuk infrastruktur, kepentingan indust perkebunan, peternakan, dan pe Laju deforestasi ini menimbulka yang dapat merusak lingkungan, lokal maupun global.
Hutan Lalindu merupakan hut yang dibiarkan tetap alami da kawasan pertambangan nikel P
n Karakterisasi Bakteri Fiksatif Nitro
n Lindung di Kawasan Pertambangan N
NA SARI1, RETNO PRAYUDYANINGSIH1 n Pengembangan Lingkungan Hidup dan Kehut dekaan Km. 16,5, Makassar, Sulawesi Selatan, K
mdana_sari@yahoo.co.id; prayudya93@yahoo. ABSTRAK
n hutan lindung yang berada di kawasan a air dan menjaga kesuburan tanah. Terjadi
yebabkan terjadinya degradasi lahan. Bakteri nsial untuk restorasi lahan marginal. Bakteri ini hususnya Nitrogen, dengan melakukan fiksasi N bakteri Rhizobia dilakukan untuk mengetahui st
n sampel tanah dilakukan dengan menentukan yang tidak terganggu (HL) dan hutan lindung pada kedalaman 0 20 cm lalu dimasukkan ke boratorium untuk proses selanjutnya. Kepadatan L) adalah 4,6 x 105cfu/gr lebih tinggi dibandi cfu/gr. Dari 14 isolat yang berhasil diisolasi innya termasuk Bradyrhizobium. Semua isolat
da pH 4 secara in vitro, tetapi tumbuh pada si untuk semua isolat.
n Lindung, Isolasi, Karakterisasi, Rhizobia
ndang No. 41 hutanan, hutan n hutan yang pokok sebagai gga kehidupan ncegah banjir, ah intrusi air suburan tanah 2014). Untuk bangunan di buat kebijakan hutan menjadi uk pemukiman, ndustri, pertanian, pertambangan. bulkan dampak an, baik secara n hutan lindung dan berada di PT. Stargate
Pasific Resources, K pertengahan tahun 2014, sebagian lahan dari huta kebakaran sehingga me degradasi lahan. Rusakn hutan menimbulkan da secara fisik, kimia, m Secara fisik, kebakaran tanah menjadi terbuka bahkan banjir. Bahan-akan mengalami pencu hujan sehingga akan b keberadaan mikroorgani dan pada akhirnya tanah unsur hara. Menurunny tanah akan menghamba pada lahan kritis.
Bakteri fiksatif merupakan salah satu m dapat memacu pertumbuha menyediakan unsur merupakan salah satu m
trogen Simbiotik
n Nikel
1 hutanan Makassar n, Kode Pos 90243 hoo.com n pertambangan nikel, adinya kebakaran pada eri Rhizobia merupakan ini mampu menyediakan N2 dari udara. Isolasi,status bakteri Rhizobia n 5 titik sampling pada ung yang terbakar (HT). ke dalam plastik sampel n bakteri Rhizobia pada ndingkan Hutan Lindung asi, 12 isolat termasuk solat bersifat aerob, motil, da pH 5 8 dimana pH
Konawe Utara. Pada hun 2014, saat musim kemarau, hutan lindung mengalami enyebabkan terjadinya usaknya vegetasi penutup dampak negatif, baik maupun biologi tanah. an hutan menyebabkan buka sehingga terjadi erosi n-bahan organik tanah ncucian (leaching) saat n berpengaruh terhadap anisme tanah potensial nah akan menjadi kahat unnya tingkat kesuburan bat proses rehabilitasi nitrogen simbiotik u mikroba potensial yang buhan tanaman dengan nitrogen. Nitrogen u makronutrien esensial
yang digunakan dalam proses sint asam amino, dan beberapa senya organik yang lain. Franche et
menyatakan bahwa senyawa ni dapat diasimilasi oleh tanaman, menjadi tersedia melalui prose nitrogen yang hanya dapat dil prokariotik. Shridhar (2012) m bahwa sekitar 386 x 1016 kg nitroge di atmosfer dan kembali ke proses siklus nitrogen. Mikr berperan dengan menambat 139 nitrogen dan 65% di antaranya ( disumbangkan oleh bakteri pem legum. Untuk menunjang keberha rehabilitasi di lahan-lahan pemanfaatan mikroba potensial salah satu alternatif strategi diterapkan. Oleh karena itu, per status bakteri fiksatif nitrogen areal hutan Lalindu.
METODE
Lokasi dan Waktu.Lokasi sampel yaitu di hutan lindung L berada di kawasan pertambanga Stargate Pacific Resources, Kona Sulawesi Tenggara. Areal sampel dibedakan menjadi berdasarkan kondisi hutan ya yaitu hutan lindung yang tida (HL) dan hutan lindung yang kebakaran (HT). Isolasi, enum karakterisasi bakteri fiksati dilakukan di laboratorium Mi Balai Penelitian dan Pe Lingkungan Hidup dan Kehutana pada bulan September Desembe
Alat Penelitian. Alat-digunakan di lapangan yaitu par dan plastik sampel. Sedangkan a digunakan di labotarium yaitu digital, Laminary Air Flow (LAF
magnetic stirrer,autoclave, incubat counter, beaker, erlenmeyer, c botol pengencer, tabung reaksi (15 ml), rak tabung reaksi, bunsen, spoit, gelas ukur, batang L, jarum (lurus dan bulat), object glass, de
mikroskop. sintesis protein, yawa nitrogen et al. (2009) nitrogen tidak n, tetapi akan proses fiksasi dilakukan oleh menambahkan trogen terdapat bumi dalam Mikroorganisme 139 x 109 kg (89 x 109 kg) pembintil akar rhasilan proses n marginal, nsial merupakan i yang dapat perlu diketahui n simbiotik di si pengambilan Lalindu yang gan nikel PT. onawe Utara, pengambilan di dua tipe yang berbeda, dak terganggu ng mengalami numerasi, dan ksatif nitrogen Mikrobiologi, Pengembangan anan Makassar ber 2015. at-alat yang parang, linggis, n alat-alat yang itu timbangan AF), hot plate, ubator, colony
, cawan petri, (15 ml dan 20 n, pipet tetes, arum inokulasi
ass, deg glass, dan
Bahan Penelitian. digunakan yaitu sampel (Yeast Extract Mannitol
(Yeast Extract Mannitol
(Sulfit Indole Motility
reagen pewarnaan Gra safranin 5%, H2O2 3%,
0,1 N, KOH, pH meter, dan aluminium foil.
Pengambilan Sam tanah diambil de menentukan 5 titik samp areal hutan lindung y (HL) dan hutan lindung Sebanyak 1 kg tanah dia 0 20 cm dan selanju dalam plastik sampel d berisi informasi tanggal plot dan areal.
Isolasi Bakteri Sebanyak 1 gram sampe dalam 9 ml NaCl 0,85% pengenceran 10-1 1 kemudian diambil seba pengenceran 10-2 10 dalam media YEMA, d 26°C selama 3 4 koloni bakteri yang tumb karakteristik morfologi kemudian ditumbuhkan dimodifikasi dengan indikator, media YEMA melihat sifat bakteri dal indikator, serta media
Blue untuk m
pertumbuhannya (Soma 1985). Setelah melakuk kemudian dibuat dalam b
Karakterisasi Nitrogen.Isolat bakteri telah diperoleh kem mikroskopik dengan pe Endospora serta uji motilitas, uji katalase, asam. Isolat yang teri
Bergey s Manual of Syst
HASIL DAN PEMBAH Kepadatan Kolon Nitrogen Simbiotik
an. Bahan-bahan yang pel tanah, media YEMA
tol Agar), media YEMB
tol Broth), media SIMA
y Agar), NaCl 0,85%, ram, Malachite green, 3%, minyak emersi, HCl r, aquadest, cling wrap, ampel Tanah. Sampel dengan sebelumnya mpling pada tiap plot di yang tidak terganggu ndung yang terbakar (HT). diambil pada kedalaman njutnya dimasukkan ke l dan diberi label yang ggal pengambilan sampel, i Fiksatif Nitrogen. pel tanah dilarutkan ke 0,85% dan dibuatkan seri 10-4. Suspensi tanah sebanyak 0,1 ml dari 10-4 dan diinokulasi ke , diinkubasi pada suhu 4 hari. Masing-masing umbuh dan menunjukkan ogi koloni yang berbeda buhkan pada media yang n penambahan larutan EMA+Congo Red untuk dalam menyerap larutan dia YEMA+Bromthymol
melihat kecepatan asegaran and Hobben, kukan pemurnian, isolat
bentuk stok bakteri. Bakteri Fiksatif ri fiksatif nitrogen yang mudian diuji secara pewarnaan Gram dan biokimia seperti uji se, dan uji ketahanan ridentifikasi mengikuti
Systemic Bacteriology. AHASAN
oloni Bakteri Fiksatif di Areal Hutan
Lindung Lalindu. Isolasi bakt nitrogen simbiotik yang dilakuk metode pengenceran bertingkat m jumlah koloni bakteri yang ber tiap jenis sampel tanah. Hasil pe koloni bakteri menunjukkan ba
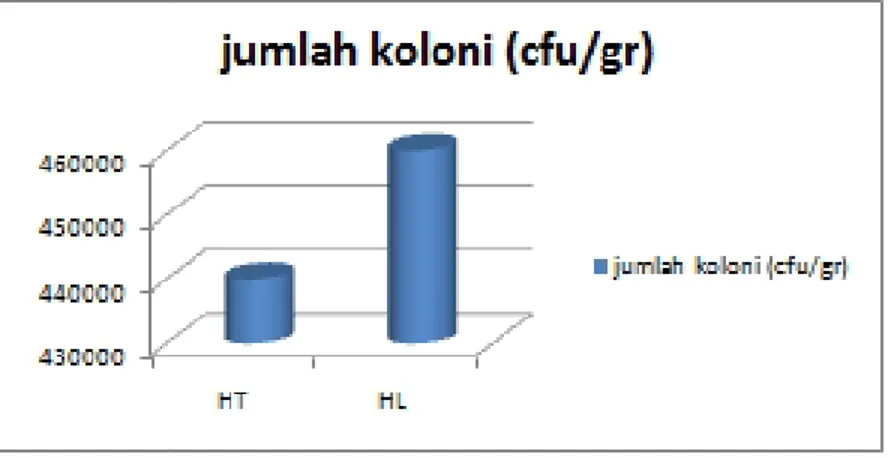
Gambar 1. J
Karakteristik Makroskop Fiksatif Nitrogen Simbiotik. S isolat yang telah diperoleh m karakteristik morfologi koloni ya beda dan tumbuh subur pada m Hasil pertumbuhan isolat pada m yang dimodifikasi dengan reagen Congo Red (CR) dan
Blue (BTB) menunjukkan ada respon terhadap larutan indika Pada media YEMA+CR, terlihat
Tabel 1. Karakteristik Morfologi K Media Pertumbuhan Yang
Isolat Kara Bentuk Elevasi HT.1.5 Irregular Flat HT.2.6 Circular Raised HT.3.2 Circular Raised HT.3.4 Irregular Flat HT.3.9 Circular Flat HT.4.1 Circular Raised HT.4.4 Circular Convex bakteri fiksatif kukan dengan t menunjukkan ervariasi pada l penghitungan bahwa jumlah
bakteri fiksatif nitrogen HL (Hutan Lindun dibandingkan areal H seperti yang terlihat pa ini.
1. Jumlah koloni bakteri fiksatif nitrogen simbiotik
opik Bakteri . Sebanyak 14 h menunjukkan yang berbeda-media YEMA. media selektif n penambahan n Bromthymol adanya variasi kator tersebut. hat bahwa isolat
tidak mampu atau han warna merah dari C
menunjukkan warna ko pink pucat (9 isolat), Sedangkan pada media bahwa 12 isolat termasu tumbuh cepat dan reaksi berwarna kuning), ser tumbuh lambat dan (media berwarna biru).
Koloni Isolat Bakteri Fiksatif Nitrogen Simbiotik ng Dimodifikasi
ararakteristik Morfologi Koloni
vasi Tepi Permukaan Warna
Undulate Smooth Putih
kecokelatan
d Entire Smooth Putih
kecokelatan
d Entire Smooth
(berlendir)
Putih kecokelatan
Curlied Smooth Putih
kecokelatan
Entire Smooth Cokelat
d Entire Smooth Putih
kekuningan
ex Entire Smooth
(berlendir)
Putih kekuningan
en simbiotik pada areal ndung) lebih tinggi HT (Hutan Terbakar) pada diagram di bawah
ik
hanya sedikit menyerap
Congo Red dengan koloni pink (1 isolat), ), dan putih (4 isolat). dia YEMA+BTB, terlihat suk ke dalam kelompok ksi bersifat asam (media serta 2 isolat lainnya n reaksi bersifat basa
.
ik Serta Respon Terhadap
Uji CR Uji BTB
Pink pucat Kuning
Pink Kuning
Pink pucat Kuning
Pink pucat Kuning
Pink pucat Kuning
Pink pucat Kuning
HT.4.5 Circular Raised HT.5.2 Circular Convex HL.1.3 Circular Raised HL.4.1 Circular Flat HL.5.4 Circular Flat HL.6.2 Irregular Raised HL.6.7 Circular Flat
Sifat dan Karakteristik M Bakteri Fiksatif Nitrogen. I bakteri kemudian dikarakteri
Tabel 2. Sifat dan Karakter Bakteri F
Isolat Pewarnaan Gram
Sifat Bentuk HT.1.5 (Negatif) Batang HT.2.6 (Negatif) Batang HT.3.2 (Negatif) Batang HT.3.4 (Negatif) Batang HT.3.9 (Negatif) Batang HT.4.1 (Negatif) Batang HT.4.4 (Negatif) Batang HT.4.5 (Negatif) Batang HT.5.2 (Negatif) Batang HL.1.3 (Negatif) Batang HL.4.1 (Negatif) Batang HL.5.4 (Negatif) Batang HL.6.2 (Negatif) Batang HL.6.7 (Negatif) Batang
Pewarnaan Gram yang dila ke-14 isolat menunjukkan bahwa diperoleh merupakan Gram Nega batang dan tidak memiliki endospor positif ditunjukkan pada uji kata terbentuknya gelembung udara preparat ditambahkan reag Begitupun pada uji motilitas, se menunjukkan hasil positi terbentuknya rambatan-rambat bakteri di sekitar bekas tusukan pada saat inokulasi. Pada uji ket secara in vitro, semua isolat ma pada pH 5 8, tapi tidak mampu t pH 4 dimana medium terlihat
d Entire Smooth Kuning
ex Entire Smooth (berlendir) Putih d Entire Smooth (berlendir) Putih kekuningan
Entire Smooth Putih
kecokelatan
Entire Smooth Putih
kecokelatan
d Lobate Smooth Putih
kekuningan
Entire Smooth Putih
kecokelatan
Mikroskopik Isolat murni erisasi untuk
mengetahui sifat dan ka Hasil pengujian dapat berikut.
i Fiksatif Nitrogen Hasil Uji Karakterisasi
Endospora Uji Katalase Uji Motilitas Uji K 4 Tidak ada + + -Tidak ada + + -Tidak ada + + -Tidak ada + + -Tidak ada + + -Tidak ada + + -Tidak ada + + -Tidak ada + + -Tidak ada + + -Tidak ada + + -Tidak ada + + -Tidak ada + + -Tidak ada + + -Tidak ada + + -dilakukan pada hwa isolat yang gatif berbentuk ndospora. Respon katalase dengan ara pada saat agen H2O2.
s, semua isolat positif dengan batan koloni usukan jarum ose ketahanan asam ampu tumbuh pu tumbuh pada hat bening dan
tidak menunjukkan ter bakteri.
Status Bakteri Simbiotik Pada Hutan koloni bakteri fiksatif ni dari tanah hutan Lalind tertinggi pada areal HL, sedangkan jumlah koloni 4.4 x 105 cfu/gr. Kond mengalami kebakar kerusakan pada veget organik tanah menjadi kematian tanaman legu mitra bakteri fiksatif ni bakteri yang berada di
Pink pucat Kuning
Putih Biru
Putih Kuning
Pink pucat Kuning
Putih Kuning
Pink pucat Kuning
Pink pucat Biru
n karakter yang dimiliki. pat dilihat pada tabel
ji Ketahanan Asam 5 6 7 8 + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + + terjadinya pertumbuhan i Fiksatif Nitrogen an Lalindu. Enumerasi nitrogen yang diisolasi ndu menunjukkan hasil L, yaitu 4.6 x 105cfu/gr, oni pada areal HT yaitu ondisi hutan yang telah karan menyebabkan etasi sehingga bahan di berkurang. Selain itu, egum yang merupakan nitrogen menyebabkan di dalam bintil akar pun
mati. Meskipun demikian, kepada Rhizobia di areal HT ini masih dibandingkan di lahan bekas tam Hasil penelitian Sari dan Pray (2016) menyatakan kepadat Rhizobia di lahan bekas tam
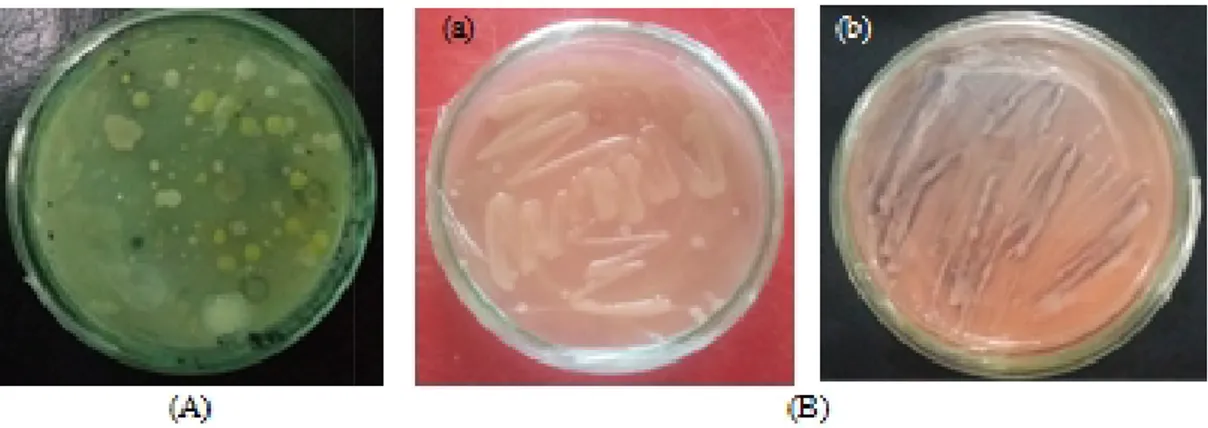
Gambar 2. (a) areal Hut
Karakteristik Morfologi Bakteri Rhizobia. Bakteri Rhi diperoleh memiliki karakteristi koloni yang berbeda-beda. berbentuk circular dan irregul
elevasi flat, raised, dan conv
memiliki tepi koloni yang berbed seperti entire, curlied, lobate, da dengan permukaan yang lembut, yang berlendir (tabel 1). Isol Rhizobia dari tanaman legum dilakukan oleh Bhargava et al
wilayah Seriarid, Tirupati, India m koloni bakteri berbentuk ci irregular, elevasi flat, raised, hingg serta tepi entire dan lobate. K (2009) menambahkan bahwa Rhi ditumbuhkan pada media yang mannitol menghasilkan eksopol (EPS) yang tinggi. Rhizobia m EPS untuk pembentukan nodul nitrogen pada tipe nodul-legum inde EPS berperan dalam inva perkembangan nodul, pelepasan benang infeksi, perkembangan ba penekanan terhadap respons
padatan bakteri sih lebih tinggi tambang nikel. rayudyaningsih datan bakteri ambang nikel
sebesar 2.5 x 105cfu/gr x 105 cfu/gr (areal reve 3.6 x 105 cfu/gr (areal r soil), dan 3.9 x 105 cf alami).
utan Lindung Alami (HL); (b) areal Hutan Lindung
ologi Koloni Rhizobia yang stik morfologi . Ada yang rreguler dengan convex. Isolat beda-beda pula, , dan undulate
but, bahkan ada Isolasi bakteri um liar yang al. (2016) di a menunjukkan circular dan hingga convex, Kumari et al. Rhizobia yang g mengandung ksopolisakarida memproduksi nodul pemfiksasi indeterminate. invasi dan san bakteri dari n bakteroid, dan spons pertahanan
tanaman dan perlindunga antimikroba tanaman (H
Koloni yang terpisa ciri-ciri morfologi kol kemudian diinokula YEMA+CR. Hasil pen bahwa semua isolat tida sedikit menyerap warna indikator (tabel 2). Se dilakukan oleh Shetta semua isolat Rhizobium
pada media yang m diinkubasi selama 3 ha tidak menyerap larutan pada media YEMA+B isolat mampu menguba warna kuning dan 2 mampu mengubah warn Harpreet et al. (2012) medium YEMA+BTB mengelompokkan bakt memliki pertumbuhan berdasarkan produksi a media. Pada medium ya koloni bakteri Rhizobi
berubah menjadi kuni produksi asam oleh mikr
r (arealbackfilling), 3.5 vegetasi tanpa top soil), l revegetasi dengan top cfu/gr (areal tersuksesi
ndung Terbakar (HT)
ndungan terhadap senyawa (Hidayat, 2013).
pisah dan menunjukkan koloni yang berbeda nokulasi pada media pengujian menunjukkan idak mampu atau hanya rna merah dari larutan Sesuai penelitian yang a et al. (2011) bahwa
zobium yang ditumbuhkan mengandung CR dan hari tumbuh cepat dan an indikator. Pengujian BTB menunjukkan 12 ngubah media menjadi 2 isolat lainnya tidak arna media (tetap biru). 2012) menyatakan bahwa B digunakan untuk bakteri Rhizobia yang n cepat dan lambat asam atau alkali pada yang mengandung BTB,
zobium dan medium kuning karena adanya ikroorganisme. Shettaet
al. (2011) menambahkan bahw asam diamati setelah isolat diinkuba pada suhu 28°C dengan meng medium menjadi kuning. Wakt pada kultur YEMB antara 2,07 da pada suhu 28°C. Bradyrhizobi
Gambar 3. A. Hasil isolasi bakteri R YEMA; B. Uji CR : (
Sifat dan Karakter Bakte Karakterisasi mikroskopik yan pada semua isolat Rhizobia m bahwa bakteri bersifat Gram ne berbentuk batang dan tidak endospora (Gambar 3). Hal ini se
Gambar 4. (a) Sel terlihat berbentuk tidak terlihat adanya endospora (di pew
Empat belas isolat membe yang positif terhadap uji katalase. menandakan isolat bersifat a membutuhkan oksigen dala
hwa produksi nkubasi 72 jam ngubah warna aktu generasi 2,07 dan 3,85 jam rhizobium yang
tumbuh lambat mem ukuran kecil (diameter setelah 7 10 hari ink danmucoid, umumnya k ataucream(Gyorgiet al
i Rhizobia dari sampel tanah hutan lindung yang di : (a) koloni berwarna putih; (b) koloni berwarna pi
teri Rhizobia. ang dilakukan menunjukkan negatif yang dak memiliki ni sesuai dengan
penelitian yang dilakuk (2010) yang menunjukk Rhizobia terseleksi yang rumput di pegununga bakteri Gram Negatif b tidak memiliki endospor
tuk batang dan berwarna merah (Gram Negatif) pada (ditandai dengan tidak adanya organel berwarna hij pewarnaan endospora (perbesaran 40 x 10)
berikan hasil se. Hasil uji ini aerob, yaitu dalam proses
metabolismenya (tabel (2010) bahwa umumny diperoleh bersifat aerob bersifat anaerob fakult
miliki koloni dengan ter sekitar 1 2 mm) inkubasi, elevasi raised
a koloni berwarna putih
al. 2010).
ng ditumbuhkan pada media pink pucat
kukan oleh Gyorgi et al. ukkan bahwa 50 isolat ang berasal dari padang gan Ciuc merupakan f berbentuk batang dan ndospora.
ada pewarnaan Gram; (b) hijau) di dalam sel pada
bel 2). Gyorgi et al. nya strain isolat yang ob dan 12 strain lainnya kultatif. Beberapa strain
mampu memanfaatkan nitrat seba elektron untuk tumbuh seca dimana nitrat diubah menjadi nitr isolat bersifat motil yang ditanda adanya rambatan-rambatan koloni sekitar bekas tusukan jarum inokul dengan penelitian Shahzad et
bahwa semua sampel bakteri Rhi
Gambar 5. (a)
Kemampuan Rhizobia unt menginfeksi tanaman, dan menam dari udara bebas dipengaruhi ol lingkungan, termasuk pH ta penelitian menunjukkan semua mampu tumbuh pada pH 4 secara mampu tumbuh pada pH 5, 6, 7, 2). Tsegaye et al. (2015) menya 44% isolat Rhizobia yang di
Trigonella foenum-graecum L. t tumbuh pada pH 4.5 dan 56% t pH 4.5 9, pertumbuhan optim 6.5 8.5. Kisaran pH optimal unt Rhizobia adalah sedikit di ba hingga agak alkali. pH media langsung berhubungan dengan pH merupakan habitat bakteri terse Rhizobia cenderung mampu tum media yang bersifat alkali.
KESIMPULAN
Rhizobia merupakan salah sa tanah potensial untuk pertumbuhan tanaman pada l Bakteri simbiotik ini mampu m unsur nitrogen yang dapat di tanaman dalam proses meta
sebagai akseptor cara anaerob, nitrit. Selain itu, ditandai dengan koloni bakteri di nokulasi. Sesuai
et al. (2012) Rhizobia yang
diisolasi dari nodul A hasil yang positif terh Rhizobia dapat menggunakan 2-6 flagel atau 1 flagela pa (Bradyrhizobium) (Soma 1985).
a) uji katalase; (b) uji ketahanan pH 4 8; (c) uji m
untuk tumbuh, nambat nitrogen uhi oleh kondisi tanah. Hasil ua isolat tidak ra in vitro, tapi 6, 7, dan 8 (tabel yatakan sekitar diisolasi dari . tidak mampu tumbuh pada imum pada pH l untuk bakteri bawah netral a secara tidak n pH tanah yang rsebut. Bakteri tumbuh pada h satu mikroba mendukung lahan kritis. pu menyediakan dimanfaatkan etabolismenya.
Isolasi bakteri Rhizobia Lalindu menunjukkan Rhizobia di Hutan Lindu (4,6 x 105 cfu/gr) diba Lindung Terbakar (4,4 x isolat yang berhasil di isolat termasuk ke
Rhizobium dan 2 isol
Bradyrhizobium. Semua bakteri aerob, motil, ti pada pH 4 secara in vitr pH 5 8. Bakteri ini hany nitrogen apabila beras legum membentuk nodul restorasi lahan marginal penyediaan unsur hara nitrogen, oleh bakteri Rh UCAPAN TERIMA K
Ucapan terima ka kepada PT. Stargate, pemerintah setempat a kami bisa melakukan p sampel penelitian pada hut di kawasan pertambanga Ucapan terima kasih Hajar, S.Hut, M.Hut
Alfalfa menunjukkan erhadap uji motillitas. bergerak dengan gela peritrik (Rhizobium) pada kutub/subkutub omasegaran and Hobben,
motilitas
obia pada hutan lindung ukkan kepadatan bakteri ndung Alami lebih tinggi dibandingkan di Hutan 4,4 x 105 cfu/gr). Dari 14 diisolasi, sebanyak 12 ke dalam kelompok solat lainnya termasuk ua isolat merupakan , tidak mampu tumbuh vitro, tetapi tumbuh pada hanya mampu menambat rasosiasi dengan akar nodul. Keberhasilan nal dapat dicapai melalui hara tanaman, terutama
Rhizobia. KASIH
kasih kami sampaikan , Konawe Utara, dan atas izinnya sehingga n pengambilan data dan da hutan lindung Lalindu ngan nikel PT. Stargate.
h juga kepada Bapak ut dan Bapak Edi
Kurniawan, S.Hut, M.Hut membantu selama melakukan penelitian di lapangan, serta A. Dania, S.Si, Hartini, SP da Ummusyahidah, S.Hut yang tela di Laboratorium Mikrobiol Penelitian dan Pengembangan Hidup dan Kehutanan Makassar. DAFTAR PUSTAKA
Bhargava, Y., J. S. R. Murthy Kumar, and M. N. R Phenotypic, stress toleranc growth promoting charac rhizobial isolates from se legumes of Semiarid Region, India. Advances in Mi Published Online January Scribes. http://scirp.org/journa Franche, C., K. Lindstrom, and
2009. Nitrogen-fixing bacter with leguminous and non plants. Plant Soil, 321 : 35 Gyorgi, E., G. Mara, I. Mathe, M.,
K. Marialigeti, B. Albert, F. S. Lanyi. 2010. Character diversty of the nitrogen fixing from a specific grassland ha Ciuc mountains. Biotechnological Letter, 15 5481.
Harpreet, K., P. Sharma, N. Kaur Gill. 2012. Phenotypic and characterization of Bradyrhi Ensifer spp. isolated from rhizosphere. Bioscience Disc : 40 46.
Hidayat, C. 2013. Struktur eksopolisakarida dalam simbi
Rhizobium. Jurnal Kajian dan Teknologi, 7 (1) : 18 32. Kementerian Kehutanan. 2014.
Kementerian Kehutanan Tahun 2013. Kumari, B. S., M. R. Ram, Mallaiah. 2009. Studi yang telah n survey dan . Sri Rahmah dan Mutiah elah membantu obiologi, Balai n Lingkungan ssar. thy, T. V. R. Rao. 2016. nce and plant racteristics of selected wild gion, Tirupati, Microbiology. nuary 2016 in ournal/aim. nd C. Elmerich. teria associated non-leguminous 59. , M., E. Laslo, F. Oancea, and terization and ing microbiota d habitat in the Romanian 15 (4) : 5474 aur, and B. S. nd biochemical rhizobium and from soybean iscovery, 3 (1) ur dan fungsi mbiosis legum-n Islam, Sailegum-ns 32. 2014. Statistik Tahun 2013. , and K. V. Studies on exopolysaccharide a production by Rhi Indigofera. Afri Microbiology Resea Sari, R. dan R. Pra Populasi dan jeni nitrogen simbiotik tambang nikel. Nasional Biologi 2016 dalam Peningk Keragaman Hayat Fakultas Matem Pengetahuan A Hasanuddin. Makass Shahzad, F., M. Shafee M. M. Tariq, and Isolation and characterization of from root nodules
sativa). Journal Sciences, 22 (2) : 522 Shetta, N. D., T. S. A
Abdel-Aal. 2011. characterization of Rhi
with woody legum Saudi Arabia condi Eurasian Journal Environment Scienc 418. Shridhar, B. S. 2012. fixing microorgani Journal of Microbiol 46 52. Somasegaran, P. and Methodes in Technology. Hawai Agriculture and Hum Tsegaye, M., F. Assefa,
Symbiotic a
characterization of nodulating
(Trigonellafoenum-grae
north and east International Journa Agricultural Researc
de and indole acetic acid
Rhizobium strains from frican Journal of search, 3 (1) : 10 14.
rayudyaningsih. 2016. enis bakteri penambat otik di lahan bekas . Prosiding Seminar 2016 Peranan Biologi ngkatan Konservasi yati , 6 Juni 2016. matika dan Ilmu Alam. Universitas kassar.
ee, F. Abbas, S. Babar, and Z. Ahmad. 2012.
and biochemical
of Rhizobium meliloti
es of Alfalfa (Medico
animal and Plant 522 524.
. Al-Shaharani, and M. 2011. Identification and ofRhizobium associated ume trees grown under condition. American-nal Agriculture and
ences, 10 (3) : 410 2. Review : Nitrogen ganisms. International obiology Research, 3 (1) : nd H. J. Hoben. 1985. Legume-Rhizobium
aii Institute of Tropical uman Resources. fa, and J. Zeleke. 2015.
and phenotypic
of Rhizobium isolates Fenugreek
-graecum L.) from st Shewa, Ethiopia. ournal of Agronomy and