commit to user
SINTESIS DAN KARAKTERISASI KIMIA FISIKA
Mg/Al-
HYDROTALCITE
SEBAGAI BAHAN BAKU ANTASIDA
Disusun Oleh :
EKA FITRIANI AHMAD
(M0307038)
SKRIPSI
Diajukan untuk memenuhi sebagian
persyaratan mendapatkan gelar Sarjana Sains
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SEBELAS MARET
SURAKARTA
commit to user
Jurusan Kimia FakultasSebelas Maret Surakarta telah
Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sebelas Maret Surakarta telah mengesahkan skripsi mahasiswa :
Ahmad NIM M0307038, dengan judul “Sintesis dan Karakterisasi ydrotalciteSebagai Bahan Baku Antasida”.
Skripsi ini dibimbing oleh :
Pembimbing I
, M.Si. Ahmad Ainurofiq, M.Si., Apt. NIP. 19640305 200003 1002 NIP. 19780319 200501 1003
Dipertahankan di depan Tim Penguji Skripsi pada : Hari : Rabu
commit to user
iii
PERNYATAAN
Dengan ini saya menyatakan bahwa skripsi saya yang berjudul “SINTESIS DAN KARAKTERISASI KIMIA FISIKA Mg/Al-HYDROTALCITESEBAGAI BAHAN BAKU ANTASIDA” adalah benar-benar hasil penelitian sendiri dan tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi, dan sepanjang pengetahuan saya juga tidak terdapat kerja atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain, kecuali yang secara tertulis diacu dalam naskah ini dan disebutkan dalam daftar pustaka.
Surakarta, 25 Juli 2012
commit to user
iv
SINTESIS DAN KARAKTERISASI KIMIA-FISIKA
Mg/Al-HYDROTALCITESEBAGAI BAHAN BAKU ANTASIDA
EKA FITRIANI AHMAD
Jurusan Kimia. Fakultas Matematika dan Ilmu Pengetahuan Alam. Universitas Sebelas Maret
ABSTRAK
Telah dilakukan sintesis dan karakterisasi kimia fisika dari Mg/Al-hydrotalcite. Penelitian ini bertujuan untuk membuat Mg/Al-hydrotalcite sebagai bahan baku antasida. Sintesis Mg/Al-hydrotalcite dengan anion interlayer karbonat dilakukan pada rasio mol Mg/Al 2 : 1 dan pH 10 selama 1 jam. Karakterisasi hasil sintesis Mg/Al-hydrotalcite menggunakan X-Ray Diffraction, X-Ray Fluorescence dan Fourier Transform Infra Red, Thermo Gravimetric-Differential Thermal Analysisdan Surface Area Analyzer, sedangkan karakterisasi kimia fisika Mg/Al-hydrotalcite sebagai bahan baku antasida meliputi penentuan berat jenis (nyata, benar, dan mampat), sifat alir (faktor Hausner, porositas, dan kompresibilitas), kandungan lembab (moisture content), pH, kapasitas penetralan asam, dan kelarutan (pH 1, pH 2, pH 3, dan pH 4).
Karakterisasi material hasil sintesis dari penelitian ini merupakan suatu material padatan yang memiliki basal spacing d003 7,61 Å, d006 3,79 Å, dan
d009 2,57 Å dan merupakan ciri Mg/Al-hydrotalcite dengan anion karbonat pada
interlayer. Pada data XRF terdapat senyawa Mg-O dan Al-O dengan perbandingan rasio mol mendekati 2 : 1. Sementara itu, keberadaan gugus fungsi diverifikasi dengan adanya gugus hidroksi pada daerah bilangan gelombang 3444,87 cm-1 dan gugus karbonat pada 1361,74 cm-1. Data ini juga didukung dengan data TG-DTA bahwa terjadi pelepasan hidroksi, karbonat dan juga terdeteksi adanya degradasi struktur Mg/Al-hydrotalcite. Pada data SAA menunjukkan bahwa pori Mg/Al-hydrotalcite merupakan kelompok mesopori. Sementara itu, karakterisasi kimia fisika dari Mg/Al-hydrotalcite hasil sintesis pada kapasitas penetralan asam dan pH sesuai denganhydrotalcitekomersial pada bahan baku antasida. Namun, memiliki perbedaan pada berat jenisnya. Hal ini dikarenakan berat molekul hydrotalciteyang digunakan berbeda dari segi struktur pembentuk anion penyeimbangnya. Mg/Al-hydrotalcite memiliki sifat alir yang baik, larut pada pH yang sangat rendah (pH=1) dan kelarutan semakin menurun seiring dengan kenaikan pH.
commit to user
v
SYNTHESIS AND CHARACTERIZATION CHEMICAL PHYSICS OF Mg/Al-HYDROTALCITE AS BASIC MATERIAL OF ANTACIDA
EKA FITRIANI AHMAD
Department of Chemistry. Faculty of Mathematics and Natural Sciences. Sebelas Maret of University
ABSTRACT
Synthesis, characterization and chemical physics characteristic test of Mg/Al-hydrotalcite had been carried out. The purpose of this research is to make Mg/Al-hydrotalcite as basic material of antacida. Mg/Al-hydrotalcite was synthesized with mole ratio of Mg/Al 2:1 and pH 10 for one hours. Characterization of synthesized Mg/Al-hydrotalcite was done by using X-Ray Diffraction, X-Ray Flourosence and Fourier Transform Infra Red, Thermo Gravimetric-Differential Thermal Analysis and Surface Area Analyzer, while the chemical physics characterization of Mg/Al-hydrotalcite as a raw material of antacids include determining specific gravity (lossed, true, and tapped), the flow properties (Housner factor, porosity, and compressibility), moisture content, pH, acid neutralization capacity, and solubility (pH 1, pH 2, pH 3 and pH 4).
Characterization of the result from synthesized material was a solid material with basal spacing of d0037.61 Å, d0063.79 Å and and d0092.57 Å which
was characteristic of Mg/Al-hydrotalcite with carbonate anions in the interlayer. The result by XRF analysis presented that there are compounds Mg-O and Al-O with a mole ratio about 2:1. Meanwhile, the functional groups verified by presence of hydroxy groups on the 3444.87 cm-1and carbonate groups at 1361.74 cm-1. The result also were supported by TG-DTA analysis that the release of hydroxide, carbonate, and also detected by degradation of the structure of Mg/Al-hydrotalcite. SAA analysis showed that the Mg/Al-hydrotalcite pore was a group of mesopores. Meanwhile, the chemical physics characterization of acid neutralization capacity and with commercial hydrotalcite of antacids. This case because of the molecular weight structure hydrotalcite whice used were different anion balanced form structure. Mg/Al-hydrotalcite has a good flow properties, soluble at extreme pH (pH = 1) and the solubility decreases with increase in pH.
.
commit to user
vi
MOTTO
Katakanlah: “Sesungguhnya shalatku, ibadahku, hidupku dan matiku
hanyalah untuk Allah, Rabb semesta alam. Tiada sekutu bagi-Nya; dan demikian
itulah yang diperintahkan kepadaku dan aku adalah orang yang pertama-tama
menyerahkan diri (kepada Allah)”
(Q.S. Al An’am: 162-163)
“Sesungguhnya sesudah kesulitan itu ada kemudahan. Maka apabila kamu
telah selesai (dari suatu urusan), Kerjakanlah dengan sungguh-sungguh”
(Alam Nasyarh: 6-7)
“Buah keberhasilan berasal dari kerja keras dan kesabaran yang tak
pernah lelah”
(Suryani Ahmad)
“Sesuatu yang belum dikerjakan, seringkali tampak mustahil; kita baru yakin
kalau kita telah berhasil melakukannya dengan baik”
commit to user
vii
PERSEMBAHAN
Alhamdulillah wa syukurillah, akhirnya sebuah karya ini dapat kupersembahkan kepada :
Allah Maha Besar atas rahmatnya, “my inspiration” Muhammad SAW.
Mama, terimakasih atas iringan doa yang tak pernah henti dan memotivasi yang tak pernah letih, seperti cahaya menerangi kegelapan.
Fakhri Irfan Zakiey, adik yang memberiku inspirasi seperti malaikat kecil yang mengajari ku banyak hal tentang kehidupan, kesabaran, kerja keras dan kasih sayang. Terus semangat adikku sayang, tetaplah berjuang untuk kehidupan. Terimakasih banyak atas pengorbananmu sehingga kakakmu ini bisa mendapatkan gelar sarjana, terimakasih banyak.
Papa, terimakasih atas pelajaran hidup yang luar biasa.
Dewi Holymarindah, terimakasih atas doamu, motivasimu dan kesabaranmu menanti kelulusanku.
commit to user
viii
KATA PENGANTAR
Puji syukur penulis panjatkan ke hadirat Allah Subhanahu Wa Ta’ala atas segala rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan skripsi dengan judul “Sintesis dan Karakterisasi Kimia Fisika Mg/Al-hydotalciteSebagai Bahan Baku Antasida”.
Skripsi ini tidak akan selesai tanpa adanya bantuan dari banyak pihak, karena itu pada kesempatan ini penulis menyampaikan terima kasih kepada :
1. Bapak Dr. Eddy Heraldy, M.Si. selaku Ketua Jurusan Kimia FMIPA UNS dan sebagai pembimbing I, yang telah memberikan banyak motivasi. Pesan moril yang akan selalu penulis ingat yaitu “Hidup harus profesional dan harus bertahan dalam tekanan apapun”.
2. Bapak Ahmad Ainurofiq, M.Si., Apt. selaku pembimbing II, yang telah memberikan motivasi dan menginspirasi penulis.
3. Bapak Edy Pramono, M.Si., selaku Pembimbing Akademik. 4. Ibu Dr. Sayekti Wahyuningsih, M.Si, selaku Penguji 1. 5. Ibu Dr. Triana Kusumaningsih, M.Si, selaku Penguji 2
6. Bapak I.F. Nurcahyo, M.Si. selaku Ketua Lab Kimia Dasar FMIPA UNS. 7. Bapak/Ibu Dosen pengajar dan semua staf Jurusan Kimia.
8. Keluarga besar penulis atas doa dan dukungannya.
9. Teman serta sahabat seperjuangan Kusworo Aris Prasetiyo S.S, Hidayat Jati S.Si, Muh. Yanwar Prasetyo S.Si, Fajar Indah Puspitasari, Meirina Kusumaningtyas, dan Dwi Wahyuni atas semangat dan dukungannya.
10. Semua pihak yang tidak dapat penulis sebutkan satu persatu.
Surakarta, 25 Juli 2012
commit to user
ix
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PENGESAHAN ... ii
HALAMAN PERNYATAAN ... iii
HALAMAN ABSTRAK ... iv
HALAMAN ABSTRACT ... v
HALAMAN MOTTO ... vi
HALAMAN PERSEMBAHAN ... vii
KATA PENGANTAR ... viii
DAFTAR ISI ... ix
DAFTAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I. PENDAHULUAN ... 1
A. Latar Belakang Masalah ... 1
B. Perumusan Masalah ... 3
1. Identifikasi Masalah ... 3
2. Batasan Masalah ... 4
3. Rumusan Masalah ... 4
C. Tujuan Penelitian ... 5
D. Manfaat Penelitian ... 5
BAB II. LANDASAN TEORI ... 6
A. Tinjauan Pustaka ... 6
1. Hydrotalcite... 6
a. Struktur hydrotalcite... 6
b. Sifat hydrotalcite ... 8
c. Sintesis Mg/Al-hydrotalcite... 9
d. Karakterisasi Mg/Al-hydrotalcite... 10
2. Antasida... 16
commit to user
x
b. Karakterisasi bahan baku antasida... .. 18
B. Kerangka Pemikiran ... 22
C. Hipotesis ... 23
BAB III. METODOLOGI PENELITIAN ... 24
A. Metode Penelitian ... 24
B. Tempat dan Waktu Penelitian ... 24
C. Alat dan Bahan ... 25
D. Prosedur Penelitian ... 26
1. Sintesis dan Karakterisasi Mg/Al-hydrotalcite ... 26
2. Karakterisasi Bahan Baku Antasida ... 26
a. Berat jenis nyata ... 26
b. Berat jenis benar ... 26
c. Berat jenis mampat ... 27
d. Kandungan lembab ... 27
e. Penentuan pH... ... 27
f. Kapasitas penetralan asam... 27
f. Kelarutan ... 27
E. Teknik Pengumpulan dan Analisis Data ... 28
BAB IV. HASIL PENELITIAN DAN PEMBAHASAN ... 30
A. Sintesis Mg/Al-hydrotalcite... 30
B. Karakterisasi Material Hasil Sintesis ... 31
1. Identifikasi Senyawa Hasil Sintesis... 31
2. Analisis Gugus Fungsi ... 34
4. Analisis Termal... 35
5. Analisis Permukaan... 37
C. Karakterisasi Bahan Baku Antasida ... 38
2. Berat Jenis ... 39
3. Sifat Alir ... 40
4. Kandungan Lembab... 42
5. pH... 42
commit to user
xi
6. Kelarutan ... 43
BAB V. KESIMPULAN DAN SARAN ... 44
A. Kesimpulan ... 44
B. Saran ... 44
DAFTAR PUSTAKA ... 46
commit to user
xii
DAFTAR TABEL
Tabel 1. Gugus fungsi Mg/Al-hydrotalcite... 12
Tabel 2. Basal spacingpuncak tertinggi Mg/Al-hydrotalcitehasil sintesis... 32
Tabel 3. Hasil analisis XRF... 33
Tabel 4. Perbandingan gugus fungsi Mg/Al-hydrotalcite... 34
Tabel 5. Hasil analisis SAA... 38
commit to user
xiii
DAFTAR GAMBAR
Gambar 1. Struktur (Cavani et al.,1991)... 7
Gambar 2. Struktur senyawa brucite(Goh et.al., 2008)... 7
Gambar 3. Skema struktur senyawa hydrotalcite(Murphyet al., 2004)... 8
Gambar 4. Aplikasi hydrotalcite(Moyo, 2009)... 8
Gambar 5. Difraktogram XRD Mg/Al-hydrotalcite(Sharma et al., 2008)... 10
Gambar 6. Kurva TG/DTA (Cavani et al.,1991)... 14
Gambar 7. Dekomposisi Mg/Al-hydrotalcite(Moyo, 2009)... 15
Gambar 8. TGA Mg/Al-hydrotalcite-CO3(Sharma et al., 2008)... 15
Gambar 9. Foto senyawa hasil sintesis... 31
Gambar 10. Profil difraktogram XRD (a) Mg/Al hydrotalcitestandar (Sharma et. al., 2008) (b) Mg/Al hydrotalcitehasil sintesis... 31
Gambar 11. Spektra Inframerah (a) Mg/Al-hydrotalcite(Sharma et al., 2007) (b) Mg/Al-hydrotalcitehasil sintesis... 34
commit to user
xiv
DAFTAR LAMPIRAN
Lampiran 1. Perhitungan sintesis Mg/Al-hydrotalcite... 54
Lampiran 2. Sintesis Mg/Al-hydrotalcite... 55
Lampiran 3. Data JCPDS Mg/Al-hydrotalcite... 56
Lampiran 4. Hasil XRD Mg/Al-hydrotalcite... 57
Lampiran 5. Perhitungan kemurnian Mg/Al-hydrotalcite... 58
Lampiran 6. Data X-Ray Flourosence(XRF) ... 59
Lampiran 7. Data Fourier Transform Infra Red(FTIR)... 60
Lampiran 8. Data Thermo Gravimetric-Differential Thermal Analysis... 61
Lampiran 9. Data Surface Area Analyzer(SAA)... 62
Lampiran 10. Penentuan berat jenis nyata dan berat jenis benar ... 64
Lampiran 11. Penentuan berat jenis mampat ... 65
Lampiran 12. Penentuan kandungan lembab dan penentuan pH... . 66
Lampiran 13. Penentuan kapasitas penetralan asam... 67
Lampiran 14. Penentuan kelarutan ... 68
Lampiran 15. Perhitungan berat jenis nyata ... 69
Lampiran 16. Perhitungan berat jenis benar... 70
Lampiran 17. Perhitungan berat jenis mampat... 71
Lampiran 18. Perhitungan porositas, faktor Hausner dan kompresibilitas... 72
Lampiran 19. Perhitungan kandungan lembab dan pH... 73
Lampiran 20. Perhitungan kapasitas penetralan asam... 74
Lampiran 21. Perhitungan kelarutan... 76
commit to user
1
BAB I
PENDAHULUAN
A. Latar Belakang
Senyawa hydrotalcite merupakan suatu hidroksida berlapis ganda yang mempunyai lapisan bermuatan negatif dengan kation pada interlayer (Bejoy, 2001). Lempung anionik seperti hydrotalcite kurang banyak terdapat di alam dibandingkan dengan lempung kationik, namun lempung anionik mudah disintesis (Zhu et al., 2005). Lapisan hidroksida mempunyai struktur mirip brucite dan dikenal sebagai layer double hydroxides (Cavani et al., 1991) dengan formula umum [M2+1-xM3+x(OH)2]x+[An-b/n].mH2O, di mana M2+ dan M3+ adalah kation
divalen dan trivalen pada posisi oktahedral dalam lapisan hidroksida yang dikelilingi 6 gugus hidroksida dengan kisaran x normal antara 0,17 sampai 0,33. Sementara itu, An- adalah anion organik atau anorganik pada interlayer yang disebabkan oleh adanya muatan positif pada permukaan hydrotalcite. Parameter m merupakan jumlah molekul H2O (Jinhong et al., 2005). Hydrotalcite biasanya
diproduksi dengan penambahan larutan Na2CO3, atau larutan NaOH yang
dicampurkan dengan larutan MgCl2dan AlCl3 (Miyataet al.,1976).
commit to user
2
Salah satu penggunaan hydrotalcite sebagai controled release yaitu hydrotalcitememiliki sifat antasida sehingga dapat di interkalasi dengan material obat yang dapat merusak mukosa lambung (Nalawade et al., 2009). Bejoy (2001) menyatakan bahwa hydrotalcitemenjadi golongan antasida yang dapat diandalkan dibandingkan dengan konvensional karena memiliki kemampuan lebih baik daripada antasida lainnya dalam menetralisasi asam lambung berlebih. Djuwantoro (1992) juga menyatakan efek laksatif (pencahar) yang ditimbulkan dari magnesium hidroksida dan efek konstipasi (sembelit) dari aluminium hidroksida dapat diatasi dengan menggunakan suatu preparat dari kombinasi kedua antasida tersebut. Mekanisme hydrotalcite yang mendasari perlindungan mukosa (selaput lendir) lambung masih tidak jelas dipahami. Namun, hydrotalcite diyakini mempunyai kemampuan membantu pepsin (enzim pencernaan dalam lambung) untuk menetralkan aktivitas anti-tukak (Bejoy, 2001) sehingga banyak industri farmasi yang memanfaatkan hydrotalcite sebagai antasida (Gunawan, 2008). Kandungan umum dari senyawa hydrotalcite pada antasida memiliki formula Al2Mg6(OH)14(CO3)2.4H2O (Anonim, 2007).
commit to user
3
beberapa kriteria, di antaranya: mampu menetralkan asam, tidak diadsorp saluran cerna, dan tidak menimbulkan efek samping (Djuwantoro, 1992).
B. Perumusan Masalah
1. Identifikasi Masalah
Hydrotalcitedapat disintesis dengan berbagai metode seperti elektrokimia, stoikiometri, pertukaran ion maupun secara kopresipitasi (Hickey et al., 2000). Namun penggunaan metode selain kopresipitasi dalam preparasi dengan anion selain karbonat sulit dilakukan, karena dimungkinkan akan terjadi kontaminasi karbon dioksida. Kesulitan pencegahan ini menyebabkan metode kopresipitasi menjadi paling umum yang digunakan dalam sintesis. Adapun perlakuan pada saat sintesis Mg/Al-hydrotalcite dapat dilakukan pada beberapa variasi suhu, pH, dan waktu (Oh et al., 2002). Menurut Hickey et al. (2000), Mg/Al-hydrotalcite terkristalisasi dengan baik pada pH 8 - 10,5. Sementara itu, Kameda et al. (2000) mensintesis Mg/Al-hydrotalcitepada temperatur 60 °C, dan pH 10 selama 1 jam.
Rasio mol Mg/Al secara khas berada pada kisaran antara 2,0 sampai 3,7 (Kameda et al., 2000). Sementara itu, Oza et al. (2006) telah membuat
Mg/Al-hydrotalcite dari bahan alam dan memperoleh kondisi optimum pada pH 8,5 - 10,5 dengan temperatur antara 60 - 70 °C. Menurut Heraldyet al.(2006),
kemurnian senyawa Mg/Al-hydrotalcite akan semakin tinggi dengan semakin berkurangnya nilai rasio mol Mg/Al. Kemudian berdasarkan penelitian sebelumnya, kondisi optimum untuk sintesis Mg/Al-hydrotalcite dicapai dengan rasio 2 : 1 (Prasasti, 2008).
commit to user
4
mendukung data FTIR, Surface Area Analyzer (SAA) untuk analisis permukaan material dan Scanning Electron Microscope (SEM) untuk menentukan morfologi yang berguna dalam menentukan permukaan sampel.
Karakterisasi Mg/Al-hydrotalcite sebagai bahan baku antasida memerlukan tahapan–tahapan proses yang meliputi preformulasi, formulasi dan proses pengontrolan. Preformulasi memerlukan pertimbangan karakteristik fisika, kimia dan biologi dari semua bahan obat yang digunakan dalam membuat produk tersebut (Ansel, 1989). Sebagai tahapan awal (preformulasi), dapat dilakukan penelitian secara in vitro dan in vivo pada karakterisasi kimia fisika untuk mengetahui karakter bahan tersebut, sehingga dapat digunakan sebagai pertimbangan dalam merancang formulasi obat untuk mencapai hasil yang diinginkan (Ogungbenle, 2009).
2. Batasan Masalah
Berdasarkan identifikasi masalah, maka perlu dibuat batasan-batasan masalah, yaitu sebagai berikut.
a. Sintesis Mg/Al-hydrotalcite dilakukan pada pH 10, suhu 70 °C, dan waktu sintesis 1 jam dengan metode kopresipitasi (Kameda et al., 2000) .
b. Rasio mol Mg/Al dibuat 2 : 1 (Heraldyet al., 2009, 2011, dan 2012).
c. Karakterisasi Mg/Al-hydrotalcite sebagai material hasil sintesis dilakukan dengan XRD, XRF, FTIR, TG-DTA dan SAA.
d. Karakterisasi kimia fisika Mg/Al-hydrotalcite sebagai bahan baku antasida meliputi beberapa pengujian yaitu berat jenis (nyata, benar, dan mampat), sifat alir (faktor Housner, porositas, dan kompresibilitas), kandungan lembab (moisture content), pH, kapasitas penetralan asam, dan kelarutan (pH 1, pH 2, pH 3, dan pH 4).
3. Rumusan Masalah a. Bagaimana karakterisasi Mg/Al-hydrotalcitehasil sintesis?
commit to user
5
C. Tujuan Penelitian
1. Mengetahui karakterisasi Mg/Al-hydrotalcite hasil sintesis dengan analisis menggunakan XRD, XRF, FTIR, TG-DTA, dan SAA.
2. Mengetahui kesesuaian karakter Mg/Al-hydrotalcite dengan hydrotalcite komersial sebagai bahan baku antasida.
D. Manfaat Penelitian
1. Memberikan informasi tentang karakterisasi dari Mg/Al-hydrotalcite hasil sintesis.
commit to user
6
BAB II
LANDASAN TEORI
A. Tinjauan Pustaka
1. Hydrotalcite a. Struktur hydrotalcite
Hydrotalcite merupakan lempung anionik yang terdiri dari tumpukan lapisan bermuatan positif dan mempunyai anion di interlayer kation tersebut (Rajamanthi et al., 2001). Pada umumnya, hydrotalcite mempunyai formula [M2+1-xM3+x(OH)2]x+[An-x/n].mH2O, dimana M II adalah kation logam divalen
seperti Mg2+, Fe2+, Ni2+, Cu2+, Co2+, Mn2+, Zn2+ atau Cd2+, M III adalah kation logam trivalen, seperti Al3+, Cr3+, Ga3+, atau Fe3+, sedangkan An- adalah CO32-,
SO42-, Cl-, NO3-, atau anion organik. Nilai x pada umumnya berkisar antara 0,17
sampai 0,33 dan m merupakan jumlah molekul H2O (Vaccari et al., 1998;
Kovanda et al., 2005). Menurut Miyata et al. (1976), hydrotalcite dalam bentuk naturalnya adalah suatu hidroksi karbonat dari magnesium dan aluminium dengan rumus Mg6Al2(OH)16CO3.4H2O.
Secara struktural, struktur kimia hydrotalcite mirip dengan brucite Mg(OH)2 dengan pergantian beberapa ion Mg2+ oleh ion Al3+. Brucite adalah
commit to user
7
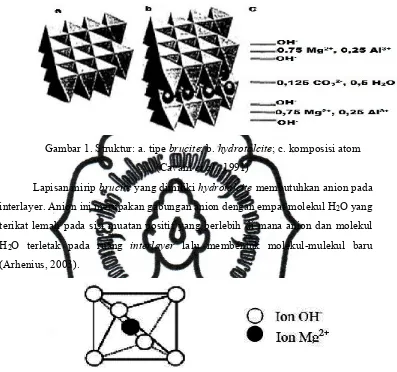
Gambar 1. Struktur: a. tipe brucite; b. hydrotalcite; c. komposisi atom (Cavani et al., 1991)
Lapisan mirip bruciteyang dimiliki hydrotalcitemembutuhkan anion pada interlayer. Anion ini merupakan gabungan anion dengan empat molekul H2O yang
terikat lemah pada sisi muatan positif yang berlebih di mana anion dan molekul H2O terletak pada ruang interlayer lalu membentuk molekul-mulekul baru
(Arhenius, 2003).
Gambar 2. Struktur senyawa brucite(Goh et al., 2008)
commit to user
Gambar 3. Skema struktur senyawab. Sifat hydrotalcite Hydrotalcite memiliki dan surface area yang tinggi. yang rendah atau mendekati kemampuan pertukaran anion 2010), serta memiliki sifat Ruang lingkup dari aplikasi
Gambar 4.
Skema struktur senyawa hydrotalcite(Murphyet al
ydrotalcite
memiliki kemampuan adsorpsi, kapasitas pertukaran yang tinggi. Selain itu, hydrotalcite juga memiliki
mendekati nol (Choy et al., 2007). Hydrotalcite mempunyai pertukaran anion yang signifikan (Barriga et al., 2002; Hussein memiliki sifat memory effect(dapat diregenerasi) (Roto et al
aplikasi hydrotalciteditunjukkan pada Gambar 4.
Gambar 4. Aplikasi hydrotalcite(Moyo, 2009)
8
et al., 2004)
commit to user
9
Selain itu, hydrotalcite dengan anion interlayer berupa CO32-mempunyai
kestabilan struktur yang baik pada kondisi pH ≤ 3,0. Anion interlayerCO3
2-akan mengikat ion H+ membentuk ion HCO23-, sedangkan OH- pada permukaan
hydrotalcitebereaksi dengan H+menghasilkan molekul H2O pada kondisi pH ≤ 3
sehingga sebagian hydrotalcite larut dalam air. Hal ini ditunjukkan oleh penurunan massa hydrotalcite yang direndam dalam larutan dengan pH ≤ 3,0 (Shiddiq, 2005).
c. Sintesis Mg/Al-hydrotalcite.
Hickey et al. (2000) menyebutkan bahwa hydrotalcite dapat disintesis dengan beberapa metode, yaitu sintesis hidrotermal, rekonstruksi struktural, elektrokimia, dan kopresipitasi atau pengendapan. Ohet al. (2002) telah membuat Mg/Al-hydrotalcite dengan metode kopresipitasi, yaitu larutan yang mengandung sumber kation magnesium dari [Mg(NO3)2] dan aluminium dari [Al(NO3)3]
dicampurkan dengan larutan yang mengandung sumber karbonat sebagai anionnya, kemudian disintesis pada pH 10–13 sampai terbentuk padatan (gel). Sementara itu, Heraldy et al. (2006) juga mensintesis Mg/Al-hydrotalcitedengan rasio mol Mg/Al 2,0 ; 2,5 dan 3,0 dari campuran magnesium klorida dan aluminium klorida melalui metode kopresipitasi secara langsung. Sintesis yang paling sering dilakukan adalah sintesis hydrotalcite dengan anion interlayer berupa CO32- secara pengendapan larutan magnesium dan aluminium
menghasilkan suatu Mg/Al-hydrotalcite. Cara ini dipilih dan disukai karena tidak perlu mencegah adanya kontaminasi dari karbon dioksida sebab hanya karbonat yang siap bergabung dan terikat dengan kuat di dalam daerah interlayer(Newman et al., 1998).
commit to user
d. Karakterisasi Mg/AlAnalisis yang sering di alam maupun yang merupakan Diffractometer (XRD),
(FTIR), Thermo Gravimetric Surface Area Analyzer(SAA).
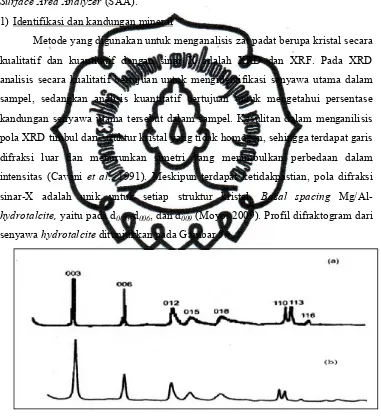
1) Identifikasi dan kandungan mineral Metode yang digunaka
kualitatif dan kuantitatif analisis secara kualitatif sampel, sedangkan analisis kandungan senyawa utama pola XRD timbul dari struktur k difraksi luar dan menurunkan intensitas (Cavani et al
sinar-X adalah unik hydrotalcite, yaitu pada
senyawa hydrotalciteditunjukkan pada Gambar 5.
Gambar 5. (a) JCPDS 14
Mg/Al-hydrotalcite
yang sering dilakukan untuk mengkarakterisasi mineral yang merupakan hasil sintesis dengan menggunakan alat (XRD), X-Ray Flourosence (XRF), Fourier Transform Infra
Gravimetric - Differential Thermal Analysis (TG-DTA), (SAA).
Identifikasi dan kandungan mineral
yang digunakan untuk menganalisis zat padat berupa kristal kuantitatif dengan sinar X adalah XRD dan XRF. Pada kualitatif bertujuan untuk mengidentifikasi senyawa utama sedangkan analisis kuantitatif bertujuan untuk mengetahui persentase
senyawa utama tersebut dalam sampel. Kesulitan dalam menganilisis XRD timbul dari struktur kristal yang tidak homogen, sehingga terdapat
menurunkan simetri yang menimbulkan perbedaan al., 1991). Meskipun terdapat ketidakpastian, pola
untuk setiap struktur kristal. Basal spacing d003, d006, dan d009(Moyo, 2009). Profil difraktogram
ditunjukkan pada Gambar 5.
Gambar 5. Difraktogram XRD Mg/Al-hydrotalcite JCPDS 14-191 (b) Mg/Al-hydrotalcite(Sharma et al., 2008)
commit to user
11
Setiap kristal mempunyai harga d yang khas sehingga dengan mengetahui harga d maka jenis kristalnya dapat diketahui. Referensi harga d dan intensitas suatu senyawa dapat diperoleh dari data Joint Committee on Powder Diffraction Standars (JCPDS) yang bersumber dari International Centre for Difraction Data
(West, 1992). Hydrotalcite dengan anion interlayer berupa CO32- dicirikan oleh
harga d sekitar 7,80 Å. Pencirian ini disebutkan dalam hasil penelitian yang dilakukan oleh Kloproggeet al. (2002) dan Hickeyet al. (2000).
Penelitian Kang et al. (2005) mendapatkan Mg/Al-hydrotalcite dengan rasio 3; 2,5; dan 2 dengan nilai d 7,90; 7,82; dan 7,65 Å. Penelitian Alnavis (2010) yang telah mensintesis Mg/Al-hydrotalcite dari brine water dengan rasio Mg/Al = 2,0 pada difraktogram XRD memiliki tiga puncak dengan intensitas tertinggi, yaitu pada harga 2θ sebesar 11,66; 23,45 dan 34,57 yang merupakan karakter pada senyawa hydrotalcite.
Sementara XRF, analisis unsur secara kuantitatif hanya memberikan informasi kandungan unsur suatu bahan, sedangkan analisis kualitatif dinyatakan dalam intensitas dengan satuan cps (count per second). Semakin besar intensitas yang muncul, maka semakin banyak kandungan unsur tersebut dalam suatu bahan (Hendayana, 1994). Ahmad et al. (2011) menggunakan analisis XRF untuk mengetahui kandungan logam yang terkandung pada Mg/Al-hydrotalcite dan diperoleh hasil Mg/Al-hydrotalcitetidak mengandung logam berbahaya.
2) Penentuan gugus fungsi.
commit to user
12
yang paling penting dalam penentuan struktur suatu senyawa organik berkisar antara 4000 cm-1– 625 cm-1(Silverstein et al., 1981).
Johnson et al. (2003) telah melaporkan adanya puncak-puncak yang khas dari vibrasi gugus-gugus fungsi pada senyawa hydrotalcite. Puncak pada bilangan gelombang 3400 cm-1 menunjukkan vibrasi ulur OH, 1400 cm-1 menunjukkan vibrasi ulur asimetris CO3, 800 cm-1 menunjukkan deformasi luar bidang CO3,
sementara pada bilangan gelombang 600 - 400 cm-1 menunjukkan vibrasi ulur M-Al-O dan vibrasi ulur serta tekuk dari M-O dengan M adalah logam. Spektra FTIR dari hydrotalcitemempunyai puncak-puncak khas seperti pada Tabel 1.
Tabel 1. Gugus fungsi Mg/Al-hydrotalcite
Gugus fungsi Bilangan gelombang (cm-1) Uluran OH dan M-O 3400 - 3500a,b
Tekukan OH 1650d
Uluran simetris C-O 1385a,c Uluran asimetris C-O 1500,5c Tekukan O=C-O 650a
Uluran Mg-O dan Al-O 400 - 600a(2 puncak)
Sumber : aKannan (1995) dalam Johnson et al. (2003), bBhaumik, et al. (2004),
c
Cosimo, et al.(1998), dYang et al.(2007).
Lakraimi et al. (2000) juga melaporkan adanya gugus-gugus fungsi pada hydrotalcite. Bilangan gelombang 3450 cm-1 menunjukkan vibrasi gugus OH, 1650 cm-1 menunjukkan vibrasi tekuk H2O dari interlayer, 647 cm-1 untuk vibrasi
M-O, 435 cm-1 untuk O-M-O, sedangkan 1360 cm-1menunjukkan vibrasi CO3.
commit to user
13
3) Analisis termal
Thermo Gravimetric Analyzer(TGA) secara otomatis mencatat perubahan berat suatu sistem bila temperaturnya berubah dengan laju tertentu. Perubahan temperatur dan berat direkam secara kontinyu.
Differential Thermal Analyzer (DTA) akan mendeteksi setiap perubahan termal yang terkait dengan peristiwa atau reaksi kimia, baik yang berjalan secara eksotermik maupun endotermik. Kedua peristiwa ini ditampilkan dalam bentuk termogram diferensial sebagai puncak maksimum dan minimum. Puncak maksimum menunjukkan peristiwa eksotermis di mana panas akan dilepaskan oleh sampel. Puncak minimum menunjukkan peristiwa endotermis di mana terjadi penyerapan panas oleh sampel.
Menurut Yang et al. (2002) analisis termal Mg/Al-hydrotalcite layered double hydroxidedapat diidentifikasi dari:
a. Pelepasan interlayer air pada temperatur 70 - 190 °C, terdapat dua fase kristal yang berbeda secara bersamaan, fase I dengan suatu basal spacing antara 7,5 -7,3 Å dan fase II dengan basal spacing ~ 6,6 Å, struktur layered double hydroxidemasih tetap utuh.
b. Pada temperatur antara 190 - 280 °C, OH-berikatan dengan Al3+ yang mulai lepas pada temperatur 190 °C dan terlepas seluruhnya pada temperatur 280 °C. Pada temperatur ini fase I diubah ke dalam fase II.
c. Pada temperatur antara 280 - 405 °C, OH- berikatan dengan Mg2+yang mulai lepas pada temperatur 280 °C dan terlepas seluruhnya pada temperatur 405 °C, degradasi dari struktur layered double hydroxide juga diamati pada daerah yang sama.
d. Pada temperatur 405 - 508 °C, CO32-mulai lepas dan terlepas seluruhnya pada
temperatur 508 °C. Pada temperatur ini, material menjadi suatu campuran larutan padatan oksida amorf metastabil.
commit to user
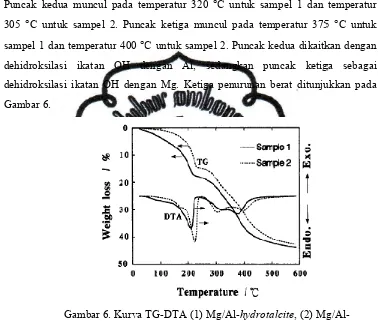
dehidroksilasi ikatan OH dehidroksilasi ikatan OH Gambar 6. disebabkan karena dehidrasi molekul air pada interlayeruntuktemperatur 210 C dan sampel 2 terjadi pada temperatur muncul pada temperatur 320 C untuk sampel 1 dan sampel 2. Puncak ketiga muncul pada temperatur 375 temperatur 400 C untuk sampel 2. Puncak kedua dikaitkan
ikatan OH dengan Al, sedangkan puncak ketiga ikatan OH dengan Mg. Ketiga penurunan berat ditunjukkan
Kurva TG-DTA (1) Mg/Al-hydrotalcite, (2) Mg dengan perlakuan termal pada 150 C (Cavani et al.,1991)
, Moyo (2009) juga menyatakan dekomposisi
commit to user
Gambar 7. DekompoSalah satu contoh anion interlayerkarbonat (
Gambar 8. Xie et al. ( mempunyai puncak endo pelepasan gugus OH endotermis pada tempe hydrotalciteterjadi pada 498
Dekomposisi Mg/Al-hydrotalcite(Moyo, 2009) ntoh bentuk termogram TG-DTA Mg/Al-hydrotalcite karbonat (Mg/Al-hydrotalcite-CO3) ditunjukkan oleh Gambar 8.
TGA Mg/Al-hydrotalcite-CO3(Sharma et al., 2008)
(2003) menyatakan termogram Mg/Al-hydrotalcite puncak endotermis pada temperatur 238 °C yang menunj
us OH-. Pelepasan karbonat ditunjukkan oleh temperatur 414 °C, sedangkan degradasi struktur i pada 498 °C (Frostet al., 2005).
15
2009)
hydrotalcitedengan ) ditunjukkan oleh Gambar 8.
., 2008) hydrotalcite
Mg/Al-commit to user
16
4) Analisis permukaan
Permukaan sebagian besar zat padat, khususnya lempung, dapat dipastikan mengandung pori-pori. Menurut Alejandre et al. (1999) permukaan pori Mg/Al-hydrotalcite dipengaruhi oleh komposisi sampel dan temperatur sehingga mempengaruhi sifat dan kegunaan.
Wright (2002) menyebutkan bahwa Mg/Al-hydrotalcite dengan anion interlayerkarbonat mempunyai surface area sekitar 100 m2/g. Hasil penelitian Johnson et al. (2003) menunjukkan bahwa Mg/Al-hydrotalcite dengan anion interlayer karbonat mempunyai surface area 53,9 m2/g. Referensi tersebut menunjukkan bahwa Mg/Al-hydrotalcite termasuk dalam klasifikasi surface areasedang.
Luas surface area zat padat dapat dihitung dengan mengukur jumlah molekul N2 yang diadsorpsi, pada penutupan monolayer dan ada beberapa
metode yang digunakan untuk menganalisis data adsorpsi gas N2 di antaranya
adalah metode Brunauer-Emmett-Teller (BET) (Rives et al., 1992). Metode BET merupakan metode analisis adsorpsi gas yang paling sering digunakan karena mudah. Persamaan BET menggambarkan hubungan antara jumlah gas nitrogen isoterm yang diadsorpsi pada 150 °C dengan tekanan parsial dan jumlah yang diadsorpsi pada penutupan monolayer (Jaquelineet al., 1999).
2. Antasida
a. Pengertian antasida
Antasida adalah senyawa yang mempunyai kemampuan menetralkan asam lambung. Antasida bermanfaat untuk mengobati penyakit saluran cerna karena mengembalikan derajat keasaman lambung pada daerah pH 3 – 5 (Anonim, 2000).
commit to user
17
karbonat dapat menyebabkan acid rebound (asam berlebih pada lambung), konstipasi (sembelit), mual, muntah, pendarahan saluran cerna dan disfungsi ginjal. Karena efek samping yang sangat merugikan ini, kalsium karbonat tidak dianjurkan untuk pengobatan ulkus peptikum (luka pada lambung atau usus dua belas jari). Pada natrium karbonat cenderung menimbulkan alkalosis sistemik, sehingga tidak dianjurkan untuk digunakan sebagai antasida dalam pengobatan ulkus peptikum. Di sisi lain, penggunaan aluminium hidroksida menetralkan asam lambungnya lambat, tetapi masa kerjanya lebih panjang. Efek samping yang utama adalah konstipasi (sembelit). Hal ini dapat diatasi dengan memberikan antasida garam Mg (Djuwantoro, 1992).
Secara umum, hydrotalcite memiliki sejumlah sifat yang membuatnya sesuai sebagai bahan baku farmasi seperti memiliki surface area yang besar dan memiliki efek sinergis interlayer(Orthman et al., 2003). Oleh karena itu, saat ini hydrotalcite merupakan salah satu formula yang telah dikembangkan sebagai golongan antasida. Hydrotalcite merupakan salah satu contoh antasida yang memiliki kemampuan lebih baik dibanding antasida lainnya dalam menetralisasi asam lambung yang berlebihan. Nalawade et al. (2009) menyatakan bahwa hydrotalcitememiliki sifat antasida sehingga dapat di interkalasi dengan material obat yang dapat merusak mukosa lambung sehingga hydrotalcite dapat diaplikasikan sebagai controled release. Hydrotalcite merupakan hydroxymagnesium aluminate complex, di mana dengan cepat asam lambung akan
berubah menjadi Mg(OH)2 dan Al(OH)3 yang sangat sulit diabsorpsi sehingga
efeknya bisa bertahan lebih lama, dan dapat mempertahankan pH lambung normal (pH = 3,5) dalam waktu lama. Selain itu, hydrotalcite juga dapat membantu melindungi mukosa lambung (selaput lendir pada lambung) sehingga tidak mudah rusak oleh asam lambung (Troy, 2005). Mekanisme hydrotalcite dalam menetralkan asam lambung/tukak peptik (HCl):
commit to user
18
b. Karakterisasi bahan baku antasida
Mg/Al-hydrotalcite hasil sintesis berupa serbuk memiliki peran utama sebagai zat aktif dan sebagai bahan awal untuk pembuatan bahan baku obat, seperti granulat, tablet bersalut, dan suspensi. Sementara itu, untuk membuat suatu bahan baku obat diperlukan tahapan–tahapan proses yang meliputi preformulasi, formulasi dan proses pengontrolan. Preformulasi memerlukan pertimbangan karakteristik fisika, kimia dan biologi dari semua bahan obat dan bahan–bahan tambahan yang digunakan dalam membuat produk tersebut (Ansel, 1989).
Karakterisasi sebagai bahan baku antasida bertujuan untuk mengetahui data-data karakter bahan obat yang dapat dijadikan pertimbangan formulator dalam merancang formulasi obat untuk mencapai hasil yang diinginkan (Ogungbenle, 2009). Oleh karena itu, sebagai tahapan preformulasi dilakukan karakterisasi sebagai bahan baku antasida terhadap Mg/Al-hydrotalcite yang meliputi beberapa pengujian.
1) Berat jenis
commit to user
19
demikian secara numerik berat jenis nyata tetap lebih kecil daripada berat jenis benar (Voigt, 1994).
2) Sifat alir
Serbuk dikarakterisasikan melalui sifat-sifat spesifiknya. Dalam teknologi serbuk, pertimbangan-pertimbangan mengikuti sifat dimensi, sifat permukaan, sifat aliran dan sifat-sifat teknologi farmasi. Sifat aliran serbuk dipengaruhi bentuk partikel dan ukuran partikel, gaya kohesi di antara partikel melalui pembentukan lapisan tipis permukaan (misalnya air) dan faktor-faktor lainnya. Kekompakan atau gaya ikat dari serbuk berdasarkan pada gaya Van der Waals antara permukaan bahan zat padat, dan hubungan muatan elektrostatik atau gaya di interlayer teradsorpsi. Sifat alir serbuk dan granulat diperbaiki melalui penambahan bahan pelincir, yang menurunkan gesekan partikel (Voigt, 1994).
commit to user
20
3) Kandungan lembab
Material yang akan dikempa harus memiliki kandungan lembab/kadar air dalam batas-batas tertentu. Hal ini penting karena berhubungan dengan sifat alir, proses pengempaan, kompatibilitas, dan stabilitas. Salah satu cara untuk mengetahui kelembaban suatu bahan padat adalah dengan perhitungan menggunakan data berdasarkan berat keringnya (Sulaiman, 2007).
Pengukuran kandungan air yang berada dalam bahan baku obat dapat dilakukan dengan beberapa cara yang tepat tergantung pada sifat bahannya. Kadar air dapat ditentukan dengan beberapa cara, antara lain: metode titrasi, destilasi dan gravimetri. Pengukuran kandungan air bertujuan untuk memberikan batasan minimal atau rentang tentang besarnya kandungan air dalam bahan, di mana nilai maksimal atau rentang yang diperbolehkan terkait dengan kemurniaan dan kontaminasi. Pada umumnya, penentuan kadar air dilakukan dengan mengeringkan bahan dalam ovenpada temperatur 105 –110 °C selama 3 jam atau sampai didapat berat yang konstan. Selisih berat sebelum dan sesudah pengeringan adalah banyaknya air yang diuapkan (Anonim, 2000).
4) Tingkat keasaman (pH)
pH adalah derajat keasaman yang digunakan untuk menyatakan tingkat keasaman atau kebasaan yang dimiliki oleh suatu larutan. Kestabilan suatu obat dapat dipengaruhi oleh beberapa faktor, antara lain panas, cahaya, oksigen, kelembaban, pengaruh pH, dan mikroorganisme. Suatu obat kestabilannya dapat dipengaruhi oleh pH, di mana reaksi penguraian dari larutan obat dapat dipercepat dengan penambahan asam (H+) atau basa (OH-) dengan menggunakan katalisator yang dapat mempercepat reaksi tanpa ikut bereaksi dan tidak mempengaruhi hasil dari reaksi (Ansel, 1989).
5) Kapasitas penetralan asam
commit to user
21
nilai pH 1,2 - 1,8 (Voigt, 1994). Ada beberapa kriteria dalam penentuan kapasitas penetralan asam (Ansel, 1989), yaitu sebagai berikut.
1. Mempunyai daya netralisasi asam lambung yang besar.
2. Netralisasi tersebut harus terjadi dengan cepat sebelum melewati lambung dan bertahan selama dua jam.
3. Netralisasi asam lambung bertujuan menjadikan derajat keasaman lambung mencapai pH 3 - 5.
Menurut Gunawan (2008), kecenderungan peningkatan nilai kapasitas penetralan asam dipengaruhi oleh ukuran partikel. Apabila ukuran dari suatu partikel antasida semakin kecil maka akan memberikan nilai kapasitas penetralan asam yang semakin besar.
6) Kelarutan
Untuk membuat suatu bahan baku obat tentunya diperlukan desain yang paling sesuai untuk setiap jenis zat aktif. Hal ini dipengaruhi sifat fisikokimia dari zat aktif tersebut, diantaranya: kelarutan, pH, bentuk kristal, inkompatibilitas (interaksi zat aktif dengan zat lain yang menimbulkan efek tidak diinginkan terhadap zat aktif), dan stabilitas. Data-data fisikokimia ini diperhitungkan dalam pemilihan bahan tambahan pada pembuatan bahan baku obat. Data-data tersebut juga mempengaruhi pemilihan bentuk obat, baik tablet, sirup, suspensi, emulsi, kapsul, dan yang lainnya. Pengetahuan mengenai kecepatan disolusi atau kelarutan sangat diperlukan untuk membantu dalam memilih medium pelarut yang paling baik untuk obat atau kombinasi obat, membantu mengatasi kesulitan-kesulitan tertentu yang timbul pada waktu pembuatan larutan farmasetis dan lebih jauh lagi, dapat bertindak sebagai standar atau uji kemurnian (Ansel, 1989).
commit to user
22
Pharmacopeiadan National Formulary, definisi kelarutan obat adalah jumlah mL pelarut dimana akan larut 1 gram zat terlarut (Martin et al.,1993).
Bahan baku obat yang diberikan di dalam saluran cerna harus mengalami proses pelepasan, sehingga zat aktif akan melarut dan selanjutnya diabsorpsi. Proses pelepasan zat aktif dan proses pelarutannya sangat dipengaruhi oleh sifat-sifat kimia fisika zat tersebut serta formulasi bahan bakunya. Salah satu sifat-sifat zat aktif yang penting untuk diperhatikan adalah kelarutan, karena pada umumnya zat baru diabsorpsi setelah terlarut dalam cairan saluran cerna.
B. Kerangka Pemikiran
Senyawa hydrotalcite merupakan suatu hidroksida berlapis ganda yang jarang ditemukan di alam, tetapi dapat disintesis dengan mudah. Hydrotalcite memiliki rumus umum [M2+1-xM3+x(OH)2]x+[An-x/n].mH2O di mana M2+ sebagai
kation divalen dapat berupa Mg2+, Ca2+, Zn2+, Cu2+, Co2+ atau Ni2+ dan M3+. Sebagai kation trivalennya dapat berupa Al3+, Fe3+ atau Cr3+, sedangkan A n-merupakan anion yang mengisi interlayer dapat berupa ion OH−, Cl−, NO3−,
CO32−, SO42−. Hydrotalcite biasanya disintesis dengan penambahan larutan
Na2CO3, atau larutan NaOH yang dicampurkan dengan larutan MgCl2dan AlCl3.
Hasil karakterisasi Mg/Al-hydrotalcitememiliki basal spacingpada d003, d006, dan
d009, sementara daerah pengamatan bilangan gelombang spektra infra merah
biasanya digunakan untuk mencirikan keberadaan gugus-gugus fungsi Mg/Al-hydrotalcite. Perubahan termal yang terkait peristiwa kimia dan perubahan massa
commit to user
23
dengan menggunakan XRF, untuk memperoleh kandungan logam utama dalam bentuk oksidanya dan juga dapat diketahui logam-logam lain yang terdapat dalam senyawa Mg/Al-hydrotalcite, analisis ini dapat menunjukkan bahwa dalam senyawa hasil sintesis tidak terdapat kandungan logam berbahaya.
Hydrotalcite merupakan material menarik karena sifat dari hydrotalcite memiliki kemampuan adsorpsi, kapasitas pertukaran anion, dan surface area yang tinggi. Salah satu penggunaan hydrotalcite dalam industri farmasi digunakan sebagai golongan antasida. Oleh karena itu, agar hydrotalcite dapat digunakan sebagai bahan baku antasida diperlukan proses karakterisasi kimia fisika.
C. Hipotesis
Hipotesis penelitian yang dapat diambil dari masalah dan kerangka pemikiran yang ada adalah sebagai berikut.
1. Karakterisasi senyawa hasil sintesis merupakan Mg/Al-hydrotalcite yang memiliki basal spacing pada d003, d006, dan d009, serta adanya gugus OH-dan
CO32-.
commit to user
24
BAB III
METODOLOGI PENELITIAN
A. Metode Penelitian
Metode yang dilakukan dalam penelitian ini adalah metode eksperimental laboratorium. Penelitian ini meliputi tiga tahap, yaitu sintesis Mg/Al-hydrotalcite, Karakterisasi Mg/Al-hydrotalcite hasil sintesis dengan XRD, XRF, FTIR, TG-DTA, dan SAA, serta karakterisasi Mg/Al-hydrotalcite sebagai bahan baku antasida.
B. Tempat dan Waktu Penelitian
Dalam penelitian ini dilakukan:
1. Sintesis, Karakterisasi Mg/Al-hydrotalcite sebagai bahan baku antasida di Laboratorium Dasar Kimia Jurusan Kimia Fakultas MIPA dan Laboratorium Pusat Universitas Sebelas Maret Sub Laboratorium Kimia, Surakarta.
2. Karakterisasi Mg/Al-hydrotalcite hasil sintesis meliputi: Identifikasi Mg/Al-Hydrotalcite menggunakan X–Ray Diffractometer (XRD) dan X-Ray Flourosence (XRF), Penentuan gugus fungsi Mg/Al-hydrotalcite menggunakan Fourier Transform Infra Red (FTIR), Analisis Termal menggunakan Thermo Gravimetric-Differential Thermal Analysis(TG-DTA), dan Analisis Permukaan menggunakan Surface Area Analyzer (SAA) di Laboratorium Terpadu Universitas Sebelas Maret, Surakarta.
commit to user
25
C. Alat dan Bahan
1. Alat – alat
Alat-alat yang digunakan dalam penelitian ini adalah: a. Seperangkat alat refluks
b. Termometer
c. Neraca analitik Sartorius d. Peralatan gelas
e. pH meter Corning 430
f. Hot platedan Magnetik Stirrer g. Piknometer 5 mL
h. Lumpang porselen
i. Ayakan berukuran 180 dan 250 mesh j. Centifuge Hermle Z 206 A
k. Oven Barnsted 2555
l. X-Ray Diffractometer(XRD) Bruker D8 Advance m. X-Ray Flourosence(XRF) Bruker S2 Ranger
n. Fourier Transform Infra Red(FTIR) Shimadzu IRPrestige-21 o. Simultaneous Thermal Analize(STA) Linseis STA PT-1600 p. Surface Area Analyzer(SAA) Quantachrome Nova Win 1200
2. Bahan-bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah: a. MgCl2.6H2O p.a (E. Merck)
b. AlCl3.6H2O p.a (E. Merck)
c. Na2CO3p.a (E. Merck)
d. AgNO3p.a (E. Merck)
e. HCl p.a 37% (E. Merck) f. NaOH p.a (E. Merck)
commit to user
26
D. Prosedur Penelitian
1. Sintesis dan Karakterisasi Mg/Al-hydrotalcite
MgCl2.6H2O dan AlCl3.6H2O ditimbang dengan komposisi rasio mol 2 : 1
sehingga massa MgCl2.6H2O 9,15 g dan AlCl3.6H2O 5,43 g dilarutkan dalam 100
mL air di dalam labu leher tiga sampai homogen. Setelah itu, larutan ditambahkan 2000 mL 0,1 M Na2CO3 dengan pH 10 dijaga konstan pada suhu 70 °C saat
direfluksselama 1 jam. setelah itu, suspensi diendapkan semalam.
Endapan Mg/Al-hydrotalcite disaring lalu dicuci dengan akuades. Pencucian ini dilakukan terus menerus hingga suspensi bebas dari ion Cl-. Keberadaan ion Cl-diketahui dengan diuji filtrat pencucian menggunakan AgNO3.
Suspensi yang terbentuk dipisahkan secara centifuge pada kecepatan 2800 rpm selama 15 menit lalu dipanaskan dengan furnacepada temperatur 80 °C selama 20 jam. Padatan kering digerus sampai halus kemudian dianalisis dengan XRD, XRF, FTIR, TG-DTA dan SAA.
2. Karakterisasi Bahan Baku Antasida a. Berat jenis nyata
Gelas ukur kosong 10 mL ditimbang, sehingga diperoleh berat gelas ukur kosong (W1). sampel Mg/Al-hydrotalcite dimasukkan ke dalam gelas ukur
sampai volume 2 mL (V), diratakan lalu ditimbang dan diperoleh berat gelas ukur yang berisi Mg/Al-hydrotalcite(W2).
b. Berat jenis benar
commit to user
27
c. Berat jenis mampat
Gelas ukur kosong 10 mL ditimbang, diperoleh berat gelas ukur kosong (W1). Sampel Mg/Al-hydrotalcite dimasukkan ke dalam gelas ukur dan
dimampatkan dengan diketuk-ketukkan sampai volumenya 2 mL (V) lalu ditimbang, diperoleh berat gelas ukur yang berisi Mg/Al-hydrotalcite mampat pada volume tertentu (W2).
d. Kandungan lembab
Sampel Mg/Al-hydrotalcite ditimbang sebanyak 0,5 g, ditempatkan pada kurs porselen lalu dipanaskan dalam oven pada temperatur 105 °C selama 3 jam. Kandungan lembab ditunjukkan oleh persentase berat Mg/Al-hydrotalcite yang sesudah dioventerhadap berat awal Mg/Al-hydrotalcite.
e. Penentuan pH
Larutan Mg/Al-hydrotalcite 2 % diukur pH nya menggunakan pH meter yang telah dikalibrasi sebelumnya, sehingga diperoleh harga pH Mg/Al-hydrotalcite.
f. Kapasitas penetralan asam
Uji kapasitas penetralan dilakukan dengan cara 0,2 gram Mg/Al-hydrotalcitedilarutkan dalam 100 mL lalu diaduk dengan menggunakan stirer dan dipanaskan pada temperatur 37 °C. Setelah itu, larutan Mg/Al-hydrotalcite dicampurkan dengan HCl 0,1 M yang telah distirerdan dipanaskan pada suhu 37 °C. Hitung pH awal campuran tersebut, kemudian dititrasi dengan NaOH dan hitung miliekuivalen HCl dari berapa banyak volume NaOH 0,1 M yang dibutuhkan untuk membuat pH 3,5 .
g. Kelarutan
commit to user
28
E. Teknik Pengumpulan dan Analisis Data
Teknik pengumpulan dan analisis data dalam penelitian ini dari awal hingga akhir diperoleh untuk menjawab rumusan masalah yang ada dan setiap data yang diperoleh merupakan acuan untuk melakukan langkah berikutnya. Dari data yang diperoleh pada sintesis dan karakterisasi Mg/Al-hydrotalcite dapat dianalisis sebagai berikut.
1. Hasil sintesis selanjutnya dikarakterisasi dengan X-Ray Diffractometer(XRD). Data puncak difraktogram dari hasil analisis XRD dari senyawa hasil sintesis dibandingkan dengan data puncak dari Mg/Al-hydrotalcite standar dari Joint Committee on Powder Diffraction Standards (JCPDS). Pembandingan ini untuk memastikan bahwa senyawa utama hasil sintesis adalah Mg/Al-hydrotalcite, sedangkan hasil data XRF untuk memastikan kandungan oksida
hasil sintesis Mg/Al-hydrotalcite.
2. Gugus-gugus fungsi yang ada di dalam Mg/Al-hydrotalcite diketahui dengan membandingkan puncak-puncak spektra FTIR Mg/Al-hydrotalcite dengan referensi. Berdasarkan strukturnya, Mg/Al-hydrotalcitememiliki gugus fungsi Mg-O, O-C-O, karbonat, dan O-H dari lapisan hidroksida dan antar lapisan Mg/Al-hydrotalcite.
3. Analisis termal dilakukan menggunakan Thermo Gravimetric-Differential Thermal Analysis (TG-DTA), di mana terjadi perubahan struktur akibat pengaruh kenaikan temperatur. Salah satu perubahan struktur adalah terjadi pelepasan gugus fungsi dengan membandingkan pada referensi sehingga analisis ini dapat memperkuat analisis FTIR
4. Analisis permukaan Mg/Al-hydrotalcite hasil sintesis diketahui dengan membandingkan nilai surface areadan average pore radius pada spektra SAA yang dihasilkan dengan referensi.
commit to user
29
a. Berat jenis nyata dan mampat dihitung dengan persamaan (Voigt, 1994):
Berat jenis = = ( ) W1 = berat gelas ukur kosong
W2 = berat gelas ukur yang berisi Mg/Al-hydrotalcite pada volume
tertentu
b. Berat jenis benar dihitung dengan persamaan:
Berat jenis benar = ( )
( ) ( ) x ρ (List, 1985)
dimana ρ = (Voigt, 1994) a = volume piknometer
b = berat piknometer kosong c = berat piknometer yang berisi air
d = berat piknometer yang berisi sampel Mg/Al-hydrotalcite e = berat piknometer yang berisi sampel Mg/Al-hydrotalcite+ air c. Porositas (E) dihitung dengan persamaan (Voigt, 1994):
E = 1 − x 100 %
d. Faktor Hausner, perbandingan berat jenis mampat dengan berat jenis nyata:
Faktor Hausner =
e. Kompresibilitas zat uji dihitung dengan persamaan (Voigt, 1994): Kompresibilitas = x 100 %
f. Kandungan lembab (% MC) dihitung dengan persamaan (Halim, 1990):
Persentase kandunga lembab = – x 100 %
g. Kapasitas penetralan asam (Anonim, 2009):
miliekuivalen
(asam) =miliekuivalen
(basa) h. Persentase kelarutan dihitung dengan persamaan:Persentase kelarutan = /
commit to user
30
BAB IV
HASIL PENELITIAN DAN PEMBAHASAN
A. Sintesis Mg/Al-hydrotalcite
Sintesis Mg/Al-hydrotalcite diawali dengan pembuatan larutan awal dengan perbandingan rasio mol Mg/Al-hydrotalcite 2 : 1, sehingga bahan awal MgCl2.6H2O yang dibutuhkan sebesar 9,15 g dan AlCl3.6H2O sebesar 5,43 g.
Perbandingan 2 : 1 digunakan karena kemurnian senyawa Mg/Al-hydrotalcite akan semakin tinggi dengan semakin berkurangnya nilai rasio mol Mg/Al.
Mg/Al-hydrotalcite disintesis berdasarkan metode yang dilakukan oleh Kameda et al. (2000), yaitu dengan metode kopresipitasi di mana anion interlayer yang digunakan berupa ion CO32-. Cara ini dipilih dan disukai karena tidak perlu
mencegah adanya kontaminasi dari karbon dioksida sebab hanya karbonat yang siap bergabung dan terikat dengan kuat di dalam daerah interlayer (Newman et al., 1998) dan keberadaan ion CO32-dapat mempercepat proses kristalisasi
Mg/Al-hydrotalcite (Kang et al., 2005). Pada metode kopresipitasi, semua kation mengendap secara simultan dalam rasio mol sesuai dengan rasio mol awalnya (Kameda et al., 2000).
Sintesis Mg/Al-hydrotalcite dilakukan dengan mereaksikan MgCl2.6H2O
dan AlCl3.6H2O dengan Na2CO3 dalam suasana basa, kemudian direfluks pada
kondisi optimum yaitu pH 10, temperatur 70 °C selama 1 jam. Pengkondisian pH larutan selama berlangsungnya sintesis sangat penting, untuk menghasilkan Mg/Al-hydrotalcite yang memiliki kristalinitas dan kemurnian yang tinggi. Jika kondisi dibawah pH optimum akan terbentuk Al(OH)3, sedangkan pada pH diatas
commit to user
31
(Anonim, 1995). Perhitungan untuk sintesis Mg/Al-hydrotalcitedapat dilihat pada Lampiran 1.
Foto senyawa hasil sintesis disajikan pada Gambar 9. Senyawa hasil sintesis yang diperoleh tersebut kemudian dikarakterisasi dengan XRD, XRF, FTIR, TG-DTA, dan SAA.
Gambar 9. Foto senyawa hasil sintesis
B. Karakterisasi Mg/Al-hydrotalciteHasil Sintesis
1. Identifikasi Senyawa Hasil Sintesis
Identifikasi senyawa hasil sintesis dilakukan dengan X-Ray Diffractometer (XRD). Analisis ini bertujuan untuk memastikan bahwa senyawa utama hasil sintesis adalah Mg/Al-hydrotalcite. Difraktogram senyawa utama hasil sintesis disajikan Gambar 10.
Gambar 10. Profil difraktogram XRD
commit to user
32
Analisis kualitatif difraktogram tersebut dilakukan dengan membandingkan harga d puncak-puncak difraktogram Mg/Al-hydrotalcitestandar
dari
International Centre for Diffraction Data
(ICDD)
. Tiga puncak tertinggi sampel sebagai penciri senyawa mempunyai harga d yang sesuai dengan Mg/Al-hydrotalcite standar, sehingga senyawa utama yang dicirikan pada difraktogram sampel tersebut adalah Mg/Al-hydrotalcite. Kloprogge et al. (2002) dan Yang et al. (2007) menyebutkan bahwa harga d 7,80 Å merupakan puncak karakterisasi Mg/Al-hydrotalcite dengan anion antar lapisan berupa CO32-. Dataharga d tiga puncak yang mencirikan Mg/Al-hydrotalcitedisajikan pada Tabel 2 dengan membandingkan harga d tiga puncak dari data-data Mg/Al-hydrotalcite standar ICDD. Data Mg/Al-hydrotalcite standar ICDD secara keseluruhan disajikan pada Lampiran 3.
Tabel 2. Basal spacingpuncak tertinggi Mg/Al-hydrotalcitehasil sintesis Basal spacing Mg/Al-hydrotalcite PDF Card#14-191 PDF Card#22-700
d003 7,61 7,69 7,84
d006 3,79 3,88 3,90
d009 2,57 2,58 2,60
Analisis kuantitatif dari difaktogram XRD adalah penentuan kandungan relatif Mg/Al-hydrotalcite. Analisis ini dilakukan dengan membandingkan intensitas relatif (I/I1) puncak-puncak difraktogram Mg/Al-hydrotalcite dengan
intensitas relatif seluruh puncak yang ada dalam sampel. Hasil perhitungan persentase kandungan relatif atau kemurnian Mg/Al-hydrotalcite dalam sampel adalah 94,45 %. Perhitungan kemurnian Mg/Al-hydrotalcite disajikan pada Lampiran 5.
commit to user
33
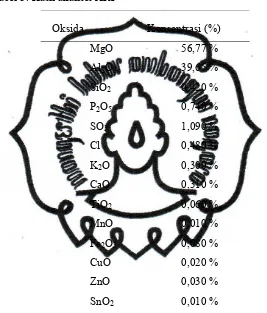
sehingga senyawa hasil sintesis ini dapat dikatakan aman sebagai bahan baku antasida. Setiap unsur akan menunjukkan puncak yang merupakan karakter dari uji kualitatif untuk unsur-unsur yang ada dalam lempung/ clay (Sumantry, 2010). Kandungan oksida Mg/Al-hydrotalcitedisajikan pada Tabel 3.
Tabel 3. Hasil analisis XRF
Oksida Konsentrasi (%) MgO 56,77 % Al2O3 39,65 %
SiO2 0,420 %
P2O5 0,740 %
SO3 1,090 %
Cl 0,480 %
K2O 0,300 %
CaO 0,310 % TiO2 0,060 %
MnO 0,010 % Fe2O3 0,080 %
CuO 0,020 % ZnO 0,030 % SnO2 0,010 %
Tabel 3 menunjukkan bahwa hasil analisis XRF pada MgO dan Al2O3
commit to user
34
2. Analisis Gugus Fungsi
Analisis untuk mengetahui karakterisasi gugus fungsi dalam Mg/Al-hydrotalcite hasil sintesis dilakukan dengan menggunakan spektrometer Fourier Transform Infra Red.Spektra FTIR Mg/Al-hydrotalcitedisajikan pada Gambar 11 dan perbandingan gugus fugsi dengan referensi ditunjukan pada Tabel 4.
Gambar 11. Spektra inframerah
(a) Mg/Al-hydrotalcite(Sharma et al., 2007) (b) Mg/Al-hydrotalcitehasil sintesis
Tabel 4. Perbandingan gugus fungsi Mg/Al-hydrotalcite
Gugus fungsi Bilangan gelombang ( ) (cm-1) Referensi Mg/Al-hydrotalcite
Uluran OH 3400 - 3500b 3444,87 Tekukan OH 1650d 1608,63 Uluran simetris O=C-O 1385a,c 1361,74
Uluran asimetris O=C-O 1500,5c 1517,98 - 1556,55 Tekukan O=C-O 650a 669,30
Uluran Mg-O dan 400 - 600a 553,57 Uluran Al-O (2 puncak) 449,41
commit to user
35
Tabel 4 menunjukkan perbandingan gugus fungsi yang ada dalam Mg/Al-hydrotalcite berdasarkan data bilangan gelombang. Bilangan gelombang pada 3444,87 cm-1 menunjukkan gugus OH stretching pada gugus hidroksi dari lembaran-lembaran Mg/Al-hydrotalcite dan molekul air yang terdapat di daerah interlayer atau antar partikel. Puncak pada bilangan gelombang 1608,63 cm-1 merupakan tekukan OH yang berasal dari molekul air pada daerah interlayer yang terikat dengan anion interlayer. Serapan untuk ion CO32- pada interlayer
diindikasikan dengan munculnya puncak pada bilangan gelombang 1361,74 cm-1 yang merupakan serapan untuk uluran simetris O=C-O dan sekitar 669,30 cm-1 yang merupakan tekukan O=C-O dari CO32-.
Uluran Mg-O dan Al-O ditunjukkan oleh dua puncak pada bilangan gelombang 449,41 dan 553,57 cm-1. Hasil ini mendekati dengan hasil penelitian Davydov (1984) dan Shiddiq (2005) yang menyebutkan bahwa puncak pada bilangan gelombang sekitar 550 cm-1 merupakan uluran Al-O sehingga bilangan gelombang 416,6 cm-1kemungkinan merupakan uluran Mg-O.
Analisis spektra FTIR di atas menunjukkan adanya ikatan Mg-O, Al-O serta gugus hidroksi dan karbonat. Hasil ini mengidentifikasikan bahwa senyawa yang dianalisis merupakan Mg/Al-hydrotalcite dengan anion interlayer CO3
2-yang mempunyai rumus kimia [Mg1-xAlx(OH)2]x+ (CO3)x/m.H2O (Heraldy et al.,
2006).
3. Analisis Termal
commit to user
terjadi perubahan berat dengan munculnya dua berat pertama terjadi sekitar Termogram DTA Mg/Al-hydrotalciteditunjukkan pada. Termogram TG-DTA (a) Mg/Al-hydrotalcitehasil sintesis (b) Mg/Al-hydrotalcite(standar) (Kang et al., 2005
n termogram TGA pada Gambar 12, dapat diketahui berat Mg/Al-hydrotalcite pada suhu tertentu yang
munculnya dua puncak endotermik pada termogram DTA. Penurunan rjadi sekitar 19,122 % disertai dengan adanya puncak en
ratur 260,025 °C yang mengindikasikan pelepasan gugus dengan hasil penelitian Xie et al. (2003) yang menun
pada temperatur 238 °C. Frost et al.(2005) menyebutkan pada lingkungan yang berbeda dalam struktur hydrotalcite
bebas air yang hilang pada temperatur rendah antara air terikat pada dirinya sendiri dalam ruang interlayer
commit to user
37
(c) hidrogen air terikat pada permukaan hidroksihydrotalcite. Air tipeb hilang antara 77 dan 170 °C dan air tipecantara 170 dan 235 °C. Suhu yang diperlukan untuk menghapus tipe molekul air bdanc menunjukkan seberapa kuat ikatan hidrogen antara air pada permukaan hidroksi hydrotalcite. Adanya pelepasan ion OH- pada interlayer dikaitkan dengan adanya dehidrasi pada Mg/Al-hydrotalcite: Mg6Al2(OH)16CO3.4H2O → Mg6Al2(OH)16CO3+ 4H2O.
Penurunan berat kedua terjadi sekitar 31,414 % disertai munculnya puncak endotermik pada temperatur 430,225 °C yang diperkirakan mengindikasikan pelepasan ion CO32- pada interlayer. Penelitian Frost et al. (2005) juga
menyebutkan bahwa pelepasan ion CO32- terjadi pada suhu 410 °C. Adanya
pelepasan ion CO32-pada interlayerdikaitkan dengan adanya dekarboksilasi pada
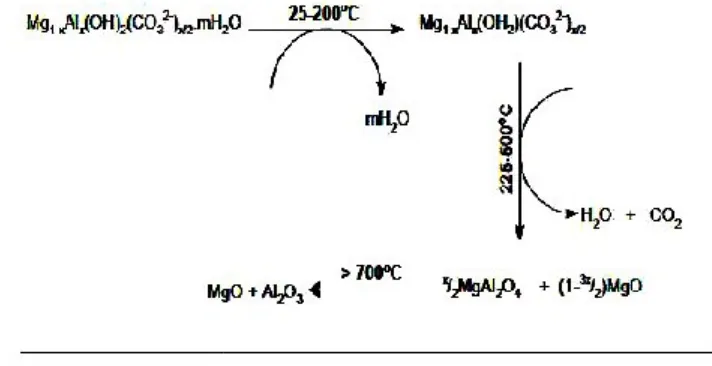
Mg/Al-hydrotalcite:
Mg6Al2(OH)16CO3.4H2O→MgAl2O + 5MgO + CO2+ 12H2O + 3/2O2
Zhao et al. (2003) menyatakan bahwa senyawa Mg/Al-hydrotalcite mempunyai dua penurunan berat, yaitu pada 285 °C terjadi pelepasan OH- dan pada 448,5 °C terjadi pelepasan anion interlayer. Analisis termal ini menunjukkan bahwa Mg/Al-hydrotalcitemengandung gugus OH-dan CO32-.
Mg/Al-hydrotalcite dimungkinkan mulai terdegradasi pada temperatur di atas 450 °C, yaitu sekitar 464,325 °C. Fakta ini diperkuat dengan hasil penelitian Frost et al. (2005) yang menunjukkan bahwa degradasi struktur Mg/Al-hydrotalciteterjadi pada temperatur 498 °C.
4. Analisis Permukaan
commit to user
Dari data pada Tabel 5 diketahui bahwa surface area Mg/Al-hydrotalcite sebesar 93,705 m2/g mendekati hasil penelitian Jaqueline et al. (2009) yang menyatakan bahwa surface area Mg/Al-hydrotalcite 87 m2/g. Sedangkan, Kovanda et al. (2005) menyebutkan surface area dari Mg/Alhydrotalcite 80 -90 m²/g. Referensi tersebut menunjukkan bahwa Mg/Al-hydrotalcite termasuk dalam klasifikasi luas permukaan sedang karena jika ukuran luas permukaan suatu padatan 50 - 100 m2/g dapat diklasifikasikan sebagai ukuran luas permukaan sedang (Agustine, 1996). Selain itu, data Average pore radius Mg/Al-hydrotalcite sebesar 10,808 Å menunjukkan pori berukuran mesopori. Menurut Oscik (1982), jika jari-jari pori berukuran 10 - 100 Å, maka diklasifikasikan ke dalam ukuran mesopori.
C. Karakterisasi Bahan Baku Antasida
commit to user
39
Tabel 6. Karakterisasi Mg/Al-hydrotalcitesebagai bahan baku antasida
No Karakterisasi Mg/Al-hydrotalcite hydrotalcitekomersial
commit to user
40
pori dalam partikel (Elfi et al., 2007), sedang berat jenis nyata adalah berat jenis yang dihitung sekaligus dengan porinya, sehingga berat jenis nyata < berat jenis benar (Voigt, 1994). Kemudian berat jenis mampat Mg/Al-hydrotalcite yang disajikan pada Tabel 6 diperoleh 0,686 ± 0,007 g/mL. Berat jenis mampat dinyatakan sebagai berat dimana satuan massa suatu produk berbentuk serbuk berada pada kumpulannya yang terpadat tanpa perubahan bentuk dari partikelnya. Perhitungan berat jenis selengkapnya disajikan pada Lampiran 15, Lapiran 16 dan Lampiran 17.
Hasil analisis berat jenis Mg/Al-hydrotalcite sedikit berbeda dengan hydrotalciteyang telah terstandarisasi (Gunawan, 2008) di mana berat jenis nyata (lossed) sebesar 0,33 g/mL dan berat jenis mampat (Tapped) sebesar 0,48 g/mL. Perbedaan ini dikarenakan berat molekul hydrotalcite yang digunakan berbeda dari segi struktur pembentuk anion penyeimbangnya. Selain itu, berat jenis suatu zat selain dipengaruhi oleh massa zat dan volume zat, juga dipengaruhi oleh banyak atau sedikitnya faktor kontaminan pada saat sintesis dalam zat tersebut.
2. Sifat Alir
Sifat alir serbuk merupakan faktor kritis dalam produksi obat padat. Hal ini karena sifat alir serbuk berpengaruh pada peningkatan reprodusibilitas pengisian ruang kompresi pada pembuatan tablet dan kapsul, sehingga menyebabkan keseragaman berat dan efek farmakologinya lebih baik (Fudholi, 1998).
commit to user
41
Sementara itu, Mg/Al-hydrotalcite mempunyai nilai porositas 67,215 ± 0,295 % yang disajikan pada Tabel 6. Hal ini menunjukkan pori-pori ruang antarpartikel yang cukup besar karena berdasarkan data SAA menunjukkan bahwa ukuran Mg/Al-hydrotalcite hasil sintesis tergolong ukuran mesopori, sehingga adanya pori akan mempengaruhi proses kimia fisika, misalnya kecepatan aliran, pengukuran kelembaban, dan lain-lain (Parikh, 1997). Material berpori didefinisikan sebagai material yang mempunyai pori sehingga mempunyai surface area yang besar. Secara umum, material berpori mempunyai nilai porositas 0,20 - 0,95 yang merupakan fraksi volume pori terhadap volume total material.
Semakin besar ukuran pori, maka akan memperlambat kecepatan aliran serbuk dan dapat memberikan peluang untuk meningkatkan kelembaban. Besarnya nilai porositas juga disebabkan karena bentuk partikel serbuk yang tidak sferis, sehingga akan memperbesar pori antarpartikel (Henny et al., 2007). Perhitungan porositas selengkapnya disajikan pada Lampiran 18.
Berdasarkan hasil pengukuran kompresibilitas, diperoleh persentase kompresibilitas Mg/Al-hydrotalcitesebesar 21,138 ± 0,244 % yang disajikan pada Tabel 6. Secara umum, jika persen kompresibilitas lebih dari 25 % dianggap sifat alirannya buruk dan jika dibawah 15 % maka sifat alirannya baik (Wicaksono et al., 2010). Persen kompresibilitas yang baik adalah 12 – 16 % dan persen
kompresibilitas 18 – 21 % termasuk sedang (Elfi et al., 2007). Perhitungan kompresibilitas selengkapnya disajikan pada Lampiran 18.
commit to user
42
3. Kandungan Lembab
Kandungan lembab/kadar air dianalisis menggunakan metode gravimetri, dengan cara menghitung selisih massa H2O sebelum dan setelah sampel
Mg/Al-hydrotalcite dipanaskan (Roto et al., 2008). Menurut Halim (1990), kadar air ditetapkan dengan rumus:
Persentase kandungan lembab = – x 100 %
Hasil penentuan kandungan lembab Mg/Al-hydrotalcite sebesar 9,653 ± 0,279 % (b/b) yang disajikan pada Tabel 6. Menurut Anonim (1971), standar kualitas kadar air (moisture content) umumnya adalah sekitar 10 %. Selain itu, faktor lain yang mempengaruhi kandungan lembab pada Mg/Al-hydrotalcite relatif tinggi, karena menurut Saksono (2002), semakin banyaknya jumlah senyawa Mg dalam garam, maka akan semakin bertambah pula kemampuannya untuk mengabsorp uap air dari udara, sehingga akan meningkatkan jumlah kandungan air dalam garam. Pengaruh jumlah kadar air pada suatu bahan akan mempengaruhi kualitas karena apabila jumlah moisture content melebihi standar maksimum maka memungkinkan terjadinya penurunan daya simpan, cepat rusak, dan berjamur yang akhirnya berpengaruh pada kualitas bahan baku. Perhitungan % kadar air disajikan pada Lampiran 19.
4. Tingkat keasaman (pH)