Kadar Logam Berat Timbal (Pb) pada Akar Mangrove
Avicennia marina
di Perairan Teluk Kendari
Heavy Metal Acumulattion of Lead (Pb) of Mangrove Avicennia marina Roots
in Kendari Bay
Deri *), Emiyarti **) dan La Ode Alirman Afu ***)
Program Studi Manajemen Sumberdaya Perairan FPIK Universitas Haluoleo Kampus Hijau Bumi Tridharma Kendari 93232
e-mail : * [email protected], ** [email protected] dan ***[email protected]
Abstrak
Penelitian ini dilaksanakan pada bulan Mei-Juni 2012 dengan tujuan untuk mengetahui kadar logam berat Timbal (Pb) pada akar mangrove jenis A. marina di perairan Teluk Kendari, Sulawesi Tenggara. Penentuan stasiun pengamatan dilakukan secara purposive sampling berdasarkan lokasi atau daerah yang memiliki jenis mangrove A. marina. Parameter yang diukur meliputi parameter fisika yakni suhu, parameter kimia yaitu salinitas dan pH dan sampel air, sementara pada parameter biologi yaitu akar mangrove A. marina. Analisis logam Timbal (Pb) dilakukan di Laboratorium Balai Besar Laboratorium Kesehatan Makassar, Provinsi Sulawesi Selatan dengan menggunakan AAS (Atomic Absorption Spectrophotometric). Hasil pengukuran parameter fisika-kimia perairan dari ke tiga stasiun nilai suhu tertinggi terdapat di stasiun I dengan kisaran 24-280C dan suhu terendah terdapat di stasiun III dengan kisaran 22-240C. Kisaran salinitas tertinggi berada di stasiun III yaitu 5-12 ppt, diikuti dengan stasiun II dan I berturut-turut 3-10 ppt dan 3-9 ppt. Untuk pH hasil penelitian menunjukkan bahwa kisaran nilai dari tiap stasiun tidak jauh berbeda dimana berturut-turut stasiun I yaitu 6 stasiun II yaitu 5-7, dan stasiun III berkisar antara 3-6. Selanjutnya kadar logam berat Timbal (Pb) pada akar A. marina dari ke tiga stasiun menunjukkan bahwa kisaran tertinggi berada pada stasiun III yaitu 0,007-0,023 mg/L, kemudian pada stasiun II dengan kisaran 0,005-0,013 mg/L dan kadar logam berat Timbal (Pb) terendah terdapat di stasiun I dengan kisaran 0,005-0,010 mg/L. Hasil penelitian menunjukkan bahwa kadar logam berat Timbal Pb pada akar A. marina telah melewati ambang batas baku mutu air laut untuk biota laut yang ditetapkan oleh Kepmen LH No. 51 tahun 2004 yaitu 0,008 mg/L.
Kata Kunci : Mangrove, Avicennia marina, logam timbal (Pb)
Abstract
Heavy metal accumulation of Lead (Pb) in mangrove Avicennia marina roots in Kendari bay was examined from May-June 2012. Purposive sampling was selected to determine sampling stations. Several phisyco-chemical parameters (temperature, salinity, pH, level of Pb) and biology (roots of A. marina ) were analyzed. Pb examination was conducted in Laboratory of Health of Makassar, South Sulawesi using Atomic Absorption Spectrophotometric (AAS). Results showed that the highest temperature was monitored in station I and the lowest was in station III ranging 24-280C and 22-240C respectively. The highest salinity level was found in station III that reached 5-12 ppt, followed by station II and I namely 3-10 ppt and 3-9 ppt. Moreover, pH analysis showed that there was significantly difference in which station I was 6, station II was 5-7 and station III was 3-6. Meanwhile, the highest level of Pb observal in A. marina roots was in station III reaching 0,007-0,023 mg/L followed by station II ranged 0,005–0,013 mg/L and station I with the range of 0,005–0,010 mg/L. The study revealed the level of Pb in A. marina roots exceeded the determined standard 0,008 mg/L based on Decree of Ministry of Environment No. 51 2004 to support marine biota.
Key words: Mangrove, Avicennia marina, metal lead (Pb)
Pendahuluan
Upaya pemanfaatan wilayah pesisir hingga saat ini telah menunjukkan peningkatan yang tinggi dalam rangka menunjang ekonomi negara dan kesejahteraan masyarakat. Upaya-upaya pemanfaatan ini diantaranya melalui
kegiatan pencucian kendaraan bermotor,
perdagangan, pemukiman, pembuangan sampah, jasa transportasi laut dan industri. Dilain pihak,
telah disadari bahwa beberapa daerah pesisir telah menunjukkan adanya gejala kerusakan lingkungan sebagai akibat dari aktivitas manusia dalam upaya pemanfaatan sumberdaya wilayah pesisir.
Perairan pesisir merupakan salah satu dari lingkungan perairan yang banyak mendapat pengaruh dari buangan limbah, baik yang berasal dari daratan maupun di laut lepas. Kenyataannya perairan pesisir dalam menampung dan mengurai
limbah yang terbatas menimbulkan
penumpukkan limbah yang lambat laun
menimbulkan pencemaran.
Berkaitan dengan tingkat pencemaran di wilayah perairan khususnya di beberapa kawasan pesisir di Indonesia, sehingga dianggap perlu untuk melihat keterkaitan faktor penyebab timbulnya dampak terhadap kawasan tersebut. Salah satu kawasan pesisir di Indonesia adalah Teluk Kendari yang terletak di Provinsi Sulawesi Tenggara.
Teluk Kendari merupakan salah satu kawasan yang berdekatan dengan pusat kegiatan
masyarakat. Kondisi seperti ini akan
menyebabkan terjadinya ancaman di sekitar teluk. Salah satu sumber pencemaran yang
berasal dari aktivitas penduduk adalah
dihasilkannya limbah logam berat seperti Timbal (Pb), Tembaga (Cu), Raksa (Hg), Besi (Fe), Mangan (Mn), Seng (Zn), Kromium (Cr), dan Nikel (Ni) yang mungkin saja telah ada disana.
Keberadaan kadar logam berat yang terlarut baik pada air laut, maupun sedimen sangat tergantung pada baik buruknya kondisi perairan tersebut. Semakin tinggi aktivitas yang terjadi disekitar perairan baik di darat maupun areal pantainya maka kadar logam berat dapat meningkat pula.
Timbal (Pb) merupakan salah satu logam berat yang sangat berbahaya bagi kesehatan manusia serta merupakan unsur logam berat yang tidak dapat terurai oleh proses alam (Zhang., et al, 2007). Putra (2002) menambahkan, secara alamiah, Pb dapat masuk ke dalam badan perairan melalui pengkristalan diudara dengan bantuan air hujan, melalui proses modifikasi dari batuan mineral akibat hempasan gelombang dan angin. Pb yang masuk ke dalam badan perairan merupakan dampak dari aktivitas kehidupan manusia. Diantaranya adalah air buangan (limbah) dari industri yang berkaitan dengan Pb.
Mangrove merupakan salah satu
ekosistem pesisir yang mempunyai peranan penting di estuari. Ekosistem mangrove memiliki tingkat produktivitas paling tinggi dibandingkan dengan ekosistem lainnya. Secara ekologis mangrove memiliki banyak fungsi sebagai penghasil sejumlah detritus, perangkap sedimen, pelindung pantai dari hempasan gelombang air laut serta penyerap logam berat dan pestisidan yang menvemari laut.
Panjaitan (2009), mengemukakan
bahwa mangrove memiliki kemampuan dalam
menyerap bahan-bahan organik dan non organik dari lingkungannya kedalam tubuh melalui membran sel. Proses ini merupakan bentuk adaptasi mangrove terhadap kondisi
lingkungan yang ekstrim. Amin (2001),
menambahkan melalui akarnya, vegetasi ini dapat menyerap logam-logam berat yang terdapat pada sedimen maupun kolom air.
Satu diantara beberapa spesies mangrove yang memiliki kemampuan menyerap logam
berat adalah Api-api (Avicennia marina).
Rohmawati (2007), mengemukakan bahwa
pohon A. marina memiliki upaya
penanggulangan materi toksik lain diantaranya
dengan melemahkan efek racun melalui
pengenceran (dilusi), yaitu dengan menyimpan banyak air untuk mengencerkan konsentrasi logam berat dalam jaringan tubuhnya sehingga mengurangi toksisitas logam tersebut.
Berdasarkan uraian di atas, telah
dilakukan penelitian tentang Kadar Logam Berat Timbal (Pb) pada Akar Mangrove A. marina di Perairan Teluk Kendari.
Meningkatnya berbagai kegiatan
pembangunan berupa, pelabuhan, transportasi darat, pertanian, pemukiman, pelayaran dan penangkapan ikan di kawasan Teluk Kendari di duga dapat mempengaruhi kualitas perairannya. Limbah-limbah yang berasal dari
aktivitas manusia dan kegiatan-kegiatan
pembangunan tersebut dapat mencemari
ekosistem mangrove khususnya mangrove jenis
A. marina yang berada di Teluk Kendari.
Berdasarkan beberapa permasalahan
yang ada maka peneliti bermaksud mengkaji kadar logam berat Timbal (Pb) pada akar mangrove A. marina di perairan Teluk Kendari.
Penelitian ini dilakukan dengan tujuan untuk mengetahui kadar logam berat Timbal (Pb) pada akar mangrove jenis A. marina di perairan Teluk Kendari.
Penelitian ini diharapkan dapat menjadi
bahan informasi bagi peneliti mengenai
kemampuan mangrove jenis A. marina dalam
meyerap logam berat, dapat memberikan
gambaran dan informasi kepada masyarakat Kota Kendari tentang kondisi perairan Teluk Kendari dan dapat dijadikan acuan bagi pemerintah dalam
melestarikan ekosistem mangrove jenis A.
Metode Penelitian
Penelitian ini dilaksanakan pada bulan Mei sampai Juni 2012 bertempat di perairan Teluk Kendari, Provinsi Sulawesi Tenggara. Analisis logam berat dan kualitas air dilakukan di laboratorium Balai Besar
Laboratorium Kesehatan Makassar, Provinsi Sulawesi Selatan dengan menggunakan AAS (Atomic Absorption Spectrophotometric).
Alat dan bahan yang digunakan adalah sebagai berikut :
Tabel 1. Alat-alat yang digunakan
No Alat Satuan Kegunaan Keterangan
1 Thermometer 0C Suhu Secara Exitu
2 Handrefraktometer ppt Salinitas Secara Exitu
3 pH meter - pH air Secara Exitu
4 Botol sampel mg/L Sampel air Pb Secara Exitu
5 Pisau/parang - Akar Avicennia marina Secara Exitu
Bahan yang digunakan dalam penelitian ini yaitu larutan Asam Sulfat (H2SO4
-) yang digunakan sebagai pengawet sampel air.
Kegiatan survei pendahuluan dilakukan untuk mengetahui gambaran umum lokasi penelitian berupa keberadaan mangrove jenis
Avicennia marina di lokasi tersebut, sehingga
lebih mudah untuk menetukan stasiun
pengamatan.
Penentuan stasiun penelitian dilakukan
secara purposive sampling, yaitu stasiun
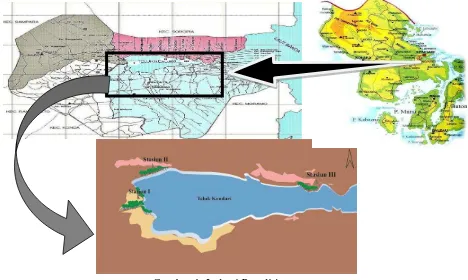
penelitian ditentukan berdasarkan lokasi atau daerah yang memiliki jenis mangrove A. marina, penentuan stasiun pengambilan sampel di dasarkan pada karakteristik lingkungan sekitar Teluk Kendari yang dibagi ke dalam 3 stasiun pengamatan dengan karakteristik sebagai berikut:
I. Stasiun I berada di Kelurahan Korumba
yang merupakan daerah aliran Sungai Wanggu (03058’00.2” LS-122033’01.2” BT)
II. Stasiun II berada di Kelurahan
Lahundape yang berada di sekitar
Swisbell Hotel (03058’08.5” LS
-122033’01.2” BT)
III. Stasiun III berada di Kelurahan Tipulu yang merupakan daerah yang berhubungan langsung dengan perairan
Teluk Kendari (03058’48.9” LS
-122031’49.4” BT).
Pada setiap stasiun tersebut dilakukan pengambilan sampel yang meliputi parameter kualitas air. Gambar lokasi penelitian tersaji pada Gambar 1.
Metode Pengambilan Sampel
Pengambilan sampel air adalah untuk mengukur kualitas air berupa suhu, salinitas dan pH. Pengukuran dan pengamatan dilakukan secara langsung dengan melakukan 3 kali ulangan pada setiap stasiun pengamatan.
Kadar logam berat Timbal (Pb) pada akar dapat diketahui dengan mengambil
sampel akar mangrove A. marina dengan ukuran
diameter batang berkisar 25-30 cm, tinggi berkisar 3-5 m. Sampel akar yang diambil dari 3 titik pengambilan dikeringkan selama beberapa minggu untuk menghilangkan kadar airnya. Kemudian sampel akar dihaluskan dengan menggunakan blender, sedangkan untuk air dapat langsung dianalisis.
Sampel akar ditimbang sebanyak 5 gr kemudian dimasukkan ke dalam tanur pada suhu 450-5000C (pengabuan) selama ± 1 jam. Setelah proses pengabuan selesai selanjutnya sampel akar tersebut dilarutkan dengan menambahkan 10 ml
HNO3. Kemudian ditambahkan akuades sampai
volume menjadi 50 ml.
Larutan tersebut dipanaskan dengan
hot plate sampai mendidih dan volume berkurang 30 ml. Bila belum terjadi kabut ulangi penambahan HNO3 sebanyak 20 ml pada larutan tersebut, kemudian dipanaskan kembali hingga terjadi kabut.
Setelah terjadi kabut tambahkan kembali larutan dengan akuades sehingga volume sampel menjadi 50 ml, lalu diendapkan. Larutan yang telah diendapakan disaring fasa airnya dengan kertas saring. Larutan yang diperoleh siap
dianalisis dengan menggunakan AAS (Atomic
Absorption Spectrophotometric).
Untuk mengetahui kadar logam berat Timbal (Pb) pada air dapat diketahui dengan mengambil air dengan menggunakan botol sampel, dari setiap stasiun pengamatan dengan 3 kali ulangan.
Sampel air laut di ukur 100 ml, kemudian
di tambahkan 10 ml HNO3 pekat. Panaskan
dalam hot plate sampai volume berkurang 30 ml. Tambahkan kembali larutan dengan akuades sampai volume menjadi 100 ml, kemudian di endapkan. Larutan yang telah diendapkan disaring frasa airnya dengan kertas saring. Larutan yang diperoleh siap dianalisis dengan
menggunakan AAS (Atomic Absorption
Spectrophotometric).
Logam Timbal (Pb) ditimbang sebanyak 1 g. Kemudian dilarutkan dengan akuades dalam labu takar 1000 ml. Larutan tersebut mengandung 1000 ppm yang dinamakan larutan induk. Sebanyak 10 ml dari larutan
induk dipipet lalu dimasukkan ke dalam labu takar 100 ml kemudian ditambahkan akuades sampai garis tanda akhir. Larutan yang diperoleh mengandung kosentrasi 100 ppm. Dari larutan 100 ppm. Dari larutan 100 ppm dipipet sebanyak 10 ml lalu dimasukkan ke dalam labu takar 100 ml kemudian ditambahkan akuades sampai garis tanda akhir untuk mendapatkan larutan dengan kosentrasi 10 ppm. Dibuat larutan dengan kosentrasi 10 ppm sebanyak 5 ulangan untuk mempermudah larutan standar berikutnya.
Untuk mendapatkan larutan standar dengan kosentrasi 0,2; 0,4; 0,6; 0,8; dan 1 ppm, berturut-turut di pipet sebanyak 2 ml, 4 ml, 6 ml, 8 ml dan 10 ml dari larutan 10 ppm lalu masing-masing dimasukkan ke dalam labu takar 100 ml kamudian ditambahkan akuades sampai garis tanda akhir.
Alat AAS diset terlebih dahulu,
kemudian dikaliberasikan dengan kurva standar dari logam Pb dengan kosentrasi 0,2; 0,4; 0,6; 0,8; dan 1 ppm. Diukur absorbansi atau kosentrasi masing-masing sampel.
Analisis Data
Untuk mengetahui kosentrasi logam
berat yang sebenarnya digunakan rumus
Hutagalung dan Permana (1994) pada persamaan
(1) berikut:
K. sebenarnya =K AAS x V. p W. s
Dimana :
K. sebenarnya = Konsentrasi sebenarnya (mg/kg)
K AAS = Konsentrasi Atomic Absorption
Spectrophotometric (mg/L)
V.p = Volume pelarut (L)
W.s = Berat Sampel (mg)
Data yang diperoleh dari hasil
perhitungan selanjutnya dianalisis dengan
menggunakan analisis deskriptif. Analisis
deskriptif digunakan untuk menjelaskan atau menggambarkan kadar logam berat Timbal (Pb) pada akar mangrove A. marina.
Hasil
1. Gambaran Umum Lokasi Penelitian
Secara gegografis Perairan Teluk Kendari di kelilingi oleh daratan Kota Kendari sebagai ibu kota Propinsi Sulawesi Tenggara yang terletak diantara 3057’50”-3059’30” LS dan
122031’50”-122036’30” BT (Pemda Kota
Kendari, 2000). Ditinjau dari segi administratif, teluk kendari mempunyai batasan wilayah sebagai berikut :
Sebelah Utara berbatasan dengan Kecamatan
Kendari dan Kendari Barat;
Sebelah Timur berbatasan dengan Pulau
Bungkutoko;
Sebelah Selatan berbatasan dengan
Kecamatan Poasia dan Abeli;
Sebelah Barat berbatasan dengan Kecamatan Mandonga dan Kambu.
Kawasan Kota Kendari banyak dilalui sungai-sungai yang sebagian besar bermuara di perairan Teluk kendari, diantaranya Sungai Wanggu dan Sungai Kambu yang umumnya mengalir sepanjang tahun dengan debit aliran diperkirakan lebih dari 3 m3/detik (BAPPEDA Tingkat I Sulawesi Tenggara dan Universitas Haluoleo 1998 dalam Alirman, 2005).
2. Kondisi Lingkungan Perairan (Suhu Air, Salinitas dan pH Air)
a. Suhu Air
Kisaran nilai suhu dari tiap stasiun pengamatan di perairan Teluk Kendari dapat dilihat pada Gambar 2 berikut:
Gambar 2. Suhu pada setiap stasiun pengamatan
Kisaran nilai suhu tertinggi terdapat di stasiun I dengan kisaran 24-280C selanjutnya stasiun II dengan kisaran 23-250C dan suhu
terendah terdapat di stasiun III dengan kisaran 22-240C.
b. Salinitas
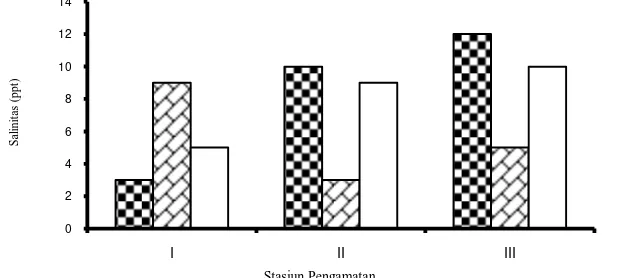
Kisaran nilai salinitas dari tiap stasiun pengamatan di perairan Teluk Kendari dapat di liat pada gambar 3 berikut:
Gambar 3. Salinitas pada setiap stasiun pengamatan
0 5 10 15 20 25 30
I II III
S
u
h
u
(
0C)
Stasiun Pengamatan
Sub Stasiun 1
Sub Stasiun 2
Sub Stasiun 3
0 2 4 6 8 10 12 14
I II III
S
al
ini
ta
s
(ppt
)
Stasiun Pengamatan
Sub Stasiun 1
Sub Stasiun 2
c. pH Air
Kisaran Nilai pH dari tiap stasiun pengamatan di perairan Teluk Kendari dapat di lihat pada Gambar 4 berikut:
Gambar 4. pH pada setiap stasiun pengamatan
Kisaran nilai pH dari tiap stasiun tidak jauh berbeda dimana berturut-turut stasiun I yaitu
6 stasiun II yaitu 5-7, dan stasiun III berkisar antara 3-6.
3. Kadar Logam Berat Timbal (Pb) pada Air
Berdsarkan hasil analisa data tentang kadar logam berat Pb pada air di sekitar area mangrove
A. marina di peroleh hasil yang berbeda-beda
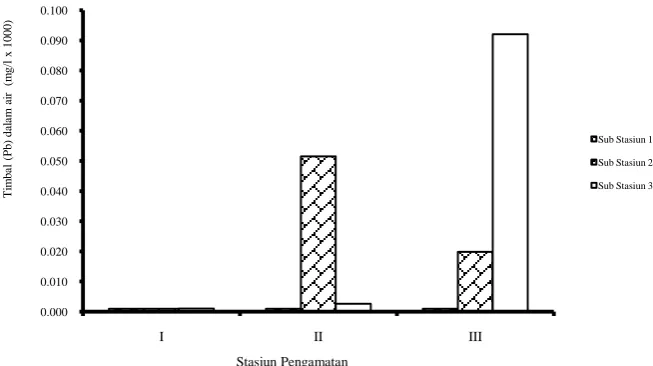
antara ketiga stasiun. Gambar 5 menunjukkan kisaran kadar logam berat Timbal (Pb) pada air.
Gambar 5. Kadar logam berat timbal (Pb) pada air
Kadar logam berat Timbal (Pb) di air pada stasiun III lebih tinggi dengan kisaran nilai
0,001x10-3-0,092x10-3 mg/L di bandingkan
stasiun I dan II dengan kisaran berturut-turut 0,001x10-3-0,001x10-3 mg/L dan 0,001x10-3 -0,052x10-3 mg/L.
0 1 2 3 4 5 6 7 8
I II III
pH
A
ir
Stasiun Pengamatan
Sub Stasiun 1
Sub Stasiun 2
Sub Stasiun 3
0.000 0.010 0.020 0.030 0.040 0.050 0.060 0.070 0.080 0.090 0.100
I II III
T
im
b
a
l
(P
b
)
da
la
m
a
ir
(m
g/l
x
1000)
Stasiun Pengamatan
Sub Stasiun 1
4. Kadar Logam Berat Timbal (Pb) pada Akar Avicennia marina
Berdasarkan hasil pengukuran kadar logam berat Timbal (Pb) pada akar A. marina
dengan menggunakan metode AASmenunjukkan
bahwa dari tiap stasiun memiliki kadar logam berat yang berbeda. Untuk lebih jelasnya hasil pengukuran ketiga stasiun disajikan pada Gambar 6.
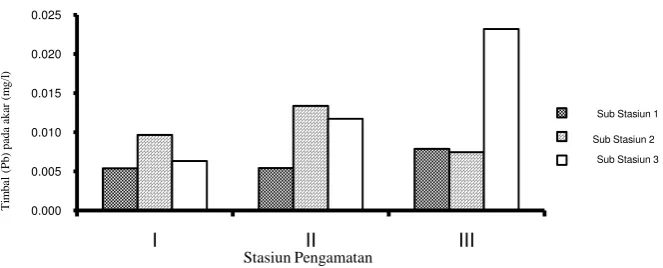
Kadar logam berat Timbal (Pb) pada akar mangrove A. marina dari ke tiga stasiun
menunjukkan bahwa kisaran tertinggi berada pada stasiun III yaitu 0,007-0,023 mg/L, kemudian pada stasiun II dengan kisaran 0,005-0,013 mg/L dan kandungan logam berat Timbal (Pb) terendah terdapat di stasiun I dengan kisaran 0,005-0,010 mg/L.
Gambar 6. Kadar logam berat Timbal (Pb) pada akar A. marina
Pembahasan
1. Kondisi Lingkungan Perairan (Suhu Air, Salinitas, dan pH Air)
a. Suhu Air
Mukhtasor (2007), mengemukakan suhu
merupakan salah satu parameter untuk
mempelajari transportasi dan penyebaran polutan yang masuk ke lingkungan laut. Sementara menurut Effendi (2000), berpendapat bahwa suhu suatu badan air dipengaruhi oleh musim, lintang (latitude), ketinggian dari permukaan laut (altitude), waktu dalam satu hari, sirkulasi udara, penutupan awan, dan aliran serta kedalaman dari badan air.
Perubahan suhu berpengaruh terhadapa proses, fisika, kimia dan biologi badan air. Berdasarkan Gambar 2 Perbedaan suhu air pada tiap stasiun diakibatkan adanya perbedaan intensitas cahaya yang mengenai air ataupun di sebabkan karena jumlah vegetasi tutupan mangrove. Pada stasiun I tampak bahwa jumlah vegetasi mangrove lebih sedikit dibandingkan dengan stasiun II dan III. Selain itu tingginya suhu di stasiun I dipengaruhi oleh waktu pengambilan sampel dimana dilakukanyang dilakukan pada siang hari.
Suhu merupakan salah satu parameter untuk mempelajari transportasi dan penyebaran polutan yang masuk ke lingkungan laut. Mukhtasor (2007), menyatakan bahwa biasanya
suhu air laut berkisar antara -2 sampai 300C. Sedangkan kisaran suhu yang baik bagi
kehidupan organisme adalah 18-300C.
Berdasarkan hal tersebut, maka suhu perairan di lokasi penelitian digolongkan masih baik serta dapat mendukung kehidupan organisme yang hidup di dalamnya.
b. Salinitas
Salinitas adalah konsentrasi dari total ion yang terdapat di perairan Boyd (1988)
dalam Effendi (2000). Berdasarkan Gambar 3 kisaran salinitas tertinggi berada di stasiun III yaitu 5-12 ppt, hal ini disebabkan karena stasiun ini berada di Teluk Kendari sehingga masukkan air laut lebih besar di bandingkan dengan air tawar. Mukhtasor (2007), salinitas bertambah di permukaan laut karena evaporasi dan percampuran yang disebabkan oleh arus maupun oleh upwelling, sehingga air akan menjadi lebih kental. Sementara kisaran nilai salinitas terendah berada di stasiun I yaitu 3-9 ppt karena stasiun ini berada di kawasan perairan Sungai Wanggu. Burzynski and Zurek (2007) menambahkan nilai salinitas pada perairan pesisir sangat dipengaruhi oleh masukkan air tawar dari sungai.
Hutagalung (1991) dalam Mukhtasor
(2007), mengemukakan bahwa nilai salinitas
perairan laut dapat mempengaruhi faktor
konsentrasi logam berat yang mencemari lingkungan laut, dimana penurunan salinitas pada
perairan dapat menyebabkan tingkat
bioakumulasi logam berat pada organisme semakin meningkat.
c. pH Air
Kisaran pH air 6-8 masih dikatakan normal, sedangkan pH air tercemar seperti air buangan berbeda-beda tergantung jenis air buangannya. Perubahan keasaman pada air buangan, baik kearah alkali (pH diatas 7) maupun ke arah asam (pH dibawah 7), akan sangat mengganggu kehidupan didalam perairan tersebut. Nilai pH suatu perairan menggambarkan keseimbangan antara asam dan basa dalam air dan yang diukur adalah konsentrasi ion hidrogen.
Berdasarkan Gambar 4, hasil penelitian menunjukkan bahwa kisaran nilai pH dari tiap stasiun tidak jauh berbeda dimana berturut-turut stasiun I yaitu 6 stasiun II yaitu 5-7, dan stasiun III berkisar antara 3-6. Secara umum nilai pH di
setiap stasiun tidak jauh berbeda yang
menunjukkan bahwa perairan tersebut bersifat asam. Hal ini disebabkan karena stasiun penelitian sebagian besar adalah daerah rawa yang memiliki nilai derajat keasaman yang rendah yang kemungkinan dipengaruhi oleh banyaknya bahan organik yang meningkatkan
proses penguraian. Yan, et al., (2010)
mengemukakan bahwa penurunan pH akan menyebabkan toksisitas logam berat menjadi semakin besar dimana sebagian besar biota akuatik sensitif terhadap perubahan yang sangat mempengaruhi proses biokimiawi perairan. Namun secara umum pengukuran nilai derajat keasaman berdasarkan Kepmen LH NO. 51 tahun 2004, ke tiga stasiun penelitian tersebut masih mendukung kehidupan organisme perairan di sekitarnya.
2. Kadar Logam Berat Timbal (Pb) pada Air
Sumber timbal bisa berasal dari
kenderaan yang menggunakan bahan bakar bertimbal dan juga dari biji logam hasil pertambangan, peleburan, pabrik pembuatan timbal atau recycling industri, debu, tanah, cat, mainan, perhiasan, air minum, permen, keramik, obat tradisional dan kosmetik (Marchand, et al.,
2011).
Pencemaran laut terjadi karena laut menerima zat-zat pencemar baik yang merupakan zat padat maupun cair terutama yang dibawa oleh sungai sebagai tempat yang paling mudah membuang limbah yang akhirnya bermuara di laut. Banyaknya zat pencemar yang masuk ke laut telah melampaui daya dukungnya sehingga laut menjadi sangat kotor dan tercemar (MacFarlane, et al., 2000).
Effendi (2000), menyatakan bahan
pencemar memasuki badan air melalui berbagai cara seperti pembuangan limbah oleh industri, pertanian, domestik dan perkotaan, dan lain-lain. Palar (2004) dalam Rohmawati (2007), juga menjelaskan logam-logam lingkungan perairan umumnya berada dalam bentuk ion. Ion-ion tersebut ada yang berupa ion bebas, pasangan ion organik, ion-ion kompleks dan bentuk-bentuk ion lainnya. Umumnya logam-logam yang terdapat dalam tanah dan perairan dalam bentuk persenyawaan, seperti senyawa hidroksida, senyawa oksida, senyawa karbonat dan senyawa sulfida. Senyawa-senyawa itu sangat mudah larut dalam air.
Berdasarkan Gambar 5, hasil analisa data tentang kadar logam berat Pb pada air di sekitar area mangrove A. marina dengan menggunakan metode AAS di peroleh hasil bahwa kadar logam berat Timbal (Pb) di air pada stasiun III lebih tinggi dengan kisaran nilai
0,001x10-3-0,092x10-3 mg/L di bandingkan
stasiun I dan II dengan kisaran berturut-turut 0,001x10-3-0,001x10-3 mg/L dan 0,001x10-3 -0,052x10-3 mg/L.
Hasil analisis menunjukkan bahwa
stasiun III lebih banyak menerima masukkan limbah yang mengandung Pb. Hal ini di pengaruhi oleh aktivitas perkapalan berupa sarana transportasi dan jalur pengangkutan barang, aktivitas pemukiman juga mempengaruhi jumlah kadar logam berat di lingkungan perairan Teluk Kendari. Umumnya kandungan logam yang terukur di setiap stasiun cenderung seragam dengan variasi konsentrasi yang relatif kecil.
Emiyarti (2004), mengemukakan bahwa hal tersebut di sebabkan oleh tipe perairan di daerah penelitian adalah semi tertutup yang terlindung oleh Pulau Bungkutoko sehingga sirkulasi air yang terjadi secara vertikal akan mendistribusikan unsur logam berat secara merata di perairan.
Berdasarkan kisaran nilai yang di dapatkan dari tiap stasiun selama penelitian bila dibandingkan dengan baku mutu yang telah ditetapkan Kempen LH No. 51 Tahun 2004 baku mutu logam berat Timbal (Pb) untuk air laut yaitu sebesar 0,005 mg/L dapat dinyatakan bahwa perairan tersebut masih berada di bawah ambang batas dan masih mendukung kehidupan organisme perairan.
3. Kadar Logam Berat Timbal (Pb) pada Akar Avicennia marina
yang mampu tumbuh dan berkembang pada
daerah pasang surut pantai berlumpur
(Thampanya, et al., 2002).
Secara alami Pb di perairan bersumber dari partikel udara berupa asap kendaraan yang dibawa hujan dan secara non alami akibat aktivitas manusia berupa buangan limbah cair dan padat yang memungkinkan terlapisnya
pneumatophora dengan sampah yang akan mengakibatkan kematian pohon-pohon
mangrove (Blackmore, 2000 dalam Joyeux, et
al., 2004).
Mulyadi (2009), mengemukakan secara umum mangrove yang tumbuh di ujung sungai besar berperan sebagai penampungan terakhir bagi limbah dari aktivitas perkotaan yang terbawa aliran sungai. Limbah padat dan cair yang terlarut dalam air sungai terbawa arus menuju muara sungai dan laut lepas. Area
hutan mangrove akan menjadi daerah
penumpukan limbah, terutama jika polutan yang masuk ke dalam lingkungan estuari melampaui kemampuan pemurnian alami oleh air. Mangrove alami berperan efektif dalam melindungi pantai dari tekanan alam dan erosi.
Logam berat yang masuk ke dalam
lingkungan perairan akan mengalami
pengendapan, pengenceran dan dispersi,
kemudian diserap oleh organisme yang hidup di perairan tersebut (Defew, et al., 2004).
Berdasarkan hasil penelitian yang
dilakukan di ketahui bahwa tumbuhan Faktor konsentrasi, kemampuan tumbuhan dalam mengakumulasi ion sampai tingkat konsentrasi tertentu, bahkan dapat mencapai beberapa tingkat lebih besar dari konsentrasi ion dalam mediumnya; 2) Perbedaan kuantitatif akan kebutuhan hara yang berbeda pada tiap jenis tumbuhan.
Secara umum, logam berat untuk pertumbuhan dan perkembangan tumbuhan dibagi menjadi dua yaitu logam esensial dan non esensial. Cu dan Zn merupakan logam yang termasuk esensial, sedangkan Pb merupakan logam non esensial bagi tumbuhan (Yoon, et al., 2006).
Hasil pengukuran kadar logam berat Timbal (Pb) pada akar mangrove A. marina dari ke tiga stasiun menunjukkan bahwa kisaran tertinggi berada pada stasiun III yaitu
0,007-0,023 mg/L, kemudian pada stasiun II dengan kisaran 0,005-0,013 mg/L dan kandungan logam berat Timbal (Pb) terendah terdapat di stasiun I dengan kisaran 0,005-0,010 mg/L.
Pada stasiun III dan II kadar Pb lebih tinggi dibandingkan dengan kedua stasiun I. Hal
ini disebabkan karena pada stasiun ini
dipengaruhi oleh aktivitas Teluk Kendari berupa pelabuhan, industri, aktivitas pemukiman yang menjadi sumber adanya logam berat Timbal (Pb) di akar mangrove, disamping itu kondisi perairan teluk yang semi tertutup menyebabkan seluruh aktivitas daratan akan bermuara ke arah pantai.
Pohon api-api (A. marina) memiliki akar yang tumbuh dengan jarak teratur secara vertikal dari akar horizontal yang terbenam di dalam tanah (Alongi, 2008).
Berdasarkan hasil penelitian yang telah dilakukan dapat diketahui bahwa jumlah kadar logam berat Timbal (Pb) di akar dan kolom air menunjukkan perbedaan yang signifikan dimana jumlah akumulasi logam berat Timbal (Pb) pada akar mangrove A. marina lebih besar di bandingkan pada air yang berada di sekitar area mangrove. Dalam hal ini dapat di nyatakan
bahwa tumbuhan A. marina mempunyai
kemampuan dalam menyerap materi toksik di lingkungan. MacFarlane, et al., (2000), mangrove merupakan tumbuhan tingkat tinggi di kawasan pantai yang dapat berfungsi untuk menyerap bahan-bahan organik dan non-organik sehingga dapat dijadikan bioindikator logam berat. Hal ini di dukung oleh penelitian yang dilakukan oleh
Rohmawati (2007), menjelaskan bahwa
tumbuhan A. marina mampu mengakumulasi
logam berat. Begitu pula penelitian yang dilakukan oleh Amin (2001), juga menjelaskan
bahwa tumbuhan A. marina juga mampu
mengakumulasi logam berat Cu dan Pb pada
bagian organ akar, dan juga mampu
mengakumulasi dibagian daun, baik daun muda maupun daun tua.
Berdasarkan Kepmen LH No. 51 tahun 2004 kisaran nilai yang di dapatkan selama penelitian diketahui bahwa pencemaran logam berat Timbal Pb termasuk tingkat pencemaran polusi berat karena kandungan logam berat Pb telah melebihi ambang batas kandungan logam berat alamiah di perairan laut yaitu 0,008 mg/L.
Menurut Darmono (2001) dalam Rohmawati
kandungan logam berat dalam air dan organisme yang hidup di dalamnya sangat rendah, bahkan tidak terdeteksi.
Simpulan
1.
Kadar logam berat Timbal (Pb) pada akarAvicennia marina di setiap stasiun penelitian secara umum telah melewati ambang batas baku mutu yang ditetapkan oleh Kepmen LH No. 51 tahun 2004 tentang baku mutu air laut untuk biota laut yaitu 0,008 mg/l.
2.
Mangrove A. marina mampu mengakumulasi logam berat Timbal (Pb) sehingga dapatdijadikan sebagai indikator pencemaran
logam berat Timbal (Pb).
Persantunan
Penulis menyampaikan ucapan terima kasih kepada Pembimbing I Emiyarti, S.Pi, M.Si dan Pembimbing II La Ode Alirman Afu, S.Pd, M.Si serta Kepala Laboratorium Fakultas Perikanan dan Ilmu Kelautan Ruslaeni, M.Si, M.Pi atas bantuannya dalam menyusun dan melakukan analisis sampel penelitian.
Daftar Pustaka
Alirman, A. 2005. Pengaruh Limbah Organik
Terhadap Kualitas Perairan Teluk
Kendari Sulawesi Tenggara. Tesis
Magister. Sekolah Pascasarjana. Institut Pertanian Bogor. Bogor. 111 hal. Alongi, D. M. 2008. Mangrove forests:
Resilience, Protection from Tsunamis, and Responses to Global Climate Change. Estuarine, Coastal and Shelf Science 76: 1-13
copper and cadmium on photosynthesis in cucumber cotyledons. Photosynthetica 45, 239–244.
Defew, L. H.., M.M. James, and M.G. Hector.
2004. An Assessment of Metal
Contamination in Mangrove Sediments and Leaves from Punta Mala Bay, Pacific Panama. Marine Pollution Bulletin. 50: 547-552.
Effendi, H. 2000. Telaahan Kualitas Air. Jurusan
Manajemen Sumberdaya Perairan
Fakultas Perikanan Dan Ilmu Kelautan. IPB. Bogor, 258 hal.
Emiyarti. 2004. Karakteristik Fisika Kimia
Substrat dan Hubungannya dengan
Struktur Komunitas Makrozoobentos di Perairan Teluk Kendari. Tesis Pasca Sarjana. IPB. Bogor.
Fitter, A.H dan Hay, R.K.M. 1991. Fisiologi Lingkungan Tanaman. Gajah Mada Universitas Press. Yogyakarta, 286 hal. Focil Indonesia-Lestari. 2008. Cida Jaringan
Guru PKLH Kota Kendari. Sulawesi Tenggara. 2-4p.
Joyeux, J.C., E. A. C. Filho, and C. De Jesus. 2004. Trash Metal Contamination in Estusrine Fishes from Vitoria Bay, ES, Brazil. Brazilian Archieves of Biology and Technology, 47 (5) : 765-774. MacFarlane, G.R., M.D. Burchett. 2000. Cellular
Distribution of Copper, Lead and Zinc in the Grey Mangrove, Avicennia marina
(Forsk.) Vierh. Aquatic Botany 68: 45– 59.
Marchand, C., M. Allenbach, E. Lallier-Vergès, 2011. Relationships between heavy metals distribution and organic matter
cycling in mangrove sediments
(Conception Bay, New Caledonia). Geoderma, 160: 444–456.
Mukhtasor, 2007. Pencemaran Pesisir dan Laut. Pradnya Paramita. Jakarta, 322 hal. Mulyadi, E., Laksmono. R., Aprianti. D., 2009.
Fungsi Mangrove Sebagai Pengendali Pencemar Logam Berat. Jurnal Ilmiah Teknik Lingkungan, 1:33-40.
Palar, H., 1994. Pencemaran dan Toksikologi Logam Berat. Rineka Cipta. Jakarta, 289 hal.
Panjaitan, G. Y., 2009. Akumulasi Logam Berat Tembaga (Cu) Dan Timbal (Pb) Pada
Pohon Avicennia marina Di Hutan
Mangrove. Skripsi. Departemen
Kehutanan Fakultas Pertanian
Universitas Sumatera Utara. Medan. 58 hal.
Putra, K. G. D., 2002. Petunjuk Teknis Pemantauan Kualitas Air. Undayana University Press. Denpasar, 275 hal. Rohmawati, 2007. Daya Akumulasi Tumbuhan
Avicennia marina Terhadap Logam Berat (Cu, Cd, Hg) Di Pantai Kenjeran
Surabaya. Skripsi Jurusan Biologi
Fakultas Sains Dan Biologi. Universitas Islam Negeri Malang. 53 hal.
Thampanya, U., J. E. Vermaat., J. Terrados. 2002. The Effect of Increasing Sediment Accretion on the Seedlings of Three
Common Thai Mangrove Species.
Aquatic Botany, 74: 315–325
a Common Mangrove Species in South China, with and without Cotyledons. Aquatic Botany, 92: 112–118
Yoon, J., C. Xinde, Z. Qixing , and L.Q. Ma. 2006. Accumulation of Pb, Cu, and Zn in
Native Plants Growing on a
Contaminated Florida Site. Science of the Total Environment:456-464.
Zhang, F.Q., Wang, Y.S., Lou, Z.P., Dong, J.D., 2007. Effect of heavy metal stress on
antioxidative enzymes and lipid
peroxidation in leaves and roots of two
mangrove plant seedlings (Kandelia