IMMUNOTHERAPY PADA MULTIPLE MYELOMA
Oleh
MULIANIFAKULTAS KEDOKTERAN
UNIVERSITAS UDAYANA
i
UCAPAN TERIMA KASIH
Pertama-tama perkenankanlah penulis memanjatkan puji syukur ke hadapan Ida Sang Hyang Widhi Wasa/Tuhan Yang Maha Esa, karena atas asung wara nugraha-Nya/karunia-Nya, tulisan ini dapat diselesaikan.
Pada kesempatan ini kami menyampaikan terima kasih kepada Bapak Dekan
Fakultas Kedokteran Universitas Udayana dan dr. I G. A. Widianti, M. Biomed.,
selaku Ketua Bagian Anatomi Fakultas Kedokteran Universitas Udayana yang telah
memberikan kesempatan untuk membuat tulisan ini.
Penulis menyadari bahwa tulisan ini masih jauh dari kesempurnaan, sehingga sangat diharapkan adanya kritik dan saran yang bersifat membangun.
Denpasar, Desember 2015
ii DAFTAR ISI
Halaman SAMPUL
UCAPAN TERIMA KASIH ... i
DAFTAR ISI ... ii
DAFTAR GAMBAR ... iii
DAFTAR TABEL ... iv
DAFTAR SINGKATAN DAN LAMBANG... v
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Tujuan ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1. Biologi Molekuler Keganasan Sel Limfoid. ... 4
2.2. Antigen dan Imunogenitas Tumor ... 5
2.3. Multiple Myeloma ... 7
2.4. Respon Imun terhadap Tumor ... 17
2.5. Immunotherapy ... 19
SIMPULAN ... 30
iii
DAFTAR GAMBAR
Halaman
2.1 Mekanisme terbentuknya TSTA dan TATA ... 6
2.2 Asal mula multiple myeloma ... 8
2.3 Imunoglobulin rantai λ pada multiple myeloma ... 9
2.4 Bence Jones Protein ... 10
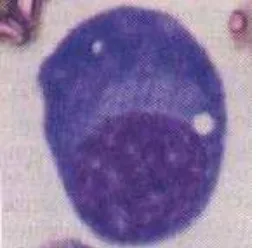
2.5 Sel plasma normal ... 11
2.6 A. Plasmacytoma pada soft tissue; B. Aspirasi sumsum tulang multiple myeloma, sel-sel plasma dan plasmablas menggantikan jaringan hematopoesis normal... 11
2.7 Protein M pada immunoelectrophoresis... 12
2.8 Lesi osteolitik pada os humerus dekstra ... 14
2.9 Mekanisme tumor menghindari sistem imun ... 18
2.10 Vaksin dari sel dendritik yang diberi antigen tumor ... 23
2.11 Vaksin dari sel dendritik yang telah ditransfeksi DNA ... 24
2.12 Immunotherapy dengan costimulator ... 25
2.13 Vaksinasi dengan sel tumor yang mengekspresikan GM-CSF ... 26
iv
DAFTAR TABEL
Halaman
2.1 Antigen tumor yang dikenal oleh limfosit T ... 7
2.2 Beberapa penyakit yang berkaitan dengan monoklonal imunoglobulin ... 8
2.3 Gejala klinis dan patofisiologi multiple myeloma ... 13
2.4 Klasifikasi multiple myeloma ... 16
v
DAFTAR SINGKATAN DAN LAMBANG ACT : Adoptive Cell Therapy
ADCC : Antibody Dependent Cell (mediated) Cytotoxicity AFP : Alpha Feto Protein
APC : Antigen Presenting Cell CD : Cluster of Differentiation CD4+ : Cluster of Differentiation 4+ CD8+ : Cluster of Differentiation 8+
CpG : Synthetic Cytosine Phosphate-Guanosine CTL : Cytotoxic T lymphocyte
CTL-Ps : Cytotoxic T Lymphocyte Precursors DC : Dendritic Cell
DNA : Deoxyribonucleic Acid Fc : Fragment crystallizable
G-CSF : Granolocyte Colony Stimulating Factor G-CSF : Granulocyte-Colony Stimulating Factor
GM-CSF : Granulocyte Monocyte-Colony Stimulating Factor Id : Idiotypic portion
IMiDS : Immunomodulatory Drugs KLH : Keyhole Limpet Haemocyanin LeY : Lewis Y antigen
mAb : Antibodi monoklonal
vi MM : Multiple Myeloma
NK : Natural Killer
PSA : Prostate Specific Antigen RNA : Ribose Nucleic Acid SD : Sel Dendritik
TAA : Tumor Associated Antigen
TATA : Tumor-Associated Transplantation Antigen
Tc : T cytotoxic
TGF- : Transforming Growth Factor
Th : T helper
TIL : Tumor-infiltrating lymphocytes TNF : Tumor Necrosis Factor
TSA : Tumor Specific Antigen
TSTA : Tumor-Specific Transplantation Antigen
1 BAB I PENDAHULUAN 1.1 Latar Belakang
Manusia sebagai mahluk hidup, tidak dapat hidup sendiri. Melainkan memerlukan mahluk lain dalam hidupnya sehingga dikatakan mahluk sosial. Dalam kehidupan sosialnya, manusia berinteraksi satu sama lain dan juga lingkungannya.
Sayangnya, lingkungan banyak mengandung bermacam-macam agen infeksi seperti virus, jamur dan parasit. Agen tersebut dapat mangakibatkan kerusakan patologis dan akhirnya membunuh hospes bila tidak tertangani dengan baik Wahab dan Julia, 2002).
Normalnya, tiap individu memiliki sistem imun untuk melawan agen infeksi. Respon imun merupakan tanggapan sistem imun terhadap agen asing atau antigen. Proses ini terjadi bila telah terjadi pengenalan antigen oleh sel-sel limfosit (Wahab dan Julia, 2002).
Bila respons imun baik, maka agen infeksi dapat dilawan dan tubuh tetap sehat. Namun kadang terjadi penyimpangan dan gangguan sistem tersebut, seperti misalnya pada penyakit-penyakit alergi, autoimun dan kanker.
Demikian pula pada multiple myeloma, terjadi proliferasi abnormal sel plasma ganas. Kanker tersebut menghasilkan monoclonal immunoglobulin dan menginvasi dan menghancurkan jaringan tulang sekitar (Berenson, 2008).
2
walaupun faktor kromosomal dan genetik, radiasi dan kimia diperkirakan menjadi penyebabnya (Berenson, 2008).
Manifestasinya meliputi: nyeri tulang, insufisiensi ginjal, hiperkalsemia, anemia dan infeksi berulang. Penyakit ini bersifat progresif dan fatal, tapi akhir-akhir ini usia hidup penderita meningkat sampai lebih dari 5 tahun dengan pengobatan yang tepat. Respons terhadap terapi maupun prognosis berkaitan erat dengan lineage dan stadium diferensiasi sel. Untuk itu, penyakit ini perlu didiagnosis dengan pasti (Kresno, 2003).
Diagnosis pasti ditemukan dari adanya M-protein, lytic bone lesions, light-chain proteinuria, atau excessive marrow plasma cells (Berenson, 2008). Penyakit
ini dapat diobati dengan pemberian terapi spesifik, suportif maupun immunotherapy. Namun kedua cara yang pertama seringkali mengalami
kegagalan sehingga sekarang dikembangkan immunotherapy. Cara tersebut menggunakan cara-cara imunologis dalam mengontrol tumor sehingga dapat mengeradikasi tumor primer, metastasis dan residu yang tertinggal setelah terapi spesifik (konvensional). Eradikasi spesifik tumor dengan kerusakan minimal terhadap sel normal host merupakan hasil immunotherapy ideal yang diharapkan terjadi (Kresno, 2003).
3
peran sistem imun sebagai immunotherapy dalam mencegah pertumbuhan tumor spontan, meningkatkan surveillance terhadap tumor, menginduksi resistensi terhadap sisa sel ganas dan kekambuhan tumor, menghambat perkembangan tumor lebih lanjut dan dalam menentukan jenis pengobatan (Kresno, 2003). Karena itu, dalam tulisan ini penulis akan membahas mengenai peran immunotherapy dalam mengobati multiple myeloma.
1.2 Tujuan
1. Untuk mengetahui lebih banyak tentang multiple myeloma.
4 BAB II
TINJAUAN PUSTAKA
2.1 Biologi Molekuler Keganasan Sel Limfoid
Keganasan, termasuk keganasan sel limfoid terjadi karena akumulasi kelainan genetik dalam sel. Pertumbuhan sel diatur oleh protoonkogen (growth promoting oncogenes) dan tumor suppressor gene. Kedua gen tersebut
memproduksi protein yang akan meningkatkan dan menekan pertumbuhan sel sesuai kebutuhan (Kresno, 2003a).
Normalnya, sebagian besar onkogen dan gen supresor mengatur siklus sel secara langsung. Aktivasi onkogen berlebihan terjadi melalui perubahan struktur gen, translokasi kromosom, peningkatan ekspresi gen atau mutasi faktor-faktor yang mengontrol ekspresi gen yang bersangkutan. Akibatnya, sel-sel akan berproliferasi aktif. Proliferasi yang berlebihan ini dicegah oleh gen supresor (Kresno, 2003a).
Bila gen supresor mengalami mutasi, maka akan mengakibatkan supresi pertumbuhan sel menghilang. Hal-hal tersebut di atas akan menyebabkan hilangnya kontrol pertumbuhan sehingga sel bertransformasi menjadi ganas (Kresno, 2003a).
5
disebut dengan immune surveillance (Kresno, 2003a; Subowo, 2009). Pertumbuhan, proteksi maupun penolakan tumor dipengaruhi oleh komponen dan mekanisme efektor sistem imun serta imunogenitas tumor (Kresno, 2003a).
2.2 Antigen dan Imunogenitas Tumor
Kanker mengekspresikan berbagai jenis molekul yang kemudian dikenali oleh sistem imun sebagai antigen asing (Subowo, 2009). Proteksi sistem imun terhadap timbulnya tumor disebut dengan imunitas tumor. Imunitas sejati terjadi hanya pada tumor yang mengekspresikan antigen imunogenik (Baratawijaya dan Rengganis, 2009).
Antigen ini digunakan sebagai sasaran sistem imun untuk dihancurkan secara spesifik. Menurut gambaran ekspresinya pada sel tumor dan sel normal, antigen tersebut dapat dibagi menjadi: tumor specific antigen (TSA) dan tumor associated antigen (TAA). Respon imun terhadap TSA dapat menghancurkan sel tumor tanpa
merusak sel yang sehat. Berikut termasuk dalam TSA: protein yang diproduksi akibat mutasi satu atau lebih gen dan protein dalam tumor yang diinduksi virus. Namun, keuntungan TSA belum jelas (Baratawijaya dan Rengganis, 2009).
6
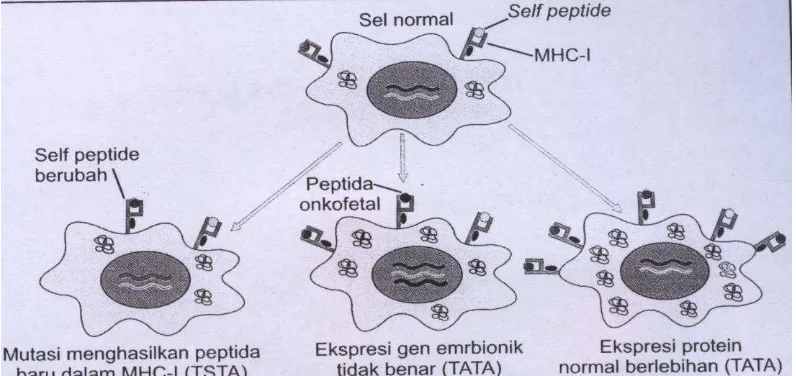
Sementara, TATA tidak spesifik bagi tumor dan dapat merupakan protein yang diekspresikan pada sel normal saat fetus dan tidak menimbulkan respons imun. Normalnya, tidak diekspresikan pada dewasa. Antigen yang tidak spesifik tumor, disebut juga dengan TAA (Baratawijaya dan Rengganis, 2009).
Gambar 2.1 Mekanisme terbentuknya TSTA dan TATA (Baratawijaya dan Rengganis, 2009)
Beberapa antigen yang termasuk dalam TAA, antara lain: oncofetal antigen, tissue-specific differentiation antigen (melanoma differentiation antigen gp 100,
7
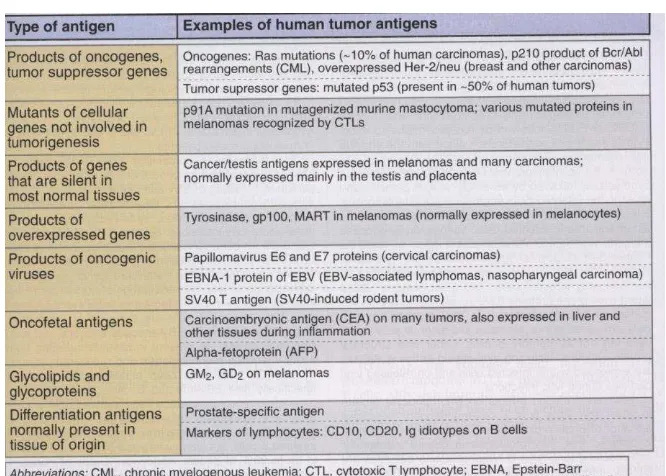
Tabel 2.1 Antigen tumor yang dikenal oleh limfosit T (Abbas, Lichtman and Pillai, 2007b)
2.3Multiple myeloma
Multiple myeloma merupakan proliferasi abnormal sel plasma ganas. Kanker
ini menghasilkan monoclonal immunoglobulin yang menginvasi dan menghancurkan jaringan tulang sekitar (Berenson, 2008).
8
Tabel 2.2 Beberapa penyakit yang berkaitan dengan monoklonal imunoglobulin (Henry, 2001).
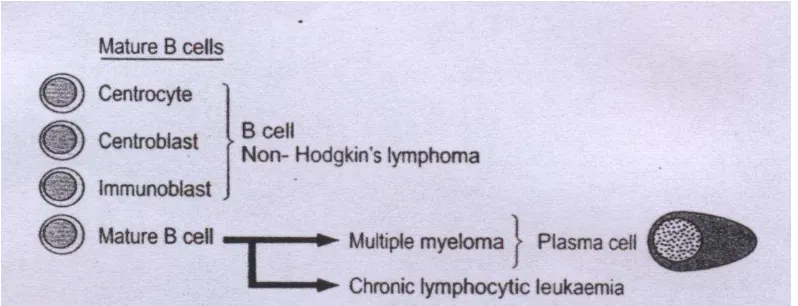
Sel B matur atau sel plasma ganas seperti pada multiple myeloma mempunyai ciri-ciri yang sama dengan sel B pada stadium diferensiasi yang sudah lanjut. Sel plasma normal maupun sel myeloma termasuk dalam sel B stadium diferensiasi terminal (Kresno, 2000).
Gambar 2.2 Asal mula multiple myeloma (Peakman and Vergani, 2006).
9
imunoglobulin dengan struktur dan sifat yang identik dalam hal susunan H dan L-chain, spesifisitas, kecepatan migrasi serta sifat lain. Imunoglobulin ini disebut
juga sebagai M-protein atau paraprotein yang umumnya tersusun dari satu kelas H-chain (baik rantai gama, alfa, mu, delta ataupun epsilon) dan satu jenis L-chain,
yaitu kappa dan lambda. Akibatnya terbentuk imunoglobulin yang homogen (Rose, 2002; Kresno, 2003a). Jenis M-protein tersebut adalah IgG (37% penderita myeloma) dan IgA (27%), kadang-kadang terdapat IgD pada 1,5% kasus dan IgE sebesar 0,1% (Baratawijaya, 2009). Baik pada penderita yang menghasilkan IgG maupun IgA, sebanyak 40% memiliki Bence Jones proteinuria sebagai hasil sekresi sel plasma pada 15 – 20% penderita. Proteinuri tersebut menunjukan adanya monoclonal atau light chain bebas dalam urin. Hal ini merupakan diagnosis pasti multiple myeloma (Berenson, 2008).
10
Gambar 2.4 Bence Jones Protein (Cruse, 1999)
Penyebab terjadinya multiple myeloma belum diketahui dengan pasti, diduga akibat radiasi, infeksi virus, stimulasi antigen berulang kali, dan genetik. Gejala klinik tergantung dari ada tidaknya organ yang menunjukkan kelainan sekunder, misalnya kelainan faal ginjal, saraf, jantung, gangguan hemostasis dan lain-lain (Kresno, 2000). Gejalanya dapat berupa: amiloidosis, nyeri tulang dan penekanan saraf akibat lesi osteolitik, anemia, infeksi (akibat netropenia), perdarahan, gagal ginjal, sindrom hiperviskositas, parestesia atau paraplegia. Kadang pada penderita tidak tampak adanya gejala (Bakta, 2007).
11
sel plasma abnormal dengan inti besar, bizarre, ukuran bervariasi dan sering ada bentukan multinukleus (Bakta, 2007).
Gambar 2.5 Sel plasma normal (Abbas, Lichtman and Pillai, 2007a)
Gambar 2.6 A. Plasmacytoma pada soft tissue; B. Aspirasi sumsum tulang multiple myeloma, sel-sel plasma dan plasmablas menggantikan jaringan
hematopoesis normal (Bernadette and Rodak, 2002)
Dari analisis yang dilakukan oleh Peinert dan kawan-kawan pada 81 sampel sumsum tulang, menunjukkan adanya ekspresi sedang antigen LeY pada sel plasma penderita myeloma sebanyak 52% kasus (Peinert et al, 2010). Normalnya sel T tidak dapat mengenali antigen ini (Westwood et al, 2005).
12
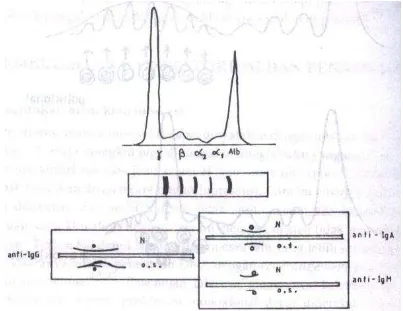
M-protein (1%). Pada multiple myeloma tipe IgA, spike sering terdapat pada daerah globulin beta (Bakta, 2007).
Gambar 2.7 Protein M pada immunoelectrophoresis (Kresno, 2003b)
13
Selain kriteria major juga ada kriteria minor, yaitu: anemia, hiperkalsemia, oostegangguan fungsi ginjal yang dinyatakan dengan peningkatan kadar kreatinin dan karnofsky performance 70%. Terkadang tidak dijumpai adanya protein-M. Keadaan ini termasuk kasus nonsekretorik karena itu diperlukan penentuan monoklonalitas sel plasma dengan mengidentifikasi sIg, khususnya rantai-L monoklonal (Kresno, 2000).
14
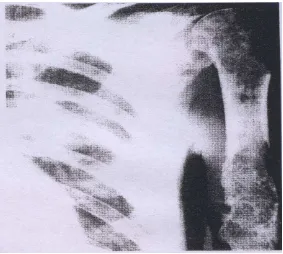
Gambar 2.8 Lesi osteolitik pada os humerus dekstra (Beutler, 2001).
Prognosis penyakit ini sangat bervariasi, sebagian besar ditentukan oleh tingkat penyakit. Durie dan Salmon membuat kriteria klasifikasi tingkat penyakit sebagai berikut (Bakta, 2007):
1 Stadium I, bila memenuhi seluruh kriteria berikut: a. Foto rongent normal atau osteolitik soliter.
b. Kadar Hb > 10 g/dl, kalsium serum 12 mg/dl dan IgG < 5 g/dl atau IgA < 3 g/dl dalam serum atau rantai ringan dalam urine < 4 g/24 jam.
2 Stadium II, bila tidak memenuhi kriteria stadium I atau III. 3 Stadium III, jika memenuhi satu atau lebih kriteria berikut:
15
b. Kadar Hb < 8,5 g/dl, kalsium serum > 12 mg/dl, dan IgG > 7 g/dl atau IgA > 5 g/dl atau light chain dalam urin > 12 g/24 jam.
Klasifikasi tadi memiliki subklasifikasi berdasarkan kadar serum kreatinin, yaitu:
A: bila serum kreatinin < 2 mg/dl B: bila serum kreatinin > 2 mg/dl
Selain berdasarkan klasifikasi di atas, prognosis ditentukan pula oleh kadar 2-microglobulin serum (Braunwald, 2003; Nagura, 2007). Penderita dengan
stadium IA dan kadar 2-microglobulin < 0,004 g/dl (< 4 µg/ml) memiliki harapan hidup 4γ bulan. Harapan hidup pada stadium II dengan kadar 2-microglobulin
16
Tabel 2.4 Klasifikasi multiple myeloma (Braunwald, 2003)
17
memuaskan. Oleh karena itu sekarang dikembangkan cara ketiga, yaitu terapi dengan mempergunakan sistem imun.
2.4 Respon Imun terhadap Tumor
Seperti yang telah disebutkan di atas, antigen tumor dapat menimbulkan respon imun, baik humoral maupun selular. Pada imunitas humoral, sel tumor dapat dihancurkan secara langsung, dengan bantuan komplemen maupun melalui sel efektor ADCC. Cara yang terakhir dilakukan dengan menggunakan Fc receptor-bearing macrophage atau sel NK sebagai mediator dalam
menghancurkan tumor. Kemampuan antibodi untuk mengeliminasi sel tumor sebagian besar dilakukan in vitro dan hanya terdapat sedikit bukti bagi sistem imun humoral dalam melawan tumor (Abbas, Lichtman and Pillai, 2007b).
18
dilisiskan oleh CTLs. Makrofag juga diaktifkan oleh IFN- untuk membunuh sel tumor (Abbas, Lichtman and Pillai, 2007b).
Umumnya tumor tumbuh ketika sistem imun sedang lemah (Male et al, 2006). Berarti pada tumor terdapat mekanisme untuk menghindarkan diri dari imunitas spesifik dan non spesifik. Mekanisme-mekanisme tersebut antara lain: sel tumor tidak mempunyai sel B7 (CD 80) dan CD 86 yang berfungsi sebagai kostimulator, tidak mengekspresikan MHC-I, memacu apoptosis sel Tc, menghasilkan sitokin (TGF- ) yang bersifat imunosupresif dan musin yang menyamarkan antigen serta kehilangan ekspresi antigen yang memicu respons imun (Abbas, Lichtman and Pillai, 2007b; Baratawijaya dan Rengganis, 2009).
19
2.5 Immunotherapy
Immunotherapy adalah pengobatan dengan menginduksi, mempertinggi atau
mensupresi respons imun (Abbas and Licthman, 2006). Terapi tersebut dapat diklasifikasikan menjadi active dan suppressive immunotherapies. Klasifikasi pertama bertujuan mendatangkan atau memperkuat respon imun. Sedangkan yang kedua bertujuan mereduksi, mensupresi secara langsung terhadap respons imun, seperti misalnya pada kasus autoimun atau alergi (Masihi, 2001).
Zat aktif immunotherapy disebut dengan immunomodulators. Beberapa agen yang termasuk dalam immunomodulators adalah cytokines, granulocyte colony-stimulating factor (G-CSF), interferons, imiquimod, fraksi membran selular dari
mikroorganisme bakterial, IL-12, bermacam-macam chemokine, synthetic cytosine phosphate-guanosine (CpG), oligodeoxynucleotides dan glucans. Keuntungan cara ini antara lain: efek samping yang dihasilkan lebih sedikit, sedikit menyebabkan resistensi pada bakteri (Masihi, 2001).
Berikut termasuk dalam Immunotherapy, yaitu: antibodi monoklonal, manipulasi signal kostimulator untuk meningkatkan imunitas, imunotoksin, sitokin, peningkatan aktivitas APC, vaksinasi dengan sel dendritik, immunotherapy aktif dan imunisasi dengan antigen virus serta ACT (Baratawijaya
dan Rengganis, 2009).
20
langsung ke tempat tumor. Namun anti ini juga merusak sel-sel yang normal. Bila dilabel dengan bahan radioaktif dapat pula digunakan untuk mengetahui luas metastasis limfoma dalam tubuh (Baratawijaya dan Rengganis, 2009).
Tabel 2.5 Antibodi monoklonal yang digunakan untuk pengobatan tumor (Baratawijaya dan Rengganis, 2009).
Hanya sedikit sel-sel myeloma yang mengekspresikan CD20 (rituximab). Sedangkan terapi antibodi lain yang potensial terhadap MM adalah alemtuzumab (CamPath-1H). Antibodi tersebut melawan protein permukaan sel CD52 yang umumnya diekspresikan pada limfosit T dan B. Alemtuzumab mengakibatkan lisis sel dan menghambat pertumbuhan sel-sel primer dan ganas melalui berbagai mekanisme termasuk fiksasi complement dan antibody dependent cell mediated cytotoxicity. Akhir-akhir ini, telah diketahui bahwa CD52 diekspresikan pada sel
MM dengan kadar yang bervariasi. Ikatan silang antara reseptor CD52 dengan alemtuzumab dapat menginduksi hambatan pertumbuhan dan efek apoptosis sel-sel myeloma secara langsung (Gasparetto, 2004).
21
dipresentasikan pada sel-sel dendritik sehingga dapat menginduksi respons imun spesifik pada penderita multiple myeloma. Namun, perlu dipertimbangkan pemilihan penderita yang memiliki respons imun cukup untuk melawan antigen. Dapat pula dikombinasi dengan immunotherapy yang lain, seperti: G-CSF atau vaksin keyhole limpet haemocyanin (KLH) (Yi et al, 2002).
Signal kostimulator dapat meningkatkan imunitas tumor sehingga prekursor CTL (CTL-Ps) dapat diaktifkan. Bila signal kostimulator tidak ada, maka CTL-Ps tidak akan berproliferasi menjadi sel efektor CTL. Adanya gen yang menyandi ligand B7 menyebabkan CTL-Ps berdiferensiasi menjadi CTL efektor (Baratawijaya dan Rengganis, 2009).
Peinert dan kawan-kawan telah mengembangkan suatu vektor retrovirus yang dapat mengkode reseptor sel chimeric T. Reseptor tersebut akan mengenali antigen LeY dalam MHC-independent manner dan mengirimkan costimulatory signal untuk mengaktivasi sel T (Peinert et al, 2010). Reseptor ini terdiri dari rantai tunggal antibodi anti-Le(Y) yang dihubungkan dengan daerah cytoplasmic signaling yang dibentuk oleh CD28 dan CD3-zeta (Westwood et al, 2005). Telah
sel-22
sel kanker dapat menjadi sasaran efektif bagi sel T yang mengekspresikan reseptor chimeric baik secara in vitro maupun in vivo pada tikus (Peinert et al, 2010).
Pada imunotoksin, mAb yang digunakan bersama-sama toksin terhadap TAA akan dapat mencegah proses selular. Sementara bila bersama dengan radioisotop akan membantu membunuh DNA dan melepas partikel dengan energi yang tinggi. Cara tersebut kurang berhasil karena memerlukan dosis yang tinggi dan toksik bagi sumsum tulang (Baratawijaya dan Rengganis, 2009).
Respon imun terhadap tumor dapat ditingkatkan oleh sitokin. Jenis-jenis sitokin yang dapat digunakan sebagai tumor ialah: IFN-α, IFN- , IFN- , IL-2, IL-4, IL-6, IL-12, GM-CSF dan TNF. Walaupun demikian, terapi dengan cara ini jarang dilakukan karena sangat sulit untuk mengetahui letak intervensinya dengan tepat (Baratawijaya dan Rengganis, 2009). Pada MM, interferon dapat memperpanjang harapan hidup penderita.
Aktivitas APC yang meningkat akan memodulasi imunitas tumor. Sel dendritik tikus yang dibiakkan dengan GM-CSF dan fragmen tumor dapat mengaktifkan sel Th dan CTL spesifik untuk antigen tumor. Beberapa ajuvan meningkatkan aktivasi makrofag, molekul MHC II dan kostimulator B7 serta ekspresi berbagai sitokin. Makrofag yang aktif merupakan aktivator Th. Akibatnya respon imun baik selular maupun humoral meningkat (Baratawijaya dan Rengganis, 2009).
23
yang telah aktif (memiliki respons anti tumor spesifik) kemudian dikembalikan ke tubuh pasien. Dalam tubuh penderita, sel ini akan mempresentasikan antigen pada effector lymphocytes (CD4+ T cells, CD8+ T cells, dan sel-sel dendritik yang
khusus serta sel B). Hal ini akan menginisiasi repons cytotoxic melawan antigen dan apa pun yang mempresentasikan antigen ini sehingga dapat digunakan dalam immunotherapy kanker. Antigen tumor yang dipresentasikan pada sel-sel dendritik
merupakan target sistem imun (Overes, 2009). Vaksin sel dendritik ini telah digunakan pada penderita MM dengan menggunakan Id sebagai antigen sasaran (Gasparetto, 2004)
Gambar 2.10 Vaksin dari sel dendritik yang diberi antigen tumor (Abbas, Lichtman and Pillai, 2007b)
24
Telah dikembangkan teknologi yang melibatkan transfeksi DC dengan tumor yang berasal dari RNA. Transfeksi ini mampu menimbulkan aktivitas anti tumor yang sesuai. Telah ditemukan bahwa DC yang aktif dapat menimbulkan CTLS in vitro ketika diinfus dengan MM RNA (Gasparetto, 2004). CTLs tersebut mengandung sel T CD4+ dan CD8+ (Wen, 2002). Cytotoxicity terhadap sel target adalah MHC 1 dan sedikit MHC 2 serta tergantung terutama pada perforin-mediated pathway. CTLs terutama mensekresi IF- dan TNF α pada stimulasi
antigenik yang mengindikasikan sel T subset tipe 1. Telah ditemukan bahwa tumor cell lysate-primed CTLs hanya membunuh sel myeloma, bukan autologous
lymphocytes. Penemuan ini memberikan dasar immunotherapy MM yang rasional
(Wen, 2002).
25
Antigen tumor yang dipresentasikan pada sel T tanpa dibantu oleh molekul kostimulator akan mengakibatkan terjadinya anergi. Untuk mencegah anergi sel T digunakan immunotherapy aktif, yaitu dengan menginfuskan sitokin. Sel T dan NK akan diaktifkan langsung oleh IL-2, namun IL-2 mempunyai efek samping yang berat, misalnya: kebocoran kapiler, edem dan hipotensi. Selain itu, dapat pula diberikan IFN sistemik karena memiliki efek anti-proliferasi dan meningkatkan ekspresi MHC-1. Peningkatan ekspresi ini terutama oleh IFN-α maupun IFN- (Baratawijaya dan Rengganis, β009).
Terapi juga dapat dilakukan dengan melakukan imunisasi antigen virus. Hal tersebut didasarkan karena beberapa jenis tumor disebabkan pula oleh virus onkogenik. Vaksinasi sudah dapat dilakukan pada Burkitt lymphoma dan kanker cervix. Vaksinasi tersebut bertujuan untuk memacu sel Tc efektor sehingga dapat
mencegah terjadinya kanker (Baratawijaya dan Rengganis, 2009).
26
Gambar 2.13 Vaksinasi dengan sel tumor yang mengekspresikan GM-CSF (Abbas, Lichtman and Pillai, 2007b)
Baik antibodi maupun sel T mampu mengendalikan pertumbuhan sel myeloma melalui pengenalan spesifik idiotypic portion (Id) myeloma-specific immunoglobulin protein (MM-Ig). Vaksinasi dengan Id conjugates dapat memicu
respons Id-specific humoral dan sel T pada beberapa penderita bahkan setelah terapi dengan dosis tinggi dan transplantasi autologous (Gasparetto, 2004).
Protein Id yang disekresi sel plasma myeloma, spesifik untuk tumor tapi merupakan antigen yang lemah. Immunotherapy berdasarkan Id pada penderita myeloma menunjukkan hasil yang mengecewakan (Gasparetto, 2004).
Berbagai TAA yang telah diidentifikasi dalam sel myeloma dapat menjadi target yang selektif bagi sistem imun (Houet and Veelken, 2006; Rosenblatt and Avigan, 2008). Keuntungan cara ini adalah dapat mempresentasikan antigen yang spesifik dan potensial terhadap sel efektor. Disfungsi sel efektor dan peningkatan jumlah sel T regulatory membatasi efek immunotherapy. Strategi untuk meningkatkan immunotherapy pada penyakit ini mencakup: mengurangi jumlah sel T regulatory, mengkombinasikan immunotherapy aktif dan pasif, penggunaan cytokine adjuvants, serta pemakaian immunotherapy bersamaan dengan
27
Imunisasi stem cell donor dengan antigen myeloma dapat meningkatkan efek dan hasil allogeneic stem cell transplantation. Immunotherapy aktif sedang diteliti untuk digunakan sebagai pilihan pengobatan multiple myeloma. Imunisasi terhadap clonal immunoglobulin myeloma memicu sistem imun pada tikus (Houet and Veelken, 2006).
Obat-obat imunomodulator (IMiDS), yaitu analog thalidomide memiliki sifat pleiotropik anti myeloma, antara lain efek immune modulation, anti-angiogenic, anti inflamasi, dan anti proliferasi. Berdasarkan data in vitro, terlihat bahwa efek anti proliferasi dan downregulation cytokine adalah anti MM yang paling penting. Dosis thalidomide yang rendah telah dapat menimbulkan efek tersebut (Gasparetto, 2004). Walaupun dikatakan bahwa efek costimulatory obat terhadap sel T dan NK itu sangat unik dan penting dalam menciptakan aktivitas imun anti MM namun belum dibuktikan secara in vivo (Quach H et al, 2010). Sayangnya, thalidomide sering meimbulkan efek samping seperti: neuropati perifer, thromboembolic, sedasi, konstipasi, kelainan congenital, neutropenia, hipotiroidisme, kemerahan dan bradikardi (Gasparetto, 2004).
28
monocyte chemotactic protein-1, TNF-α dan IF- serta mungkin memperbanyak rituximab-associated antibody-dependent cellular cytotoxicity (Reddy et al, 2008).
Bortezomid (velcade, juga dikenal sebagai PS-341 dan MLN341) adalah inhibitor proteasome yang reversibel. Seperti yang telah diketahui, proteasome merupakan suatu kompleks protein besar yang mendegradasi ubiquinated protein. Disregulasi degradasi protein memiliki efek yang besar terhadap pertumbuhan tumor dan mengakibatkan apoptosis sel. Bortezomid bersifat cytotoxic terhadap sel kanker secara in vitro sedangkan secara in vivo, menyebabkan pertumbuhan tumor melambat pada hewan coba dengan MM. Pada beberapa penelitian, respons penderita bervariasi antara 30-50% (Gasparetto, 2004).
Sementara Adoptive Cell Therapy (ACT) menggunakan T cell-based cytotoxic untuk melawan kanker. Sel T yang telah memiliki reaktivitas alami pada
sel kanker dibuat lebih efektif secara in vitro dan kemudian ditransfer ke dalam tubuh penderita. Misalnya, sel T yang secara alami memiliki reaktivitas pada penderita kanker, ditemukan menginfiltrasi tumor. Tumor-infiltrating lymphocytes (TIL) dapat dibuat lebih efektif secara invitro menggunakan konsentrasi IL-2 yang tinggi, anti-CD3 dan allo-reactive feeders. Sel tersebut dapat ditransfer kembali ke tubuh penderita dengan pemberian IL-2 untuk memperkuat aktivitasnya. Beberapa tumor mengecil sampai tidak terdeteksi (Khattar, Chen, Stepkowski, 2009; Motohashi and Nakayama, 2009).
29
Gambar 2.14 Immunotherapy dengan Adoptive Cell Therapy (Abbas, Lichtman and Pillai, 2007b)
30 SIMPULAN
Pertumbuhan sel diatur oleh protoonkogen (growth promoting oncogenes) dan tumor suppressor gene. Aktivitas protoonkogen yang berlebihan ataupun mutasi suppressor gene akan mengakibatkan sel bertransformasi menjadi ganas.
Kanker mengekspresikan antigen imunogenik yang dapat dikenali oleh sistem imun sehingga dapat dihancurkan secara spesifik. Antigen tumor dapat dibagi menjadi: tumor specific antigen (TSA) dan tumor associated antigen (TAA).
Multiple myeloma merupakan proliferasi abnormal sel plasma ganas yang
menghasilkan monoclonal immunoglobulin dan menginvasi serta menghancurkan jaringan tulang sekitar.
Kondisi ini diduga akibat radiasi, infeksi virus, stimulasi antigen berulang kali, dan genetik. Gejala klinik tergantung dari ada tidaknya organ yang menunjukkan kelainan sekunder, misalnya kelainan faal ginjal, saraf, jantung, gangguan hemostasis dan lain-lain.
Untuk mendiagnosis penyakit ini, perlu dilakukan pemeriksaan: darah lengkap (CBC) dengan platelets, pengecatan darah perifer, ESR, BUN, kreatinin, kalsium, asam urat dan laktat dehidrogenase (LDH), elektroforesis protein serum dan urin, x-rays (skeletal survey), pemeriksaan sumsum tulang.
31
Prognosis penyakit ini sangat ditentukan oleh tingkat penyakit dan kadar 2-microglobulin serum sangat menentukan prognosis penderita.
Pengobatan untuk penyakit tersebut, yaitu dengan: terapi spesifik, suportif dan dengan imunomodulator (seperti interferon). Keberhasilan kedua terapi yang pertama kurang memuaskan karena itu sekarang sedang dikembangkan cara ketiga, yaitu terapi dengan mempergunakan sistem imun (immunotherapy).
Antigen tumor dapat menimbulkan respon imun, baik humoral maupun selular. Pada respon pertama, sel tumor dapat dihancurkan secara langsung, dengan bantuan komplemen maupun melalui sel efektor ADCC. Sedangkan pada imunitas seluler, sel T memegang peranan penting. Sekarang ini, immunotherapy lebih banyak dibuat berdasarkan respon sel T. Mekanisme utama sistem ini adalah penghancuran sel tumor oleh CD8+ atau CTLs.
Umumnya pertumbuhan tumor terjadi ketika sistem imun sedang lemah karena adanya mekanisme tumor untuk menghindarkan diri dari sistem imun.
Immunotherapy adalah pengobatan dengan menginduksi, mempertinggi atau
mensupresi respons imun yang diklasifikasikan menjadi active dan suppressive immunotherapies (immunotherapy pasif). Keuntungan pengobatan cara ini antara lain: efek samping yang dihasilkan lebih sedikit, sedikit menyebabkan resistensi pada bakteri
32
Pada MM, yang menjadi pilihan terapi antara lain: alemtuzumab (CamPath-1H), reseptor sel chimeric T yang akan mengenali antigen LeY dan mengaktivasi sel T, interferon, vaksin dengan sel dendritik baik matur maupun imatur, imunisasi stem cell donor dengan antigen myeloma, obat-obat immunomodulator. Immunotherapy aktif sedang diteliti untuk digunakan sebagai pilihan pengobatan
multiple myeloma.
33
DAFTAR PUSTAKA
Abbas, AK., Lichtman, AH., Pillai, S. 2007a. Cellular and Molecular Immunology. 6th. Ed. Philadelphia: Saunders Elsevier. p. 55. Abbas, AK., Lichtman, AH., Pillai, S. 2007b. Cellular and Molecular
Immunology. 6th. Ed. Philadelphia: Saunders Elsevier. p. 397-417.
Abbas, AK., Lichtman, AH. 2006. Basic Immunology Function and Disorders of The Immune System. 2nd. Ed. Philadelphia: Saunders Elsevier. p. 277. Bakta, IM. 2007. Hematologi Klinik Ringkas. 1st. Ed. Jakarta: EGC. p. 220-9. Baratawijaya, KG., Rengganis, I. 2009. Imunologi Dasar. 8th. Ed. Jakarta: Balai
Penerbit FKUI. p. 451-476.
Berenson, MD. 2008. Multiple Myeloma. Available from:
http://www.merck.com/mmpe/sec11/ch144/ch144e.html. Access 20 Feb 2010.
Bernadette, F., Rodak. 2002. Hematology Clinical Principles and Applications. 2nd. Ed. Philadelphia: Saunders. p. 502-39.
Beutler, E., et al. 2001. Williams Hematology. 6th. Ed. New York: Mc Graw Hill. p. 1279-98.
Braunwald, E., et al. 2003. Harrison`s Principles of Internal Medicine. 15th. Ed. Boston: Mc. Graw Hill. p. 727-32.
Cruse, JM., Lewis, RE. 1999. Atlas of Immunology. London: CRC Press. p. 322-3.
Dudley, ME., et al. 2002. Cancer regression and autoimmunity in patients after clonal repopulation with antitumor lymphocytes. Science, 298(5594):850– 854.
Fischbach, FT., Dunning, MB. 2004. A Manual of Laboratory and Diagnostic Test. 7th. Ed. Philadelphia: Lippincott Wiliams and Wilkins. p. 533. Gasparetto, C. 2004. Stem Cell Transplantation for Multiple Myeloma. Cancer
Control, 11(2).
34
Nairn, R., Helbert, M. 2007. Immunology for Medical Students. 2nd. Ed. Philadelphia: Mosby Elsevier. p. 279-87.
Henry, JB. 2001. Clinical Diagnosis and Management by Laboratory Methods. 12th. Ed. Philadelphia: WB. Saunders Company. p. 887-91.
Houet, L., Veelken, H. 2006. Active immunotherapy of multiple myeloma. Eur J Cancer, Jul;42(11):1653-60.
Khattar, M., Chen, W., Stepkowski, SM. 2009. Expanding and converting
regulatory T cells: a horizon for immunotherapy. Archivum Immunologiae et Therapiae Experimentalis, 57(3):199.
Kresno, SB. 2002. Keganasan Sistem Imun. In: Kresno, SB. Imunologi: Diagnosis dan Prosedur Laboratorium. 3th. Ed. Jakarta: FKUI. p. 141-54.
Kresno, SB. 2003a. Imunologi: Diagnosis dan Prosedur Laboratorium. 4th. Ed. Jakarta: FKUI. p. 208-65.
Kresno, SB. 2003b. Imunologi: Diagnosis dan Prosedur Laboratorium. 4th. Ed. Jakarta: FKUI. p. 407-11
Male, D., et al. 2006. Immunology. 7th. Ed. Canada: Elsevier. p. 401-19. Masihi, KN. 2001. Fighting infection using immunomodulatory agents. Expert
Opinion on Biological Therapy, July;1(4): 641-653.
Motohashi, S., Nakayama, T. 2009. Natural killer T cell-mediated immunotherapy for malignant diseases. Frontiers in Bioscience,1:108–116.
Nagura, E. 2007. Prognositic Factor in Multiple Myeloma. Nippon Rinsho, Dec;65(12):2351-6.
Overes, IM. 2009. Efficient Activation of LRH-1-specific CD8+ T-cell Responses From Transplanted Leukemia Patients by Stimulation With P2X5 mRNA-electroporated Dendritic Cells. Journal of Immunotherapy, 32(6):539. Peakman, M., Vergani, D. 2006. Basic Clinical Immunology. 6th. Ed.
Philadelphia: Churchill Livingston. p. 294-7.
35
Quach, H., et al. 2010. Mechanism of action of immunomodulatory drugs (IMiDS)in multiple myeloma. Leukemia, Jan;24(1):22-32.
Reddy, N., et al. 2008. Immunomodulatory drugs stimulate natural killer-cell function, alter cytokine production by dendritic cells, and inhibit
angiogenesis enhancing the anti-tumour activity of rituximab in vivo. Br J Haematol, Jan;140(1):36-45.
Rose, NR., et al. 2002. Manual of Clinical Laboratory Immunology. 6th. Ed. Washington: ASM Press. p. 66-94.
Rosenblatt, J., Avigan, D. 2008. Cellular Immunotherapy for Multiple Myeloma. Best Pract Res Clin Haematol, Sep;21(3):559-77.
Subowo. 2009. Imunobiologi. 2nd. Ed. Jakarta: Sagung Seto. p. 272-85.
Wahab, AS., Julia, M. 2002. Sistem Imun. In: Wahab, AS., Julia, M. Sistem Imun, Imunisasi, & Penyakit Imun. 1st. Ed. Jakarta: Penerbit Widya Medika. p. 1-37.
Wen, YJ., et al. 2002. Tumor lysate-specific cytotoxic T lymphocytes in multiple myeloma: promising effector cells for immunotherapy. Blood,
May;99(9):3280-5.
Westwood, JA., et al. 2005. Adoptive transfer of T cell modified with a
humanized chimeric receptor gene inhibits growth of Lewis-Y-expressing tumors in mice. Proc Natl Acad Sci U S A, Dec;102(52):19051-6.