TESIS
PENINGKATAN KADAR
S100β
DAN
KADAR INTERLEUKIN-6 SERUM BERKORELASI DENGAN
TINGKAT KEPARAHAN DELIRIUM PADA PASIEN GERIATRI
YANG DIRAWAT DI RSUP SANGLAH
YOSEF SAMON SUGI
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
TESIS
PENINGKATAN
KADAR S100β DAN
KADAR INTERLEUKIN-6 SERUM BERKORELASI DENGAN
TINGKAT KEPARAHAN DELIRIUM
PADA PASIEN GERIATRI YANG DIRAWAT
DI RSUP SANGLAH
YOSEF SAMON SUGI NIM 1014048107
PROGRAM MAGISTER
PROGRAM STUDI ILMU BIOMEDIK
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
DENPASAR
PENINGKATAN
KADAR S100β DAN
KADAR INTERLEUKIN-6 SERUM BERKORELASI DENGAN
TINGKAT KEPARAHAN DELIRIUM
PADA PASIEN GERIATRI YANG DIRAWAT
DI RSUP SANGLAH
Tesis untuk Memperoleh Gelar Magister
pada Program Magister, Program Studi Ilmu Biomedik,
Program Pascasarjana Universitas Udayana
YOSEF SAMON SUGI NIM 1014048107
PROGRAM MAGISTER
PROGRAM STUDI ILMU BIOMEDIK
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
DENPASAR
Lembar Pengesahan
TESIS INI TELAH DISETUJUI
TANGGAL……….
Pembimbing I, Pembimbing II,
Dr. dr. R.A.Tuty Kuswardhani,SpPD-KGER.MARS dr. I.G.P. Suka Aryana, SpPD-KGER NIP. 195911041989032003 NIP. 197103292006041001
Mengetahui
Ketua Program Studi Ilmu Biomedik Direktur
Program Pascasarjana Program Pascasarjana
Universitas Udayana, Universitas Udayana,
Dr.dr. Gde Ngurah Indraguna Pinatih, M.SC, Prof.Dr.dr. A.A Raka Sudewi, Sp.S(K) SpGK
Tesis Ini Telah Diuji pada Tanggal………….
Panitia Penguji Tesis Berdasarkan SK Rektor Universitas Udayana, No…………, Tanggal……….
Ketua : Dr. dr. R.A.Tuty Kuswardhani,SpPD-KGER.MARS
Anggota :
1. dr. I Gusti Putu Suka Aryana, Sp.PD-KGER 2. dr. Nyoman Astika, Sp.PD-KGER
UCAPAN TERIMA KASIH
Pertama-tama perkenankanlah penulis memanjatkan puji syukur kehadirat Tuhan Yang
Maha Esa, karena hanya atas karunia dan izin Nya tesis yang berjudul “Peningkatan Kadar
S100β dan Kadar Interleukin-6 Serum Berkorelasi dengan Tingkat Keparahan Delirium
pada Pasien Geriatri yang Dirawat di RSUP Sanglah” dapat diselesaikan dalam rangka
menyelesaikan pendidikan di Program Pascasarjana pada Program Studi Ilmu Kedokteran
Biomedik Universitas Udayana.
Tulisan ini disusun untuk memenuhi persyaratan tugas akhir studi yang dijalani Penulis
untuk memperoleh Gelar Magister pada Program Magister Program Studi Ilmu Kedokteran
Biomedik, Program Pascasarjana Universitas Udayana.
Pada kesempatan ini perkenankanlah penulis menyampaikan rasa hormat, rasa kagum dan
penghargaan serta terima kasih yang sebesar-besarnya kepada :
1. Dr. dr. R.A. Tuty Kuswardhani, SpPD-KGER.MARS selaku Pembimbing I, yang telah
memberikan banyak sekali masukan dan bimbingan serta semangat kepada penulis selama
penyusunan tesis ini.
2. dr. I Gusti Putu Suka Aryana, SpPD-KGER selaku pembimbing II, yang telah banyak
memberikan bimbingan, banyak sumber masukan dan dorongan serta semangat kepada
penulis selama penyusunan tesis ini.
3. Bapak Rektor Universitas Udayana saat itu, Prof. Dr. dr. I Made Bakta, Sp.PD-KHOM yang
telah memberikan kesempatan kepada penulis untuk mengikuti pendidikan Magister pada
Program Studi Ilmu Kedokteran Biomedik Universitas Udayana.
telah memberikan kesempatan kepada penulis untuk mengikuti pendidikan Magister pada
Program Studi Ilmu Kedokteran Biomedik Universitas Udayana.
5. Dekan Fakultas Kedokteran Universitas Udayana, Prof. Dr. dr. Putu Astawa, Sp.OT. M.Kes
yang telah memberikan kesempatan kepada penulis untuk mengikuti pendidikan Magister
pada Program Studi Ilmu Kedokteran Biomedik Universitas Udayana
6. Ibu Direktur Program Pascasarjana Universitas Udayana, Prof. Dr. dr. Anak Agung Raka
Sudewi, Sp.S(K) yang telah memberikan kesempatan kepada penulis untuk mengikuti
pendidikan Magister pada Program Studi Ilmu Kedokteran Biomedik Universitas Udayana.
7. Dr.dr. Gde Ngurah Indraguna Pinatih, M.SC, SpGK selaku ketua Program Studi Ilmu Kedokteran
Biomedik Universitas Udayana yang telah memberikan kesempatan kepada penulis untuk
mengikuti pendidikan Magister pada Program Studi Ilmu Kedokteran Biomedik Universitas
Udayana.
8. Dr. dr. Ketut Suega, SpPD-KHOM selaku Kepala Bagian/SMF Ilmu Penyakit Dalam FK
Universitas Udayana, atas kesempatan kepada penulis untuk mengikuti pendidikan Ilmu
Penyakit Dalam Fakultas Kedokteran Universitas Udayana.
9. Kepala Program Studi Ilmu Penyakit Dalam, Prof. Dr. dr. IDN. Wibawa SpPD KGEH atas
kesempatan kepada penulis untuk mengikuti pendidikan Ilmu Penyakit Dalam Fakultas
Kedokteran Universitas Udayana.
10.dr. Nyoman Astika, SpPD-KGER, Dr. dr. Wayan Sudhana, SpPD-KGH, dan Dr. dr. Desak
Made Wihandani, M.Kes, selaku penguji yang telah banyak memberikan bimbingan dan
masukan kepada penulis selama penyusunan tesis ini.
11.Prof. Dr. dr Tjok Raka Putra, SpPD-KR, sebagai mantan Kepala Bagian /SMF Ilmu Penyakit
mantan Ketua Program Studi Ilmu Penyakit Dalam FK Unud/ RSUP Sanglah yang pada
masanya telah memberi kesempatan kepada penulis untuk mengikuti pendidikan spesialisasi.
12.Para dosen pengajar dan rekan-rekan residen Bagian/SMF Ilmu Penyakit Dalam FK
UNUD/RSUP Sanglah yang tidak dapat disebutkan satu persatu, yang selalu memberikan
doa dan dorongan.
13.Ayahanda Drs. Yoseph Sugi, MSc beserta ibunda Petronela Neno atas doa, dukungan dan
pengertiannya selama menempuh pendidikan
14.Kakak dan adik, Fransiska V. Sugi, Antonius R.B. Ola, Maria D.N Sugi, Felix Sugi dan
Gavriel A. Sugi atas doa, dukungan dan pengertiannya selama menempuh pendidikan.
15.dr. Petrus Irianto, dr. Anselmus Ake, dr. Yohanes SP, teman-teman “IRB 2010” dan
teman-teman lainnya, terimakasih atas motivasi dan persahabatan yang kalian berikan selama ini.
Penulis juga sangat berterima kasih kepada semua pihak yang telah ikut membantu dalam
pelaksanaan dan penyelesaian tesis ini, semoga Ida Sang Hyang Widhi Wasa, Tuhan Yang
Maha Esa, senantiasa melimpahkan berkat dan rahmat-Nya kepada mereka semua.
Akhir kata, tiada gading yang tidak retak, untuk itu penulis berharap dengan segala
kekurangan dalam tugas akhir ini dapat memberikan manfaat bagi penulis pribadi, bagi program
pendidikan Magister Program Studi Ilmu Biomedik, Program Pascasarjana Universitas Udayana,
serta pihak-pihak lain yang berkepentingan.
Denpasar, April 2016
Penulis,
ABSTRAK
PENINGKATAN KADAR S100β DAN
KADAR INTERLEUKIN-6 SERUM BERKORELASI DENGAN TINGKAT KEPARAHAN DELIRIUM PADA PASIEN GERIATRI
YANG DIRAWAT DI RSUP SANGLAH
Delirium adalah sebuah sindrom neuropsikiatrik yang kompleks dengan onset yang akut dan berfluktuasi. Pasien-pasien yang mengalami delirium, ketika dibandingkan dengan pasien-pasien yang tidak mengalami delirium, menjalani perawatan yang lebih lama. S100β merupakan
calcium-binding protein yang disekresi oleh astrosit dibawah pengaruh kondisi metabolik stres dan merupakan biomarker yang menandakan kerusakan dari sistem saraf pusat. Sedangkan peningkatan kadar IL-6 (penanda neuroinflamasi) berhubungan dengan risiko terjadinya delirium. Penelitian ini bertujuan untuk mengetahui adanya korelasi antara kadar S100β dan kadar interleukin-6 serum dengan tingkat keparahan delirium pada pasien geriatri.
Rancangan penelitian ini merupakan penelitian potong lintanganalitik untuk mengetahui korelasi antara kadar S100β serum dan kadar interleukin-6 serum dengan tingkat keparahan delirium.Tingkat keparahan delirium diukur menggunakan kuesioner. Setiap subyek penelitian akan dilakukan pemeriksaan kadar S100β dan kadar IL-6 serum dengan menggunakan metode ELISA.
Penelitian ini melibatkan 72 subyek penelitian, laki-laki 38 (52,8%) dan perempuan 34 (47,25%). Rerata usia subyek adalah 68 ± 6,96. Median S100B 5520 pg/ml (950,87-7741,89 pg/ml). Median IL-6 86,19 pg/ml (1,03-376,80 pg/ml). Median MDAS 17 (13-24). Tidak didapatkan korelasi antara kadar S100B serum dengan tingkat keparahan delirium (r = -0,038, p = 0,752). Tetapi, pada penelitian ini didapatkan korelasi antara kadar IL-6 dan Charlson’s age -comorbidity index dengan tingkat keparahan delirium (r = 0.421, p = 0.000; r = 0,483, p = 0,000,).
Pada penelitian ini tidak didapatkan korelasi antara kadar S100B serum dengan tingkat keparahan delirium, tetapi didapatkan korelasi antara kadar IL-6 dan skor CACI dengan tingkat keparahan delirium.
ABSTRACT
INCREASING LEVELS OF S100β AND INTERLEUKIN-6 SERUM CORRELATE WITH DELIRIUM SEVERITY IN GERIATRIC PATIENTS
THAT ADMITTED IN SANGLAH HOSPITAL
Delirium is a complex neuropsychiatric syndrome with acute onset and fluctuating. Patients who experienced delirium, when compared with patients who did not experience delirium, have longer hospital stay. S100β is a calcium-binding protein secreted by astrocytes under the influence of metabolic stress conditions and a biomarker that indicates damage of the central nervous system. While increased levels of IL-6 (a marker of neuroinflamasi) associated with risk of delirium. Aim of this study is to investigate the correlation between levels of S100β and levels of interleukin-6 with the severity of delirium in elderly patients.
The study design was cross-sectional analytical study on the correlation between levels of S100β and levels of interleukin-6 with severity of delirium. Delirium severity was measured using a Memorial Delirium Assesment Scale (MDAS) questionnaire. Levels of S100β and IL-6 will be measured using the ELISA.
The study involved 72 study subjects, 38 males (52.8%) and 34 women (47.25%). The mean age of subjects was 68 ± 6.96. Median S100B 5520 pg / ml (950.87 to 7741.89 pg / ml). Median IL-6 63.58 pg / ml (1.03 to 376.80 pg / ml). Median MDAS 17 (13-24). In this study, there is no correlation between levels of S100B with severity of delirium (r = -0.038, p = 0.752). However, there is significant correlation between levels of IL-6 and Charlson's age-comorbidity index with the severity of delirium (r = 0.421, p = 0.000; r = 0,483, p = 0,000).
In this study, there is no correlation between levels of S100B with the severity of delirium, but levels of IL-6 and scores of CACI have correlation with the severity of delirium.
DAFTAR ISI
Halaman
SAMPUL DALAM ...i
PRASYARAT GELAR ...ii
LEMBAR PERSETUJUAN ... iii
PENETAPAN PANITIA PENGUJI ... iv
UCAPAN TERIMAKASIH ... v
ABSTRAK ... ix
ABSTRACT ... x
DAFTAR ISI ... xi
DAFTAR TABEL ... xv
DAFTAR GAMBAR ... xvi
DAFTAR SINGKATAN ... xvii
DAFTAR LAMPIRAN ……… ... xix
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 3
1.3 Tujuan Penelitian ... 3
1.4 Manfaat Penelitian ... 3
BAB II KAJIAN PUSTAKA ... 5
2.1.1 Definisi Delirium ... 5
2.1.2 Epidemiologi ... 5 2.1.3 Etiologi 6 2.1.4 Patogenesis ... 8
2.1.5 Gambaran Klinis ... 9
2.1.6 Diagnosis... 14
2.2 Peranan Neuroinflamasi pada Delirium ... 17
2.2.1 Kondisi Klinis dengan Reaksi Inflamasi Sistemik yang Mencetuskan terjadinya delirium ... 17
2.2.2 Efek Inflamasi Sistemik Akut terhadap Otak ... 19
2.2.2.1 Dari Proses Inflamasi Sistemik menjadi Neuroinflamasi 19
2.2.2.2 Kerusakan Sawar Darah Otak ... 20
2.2.2.3 Respon Sistem Saraf Pusat yang Diperantarai oleh Molekul-Molekul dalam Sirkulasi Sistemik ... 21
2.2.2.4 Inflamasi Sistemik Akut dan Disfungsi Neurokognisi .... 22
2.3 Peranan Proses Penuaan pada Delirium………. 25
2.4 Biomarker Delirium ... 26
2.4.1 S100 Calcium Binding Protein B (S100β) ... 29
2.4.2 Interleukin-6 ... 30
2.5 Instrumen Diagnosis Delirium ... 30
2.5.1 Confusion Assesment Scale (CAM) ... 31
BAB III KERANGKA BERPIKIR, KONSEP DAN HIPOTESIS PENELITIAN .... 35
3.1 Kerangka Berpikir ... 35
3.2 Konsep Penelitian ... 37
3.3 Hipotesis ... 37
BAB IV METODE PENELITIAN ... 38
4.1 Rancangan Penelitian ... 38
4.2 Lokasi dan Waktu Penelitian ... 38
4.3 Ruang Lingkup Penelitian ... 38
4.4 Penentuan Sumber Data Penelitian ... 38
4.5 Sampel dan Besar Sampel ... 39
4.6 Variabel Penelitian ... 40
4.7 Definisi Operasional Variabel ... 40
4.8 Alat dan Bahan Penelitian ... 41
4.9 Prosedur Penelitian ... 42
4.10 Alur Penelitian ... 43
4.11 Analisis Data ... 43
BAB V HASIL DAN PEMBAHASAN ... 45
5.1 Karakteristik Subyek Penelitian ... 45
5.2 Hubungan antara Kadar S100B dengan Tingkat Keparahan Delirium . 47 5.3 Hubungan antara Kadar IL-6 dengan Tingkat Keparahan Delirium ... 51
Keparahan Delirium ... 54
5.5 Keterbatasan Penelitian ... 57
BAB VI SIMPULAN DAN SARAN ... 58
6.1 Simpulan ... 58
6.2 Saran ... 58
DAFTAR PUSTAKA ... 59
DAFTAR TABEL
Halaman
2.1 Beberapa Instrumen Klinis untuk Diagnosis Delirium... 24
5.1 Karakteristik Subyek Penelitian ... 47
5.2 Hasil Uji Korelasi antara Kadar S100B, Kadar IL-6 dan Charlson’s Age Comorbidity Index
dengan Tingkat Keparahn Delirium ... 48
DAFTAR GAMBAR
Halaman
2.1 Model Multifaktorial dari Delirium ... 8
2.2 Teori-teori Terjadinya Delirium ... 9
2.3 Pengenalan dan Propagasi dari Rangsangan Imun Perifer pada SSP .... 22
3.1 Kerangka Berpikir ... 34
3.2 Konsep Penelitian ... 35
4.1 Alur Penelitian ... 41
5.1 Korelasi antara kadar S100B dengan Tingkat Keparahan Delirium…... 48
5.2 Grafik Perbandingan rerata kadar S100B pada kelompok delirium ringan,
sedang dan berat………... 51
5.3 Korelasi antara kadar IL-6 dengan Tingkat Keparahan Delirium……… 52
5.4 Grafik Perbandingan rerata kadar IL-6 pada kelompok delirium
ringan, sedang dan berat……… ... 54
5.5 Korelasi antara CACI dengan Tingkat Keparahan Delirium ... 55
5.6 Grafik Perbandingan rerata skor CACI pada kelompok delirium
DAFTAR SINGKATAN
Apo : Apolipoprotein
AMTS : Abbreviated Mental Test Score
BDNF : Brain-derived Growth Factor
CACI : Charlson’s Age-Comorbidity Index
CAM : Confusion Assesment Scale
CD : Class of Differentiation
CRP : C-reactive protein
DOSS : Delirium Observational Screening Scale
DRS : Delirium Rating Scale
DSM : Diagnostic and Statistic Manual
EEG : Elektroensefalografi
FDA : Food and Drug Asociation
GABA : Gamma Aminobutyric Acid
GAR : Global Attentiveness Rating
HELP : Hospital Elder Life Program
MDAS : Memorial Delirium Assesment Scale
MMSE : Mini Mental Scale Examination
MRI : Magneting Resonance Imaging
NICE : National Institute for Health and Care
Excellence
NSE : Neuro-specific Enolase
ROS : Reactive Oxygen Species
S100 Calcium Binding Protein B : S100β
SAA : Serum Aktivitas Antikolinergik
SN : Substantia Nigra
SSP : Sistem Saraf Pusat
TLR : Toll-like Receptor
DAFTAR LAMPIRAN
Lampiran 1. Ethical Clearance……… 62
Lampiran 2. Informed Consent………... 64
Lampiran 3. Formulir Persetujuan….………..…... 66
Lampiran 4. Rencana Jadwal Penelitian ……….. 67
Lampiran 5. Anggaran Biaya Penelituan ……… 68
Lampiran 6. Formulir Pengumpulan Data……….. 69
Lampiran 7. Prosedur Pemeriksaan S100B Serum ……….. 77
Lampiran 8. Prosedur Pemeriksaan IL-6 Serum……….. 78
1 B A B I
PENDAHULUAN
1.1Latar belakang
Delirium yang dikenal juga dengan sebutan acute confusional state adalah
sebuah sindrom neuropsikiatrik yang kompleks dengan onset yang akut dan
berfluktuasi. Sindrom ini mempengaruhi kesadaran dan fungsi kognitif yang
mungkin diikuti oleh peningkatan aktivitas psikomotor. Selain itu delirium juga
mempengaruhi atensi dan pada beberapa pasien ada yang mengalami gangguan
depresi (Mittal dkk, 2011).
Pada penelitian yang terbaru di Inggris, prevalensi delirium sebesar 20% pada
pasien yang dirawat di rumah sakit. Beberapa penelitian menunjukkan sekitar
14%-24% pasien usia lanjut dirawat di rumah sakit karena delirium dan delirium sendiri
terjadi pada 50% pasien usia lanjut yang dirawat di rumah sakit (Saxenal, 2009).
Pasien-pasien yang mengalami delirium, ketika dibandingkan dengan
pasien-pasien yang menderita penyakit yang sama tetapi tidak mengalami delirium,
menjalani perawatan yang lebih lama, rata-rata 5-10 hari lebih lama meskipun telah
dilakukan kontrol terhadap beberapa kovariat (Boettger, 2014).
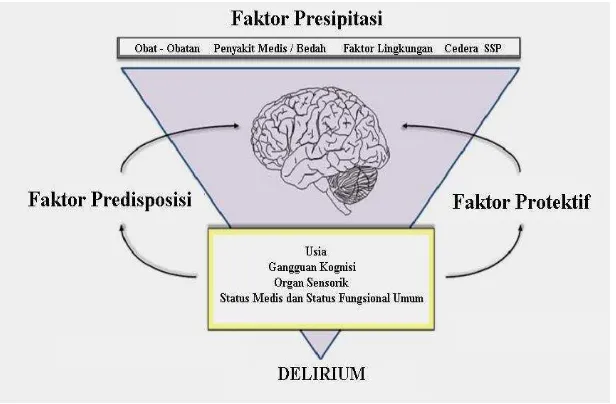
Penyebab delirium merupakan multifaktorial. Adanya interaksi antara faktor
presipitasi (infeksi, inflamasi, pembedahan, trauma dan obat-obat psikoaktif) , faktor
predisposisi (usia, gangguan kognitif dan sensoris, penyakit komorbid) dan faktor
protektif menyebabkan terjadinya ketidakseimbangan neurotransmiter di otak. Pada
pasien geriatri biasanya menggunakan Charlson’s Age Comorbidity Index untuk
menilai pengaruh usia dan penyakit komorbid terhadap angka morbiditas dan angka
2
sawar darah otak yang ditandai dengan peningkatan kadar S100 Calcium Binding
Protein β (S100β) dan perubahan pada transmisi sinaptik, tingkat eksitabilitas sel
saraf dan aliran darah otak, yang menyebabkan gejala neurobehavioral dan kognitif
(Cerejeira, 2010). Pada sebuah penelitian case–control tahun 2011 menemukan
hubungan antara aktivitas mikroglia, sel astrosit dan interleukin (IL)-6 dengan
delirium, dimana peningkatan kadar IL-6 berhubungan dengan risiko terjadinya
delirium (Van Munster, 2011).
Protein S100β merupakan calcium-binding protein yang disekresi oleh
astrosit dibawah pengaruh kondisi metabolik stres dan merupakan biomarker yang
menandakan kerusakan dari sistem saraf pusat (SSP) (Maldonado, 2013). Beberapa
penelitian menunjukkan peningkatan kadar serum S100β pada pasien-pasien yang
mengalami delirium dan berhubungan dengan tingkat keparahan dari delirium
(Stoicea, 2014).
Delirium sering tidak dikenali dan salah terdiagnosis oleh tenaga medis
profesional dimana sekitar sepertiga sampai dua pertiga kasus delirium tidak
terdiagnosis. Studi terbaru di bagian gawat darurat menyimpulkan bahwa dokter di
unit gawat darurat melewatkan diagnosis delirium pada 76% kasus. Hal ini
berhubungan dengan beberapa faktor seperti sifat delirium yang fluktuatif, tumpang
tindih dengan demensia dan depresi, jarangnya pemeriksaan rutin terhadap kognitif
secara formal di rumah sakit umum, kurang apresiasi terhadap konsekuensi klinis,
dan gagal memikirkan pentingnya diagnosis tersebut (Han, 2010).
Secara klinis penegakan diagnosis delirium dapat menggunakan beberapa alat
bantu yaitu Confusion Assesment Method (CAM), Diagnostic and Statistic Manual
3
(DRS), Delirium Observational Screening Scale (DOSS), Nursing Delirium
Screening Scale dan Global Attentiveness Rating (GAR). CAM merupakan
instrumen skrining delirium yang banyak digunakan berdasarkan kriteria DSM-III-R.
CAM dapat digunakan dengan mudah pada kondisi klinis rutin oleh staf medis
nonpsikiatrik atau staf perawat dengan latihan sebelumnya. Sedangkan untuk
mengukur severitas dari delirium, pemeriksaan MDAS dan DRS merupakan alat
bantu yang paling sering dipakai (Adamis, 2010; Grover, 2012).
1.2Rumusan masalah
Berdasarkan latar belakang masalah di atas, dapat dirumuskan masalah
penelitian sebagai berikut:
Apakah peningkatan kadar S100β dan kadar IL-6 serum berkorelasi dengan
tingkat keparahan delirium pada pasien geriatri?
1.3Tujuan penelitian
1.3.1 Tujuan umum
Untuk mengetahui faktor-faktor yang mempengaruhi tingkat keparahan
delirium pada pasien geriatri.
1.3.2 Tujuan khusus
Untuk membuktikan adanya korelasi antara kadar S100β dan kadar
interleukin-6 serum dengan tingkat keparahan delirium pada pasien geriatri.
1.4 Manfaat penelitian
1.4.1 Manfaat akademik/ilmiah
Jika peningkatan kadar S100β serum dan kadar IL-6 terbukti berkorelasi
dengan tingkat keparahan delirium, maka dapat memberikan kontribusi
4
1.4.2 Manfaat praktis
Memberikan masukan untuk stratifikasi tingkat keparahan delirium, sehingga
bermanfaat untuk diagnosis dan pengobatan dini delirium pada pasien
1
BAB II
KAJIAN PUSTAKA
2.1 Delirium
2.1.1 Definisi
Kata delirium berasal dari istilah latin delirareyang berarti menjadi “gila atau
marah”. Istilah ini telah didokumentasikan di dalam literatur medis selama lebih dari
2000 tahun. Pertama kali dilaporkan pada masa Hippocrates yang menggunakan
istilah phrenitis (gila) dan lethargus (letargi) untuk mendeskripsikan delirium subtipe
hiperaktif dan hipoaktif. Sebagai istilah medis, delirium pertama digunakan oleh
Celsus di abad pertama setelah Masehi untuk mendeskripsikan gangguan mental
yang berhubungan dengan demam atau trauma kepala ( Mittal dkk., 2011) .
Berbagai istilah telah digunakan dalam literatur untuk mendeskripsikan
delirium, meliputi acute confusional state, acute brain syndrome, acute cerebral
insufficiency, dan toxic-metabolic encephalopathy. Namun, delirium sekarang
menjadi istilah yang dipilih dan disarankan untuk menerima istilah acute confusional
syndrome sebagai sinonim untuk sindrom ini (Fong., 2009; Mittal dkk., 2011).
Delirium merupakan adalah sebuah sindrom neuropsikiatrik yang kompleks
dengan onset yang akut dan berfluktuasi. Sindrom ini mempengaruhi kesadaran dan
fungsi kognitif yang mungkin diikuti oleh peningkatan aktivitas psikomotor. Selain
itu delirium juga mempengaruhi atensi dan pada beberapa pasien ada yang
mengalami gangguan depresi (Mittal dkk., 2011).
2.1.2 Epidemiologi
Delirium adalah kondisi yang sering terjadi dan bersifat serius, terutama pada
lanjut usia yang dirawat di rumah sakit, dan menyerang sekitar 30% diantaranya.
2
Studi terbaru melaporkan prevalensi delirium sebesar 10-31% saat pasien masuk dan
insiden 3-29% selama masa rawat (Boettger, 2014).
Risiko meningkat secara eksponensial di ruang rawat intensif, dengan
prevalensi mencapai 80% dan di unit rawat paliatif dimana prevalensi dilaporkan
sebesar 85%. Angka yang lebih tinggi juga ditemukan di kondisi bedah dengan
insiden dilaporkan 10-70% setelah pembedahan, terutama pada pasien yang
menjalani operasi kardiotoraks, prosedur ortopedi emergensi (perbaikan fraktur
panggul), bedah vaskuler, atau operasi katarak (Munster, 2009). Studi pada lanjut
usia yang datang ke unit gawat darurat melaporkan prevalensi 5-30% (Han, 2009).
Selain sebagai tempat rawat jangka panjang, penghuni panti jompo
merepresentasikan kelompok yang rentan, dan diperkirakan prevalensi delirium
sekitar 3,4-33,3%. Di masyarakat, sesuai perkiraan, prevalensi rendah, berkisar
antara 1-2% (Miller, 2008).
2.1.3 Etiologi
Etiologi delirium biasanya multifaktorial. Namun, penelitian telah berhasil
mengidentifikasi faktor risiko konsisten untuk delirium yang diklasifikasikan
menjadi dua kelompok yakni faktor predisposisi dan faktor presipitasi. Faktor
predisposisi adalah faktor yang membuat orang lanjut usia lebih rentan terhadap
delirium dan faktor presipitasi terdiri dari faktor akut yang mencetuskan terjadinya
delirium. Kombinasi kedua faktor itu harus ada pada orang lanjut usia yang delirium.
Faktor predisposisi yang paling sering adalah usia lanjut, jenis kelamin pria,
demensia dan depresi yang telah ada sebelumnya, gangguan visual dan pendengaran,
ketergantungan fungsional, frailty, gangguan sensoris, dehidrasi dan malnutrisi,
polifarmasi (terutama obat psikoaktif), penyalahgunaan alkohol dan kondisi medis
3
Adapun beberapa faktor risiko terkait dengan delirium diantaranya usia yang
lebih dari 65 tahun, adanya riwayat delirium, riwayat trauma/pembedahan, adanya
komorbid demensia, depresi, gagal ginjal, penyakit hati, penurunan fungsi
penglihatan dan pendengaran, serta adanya pengobatan spesifik (antikolinergik,
narkotika, benzodiazepines, hipnotiks, anti inflamasi, beta bloker, diuretiks, dan
antidepresan). Selain itu faktor risiko lain yang memicu delirium yakni adanya
multifarmaka, stimulus lingkungan yang berlebihan, ketergantungan alkohol/obat,
abnormalitas metabolik (elektrolit,kadar gula), infeksi akut (infeksi saluran kemih,
pneumonia), serta ketidakadekuatan kontrol rasa nyeri (Maldonado, 2013). Setelah
bertambah tuanya usia, demensia menjadi faktor risiko paling sering kedua untuk
terjadinya delirium. Menurut Inouye pada tahun 2006, kerentanan yang mendasari
otak pada pasien demensia dapat menjadi predisposisi bagi mereka untuk mengalami
delirium, sebagai akibat gangguan yang berhubungan dengan penyakit medis akut,
obat, serta faktor lingkungan (Inouye, 2006). Menurut Saxena dan Lawley pada
tahun 2009, faktor presipitasi yang paling sering adalah: penyakit yang terjadi
bersamaan (misalnya infeksi), komplikasi iatrogenik, gangguan metabolik, kondisi
neurologis primer (misalnya stroke akut), operasi, obat (terutama benzodiazepin,
analgetik narkotik, dan obat dengan efek antikolinergik). Nyeri yang tak terkontrol
juga berhubungan dengan terjadinya delirium. Faktor lingkungan seperti masuk
ruang rawat intensif, pasien dalam kondisi terikat, atau kateterisasi kandung kemih
juga berkontribusi pada terjadinya delirium. Dalam konteks ini, Inouye dan
Charpentier pada tahun 1996 menyajikan suatu model untuk memprediksikan
terjadinya delirium pada pasien lanjut usia yang dirawat di rumah sakit, dengan
4
penggunaan lebih dari tiga obat pada hari sebelumnya, penggunaan kateter kandung
kemih, dan kejadian iatrogenik), berhubungan dengan sejumlah faktor presipitasi
(Cerejeira, 2010).
Gambar 1.
Model Multifaktorial dari Delirium (Maldonado, 2013)
2.1.4 Patogenesis Delirium
Walaupun prevalensi dan angka morbiditasnya yang tinggi, mekanisme
patogenesis dari delirium masih belum jelas sampai saat ini. Selama beberapa tahun
ini, proses metabolik telah diperkirakan sebagai penyebab dari delirium. Sekitar lima
puluh tahun lalu, Engel dan Romano mengatakan bahwa terganggunya fungsi
metabolik mendasari terjadinya delirium dan hal ini digambarkan dengan terjadinya
gangguan pada berbagai fungsi kognisi. Oleh karena itu, delirium merupakan
sindrom neurobehavioral yang disebabkan oleh disregulasi aktivitas sel saraf akibat
gangguan sistemik (Maldonado, 2013).
Dalam beberapa tahun ini, beberapa teori telah dikemukan telah mencoba
menjelaskan proses yang menyebabkan terjadinya delirium. Setiap teori yang
5
spesifik. Beberapa teori telah diusulkan sebagai penyebab dari delirium, diantaranya
adalah teori neuroinflamatory, neuronal aging, stres oksidatif, defisiensi
neurotransmiter, neuroendokrin, disregulasi diurnal dan network conectivity. Sampai
saat ini belum ada mekanisme patofisiologi tunggal yang telah didentifikasi sebagai
penyebab delirium. Hampir semua teori-teori ini saling melengkapi bukan saling
bersaing dalam menjelaskan terjadinya delirium. Oleh karena itu, teori-teori ini
tampaknya tidak ada yang mampu menjelaskan secara sendiri-sendiri penyebab
ataupun gejala delirium. Tetapi dua atau lebih teori-teori ini bersama-sama
menyebabkan gangguan biokimiawi yang kemudian menyebabkan terjadinya
delirium (Maldonado, 2013).
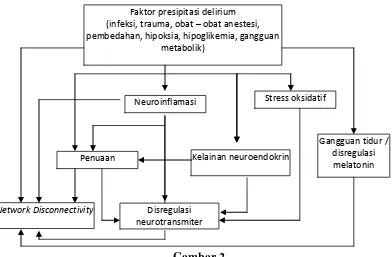
Gambar 2.
Gambaran skematik yang menunjukkan interrelationship dari teori-teori ini dalam patofisologi terjadinya delirium (Maldonado, 2013).
2.1.5 Gambaran Klinis
Berdasarkan kriteria DSM-IV, delirium dicirikan oleh gejala yang mulainya
sangat cepat (biasanya dalam beberapa jam sampai hari) dan cenderung berfluktuasi,
Faktor presipitasi delirium
(infeksi, trauma, obat – obat anestesi,
6
dengan perubahan tingkat kesadaran, ketidakmampuan berfokus, perhatian yang
bertahan atau teralih, dan perubahan kognitif (seperti gangguan memori, disorientasi,
gangguan bahasa) atau terjadinya gangguan perseptual hanya dapat dijelaskan oleh
demensia. Lebih lanjut, terdapat bukti dari anamnesis, pemeriksaan fisik, atau
temuan laboratoris bahwa gangguan tersebut disebabkan oleh konsekuensi fisiologis
langsung dari suatu kondisi medis umum, atau intoksikasi/withdrawal senyawa, atau
karena berbagai penyebab (Popeo, 2011; Martins dan Fernandes, 2012).
Awal perjalanan yang tiba-tiba dan akut adalah gambaran sentral delirium.
Oleh karena itu, penting bagi kita untuk memastikan tingkat fungsi kognitif dasar
pasien serta perjalanan perubahan kognitifnya. Kesadaran sebagai fungsi otak
memungkinkan kewaspadaan terhadap dirinya sendiri serta kewaspadaan terhadap
lingkungannya dan dicirikan oleh dua aspek utama: tingkat dan isi kesadaran.
Tingkat kesadaran mencerminkan bangkitan kewaspadaan: bangun, tidur, atau koma.
Isi kesadaran, atau bagiannya, dialami oleh subyek sebagai kewaspadaan terhadap
dirinya sendiri serta lingkungannya saat subyek bangun dan sadar baik. Isi kesadaran
dan kognitif hanya dapat diperiksa jika subyek minimal memiliki tingkat kesadaran
tertentu (Browne, 2010; Popeo, 2011; Martins dan Fernandes, 2012).
Pada delirium, gangguan kesadaran adalah salah satu manifestasi paling awal,
yang sering berfluktuasi, terutama di malam hari saat stimulasi lingkungan berada
pada titik terendah. Tingkat kesadaran dapat berflukutasi pada yang paling ekstrim
untuk pasien yang sama, atau dapat muncul dengan tanda yang lebih ringan seperti
mengantuk atau gangguan tingkat perhatian. Faktanya, pasien dapat tampak
7
Ektrim yang berlawanan, sangat waspada, juga dapat terjadi, terutama pada kasus
withdrawal alkohol atau obat sedatif (lebih jarang pada lanjut usia).
Perhatian adalah proses yang memungkinkan kita untuk memilih stimulus
yang relevan dari lingkungan, berfokus dan mempertahankan respon perilaku
terhadap stimulus tersebut, dan mengubah aktivitas mental menuju stimulus yang
lebih baru, mengorientasi ulang perilaku seseorang, berdasarkan relevansi stimulus.
Perhatian merupakan fungsi yang berbeda dari kesadaran, namun tetap bersifat
dependen. Oleh karena itu, berbagai derajat perhatian masih mungkin ditemukan
pada subyek yang sadar baik, namun perhatian dan konsentrasi penuh tidak mungkin
ditemukan pada penurunan kesadaran. Faktanya, perhatian dapat menurun secara
patologis pada kondisi organik, biasanya dengan penurunan kesadaran tertentu
(Browne, 2010; Popeo, 2011; Martins dan Fernandes, 2012).
Pada delirium, terjadi penurunan perhatian dan juga dikatakan sebagai salah
satu dari gambaran kardinal yang penting. Biasanya pasien tersebut mudah dialihkan
perhatiannya oleh stimulus yang irelevant, atau memiliki kesulitan mengingat apa
yang dikatakan pada anamnesis. Lebih lanjut, pertanyaan sebagian besar harus
diulang karena perhatian subyek menyimpang. Biasanya terjadi defisit global atau
multipel dalam hal kognitif, meliputi gangguan memori dan disorientasi. Faktanya,
karena penurunan perhatian, registrasi informasi baru dapat terganggu sehingga
mempengaruhi memori dan fungsi orientasi tertentu (Browne, 2010; Popeo, 2011;
Martins dan Fernandes, 2012).
Memori jangka pendek adalah yang paling sering terkena, namun kembalinya
informasi yang telah tersimpan juga dapat terganggu. Misalnya pasien mungkin tidak
8
Disorientasi biasanya sering terjadi, yang pertama terhadap waktu, berikutnya
terhadap tempat. Namun, disorientasi dikatakan abnormal pada pasien rawat inap
dengan sakit berat yang lama, tanpa acuan hari atau bulan. Fungsi pikir dan bicara
menjadi tumpang tindih dan keduanya dapat terganggu pada kondisi delirium
tertentu (Martins dan Fernandes, 2012).
Kesulitan bahasa dan gangguannya pada pasien delirium mungkin lebih
berhubungan dengan gangguan bangun dan tingkat perhatian, bukan penyebab
spesifik, atau tetap masih tetap dapat menunjukkan terjadinya perubahan proses.
Pada kasus gangguan global yang berat, konfabulasi dapat mendominasi, sehingga
hanya ada sedikit kemungkinan untuk menilai bahasa, memori, dan isi pikiran.
Seringkali bahasa dan bicara, yang mencakup membaca, hanya sedikit terpengaruh
dibanding menulis, terutama pada kondisi ringan atau stadium awal. Sejumlah hal
spesifik pada gangguan bahasa ditemukan dalam perjalanan delirium. Dalam satu
studi, sering ditemukan salah menyebutkan, sama seringnya dengan yang ditemukan
pada pasien demensia, namun berbeda dimana lebih sering terjadi dalam bentuk
gangguan kata dan salah menyebut nama yang tidak terkait. Gangguan kata dapat
dijelaskan oleh perseverasi. Pasien mengulang kata-kata yang sebelumnya diucapkan
(sehingga menjadi perseverasi), bukan kata yang diharapkan yang tidak dapat
ditemukan atau diucapkan oleh subyek. Salah menyebut yang tidak terkait adalah
penggunaan kata yang benar-benar berbeda arti dengan kata yang diharapkan
sehingga tidak berhubungan dengan konteks, tidak seperti parafasia (Maldonado,
2013).
Gambaran klinis lain adalah pikiran yang tidak terorganisir, bermanifes
9
atau tidak logis. Pasien mungkin tidak mampu membuat keputusan yang tepat, atau
melakukan tugas sederhana. Penilaian dan pikirannya buruk dan dapat pula timbul
delusi pada sekitar 30% kasus, terutama dengan sifat paranoid atau persekutor
(Popeo, 2011).
Gangguan persepsi juga dapat dideskripsikan pada subyek dengan delirium
yang meliputi ilusi dan misinterpretasi, muncul dari salah kesan terhadap stimulus
yang sebenarnya. Misalnya, pasien menjadi agitasi dan ketakutan, percaya bahwa
bayangan dalam ruangan adalah orang yang akan menyerang. Gangguan persepsi
juga dapat meliputi halusinasi, dimana sebenarnya tidak ada obyek. Halusinasi visual
merupakan yang paling sering terjadi, terutama di malam hari, dan pada sejumlah
kasus dapat terjadi di siang hari segera setelah pasien menutup mata. Isi halusinasi
cenderung sederhana, kadang hanya berupa warna, garis, atau bentuk. Namun, juga
dapat meliputi hewan yang berbahaya atau gambar aneh (Martin dan Fernandes,
2012).
Terdapat gambaran klinis lain yang sering berhubungan dengan delirium
yang tidak dimasukkan ke dalam kriteria diagnosis. Salah satunya adalah gangguan
siklus tidur-bangun, bercirikan ngantuk berlebihan di siang hari dengan insomnia di
malam hari, fragmentasi, dan kurang tidur atau siklus tidur yang benar-benar
terbalik. Sejumlah studi telah menemukan potensi peran gangguan tersebut, terutama
gangguan irama sirkadian dan fragmentasi tidur sebagai faktor kontributor penting
pada sindrom sundowning. Fenomena ini ditemukan pada pasien delirium yang
bercirikan perburukan perilaku disruptif di sore atau malam hari. Sindrom ini juga
dapat disebabkan oleh kelelahan dan penurunan input sensorik di malam hari
10
Gangguan perilaku psikomotor adalah gambaran klinis lain pada delirium,
dengan aktivitas motorik yang meningkat atau menurun. Pada kasus pertama, pasien
dapat mengalami gelisah atau seringnya perubahan posisi yang tiba-tiba. Di sisi lain,
pasien juga dapat menunjukkan kelesuan atau letargi, mendekati kondisi stupor.
Gangguan emosi seperti cemas, ketakutan, iritabilitas, kemarahan, depresi, dan
euforia juga dapat terjadi. Gejala tersebut sering dipengaruhi oleh berbagai faktor
seperti kondisi medis atau bedah, karakteristik personal, gangguan psikiatrik
premorbid, atau peristiwa hidup terbaru (Boettger, 2012).
Delirium seharusnya berada dalam kategori gangguan kesadaran yang lebih
luas. Adapun beberapa penelitian menyarankan penggunan derajat untuk yang paling
berat sampai yang paling ringan: koma, kondisi vegetatif persisten, stupor, mutisme
akinetik, kondisi sadar minimal, delirium/kondisi konfusional. Taksonomi tersebut
akan menjadi satu kesatuan dengan suatu “area abu-abu” atau regio transisi yang
membatasi antara satu derajat dengan derajat lainnya. Pendekatan ini akan
memungkinkan kesatuan beratnya penyakit tersebut terkait delirium itu sendiri, yang
saat ini telah ditinggalkan pada DSM-IV (Boettger, 2013).
2.1.6 Diagnosis
Delirium sering tidak dikenali dan salah terdiagnosis oleh profesional medis.
Sekitar sepertiga sampai dua pertiga kasus delirium tidak terdiagnosis. Studi terbaru
di bagian gawat darurat menyimpulkan bahwa dokter di unit gawat darurat
melewatkan diagnosis delirium pada 76% kasus. Hal ini berhubungan dengan faktor
seperti sifat delirium yang fluktuatif, tumpang tindih dengan demensia dan depresi,
jarangnya pemeriksaan rutin terhadap kognitif secara formal di rumah sakit umum,
11
diagnosis tersebut. Empat faktor risiko independen untuk tidak dikenalinya delirium
oleh perawat: delirium hipoaktif, usia sangat tua, gangguan penglihatan, dan
demensia (Han, 2010).
Perlu dipikirkan tentang onset akut delirium dan perjalanannya yang
fluktuatif. Penting untuk memastikan tingkat fungsi kognitif dasar pasien serta
perjalanan perubahan kognitifnya. Dengan cara ini, diagnosis lebih mudah dibuat
jika sebelumnya terdapat pemeriksaan kemampuan kognitif. Dalam anamnesis,
penting untuk mencari informasi dari anggota keluarga/caregiver, dan/atau staf
medis dan perawat. Selanjutnya, pasien harus diperiksa lebih dari satu kali sehari di
siang hari unruk mendeteksi kemungkinan fluktuasi gejala ( Mittal dkk., 2011).
Adapun pemeriksaan lengkap yang perlu dilakukan untuk membantu
menegakkan diagnosis delirium yakni diantaranya pemeriksaan neurologi,
pemeriksaan tingkat kesadaran dengan Glasgow Coma Scale, serta pemeriksaan
fungsi kognitif dengan alat yang sudah terstandardisasi seperti abbreviated mental
test score (AMTS). Disamping itu perlu dievaluasi adanya kondisi demam dan
ketergantungan alkohol. Adapun pemeriksaan penunjang yang perlu dilakukan untuk
mengevaluasi adanya penyebab dasar, yakni pemeriksaan darah lengkap, elektrolit,
kalsium, urea darah, test fungsi hati dan tiroid, kadar gula darah, foto polos dada,
elektrokardiografi, kultur darah, serta urinalisis ( Mittal dkk., 2011).
Penurunan perhatian adalah ciri penting lain pada delirium. Pemeriksaan
kognitif harus meliputi alat skrining kognitif global (misalnya: Mini Mental State
Examination,MMSE) serta pemeriksaan perhatian. Terdapat instrumen skrining yang
dapat mendeteksi penurunan perhatian secara cepat dan cukup sering digunakan
yaitu Digit Span Test dan Trail Making Test. Dalam konteks ini, penting pula untuk
12
kondisi lainnya, misalnya kelelahan. Bahkan, berdasarkan beratnya delirium, tugas
kognitif dapat dipengaruhi secara proporsional oleh perhatian yang dibutuhkan pada
tugas tersebut (Grover., 2012).
Berdasarkan pedoman internasional terbaru (NICE 2010), semua orang tua
yang dirawat di rumah sakit atau tempat perawatan jangka panjang harus diskrining
untuk mencari tahu faktor risiko terjadinya delirium dan gangguan kognitif
menggunakan uji kognitif singkat (misalnya MMSE). Jika teridentifikasi perubahan
baru atau fluktuasi pada fungsi kognitif, persepsi, fungsi fisik, atau perilaku sosial
pada mereka yang berisiko, pemeriksaan klinis harus dilakukan berdasarkan kriteria
DSM-IV atau Confusion Assesment Method (CAM) untuk menegakkan diagnosis.
Evaluasi ini harus dikerjakan oleh profesional medis yang terlatih baik (Grover,
2012).
Confusion Assesment Method merupakan instrumen skrining delirium yang
banyak digunakan berdasarkan kriteria DSM-III-R. CAM dapat digunakan dengan
mudah pada kondisi klinis rutin oleh staf medis nonpsikiatrik atau staf perawat
dengan latihan sebelumnya. Versi singkatnya meliputi algoritme diagnostik,
berdasarkan empat ciri kardinal delirium yakni (1) onset akut dan perjalanan
fluktuatif; (2) penurunan perhatian; (3) pikiran tak terorganisir; dan (4) perubahan
tingkat kesadaran. Diagnosis delirium berdasarkan CAM membutuhkan ciri 1, 2,
disertai 3 atau 4 (Vietarra DW., 2012). Pada ruang rawat kritis (Intensive Care Unit,
ICU) atau ruang pemulihan pasca bedah, terutama pada pasien yang tidak dapat
berkomunikasi secara verbal, CAM-ICU (adaptasi dari CAM) harus digunakan. Studi
review terbaru menguatkan rekomendasi ini untuk mendukung penggunaan CAM
13
Identifikasi penyebab dasar penting untuk diagnosis delirium. Karena itu,
pemeriksaan fisik dan neurologis sangat penting, membantu menyingkirkan penyakit
infeksi, metabolik, endokrin, kardiovaskuler, dan penyakit serebrovaskuler.
Pemeriksaan fisik harus mencakup evaluasi tanda vital dengan saturasi oksigen.
Pemeriksaan umum harus difokuskan pada fungsi jantung dan paru. Di luar itu,
pemeriksaan neurologis harus memasukkan status mental dan temuan fokal.
Pendekatan diagnostik harus mencakup tes berikut seperti darah lengkap, kadar
ureum darah, kreatinin serum, elektrolit, gula darah, C-reactive protein (CRP), fungsi
hati, dan fungsi tiroid. Penting pula untuk mengidentifikasi penggunaan obat dan
senyawa lain misalnya alkohol atau benzodiazepin, yang dapat berkontribusi pada
penyakit ini (Mittal dkk, 2011).
Tidak ada pemeriksaan laboratorium, pencitraan otak atau tes lain yang lebih
akurat dibanding pemeriksaan klinis. Namun, mereka dapat berguna untuk
mengidentifikasi kemungkinan penyebab delirium dan faktor kontributor yang dapat
dikoreksi. Pada sejumlah kondisi, pencitraan otak dan elektroensefalografi (EEG)
bermanfaat, jika terdapat bukti kuat adanya penyebab intrakranial, berdasarkan
pemeriksaan klinis (misalnya perubahan status mental setelah terjadi benturan pada
kepala) atau jika tanda neurologis fokal atau aktivitas kejang terdeteksi saat
dilakukan pemeriksaan fisik (Choi, 2012)
2.2 Peranan Neuroinflamasi pada Delirium
2.2.1 Kondisi Klinis dengan Reaksi Inflamasi Sistemik yang Mencetuskan
terjadinya Delirium
Inflamasi sistemik sering merupakan gambaran yang nyata dari beberapa
14
ini melibatkan kerusakan jaringan dan atau infeksi. Oleh karena itu, delirium
merupakan manifestasi yang paling sering dari disfungsi multiorganik. Misalnya
pada kondisi sepsis, yang merupakan gambaran klinis dari infeksi saluran kemih atau
pneumonia (khususnya pada pasien lansia yang mengalami dementia) (Siami dkk.,
2008) atau merupakan komplikasi dari pembedahan mayor (O’Keeffe, Chonchubair,
1994).
Infeksi perifer mengaktivasi kaskade inflamasi yang diikuti pengenalan
komponen spesifik dari mikroorganisme, misalnya lipopolisakarida (LPS) dari
bakteri gram negatif, oleh fagosit dalam sirkulasi (Sheng dkk., 2003). Banyak sekali
faktor-faktor, misalnya kerusakan jaringan, kehilangan darah, nyeri dan anestesi
dapat mempengaruhi fungsi dari sel imunokompeten dan menghasilkan mediator
inflamasi. Bahkan pada kondisi yang steril, inflamasi dapat dipicu oleh kerusakan
jaringan dengan pelepasan ligan endogen, termasuk heat shock protein, hialuronan,
β-defensin dan kristal asam urat. Sitokin proinflamasi yang dihasilkan oleh makrofag
dan monosit, termasuk tumor necrosis alpha (TNF-α) dan IL-1 akan merangsang
ekspresi dari beberapa mediator yang berfungsi untuk menghasilkan sel inflamasi
lainnya yang akan merusak jaringan. Oleh karena itu, pada awalnya terjadi respon
imun lokal kemudian akan menyebar ke seluruh tubuh, sehingga respon sistemik
akan meningkatkan kadar sitokin dalam sirkulasi. Pada pembedahan jantung,
cardiopulmonal bypass tampaknya merupakan faktor risiko utama yang
mengaktivasi komplemen dan mensekresikan sitokin proinflamasi yang berkontribusi
terhadap disfungsi multiorgan postoperasi. Peningkatan kadar mediator inflamasi
juga berhubungan dengan disfungsi organ postoperasi pada pembedahan nonkardiak
15
Pada banyak kondisi medis dan bedah, dimana delirium paling banyak
terjadi, pelepasan dan produksi mediator proinflamasi ke dalam sirkulasi merupakan
bagian dari proses patofisiologi. Bukti nyata yang secara langsung membuktikan
keterlibatan inflamasi sistemik dalam hal terjadinya delirium berasal dari beberapa
penelitian yang menyatakan bahwa kadar CRP, IL-6, IL-8 dan TNF-α tinggi pada
pasien yang mengalami delirium postoperasi dibandingkan dengan yang tidak
mengalami delirium (Van Munster dkk., 2008).
2.2.2 Efek Inflamasi Sistemik Akut terhadap Otak
2.2.2.1 Dari Proses Inflamasi Sistemik menjadi Neuroinflamasi
Saat ini sudah terbukti bahwa sel SSP bereaksi terhadap adanya sinyal imun
perifer, yang menyebabkan terjadinya produksi dari sitokin dan mediator inflamasi
lainnya di otak, kemudian terjadi proliferasi sel dan aktivasi
hypothalamus-pituitary-adrenal axis melalui interaksi sistem yang kompleks. Respon imun alamiah ini
merupakan mekasime adaptasi yang penting karena mengatur respon sentral untuk
melawan infeksi akut. Beberapa mekanisme yang terlibat dalam respon ini adalah
(Hopkins, 2007):
1. Pengenalan langsung terhadap sinyal patogen atau mediator inflamasi pada
daerah-daerah dimana sawar darah otak terganggu atau tidak ada.
2. Sistem transport sitokin pada sawar darah otak yang bergantung pada energi
(energy-dependent) atau diproduksinya second messenger aktif di dalam sawar
darah otak.
3. Pengenalan aktivasi respon umun perifer oleh sel saraf sensoris yang membawa
16
2.2.2.2 Kerusakan Sawar Darah Otak
Penelitian-penelitian pada binatang menunjukkan bahwa rangsangan
inflamasi perifer berhubungan dengan perubahan fungsi dan molekuler sawar darah
otak. Peningkatan permeabilitas sawar darah otak dan perubahan ekspresi protein
tight-junctional dilaporkan pada tiga model inflamasi yang berbeda. Injeksi LPS
merangsang kaskade inflamasi pada fase awal yang menyebabkan kerusakan sawar
darah otak, over-expresion dari molekul adhesi di sel endotel, perekrutan dan
infiltrasi dari derivat sel darah putih ke dalam jaringan otak (Nishioku, 2009).
Penelitian postmortem pada jaringan otak manusia juga menunjukkan hubungan
antara inflamsi sistemik dengan aktivasi sel sel endotel dan sel perivaskular.
Walaupun konfirmasi neuropatologi dari kerusakan sawar darah otak pada manusia
sangat sulit untuk dibuktikan, namun peningkatan kadar S100B dapat
dipertimbangkan sebagai bukti terjadinya peningkatan permeabilitas sawar darah
otak (Munster dkk, 2010). Oleh karena itu, beberapa kondisi yang berhubungan
dengan inflamasi sistemik akut (misalnya syok sepsis dan pembedahan jantung)
mungkin berhubungan dengan disfungsi sawar darah otak. Demikian juga, kerusakan
sawar darah otak selama episode delirium dapat disimpulkan dari penelitian yang
menunjukkan peningkatan kadar S100B serum pada pasien lansia yang menderita
penyakit medis. Begitu pula delirium yang terjadi pada fase awal syok sepsis,
berhubungan dengan leucoencephalopathy pada otak. Hal inilah yang diperkirakan
sebagai penyebab terjadinya kerusakan sawar darah otak. Sebagai tambahan, faktor
lain yang mempengaruhi struktur dan fungsi dari sawar darah otak adalah hipoksia,
17
2.2.2.3 Respon Sistem Saraf Pusat yang Diperantarai oleh Molekul-molekul dalam
Sirkulasi Sistemik
Pada SSP, bermacam-macam molekul, seperti LPS dapat berinteraksi secara
langsung dengan reseptor yang terdapat dalam sel endotel dan sel parenkim otak. Sel
mikroglia merupakan sel yaang paling bisa mendeteksi perubahan pada lingkungan
SSP melalui banyak resptor inti dan reseptor permukaan. Oleh karena itu, pada SSP
tikus, sel yang terletak pada pembuluh darah besar dan mikroglia mengekspersikan
Toll-like Recptor 4 (TLR4; reseptor dari LPS). Aktivasi TLR4 merupakan kunci
utama dalam respon inflamasi SSP terhadap LPS perifer. Ada juga bukti yang
menyatakan bahwa mediator lainya juga berpengaruh terhadap komunikasi antara sel
perifer dengan otak, termasuk TNF-α dan protein chemoattractant monosit. Sekali
teraktivasi, mikroglia mengalami perubahan morfologi dan bersamaan dengan itu,
mikroglia mengekspresikan beberapa molekul seperti MHC klas I, CD45, CD4,
ICAM-1, VLA-4, LFA-4 dan Fas. Setelah terstimulasi, beberapa mikroglia
mengekspersikan MHC klas II dan molekul B7. Perubahan ini bergabung dengan
produksi dari sitokin proinflamasi oleh mikroglia (TGF-B1, IL-1B, TNFa, IGF-1),
spesies oksigen reaktif (Reactive Oksigen Species, ROS) dan ekspansi dari populasi
mikroglia melalui proliferasi dari sel dan perekrutan dari sekitarnya atau melalui
darah (Block dkk., 2007).
Pengenalan awal rangsangan inflamasi di sawar darah otak diikuti oleh
aktivasi kaskade inflamasi yang mengakibatkan pergerakan sel-sel berdekatan dan
unit struktural neurovaskular. Sel endotel, astrosit, mikroglia, sel periset dan lamina
basal berinterkasi melalui perantaraan mediator inflamasi, termasuk sitokin, kemokin
18
mengantarkan sinyal di dalam unit neurovaskular kepada bagian otak lainnya dengan
menggunakan kontrol multimodal dari transmisi sinaptik, eksitabilitas sel saraf dan
aliran darah otak (Block dkk., 2007).
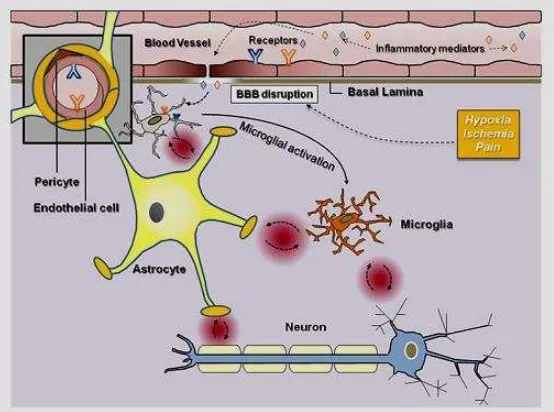
Gambar 3. Pengenalan dan propagasi dari rangsangan imun perifer pada SSP. Interakasi awal dari mediator inflamasi (sitokin proinflamasi dan LPS) dengan unit neurovaskular terjadi melalui beberapa reseptor dan berkaitan dengan peningkatan permeabilitas sawar darah otak (Cerejeira dkk, 2010).
2.2.2.4 Inflamasi Sistemik Akut dan Disfungsi Neurokognisi
Hasil akhir dari inflamasi sistemik tidak hanya berhubungan dengan delirium
tetapi juga dengan banyak gejala neuropsikiatri. Pada manusia yang sehat, studi
eksperimental dengan menggunakan endotoksin bakteri ternyata berefek terhadap
fungsi kognisi, status emosional dan pola tidur. Sitokin dalam sirkulasi mengalami
peningkatan setelah pemberian dosis sangat rendah dari LPS (0.2 ng/KgBB) dan
perubahan ini mempunyai pengaruh negatif terhadap memori (Qin., 2007). Yang
terbaru adalah sebuah penelitian menggunakan magneting resonance imaging (MRI)
yang mendokumentasikan tentang injeksi LPS pada manusia sehat ternyata
19
ini berhubungan dengan peningkatan aktivitas substansia nigra (SN) kiri (Brydon,
2008).
Perubahan fungsi kognitif yang terjadi setalah inflamasi sistemik yang akut
diperkirakan sebagai akibat dari interaksi selular dan molekular yang sinergis pada
bagian-bagian otak yang berbeda dan terutama pada hipokampus. Sitokin
proinflamatory IL-1 telah lama dikenal sebagai perusak hipokampus dan mempunyai
peranan penting pada proses neurofisiologis dari konsolidasi memori, dan modulasi
plastisitas sinaptik. 6 juga mempengaruhi disfungsi hipokampus. Sebaliknya,
IL-10 tampaknya mengimbangi efek IL-1 dan IL-6, dengan cara menghambat pengaruh
inflamasi sistemik terhadap perubahan kognisi dan perilaku. Demikian juga,
penurunan ekspresi hipokampal brain-derived growth factor (BDNF) dan
peningkatan stres oksidatif karena disfungsi mitokondria juga berpengaruh pada
defisit kemampuan belajar dan memori yang berhubungan dengan neuroinflamasi.
Hal ini memberi kesan bahwa reaksi kombinasi otak untuk menghasilkan ROS,
sitokin proinflamasi, metaloproteinase, Nitrit Oksida (NO) dan kemokin
menyebabkan perubahan fungsional pada sel saraf, kemudian mempengaruhi
beberapa proses misalnya: plastisitas sinaptik, potensiasi jangka panjang, dan dapat
mengganggu memori dan proses belajar.
Ada bukti bahwa aktivasi mikroglia dan astrosit oleh sistem imun perifer
dapat mengakibatkan ketidak seimbangan Bax/Bcl-2 dan mempengaruhi sel
intraparenkim otak. Pada kasus yang fatal, misalnya syok sepsis, Sharsat dkk
melaporkan bahwa terjadi apoptosis sel glial dan sel saraf dalam pusat otonomik di
otak manusia. Lee dkk menduga bahwa aktivasi amyloidegenesis berhubungan
20
mengakibatkan apoptosis dan kematian sel saraf serta disfungsi neurokognisi.
Rangkaian proses ini terjadi dalam sistem saraf pusat setelah adanya stimulasi
sistem imun perifer. Oleh karena itu, sekali terjadi paparan LPS atau TNF-α dapat
menimbulkan kehilangan saraf dopaminergik yang signifikan dalam SN, sekitar 27%
dalam tujuh bulan pertama dan bertambah berat (47%) dalam sepuluh bulan setelah
paparan pertama.
Secara keseluruhan, data-data ini menunjukkan bahwa paparan akut terhadap
inflamasi sistemik menyebabkan sindrom klinis neurokognisi yang dapat disamakan
dengan delirium. Hal ini disebabkan oleh reaksi neuroinflamasi yang mempengaruhi
fungsi sel saraf dan sinaptik. Sintesis asetilkolin sangat sensitif terhadap perubahan
homeostasis otak, dimana proses neuroinflamasi menimbulkan defisit kolinergik
yang berkaitan dengan ketidakseimbangan neurotransmiter lainnya, misalnya
dopamin, serotonin dan norephineprin. Ilmu pengetahuan saat ini tidak dapat
menjelaskan secara lengkap mekanisme yang pasti tentang apakah perubahan
struktural, fungsional dan neurokimiawi menimbulkan gejala kognisi, perilaku dan
emosional. Data dari bagian anestesi menggambarkan bahwa beberapa gejala utama
delirium melibatkan perubahan aspek dinamik dari aktivitas sel saraf, kemudian
mempengaruhi kemampuan otak untuk mengintegrasikan informasi melalui
diskoneksi fungsional dari struktur-struktur anatomi yang berbeda. Demikian juga,
perbedaan gambaran klinis mungkin timbul karena gangguan pada bagian otak yang
berbeda, yang dikenal sebagai pusat kesadaran, perhatian dan kewaspadaan.
Kemudian, mekanisme neuroinflamasi ini juga mungkin terlibat dalam beberapa
21
2.3 Peranan Proses Penuaan pada Delirium
Proses penuaan yang disertai perubahan fisiologis pada penuaan merupakan
faktor risiko terjadinya delirium. Proses penuaan berhubungan perubahan pada otak
misalnya pengaturaran neurotransmiter yang berkaitan dengan stress metabolik,
penurunan aliran darah otak , penurunan densitas vaskuler, kehilangan sel saraf
(terutama pada locus cereleus dan substantia nigra) dan penurunan transduksi
intraseluler. Proses-proses ini yang menjelaskan mengapa proses penuaan berkaitan
dengan beberapa gangguan defisist kognitif dan peningkatan risiko dementia.
Beberapa penelitian menyatakan bahwa ada hubungan resiprokal antara delirium dan
penurunan fungsi kognitif. Dementia merupakan faktor risiko utama delirium pada
pasien-pasien usia lanjut dan kelanjutan proses delirium itu sendiri tampaknya
meningkatkan risiko penurunan fungsi kognisi, termasuk dementia.
Penuaan itu sendiri menunjukkan peningkatan jumlah mediator inflamasi di
dalam sirkulasi yang menunjukkan bahwa proses neurodegenerasi kronik yang
disebakan oleh respon inflamasi mengaktivasi sel mikroglia SSP. Sel mikroglia ini
menghasilkan respon inflamasi yang berlebihan terhadap perubahan imunologi.
Perubahan pada sistem imun yang berkaitan dengan penuaan (immunosenescence)
menyebabkan peningkatan sekresi sitokin oleh jaringan adiposit. Hal ini merupakan
penyebab utama inflamasi kronik, yang lebih dikenal sebagai “inflammaging”.
Proses inflamasi ini mungkin berkontribusi terhadap progresifitas penyakit melalui
produksi mediator inflamasi. Proses penuaan berhubungan dengan peningkatan nilai
baseline dua sampai empat kali mediator inflamasi termasuk sitokin dan protein fase
akut. Faktor-faktor lain yang berpengaruh terhadap delirium pada pasien usia lanjut
22
sensitivitas terhadap obat-obatan dan rendahnya threshold terhadap efek obat-obat
antikoloinergik.
Beberapa mekanisme utama yang berhubungan dengan peningkatan risiko
terjadinya delirium pada usai lanjut:
1. Kehilanagn sel saraf terutama pada lokus coereleus dan substantia nigra.
2. Perubahan pada berbagai sistem neurotransmitter.
3. Penurunan intergritas white matter yang berhubungan dengan usia.
4. Penurunan aliran darah otak, terutama pada gyrus cingulate anterior, basal
ganglia bilateral, bagian prefrontal kiri, bagian frontal lateral kiri dan bagian
temporal superior kiri, dan korteks insular.
5. Penurunan metabolisme oksigen pada otak.
6. Berkurangnya suplai oksigen (misalnya hipoksia).
7. Berkurangnya metabolism oksidatif otak.
2.4 Biomarker Delirium
Untuk meningkatkan diagnosis dan perawatan delirium, beberapa
biomarker telah diteliti sebagai alat penunjang untuk stratifikasi, diagnosis,
monitoring dan prognosis delirium. Penelitian-penelitian telah direview dan tidak
ditemukan evidence yang menyokong kegunaan klinis dari biomarker delirium,
walaupun beberapa biomarker seperti S100B, insulin-like growth factor (IGF)-1 dan
beberapa marker inflamasi telah menunjukkan hasil yang menjanjikan untuk
dievaluasi pada penelitian-penelitian berikutnya. Untuk meningkatkan diagnosis dan
perawatan, para peneliti telah mengidentifikasi beberapa biomarker yang mungkin
membantu dalam diagnosi, severitas, perkembangan terapi terbaru, monitoring
23
Patofisiologi delirium belum bisa dijelaskan dengan pasti dan mungkin
menunjukkan respon otak terhadap stres lokal atau sistemik yang melibatkan
interaksi jalur biologi sentral dan perifer yang menimbulkan gejala klinis delirium.
Ada dua hipotesis utama untuk menjelaskan mekanisme terjadinya delirium, yaitu:
teori neurotransmiter dan teori inflamasi. Teori neurotransmiter menggambarkan
kelebihan atau kekurangan beberapa neurotransmiter mengakibatkan timbulnya
gejala yang berhubungan dengan delirium. Seperti yang sudah dikemukan bahwa
delirium merupakan akibat dari interaksi yang kompleks antara berbagai faktor
presiposisi dan faktor presipitasi. Interaksi ini mengakibatkan ketidakseimbangan
neurotransmiter yang mengakibatkan terjadinya delirium, dimana terjadi pelepasan
dopamin yang berlebihan, defisiensi sintesis asetilkolin dan tinggi atau rendahnya
kadar serotonin dan gamma-amino-butiric-acid (GABA) (Cerejeira, 2012).
Teori inflamasi menekankan pada peran dari sitokin sebagai respon terhadap
adanya stressor pada delirium, termasuk diantaranya IL-1, IL-6, interferon
danTNF-α. Teori ini menggambarkan kesamaan gangguan berikut yang disebabkan oleh
pelepasan sitokin dan delirium. Berdasarkan penelitian pada binatang, kedua teori ini
tidak dapat berdiri sendiri melainkan saling mempengaruhi satu sama lain dalam
menjelaskan terjadinya delirium. Beberapa biomarker telah dihubungkan dengan
risiko terjadinya delirium, menilai aktivitas penyakit dan juga dihubungkan dengan
derajat severitas delirium itu sendiri. Genetik marker seperti Apolipoprotein (Apo)-E,
marker inflamasi (IL-6, IL-8, Kortisol, CRP) dan IGF-1 telah dihubungkan dengan
risiko terjadinya delirium pada pasien usia lanjut. Alel Apo-E merupakan faktor
risiko terjadinya delirium dan durasi delirium yang lebih lama. Tingginya kadar IL-8,
24
rendahnya kadar IGF-1. Dalam hal diagnosis dan penilaian aktivitas penyakit, serum
aktifitas antikolinergik (SAA), mediator inflamasi (IL-6 dan IL-8) dan IGF-1 juga
berkorelasi sangat kuat dengan delirium (Cerejeira dkk, 2012). Sedangkan kadar
S100B dan neuro-specific enolase (NSE) berhubungan dengan derajat severitas
delirium, dimana S100B merupakan faktor yang paling konsisten berhubungan
dengan delirim setelah dilakukan adjustmen terhadap beberapa variabel perancu (Aly
dkk., 2014).
Biomarker memegang peranan penting dalam menjelaskan patofisologi
delirium. Diagnosis, prognosis dan pengaruh jangka panjang dari delirium.
Biomarker dapat sangat berguna untuk perkembangan terapi delirium dan secara
tidak langsung bermanfaat untuk menilai severitas delirium. Secara umum biomarker
dapat diklasifikasikan menjadi dua kelompok, yaitu biomarker yang berhubungan
dengan risiko terjadinya delirium dan biomarker yang menggambarkan delirium itu
sendiri, dalam hal ini diagnosis, severitas dan lama delirium terjadi (Khan dkk.,
2011).
Keadaan tumpang tindih ditemukan antara marker inflamasi pada delirium
dan sistem kolinergik pasien. Asetilkolin bersifat menghambat pelepasan sitokin
proinflamasi IL-6 sehingga mengontrol inflamasi pada otak. Oleh karena itu,
proses-proses yang menyebabkan sistem kolinergik gagal dengan berkurangnya simpanan
asetilkolin mungkin akan menyebabkan kontrol yang inadekuat terhadap kaskade
inflamasi dan mempengaruhi terjadinya delirium. Delirium juga dapat dilihat sebagai
perilaku penyakit yang diakibatkan oleh sitokin. Sitokin-sitiokin ini menyebabkan
terjadinya demam, kelemahan dan letargi sehingga menyebabkan gangguan
25
terutama pada usia lanjut dengan penyakit neurodegenratif misalnya penyakit
Alzheimer. Siklus berulang ini terus berlangsung, regulasi yang tidak adekuat dari
inflamasi karena menurunnya aktivitas kolinergik. Regulasi yang tidak adekuat ini
menjelaskan interaksi yang kompleks anatar teori inflamasi dan teori neurtransmiter
(Cerejeira dkk., 2012).
2.4.1 S100 Calcium Binding Protein B (S100B)
S100 merupakan protein dengan berat molekul 20kDa termasuk pada
superfamili S100/calmodulin/troponin C dari protein calcium binding EF-hand. S100
diisolasi dari otak manusia dan diperkirakan sebagai protein spesifik pada sel glia.
Sampai saat ini, ada 20 monomer family S100 yang telah teridentifikasi berdasarkan
kesamaan fungsi dan struktur. Hampir semua protein S100 dalam bentuk dimer dan
diakspresikan oleh sel-sel yag khusus. Dua monomer S100 (S100A1 dan S100B)
terdapat pada sel glia sistem saraf pusat dan pada beberapa sel perifer, misalnya: sel
Schwan, sel melanosit, sel adiposit dan sel kondrosit. Disamping itu, kedua monomer
ini juga ditemukan pada beberapa penyakit keganasan seperti melanoma, glioma,
karsinoma tiroid dan renal cell carcinoma (Macedo dkk., 2014). Pengukuran kadar
S100B pada serum telah menunjukkan kegunaan klinik untuk monitoring terapi dan
prognosis pasien dengan melanoma maligna. Beberapa penelitian juga menyatakan
bahwa kadar S100B serum berguna dalam manajemen pasien dengan cedera kepala,
henti jantung, pembedahan jantung dan stroke (Heizmann, 2002).
S100B merupakan biomarker yang menunjukkan injuri secara langsung pada
sel saraf, misalnya cedera kepala dan penyakit cerebrovascular. S100B menunjukkan
hal yang menjanjikan untuk menilai tingkat keparahan delirium. Astrosit melepaskan