xvii
INTISARI
Malaria merupakan salah satu penyakit utama yang menjadi penyebab kematian pada daerah beriklim tropis, salah satunya Indonesia. Peningkatan morbiditas dan mortalitas akibat malaria disebabkan oleh resistensi plasmodia (utamanya P. falciparum) terhadap antimalaria yang umum digunakan. Dibutuhkan antimalaria kelas baru yang dapat mengatasi permasalahan ini. Pengembangan desain senyawa antimalaria baru dapat dilakukan dengan metode analisis hubungan kuantitatif struktur-aktivitas. Penelitian ini bertujuan untuk mengetahui hubungan kuantitatif antara struktur dan aktivitas senyawa vinkadiformina dan turunannya berdasarkan log 1/IC50. IC50 merupakan konsentrasi yang dapat menghambat pertumbuhan plasmodia malaria sebanyak 50%.
Penelitian ini menggunakan rancangan eksperimental kuasi. Sebagai variabel bebas digunakan 17 deskriptor teoretis (elektronik, sterik, dan hidrofobisitas). Sebagai variabel tergantung digunakan log 1/IC50. Data deskriptor diperoleh dengan perhitungan semiempiris MNDO menggunakan program komputer HyperChem Pro ver.6.0. Data diolah secara statistik menggunakan analisis regresi multivariat metode backward dengan program SPSS 11.0 for Windows.
Analisis statistik menghasilkan 4 model persamaan dan ditunjukkan bahwa model 2 memenuhi kriteria statistik dan dapat dipilih sebagai model persamaan terbaik, dengan persamaan :
log (1/IC50) = 28,8758 + (22,7560qC1) + (14,2669qC2) + (33,7110qC3) + (-27,2900qN) + (-10,0545qC7) + (-1,0678qC8) + (79,9843qC9)
+ ( 0,5394ΔE) + (-0,0067V) + (-0,5904 MR) + (0,7226∂) + (0,0285 M) + (0,8408 log P)
Model persamaan tersebut dapat digunakan untuk memprediksikan aktivitas antimalaria senyawa-senyawa baru turunan vinkadiformina. Berdasarkan model persamaan terbaik diperoleh 15 senyawa baru turunan vinkadiformina yang memiliki aktivitas antimalaria.
Kata kunci : HKSA, turunan vinkadiformina, MNDO, regresi linier multivariat
ABSTRACT
Malaria is one of the primary disease that causes deathness in many tropical countries, such as Indonesia. The increasing of morbidity and mortality by malaria is caused by the resistency of plasmodium (primarily P. falciparum) to antimalarial that commonly used. Antimalarial from a new class is needed. Design of antimalarial from new class could be made by using quantitative structure-activity relationship analysis. This research is aimed to know the quantitative relationship between structure and activity of vincadifformine and its derivatives based on log 1/IC50. IC50 is concentration that can inhibit 50% of the malarial plasmodia’s growth.
This research use a quasi experimental design. Seventeen descriptors were used as dependent variabel (electronic, steric, and hydrophobicity). Log 1/IC50 is used as independent variabel. Descriptor data is obtained by semiempirical MNDO calculation using HyperChem Pro ver.6.0 computer programme. Data was analysed statisticaly by multivariate linear regression backward method by using SPSS 11.0 for Windows.
Statistic analysis gave 4 equation models and the second model showned to fulfil the statistic criteria. The second model could be selected as the best equation model.
log (1/IC50) = 28.8758 + (22.7560qC1) + (14.2669qC2) + (33.7110qC3) + (-27.2900qN) + (-10.0545qC7) + (-1.0678qC8) + (79.9843qC9)
+ ( 0.5394ΔE) + (-0.0067V) + (-0.5904 MR) + (0.7226∂) + (0.0285 M) + (0.8408 log P)
This model can be used to predict the activity of new vincadifformine’s derivatives. There are 15 vincadifformine’s derivatives which could give antimalarial activity based on the best equation model.
Keyword : QSAR, vincadifformine’s derivatives, MNDO, multivariate linier regression
HUBUNGAN KUANTITATIF STRUKTUR-AKTIVITAS SENYAWA VINKADIFORMINA DAN TURUNANNYA SEBAGAI SENYAWA
ANTIMALARIA BERDASARKAN PARAMETER TEORETIS
HASIL PERHITUNGAN SEMIEMPIRIS
Modified Neglect of Diatomic Overlap (MNDO)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh:
Dominika Anny Yanuarti NIM : 038114129
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2007
HUBUNGAN KUANTITATIF STRUKTUR-AKTIVITAS SENYAWA VINKADIFORMINA DAN TURUNANNYA SEBAGAI SENYAWA
ANTIMALARIA BERDASARKAN PARAMETER TEORETIS
HASIL PERHITUNGAN SEMIEMPIRIS
Modified Neglect of Diatomic Overlap (MNDO)
Oleh:
Dominika Anny Yanuarti
NIM : 038114129
Skripsi ini telah disetujui oleh
Pembimbing Utama
Tanggal
(Drs. Iqmal Tahir, M.Si.)
Pembimbing Pendamping
Tanggal
(Drs. Mulyono, Apt.)
iv
Pengesahan Skripsi Berjudul
HUBUNGAN KUANTITATIF STRUKTUR-AKTIVITAS SENYAWA VINKADIFORMINA DAN TURUNANNYA SEBAGAI SENYAWA
ANTIMALARIA BERDASARKAN PARAMETER TEORETIS
HASIL PERHITUNGAN SEMIEMPIRIS
Modified Neglect of Diatomic Overlap (MNDO)
Oleh :
Dominika Anny Yanuarti NIM : 038114129
Dipertahankan di hadapan Panitia Penguji Skripsi Fakultas Farmasi
3. Christine Patramurti, M.Si., Apt. ...
4. Dra. Agnes Nora Iska Harnita, M.Si, Apt. ………..
Kupersembahkan karya tulis ini kepada Allah Yang Maha Kuasa, yang
berkenan mengulurkan tangan-Nya dengan penuh rahmat padaku,
Kedua orang tua, ketiga kakakku, orang-orang terbaik dalam hidupku ;
Alm. Alloysius Hormat dan M.Y. Sulastri
Aku hanya berjalan, ya..aku berjalan dalam bimbingan-Mu ya Allah.
Aku berpengharapan, ya…aku berpengharapan dalam Kuasa-Mu ya Tuhan.
Biarlah apa yang telah kukerjakan menjadi persembahan hidupku pada-Mu
vi
PRAKATA
Puji syukur penulis panjatkan kepada Allah Yang Maha Kuasa, karena
berkat rahmat dan kasih-Nya, penulis dapat menyelesaikan skripsi yang berjudul
“Hubungan Kuantitatif Struktur-Aktivitas Senyawa Vinkadiformina dan
Turunannya Sebagai Senyawa Antimalaria Berdasarkan Parameter Teoretis Hasil
Perhitungan Semiempiris Modified Neglect of Diatomic Overlap (MNDO)”.
Skripsi ini merupakan salah satu syarat untuk memperoleh gelar Sarjana Farmasi
(S.Farm) di Fakultas Farmasi Universitas Sanata Dharma.
Penulis ingin mengucapkan terima kasih yang sebesar-besarnya kepada
pihak-pihak yang telah terlibat dalam penyusunan skripsi ini, antara lain :
1. Fakultas Farmasi Universitas Sanata Dharma yang telah memberikan
pendidikan dan pengajaran kepada penulis.
2. Bapak Drs. Iqmal Tahir, M.Si. selaku pembimbing utama yang telah
memberikan bimbingan, kritik dan saran selama penyusunan skripsi ini.
3. Bapak Drs. Mulyono, Apt. selaku pembimbing pembantu yang berkenan
memberikan bimbingan, pengarahan, kritik dan saran, serta diskusi-diskusi
yang sangat memotivasi penulis.
4. Ibu Christine Patramurti, M.Si., Apt. selaku dosen penguji yang berkenan
meluangkan waktu untuk menguji, memberikan kritik dan saran demi
kesempurnaan skripsi ini.
5. Ibu Dra. Agnes Nora Iska Harnita, M.Si., Apt. selaku dosen penguji yang telah
meluangkan waktu untuk menguji, memberikan kritik dan saran yang
memotivasi penulis untuk menyempurnakan skripsi ini.
6. Bapak Yuventius Marsidi dan Ibu Yuliana Sukinem, kedua orang tua yang
telah memberikan doa restu dan dukungan moral bagi penulis, sehingga
penulis dapat menyelesaikan skripsi ini.
7. Alm. Alloyisius Hormat dan M.Y. Sulastri yang telah berkenan menjadi
bagian dalam proses kehidupan penulis dan secara tidak langsung menjadi
bagian dalam proses penyusunan skripsi ini.
8. Agustinus Eko Yudiarto, Bertin Asti Maryani, dan Christa Artiningtyas, ketiga
kakakku yang memberikan dukungan moral dan finansial selama penyusunan
skripsi.
9. Nugraha Adi Hartantyo dan Ariyanto, teman-teman seperjuangan yang
bersama-sama mengalami jatuh bangun selama proses penyusunan skripsi.
Menjalani skripsi bersama kalian adalah pengalaman yang sangat berharga.
10.Patric Gagah Sempati yang selalu meluangkan waktu untuk mendengar keluh
kesahku selama menyusun skripsi. Terima kasih telah berada di sampingku
saat aku membutuhkanmu.
11.Teman-teman kelas C angkatan 2003 yang memberikan dorongan dan
semangat bagi penulis untuk menyelesaikan skripsi. Semoga kebersamaan dan
persahabatan kita tidak akan lekang oleh waktu.
12.Teman-teman di Asrama Putri Canna, terutama Ranti, Diah, Tyas, Shinta, Ina,
dan Wida yang selalu memberikan semangat bagi penulis selama proses
penyusunan skripsi.
13.Teman-teman di Komunitas Lektor Gereja Santo Antonius Kotabaru yang
mendukung penulis secara moral dan spiritual. Terima kasih atas perhatian
viii
dan pengertian yang telah kalian berikan selama penulis menyelesaikan
skripsi.
14.Semua pihak yang tidak dapat penulis sebutkan satu per satu. Terima kasih
atas bantuan dan dukungan yang telah diberikan, sehingga penulis dapat
menyelesaikan skripsi ini.
Dengan segala kerendahan hati, penulis menyadari bahwa skripsi ini
masih jauh dari sempurna, oleh karena itu penulis membuka diri terhadap kritik
dan saran yang bersifat membangun. Penulis berharap, semoga skripsi ini dapat
bermanfaat bagi perkembangan ilmu pengetahuan.
Penulis
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini
tidak memuat karya atau bagian karya orang lain, kecuali yang telah disebutkan
dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Yogyakarta,……….
Penulis
x
DAFTAR ISI
HALAMAN JUDUL... ii
HALAMAN PERSETUJUAN PEMBIMBING ... iii
HALAMAN PENGESAHAN... iv
HALAMAN PERSEMBAHAN ... v
PRAKATA... vi
PERNYATAAN KEASLIAN KARYA ... ix
DAFTAR ISI... x
DAFTAR TABEL... xiii
DAFTAR GAMBAR ... xiv
DAFTAR LAMPIRAN... xv
DAFTAR SINGKATAN DAN ARTI LAMBANG ... xvi
INTISARI... xvii
ABSTRACT... xviii
BAB I PENGANTAR ... 1
A. Latar Belakang ... 1
1. Permasalahan ... 4
2. Keaslian penelitian ... 4
3. Manfaat penelitian... 4
B. Tujuan Penelitian ... 4
BAB II PENELAAHAN PUSTAKA... 6
A. Malaria ... 6
B. Pengelompokan Senyawa Antimalaria ... 9
C. Mekanisme Kerja Senyawa Antimalaria ... 18
D. Vinkadiformina ... 22
E. Hubungan Kuantitatif Struktur dan Aktivitas ... 24
F. Kimia Komputasi ... 26
G. Analisis Statistik ... 30
H. Keterangan Empiris... 34
BAB III METODE PENELITIAN ... 35
A. Jenis dan Rancangan Penelitian ... 35
B. Variabel dan Definisi Variabel... 36
C. Bahan dan Alat Penelitian... 37
1. Bahan penelitian... 37
2. Alat penelitian ... 37
D. Tata Cara Penelitian ... 40
1. Optimasi geometri senyawa vinkadiformina dan turunannya dengan metode MNDO ... 40
a. Penggambaran struktur senyawa... 40
b. Penomoran senyawa ... 41
c. Optimasi geometri... 41
2. Perhitungan sifat kimia fisika molekul senyawa vinkadiformina dan turunannya ... 41
E. Analisa Data dan Hasil... 42
1. Analisis regresi linear multivariat ... 42
2. Analisis kriteria statistik model persamaan matematis ... 42
xii
BAB IV HASIL DAN PEMBAHASAN ... 44
A. Optimasi Geometri Menggunakan Metode Semiempiris MNDO ... 44
B. Perhitungan Sifat Kimia Fisika dengan Metode Semiempiris MNDO... 47
C. Analisis Hasil...49
1. Analisis regresi linear multivariat...49
2. Model persamaan terbaik ... 55
D. Rancangan Senyawa Hipotetik Turunan Vinkadiformina Berdasarkan Model Persamaan Terbaik ... 61
E. Pemilihan dan Rekomendasi Senyawa Turunan Vinkadiformina Untuk Disintesis...62
BAB V KESIMPULAN DAN SARAN... 70
A. Kesimpulan ... 70
B. Saran... 70
DAFTAR PUSTAKA ... 72
LAMPIRAN... 74
BIOGRAFI PENULIS ... 79
DAFTAR TABEL
I. Struktur senyawa vinkadiformina dan turunannya ... 38
II. Data aktivitas (log 1/IC50) senyawa vinkadiformina dan turunannya... 40
III. Deskriptor-deskriptor yang digunakan pada analisis HKSA senyawa
vinkadiformina dan turunannya sebagai antimalaria ... 49
IV. Deskriptor-deskriptor pada model persamaan hasil regresi linear multivariat
metode backward... 50
V. Nilai Fhitung/Ftabel model persamaan hasil regresi linear multivariat metode
backward... 51
VI. Nilai R, adjusted R2, dan SE model persamaan hasil regresi linear
multivariat metode backward... 52
VII. Nilai PRESS model persamaan hasil regresi linear multivariat metode
backward... 54
VIII.Perbandingan nilai log 1/IC50 prediksi model persamaan 2 dengan nilai log
1/IC50 eksperimen ... 56
IX. Model rancangan senyawa turunan vinkadiformina berdasarkan model
persamaan terbaik...66
X. Data aktivitas antimalaria (log 1/IC50) model rancangan senyawa turunan
vinkadiformina...68
XI. Nilai log P model rancangan senyawa turunan vinkadiformina, senyawa
vinkadiformina dan turunannya hasil penelitian hasil penelitian Mustofa, dan
klorokuin...69
xiv
DAFTAR GAMBAR
1. Siklus perkembangan plasmodia malaria... 8
2. Struktur kuinakrin HCl... 12
3. Struktur klorokuin ... 13
4. Struktur primakuin ... 14
5. A) proguanil ; B) sikloguanil ... 15
6. Struktur pirimetamin ... 16
7. A) kuinin ; B) kuinidin... 17
8. A) sulfadoksin ; B) dapson... 17
9. Mekanisme aksi klorokuin pada tingkat molekular ... 21
10.Struktur senyawa vinkadiformina ... 22
11.Daerah sensitif senyawa vinkadiformina dan turunannya hasil penelitian Tahir dkk...24
12.Struktur senyawa vinkadiformina dengan penomeran atom tidak mengikuti kaidah tatanama senyawa dan hanya digunakan untuk penelitian ini saja ... 36
13.Senyawa vinkadiformina sebelum dioptimasi ... 45
14.Senyawa vinkadiformina setelah dioptimasi... 46
15.Grafik ukuran prediksi model persamaan 2...56
16.A) struktur indol ; B) cincin kuinolin...58
17.Daerah sensitif senyawa turunan vinkadiformina ...59
DAFTAR LAMPIRAN
1. Nilai-nilai parameter elektronik hasil perhitungan metode semiempiris MNDO
... 74
2. Nilai-nilai parameter sterik dan hidrofobisitas hasil perhitungan metode
semiempiris MNDO ... 75
3. Nilai-nilai parameter elektronik, sterik, dan hidrofobisitas seri senyawa baru
turunan vinkadiformina...76
4. Model summary hasil perhitungan metode backward menggunakan
SPSS 11.0 for Windows... 77
5. Tabel ANOVA ... 77
6. Koefisien model persamaan 2 ... 78
xvi
DAFTAR SINGKATAN DAN ARTI LAMBANG
1. ADN: asam deoksiribonukleat
2. ARN: asam ribonukleat
3. AM1: Austin Model 1
4. CNDO: Complete Neglect of Differential Overlap
5. EHOMO: Highest Occupied Molecular Orbitals Energy
6. ELUMO: Lowest Unoccupied Molecular Orbitals Energy
7. HKSA: Hubungan Kuantitatif Struktur Aktivitas
8. INDO: Intermediate Neglect of Differential Overlap
9. LFER: Linear Free Energy Relationship (hubungan energi bebas linear)
10. log1/IC50: - log konsentrasi yang dapat menghambat pertumbuhan
plasmodia sebesar 50%
11. log P: koefisien partisi obat dalam fase air dan fase lipid
12. M: Massa
13. MINDO: Modified Intermediate Neglect of Differential Overlap
14. MNDO: Modified Neglect of Diatomic Overlap
15. MR: Refraktifitas Molar
16. m: jumlah deskriptor dalam persamaan
17. NDDO: Neglect of Diatomic Differential Overlap
18. n: jumlah data
19. PM3: Parameterized Model 3
20. PRESS: Predicted Residual Sum of Squares
21. qC: muatan bersih atom C
22. qN: muatan bersih atom N
23. QSAR: Quantitative Structure Activity Relationship 24. R: koefisien korelasi
25. R2: koefisien determinasi
26. SA: Surface Area (luas permukaan)
27. SE: Standard Error
28. Sig: Signifikansi
29. V: Volume Molekular
30. ZINDO: Zerner Intermediate Neglect of Differential Overlap
31. ΔE: selisih antara ELUMO dan EHOMO
32. µ: Momen Dipol
33. ∂: Polarisabilitas Molekular
34. 2D: dua dimensi
35. 3D: tiga dimensi
INTISARI
Malaria merupakan salah satu penyakit utama yang menjadi penyebab kematian pada daerah beriklim tropis, salah satunya Indonesia. Peningkatan morbiditas dan mortalitas akibat malaria disebabkan oleh resistensi plasmodia
(utamanya P. falciparum) terhadap antimalaria yang umum digunakan.
Dibutuhkan antimalaria kelas baru yang dapat mengatasi permasalahan ini. Pengembangan desain senyawa antimalaria baru dapat dilakukan dengan metode analisis hubungan kuantitatif struktur-aktivitas. Penelitian ini bertujuan untuk mengetahui hubungan kuantitatif antara struktur dan aktivitas senyawa
vinkadiformina dan turunannya berdasarkan log 1/IC50. IC50 merupakan
konsentrasi yang dapat menghambat pertumbuhan plasmodia malaria sebanyak 50%.
Penelitian ini menggunakan rancangan eksperimental kuasi. Sebagai variabel bebas digunakan 17 deskriptor teoretis (elektronik, sterik, dan hidrofobisitas). Sebagai variabel tergantung digunakan log 1/IC50. Data deskriptor diperoleh dengan perhitungan semiempiris MNDO menggunakan program
komputer HyperChem Pro ver.6.0. Data diolah secara statistik menggunakan
analisis regresi multivariat metode backward dengan program SPSS 11.0 for Windows.
Analisis statistik menghasilkan 4 model persamaan dan ditunjukkan bahwa model 2 memenuhi kriteria statistik dan dapat dipilih sebagai model persamaan terbaik, dengan persamaan :
log (1/IC50) = 28,8758 + (22,7560qC1) + (14,2669qC2) + (33,7110qC3) +
(-27,2900qN) + (-10,0545qC7) + (-1,0678qC8) + (79,9843qC9)
+ ( 0,5394ΔE) + (-0,0067V) + (-0,5904 MR) + (0,7226∂) + (0,0285 M) + (0,8408 log P)
Model persamaan tersebut dapat digunakan untuk memprediksikan aktivitas antimalaria senyawa-senyawa baru turunan vinkadiformina. Berdasarkan model persamaan terbaik diperoleh 15 senyawa baru turunan vinkadiformina yang memiliki aktivitas antimalaria.
Kata kunci : HKSA, turunan vinkadiformina, MNDO, regresi linier
multivariat
xviii
ABSTRACT
Malaria is one of the primary disease that causes deathness in many tropical countries, such as Indonesia. The increasing of morbidity and mortality by malaria is caused by the resistency of plasmodium (primarily P. falciparum) to antimalarial that commonly used. Antimalarial from a new class is needed. Design of antimalarial from new class could be made by using quantitative structure-activity relationship analysis. This research is aimed to know the quantitative relationship between structure and activity of vincadifformine and its derivatives based on log 1/IC50. IC50 is concentration that can inhibit 50% of the malarial plasmodia’s growth.
This research use a quasi experimental design. Seventeen descriptors were used as dependent variabel (electronic, steric, and hydrophobicity). Log
1/IC50 is used as independent variabel. Descriptor data is obtained by
semiempirical MNDO calculation using HyperChem Pro ver.6.0 computer programme. Data was analysed statisticaly by multivariate linear regression backward method by using SPSS 11.0 for Windows.
Statistic analysis gave 4 equation models and the second model showned to fulfil the statistic criteria. The second model could be selected as the best equation model.
log (1/IC50) = 28.8758 + (22.7560qC1) + (14.2669qC2) + (33.7110qC3) +
(-27.2900qN) + (-10.0545qC7) + (-1.0678qC8) + (79.9843qC9)
+ ( 0.5394ΔE) + (-0.0067V) + (-0.5904 MR) + (0.7226∂) + (0.0285 M) + (0.8408 log P)
This model can be used to predict the activity of new vincadifformine’s derivatives. There are 15 vincadifformine’s derivatives which could give antimalarial activity based on the best equation model.
Keyword : QSAR, vincadifformine’s derivatives, MNDO, multivariate linier
regression
BAB I
PENGANTAR
A. Latar Belakang Penelitian
Malaria merupakan penyakit utama yang menjadi penyebab kematian
pada daerah beriklim tropis. Di Indonesia beban terbesar dari penyakit malaria ada
di provinsi-provinsi bagian timur yaitu Papua, Maluku, dan Gorontalo yang
merupakan daerah endemik penyakit malaria. Menurut Survei Kesehatan Rumah
Tangga tahun 2001, diperkirakan angka kematian spesifik akibat malaria di
Indonesia adalah 11 per 100.000 untuk laki-laki dan 8 per 100.000 untuk
perempuan (Anonim, 2004). Penyebab utama meningkatnya morbiditas dan
mortalitas akibat malaria adalah peningkatan resistensi parasit malaria terhadap
antimalaria yang umum digunakan, misalnya klorokuin. Kondisi terparah dengan
tingkat resistensi yang tinggi terhadap klorokuin terjadi pada malaria yang
disebabkan oleh Plasmodium falciparum (Rosenthal, 2003).
Peningkatan resistensi parasit terhadap antimalaria memunculkan
kebutuhan akan antimalaria dari kelas baru. Vinkadiformina adalah suatu senyawa
yang dikenal memiliki aktivitas hipotensif (Duke, 1992), namun Mustofa (2001)
telah berhasil menguji aktivitasnya sebagai antimalaria. Mustofa telah mensintesis
16 senyawa vinkadiformina dan turunannya dan menguji aktivitas antimalaria
senyawa-senyawa tersebut terhadap P. falciparum yang tergolong resisten
terhadap klorokuin yaitu FcM29-Kamerun dan P. falciparum yang sensitif
terhadap klorokuin yaitu sel Nigerian (Tahir dkk, 2005). Hasil sintesis dan
2
pengujian aktivitas antimalaria vinkadiformina, membuka jalan bagi
pengembangan dan desain senyawa vinkadiformina dan turunannya sebagai
antimalaria baru.
Pengembangan dan desain senyawa antimalaria baru dapat dilakukan
dengan berbagai metode, salah satunya dengan analisis Hubungan Kuantitatif
Struktur-Aktivitas (HKSA). Metode ini dapat mengurangi faktor trial and error
dalam sintesis obat baru. Analisis HKSA vinkadiformina sebagai antimalaria
pernah dilakukan oleh Tahir dkk (2005). Dalam penelitiannya, Tahir dkk
menganalisis HKSA 16 senyawa vinkadiformina dan turunannya yang telah diuji
aktivitasnya terhadap P. falciparum yang sensitif terhadap klorokuin (sel
Nigerian), oleh Mustofa. Dengan metode semiempiris Austin Model 1 (AM1),
Tahir dkk berhasil memperoleh model persamaan terbaik yang dapat
menggambarkan hubungan kuantitatif struktur senyawa vinkadiformina dan
turunannya dengan aktivitasnya sebagai antimalaria. Model persamaan yang
diperoleh oleh Tahir dkk memperlihatkan bahwa parameter teoretis berupa
parameter elektronik dan sterik memberikan pengaruh yang besar terhadap
aktivitas antimalaria (log 1/IC50).
Dalam penelitian ini akan dilakukan analisis HKSA 16 senyawa
vinkadiformina dan turunannya hasil sintesis Mustofa dengan menggunakan
metode semiempiris yang berbeda dengan metode yang digunakan oleh Tahir dkk,
yaitu metode semiempiris Modified Neglect of Diatomic Overlap (MNDO).
Pemilihan metode semiempiris MNDO didasarkan pada kecepatan metode ini
semiempiris yang lain seperti AM1 dan Parameterized Model 3 (PM3). Dalam
perancangan senyawa baru, dimungkinkan desain senyawa dalam jumlah yang
banyak. Oleh karena itu, penggunaan metode yang cepat dalam perhitungan
menjadi hal yang perlu dipertimbangkan. Metode semiempiris MNDO merupakan
metode yang dapat melakukan perhitungan yang cepat dan kasar. Namun
demikian, belum tentu perhitungan yang cepat dan kasar tersebut tidak dapat
menghasilkan model persamaan terbaik yang mampu menggambarkan hubungan
kuantitatif struktur-aktivitas senyawa vinkadiformina dan turunannya sebagai
senyawa antimalaria. Belum tentu pula, rancangan senyawa berdasarkan model
persamaan terbaik dari perhitungan metode semiempiris MNDO menghasilkan
aktivitas antimalaria yang lebih rendah daripada rancangan senyawa yang
didasarkan pada model persamaan terbaik hasil perhitungan metode semiempiris
AM1 atau PM3. Dalam penelitian ini diharapkan perhitungan dengan
menggunakan metode semiempiris MNDO dapat memberikan model persamaan
terbaik yang menggambarkan hubungan kuantitatif struktur senyawa
vinkadiformina dan turunannya melalui parameter teoretis yang meliputi
parameter elektronik, sterik, dan hidrofobisitas, terhadap aktivitasnya sebagai
antimalaria. Aktivitas antimalaria didasarkan pada log 1/IC50. IC50 merupakan
4
1. Permasalahan
Dari latar belakang di atas muncul permasalahan sebagai berikut:
1. Bagaimana hubungan kuantitatif antara struktur dan aktivitas senyawa
vinkadiformina dan turunannya sebagai senyawa antimalaria berdasarkan
parameter teoretis hasil perhitungan semiempiris MNDO?
2. Bagaimana struktur senyawa hipotetik turunan vinkadiformina yang memiliki
aktivitas antimalaria berdasarkan model persamaan terbaik?
2. Keaslian penelitian
Telah dilakukan penelitian mengenai hubungan kuantitatif
struktur-aktivitas senyawa vinkadiformina dan turunannya sebagai antimalaria oleh Tahir
dkk (2005). Dalam penelitian tersebut digunakan 16 senyawa vinkadiformina dan
turunannya beserta data log 1/IC50 hasil penelitian Mustofa (2001). Tahir dkk
(2005) menggunakan metode semiempiris AM1 dalam menghitung parameter
teoretis struktur senyawa vinkadiformina dan turunannya hingga ditemukan model
persamaan terbaik yang menggambarkan HKSA senyawa vinkadiformina dan
turunannya sebagai antimalaria. Penelitian ini menggunakan 16 senyawa yang
digunakan Tahir dkk, namun metode yang digunakan berbeda yaitu metode
semiempiris MNDO.
3. Manfaat penelitian
a. Manfaat teoretis
Penelitian ini diharapkan dapat memberikan informasi mengenai
hubungan antara struktur dan aktivitas senyawa vinkadiformina dan turunannya
b. Manfaat praktis
Penelitian ini diharapkan dapat menjadi acuan dalam sintesis senyawa
baru turunan vinkadiformina dan pengujian aktivitas antimalaria senyawa tersebut
baik secara in vitro maupun in vivo.
B. Tujuan Penelitian
1. Penelitian ini bertujuan untuk menggambarkan hubungan kuantitatif antara
struktur dan aktivitas senyawa vinkadiformina dan turunannya sebagai
senyawa antimalaria berdasarkan parameter teoretis hasil perhitungan
semiempiris MNDO.
2. Penelitian ini juga bertujuan untuk menggambarkan struktur hipotetik
senyawa turunan vinkadiformina yang memiliki aktivitas antimalaria
BAB II
PENELAAHAN PUSTAKA
A. Malaria
Malaria merupakan suatu penyakit plasmodia yang disebabkan oleh
protozoa, yaitu Plasmodium sp., yang masuk ke dalam tubuh tuan rumah (host)
melalui gigitan nyamuk Anopheles betina (Siswandono dan Soekardjo, 1995).
Pada manusia, spesies yang menyebabkan infeksi adalah P. falciparum, P.vivax,
P. malariae, dan P. ovale. Malaria tersian, yang diakibatkan oleh P. vivax adalah
bentuk penyakit malaria yang paling umum. Bentuk malaria tersian yang paling
berat, disebut tersian ganas, disebabkan oleh P. falciparum. Serangan oleh
spesies-spesies ini lebih jarang dibandingkan dengan P. vivax. Malaria quartan,
dengan tingkat keganasan menengah, disebabkan oleh serangan P. malariae.
Malaria macam ini lebih jarang terjadi daripada tersian ganas. P. ovale
mengakibatkan bentuk penyakit malaria yang jarang, yang disebut malaria tersian
ovale. Malaria macam ini dalam banyak hal mirip dengan malaria tersian atau
malaria P. vivax (Kier dan Roche, 1996).
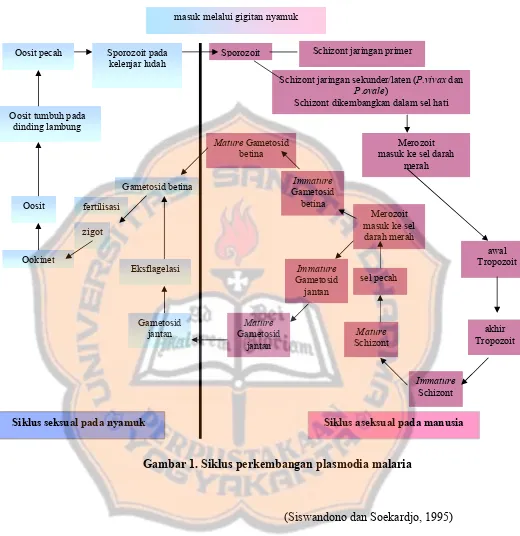
Siklus perkembangan plasmodia malaria dalam nyamuk Anopheles dan
tubuh manusia serta tempat kerja obat antimalaria dapat dilihat pada gambar 1.
Saat nyamuk Anopheles betina menggigit manusia, nyamuk mengeluarkan
sporozoit ke dalam pembuluh darah kapiler. Sporozoit kemudian dibawa oleh
darah ke dalam hati untuk bermultiplikasi dan membentuk schizont jaringan. Ini
adalah tahap pre-eritrositik atau jaringan primer. Setelah 5-16 hari, schizont pecah
sambil melepaskan ribuan merozoit yang menginfeksi sel darah merah untuk
membentuk schizont dan memulai tahap eritrositik (DiPalma, 1990 ; Neal, 1997).
Pada infeksi yang disebabkan oleh P. vivax dan P. ovale (bukan P. falciparum),
beberapa schizont dalam hati membentuk schizont jaringan sekunder dan berada
dalam keadaan dorman (disebut hipnozoit). Jaringan sekunder akan pecah
beberapa bulan kemudian, sehingga menyebabkan kambuhnya penyakit (Neal,
1997). Pada tahap terbentuknya schizont, pasien tidak mengalami gejala. Keadaan
ini bertahan hingga schizont pecah, dan melepaskan kembali merozoit beserta
pirogen ke dalam darah. Secara klinis, tahap ini ditandai dengan gejala demam,
kemudian menggigil. Gejala demam terjadi karena adanya pirogen yang
dilepaskan ke dalam darah, sedangkan gejala menggigil terjadi karena tubuh
berusaha menurunkan suhu tubuh yang tinggi. Beberapa merozoit yang kembali
dilepaskan, akan menginfeksi sel darah merah untuk membentuk schizont,
sedangkan beberapa merozoit yang lain akan mengalami perkembangan seksual
menjadi gametosit jantan dan gametosit betina (DiPalma, 1990). Bentuk gametosit
yang terhisap oleh nyamuk Anopheles betina, mengalami pertumbuhan menjadi
zigot dalam lambung nyamuk. Zigot berkembang membentuk oosit (strukturnya
bulat dan berada di dinding luar lambung). Oosit kemudian berkembang menjadi
sporozoit dan dilepaskan ke dalam rongga perut nyamuk, lalu berpindah ke
kelenjar ludah. Dari kelenjar ludah, sporozoit siap dipindahkan dan menginfeksi
manusia yang digigit oleh nyamuk Anopheles betina (siklus berjalan kembali)
8
masuk melalui gigitan nyamuk
awal Tropozoit
akhir Tropozoit
Oosit pecah Sporozoit pada
kelenjar ludah
Sporozoit Schizont jaringan primer
Schizont jaringan sekunder/laten (P.vivax dan P.ovale)
Schizont dikembangkan dalam sel hati Oosit tumbuh pada
dinding lambung masuk ke sel darah
merah
Siklus seksual pada nyamuk
Mature Gametosid
jantan
Siklus aseksual pada manusia
Gambar 1. Siklus perkembangan plasmodia malaria
B. Pengelompokan Senyawa Antimalaria
Berdasarkan perkembangan dan siklus kehidupan plasmodia yang
dipengaruhi dan indikasi klinis antimalaria tersebut, maka antimalaria dapat
dikelompokkan sebagai berikut :
1. antimalaria untuk pencegahan kausal
Antimalaria kelompok ini menghancurkan bentuk jaringan primer
plasmodia dan merozoit di hati, mulai dari tahap infeksi eritrositik, kemudian
mencegah invasi eritrosit dan penyebaran infeksi ke nyamuk Anopheles. Contoh
antimalaria kelompok ini adalah klorguanid, pirimetamin, dan primakuin
(Siswandono dan Soekardjo, 1995). Klorguanid atau nama lainnya adalah
proguanil, merupakan prototipe dari kelompok ini. Klorguanid telah digunakan
secara luas untuk pencegahan kausal malaria yang disebabkan oleh P. falciparum.
Antimalaria ini mengalami masalah resistensi, namun tetap memberikan proteksi
jika dikombinasikan dengan obat lain. Meskipun primakuin juga memiliki
aktivitas terhadap P. falciparum, antimalaria ini memiliki potensi toksik yang
tinggi dan digunakan untuk aplikasi klinis yang lain (Tracy dan Webster, 2001).
2. antimalaria untuk mencegah kekambuhan
Antimalaria ini bekerja pada bentuk schizont di jaringan laten, jaringan
sekunder atau hipnozoit dari P. vivax dan P. ovale di sel hati. Contoh antimalaria
kelompok ini adalah primakuin dan pirimetamin (Siswandono dan Soekardjo,
1995). Kelompok antimalaria ini digunakan untuk pencegahan terminal dan untuk
penyembuhan radikal dari infeksi malaria kambuhan. Primakuin adalah
10
menyembuhkan infeksi eritrositik dari jaringan sekunder plasmodia (Tracy dan
Webster, 2001).
3. antimalaria untuk pencegahan klinis dan penyembuhan supresif
Menurut Korolkovas dan Burckhalter (1976), antimalaria dapat
memberikan efek sebagai supresi atau pencegahan klinis, yaitu pencegahan dari
gejala klinis dengan bekerja pada bentuk aseksual plasmodia dalam darah. Kerja
ini dapat bersifat sementara atau permanen. Antimalaria kelompok ini bekerja
terhadap merozoit pada fase eritrositik aseksual dari plasmodia malaria dan
mengganggu schizogoni eritrositik ke bawah, sehingga serangan klinis tidak
terjadi. Antimalaria ini juga digunakan dalam terapi penyembuhan supresif untuk
eliminasi plasmodia secara lengkap. Kecuali primakuin, hampir semua antimalaria
yang digunakan secara klinis dikembangkan aktivitasnya terhadap fase aseksual
plasmodia. Berdasarkan masa kerjanya kelompok antimalaria ini dibagi menjadi
dua, yaitu :
a. schizontosida yang bekerja secara cepat
Contoh : amodiakuin, artemisinin, klorokuin, kuinin, kuinidin, meflokuin, dan
atovaquon
b. schizontosida yang bekerja secara lambat
Contoh : pirimetamin, klorguanid, sikloguanil pamoat, sulfonamida, dan
sulfon
4. gametositosida
Antimalaria kelompok ini menghancurkan bentuk eritrositik seksual
(gametosit) dari plasmodia malaria sehingga mencegah penyebaran plasmodia ke
nyamuk Anopheles (Siswandono dan Soekardjo, 1995). Klorokuin dan kuinin
memiliki aktivitas gametosidal terhadap P. vivax, P. ovale, dan P. malariae,
primakuin aktif terhadap gametosit dari P. falciparum (Siswandono dan
Soekardjo, 1995; Tracy dan Webster, 2001).
5. sporozoitosida
Antimalaria kelompok ini mampu membunuh sporozoit segera setelah
masuk dalam darah sesudah gigitan nyamuk. Waktu antimalaria ini untuk bekerja
sangat singkat oleh karena sporozoit secara cepat masuk ke sel hati sehingga
banyak antimalaria kurang efektif terhadap bentuk sporozoit tersebut. Contoh
antimalaria kelompok ini adalah klorguanid, pirimetamin, dan primakuin
(Siswandono dan Soekardjo, 1995).
6. sporontosida
Antimalaria kelompok ini bekerja pada tubuh nyamuk malaria yang
menginfeksi tuan rumah yaitu dengan mencegah pembentukan oosit dan
sporozoit. Contoh : pirimetamin, klorguanid, dan primakuin (Siswandono dan
12
Berdasarkan struktur kimianya, antimalaria dibagi menjadi 8 kelompok,
yaitu turunan 9-aminoakridin, 4-aminokuinolin, 8-aminokuinolin, biguanida,
diaminopiridin, kuinolinometanol, sulfonamida, dan sulfon.
1. Turunan 9-aminoakridin
Contoh turunan 9-aminoakridin adalah kuinakrin-HCl yang bekerja
sebagai schizontosida eritrositik, sekarang jarang digunakan sebagai antimalaria
karena tersedia obat yang lebih aktif dengan toksisitas lebih rendah (Siswandono
dan Soekardjo, 1995). Kuinakrin bersifat tumorigenik dan mutagenik dan juga
telah digunakan sebagai obat sklerosis. Kuinakrin merupakan suatu pewarna
akridin, sehingga senyawa ini dapat menyebabkan diskolorisasi kuning pada kulit
dan urin (Block, 2004).
N Cl
Gambar 2. Struktur kuinakrin HCl
2. 4-aminokuinolin
Turunan 4-aminokuinolin mempunyai aktivitas antimalaria yang lebih
tinggi dibanding kuinin atau 9-aminoakridin. Toksisitasnya relatif rendah
(Siswandono dan Soekardjo, 1995). Secara umum, klorokuin dan 4-aminokuinolin
yang lain, tidak efektif terhadap plasmodia eksoeritrosit. Klorokuin tidak dapat
mencegah kekambuhan pada malaria yang disebabkan oleh P. vivax dan P. ovale
Dari turunan 4-aminokuinolin, klorokuin menunjukkan aktivitas yang
optimal (Siswandono dan Soekardjo, 1995). Klorokuin memiliki struktur yang
mirip turunan 8-aminokuinolin yang sudah tidak digunakan lagi, yaitu pamakuin
dan pentakuin. Klorokuin memiliki rantai samping yang sama seperti kuinakrin,
tetapi berbeda pada cincin kuinolin dan residu metoksi yang tidak dimiliki oleh
kuinakrin. Gugus amin tersier pada cincin kuinolin sangat penting berperan dalam
aktivitasnya sebagai antimalaria (Siswandono dan Soekardjo, 1995). Atom klorin
pada posisi 7 dari cincin kuinolin juga memiliki pengaruh yang sangat besar
terhadap aktivitas antimalaria yang ditimbulkan, baik pada manusia maupun avian
(Tracy dan Webster, 2001).
N
Gambar 3. Struktur klorokuin
3. 8-aminokuinolin
Turunan 8-aminokuinolin aktif terhadap bentuk eksoeritrositik
plasmodia malaria yang disebabkan oleh P. vivax dan P. malariae. Mempunyai
aktivitas gametositosida, tetapi tidak aktif terhadap bentuk plasmodia eritrositik.
Turunan ini menimbulkan toksisitas lebih besar dibanding turunan
4-aminokuinolin (Siswandono dan Soekardjo, 1995). Primakuin adalah turunan
14
tidak digunakan sebagai profilaksis. Spektrum aktivitasnya paling sempit bila
dibandingkan dengan antimalaria yang lain (Block, 2004).
Pada struktur turunan 8-aminokuinolin, rantai samping yang terdiri dari
4 atom C dan amin aromatik yang merupakan amin sekunder memberikan
aktivitas antimalaria yang optimal. Gugus 6-metoksi mempunyai aktivitas optimal
meskipun batas keamanannya rendah, dan kemungkinan dapat diganti dengan
atom hidrogen atau gugus hidroksi (Siswandono dan Soekardjo, 1995).
N
Gambar 4. Struktur primakuin
4. Biguanida
Turunan biguanida merupakan schizontosida eksoeritrositik dan
eritrositik terhadap P. falciparum dan P. vivax. Toksisitasnya relatif ringan
(Siswandono dan Soekardjo, 1995). Turunan biguanida mempunyai mekanisme
kerja yang sama dengan pirimidin. Turunan ini tidak aktif, dan baru menjadi aktif
setelah tersiklisasi pada saat metabolisme menjadi suatu turunan dihidro-s-triazin
yang mirip dengan pirimetamin dan bagian pteridin senyawa asam folat.
Transformasi hayati ini digambarkan dengan proguanil. Proguanil akan
dimetabolisme menjadi sikloguanil dan metabolit inilah yang aktif sebagai
antimalaria. Sikloguanil sendiri tersedia dalam bentuk garam pamoat. Senyawa
N N
bentuk eksoeritrositik dan eritrositik P. falciparum dan P. vivax. Resistensi
terhadap senyawa ini sering terjadi (Kier dan Roche, 1996).
A B
Gambar 5. A) proguanil ; B) sikloguanil
5. Diaminopirimidin
Antimalaria yang merupakan turunan dari diaminopirimidin adalah
pirimetamin dan trimetoprim. Pirimetamin digunakan sebagai pencegahan malaria
(Korolkovas dan Burckhalter, 1976). Pirimetamin merupakan schizontosida darah
lepas lambat yang memiliki efek in vivo yang mirip dengan proguanil.
Pirimetamin memiliki potensi antimalaria yang lebih besar karena langsung
bekerja pada plasmodia, dan waktu paruhnya lebih lama daripada sikloguanil,
bentuk aktif proguanil. Berbeda dengan proguanil, pirimetamin tidak
menunjukkan efektivitas yang berarti terhadap bentuk hepatik dari P. falciparum.
Pada dosis terapetis, pirimetamin tidak dapat melakukan eradikasi terhadap
jaringan sekunder P. vivax atau gametosit dari spesies plasmodia malaria (Tracy
dan Webster, 2001).
16
6. Turunan kuinolinometanol
Turunan kuinolinometanol terdapat pada tanaman Chinchona Sp.,
terutama pada bagian kulit kayu atau korteks. Korteks kina yang diperdagangkan
mengandung alkaloid kuinin 5%, kuinidin 0,1%, sinkonin 0,3%, dan sinkonidin
0,4% (Siswandono dan Soekardjo, 1995). Bagian kuinolinometanol menjadi
penting dalam obat-obat sintetik. Turunan kuinolinometanol bekerja pada
merozoit eritrositik. Senyawa-senyawa ini tidak menyembuhkan secara tuntas,
tetapi mengurangi gejala. Kuinin digunakan pada pengobatan malaria yang
plasmodiumnya telah resisten terhadap zat-zat lain, misalnya klorokuin (Kier dan
Roche, 1996). Stereoisomer kuinin yaitu kuinidin, memiliki potensi yang lebih
besar sebagai antimalaria, tetapi kuinidin juga lebih toksik. Kuinin bersifat
mematikan terhadap semua bentuk schizont plasmodium dan gametosit P. vivax
dan P. malariae tetapi tidak untuk gametosit P. falciparum. Sekarang, spektrum
aktivitas kuinin terlalu sempit untuk penggunaan pencegahan malaria (Block,
2004).
Kuinin memiliki cincin kuinolin yang dihubungkan dengan cincin
kuinuklidin melalui jembatan alkohol. Cincin kuinolin mengandung gugus
metoksi, sedangkan cincin kuinuklidin mengikat gugus vinil. Kuinidin memiliki
struktur yang serupa dengan kuinin. Perbedaannya dengan kuinin terletak pada
N
7. Turunan sulfonamida dan sulfon
Turunan ini jarang digunakan dalam bentuk tunggal sebagai antimalaria,
biasanya dikombinasi dengan pirimetamin dan digunakan untuk pengobatan
infeksi P. falciparum yang sudah kebal terhadap klorokuin. Contoh turunan
sulfonamida yang dapat digunakan sebagai antimalaria adalah sulfadoksin,
sulfametoksipiridazin, sulfametopirazin, sulfisoksazol. Contoh sulfon yang
digunakan sebagai antimalaria adalah asedapson dan dapson (Siswandono dan
Soekardjo, 1995).
A B
18
C. Mekanisme Kerja Senyawa Antimalaria
Beberapa mekanisme aksi antimalaria telah diusulkan. Dahulu postulat
Schonhofer merupakan mekanisme aksi malaria yang telah diterima secara luas.
Schonhofer mengatakan bahwa aktivitas antimalaria membutuhkan struktur
kuinolin yang mudah dioksidasi menjadi bentuk kuinoid. Hipotesis ini sekarang
tidak digunakan lagi sejalan dengan penelitian bahwa 5,6-kuinon ternyata tidak
terbukti sebagai bentuk aktif antimalaria aminokuinolin (Korolkovas dan
Burckhalter, 1976).
Antimalaria memiliki berbagai mekanisme aksi. Pada tingkat molekular,
antimalaria beraksi dengan menghambat enzim yang terlibat dalam biosintesis
prekursor asam deoksiribonuklease (ADN) atau membentuk kompleks molekular
dengan ADN, sehingga memblok sintesis ADN dan asam ribonuklease (ARN)
plasmodia dengan menghambat polimerasi ADN dan ARN (Korolkovas dan
Burckhalter, 1976).
Turunan 9-aminoakridin, 4-aminokuinolin, dan kuinolinometanol
menunjukkan efek schizontisid yang cepat dengan dua mekanisme. Mekanisme
kerja ketiga turunan ini melibatkan lisosom (vakuola makanan) plasmodia yang
terdapat dalam sel darah merah (Block, 2004). Bentuk aseksual plasmodia malaria
dapat tumbuh dalam sel darah merah dengan mencerna hemoglobin dalam
vakuola makanan yang bersuasana asam. Hemoglobin merupakan nukleoprotein
bagi plasmodia. Proses pencernaan hemoglobin menghasilkan radikal bebas dan
heme (ferriprotoporphyrin IX) sebagai produk yang sangat reaktif. Dalam proses
kemudian berpolimerisasi menjadi pigmen malaria yang inaktif dan tidak larut.
Pigmen ini dinamakan hemozoin. Turunan 9-aminoakridin, 4-aminokuinolin, dan
kuinolinometanol merupakan schizontosida darah yang bertindak sebagai basa
lemah yang terkonsentrasi dalam vakuola makanan plasmodia yang bersuasana
asam (Tracy dan Webster, 2001). Senyawa-senyawa ini kemudian mengalami
protonasi, meningkatkan pH intravakuolar, dan terjebak di dalam vakuola
makanan karena pori-pori membran vakuola juga bermuatan positif. Kondisi ini
mempertahankan keberadaan senyawa-senyawa turunan 9-aminoakridin,
4-aminokuinolin, dan kuinolinometanol dalam hemoglobin penderita (Block, 2004).
Dengan keberadaan senyawa-senyawa tersebut dalam hemoglobin penderita,
maka aktivitas peroksidatif heme akan terhambat dan polimerisasi nonenzimatik
heme menjadi hemozoin terganggu (Tracy dan Webster, 2001). Heme yang masih
reaktif akan merusak membran plasmodia dan/ atau sel darah merah secara
oksidatif, sehingga membran mengalami lisis (Block, 2004).
Mekanisme kerja kedua dari senyawa turunan 9-aminoakridin,
4-aminokuinolin, dan kuinolinometanol melibatkan sistem cincin datar yang
dimiliki oleh senyawa-senyawa tersebut. Cincin datar yang dimiliki oleh turunan
4-aminokuinolin dan kuinolinometanol adalah cincin kuinolin, sedangkan cincin
datar yang dimiliki oleh turunan 9-aminoakridin adalah cincin akridin. Sistem
cincin datar memungkinkan senyawa-senyawa tersebut dapat berinterkalasi di
antara pasangan basa dobel heliks ADN. Perhitungan orbital molekul
menunjukkan bahwa senyawa-senyawa tersebut, terutama dalam bentuk
20
(Lowest Unoccupied Molecular Orbital) rendah (antara 0 dan -0,5β), sedang
pasangan basa guanin dan sitosin mempunyai nilai energi HOMO (Highest
Occupied Molecular Orbital) tinggi (+0,487β). Kondisi ini memungkinkan
terjadinya kompleks transfer muatan antara cincin datar senyawa-senyawa
tersebut dengan pasangan basa guanin dan sitosin, sehingga terbentuk kompleks
obat-ADN. Kompleks obat-ADN diperkuat dengan adanya ikatan rantai samping
senyawa-senyawa tersebut dengan gugus fosfat pada salah satu helaian dobel
heliks ADN. Rantai samping kuinolinometanol yang berikatan dengan gugus
fosfat adalah cincin kuinuklidin, sedangkan rantai samping 9-aminoakridin dan
4-aminokuinolin yang berikatan dengan gugus fosfat adalah atom nitrogen
terprotonasi. Selain ikatan rantai samping dengan gugus fosfat, kompleks
obat-ADN juga diperkuat dengan adanya ikatan hidrogen dengan molekul basa purin
yaitu adenin (DiPalma, 1990). Dengan terbentuknya kompleks obat-ADN, maka
transkripsi dan translasi ADN menjadi ARN akan terhambat. Hal ini akan
berpengaruh terhadap sintesis ADN dan ARN (DiPalma, 1990). Interkalasi dan
ikatan ionik yang terjadi antara klorokuin (senyawa turunan 4-aminokuinolin)
dengan ADN diperlihatkan pada gambar 13.
Turunan 8-aminokuinolin yaitu primakuin bekerja dengan mengganggu
mitokondria plasmodia (Block, 2004). Primakuin mengganggu transpor elektron,
sehingga menyebabkan perusakan oksidatif pada sistem enzim mitokondrial.
Proses ini mengakibatkan mitokondria plasmodia menggembung dan mengalami
vakuolisasi. Dalam hal ini mitokondria penderita tidak terganggu. Primakuin juga
mengalami pematangan (DiPalma, 1990). Primakuin dapat diubah menjadi
elektrofil yang bekerja sebagai mediator oksidasi-reduksi (Tracy dan Webster,
2001). Hal ini menyebabkan perusakan oksidatif pada elektron asam nukleat
dalam gametosit. Dengan demikian primakuin dapat digunakan untuk mencegah
penyebaran malaria (DiPalma, 1990). Selain bekerja dengan mengganggu transpor
elektron, primakuin juga bekerja dengan berinterkalasi di antara pasangan basa
ADN plasmodia, sama seperti turunan 9-aminoakridin, 4-aminokuinolin, dan
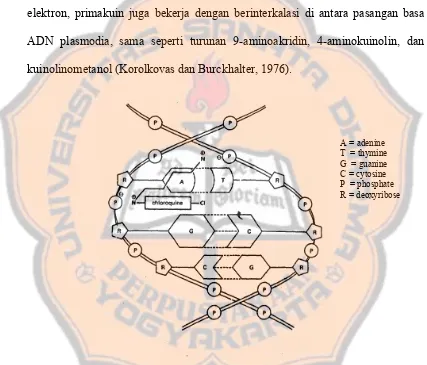
kuinolinometanol (Korolkovas dan Burckhalter, 1976).
A = adenine T = thymine G = guanine C = cytosine P = phosphate R = deoxyribose
Gambar 9. Mekanisme aksi klorokuin pada tingkat molekular
(Korolkovas dan Burckhalter,1976)
Turunan biguanida dan diaminopirimidin, mempunyai aktivitas
antimalaria karena menghambat secara selektif enzim dihidrofolat reduktase yang
22
plasmodia. Penghambatan ini mempengaruhi biosintesis plasmodia terutama
pembentukan basa purin, pirimidin, dan ADN. Meskipun turunan ini tidak bekerja
secara selektif terhadap enzim plasmodia, tetapi dapat mengikat enzim
dihidrofolat reduktase lebih kuat dibanding isoenzim pada penderita. Efek
pemblokan ini tidak berbahaya bagi penderita karena asam folinat yang
diperlukan dipasok dari luar melalui makanan (Siswandono dan Soekardjo, 1995).
Turunan sulfonamida dan sulfon dapat menghambat secara selektif
enzim dihidropteroat sintetase, yang mengkatalisis kondensasi ester pirofosfat dari
2-amino-4-okso-6-hidroksimetildihidropteridin dengan asam p-aminobenzoat
dengan asam dihidropteroat. Hambatan ini menyebabkan kematian plasmodia
(Siswandono dan Soekardjo, 1995).
D. Vinkadiformina
N H
N
O O
Gambar 10. Struktur senyawa vinkadiformina
Vinkadiformina adalah salah satu indol alkaloid yang terkandung dalam
tanaman Aspidosperma pyrifolium dan A. megalocarpon yang merupakan
tanaman tradisional Amerika dan digunakan sebagai antimalaria (Mustofa, 2001).
hipoglikemik, dan simpatolitik (Anonim, 1996). Kuehne dkk (1978) dalam jurnal
mengenai studi biomimetik sintesis alkaloid memaparkan bahwa vinkadiformina
dapat disintesis dari tetrahydro-β-carboline melalui secodine intermediate.
Penelitian terhadap senyawa indol alkaloid dari tanaman bergenus
Aspidosperma pernah dilakukan oleh Mitaine-Offer dkk (2002). Dalam penelitian
tersebut Mitaine-Offer dkk mengkombinasikan senyawa indol alkaloid
berkerangka dasar aspidospermane (dari A. pyrifolium dan A. Megalocarpon)
dengan klorokuin, kemudian menguji aktivitas antimalarianya terhadap P.
falciparum yang sensitif klorokuin dan P. falciparum yang resisten klorokuin.
Dari penelitian tersebut diperoleh hasil yang menyatakan bahwa terdapat
sinergisme dari kedua senyawa yang dikombinasikan, sehingga dihasilkan efek
antimalaria yang merupakan kumulasi dari aktivitas antimalaria senyawa yang
dikombinasi.
Pada tahun 2001, Mustofa telah berhasil mensintesis 16 senyawa turunan
vinkadiformina. Mustofa kemudian menguji aktivitas biologis yang lain dari
vinkadiformina, yaitu sebagai antimalaria. Senyawa-senyawa tersebut diuji
aktivitas antimalarianya terhadap P. falciparum yang tergolong resisten terhadap
klorokuin yaitu FcM29-Kamerun dan P. falciparum yang sensitif terhadap
klorokuin yaitu sel Nigerian (Tahir dkk, 2005).
Enambelas senyawa turunan vinkadiformina hasil sintesis Mustofa
beserta data aktivitas antimalaria (log 1/IC50) terhadap P. falciparum yang sensitif
terhadap klorokuin yaitu sel Nigerian, digunakan oleh Tahir dkk (2005) dalam
24
antimalaria. Data struktur dan aktivitas senyawa turunan vinkadiformina hasil
sintesis dan uji oleh Mustofa dapat dilihat pada tabel 1. Parameter teoretis berupa
parameter elektronik dan sterik dari keenambelas struktur senyawa merupakan
variabel bebas yang berpengaruh terhadap variabel tergantung yang berupa log
1/IC50. IC50 merupakan konsentrasi yang dapat menghambat pertumbuhan
plasmodia malaria sebanyak 50%. Dengan menggunakan metode AM1, Tahir dkk
(2005) menemukan 10 model persamaan matematis HKSA terpilih yang
kemudian diolah secara statistik hingga ditemukan model persamaan terbaik yang
dapat menggambarkan hubungan kuantitatif struktur dan aktivitas senyawa
turunan vinkadiformina sebagai antimalaria.
Model persamaan terbaik yang dihasilkan dari penelitian Tahir dkk
menyatakan bahwa deskriptor-deskriptor yang mempengaruhi aktivitas
antimalaria vinkadiformina dan turunannya adalah muatan bersih, momen dipol,
ELUMO, EHOMO, polarisabilitas molekular, dan luas permukaan. Daerah sensitif
yang diduga memberi sumbangan pengaruh terhadap kuantitas aktivitas
antimalaria, berdasarkan penelitian Tahir dkk digambarkan di bawah ini.
Gambar 11. daerah sensitif senyawa vinkadiformina dan turunannya hasil penelitian Tahir dkk
N H
E. Hubungan Kuantitatif Struktur dan Aktivitas
Penggunaan pendekatan mencoba-coba dalam usaha menemukan obat
ditinggalkan dalam bidang rancangan obat dan diusahakan penggunaan
pendekatan yang rasional. Informasi tentang turunan struktur molekul senyawa
yang dapat mengubah hasil uji eksperimental, menguraikan tentang hubungan
antara struktur dan aktivitas biologis (Sardjoko, 1993).
Hubungan struktur dan sifat adalah pendefinisian empiris kualitatif dan
kuantitatif antara sruktur molekul dengan sifat yang teramati. Hubungan struktur
dan sifat yang dikaji belakangan ini selalu merupakan hubungan matematika
secara kuantitatif. Jika sifat digambarkan sebagai aktivitas biologis-misalnya
aktivitas obat-maka dikenal sebagai hubungan kuantitatif struktur dan aktivitas
(HKSA atau QSAR = Quantitative Structure Activity Relationship) (Pranowo,
2004). Tujuan HKSA adalah untuk memprediksikan hubungan antara deskripsi
kuantitatif dari sifat-sifat fisika senyawa dan respon sistem biologis. Respon dapat
berupa perhitungan Ki inhibitor dalam pengujian enzim, pED50 dari agonis
reseptor, atau hanya pembuktian apakah suatu senyawa aktif atau inaktif secara
biologis (Davis, 1994). Tujuan lain dari HKSA adalah untuk menentukan struktur
senyawa yang dapat menghasilkan ikatan optimum dengan reseptor, dan untuk
mendesain satu seri senyawa untuk memaksimalkan informasi berkaitan dengan
struktur untuk aktivitas dari sejumlah kecil senyawa uji (Block, 2004).
Diharapkan hasil HKSA akan memberikan pengertian mengenai sifat molekular
yang sangat mempengaruhi aktivitas, dan membuka jalan bagi optimisasi aktivitas
biologis dalam satu seri senyawa (Davis, 1994).
Studi HKSA dapat menggunakan beberapa model, tetapi model yang
26
(model de novo), dan model yang didasarkan pada mekanika kuantum (Sardjoko,
1993). Pada metode Hansch dikemukakan suatu konsep bahwa hubungan struktur
kimia dengan aktivitas biologis (log 1/C) suatu senyawa dapat dinyatakan secara
kuantitatif melalui parameter-parameter sifat fisika kimia dari substituen yaitu
parameter hidrofob (π), elektronik (σ) dan sterik (Es). Model pendekatan ini
disebut pula model hubungan energi bebas linier (Linear Free Energy
Relationship = LFER), yang dinyatakan melalui persamaan regresi linier berikut:
Log 1/C = a ∑π + b ∑σ + c ∑ Es + d (1)
(Siswandono dan Soekardjo, 1995)
Respon biologis umumnya berupa resiprok (log 1/C). Hal ini dikarenakan dengan
menggunakan resiprok akan diperoleh hubungan yang valid. Dengan
menggunakan resiprok untuk respon biologis akan diperoleh kemiringan garis
regresi (slope) yang positif (Block, 2004).
F. Kimia Komputasi
Metode kimia komputasi sangat membantu dalam penelitian hubungan
kuantitatif struktur dan aktivitas. Dengan aplikasi komputasi, perhitungan sifat
kimia dan fisika suatu senyawa dapat dilakukan dengan mudah.
1. Hyperchem
Program HyperChem merupakan program kimia aplikasi 32 bit yang
dikembangkan oleh Hypercube Inc. HyperChem merupakan program yang mudah
digunakan, fleksibel, dan berkualitas. Dengan menggunakan visualisasi dan
molekular, menjadikan HyperChem lebih mudah digunakan daripada program
kimia kuantum yang lain (Pranowo, 2004).
Dengan HyperChem dapat dilakukan eksplorasi model energi permukaan
potensial secara klasik atau kuantum dengan single point, optimasi geometri atau
perhitungan dalam mencari keadaan transisi. Perhitungan single point dapat
digunakan untuk menentukan energi molekul dari struktur yang telah ditentukan
(tanpa proses optimasi). Perhitungan optimasi geometri menggunakan algoritma
minimisasi energi untuk mendapatkan struktur yang paling stabil (Pranowo,
2004).
HyperChem merupakan program yang secara teliti dapat digunakan
untuk mengetahui struktur, stabilitas, dan sifat molekul dengan menggunakan
perhitungan mekanika molekular maupun mekanika kuantum. Dalam HyperChem
terdapat metode sederhana untuk menghasilkan struktur molekul 3D. Terdapat 10
jenis metode semiempiris yang dapat digunakan untuk mengoptimasi geometri
suatu senyawa agar diperoleh struktur yang paling stabil. Perhitungan semiempiris
dapat dilakukan pada atom hidrogen sampai xenon, termasuk logam transisi.
Kesepuluh metode semiempiris yang terdapat dalam program HyperChem adalah
Extended Huckel (oleh Hoffman), Complete Neglect of Differential Overlap
(CNDO) dan Intermediate Neglect of Differential Overlap (INDO) (oleh People
dkk), Modified Intermediate Neglect of Differential Overlap (MINDO3), MNDO,
MNDO/d, dan AM1 (oleh Dewar dkk), PM3 (oleh Stewart), Zerner Intermediate
Neglect of Differential Overlap (ZINDO/1) dan ZINDO/s (oleh Zerner dkk).
28
dengan variasi himpunan basis yang dapat digunakan untuk menentukan sifat
struktur molekul secara akurat (Pranowo, 2004).
2. Metode semiempiris MNDO
Menurut Pranowo (2004), metode semiempiris adalah metode kimia
komputasi yang masih memperhitungkan penyelesaian secara kimia kuantum
sehingga sifat-sifat elektronik masih dapat diturunkan. Metode semiempiris
berdasar pada pendekatan Hartree-Fock. Pendekatan dilakukan terhadap
penyusunan matrik Fock, atau dalam penyederhanaan pada pernyataan energi
sistem. Pendekatan lain dari metode semiempiris adalah hanya
mempertimbangkan elektron valensi. Elektron dalam (core) dihitung sebagai
fungsi tolakan core-core bersama-sama dengan energi tolakan inti (Pranowo,
2004). Metode semiempiris mengurangi biaya komputasi dengan mengurangi
jumlah integral. Metode semiempiris mampu menghitung fungsi gelombang
elektronik, yang dapat digunakan untuk memprediksikan sifat-sifat kimia fisika
yang bervariasi. Metode semiempiris memberikan hasil yang sangat baik jika
informasi eksperimental telah tersedia, tetapi metode ini tidak dapat memprediksi
tipe senyawa yang tidak diketahui sama sekali (Jensen, 1999).
Langkah awal dalam mengurangi masalah komputasi adalah dengan
hanya mempertimbangkan eksplisitas elektron valensi, elektron core dihitung
dengan cara mengurangi muatan inti atau memberikan fungsi untuk memodelkan
tolakan gabungan yang disebabkan oleh elektron core dan nuklei. Hanya set basis
minimum (jumlah minimum fungsi yang dibutuhkan untuk mengakomodasi
misalnya, memiliki satu fungsi basis, dan semua atom dalam baris kedua dan
ketiga dalam tabel sistem periodik memiliki empat fungsi basis (satu s-dan satu
set p-orbital, px, py, dan pz). Sebagian besar metode semiempiris hanya
menggunakan fungsi s- dan p-, dan fungsi basis diambil sebagai orbital tipe Slater
(Jensen, 1999).
MNDO adalah metode semiempiris orbital molekular (Molecular
Orbital atau MO) self-consistent-field elektron-valensi yang menggunakan basis
minimal dari orbital atomik dan pendekatan integral Neglect of Diatomic
Differential Overlap (NDDO) (Thiel, 2001). Parameterisasi pada MNDO
dilakukan pada variabel atomik, yaitu hanya atom tunggal. MNDO, AM1, dan
PM3 diturunkan dari pendekatan dasar yang sama yaitu NDDO, dan hanya
berbeda pada perlakuan repulsi core-core dan bagaimana parameter ditentukan
(Jensen, 1999). MNDO merupakan metode semiempiris pertama yang digunakan
secara luas untuk analisis struktur organik yang beranekaragam, karena memiliki
hubungan dengan metode optimasi geometri (Lahti, 1998). MNDO mempunyai
tujuh parameter atomik (Uss, Upp, ζ, βs, βp, α) dan satu yang termasuk dalam
perhitungan interaksi multipol (pada dasarnya pemisahan antara titik muatan yang
digunakan untuk menggambarkan dipol), dan tidak ada parameter diatomik.
Integral yang tidak diatur sama dengan nol pada asumsi CNDO dihitung sebagai
interaksi multipol. Parameter atom yang sekarang tersedia adalah untuk atom H,
Li, Be, C, N, O, F, Al, Si, P, S, Cl, Zn, Ge, Br, I, Sn, Hg dan Pb (Pranowo, 2004).
Metode ini baik digunakan untuk geometri dan potensial ionisasi. Cukup
30
masalah dengan cincin yang kecil dan pasangan elektron yang berdekatan, serta
analisis transisi state (Lahti, 1998). Menurut Jensen (1999), beberapa keterbatasan
dari model MNDO adalah sebagai berikut :
a. molekul yang memiliki banyak halangan sterik, seperti neopentan, sangat
tidak stabil
b. senyawa dengan 4 cincin sangat stabil
c. interaksi yang lemah tidak dapat diprediksi (contohnya pada ikatan hidrogen)
d. molekul hipervalen, seperti sulfoksida dan sulfon, sangat tidak stabil
e. energi aktivasi untuk reaksi memutuskan dan membentuk ikatan sangat tinggi
f. struktur non klasik diprediksi tidak stabil relatif terhadap struktur klasik (misal
kation etil)
g. substituen teroksigenasi pada cincin aromatik out of plane (contohnya
nitrobenzena)
h. ikatan peroksida sangat pendek ~ 0,17 Å
i. sudut C-X-C pada eter dan sulfida sangat besar ~ 9o
G. Analisis Statistik
Dalam penelitian, biasa digunakan model suatu hubungan fungsional
antara peubah. Dengan model tersebut kelakuan sistem yang akan diteliti dapat
dipahami, diterangkan, dikendalikan, dan kemudian diprediksikan. Prediksi
memiliki arti yang khusus yaitu inter- atau ekstrapolasi (Sembiring, 2003).
Model dapat membantu penentuan hubungan sebab akibat (kausal)
kuantitatif antara struktur kimia dan aktivitas biologis melalui parameter sifat
kimia fisika, dapat dilakukan perhitungan statistik dengan bantuan komputer,
dengan menggunakan program MICROSTAT, ABSTAT, PCN, QSAR,
MINITAB, STATGRAPH, SPSS atau program yang lain (Siswandono dan
Soekardjo, 1995), namun ada tidaknya hubungan kausal antara peubah tidak dapat
diputuskan dengan hanya menggunakan data statistik. Secara umum, model
merupakan penyederhanaan dan abstraksi dari keadaan alam yang sesungguhnya.
Dalam hal ini model akan selalu berbentuk fungsi dan regresi (Sembiring, 2003).
Salah satu metode statistik yang digunakan dalam analisis HKSA adalah
metode korelasi. Metode ini mengidentifikasi hubungan kuantitatif antara
x-deskriptor dan aktivitas biologis. Hansch pertama kali menggunakan multiple
linear regression (regresi linear multivariat) sebagai metode statistik dalam
HKSA dan metode ini masih digunakan sampai sekarang (Davis, 1994). Regresi
linear multivariat hanya dibatasi untuk jumlah deskriptor kurang dari 20. Dalam
metode ini dianggap bahwa semua deskriptor tidak berkorelasi satu sama lain dan
semua deskriptor memiliki pengaruh yang penting terhadap aktivitas (Davis,
1994). Hal ini dikarenakan data yang digunakan adalah data percobaan
laboratorium yang tidak lagi menggambarkan keadaan alamiah, tetapi telah
dimanipulasi oleh peneliti (Sembiring, 2003).
Regresi linear untuk satu parameter fisika kimia dapat dinyatakan
melalui persamaan sebagai berikut :
Y = aX + b (2)
32
Regresi linear untuk dua parameter sifat fisika kimia atau lebih dapat dinyatakan
melalui persamaan sebagai berikut :
Y = aX1 + bX2 + cX3 + ....+ d (3)
dimana X1, X2, X3 = parameter – parameter sifat fisika kimia 1, 2, 3 (Siswandono
dan Soekardjo, 1995).
Keabsahan persamaan yang diperoleh dan arti perbedaan parameter yang
digunakan dalam hubungan struktur-aktivitas model Hansch dapat dilihat dengan
beberapa kriteria statistik, antara lain :
1. nilai R (koefisien korelasi)
Nilai R menunjukkan tingkat hubungan antara data aktivitas biologis
dari pengamatan percobaan dengan data hasil perhitungan berdasarkan persamaan
yang diperoleh dari analisis regresi. Koefisien korelasi bernilai mulai dari 0
sampai 1. Dalam penelitian HKSA dicoba dicapai suatu nilai R yang lebih besar
dari 0,9, sebab semakin tinggi nilai R maka semakin baik hubungannya
(Siswandono dan Soekardjo, 1995). Hubungan yang sangat kuat antara variabel
bebas dan variabel tergantung sebenarnya telah tercapai pada nilai R 0,8 sampai
dengan 1 (Anonim, 2006).
2. nilai R2 (koefisien determinasi)
Nilai R2 menunjukkan berapa persen aktivitas biologis yang dapat
dijelaskan hubungannya dengan parameter sifat fisika kimia yang digunakan.
Misalnya suatu hubungan yang mempunyai nilai R = 0,990 berarti dapat
menjelaskan (0,990)2 x 100% = 98% dari variasi antar data (Siswandono dan
3. nilai Fhitung/Ftabel
Nilai Fhitung menunjukkan kemaknaan hubungan bila dibandingkan
dengan Ftabel. Makin besar nilai Fhitung makin besar derajat kemaknaan hubungan.
Semakin tinggi nilai Fhitung semakin kecil kemungkinan hubungan tersebut adalah
karena kebetulan (Siswandono dan Soekardjo, 1995). Persamaan yang memenuhi
syarat siginifikansi pada tingkat kepercayaan 95% adalah persamaan yang
memiliki nilai Fhitung/Ftabel lebih besar dari 1 atau Fhitung lebih besar daripada Ftabel
(Yuliana, 2005).
4. nilai SE
Nilai SE merupakan simpangan baku yang menunjukkan nilai variasi
kesalahan dalam percobaan (Siswandono dan Soekardjo, 1995).
5. PRESS
Salah satu tujuan pembentukan model ialah untuk prediksi dan salah satu
patokan prediksi yang baik ialah prediksi dengan nilai yang diprediksi sama atau
hampir sama. Nilai PRESS merupakan selisih antara hasil prediksi dengan nilai
yang diprediksi (eksperimen). Model yang baik adalah model yang menghasilkan
PRESS yang kecil dalam kelompok parameter (Sembiring, 2003).
Menurut Hansch, aktivitas biologis dipengaruhi oleh parameter
elektronik, sterik, dan hidrofobisitas dari suatu senyawa (Siswandono dan
Soekardjo, 1995). Berdasarkan konsep ini, maka model persamaan terbaik juga
34
H. Keterangan Empiris
Penelitian ini dapat menghasilkan model persamaan HKSA terbaik
dengan deskriptor yang ditentukan berdasarkan hasil perhitungan semiempiris
MNDO. Dari model persamaan terbaik ini dapat digambarkan hubungan
kuantitatif struktur senyawa turunan vinkadiformina, melalui parameter teoretis
meliputi parameter elektronik, sterik, dan hidrofobisitas, dengan aktivitas yang
didasarkan pada log 1/IC50. IC50 merupakankonsentrasi yang dapat menghambat
pertumbuhan P. falciparum sebanyak 50%. Berdasarkan model persamaan
terbaik, dapat dirancang senyawa hipotetik yang diprediksi memiliki aktivitas
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini menggunakan jenis dan bentuk rancangan penelitian
eksperimental kuasi. Penelitian ini dikatakan penelitian eksperimental karena
bahan penelitian yang berupa 16 senyawa vinkadiformina dan turunannya telah
mengalami perlakuan pada penelitian sebelumnya yaitu pada penelitian Mustofa.
Dalam penelitian yang dilakukan oleh Mustofa, vinkadiformina mengalami
modifikasi struktur terutama pada cincin indol. Modifikasi ini menghasilkan satu
seri senyawa vinkadiformina dan turunannya yang kemudian diuji aktivitas
antimalarianya.
Pada penelitian eksperimen murni, pemilihan sampel dilakukan secara
acak, sedangkan pada penelitian ini pemilihan 16 struktur senyawa
vinkadiformina dan turunannya sebagai sampel tidak dapat dilakukan secara acak,
melainkan telah ditetapkan secara pasti. Data aktivitas antimalaria yang diperoleh
merupakan data sekunder. Dari penjelasan tersebut dapat dikatakan bahwa bentuk
penelitian ini termasuk dalam rancangan penelitian eksperimental kuasi.
36
B. Variabel dan Definisi Variabel
1. Variabel bebas
Variabel bebas dalam penelitian ini adalah deskriptor-deskriptor yang
mewakili parameter Hansch. Parameter elektronik berupa muatan bersih atom
yaitu qC1, qC2, qC3, qC4, qC5, qN, qC7, qC8, qC9, selisih antara energi Lowest
Unoccupied Molecular Orbitals (ELUMO) dan energi Highest Occupied Molecular
Orbitals Energy (EHOMO), yang disimbolkan dengan ΔE, polarisabilitas molekular
(∂), dan momen dipol (μ). Parameter sterik yang digunakan adalah luas
permukaan (SA), volume (V), refraktivitas molar (MR), dan massa (M).
Parameter hidrofobisitas diwakili oleh log P.
N
Gambar 12. Struktur senyawa vinkadiformina dengan penomeran atom tidak mengikuti kaidah tatanama senyawa dan
hanya digunakan untuk penelitian ini saja
2. Variabel tergantung
Variabel tergantung dalam penelitian ini adalah nilai log 1/IC50. Nilai ini
menggambarkan aktivitas senyawa vinkadiformina dan turunannya sebagai
antimalaria yang didasarkan pada konsentrasi yang dapat menghambat