BAB II
TINJAUAN PUSTAKA
2.1 Ulkus Peptikum (Peptic Ulcer)
Ulkus peptikum merupakan kerusakan pada mukosa gastrointestinal yang meluas hingga ke mukosa muskularis, yang berlangsung lama dan umumnya bergantung pada aktivitas asam lambung. Penyebab umum ulkus peptikum yaitu infeksi bakteri Helicobacter pylori dan penggunaan obat nonsteroid (Soll dan Graham, 2009).
2.1.1 Etiologi
Kebanyakan ulkus terjadi dengan adanya asam dan pepsin ketika H.pylori,
NSAID, atau faktor lain yang mengganggu pertahanan mukosa normal dan mekanisme penyembuhan. Hipersekresi asam adalah mekanisme pathogenesis utama (Berardy dan Welage, 2005).
2.1.2 Patofisiologi
Ulkus peptikum terjadi karena ketidakseimbangan antara faktor agresif (asam lambung dan pepsin) dan mekanisme yang menjaga integritas mukosa (pertahanan mukosa dan perbaikan) (Soll dan Graham, 2009).
2.1.2.1 Asam lambung dan pepsin
2.1.2.2 Pertahanan dan perbaikan mukosa
Mekanisme pertahanan dan perbaikan mukosa saluran cerna yang melindungi mukosa dari endogen berbahaya dan substansi eksogen. Mekanisme pertahanan mukosa termasuk lender dan sekresi bikarbonat, pertahanan intrinsic sel epitel dan aliran darah mukosa. Kekentalan dan pH yang hampir netral dari mukus-bikarbonat melindungi lambung dari isinya yang asam dalam lumen lambung. Perbaikan mukosa setelah cedera berhubungan dengan rewstitusi sel epitel, pertumbuhan dan regenerasi. Pemeliharaan integritas dan perbaikan mukosa dimediasi oleh produksi prostaglandin endogen. Perubahan dalam pertahanan mukosa yang disebabkan oleh H. pylori atau penggunaan NSAID adalah kofaktor yang paling penting dalam pembentukan ulkus peptikum (Berardy dan Welage, 2005).
2.1.2.3 Helicobacter pylori
Helicobacter pylori memproduksi urease dalam jumlah besar yang menghidrolisis urea dalam asam lambung dan mengubahnya menjadi amoniak dan karbon dioksida. Efek buffer lokal dari amoniak menciptakan lingkungan kecil yang netral di sekitar bakteri yang melindungi dari efek asam lambung yang mematikan. H.pylori juga memproduksi protein penghambat asam yang memungkinkan untuk beradaptasi dengan lingkungan pH rendah di lambung (Berardy dan Welage, 2005).
seluler. Lipase dan protease mendegradasi mukus, ammonia yang dihasilkan oleh urease bersifat toksik terhadap sel epitel dan penempelan bakteri meningkatkan pemasukan toksin ke dalam sel epitel. Infeksi H.pylori mengubah respon inflamasi dan merusak sel epitel secara langsung oleh mekanisme kekebalan yang dimediasi oleh sel atau secara tidak langsung dengan mengaktifkan neutrofil atau makrofag mencoba untuk memfagosit bakteri atau produk dari bakteri (Berardy dan Welage, 2005).
2.2 Sistem Penghantaran Obat Tertahan di Lambung
Penghantaran obat yang tertahan di lambung merupakan suatu pendekatan untuk memperlama waktu tinggal di lambung, dengan cara menargetkan tempat pelepasan obat secara spesifik pada bagian atas saluran pencernaan untuk efek lokal maupun sistemik. Sediaan gastroretentif dapat tetap berada di lambung untuk waktu yang lama dan karenanya dapat memperlama waktu tinggal di lambung secara signifikan (Nayak, et al., 2010).
2.2.1 Faktor yang mempengaruhi sediaan obat tertahan di lambung
yang berperan sebagai agen antikolinergik (contohnya atropine, prophanteline), opium (contohnya kodein), dan agen prokinetik (contohnya metoklopramid, kisaprid) (Streubel, et al., 2006).
2.2.2 Sistem penghantaran obat yang mengapung
Sistem penghantaran obat mengapung merupakan salah satu pendekatan yang penting untuk mencapai penahanan di lambung untuk memperoleh bioavailabilitas obat yang cukup (Singh dan Kim, 2000). Sistem penghantaran ini diperlukan untuk obat dengan tapak absorpsi di lambung atau usus halus bagian atas (Sungthongjeen, et al., 2006).
Berdasarkan mekanisme mengapungnya, sistem penghantaran obat mengapung dapat dibagi menjadi dua, yaitu sistem effervescent (pembentukan gas) dan sitem non-effervescent (Goyal, et al., 2011).
1. Sistem Effervescent (pembentukan gas)
Merupakan sistem matriks yang dibuat dengan bantuan plimer yang dapat mengembang seperti hidroksi propil metil selulosa atau polisakarida dan kitosan komponen pembentuk gas seperti natrium bikarbonat, kalsium karbonat, asam sitrat, atau asam tartrat. Sediaan ini diformulasikan sehingga ketika kontak dengan cairan lambung, akan terbentuk karbon dioksida dan terperangkap di dalam hidrokoloid yang mengembang. Hal ini menyebakan sediaan mengapung (Arora, et al., 2005)
2. Sistem non-effervescent
mengapung non-effervescent yaitu pembentuk gel atau hidrokoloid yang dapat mengembang, polisakarida, dan polimer pembentuk matriks seperti polimetakrilat, polikarbonat, poliakrilat, polistiren, dan polimer bioadhesif seperti kitosan dan karbopol. Setelah penggunaan oral, sediaan akan kontak dengan cairn lambung dan mengembang, membentuk suatu lapisan seperti gel pada permukaannya (Goyal, et al., 2011) dan berat jenis menjadi lebih kecil dari 1. Udara yang terjerat di dalam matriks yang mengembang memberikan daya bagi sediaan untuk mengapung. Gel hidrokoloid yang terbentuk ini bertindak sebagai reservoir dan memberikan pelepasan sustained release
(Arora, et al., 2005).
Keuntungan dari sistem sediaan mengapung (Rao dan Pavan, 2012)
1. Sistem penghantaran obat mengapung menguntungkan untuk obat yang diabsorbsi di lambung misalnya garam-garam ferro.
2. Sistem penghantaran obat mengapung menguntungkan untuk obat yang ditujukan untuk aksi lokal di lambung dan pengobatan ulkus, seperti antasida. 3. Sistem penghantaran obat mengapung memberikan keuntungkan untuk obat
yang memiliki tapak absorpsi yang sempit di bagian usus halus contohnya CTM.
Beberapa tipe obat yang menguntungkan bila diformulasikan menggunakan sistem mengapung diantaranya (Rao dan Pavan, 2012):
a) Obat yang memiliki aksi lokal di lambung b) Obat yang terutama diabsorbsi di lambung
e) Obat yang dengan cepat diabsorpsi di saluran pencernaan f) Obat yang terdegradasi di kolon.
Kelemahan dari sistem penghantaran obat mengapung (Rao dan Pavan, 2012):
1. Ada beberapa situasi yang mana retensi lambung tidak diinginkan. Aspirin dan obat antiinflamasi nonsteroid diketahui menyebabkan lesi pada lambung, dan pelepasan yang lambat dari obat-obat ini di lambung tidak diinginkan.
2. Obat-obat yang mengiritasi lambung atau yang tidak stabil dalam suasana asam tidak dibenarkan untuk diformulasikan dalam sistem gastroretentif. 3. Memerlukan cairan yang cukup di lambung agar sediaan dapat
mengapung. Sediaan obat ini harus diminum dengan segelas air (200-250 ml).
Adapun sediaan floating yang tersedia di pasaran diantaranya
Bentuk Sediaan Nama Obat Nama Dagang Perusahaan,Negara
Floating Controlled Release Capsules
Levodopa, Benserazide
MODAPAR Roche Products, USA
Floating Capsule Diazepam VALRELEASE Hoffmann-LaRoche, USA
Effervescent Floating
LIQUID GAVISON Glaxo Smith Kline, INDIA
Floating Liquid Alginate Preparation
Aluminium - Magnesium antacid
TOPALKAN Pierre Fabre Drug, FRANCE
Coloidal Gel Forming Floating Drug Delivery Systems
Ferrous sulphate CONVIRON Ranbaxy, INDIA
Gas-Generating Floating Tablet
Ciprofloxacin CIFRAN OD Ranbaxy, INDIA
Bilayer Floating Capsule
Misoprostal CYTOTEC Pharmacia, USA
2.3 Metronidazol
2.3.1 Sifat fisika kimia metronidazol
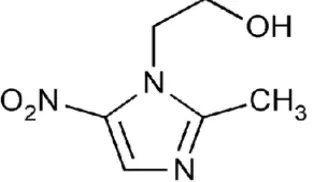
Struktur metronidazol dapat dilihat pada gambar 2.1 dibawah ini:
Gambar 2.1 Struktur kimia metronidazol
Rumus kimia metronidazol adalah C6H9N3O3 dengan nama kimia
2-metil-5-nitroimidazol-1-etanol, mempunyai berat molekul 171,16. Metronidazol mengandung tidak kurang dari 99,0% dan tidak lebih dari 101,0% C6H9N3O3,
dihitung terhadap zat yang telah dikeringkan. Pemberiannya antara lain: hablur atau serbuk hablur; putih hingga kuning pucat; tidak berbau; stabil di udara, tetapi lebih gelap bila terpapar oleh cahaya. Sukar larut dalam eter; agak sukar larut dalam air, dalam etanol dan dalam kloroform (Ditjen POM, 1995).
2.3.2 Farmakologi
Metronidazol adalah antimikroba dengan aktivitas yang sangat baik terhadap bakteri anaerob dan protozoa. Spektrum protozoanya mencakup
Metronidazol memperlihatkan daya amubisid langsung. Pada biakan E. histolytica dengan kadar metronidazol 1-2 µg/mL, semua parasit musnah dalam 24 jam. Sampai saat ini belum ditemukan amuba yang resisten terhadap metronidazol. Metronidazol juga memperlihatkan daya trikomonoiasid langsung. Pada biakan Trichomonas vaginalis, kadar metronidazol 2,5 µg/mL dapat mengancurkan 99% parasit dalam waktu 24 jam. Trofozit Giardia lambia juga dipengaruhi langsung pada kadar antara 1-50 µg/mL. Namun, saat ini telah dilaporkan bahwa Trichomonas vaginalis dan Giardia lambia secara klinis resisten terhadap metronidazol (Syarif dan Elysabeth, 2011).
2.3.3 Farmakokinetik
Absorpsi metronidazol berlangsung dengan baik sesudah pemberian oral. Satu jam setelah pemberian dosis tunggal 500 mg per oral diperoleh kadar plasma kira-kira 10 µg/mL. umumnya untuk kebanyakan protozoa dan bakteri yang sensitif, rata rata diperlukan kadar tidak lebih dari 8 µg/mL (Syarif dan Elysabeth, 2011).
Waktu paruhnya berkisar antara 8-10 jam. Pada beberapa kasus terjadi kegagalan karena rendahnya kadar sistemik. Ini mungkin disebabkan oleh absorpsi yang buruk atau metabolism terlalu cepat. Obat ini diekskresi melalui urin dalm bentuk asal dan bentuk metabolit hasil oksidasi dan glukuronidasi. Metronidazol juga diekskresi melalui air liur, air susu, cairan vagina, dan cairan seminal dalam kadar yang rendah (Syarif dan Elysabeth, 2011).
2.4. Natrium Alginat
Natrium alginat larut dengan lambat dalam air, membentuk larutan kental, tidak larut dalam etanol dan eter. Alginat ini diperoleh dari spesies Macrocystis pyrifera, Laminaria, Ascophyllum dan Sargassum (Belitz dan Grosch, 1987).
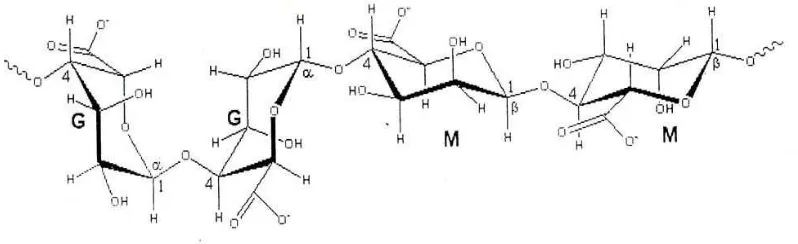
Gambar 2.2 Struktur G: - L asam guluronat dan M: - D asam mannuronat
Asam alginat adalah kopolimer biner yang terdiri dari residu -D-mannuronat (M) dan -L-asam guluronat (G) yang tersusun dalam blok-blok yang
membentuk rantai linear. Kedua unit tersebut berikatan pada atom C1 dan C4 dengan susunan homopolimer dari masing-masing residu (MM dan GG) dan suatu blok heteropolimer dari dua residu (MG) (Thom, et al., 1982).
2.5. Parafin Cair
Parafin cair terdiri atas campuran senyawa hidrokarbon cair jenuh yang diperoleh dari minyak bumi. Zat ini tidak dicerna dalam saluran lambung-usus dan hanya bekerja sebagai zat pelicin bagi isi usus dan tinja. Gunanya untuk melunakkan tinja, terutama setelah pembedahan rektal atau pada penyakit wasir (Tan dan Rahardja, 2007).
2.7. Disolusi
Proses melarutnya suatu obat disebut disolusi (Ansel, 2005). Uji disolusi yaitu uji pelarutan in vitro mengukur laju dan jumlah pelarutan obat dalam suatu media
aqueous dengan adanya satu atau lebih bahan tambahan yang terkandung dalam produk obat. Pelarutan obat merupakan bagian penting sebelum kondisi absorbsi sistemik (Shargel dan Yu, 1999).
Faktor-faktor yang mempengaruhi disolusi dibagi atas 3 kategori yaitu: a. Faktor-faktor yang be rhubungan dengan sifat fisikokimia obat, meliputi:
i. Efek kelarutan obat. Kelarutan obat dalam air merupakan faktor utama dalam menentukan laju disolusi. Kelarutan yang besar menghasilkan laju disolusi yang cepat.
ii. Efek ukuran partikel. Ukuran partikel berkurang dapat memperbesar luas permukaan obat yang berhubungan dengan medium, sehingga laju disolusi meningkat.
b. Faktor-faktor yang berhubungan dengan sediaan obat, meliputi:
bahan obat yang hidrofob, oleh karena itu disolusi bertambah, sedangkan bahan tambahan yang hidrofob dapat mengurangi laju disolusi.
ii. Efek faktor pembuatan sediaan. Metode granulasi dapat mempercepat laju disolusi obat-obat yang kurang larut. Penggunaan bahan pengisi yang bersifat hidrofil seperti laktosa dapat menambah hidrofilisitas bahan aktif dan menambah laju disolusi.
c. Faktor-faktor yang berhubungan dengan uji disolusi, meliputi :
i. Tegangan permukaan medium disolusi. Tegangan permukaan mempunyai pengaruh nyata terhadap laju disolusi bahan obat. Surfaktan dapat menurunkan sudut kontak, oleh karena itu dapat meningkatkan proses penetrasi medium disolusi ke matriks. Formulasi tablet dan kapsul konvensional juga menunjukkan penambahan laju disolusi obat-obat yang sukar larut dengan penambahan surfaktan kedalam medium ii. Viskositas medium. Semakin tinggi viskositas medium, semakin kecil
laju disolusi bahan obat.
iii. pH medium disolusi. Larutan asam cenderung memecah tablet sedikit lebih cepat dibandingkan dengan air, oleh karena itu mempercepat laju disolusi (Gennaro, 2000). Obat-obat asam lemah disolusinya kecil dalam medium asam, karena bersifat nonionik, tetapi disolusinya besar pada medium basa karena terionisasi dan pembentukan garam yang larut (Martin, et al., 1993).
a. Metode Keranjang (Basket )
Metode keranjang terdiri atas keranjang silindrik yang ditahan oleh tangkai motor. Keranjang menahan cuplikan dan berputar dalam suatu labu bulat yang berisi media pelarutan. Keseluruhan labu tercelup dalam suatu bak yang bersuhu konstan 37 oC. Kecepatan berputar dan posisi keranjang harus memenuhi rangkaian syarat khusus dalam USP yang terakhir beredar. Tersedia standar kalibrasi pelarutan untuk meyakinkan bahwa syarat secara mekanik dan syarat operasi telah dipenuhi.
b. Metode Dayung (Paddle)
Metode dayung terdiri atas suatu dayung yang dilapisi khusus, yang berfungsi memperkecil turbulensi yang disebabkan oleh pengadukan. Dayung diikat secara vertikal ke suatu motor yang berputar dengan suatu kecepatan yang terkendali. Tablet atau kapsul diletakkan dalam labu pelarutan yang beralas bulat yang juga berfungsi untuk memperkecil turbulensi dari media pelarutan. Alat ditempatkan dalam suatu bak air yang bersuhu konstan, seperti pada metode basket dipertahankan pada 37 oC. Posisi dan kesejajaran dayung ditetapkan dalam USP. Metode dayung sangat peka terhadap kemiringan dayung. Pada beberapa produk obat, kesejajaran dayung yang tidak tepat secara drastis dapat mempengaruhi hasil pelarutan. Standar kalibrasi pelarutan yang sama digunakan untuk memeriksa peralatan sebelum uji dilaksanakan.
c. Metode Disintegrasi yang Dimodifikasi
tidak akan jatuh melalui saringan. Metode ini jarang digunakan dan dimasukkan dalam USP untuk suatu formulasi obat lama. Jumlah pengadukan dan getaran membuat metode ini kurang sesuai untuk uji pelarutan yang tepat (Shargel dan Yu, 1999).