PENGESAHAN SKRIPSI
FORMULASI DAN EVALUASI SECARA
IN VITRO
FLOATING MUCOADHESIVE BEADS
DARI
METRONIDAZOL DENGAN BASIS
ALGINAT-KITOSAN
OLEH:
ALI WARDANA SITEPU NIM 101501043
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: 26 Agustus 2014
Pembimbing I,
Prof. Dr. M.T. Simanjuntak, M.Sc., Apt. NIP 195212041980021001
Panitia Penguji
Prof. Dr. Karsono, Apt. NIP 195409091982011001
Prof. Dr. M.T. Simanjuntak, M.Sc., Apt. NIP 195212041980021001
Dr. Kasmirul R. Sinaga, M.S., Apt. NIP 195504241983031003
Dra. Lely Sari Lubis, M.Si., Apt. NIP 195404121987012001
Medan, Oktober 2014 Fakultas Farmasi
Universitas Sumatera Utara Dekan,
Pembimbing II,
KATA PENGANTAR
Puji syukur kehadirat Tuhan Yang Maha Esa oleh karena kasih
karunia-Nya penulis dapat menyelesaikan penyusunan skripsi yang berjudul “Formulasi
Dan Evaluasi Secara In Vitro Floating Mucoadhesive Beads Dari Metronidazol
Dengan Basis Alginat-Kitosan”. Skripsi ini diajukan sebagai salah satu syarat
untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi Universitas
Sumatera Utara.
Pada kesempatan ini penulis mengucapkan terima kasih yang
sebesar-besarnya kepada Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas
Farmasi Universitas Sumatera Utara, yang telah memberikan bantuan serta
fasilitas selama pendidikan, kepada Prof. Dr. M.T. Simanjuntak, M.Sc., Apt., dan
Prof. Dr. Hakim Bangun, Apt., selaku dosen pembimbing yang telah membimbing
penulis dengan penuh kesabaran selama penelitian. Ucapan terima kasih juga
disampaikan kepada Prof. Dr. Karsono, Apt., Dr. Kasmirul Ramlan Sinaga, M.S.,
Apt., dan Dra. Lely Sari Lubis, M.Si., Apt., selaku dosen penguji yang telah
memberikan saran, arahan, kritik, dan masukan kepada penulis dalam
penyelesaian skripsi ini, kepada T. Ismanelly Hanum, S.Si., M.Si., Apt., selaku
dosen pembimbing akademik yang telah memberikan arahan dan bimbingan
kepada penulis selama ini, serta Bapak dan Ibu staf pengajar Fakultas Farmasi
USU yang telah mendidik penulis selama masa perkuliahan.
Ucapan terima kasih dan penghargaan yang sebesar-besarnya kepada
Ayah dan Ibunda tercinta Kasinan Sitepu dan Sukahati br Milala, serta Karmila
penulis dan kepada sahabat-sahabat terdekat yang begitu mendukung dan
mendoakan penyelesaian skripsi ini.
Penulis menyadari bahwa tulisan ini masih jauh dari sempurna. Untuk itu
penulis mengharapkan kritik dan saran yang membangun dari semua pihak untuk
perbaikan skripsi ini. Akhir kata penulis berharap semoga skripsi ini dapat
bermanfaat bagi ilmu pengetahuan khususnya di bidang farmasi.
Medan, Oktober 2014
Penulis,
Formulasi dan Evaluasi Secara In Vitro Floating Mucoadhesive Beads dari Metronidazol dengan Basis Alginat-Kitosan
Abstrak
Salah satu kendala utama pada pengobatan ulkus yang disebabkan oleh H. pylori dengan sediaan konvensional adalah waktu tinggal obat yang singkat didalam lambung. Adapun beberapa sistem penghantaran obat ke lambung adalah
floating dan mucoadhesive. Adapun tujuan dari penelitian ini adalah untuk membuat sediaan yang dapat bertahan lebih lama dalam lambung yang memiliki sifat floating dan mucoadhesive.
Floating mucoadhesive beads dibuat dengan menggunakan basis alginat kitosan dan dibuat dalam 11 formula dengan 3 kelompok formula. Kelompok 1 (F1) tanpa penyalutan, kelompok 2 (F2-F6) salut Eudragit RS 100, dan kelompok 3 (F7-F11) salut pertama dengan Eudragit RS 100 dan salut kedua dengan kalsium alginat. Diameter sediaan diukur dengan menggunakan micrometer.
Floating lag time dan floating time diukur pada gelas beker yang berisi medium lambung. Sifat mucoadhesive dari beads diuji dengan menggunakan tensiometer DuNoy menggunakan lambung tikus. Efisiensi penjeratan diukur terhadap 20 beads dan ditentukan jumlah metronidazol yang terjerat didalam beads. Pelepasan metronidazol dari beads dilakukan dengan menggunakan metode dayung USP dalam medium lambung buatan (pH 1,2). Kadar metronidazol diukur dengan menggunakan spektrofotometer ultraviolet pada panjang gelombang 277 nm.
Dari pengukuran didapat diameter beads adalah 2,70 mm sampai 3,27 mm.
Floating lag time dari semua beads adalah 0 menit sedangkan floating time lebih dari 12 jam. Dari uji mucoadhesive didapat gaya mucoadhesive adalah 1,14 sampai 2,06 dyne/mm2. Efisiensi penejaratan dari floating mucoadhesive beads berada pada rentang 62,24% sampai 76,46%. Pada uji pelepasan metronidazol dari beads menunjukkan bahwa beads dapat dijadikan pelepasan terkontrol, dimana semakin tinggi konsentrasi Eudragit RS 100 maka laju pelepasan metronidazol dari beads semakin lambat. Dari percobaan ini didapat hasil maksimal yaitu pada F11 dimana beads dapat melepaskan 83% metronidazol dalam 12 jam. Kinetika pelepasan metronidazol dari beads mengikuti kinetika pelepasan model Higuchi. Berdasarkan hasil penelitian maka dapat disimpulkan bahwa F11 adalah potensial digunakan sebagai sediaan sustained release gastro retentive drug delivery system dari metronidazol.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFAR TABEL ... xii
DAFTAR GAMBAR ... xiii
DAFTAR LAMPIRAN ... xvi
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 4
1.4 Tujuan Penelitian ... 4
1.5 Manfaat Penelitian ... 4
1.6 Kerangka Penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 6
2.1 Ulkus Peptikum (Peptic Ulcer) ... 6
2.2 Gastroretentive Drug Delivery Sistem ... 7
2.3 Sistem Floating ... 8
2.3.1.1 Bentuk sediaan floating effervescent ... 9
2.3.1.2 Bentuk sediaan floating non-effervescent ... 9
2.3.2 Keuntungan FDDS ... 9
2.3.3 Kerugian FDDS ... 10
2.4 Sistem Mucoadhesive ... 10
2.4.1 Pengertian bioadhesive ... 10
2.4.2 Mekanisme bioadhesive ... 11
2.4.3 Teori bioadhesive ... 13
2.5 Metronidazol ... 15
2.5.1 Sifat fisika kimia metronidazol ... 15
2.5.2 Farmakologi ... 15
2.5.3 Farmakokinetik ... 16
2.5.4 Efek samping ... 16
2.6 Alginat ... 16
2.6.1 Struktur kimia ... 18
2.6.2 Sifat alginat ... 19
2.7 Kitosan ... 19
2.7.1 Struktur kimia kitosan ... 20
2.7.2 Sifat kitosan ... 21
2.7.3 Aplikasi farmasetik kitosan ... 21
2.8 Eudragit ... 22
2.8.1 Struktur kimia ... 22
2.8.2 Jenis polimer ... 23
2.9 Disolusi ... 25
2.9.1 Faktor faktor yang mempengaruhi laju disolusi ... 27
2.9.2 Metode disolusi ... 29
BAB III METODE PENELITIAN ... 31
3.1 Alat - Alat Penelitian ... 31
3.2 Bahan – Bahan Penelitian ... 31
3.3 Prosedur Penelitian ... 31
3.3.1 Pembuatan larutan kalsium klorida 0,15 M ... 31
3.3.2 Pembuatan medium lambung buatan medium pH 1,2 . 31 3.3.3 Pembuatan kurva serapan dan kurva kalibrasi metronidazol ... 32
3.3.3.1 Pembuatan larutan induk baku metronidazol dalam medium pH 1,2 ... 32
3.3.3.2 Pembuatan kurva serapan metronidazol dalam medium pH 1,2 ... 32
3.3.3.3 Pembuatan kurva kalibrasi metronidazol dalam medium pH 1,2 ... 32
3.3.4 Pembuatan beads alginat – kitosan ... 32
3.3.5 Pembuatan beads salut eudragit rs 100 ... 33
3.3.6 Pembuatan beads salut eudragit rs 100 dan kalsium alginat ... 33
3.3.7 Penentuan diameter floating mucoadhesive beads ... 33
3.3.8 Pengukuran floating lag time ... 34
3.3.9 Pengukuran floating time ... 34
3.3.10 Efisiensi penjeratan ( entrapment efficiency) ... 34
BAB IV HASIL DAN PEMBAHASAN ... 36
4.1 Pembuatan Floating Mucoadhesive Beads ... 36
4.2 Penenentuan Diameter Floating Mucoadhesive Beads ... 36
4.3 Scanning Electron Microscopy ... 39
4.3.1 Beads alginat-kitosan ... 39
4.3.2 Beads alginat-kitosan salut eudragit rs 100 30% ... 40
4.3.3 Beads alginat-kitosan salut eudragit rs 100 30% dan kalsium alginat ... 41
4.4 Pengukuran Floating Lag Time ... 41
4.5 Pengukuran Floating Time ... 43
4.6 Uji Mucoadhesive ... 44
4.7 Efisiensi Penjeratan (Entrapment Efficiency) ... 45
4.8 Pelepasan Metronidazol dari Floating Mucoadhesive Beads 46 4.8.1 Tanpa penyalutan ... 46
4.8.2 Salut eudragit rs 100 ... 47
4.8.3 Salut eudragit rs 100 dan kalsium alginat ... 49
4.8.4 Perbedaan jenis penyalut ... 52
4.9 Kinetika Pelepasan Metronidazol dari Beads Alginat .Kitosan ... 54
BAB V KESIMPULAN DAN SARAN ... 67
5.1 Kesimpulan ... 67
5.2 Saran ... 67
DAFTAR TABEL
Tabel Halaman
Tabel 2.1: Menunjukkan perbandingan asam uronat dalam berbagai sepsies Alga yang ditentukan dengan spektroskopi NMR high-field ... 17
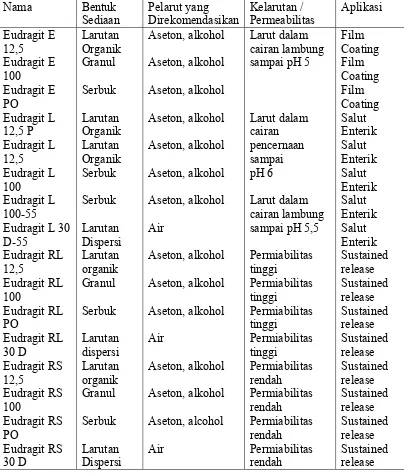
Table 2.2: Jenis dan pemerian polimer eudragit ... 24
Tabel 3.1: Formula floating mucoadhesive beads... 34
Table 4.1: Diameter sediaan floating mucoadhesive beads dari
.Metronidazol dengan basis alginat-kitosan ... 37
Tabel 4.2: Floating lag time floating mucoadhesive beads dari
.Metronidazol dengan basis alginat-kitosan ... 42
Tabel 4.3: Floating time floating mucoadhesive beads dari
.Metronidazol dengan basis alginat-kitosan ... 43
Tabel 4.4: Daya mucoadhesive dari floating mucoadhesive beads dari
.Metronidazol dengan basis alginat-kitosan ... 45
Tabel 4.5: Persen efisiensi penjeratan floating mucoadhesive beads dari
Metronidazol dengan basis alginat-kitosan ... 46
Tabel 4.6: Pelepasan metronidazol dari beads salut eudragit rs 100 ... 47
Tabel 4.7: Pelepasan metronidazol dari beads salut eudragit rs 100 dan
.kalsium alginat ... 50
Tabel 4.8: Nilai AUC0-80% dari floating mucoadhesive beads ... 52
Tabel 4.9: Korelasi kinetika pelepasan metronidazol orde nol, orde satu,
DAFTAR GAMBAR
Gambar Halaman
Gambar 1.1: Kerangka penelitian ... 5
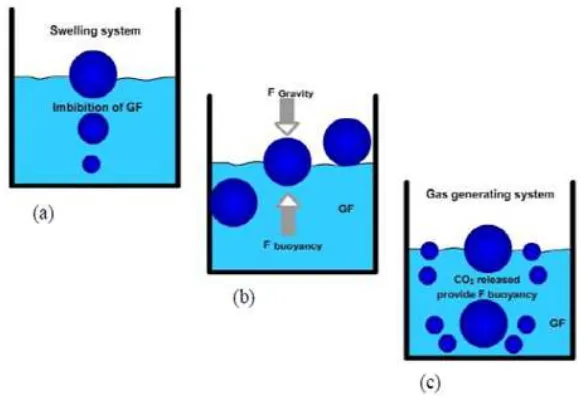
Gambar 2.1: Mekanisme sistem floating ... 8
Gambar 2.2: Skematik tegangan permukaan antara material polimer bioadhesif dan mukosa saluran cerna ... 13
Gambar 2.3: Ikatan mekanis melalui interpentrasi rantai polimer Bioadhesif dan rantai polimer mukus ... 14
Gambar 2.4: Struktur kimia metronidazol ... 15
Gambar 2.5: Struktur kimia alginat (a. monomer alginat, b. konformasi alginat, c. distribusi monomer) ... 18
Gambar 2.6: Struktur kimia kitosan ... 20
Gambar 2.7: Struktur kimia eudragit ... 23
Gambar 2.8: Disolusi obat dari suatu padatan matriks ... 27
Gambar 4.1: A. Formula 1, B. Formula 2, C. Formula 3, D. Formula 4, E. Formula 5, F. Formula 6, G. Formula 7, H. Formula 8, I. Formula 9, J. Formula 10, K. Formula 11 ... 39
Gambar 4.2: Foto SEM beads alginat-kitosan (perbesaran 50x, 500x .dan 1000x) ... 40
Gambar 4.3: Foto SEM beads alginat-kitosan salut eudragit rs 100 30% (perbesaran 50x, 500x dan 1000x) ... 40
Gambar 4.4: Foto SEM beads alginat-kitosan salut eudragit rs 100 30% dan kalsium alginat (perbesaran 50x, 500x dan 1000x) ... 41
Gambar 4.5: Pengukuran floating lag time dari floating mucoadhesive beads ... 42
Gambar 4.6: Pengukuran floating time dari floating mucoadhesive beads ... 43
Gambar 4.7: Grafik pengaruh konsentrasi eudragit rs 100 terhadap laju pelepasan metronidazol dari beads ... 48
Gambar 4.9: Pengaruh penyalutan beads terhadap laju pelepasan
metronidazol dari beads ... 53
Gambar 4.10: Grafik kinetika pelepasan orde Higuchi dari pelepasan
metronidazol dari beads Formula 1 ... 55
Gambar 4.11: Grafik kinetika pelepasan orde Korsmeyer-peppas dari
pelepasan metronidazol dari beads Formula 1 ... 56
Gambar 4.12: Grafik kinetika pelepasan orde Higuchi dari pelepasan
metronidazol dari beads Formula 2 ... 56
Gambar 4.13: Grafik kinetika pelepasan orde Korsmeyer-peppas dari
pelepasan metronidazol dari beads Formula 2 ... 57
Gambar 4.14: Grafik kinetika pelepasan orde Higuchi dari pelepasan
metronidazol dari beads Formula 3 ... 57
Gambar 4.15: Grafik kinetika pelepasan orde Korsmeyer-peppas dari
pelepasan metronidazol dari beads Formula 3 ... 58
Gambar 4.16: Grafik kinetika pelepasan orde Higuchi dari pelepasan
metronidazol dari beads Formula 4 ... 58
Gambar 4.17: Grafik kinetika pelepasan orde Korsmeyer-peppas dari
pelepasan metronidazol dari beads Formula 4 ... 59
Gambar 4.18: Grafik kinetika pelepasan orde Higuchi dari pelepasan
metronidazol dari beads Formula 5 ... 59
Gambar 4.19: Grafik kinetika pelepasan orde Korsmeyer-peppas dari
pelepasan metronidazol dari beads Formula 5 ... 60
Gambar 4.20: Grafik kinetika pelepasan orde Higuchi dari pelepasan
metronidazol dari beads Formula 6 ... 60
Gambar 4.21: Grafik kinetika pelepasan orde Korsmeyer-peppas dari
pelepasan metronidazol dari beads Formula 6 ... 61
Gambar 4.22: Grafik kinetika pelepasan orde Higuchi dari pelepasan
metronidazol dari beads Formula 7 ... 61
Gambar 4.23: Grafik kinetika pelepasan orde Korsmeyer-peppas dari
pelepasan metronidazol dari beads Formula 7 ... 62
Gambar 4.24: Grafik kinetika pelepasan orde Higuchi dari pelepasan
metronidazol dari beads Formula 8 ... 62
Gambar 4.25: Grafik kinetika pelepasan orde Korsmeyer-peppas dari
pelepasan metronidazol dari beads Formula 8 ... 63
Gambar 4.27: Grafik kinetika pelepasan orde Korsmeyer-peppas dari
pelepasan metronidazol dari beads Formula 9 ... 64
Gambar 4.28: Grafik kinetika pelepasan orde Higuchi dari pelepasan
metronidazol dari beads Formula 10 ... 64
Gambar 4.29: Grafik kinetika pelepasan orde Korsmeyer-peppas dari
pelepasan metronidazol dari beads Formula 10 ... 65
Gambar 4.30: Grafik kinetika pelepasan orde Higuchi dari pelepasan
metronidazol dari beads Formula 11 ... 65
Gambar 4.31: Grafik kinetika pelepasan orde Korsmeyer-peppas dari
DAFTAR LAMPIRAN
Lampiran Halaman
Lampiran 1: Sertifikat analisis metronidazol ... 71
Lampiran 2: Kurva serapan larutan metronidazol 12 mcg/ml dalam medium lambung buatan pH 1,2 ... 72
Lampiran 3: Pengukuran kurva kalibrasi larutan metronidazol dengan berbagai konsentrasi pada panjang gelombang 277 nm dalam mMedium pH 1,2 ... 73
Lampiran 4: Data pelepasan metronidazol dari beads Formula 1 ... 74
Lampiran 5: Data pelepasan metronidazol dari beads Formula 2 ... 76
Lampiran 6: Data pelepasan metronidazol dari beads Formula 3 ... 78
Lampiran 7: Data pelepasan metronidazol dari beads Formula 4 ... 80
Lampiran 8: Data pelepasan metronidazol dari beads Formula 5 ... 83
Lampiran 9: Data pelepasan metronidazol dari beads Formula 6 ... 86
Lampiran 10: Data pelepasan metronidazol dari beads Formula 7 ... 89
Lampiran 11: Data pelepasan metronidazol dari beads Formula 8 ... 92
Lampiran 12: Data pelepasan metronidazol dari beads Formula 9 ... 95
Lampiran 13: Data pelepasan metronidazol dari beads Formula 10 ... 97
Lampiran 14: Data pelepasan metronidazol dari beads Formula 11 ... 101
Lampiran 15: Data AUC pelepasan metronidazol dari floating mucoadhesive beads Formula 1 ... 104
Lampiran 16: Data AUC pelepasan metronidazol dari floating mucoadhesive beads Formula 2 ... 105
Lampiran 17: Data AUC pelepasan metronidazol dari floating mucoadhesive beads Formula 3 ... 106
Lampiran 18: Data AUC pelepasan metronidazol dari floating mucoadhesive beads Formula 4 ... 107
Lampiran 20: Data AUC pelepasan metronidazol dari floating
mucoadhesive beads Formula 6 ... 109
Lampiran 21: Data AUC pelepasan metronidazol dari floating mucoadhesive beads Formula 7 ... 110
Lampiran 22: Data AUC pelepasan metronidazol dari floating mucoadhesive beads Formula 8 ... 111
Lampiran 23: Data AUC pelepasan metronidazol dari floating mucoadhesive beads Formula 9 ... 112
Lampiran 24: Data AUC pelepasan metronidazol dari floating mucoadhesive beads Formula 10 ... 113
Lampiran 25: Data AUC pelepasan metronidazol dari floating mucoadhesive beads Formula 11 ... 114
Lampiran 26: Uji statistik Formula 1-6 ... 115
Lampiran 27: Uji statistik Formula 7-11 ... 117
Lampiran 28: Uji statistik pengaruh penyalutan ... 118
Lampiran 29: Gambar alat ... 119
Formulasi dan Evaluasi Secara In Vitro Floating Mucoadhesive Beads dari Metronidazol dengan Basis Alginat-Kitosan
Abstrak
Salah satu kendala utama pada pengobatan ulkus yang disebabkan oleh H. pylori dengan sediaan konvensional adalah waktu tinggal obat yang singkat didalam lambung. Adapun beberapa sistem penghantaran obat ke lambung adalah
floating dan mucoadhesive. Adapun tujuan dari penelitian ini adalah untuk membuat sediaan yang dapat bertahan lebih lama dalam lambung yang memiliki sifat floating dan mucoadhesive.
Floating mucoadhesive beads dibuat dengan menggunakan basis alginat kitosan dan dibuat dalam 11 formula dengan 3 kelompok formula. Kelompok 1 (F1) tanpa penyalutan, kelompok 2 (F2-F6) salut Eudragit RS 100, dan kelompok 3 (F7-F11) salut pertama dengan Eudragit RS 100 dan salut kedua dengan kalsium alginat. Diameter sediaan diukur dengan menggunakan micrometer.
Floating lag time dan floating time diukur pada gelas beker yang berisi medium lambung. Sifat mucoadhesive dari beads diuji dengan menggunakan tensiometer DuNoy menggunakan lambung tikus. Efisiensi penjeratan diukur terhadap 20 beads dan ditentukan jumlah metronidazol yang terjerat didalam beads. Pelepasan metronidazol dari beads dilakukan dengan menggunakan metode dayung USP dalam medium lambung buatan (pH 1,2). Kadar metronidazol diukur dengan menggunakan spektrofotometer ultraviolet pada panjang gelombang 277 nm.
Dari pengukuran didapat diameter beads adalah 2,70 mm sampai 3,27 mm.
Floating lag time dari semua beads adalah 0 menit sedangkan floating time lebih dari 12 jam. Dari uji mucoadhesive didapat gaya mucoadhesive adalah 1,14 sampai 2,06 dyne/mm2. Efisiensi penejaratan dari floating mucoadhesive beads berada pada rentang 62,24% sampai 76,46%. Pada uji pelepasan metronidazol dari beads menunjukkan bahwa beads dapat dijadikan pelepasan terkontrol, dimana semakin tinggi konsentrasi Eudragit RS 100 maka laju pelepasan metronidazol dari beads semakin lambat. Dari percobaan ini didapat hasil maksimal yaitu pada F11 dimana beads dapat melepaskan 83% metronidazol dalam 12 jam. Kinetika pelepasan metronidazol dari beads mengikuti kinetika pelepasan model Higuchi. Berdasarkan hasil penelitian maka dapat disimpulkan bahwa F11 adalah potensial digunakan sebagai sediaan sustained release gastro retentive drug delivery system dari metronidazol.
BAB I PENDAHULUAN
1.1Latar Belakang
Sistem penghantaran obat tinggal di lambung sangat menguntungkan
untuk beberapa obat untuk meningkatkan bioavailabilitas dan menurunkan dosis
terapinya. Diantara berbagai sediaan sistem tinggal di lambung, floating dan bio
(muco)-adhesive adalah yang paling banyak diteliti untuk meningkatkan efek
terapi dan meningkatkan bioavailabilitas sediaan yang tinggal di lambung
(Malakar dan Nayak, 2013).
Daya mengapung sistem floating dibatasi jumlah cairan lambung yang
hanya mempunyai persentase yang sedikit pada komposisi isi lambung untuk
mengapung sehingga sediaan dapat jatuh dan terbawa keluar dari lambung, daya
mengapung dari sediaan mungkin sangat terbatas yaitu hanya 3-4 jam (waktu
pengosongan lambung normal). Sistem bioadhesive menempel pada lapisan epitel
mukosa lambung, yang mana dapat terlepas dari mukosa dan dibawa keluar dari
lambung akibat adanya pengaruh dari motilitas lambung. Keterbatasan dari sistem
floating dan mucoadhesive tersebut memungkinkan untuk menggabungkannya
menjadi sistem floating bioadhesive yang akan dapat meningkatkan waktu kontak
dengan lapisan epitel lambung, efikasi terapetik dan bioavailabilitas obat (Rathi,
et al., 2012).
Bahan bahan yang berpotensi pada pembuatan sediaan mucoadhesive
untuk penghantaran obat merupakan biopolimers yang dapat digunakanan pada
dilaporkan dari penelitian sebelumnya yaitu pektin, natrium karboksi metil
selulosa (Na CMC), natrium alginat dan kitosan ( Ali dan Bakalis, 2011).
Menurut penelitian sebelumnya, polielektrolit kompleks dalam bentuk
mikrosphere dan beads yang dibentuk oleh polimer kationik dan polimer anionik
dapat meningkatkan waktu pelepasan obat atau pelepasan terkontrol. Contoh
polielektrolit kompleks untuk mengontrol pelepasan obat yang sering digunakan
yaitu alginat/kitosan, kitosan-mikropartikel multicore selulosa, kitosan berlapis
pektin, kitosan/poli (asam akrilat) kompleks, poli (vinil alkohol)/natrium alginat,
poli (acid-g-metakrilat etilena glikol) partikel (Piyakulawat, et al., 2007).
Menurut Honary, et al., (2009), telah terjadi peningkatan minat dalam
studi alginat-kitosan sebagai mikropartikel untuk penghantaran terkontrol pada
protein dan obat karena sifatnya yang biokompatibel, biodegradable dan sifat
mucoadhesivenya. Sebuah studi pada penggabungan kitosan dengan alginat
menggunakan label radioaktif pada kitosan menunjukkan bahwa ikatan kedua
polimer menunjukkan dengan jelas adanya sifat mengurangi berat molekul
rata-rata kitosan dan meningkatkan porositas dari alginat gel.
Kitosan (diperoleh dari deasetilasi kitin) adalah polimer kationik yang
telah banyak diusulkan untuk digunakan dalam pembuantan sediaan beads oleh
sejumlah peneliti. Kitosan terpilih sebagai polimer dalam pembuatan
mucoadhesive microsphere/beads karena memiliki sifat mucoadhesive yang baik
dan bersifar biodegradable (Patel, et al., 2005). Sedangkan alginat memiliki sifat
yang unik dalam pembentukan gel dengan adanya kation multivalent seperti
ion-ion kalsium dalam medium air. Penambahan polikation-ion seperti kitosan dengan
yang bermuatan negatif. Ketika butiran kalsium-alginat ditambahkan ke dalam
larutan kitosan, interaksi elektrostatik gugus karboksilat dari alginat dengan gugus
amin dari kitosan menghasilkan pembentukan sebuah membran. Proses ini telah
banyak digunakan dalam pembuatan membran alginat-kitosan dengan inti gel
kalsium-alginat yang padat. Ada banyak keuntungan penyalutan dengan kitosan,
seperti peningkatan jumlah muatan obat dan sifat bioadesive, juga sifat pelepasan
obat yang diperlama (Farahani, et al., 2006).
Untuk penelitian lebih lanjut tentang pemanfaatan alginat dan kitosan
maka peneliti tertarik untuk meneliti pembuatan floating mucoadhesive beads dari
alginat kitosan dengan menggunakan metronidazol sebagai model obat.
Metronidazol adalah obat antibiotik yang digunakan terutama dalam pengobatan
infeksi yang disebabkan oleh organisme yang rentan, terutama bakteri anaerob
dan protozoa. Metronidazol diserap dengan baik secara oral dengan eliminasi
plasma dengan waktu paruh mulai 6 - 7 jam (Mourya, et al., 2010). Karena waktu
paruh eliminasinya singkat, maka metronidazol perlu dibuat dalam bentuk sediaan
pelepasan terkontrol yang bertahan dalam lambung seperti mucoadhesive beads.
1.2Perumusan Masalah
Berdasarkan uraian diatas, diambil perumusan masalah yaitu:
a. Apakah beads dari metronidazol dengan basis alginat-kitosan merupakan
sediaan floating-mucoadhesive?
b. Apakah pelepasan metronidazol dari beads floating-mucoadhesive dengan
1.3Hipotesis
a. Beads dari metronidazol dengan basis alginat – kitosan merupakaan
sediaan floating-mucoadhesive.
b. Pelepasan metronidazol dari beads floating-mucoadhesive dengan basis
alginat kitosan merupakan pelepasan terkontrol.
1.4Tujuan Penelitian
a. Untuk mengetahui sifat floating-mucoadhesive sediaan beads dari
metronidazol dengan basis alginat–kitosan.
b. Untuk mengetahui pelepasan terkontrol metronidazol dari beads floating
-mucoadhesive dengan basis alginat-kitosan.
1.5Manfaat Penelitian
Manfaat penelitian ini adalah untuk mengetahui sifat floating
-mucoadhesive dan profil pelepasan metronidazol dari beads floating
-mucoadhesive alginat - kitosan dalam perkembangan penelitian tentang
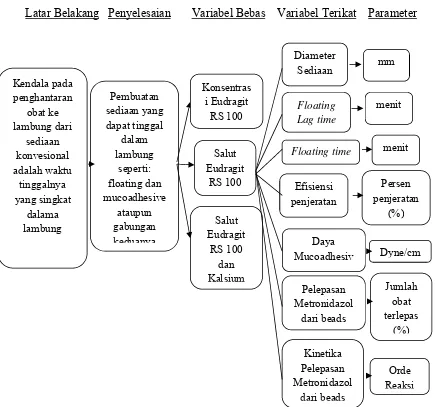
1.6Kerangka Penelitian
Penelitian ini dilaksanakan dengan mengacu pada kerangka konsep seperti
ditunjukkan pada Gambar 1:
Latar Belakang Penyelesaian Variabel Bebas Variabel Terikat Parameter
Gambar 1.1. Kerangka penelitian
BAB II
TI NJAUAN PUSTAKA
2.1 Ulkus Peptikum (Peptic Ulcer)
Ulkus peptikum merupakan daerah ekskoriasi mukosa yang disebabkan
kerja pencernaan getah lambung. Penyebab ulkus peptikum yang biasa adalah
terlalu banyak sekret getah lambung dalam hubungannya dengan derajat
perlindungan yang diberikan oleh lapisan mukus lambung dan duodenum serta
netralisasi asam lambung oleh getah duodenum. Diingatkan bahwa semua daerah
yang dalam keadaan normal terpapar getah lambung disuplai banyak kelenjar
mukosa, mulai dengan kelenjar mukosa komposita pada bagian bawah esofagus,
kemudian lambung, sel leher mukosa glandula gastrika, glandula pilorika dalam
yang terutama menyekresi mucus, akhirnya kelenjar Brunner pada duodenum atas
yang menyekresi mukus yang sangat alkali (Guyton, 1990).
Selain dari perlindungan mukus dari mukosa, duodenum juga dilindungi
oleh sekresi usus halus yang alkali, yang mengandung banyak natrium bikarbonat
yang menetralkan asam hidroklorida getah lambung, jadi menonaktifkan pepsin
sehingga mencegah pencernaan mukosa. Dua mekanisme tambahan yang
menjamin netralisasi getah lambung (Guyton, 1990) adalah:
1. Bila asam yang berlebihan masuk duodenum ia secara refleks menghambat
sekresi dan peristaltik lambung, karena itu mengurangi kecepatan
pengosongan lambung. Hal ini memungkinkan sekret pankreas mempunyai
waktu yang lebih lama untuk masuk ke duodenum dan menetralkan asam
2. Adanya asam dalam usus halus mengeluarkan sekretin dari mukosa usus
halus, kemudian sekretin melalui darah menuju ke pancreas untuk
merangsang sekresi cepat getah pankreas mengandung natrium bikorbat
konsentrasi tinggi, jadi membuat lebih banyak natrium bikarbonat tersedia
untuk menetralkan asam.
2.2 Gastroretentive Drug Delivery Sistem
Sistem penghantaran obat tinggal di lambung (GDDS) adalah salah satu
cara untuk memperpanjang waktu tinggal sediaan di dalam lambung, dengan
maksud untuk pemberiaan obat lokal pada saluran cerna bagian atas ataupun
untuk efek sistemik (Nayak, et al., 2010). Keuntungan dari penggunaan sistem
penghantaran obat tinggal di lambung adalah untuk menurunkan perubahan
pelepasan obat, pengobatan lokal dan aksi lokal, dan untuk meningkatkan
bioavailabilitas obat yang absorpsinya terbatas di dalam saluran cerna. Adapun
metode untuk membuat sediaan tinggal di lambung adalah:
- Penambahan bahan yang memperlambat pelepasan, seperti makanan, atau
obat, sebagai contoh propanthilen.
- Penggunaan bahan yang berat jenisnya tinggi: bahan dengan berat jenis tinggi
( 2.5g/cm3) akan mempunyai waktu tinggal yang lama di saluran cerna. Hal
ini dapat dicapai dengan penambahan bahan seperti barium sulfat.
- Pengubahan ukuran/bentuk sistem penghantaran dengan menggunakan
lapisan polimer, balon hidrogel yang mengembang, atau polimer yang
mempunyai ukuran besar untuk melewati sphingter pylorus.
- Sistem bioadesi. Sistem ini memunyai daya lengket terhadap mukosa.
pengosongan lambung. Sistem ini tidak dipengaruhi waktu pengosongan
lambung dan mempunyai pengaruh gravitasi yang kecil dibandingkan bahan
bahan lain yang terdapat di lambung (Aulton, 2008).
2.3 Sistem Floating
Sistem floating atau Hydrodynamically controlled sistem adalah sistem
yang memiliki berat jenis rendah yang mempunyai kemampuan untuk mengapung
(floating) diatas isi lambung dan kemampuan di dalam lambung tanpa dipengaruhi
laju pengosongan lambung pada suatu periode waktu yang lama. Ketika sistem ini
mengapung pada komposisi lambung, obat dilepas secara perlahan pada laju yang
diinginkan. Setelah melepaskan obat, sisa dari sediaan akan dikeluarkan dari
lambung (Arora, et al., 2005).
2.3.1 Pembagian sistem floating
Sistem penghantaran floating dibagi berdasarkan pada variable
formulasinya: effervescent dan sistem non-effervescent.
2.3.1.1 Bentuk sediaan floating effervescent
Ada beberapa jenis matriks yang dipakai untuk membantu pembuatan
sediaan floating yaitu polimer yang dapat mengembang seperti metil selulosa dan
kitosan dan berbagai bahan effervescent, sebagai contoh natrium bikarbonat,
asam tartrat, dan asam sitrat. Sistem ini diformulasi dimana ketika sediaan kontak
dengan asam lambung, akan dilepaskan gas CO2 dan gas terperangkap dalam
hidrokoloid yang mengembang sehingga sediaan akaan mempunyai kemampuan
untuk mengapung.
2.3.1.2 Bentuk sediaan floating non-effervescent
Bentuk sediaan floating non-effervescent menggunakan bentuk gel atau
jenis hidrokoloid selulosa yang dapat mengembang, polisakarida, dan polimer
bentuk matriks seperti polikarbonat, poliakrilat, polimetakrilat, dan polistiren.
Metode formulasi mecakup pendekatan sederhana dengan cara mencampur obat
dengan pembentuk gel-hidrokoloid. Setelah pemberian oral sediaan akan
mengembang ketika kontak dengan cairan lambung dan membentuk massa
dengan berat jenis 1. Udara yang terjerat di dalam matriks yang mengembang
membuat sediaan akan mengapung (Arora, et al., 2005).
2.3.2 Keuntungan FDDS
Keuntungan FDDS adalah sebagai berikut:
1. Sistem floating sangat menguntungkan untuk obat yang dimaksudkan untuk
aksi lokal seperti lambung. Contoh: antasida
2. Obat obat yang bersifat asam seperti aspirin dapat menyebabkan iritasi pada
dinding lambung ketika berkontak dengan lambung. Oleh karena itu FDDS
3. Sistem floating sangat menguntungkan untuk obat obat yang diabsorpsi di
saluran cerna. Contoh: Garam Fero, antasida
4. Penghantaran obat yang diperpanjang seperti sediaan floating, tablet atau
kapsul, akan terdisolusi di dalam cairan lambung. Sediaan floating terlarut
pada cairan lambung akan segera diabsorbsi di usus halus setelah waktu
pengosongan lambung.
5. Semua obat akan diabsorpsi secara sempurna dari bentuk sediaan floating
walaupun dalam larutan dengan pH alkali di saluran pencernaan.
2.3.3 Kerugian FDDS
Adapaun kerugian dari sistem FDDS adalah:
1. Sistem floating tidak cocok untuk obat obat yang mempunyai kelarutan dan
stabilitas yang rendah di saluran pencernaan.
2. Sistem ini membutuhkan cairan lambung yang banyak untuk menjaga sediaan
tetap mengapung.
3. Obat obat yang secara cepat dieliminasi dari tubuh seperti obat-obat yang
megalami first pass metabolism tidak cocok menjadi kandidat obat ini
(Gopalakrishnan dan Chenthilnathan, 2011).
2.4 Sistem Mucoadhesive
2.4.1 Pengertian bioadhesive
Isitilah bioadhesive digunakan untuk menjelaskan ikatan antara dua
permukaan biologi atau ikatan antara permukaan biologi dengan permukaan bahan
bahan sintesis. Pada sistem penghantaran obat dengan bioadhesive ini digunakan
penghantaran obat sistem bioadhesive adalah jaringan sel halus (seperti sel epitel),
pada kenyataannya ikatan mungkin terjadi dengan lapisan sel, lapisan mukus,
ataupun kombinasi dari keduanya. Ikatan antara mukus dengan polimer, disebut
juga dengan mucoadhesive yang digunakan sebagai sinonim bioadhesive. Pada
umumnya, bioadhesive adalah istilah yang digunakan untuk menggambarkan
ikatan dari sistem biologis atau derivat substansi biologis, dan mucoadhesive
hanya digunakan untuk menggambarkan ikatan yang mencakup mukus dan
permukaan mukosa (Chickering dan Mathiowitz, 1999).
2.4.2 Mekanisme bioadhesive
Untuk membuat sistem penghantaran obat sistem bioadhesive, ini sangat
penting untuk menggambarkan dan menngetahui gaya yang berperan penting
dalam pembentukan bentuk ikatan adhesif. Banyak penelitian yang focus untuk
menganalisis interaksi bioadhesive dengan polimer hidrogel dan jaringan halus.
Adapun proses yang mencakup pembentukan ikatan bioadhesive telah
digambarkan dalam tiga langkah yaitu: (a) pembasahan dan pengembangan
polimer untuk memulai kontak dengan jaringan biologis, (b) Interpenetrasi rantai
polimer bioadhesive dan penggabungan rantai polimer dan rantai mukus, (c)
pembentukan ikatan kimia yang lemah pada penggabungan rantai polimer dan
mukus (Chickering dan Mathiowitz, 1999).
a. Ikatan kimia
Tipe ikatan kimia mencakup ikatan yang kuat yaitu ikatan primer seperti
ikatan kovalen), dan juga ikatan kimia yang lemah seperti ikatan sekunder seperti
digambarkan pada buku ini, kedua jenis interaksi tersebut telah dimanfaatkan
untuk membuat sediaan sistem bioadhesive (Chickering dan Mathiowitz, 1999).
Meskipun sistem ini didesain untuk membentuk ikatan kovalen dengan
protein pada permukaan sel akan mengasilkan beberapa keuntungan, namun ada
tiga faktor yang membatasi kegunaan dari ikatan yang permanen. Pertama, lapisan
mukus mungkin menghambat secara langsung kontak antara polimer dengan
jaringan. Kedua, ikatan kimia yang permanen dengan epitel mungkin tidak akan
menghasilkan yang dapat bertahan lama karena pada umumnya sel epitel
diregenerasi setiap 3 sampai 4 hari. Ketiga, biokompatibilas dari ikatan yang dapat
menghasilkan masalah signifikan (Chickering dan Mathiowitz, 1999).
Untuk alasan itu, maka banyak penelitian yang difokuskan pada
pembuatan hidrogel, sistem mucoadhesive yang memiliki ikatan kimia yang lain
seperti interaksi van der Waals atau ikatan hydrogen. Selanjutnya, polimer yang
memiliki berat bolekul besar dan dengan konsentrasi reaktif yang tinggi, yaitu
gugus polar (seperti –COOH dan –OH) yang berperan dalam pembuatan ikatan
mucoadhesive (Chickering dan Mathiowitz, 1999).
b. Ikatan mekanis atau fisika
Ikatan mekanis dapat terjadi seperti interaksi fisika antara permukaan yang
sama untuk menggambungkan dua bentuk susunan. Secara makroskopik, ikatan
ini dapat dilihat penggabungan fisik dari rantai mukus dengan rantai polimer yang
fleksibel dan/atau interpenetrasi dari rantai mukus kedalam pori dari substrat
polimer. Laju penetrasi rantai polimer kedalam lapisan mukus tergantung pada
fleksibelitas rantai dan koefisien difusi masing masing. Kekuatan dari ikatan
yang mempengaruhi kekuatan ikatan mencakup keberadaan air, waktu kontak
antar material, dan panjang dan fleksibilitas rantai polimer (Chickering dan
Mathiowitz, 1999).
2.4.3 Teori bioadhesive
A. Teori elektronik
Hipotesis dari teori elektronik didasarkan pada asumsi bahwa material
bioadhesive dan material target biologis mempunyai struktur elektorn yang
berbeda. Pada asumsi ini, ketika dua material kontak satu sama lain, akan terjadi
perpindahan electron untuk menghasilkan bentuk yang stabil, yang menyebabkan
pembentukan dua lapisan pada muatan electron yaitu pada material bioadhesive –
permukaan material biologis (Chickering dan Mathiowitz, 1999).
B. Teori adsorpsi
Teori adsorpsi menyatakan ikatan bioadhesive dibentuk antara suatu
substrat bioadhesive dan jaringan atau mukosa melalui interaksi van der Waals,
ikatan hydrogen, dan gaya yang berkaitan. Meskipun gaya yang dihasilkan lemah,
namun jumlah dari interaksi dapat menghasilkan adhesive yang kuat (Chickering
dan Mathiowitz, 1999).
C. Teori pembasahan
Gambar 2.2. Skematik tegangan permukaan antara material polimer
Kemampuan dari bioadhesive atau mukus untuk menyebar dan
membentuk kontak yang mandalam dengan substrat yang cocok adalah salah satu
faktor yang penting pada pembentukan ikatan. Teori pembasahan, ditemukan pada
umumnya pada adhesive cairan, menggunakan tegangan antar permukaan untuk
memperhitungan penyebaran dan sifat adhesifnya (Chickering dan Mathiowitz,
1999).
D. Teori difusi
Konsep dari interpenetrasi dan penggabungan rantai polimer bioadhesive
dengan rantai polimer mukus menghasilkan ikatan adhesive yang semipermanen
yang disebut dengan teori difusi. Teori ini menganggap ikatan akan semakin kuat
dengan meningkatnya tingkat penetrasi dari rantai polimer kedalam lapisan
mukus. Penetrasi dari rantai polimer kedalam lapisan mukus, tergantung dari
gradien konsentrasi dan koefisien difusi.
Gambar 2.3: Ikatan mekanis melalui interpentrasi rantai polimer bioadhesive
dan rantai polimer mukus
E. Teori fraktur
Barangkali teori yang paling banyak diaplikasikan pada pemahaman
tentang bioadhesive melalui pengukuran secara mekanis adalah teori fraktur.
2.5 Metronidazol
2.5.1 Sifat fisika kimia metronidazol
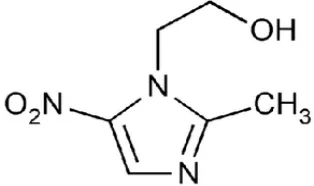
Struktur metronidazol dapat dilihat pada gambar 2.1 dibawah ini:
Gambar 2.4. Struktur kimia metronidazol
Rumus kimia metronidazol adalah C6H9N3O3 dengan nama kimia
2-metil-5-nitroimidazol-1-etanol, mempunyai berat molekul 171,16. Metronidazol
mengandung tidak kurang dari 99,0% dan tidak lebih dari 101,0% C6H9N3O3,
dihitung terhadap zat yang telah dikeringkan. Pemberiannya antara lain: hablur
atau serbuk hablur; putih hingga kuning pucat; tidak berbau; stabil di udara, tetapi
lebih gelap bila terpapar oleh cahaya. Sukar larut dalam eter; agak sukar larut
dalam air, dalam etanol dan dalam kloroform (Ditjen POM, 1995).
2.5.2 Farmakologi
Metronidazol memperlihatkan daya amubisid langsung. Pada biakan E.
histolytica dengan kadar metronidazol 1 - 2 µg/mL, semua parasit musnah dalam
24 jam. Sampai saat ini belum ditemukan amuba yang resisten terhadap
metronidazol. Metronidazol juga memperlihatkan daya trikomonoiasid langsung.
Pada biakan Trichomonas vaginalis, kadar metronidazol 2,5 µg/mL dapat
mengancurkan 99% parasit dalam waktu 24 jam. Trofozit Giardia lambia juga
dipengaruhi langsung pada kadar antara 1 - 50 µg/mL. Namun, saat ini telah
dilaporkan bahwa Trichomonas vaginalis dan Giardia lambia secara klinis
2.5.3 Farmakokinetik
Metronidazol diserap dengan baik setelah pemberiaan oral dan dianjurkan
sebagai obat penyeling atau pengganti pada penyakit intestinal yang ringan dan
berat, serta yang tanpa gejala. Satu jam setelah pemberian dosis tunggal 500 mg
per oral diperoleh kadar plasma kira-kira 10 µg/mL. umumnya untuk kebanyakan
protozoa dan bakteri yang sensitif, rata rata diperlukan kadar tidak lebih dari 8
µg/mL (Syarif dan Elysabeth, 2013; Foye, 1996)
Waktu paruhnya berkisar antara 8-10 jam. Pada beberapa kasus terjadi
kegagalan karena rendahnya kadar sistemik. Ini mungkin disebabkan oleh
absorpsi yang buruk atau metabolisme terlalu cepat. Obat ini diekskresi melalui
urin dalam bentuk asal dan bentuk metabolit hasil oksidasi dan glukuronidasi.
Metronidazol juga diekskresi melalui air liur, air susu, cairan vagina, dan cairan
seminal dalam kadar yang rendah (Syarif dan Elysabeth, 2013).
2.5.4 Efek Samping
Efek samping nampaknya banyak dan terutama menyangkut saluran
lambung-usus, persendian, dan saraf rasa. Adapaun efek samping tersebut adalah
mual, muntah, gangguan pengecapan, lidah kasar, gangguan saluran cerna, ruam,
urtikaria dan angioudem; kadang kadang timbul rasa lesu, mengantuk pusing,
ataksia, urin bewarna gelap dan anafilaksis. Neuritis perifer pada penggunaan
jangka panjang, serangan epilepsy transein, leukopenia (Foye, 1996; Sukandar,
dkk., 2008).
2.6 Alginat
Alginat adalah kopolimer yang tersusun dari α-L-Guluronat dan β-D-Mannuronat.
Alginat komersil umumnya diproduksi dari Laminaria hyperborean, Macrocystis
pyrifera, Laminaria digitata, Ascophyllum nodosum, Laminaria japonica, Edonia
maxima, Lessonia nigrescens, Durvillea Antarctica, dan Sargassum sp (Draget, et
al., 2005).
Berikut ini adalah tabel perbandingan asam uronat dari berbagai spesies
alga, yaitu:
Tabel 2.1. Menunjukkan perbandingan asam uronat dalam berbagai sepsies alga .. ..yang ditentukan dengan spektroskopi NMR high-field.
Jenis FG FM FGG FMM FGM,MG
Laminaria japonica
Laminaria digitata
Laminaria hyperborea, blade
Laminaria hyperborea, stipe
Laminaria hyperborean, outer cortex
Lessonia nigerescens
Ecklonia maxima
Macrocystis pyrifera
Durviella antarctia
Ascophyllum nodosum, fruiting body
Ascophyllum nodosum, old tisue
0,35
Perbandingan yang bervariasi dari asam uronat menyebabkan perbedaan
sifat produk yang dihasilkan. Alginat yang mengandung asam guluronat yang
2.6.2 Sifat alginat
Kelarutan alginat dalam air ditentukan oleh tiga parameter, yaitu:
- pH pelarut merupakan parameter penting karena akan menentukan adanya
muatan elektrostatik pada residu asam uronat
- Kekuatan ionik total zat terlarut juga memainkan peranan penting (efek
salting-out kation-kation non-gelling), dan
- Kandungan dari ion-ion pembentuk gel dalam pelarut membatasi kelarutan
(Draget, et al., 2005).
Alginat secara luas digunakan pada pambuatan produk makanan dan
sediaan farmasi oral maupun topikal. Alginat dipilih karena sifatnya yang
nontoksik dan juga tidak mengiritasi. Pada pembuatan tablet dan kapsul, alginat
digunakan sebagai pengikat dan bahan desintegran pada konsentrasi 1-5% w/w.
Alginat juga banyak digunakan sebagai bahan pengental dan suspending agent
pada pembuatan pasta, krim, dan gel; dan juga sebagai stabilizing pada pembuatan
emulsi minyak dalam air (Rowe, et al., 2009).
2.7 Kitosan
Kitin adalah salah satu polisakarida yang melimpah terdapat di alam.
Kitosan adalah polisakarida alam yang diperoleh melalui deacetilasi kitin yang
banyak ditemukan ditemukan pada kulit kepiting dan udang, kulit ari serangga,
dan pada dinding sel fungi. Kitosan mempunyai sifat yang aman, biokompatibel
dan biodegradebel. Penggunaan kitosan telah banyak dipakai pada penelitian
biopharmaceutical seperti mucoadhesive, peningkat penetrasi, teknologi vaksin,
terapi gen, dan penyembuh luka. Adapaun aplikasi kitosan adalah pada sediaan
2.7.2 Sifat kitosan
Kitosan dapat larut pada asam organic seperti asam formiat dan asam
asetat pada pH dibawah 6,2 melalui protonasi gugus amino bebas pada struktur
molekulnya. Kitosan sukar larut pada asam asetat murni. Pada umunya, sifat
larutan kitosan tergantung pada beberapa parameter seperti tingkat deacetilasi,
kekuatan ion, konsentrasi, temperature, konsentrasi asam, jenis asam, dan
distribusi gugus asetil di sepanjang rantai.
Sama seperti polimer alam pada umunya, kitosan mempunyai sifat
ampifilik yang mana dapat mempengaruhi sifat fisikanya dalam larutan dan
padatan. Hal ini ditunjukkan dengan adanya gugus hidrofil amino dan gugus
hidrofob acetamido pada struktur molekul. Tidak seperti polisakarida pada
umumnya, kitosan dapat mempunyai muatan positif yang kuat karena dia
memiliki jumlah gugus amino yang banyak, dengan demikian polimer ini
mempunyai banyak sifat yang sangat dapat digunakan seperti kemampuan untuk
bergabung dengan polimer lain ketika dicampur. Kitosan juga memiliki banyak
sifat yang menguntungkan seperti biodegredebel, biokompatibilitas, tidak toksik
dan mempunyai aktivitas antibakteri (El-Hefian dan Yahaya, 2010).
2.7.3 Aplikasi farmasetik kitosan
Kitosan mendapat perhatian yang serius sebagai bahan tambahan dalam aplikasi
farmasetik beberapa tahun belakangan ini, karena mempunyai bikompatibilitas
yang baik dan sifatnya yang tidak toksik pada penggunaan pembuatan sediaan
konvensional maupun bentuk sediaan yang baru. Adapaun aplikasi dari kitosan
(Yogeshkumar, et al., 2013) adalah sebagai berikut:
- Bahan pengikat pada granulasi basah
- Pembawa obat pada sistem mikropartikel
- Sistem penghantaran obat melalui Film
- Untuk membuat hidrogel, bahan yang digunakan untuk meningkatkan
viskositas.
- Bahan pembasah, dan untuk meningkatkan disolusi obat yang mempunyai
kelarutan yang rendah
- Disintegrant
- Polimer bioadesif
- Penghantaran obat terkontrol
- Untuk meningkatkan laju absorpsi.
2.8 Eudragit
Eudragit adalah suatu nama dagang dari perusahaan Jerman yaitu Rohm
GmbH & Co. KG. Darmstadt, yang pertama kali dipasarkan pada tahun 1950an.
Eudragit dibuat dengan cara polimerisasi asam akrilat atau asam metakrilat atau
bentuk esternya seperti butyl ester atau dimetilaminoetil ester. Polimer Eudragit
tersedia dalam banyak jenis dengan bentuk fisik yang berbeda (larutan dalam air,
larutan dalam pelarut organic, granul, dan serbuk). Tipe polimer Eudragit terbagi
atas (lihat Tabel 2.2).
2.8.1 Struktur Kimia
Polimer Eudragit adalah suatu kopolimer derivat bentuk ester dari akrilat
dam asam metakrilat, yang sifat fisika-kimianya ditentukan oleh gugus fungsinya
2.8.3 Aplikasi Eudragit pada penghantaran obat - Pada sistem penghantaran ke ophthalmik
Masalah utama yang dihadapi pada pengobatan mata adalah kemampuan
untuk mencapai konsentrasi yang optimal pada tempat kerja. Bioavailabilitas yang
rendah dari obat pada sediaan obat mata adalah disebabkan oleh produksi air
mata, absorpsi yang kurang baik, lama tinggal obat, dan impermeabilitas dari
Table 2.2. Jenis dan pemerian polimer Eudragit Nama Bentuk
Aseton, alkohol
Aseton, alkohol
Air
Aseton, alkohol
epitel kornea. Eudragit memperlihatkan sifat yang baik, seperti tidak toksik,
bermuatan positif dan memiliki sifat sebagai pelepasan terkontrol yang
membuatnya cocok untuk aplikasi pada sediaan obat mata.
- Bukal dan sublingual drug delivery
Masalah yang umum dihadapi pada penghantaran obat ke bukal adalah
kurangnya waktu kontak sediaan dengan tempat absorpsi obat. Akibatnya, polimer
bioadesif merupakan pilihan yang tepat pada sistem penghantaran obat melalui
bukal. Polimer yang dapat lengket jaringan keras dan lunak telah digunakan
beberapa tahun terakhir pada dunia pembedahaan dan kedokteran gigi. Ada
beberapa golongan polimer yang telah diselidiki yang dapat digunakan sebagai
mukoadesif. Adapaun polimer sintetik yang tersusun dari monomer cyanoakrilat,
asam poliakrilat, dan derivate polimethacrylate .
- Gastroretentive Drug Delivery
Adapun sediaan gastroretentive yang diingini saat ini adalah; mempunyai
berat jenis yang rendah sehingga dapat membuat sediaan mengapung di dalam
cairan lambung, mempunyai berat jenis yang tingggi sehingga sediaan dapat
tinggal di bagian bawah lambung, membesar atau mengembang di dalam saluran
cerna (lambung) sehingga tidak akan dapat melewati sphinkter pylorus. Semua
teknik yang diiinginkan tersebut dapat kita dapat dengan menggunakan Eudragit
yang berbeda beda ( Joshi, 2013).
2.9 Disolusi
Disolusi adalah suatu proses dimana suatu fase padat dimasuki oleh suatu
pelarut dan membentuk suatu kesetimbangan larutan. Proses disolusi obat melalui
dan fase pelarut-pelarut dan interaksi zat terlarut –pelarut. Reaksi yang heterogen
yang merupakan keseluruhan proses pemindahan masa dapat dikategorikan
menjadi: (i) Pemindahan zat terlarut dari fase padat, dan (ii) Penyesuaian antara
zat terlarut didalam fase cair, dan (iii) Difusi dan/atau perpindahan zat terlarut
melalui antarmuka padat/cair ke dalam fase bulk (Kramer dan Dressman, 2005).
Disolusi merupakan tahapan yang membatasi atau tahap yang mengontrol
laju bioabsorpsi obat-obat yang mempunyai kelarutan rendah, karena tahapan ini
merupakan tahapan yang paling lambat dan berbagai tahapan yang ada dalam
tahapan pelepasan obat dari bentuk sediaanya dan perjalanannya kedalam sirkulasi
sistemik.
Laju dimana suatu padatan melarut didalam suatu pelarut dapat dihitung
dengan persamaan:
atau
Ket: M: massa zat terlarut
D: Koefisien difusi dari zat terlarut Cs: kelarutan zat padat
S: luas permukaan kontak’ C: konsentrasi zat terlarut
h: ketebalan lapisan difusi V: volume larutan
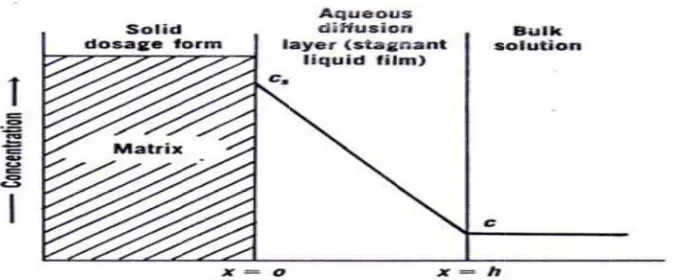
Dalam teori disolusi dianggap bahwa lapisan difusi air atau lapisan cairan
stagnan dengan ketebalan h ada pada permukaan zat padat yang sedang
berdisolusi. Ketebalan h ini menyatakan lapisan pelarut stasioner didalam mana
molekul molekul zat terlarut berada dalam konsentrasi dari Cs sampai C.
Dibelakang lapisan difusi statis tersebut, pada harga x yang lebih besar dari h,
terjadi percampuran dalam larutan, dan obat terdapat pada konsentrasi yang sama,
2. Faktor yang berhubungan dengan bentuk sediaan obat a. Faktor formulasi
Laju disolusi obat murni dapat dipengaruhi secara siknifikan dengan
penambahan bahan tambahan selama proses produksi pada pembuatan sediaan
padat.
b. Diluent dan desintegran
Dengan peningkatan konsentrasi desintegran (pati dari 5% - 20%)
menghasilkan peningkatan laju disolusi. Dengan penambahan bahan yang bersifat
hidrofobik akan menurunkan luas permukaan obat yang kontak sedangkan
dengan penambahan bahan hidrofilik akan meningkatkan luas permukaan kontak
sehingga akan meningkatkan laju disolusi dari obat.
c. Efek bahan pengikat dan bahan penggranulasi
Perbedaan bahan pengikat yang digunakan pada pembuatan tablet akan
menghasilkan profil disolusi yang berbeda pula. Granulasi basah adalah yang
paling umum digunakan untuk meningkatkan laju disolusi dari bahan obat yang
kurang larut dengan cara pemasukan bahan hidrofilik ke permukaan granul.
3. Faktor faktor yang berhubungan uji disolusi a. Temperature
Kelarutan obat sangan tergantung pada temperature, oleh karena itu
selama disolusi temperature harus dijaga dengan ketat dan dijaga perbedaannya
tidak lebih dari 0.5oC. Pada umumnya, temperature disolusi dijaga 37oC selama
b. pH medium disolusi
Pada umumnya dalam penelitian digunakan medium berupa 0,1 N HCl
atau larutan buffer yang pH nya disesuaikan dengan pH caira lambung (pH 1,2).
c. Tegangan permukaan medium disolusi
Tegangan permukaan medium menunjukkan pengaruh yang siknifikan
terhadap laju disolusi dari obat dan laju pelepasan dari sediaan padat.
d. Viskositas medium disolusi
Semakin tinggi viskositas medium, semakin kecil laju disolusi bahan obat
(Gennaro, 2000).
2.9.2 Metode disolusi
United States Pharmacopeia (USP) XXX memberi beberapa metode resmi
untuk melaksanakan uji pelarutan yaitu:
a. Metode Keranjang
Metode keranjang menggunakan bejana yang dibuat dari gelas atau bahan
yang inert, dan transparan dan silinder berbentuk keranjang. Bejana disolusi
dimasukkan kedalam penangas air yang cocok dan dengan ukuran yang tepat atau
dipanaskan dengan alat yang cocok seperti jaket pemanas. Penangas air atau alat
pemanas diatur sedemikian rupa sehingga suhu pada pejana dapat dijaga 37 ± 0,5
o
C sepanjang pegujian dan dijaga suhu tetap konstan. Kecepatan pengadukan
didasarkan pada kecepatan putaran batang penyangga dimana harus dijaga dengan
b. Metode Dayung
Menggunakan alat yang sama seperti alat 1 (metode keranjang), kecuali
keranjang yang ada pada alat 1 diganti dengan dayung sebagai pengaduk. Batang
penyangga diatur sedemikian rupa supaya jaraknya dari pusat tidak lebih dari 2
mm dari poros vertikal dari bejana dan berputar secara halus sehingga tidak ada
pengaruh siknifikan yang dapat mempengaruhi hasil pengujian. Jarak antara
dasar dayung dengan sampel (dasar labu) selama penghujian berada pada rentang
25 ± 2 mm dan dijaga tetap konstan.
Uji disolusi merupakan salah satu uji yang kritis dalam penentuan kuliatas
suatu produk. Pada umumnya, uji disolusi dari suatu sediaan padat oral
menggunakan metode keranjang (USP Appratus 1) atau metode dayung (USP
Appratus 2) dengan kecepatan pengadukan (100 rpm untuk metode keranjang dan
50 – 75 rpm dengan metode dayung), dengan menggunakan larutan buffer dengan
kisaran pH 1,2 - 6,8. Sampel disolusi dianalisis setiap interval 15 menit untuk
sedian lepas cepat (konvensional) atau interval satu jam pada sediaan extended
release sampil didapat persen kumulatis tidak kurang dari 85%. Untuk sediaan
yang tidak larut didalam air ditambahkan sedikit surfaktan untuk membentuk
kondisi sink (Kramer dan Dressman, 2005).
BAB III
METODE PENELITIAN
3.1Alat-Alat Penelitian
Alat disolusi metode dayung (Erweka), Spektrofotometer (Shimadzu
UV1800), TM3000 (BSE COMPO), Neraca Analitik (Boeco), Tensiometer
DuNoy, Magnetic Stirrer, gelas arloji, stopwatch, termometer, pH meter (Hanna),
jangka sorong, labu tentukur 1000 ml (MBL), labu tentukur 25 ml (Pyrex), beaker
glass 1000 ml (Pyrex), gelas ukur 1000 ml (Pyrex), gelas ukur 10 ml (Pyrex), mat
pipet 2 ml (MBL) dan alat-alat laboratorium yang biasa digunakan.
3.2 Bahan–Bahan Penelitian
Natrium alginat 500-600 cp (Wako Pure Chemical Industries, Ltd. Japan),
Metronidazol (Aarti Drugs, Ltd. India), Kitosan (Funakoshi, Co. Ltd. Japan),
Eudragit RS 100 dan bahan-bahan yang berkualitas pro analysis (E Merck):
kalsium klorida, asam klorida, natrium klorida, dan aseton. Aquadest diperoleh
dari laboratorium Farmasi Fisik, Fakultas Farmasi, USU.
3.3 Prosedur Penelitian
3.3.1 Pembuatan larutan kalsium klorida 0,15 M
Kalsium klorida ditimbang 22,053 gram kemudian dilarutkan dengan aqua
bebas CO2 secukupnya sampai 1000 ml (Ditjen POM, 1995).
3.3.2 Pembuatan medium lambung buatan (medium pH 1,2)
Natrium klorida sebanyak 2 g ditambahkan asam klorida pekat sebanyak 7
3.3.3 Pembuatan kurva serapan dan kurva kalibrasi metronidazol
3.3.3.1 Pembuatan larutan induk baku Metronidazol dalam medium pH 1,2 Metronidazol ditimbang 25 mg kemudian dimasukkan dalam labu tentukur
100 ml, diaduk sampai larut, kemudian dicukupkan dengan medium lambung
buatan (medium pH 1,2) sampai garis tanda. Konsentrasi metronidazol adalah 250
mcg/ml.
3.3.3.2 Pembuatan kurva serapan Metronidazol dalam medium pH 1,2
Dari larutan induk baku metronidazol dipipet 1,2 ml, dimasukkan kedalam
labu tentukur 25 ml, kemudian dicukupkan dengan medium lambung buatan
(medium pH 1,2) sampai garis tanda. Konsentrasi metronidazole adalah 12
mcg/ml. serapan diukur pada panjang gelombang 200–400 nm.
3.3.3.3 Pembuatan kurva kalibrasi Metronidazol dalam medium pH 1,2 Dari larutan induk baku metronidazol dibuat larutan metronidazol dengan
berbagai konsentrasi yaitu 1, 2, 4, 6, 8, 10, 12, 14, dan 16 mcg/ml dengan cara
memipet larutan induk baku masing-masing 0,1; 0,2; 0,4; 0,6; 0,8; 1; 1,2; 1,4 dan
1,6 ml kedalam labu tentukur 25 ml, kemudian ditambahkan dengan medium
lambung buatan (medium pH 1,2) sampai garis tanda. Serapan diukur pada
panjang gelombang maksimum yang diperoleh.
3.3.7 Penentuan diameter floating mucoadhesive beads
Beads yang sudah kering dipilih secara acak dan diameter beads
3.3.12 Uji pelepasan obat secara in vitro
Uji pelepasan obat dilakukan dengan menggunakan metoda dayung USP.
Kedalam wadah disolusi dimasukkan 900 mL medium disolusi dan diatur suhu
37±0,5OC dengan kecepatan pengadukan diatur 50 rpm. Ke dalam wadah tersebut
dimasukkan sejumlah beads yang setara 250 mg metronidazol. Pada interval
waktu tertentu diambil aliquot sebanyak 2 mL dan dijaga volumenya tetap 900
mL. Pengambilan dilakukan pada tempat yang sama yaitu pertengahan antara
permukaan medium disolusi dan bagian atas dari dayung tidak kurang 1 cm dari
BAB IV
HASIL DAN PEMBAHASAN
4.1 Pembuatan Floating Mucoadhesive Beads
Beads dibuat dengan menambahkan metronidazol ke dalam larutan alginat
kitosan yang kemudaian diteteskan ke dalam larutan CaCl2 menggunakan pipet
Komagome dan dibiarkan selama 15 menit dan selanjutnya dicuci dengan
aquadest selama 15 menit dan dikeringkan (Formula 1).
Untuk Formula 2-6, beads alginat kitosan yang sudah kering disalut
dengan larutan Eudragit RS 100 dengan konsentrasi tertentu. Beads dari Formula
1 dimasukkan kedalam larutan Eudragit RS 100 dan di stirrer selama 30 menit.
Setelah itu beads dikumpulkan dan dimasukkan kedalam lemari asam dibiarkan
sampai semua pelarut organik yang digunakan menguap sempurna sehingga tidak
terdapat residu pelarut organik di dalam beads yang dibuat.
Beads dari Formula 2-6, disalut kembali dengan larutan alginat 2% lalu
direndam dalam larutan CaCl2 dan langsung dibilas dengan aquadest lalu
dikeringkan (Formula 7-11).
4.2 Penenentuan Diameter Floating Mucoadhesive Beads
Diameter dari beads ditentukan dengan menggunakan alat micrometer.
Sebanyak lima buah beads diambil secara acak dan ditentukan diameternya.
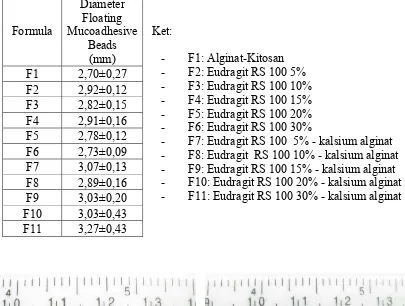
Diameter dari beads masing masing formula dapat dilihat pada table 4.1.
Berdasarkan hasil uji statistik dengan ANOVA (Analysis of variance) pada
interval konfidensi 95% (α = 0,05%) terhadap diameter beads tidak terdapat
langsung dapat dilihat adanya tiga kelompok diameter beads. Kelompok 1 yaitu
F1 yang memiliki diameter terkecil, kelompok 2 yaitu F2-F6 yang memiliki
diameter lebih besar dari kelompok 1, hal ini disebabkan karena pada F2-F6
adanya penyalutan dengan Eudragit RS 100, dan kelompok 3 yaitu formula 7-11
yang mempunyai diameter paling besar dari semuanya karena selain disalut
dengan Eudragit RS 100 formula ini juga disalut lagi dengan kalsium-alginat.
Table 4.1. Diameter floating mucoadhesive beads
Ket:
- F1: Alginat-Kitosan - F2: Eudragit RS 100 5% - F9: Eudragit RS 100 15% - kalsium alginat - F10: Eudragit RS 100 20% - kalsium alginat - F11: Eudragit RS 100 30% - kalsium alginat
Gambar 4.3: Formula 3 Gambar 4.4: Formula 4
Gambar 4.5: Formula 5 Gambar 4.6: Formula 6
Gambar 4.11: Formula 11
4.8 Pelepasan Metronidazol dari Floating Mucoadhesive Beads 4.8.1 Tanpa Penyalutan
Data pelepasan metronidazol dari Floating mucoadhesive beads pada F1
(tanpa penyalutan) dapat dilihat pada Tabel 4.6. Dari tabel dapat dilihat bahwa
floating mucoadhesive beads melepaskan metronidazol sebanyak 94,30% pada
waktu 180 menit. Dengan nilai AUC0-80% adalah 3215,22±28.11 %.menit.
4.8.2 Salut Eudragit RS 100
Pelepasaan metronidazol dari Floating Mucoadhesive beads F2-F6 yang
disalut dengan Eudragit RS 100 dapat dilihat pada tabel 4.6:
4.8.4 Perbedaan Jenis Penyalut
Pengaruh penyalutan floating mucoadhesive beads terhadap laju pelepasan
Gambar 4.19: Pengaruh penyalutan floating mucoadhesive beads terhadap laju pelepasan metronidazol dari beads
Dari Grafik 4.19 dapat dilihat dengan jelas penyalutan beads sangat
mempengaruhi laju pelepasan metronidazol dari floating mucoadhesive beads.
Dengan penyalutan Eudragit RS 100 didapat laju pelepasan metronidazol dari
beads semakin lambat dan ketika disalut lagi dengan kalsium-alginat, laju
pelepasan menjadi lebih lambat lagi.
Berdasarkan hasil uji statistik dengan Nonparametric Test (Kruskal Wallis
test) interval konfidensi 95% (α = 0,05%) terhadap AUC0-80% ketiga formula
didapat perbedaan yang signifikan nilai AUC dari setiap formula dengan nilai
signifikansi 0,027. Dimana urutan dari rendah ke tinggi adalah F1, F6, dan F7. 0
20 40 60 80 100 120
0 10 30 60 120 180 240 300 360 420 480 540 600 660 720 Tanpa Salut
Salut Eudragit RS 100
Salut Eudragit RS 100 dan Kalsium Alginat
Waktu (menit)
Jumlah
obat
terlepas
4.9 Kinetika Pelepasan Metronidazol dari Floating Mucoadhesive Beads Kinetika pelepasan metronidazol dari beads dilakukan terhadap empat
model matematika yaitu: orde nol, orde satu, model Higuchi dan
Korsmeyer-peppas. Penentuan kinetika pelepasan metronidazol dari beads dilakukan untuk
mengetahui berapa persen obat yang dilepaskan pada waktu-waktu tertentu.
Dengan memplotkan hasil uji pelepasan kesebelas formula dalam grafik
waktu versus persen kumulatif, logaritma persen kumulatif versus waktu, persen
kumulatif versus akar waktu dan logaritma persen kumulatif versus logaritma
waktu maka dapat diperoleh nilai korelasi (R2) dari masing- masing formula
matriks alginat- kitosan.
Tabel 4.9: Korelasi kinetika pelepasan metronidazol orde nol, orde satu, model Higuchi dan Korsmeyer-peppas dari beads
Formul
Dari tabel 4.9 dapat dilihat harga n dari F1 dan F2 adalah 0,584 dan 0,835
yang berarti mekanisme pelepasan melalui proses Anomalus (non-Fiks) yaitu
proses Super case 2 transport yaitu dimana laju penetrasi air lebih rendah dari
pada laju relaksasi polimer. Hal ini disebabkan karena Eudragit RS 100
merupakan polimer yang tidak larut dan tidak permeabel.
Dari hasil plot kesebelas formula seperti yang ditunjukkan pada Tabel 4.9,
diperoleh bahwa kinetika pelepasan untuk kesebelas formula adalah mengikuti
model Higuchi.
BAB V
KESIMPULAN DAN SARAN
5.1Kesimpulan
- Dari pengukuran mucoadhesive dan waktu floating menunjukkan bahwa
beads floating mucoadhesive memiliki sifat floating dan mucoadhesive
dengan floating lag time 0 menit dan floating time lebih dari 12 jam serta
daya mucoadhesive 1,14 – 2,06 dyne/cm2. Beads memiliki daya lengket
terhadap mukosa lambung dan juga memungkinkan untuk mengapung di
dalam lambung jika cairan lambung cukup tersedia.
- Profil pelepasan metronidazol dari beads menunjukkan hasil maksimal yaitu
pada F11 di mana beads dapat melepaskan 83% metronidazole dalam 12 jam.
Jadi dapat dibuktikan bahwa floating mucoadhesive beads dengan basis
alginat kitosan dapat dijadikan sediaan pelepasan terkontrol untuk obat obat
yang kerjanya di lambung ataupun saluran cerna bagian atas.
5.2 Saran
Disarankan pada peneliti selanjutnya untuk melanjutkan penelitian tentang
floating mucoadhesive beads dengan basis alginat kitosan secara in vivo untuk
melihat profil pelepasan obat dan mengetahui sifat floating dan mucoadhesive
secara in vivo.
DAFTAR PUSTAKA
Ali, M.F., dan Bakalis, S. (2011). Mucoadhesive Polymers for Food Formulation.
Procedia Food Science. 11(1): 68-75.
Arora, S., Ali, J., Ahuja, A., Kharm R.K., dan Baboota, S. (2005). Floating Druf Delivery System: A Review. AAPS PharmSciTech. 6(3): 375-378.
Aulton, M.E. (2007). Aulton’s Pharmaceutics: The Design and Manufacture of Medicines. Philadelphia: Elseiver. Hal. 483-499.
Chickering III, D.E., dan Mathiowitz, E. (1999). Theories of Bioadhesion. Dalam Bioadhesive Drug Delivery System: Fundamentals, Novel Approaches, and Development. New York: Marcel Dekker Inc. Hal. 1-8.
Ditjen POM. (1995). Farmakope Indonesia.Edisi IV. Jakarta: Departemen Kesehatan RI. Hal. 560-561: 1066, 1084-1085, 1143-1144.
Draget, K.I., Smidsrod O., dan Skjak, B.G. (2005). Polysaccharides and Polyamides in the Food Industry. Properties, Production, and Patents. Weinheim: Wiley-VCH Verlag GmbH & Co. KGaA: Hal. 1-20.
El-Hefian, E.A., dan Yahaya, A.H. (2010). Rheological Study of Chitosan and its Blends: An Overview. Maejo International Journal of Science and Technology. 4(2): 210-220.
Farahani, T.D., Farahani, E.V., dan Mirzadeh, H. (2006). Swelling Behaviour of Alginate-N-O_Carboxymethyl Chitosan Gel Beads Coated By Chitosan.
Iranian Polymer Journal. 15(5): 405-415.
Foye, W.O. (1996). Kimia Medisinal. Yogyakarta: Gadjah Mada University Press. Hal. 1604-1605.
Gennaro, A.R. (2000). Remington: The Science and Practice of Pharmacy. Edisi Keduapuluh. Philadelphia: Lippincott Williams & Wilkins. Hal. 654-665.
Gopalakrishnan, S., dan Chenthilnathan, A. (2011). Floating Drug Delivery System: A Review. Journal of Pharmaceutical Science and Technology.
3(2): 548-554).
Guyton, A.C. (1990). Fisiologi Manusia dan Mekanisme Penyakit. Jakarta: EGC Penerbit Buku Kedokteran. Hal. 606-608.