199
MEKANISME
DEOXYCORTICOSTERONE
ACETATE
(DOCA)-GARAM
TERHADAP PENINGKATAN TEKANAN DARAH PADA HEWAN COBA
Nour Athiroh Abdoes Sjakoer
*)
Nur Permatasari
**)
*)FMIPA-Jurusan Biologi Universitas Islam Malang
**) Laboratorium Farmakologi Fakultas Kedokteran Universitas Brawijaya
Abstract
Over the past 50 years various animal models of hypertension have been develop, predominantly in the rat. Various models of experimental hypertension have been primarily develop to obtain information on the etiopathogenesis of hypertension. The animal models of hypertension share many features which are common to human hypertension. Many of these models have been develop by utilizing the etiological factors are presumed to be responsible for human hypertension. Various studies have been done and continues to be developed as an integrated control of blood pressure regulation in animals with hypertension, so the strategy development, prevention, and treatment of hypertension can be treated with either. The most common human primary hypertension, is often presented by genetic models of hypertension such as SHR, Dahl, and Transgenic. As to demonstrate the role of the environment with models of stress. Secondary hypertension is affected by the kidneys (by the 2K1C method) and hormone (endocrine) with Deoxycorticosterone Acetate (DOCA)-salt method. To understand the pathogenesis and discuss the treatment and prevention of hypertension, it is necessary to develop the condition of hypertension animal models. A form of animal models of hypertension by the administration of DOCA. DOCA produces hypertension in rats. Mineralocorticoid DOCA is qualitatively the same role with the aldosterone. Mineralocorticoid hormones are involved in sodium retention. There is increased DOCA-induced reabsorption of salt and water leading to increased blood volume and hence increased blood pressure. There is also increased secretion of vasopressin leading to water retention and vasoconstriction. In addition, altered activity of RASS leads to increased sympathetic activity.
Keywords: Deoxycorticosterone Acetate (DOCA)-salt, blood pressure, sodium retension, and animal models hypertension
PENGANTAR
Hipertensi dan penyakit kardiovaskular adalah penyakit penyebab kematian yang paling umum yang terjadi diberbagai negara maju. Hipertensi merupakan penyakit multifaktorial yang melibatkan interaksi kompleks antara faktor genetik dan lingkungan. Penggunaan model hewan coba hipertensi telah memberikan informasi yang berharga mengenai berbagai aspek hipertensi, termasuk etiologi, patofisiologi, komplikasi, dan pengobatan. Etiologi hipertensi adalah heterogen, banyak model hewan percobaan telah dikembangkan untuk meniru aspek hipertensi manusia. Pilihan model hewan akan ditentukan berdasarkan tujuan penelitian, keterbatasan dana, dan keahlian teknis. Kategori model hipertensi adalah: renovaskular, parenkim ginjal, induksi farmakologi, akibat pengaruh lingkungan, dan genetik. Ada perbedaan besar antara hipertensi pada hewan dan manusia, termasuk perbedaan
dalam mekanisme homeostatis dan patofisiologi, sehingga pemahaman yang menyeluruh dari model hewan dan analisis yang teliti diperlukan sebelum ekstrapolasi temuan pada hewan untuk manusia (Plehm, et.al., 2009).
Pengembangan model eksperimental dari hipertensi telah banyak dikaji dari berbagai faktor yang terkait dengan pengaturan tekanan darah, pewarisan sifat-sifat hipertensi, dan tanggapan selular pada cedera. Model eksperimental memungkinkan pengembangan intervensi ditujukan tidak hanya pada penurunan tekanan darah, tetapi juga cedera organ target. (Lerman, et.al., 2005).
200
dipengaruhi oleh genetik maupun lingkungan (Pinto, et.al., 1998 ; Badyal, et.al., 2003).
Berbagai penelitian telah dilakukan dan terus dikembangkan sebagai pengendalian terpadu terhadap regulasi tekanan darah pada hewan hipertensi sehingga strategi pengembangan, pencegahan, dan pengobatan hipertensi dapat teratasi dengan baik. Dalam rangka untuk memahami patogenesis dan untuk mempelajari pengobatan dan pencegahan penyakit hipertensi, maka perlu mengembangkan model hewan kondisi hipertensi. Salah satu cara model hewan
hipertensi dengan pemberian
Deoxycorticosterone acetate (DOCA)-garam. DOCA-garam akan meningkatkan tekanan darah sehingga terjadi hipertensi.
Berdasarkan pemaparan tersebut perlu dikaji mekanisme DOCA-garam terhadap peningkatan tekanan darah serta model hewan hipertensi. Model penginduksian DOCA-garam pada hewan uji merupakan kajian yang penting untuk membuat hewan uji hipertensi.
Perumusan Masalah
Bagaimana mekanisme
Deoxycorticosterone acetate (DOCA)-garam terhadap peningkatan tekanan darah serta apa saja model hewan hipertensi?
Tujuan Penelitian
Untuk menjelaskan mekanisme Deoxycorticosterone acetate (DOCA)-garam terhadap peningkatan tekanan darah serta untuk mengetahui model hewan hipertensi.
Manfaat Penelitian
Memberikan informasi ilmiah tentang mekanisme Deoxycorticosterone acetate (DOCA)-garam terhadap peningkatan tekanan darah serta mengetahui model hewan hipertensi
TINJAUAN PUSTAKA Regulasi Tekanan Darah
Gambar 1. Regulasi Tekanan Darah Berbagai aktivitas organ yang berperan terhadap regulasi
yaitu otak, jantung, ginjal, dan pembuluh darah (Guyton, 1998)
.
Upaya menjaga agar aliran darah dalam sirkulasi sistemik tidak naik atau turun disebabkan oleh tekanan darah yang berubah-rubah, maka penting untuk mempertahankan tekanan arteri rata-rata dalam batas konstan. Hal tersebut dapat dicapai melalui serangkaian mekanisme yang meliputi (Guyton, 1998):
Pengaturan Melalui Saraf.
Pengaturan tekanan arteri dalam jangka waktu pendek selama beberapa detik atau menit, hampir seluruhnya dicapai melalui refleks saraf. Salah satu yang paling penting ialah refleks baroreseptor. Bila tekanan darah terlalu tinggi, reseptor khusus yang disebut baroreseptor akan diaktifkan. Reseptor tersebut terletak di dinding aorta dan arteri karotis interna. Baroreseptor kemudian mengirimkan sinyal ke medulaoblongata di batang otak. Dari media dikirimkan sinyal melalui susunan saraf otonom yang menyebabkan (a) pelambatan jantung, (b) pengurangan kekuatan kontraksi jantung, (3) dilatasi arteriol, dan (d) dilatasi vena besar. Kesemuanya bekerja bersama untuk menurunkan tekanan arteri ke arah normal. Efek sebaliknya terjadi bila tekanan terlalu rendah baroreseptor menghilangkan rangsangannya (Guyton, 1998 ; Taddei, et.al., 2002).
Sistem saraf simpatis merupakan bagian dari sistem saraf otonom, untuk sementara waktu akan meningkatkan tekanan darah selama respon reaksi fisik tubuh terhadap ancaman dari luar. Disamping itu juga meningkatkan kecepatan dan kekuatan denyut jantung, juga mempersempit sebagian besar arteri, tetapi memperlebar arteri di daerah tertentu (misalnya otot rangka, yang memerlukan pasokan darah yang lebih banyak). Ada kalanya mengurangi pembuangan air dan garam oleh ginjal, sehingga akan meningkatkan volume darah dalam tubuh. Melepaskan hormon epinefrin (adrenalin) dan norepinefrin (noradrenalin), merangsang jantung dan
pembuluh darah. (Goodman and Gilman’s,
2006).
Pengaturan Melalui Ginjal.
201 Mekanisme hemodinamik sangat sederhana.
Bila tekanan arteri naik melewati batas normal, tekanan yang besar dalam arteri renalis akan menyebabkan lebih banyak cairan yang disaring sehingga air dan garam yang dikeluarkan dari tubuh juga meningkat. Hilangnya air dan garam akan mengurangi volume darah, dan sekaligus menurunkan tekanan darah kembali normal. Sebaliknya bila tekanan turun di bawah normal, ginjal akan menahan air dan garam sampai tekanan naik kembali menjadi normal (Guyton, 1998 ; Oates and Brown, 2001).
Ginjal mengendalikan tekanan darah, jika tekanan darah meningkat, ginjal akan menambah pengeluaran garam dan air, dan akan menyebabkan berkurangnya volume darah dan mengembalikan tekanan darah ke normal. Jika tekanan darah menurun, ginjal akan mengurangi pembuangan garam dan air, sehingga volume darah bertambah dan tekanan darah kembali normal. Ginjal juga bisa meningkatkan tekanan darah dengan menghasilkan enzim yang disebut renin, yang memicu pembentukan hormon angiotensin, yang selanjutnya akan memicu pelepasan hormon aldosterone (Oates and Brown, 2001).
Mekanisme yang terlibat dalam mengontrol tekanan darah normal telah dimodifikasi, Regulasi tekanan darah dipengaruhi oleh peran ginjal. Bukti menunjukkan peran yang jelas untuk pemrograman dari ginjal dalam pengembangan hipertensi. Mekanisme utama yang dibahas sampai saat ini meliputi perubahan dalam fungsi ginjal sistem renin-angiotensin. Organ lain yang berperan yaitu sistem organ utama kardiovaskular (otak, pembuluh darah, dan jantung) dalam pemrograman hipertensi. Tubuh memiliki suatu sistem untuk mengatur tingginya tekanan darah, yakni sistem renin-angiotensin. Sel-sel tertentu dari ginjal dapat memprodusir renin, yang dilepaskannya bilamana tekanan darah di glomeruli menurun. Hal ini terjadi bila jumlah darah yang mengalir melalui ginjal berkurang, misalnya karena menurunnya volume darah atau karena penciutan setempat dari arteri ginjal. Dalam darah, renin bergabung dengan suatu zat protein tertentu dengan menghasilkan angiotensin yang antara lain memiliki khasiat meninggikan tekanan darah sebagimana neurohormon noradrenalin (vasokonstriksi) atau dengan jalan sekresi hormon aldosterone dengan retensi natrium dan naiknya volume darah (Oates and Brown, 2001 ; Taddei, et.al., 2002).
Pengaturan Melalui Jantung dan Pembuluh Darah
Pengaturan tekanan darah arteri rata-rata dilakukan dengan mengontrol curah jantung, resistensi perifer total dan volume darah. Tekanan darah arteri rata-rata adalah gaya rata-rata yang merupakan gaya utama yang mendorong darah ke jaringan. Tekanan ini harus diatur secara ketat karena tekanan tersebut harus cukup tinggi untuk menghasilkan gaya dorong, karena tanpa tekanan ini, otak dan jaringan lain tidak akan menerima aliran yang adekuat. Disamping itu tekanan tidak boleh terlalu tinggi sehingga menimbulkan beban kerja tambahan bagi jantung dan meningkatkan resiko kerusakan pada pembuluh (Taddei, et.al., 2002).
Faktor yang mempengaruhi curah jantung yaitu kecepatan denyut jantung dan volume sekuncup. Kecepatan denyut jantung ditentukan oleh pengaruh saraf otonom, sedangkan volume sekuncup ditentukan oleh aliran balik vena dan aktifitas simpatis. Aliran balik vena ditentukan oleh katup vena, denyut jantung, tekanan yang terjadi pada darah oleh kontraksi jantung, peningkatan aktifitas simpatis, pompa otot rangka, pompa respirasi, peningkatan volume darah. Faktor yang mempengaruhi resistensi perifer total yaitu jari-jari arteri dan viskositas darah. Jari-jari-jari arteri ditentukan oleh kontrol intrinsik dan ekstrinsik. Kontrol intrinsik digunakan untuk menyesuaikan aliran darah melalui suatu jaringan dengan kebutuhan metabolik jaringan tersebut dan diperantarai oleh faktor-faktor jaringan yang bekerja pada otot polos arteri. Kontrol intrinsik meliputi perubahan metabolik lokal menyangkut oksigen, karbondioksida, pengeluaran histamin respon miogenik terhadap peregangan. Kontrol ekstrinsik digunakan untuk mengatur tekanan darah terutama diperantarai oleh pengaruh simpatis dan otot-otot polos arteri. Kontrol ekstrinsik meliputi aktifitas simpatis, epinefrin, norepinefrin, angiotensinII, dan vasopressin. Sedangkan viskositas darah dipengaruhi oleh jumlah sell darah merah dan konsentrasi protein plasma (Taddei, et.al., 2002 ; Guyton, 1998).
202
jaringan berdilatasi, arteri di lingkungan lain akan mengalami konstriksi. Untuk mempertahankan tekanan darah arteri yang adekuat, darah mengalir tidak saja ke jaringan yang mengalami vasodilatasi, tetapi juga ke otak harus mendapat pasokan darah konstan. Tekanan arteri rata-rata dipantau oleh baroreseptor di dalam sirkulasi. Apabila reseptor mendeteksi adanya penyimpangan dari normal, akan terjadi respon refleks untuk memulihkan tekanan arteri ke nilai normal. Penyesuaiannya terdiri dari penyesuaian jangka pendek dan jangka panjang. Penyesuaian jangka pendek (dalam beberapa detik) dilakukan dengan mengubah curah jantung dan resistensi perifer total, diperantarai oleh pengaruh saraf otonom pada jantung, vena dan arteri. Penyesuaian jangka panjang (dalam beberapa menit atau hari) melibatkan penyesuaian volume darah total dengan memulihkan keseimbangan garam dan air (Guyton, 1998 ; Oates and Brown, 2001). Regulasi tekanan darah akan diketahui peranannya melalui pendekatan eksperimen hewan coba hipertensi. Berbagai eksperimen model hewan hipertensi mengacu pada organ-organ yang berpengaruh pada regulasi tekanan darah seperti otak, jantung, ginjal, dan pembuluh darah.
Kajian Model Hewan Hipertensi
Berbagai model hipertensii eksperimental telah dikembangkan terutama untuk memperoleh informasi tentang asal etiopatho-hipertensi. Model ini juga digunakan untuk pemeriksaan potensi agen antihipertensi secara farmakologis. Model hewan uji hipertensi dahulu jarang digunakan untuk pengujian obat antihipertensi potensial. Seiring dengan perkembangan ilmu dan teknologi, maka untuk membuktikan suatu mekanisme obat tertentu terhadap hipertensi maka penggunaan model hewan ditingkatkan untuk menjelaskan pengujian tersebut.
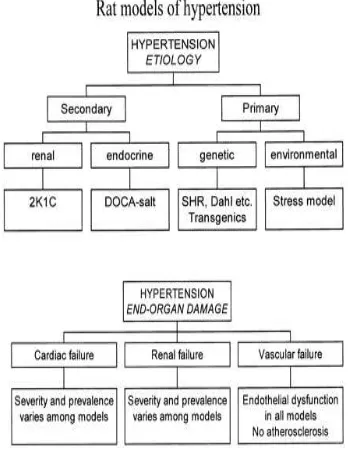
Gambar 2. Model Tikus Hipertensi
Bagan di atas menggambarkan etiologi hipertensi. Berdasarkan etiologinya, hipertensi terdiri dari hipertensi primer dan sekunder. Hipertensi primer dipengaruhi oleh faktor genetik dan peran lingkungan. Pada hipertensi primer, hewan uji tikus yang digunakan untuk membuktikan peran genetiknya yaitu SHR, Dahl, dan transgenik. Adapun untuk membuktikan peran lingkungannya yaitu dengan model stres. Hipertensi sekunder dipengaruhi oleh ginjal (dengan metode 2K1C) dan hormon (endokrin) dengan metode DOCA-garam. Bagan bawah menampilkan keterlibatan organ akhir yang terlihat dalam berbagai model tikus hipertensi (Sun and Zhang, 2005)
Akhir-akhir ini banyak hewan-hewan yang digunakan sebagai model hipertensi yang dimaksudkan untuk membuka wawasan baru patogenesis hipertensi. Hewan model dapat menggambarkan sebagian gambaran hipertensi pada manusia dan harus memenuhi kriteria sebagai berikut: termasuk kelompok hewan kecil, mudah diperlakukan dan diperbanyak, dapat digunakan untuk menduga potensi obat-obat antihipertensi, dapat bertahan dengan mengkonsumsi makanan yang dibatasi, dan dapat dibandingkan dengan hipertensi pada manusia. (Pinto, et.al., 1998 ; Badyal, et.al., 2003).
203 untuk model tertentu, perlu membandingkan
model tikus yang berbeda. Pada hipertensi primer menggunakan model stres, Spontaneous Hypertension Rat (SHR), Dahl, dan transgenik TGR (mRen2). Pada hipertensi sekunder meliputi deoxycorticosterone acetate (DOCA)-garam dan dua-ginjal satu-klip (2 Kydney 1 Clip = 2K1C). Pada umumnya hipertensi mempunyai gejala yang serupa, karena semua model menunjukkan hipertrofi jantung, dan semua menunjukkan gangguan relaksasi. Namun seringkali terjadi kerusakan pada akhir organ seperti gagal jantung, stroke, dan gagal ginjal, terjadi hanya dalam beberapa model tikus hipertensi. Beberapa obat mampu menurunkan tekanan darah, tetapi tidak mampu mencegah kerusakan akhir organ (misalnya hydralazine dalam model SHR). Dengan demikian tidak semua kelas antihipertensi sama-sama efektif dalam semua model tikus hipertensi. Endotelin tidak efektif dalam modell SHR, namun memiliki efek menguntungkan dalam modell DOCA-garam (Pinto, et.al., 1998).
Model hewan hipertensi dikembangkan sebagai wawasan baru untuk menjelaskan patogenesis hipertensi. Banyak model tersebut yang dikembangkan dengan menggunakan faktor-faktor penyebab yang diduga bertanggung jawab untuk hipertensi manusia, seperti konsumsi garam yang berlebihan, hiperaktif dari sistem Renin-Angiotensin-Aldosterone (RAAS) dan faktor genetik.. Hipertensi terjadi karena adanya kenaikan tekanan darah (Badyal, et.al., 2003).
Hipertensi esensial (primer) penyebab pasti belum diketahui. Berbagai faktor diduga sebagai penyebab hipertensi primer, seperti bertambahnya umur, stres psikologis, dan hereditas (keturunan). Kurang lebih 90% penderita hipertensi tergolong hipertensi primer sedangkan 10%-nya tergolong hipertensi sekunder. Pada 70-80% kasus hipertensi esensial, didapatkan riwayat hipertensi di dalam keluarga (Oates and Brown, 2001). Faktor lingkungan seperti stres, kegemukan (obesitas) dan kurang olahraga juga berpengaruh terhadap timbulnya hipertensi esensial (Oates and Brown, 2001). Hubungan antara stres dengan hipertensi, diduga melalui aktivasi saraf simpatis (Oates and Brown, 2001).
Hipertensi sekunder adalah hipertensi yang penyebabnya dapat diketahui, antara lain kelainan pembuluh darah ginjal, gangguan kelenjar tiroid (hipertiroid), penyakit kelenjar
adrenal (hiperaldosteroneisme), dan lain lain (Oates and Brown, 2001). Model tikus hipertensi sekunder dengan menggunakan model pemberian DOCA-garam atau dengan model 2K1C pada ginjal (Sun and Zhang, 2005).
Model Stress Hipertensi
Penelitian dari Knardahl et.al., (1988) dalam Pinto, et.al., (1998) pada tikus yang diberi stres dengan kejutan listrik pada kaki dan bunyi dapat meningkatkan tekanan darah dan peningkatan denyut jantung. Hal ini disebabkan karena adanya peningkatan adrenalin dan noradrenalin secara bermakna.
Denton et.al. dalam Zimmerman and Frohlich (1990) meneliti kelinci-kelinci yang diberi stres dengan meletakkan jaket pada punggung kelinci selama 10 hari. Asupan garam meningkat sampai 15 mmol/hari selama 10 hari dan menurun kadarnya sampai ke garis dasar setelah jaket diangkat. Untuk menentukan bahwa diet asupan garam atau stres yang menjadi penentu utama dari stres kronik yang menyebabkan hipertensi (chronic stress-induced hipertensi). Henry dan Stephen dalam Zimmerman and Frohlich (1990) mengevaluasi perubahan tekanan darah pada tiga kelompok tikus yang diberi stres secara psikososial dengan diet makanan yang mengandung 20, 30, dan 800 mmol natrium perhari selama 4 bulan. Ketiga kelompok tikus tersebut pada akhirnya terjadi kenaikan tekanan darah 40 mmHg selama 4 bulan, dengan demikian stres dapat menyebabkan perubahan tekanan darah tanpa bergantung pada asupan garam.
204
Efek ini dapat menyebabkan hipertropi endotel dan sepertinya menurunkan ukuran lumen, sehingga menyebabkan peningkatan tekanan. Disamping itu peningkatan aterosklerosis seringkali tampak pada hewan-hewan setelah stres kronik penginduksi hipertensi, yang juga mengurangi lumen dan dapat menyebabkan peningkatan tekanan darah yang irreversibel. Dengan munculnya teknik-teknik baru dalam bidang biologi seluler dan molekuler, mungkin akan ditemukan beberapa faktor-faktor penginduksi tekanan darah yang merangsang hipertropi dinding pembuluh darah (Badyal, et.al, 2003 ; Zimmerman and Frohlich, 1990 ).
Kajian SHR, Dahl, dan Transgenik Kajian SHR
Pada model SHR terjadi kerusakan organ akhir seperti hipertrofi jantung, gagal jantung dan disfungsi ginjal. Namun, tidak menunjukkan masalah pada pembuluh darah, aterosklerosis atau trombosis vaskular makroskopik, tidak memiliki kecenderungan untuk berkembang menjadi stroke pada kondisi awal, namun pada tahap berikutnya model SHR rawan menuju stroke dan mempunyai kecenderungan yang kuat untuk mati. SHR telah banyak digunakan untuk mengevaluasi faktor-faktor genetik dalam hipertensi. SHR adalah model yang paling populer, walaupun secara fakta hanya mewakili sebagian kecil dari beragam etiologi hipertensi (Pinto, et.al., 1998 ; Badyal et.al., 2003). Hipertensi pada model SHR terjadi pada 5-6 minggu, tekanan darah sistol mencapai 180 dan 200 mmHg. Pada umur 40-50 minggu sudah menunjukkan karakteristik penyakit kardiovaskular, seperti kerusakan pembuluh darah dan hipertrofi jantung (Pinto, et.al., 1998).
Kajian Dahl
Diet hipertensi terjadi peningkatan asupan garam secara fisiologis, ginjal normal memiliki kemampuan mengeluarkan beban garam sehari-hari tanpa memungkinkan peningkatan yang ditandai dalam volume ekstraseluler. Data epidemiologi telah menunjukkan bahwa semakin tinggi rata-rata asupan natrium pada populasi tertentu, maka semakin besar pula prevalensi hipertensi tersebut. Asupan tinggi garam, akan menyebabkan hipertensi seperti pada sampel tikus, kelinci dan anak ayam. Hipertensi terjadi setelah mengganti air minum dengan natrium
klorida 1-2% selama 9-12 bulan (Badyal, et.al., 2003)
Tikus sensitif garam Dahl menjadi hipertensi berat dan fatal ketika diberi makan diet tinggi garam, sedangkan tikus yang resisten garam tidak mengembangkan hipertensi berat. Tikus setelah mengkonsumsi garam (8% NaCl), tekanan darah naik tajam, ke tingkat sedikit lebih tinggi dari yang ditemukan di SHR. Meskipun hipertrofi jantung sebanding dengan yang ditemukan pada SHR (hingga 32%), terjadi gagal jantung usia 4-5 bulan (Badyal, et.al., 2003).
Model tikus hipertensi dengan pemberian propilthiourasil (1,25 mg/kg/hari) secara oral, NaCl (3,75 g/kg/hari) satu kali sehari selama 14 hari, dan pemberian dosis tunggal adrenalin (1,2 myu g/kg) secara intraperitonial. Hasil menunjukkan pemberian propilthiourasil (PTU) dan adrenalin meningkatkan denyut jantung (2,690 ± 0,1958 Hz dan 2,726 ± 0,2007 Hz). Pemberian NaCl meningkatkan stroke volume Atenolol menurunkan denyut jantung tikus yang diinduksi PTU (1,094 ± 0,2284 Hz) dan mencegah peningkatan denyut jantung tikus yang diinduksi adrenalin. Sedangkan kaptopril menurunkan stroke volume tikus yang diinduksi NaCl (Martha, 2007).
Transgenik Tikus Overexpressing Mouse
Ren2 Gen (TGR (mRen2)
Gen Ren-2 tikus menyebabkan hipertensi berat, mematikan pada tikus homozigot jika tidak diobati dengan ACE-inhibitor. Model tikus ini dicirikan oleh dua fitur penting yaitu bentuk dan warisan genetik hipertensi. Meskipun perubahan genetik sudah jelas diketahui, namun tetap sulit dipahami. Jelas bahwa hipertensi pada tikus ini terkait dengan aktivitas renin-meningkat, tetapi mekanisme jelasnya belum terungkap. Tikus heterozigot 70% bertahan hidup sampai usia 5 bulan. Penghambatan dari sistem renin -angiotensin efektif menurunkan tekanan darah, dan melemahkan perkembangan hipertrofi jantung dan meningkatkan relaksasi tergantung endotel (Badyal, et.al., 2003).
Dua-Ginjal Satu-Klip (2K1C=2 Kidney 1
Clip)
205 pengembangan beragam model hewan untuk
hipertensi. Pada hipertensi yang berlangsung lama, akan terjadi berbagai perubahan pada sistem neurohormonal yang terkait dengan keseimbangan cairan dan elektrolit. Dalam keadaan ini, korteks adrenal akan banyak menghasilkan aldosterone sebagai hormon yang bertanggung jawab terhadap keseimbangan cairan dan elektrolit. Konsekuensi dari keadaan ini adalah aldosterone akan mempengaruhi reseptor dan molekul signaling pada pembuluh darah sehingga menginduksi vasokonstriksi dan berefek langsung terhadap proses remodeling pada ventrikel kiri (Pinto, et.al., 1998 ; Badyal et.al., 2003).
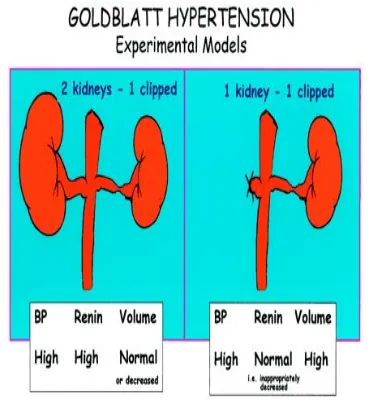
Gambar 3. Model Eksperimen Goldblatt Hipertensi Gambar kanan 2 ginjal satu jepitan menyebabkan peningkatan tekanan darah, kadar renin tinggi dan volume darah normal atau terjadi penurunan, gambar kiri 1 ginjal 1 jepitan menyebabkan tekanan darah tinggi, kadar renin normal, dan volume darah tinggi (Bruno, et.al., 2004)
Secara alami tikus 2K1C sebagian bergantung pada teknik yang digunakan untuk mempersempit arteri ginjal terutama pada ukuran klip dan usia tikus, akibatnya terjadi hipertrofi jantung berkisar 25-50%. (Pinto, et.al., 1998).
Armenia, dkk., (2007) telah melakukan penelitian menggunakan model tikus hipertensi dengan cara menjepit salah satu arteri ginjal tikus (tikus hipertensi Goldblatt 2K1C=2 Kidney 1 clip) suatu model yang secara klinis identik dengan hipertensi ginjal. Penggunaan model tikus ini analog dengan keadaan hipertensi ginjal secara klinis pada manusia. Dengan menggunakan model ini, respon
penurunan tekanan darah akibat pemberian obat akan lebih jelas teramati.
Tekanan darah tikus dikatakan hipertensi apabila tekanan darah sistol melebihi 120 mmHg (Guyton, 2006). Menurut Badyal, et.al., (2003); Sherwood (2007), penyempitan arteri ginjal merangsang pengeluaran renin dari sel juxtaglomerulus ginjal. Renin akan memecah angiotensinogen menjadi angiotensin I (AI). AI yang relatif tidak aktif dikonversi olah ACE menjadi angiotensin II (AII). AII bekerja pada reseptor otot polos vaskular, korteks adrenal, jantung, dan SSP untuk menimbulkan konstriksi arteri dan venul, stimulasi sintesis, dan sekresi aldosterone, stimulasi jantung dan saraf simpatis. Akibatnya terjadi peningkatan resistensi perifer, reabsorbsi natrium dan air, serta peningkatan denyut jantung dan curah jantung yang akhirnya meningkatkan tekanan darah. Hasil penelitian Armenia, dkk., (2007) 100% tikus Goldblatt 2K1C selama ± 4 minggu memperlihatkan peningkatan tekanan darah yaitu 169±24 mmHg. Menurut Badyal, et.al., (2003) tekanan sistol tikus Goldblatt 2K1C selama ±5 minggu adalah 170±9 mmHg.
Studi Perbandingan Model Hewan Coba Hipertensi
Berdasarkan paparan sebelumnya setiap model hipertensi mempunyai kelebihan dan kekurangan. Pelajaran yang paling penting dari perbandingan langsung dari model-model hewan adalah meskipun kasus hipertensi sangat heterogen, namun model hipertensi menunjukkan persamaan pada kerusakan organ. Semua model pada hewan uji tikus menunjukkan hipertrofi jantung, dan semua menunjukkan gangguan relaksasi yang bergantung endotel (isolated organ). Beberapa obat dapat menurunkan tekanan darah tetapi tidak mencegah kerusakan akhir organ (misalnya hydralazine dalam SHR). Selain itu, tidak semua kelas antihipertensi sama-sama efektif dalam semua model tikus hipertensi: endotelin-reseptor antagonis tidak efektif dalam SHR, namun memiliki efek menguntungkan dalam model DOCA-garam. Kelebihan pada model SHR dan transgenik, kemampuan untuk secara khusus memperkenalkan membangun genetik dan dengan demikian membiakkan hewan transgenik, juga telah membuka kemungkinan baru untuk penelitian hipertensi.
206
tikus transgenik seringkali hewan coba mengalami hipertensi berat dan hewan coba mendadak mati, model tersebut merupakan model hipertensi dengan renin tinggi. Model tikus hipertensi menampilkan berbagai macam gangguan biokimia, stres mekanik merupakan tingkat absolut tekanan darah, dan ketika di atas ambang tertentu akan selalu menyebabkan kerusakan organ (misalnya stroke SHR TGR rawan dan homozigot (mRen2). Walaupun SHR adalah model yang paling populer, namun secara fakta hanya mewakili sebagian kecil dari beragam etiologi hipertensi.
Alternatif berikutnya yaitu menggunakan model tikus hipertensi sekunder. Dalam rangka untuk menyelidiki morbiditas yang terkait dengan hipertensi, sangat relevan untuk memilih model dengan etiologi dapat diketahui sampai batas tertentu misalnya DOCA-garam, 2K1C, sehingga pendekatan yang lebih rasional dapat dilakukan. Aspek penting lainnya adalah bahwa model yang berbeda dapat dilihat untuk mewakili berbagai jenis hipertensi. Namun kelemahan pada model 2K1C tersebut bahwa model 2K1C merupakan model hipertensi renin tinggi. Pada hewan coba terjadi kerusakan akhir organ sangat tergantung pada angiotensin II dan sangat peka terhadap penghambatan RAAS, menyebabkan hipertensi berat, dan kematian dini pada hewan coba.
Disamping itu model tersebut relatif lama untuk meningkatkan tekanan darah. Pada model stres terjadi tekanan darah setelah 4 bulan, pada SHR terjadi kenaikan darah setelah 5-6 minggu, Dahl 9-12 bulan, 2K1C yaitu 4 minggu, model transgenik setelah 5 bulan. Bentuk yang lebih fatal dari kerusakan akhir organ seperti gagal jantung, stroke dan gagal ginjal, terjadi hanya dalam subset dari tikus hipertensi.
Berdasarkan fenomena tersebut, maka model Deoxycorticosterone acetate (DOCA)-garam lebih visible untuk dijadikan model hipertensi hewan coba. Hal-hal yang mendukung yaitu: pemaparan DOCA-garam lebih cepat meningkatkan tekanan darah yaitu setelah 1 bulan pemaparan atau pada minggu ke 8 terjadi kenaikan tekanan darah, jarang terjadi kerusakan organ yang fatal, pada DOCA-garam kadar renin rendah. Dengan demikian berikutnya akan dibahas mekanisme DOCA-garam pada peningkatan tekanan darah.
PEMBAHASAN
Kajian Deoxycorticosterone Acetate (DOCA)-Garam
Deoxycorticosterone adalah hormon steroid yang dihasilkan oleh kelenjar adrenal yang memiliki aktifitas sebagai mineralokortikoid dan bertindak sebagai prekursor aldosterone. Jalur utama untuk produksi aldosterone yaitu pada zona glomerulosa adrenal. Sebagian besar deoxycorticosterone sebagai cortexon, 11 deoxycorticosterone, deoxycortone B disekresikan oleh zona fasculiata dari korteks adrenal juga mensekresi kortisol. Pemberian suntikan deoxycorticosterone tidak menyebabkan ekskresi kalium bila asupan natrium rendah (Don and Lo, 2007).
DOCA-garam merupakan salah satu model hipertensi sekunder karena pengaruh endokrin (hormon). Hormon adalah zat yang dilepaskan ke dalam aliran darah dari suatu kelenjar atau organ yang mempengaruhi kegiatan di dalam sel-sel. Sebagian besar hormon merupakan protein yang terdiri dari rantai asam amino dengan panjang yang berbeda-beda. Sisanya merupakan steroid, yaitu zat lemak yang merupakan derivat dari kolesterol. Hormon dalam jumlah yang sangat kecil bisa memicu respon tubuh yang sangat luas. Deoxycorticosterone merupakan salah satu hormon yang dihasilkan di korteks adrenal (Blacker, 1992 ; Don and Lo, 2007).
207
Addison’s) mengarah pada hipotensi,
hyperkalemia, penurunan curah jantung, dan syok. Kelebihan mineralkortikoid menyebabkan hipertensi dan hypokalemia. Hormon terikat kepada reseptor di permukaan sel atau di dalam sel. Ikatan antara hormon dan reseptor akan mempercepat, memperlambat atau merubah fungsi sel. Pada akhirnya hormon mengendalikan fungsi dari organ secara keseluruhan, mengendalikan volume cairan dan
kadar air dan garam di dalam darah (Don and Lo, 2007).
Natrium adalah kation utama dalam cairan ekstraseluler dan hanya sejumlah kecil natrium berada dalam cairan intraseluler. Natrium menjaga keseimbangan asam dan basa di dalam tubuh dengan mengimbangi zat-zat yang membentuk asam. Natrium berperan dalam transmisi saraf dan kontraksi otot. Natrium berperan pula dalam absorpsi glukosa dan sebagai alat angkut zat-zat gizi lain melalui membran.. Kalium merupakan ion bermuatan positif, akan tetapi berbeda dengan ion natrium, kalium terutama terdapat di dalam sel, sebanyak 95% kalium berada di dalam cairan intraselluler. Peranan kalium mempunyai kemiripan dengan natrium, kalium bersama dengan klorida membantu menjaga tekanan osmotis dan keseimbangan asam basa. (Goodman and Gilman’s, 2006).
Perpindahan air diantara cairan ekstraseluler dan intraseluler ditentukan oleh kekuatan osmotik. Osmosis adalah perpindahan air menembus membran semipermiabel ke arah yang mempunyai konsentrasi partikel lebih rendah. Natrium klorida pada cairan ekstraseluler dan kalium dengan zat-zat organik pada cairan intraseluler, adalah zat-zat terlarut yang tidak dapat menembus dan sangat berperan dalam menentukan konsentrasi air pada kedua sisi membran. Hampir seluruh natrium yang dikonsumsi (3-7 gram sehari) diabsorpsi terutama di usus halus (Boulanger and Vanhoutte, 1994 ; Marney and Brown, 2007).
Mekanisme pengaturan keseimbangan volume tergantung pada perubahan volume sirkulasi efektif. Volume sirkulasi efektif adalah bagian dari volume cairan ekstraseluler pada ruang vaskuler yang melakukan perfusi aktif pada jaringan. Pada orang sehat volume cairan ekstraseluler umumnya berubah sesuai dengan sirkulasi efektifnya dan berbanding secara proporsional dengan natrium tubuh total. Natrium diabsorpsi secara aktif setelah itu
dibawa oleh aliran darah ke ginjal, natrium disaring dan dikembalikan ke aliran darah dalam jumlah yang cukup untuk mempertahankan taraf natrium dalam darah. Kelebihan Natrium yang jumlahnya mencapai 90-99 % dari yang dikonsumsi, dikeluarkan melalui urin. Pengeluaran urin ini diatur oleh hormon aldosterone yng dikeluarkan kelenjar adrenal bila kadar Natrium darah menurun. Aldosterone merangsang ginjal untuk mengasorpsi natrium kembali. Jumlah natrium dalam urin tinggi bila konsumsi tinggi dan rendah bila konsumsi rendah (Boulanger and Vanhoutte, 1994 ; Marney and Brown, 2007).
Garam dapat memperburuk hipertensi pada orang secara genetik sensitif terhadap natrium, misalnya orang Afrika-Amerika, lansia, dan orang hipertensi atau diabetes. Asosiasi jantung Amerika menganjurkan setiap orang untuk membatasi asupan garam tidak lebih dari 6 gram per hari. Pada populasi dengan asupan natrium lebih dari 6 gram per hari, tekanan darahnya meningkat lebih cepat dengan meningkatnya usia, serta kejadian hipertensi lebih sering ditemukan. Hubungan antara restriksi garam dan pencegahan hipertensi masih belum jelas. Namun berdasarkan studi epidemiologi diketahui terjadi kenaikan tekanan darah ketika asupan garam ditambah (Blacker, 1992).
208
Mekanisme Deoxycorticosterone Acetate
(DOCA)-Garam terhadap Peningkatan Tekanan Darah
Model endokrin hipertensi diinduksi oleh mineralokortikoid (Deoxycorticosterone Acetate). Mineralokortikoid dapat meningkatkan reabsorpsi ion Na+ serta ekskresi ion K+ serta H+ di tubulus distal pada hiperkortisisme. (Blacker, 1992).
Selye et.al. dalam Badyal, et.al., (2003) adalah orang yang pertama kali membuktikan bahwa Deoxycorticosterone Acetate (DOCA) menghasilkan hipertensi pada hewan uji tikus. DOCA termasuk mineralokortikoid menyebabkan retensi natrium dan air dalam tubuh sampai terjadi diuresis dan peningkatan tekanan pada ginjal. Pemaparan DOCA-garam menghasilkan hipertensi pada tikus (Badyal, et.al., 2003). Ada peningkatan reabsorbsi DOCA-diinduksi garam dan air menyebabkan volume darah meningkat dengan demikian terjadi peningkatan tekanan darah. Reabsorpsi natrium dapat menyebabkan peningkatan reabsorpsi air dan peningkatan tekanan darah. Ada peningkatan vasopresin menyebabkan retensi air dan vasokonstriksi. Aktifitas RAAS menyebabkan peningkatan aktivitas simpatis.
Deoxycorticosterone salah satu mineralkortikoid secara kualitatif mempunyai kemiripan dengan aldosterone, serta merupakan hormon steroid yang berperan penting pada ginjal. Untuk mengatur volume cairan ekstraseluler, aldosterone akan mengurangi ekskresi NaCl (garam) dengan cara mereabsorpsinya dari tubulus ginjal. Naiknya konsentrasi NaCl akan diencerkan kembali dengan cara meningkatkan volume cairan ekstraseluler yang pada gilirannya akan meningkatkan volume dan tekanan darah (Don and Lo, 2007).
Aldosterone aldosteroneisme merupakan suatu keadaan yang mempengaruhi kadar natrium, kalium, bikarbonat dan klorida dalam darah, yang menyebabkan tekanan darah tinggi. Aldosterone adalah hormon yang dihasilkan dan dilepaskan oleh kelenjar adrenal, memberikan sinyal kepada ginjal untuk membuang lebih sedikit natrium dan lebih banyak kalium. Pembentukan aldosterone sebagian diatur oleh kortikotropin pada hipofisa dan sebagian lagi oleh mekanisme kontrol pada ginjal (sistem renin-angiotensin-aldosterone). Renin adalah enzim yang dihasilkan di dalam ginjal dan bertugas mengendalikan pengaktifan hormon angiotensin, yang merangsang
pembentukan aldosterone oleh kelenjar adrenal (Boulanger and Vanhoutte, 1994 ; Marney and Brown, 2007).
Aldosterone merupakan
mineralokortikoid kuat yang mendukung retensi natrium dan peningkatan tekanan arteri. Terlepas dari kerjanya dalam meregulasi tekanan darah, aldosterone juga memiliki peran dalam terjadinya hipertrofi jantung. Dalam miokardium, aldosterone bekerja melalui reseptor mineralokortikoid untuk meningkatkan deposisi matriks ekstraselular dan kolagen. Adapun menurut Gharbawy, et.al., (2001) pada model binatang coba, konsentrasi aldosterone tinggi dalam sirkulasi menstimulasi terjadinya fibrosis pada miokardium, sehingga terjadi hipertrofi ventrikel kiri.
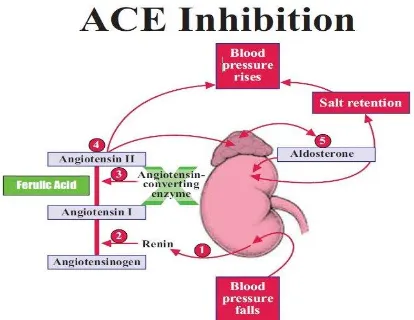
Gambar 4. Mekanisme ACEInhibition
1. Renin dihasilkan oleh ginjal sebagai respon terhadap adanya katekolamin, penurunan kadar natrium plasma, dan penurunan aliran darah ginjal
2. Renin selanjutnya mengubah angiotensinogen menjadi angiotensin I, yang merupakan dekapeptida yang tidak aktif
3. Angiotensin I diubah menjadi angiotensin II oleh ACE (Angiotensin-ConvertingEnzyme)
4. Angiotensin II berefek vasokonstriktor kuat, meningkatkan aktivitas sistim saraf simpatis, merangsang produksi aldosterone Dengan adanya angiotensin II sekresi aldosterone meningkat menyebabkan retensi garam natrium dan air. Keadaan ini akan meningkatkan tekanan darah (Boulanger, and Vanhoutte. 1994 dan Marney and Brown 2007) (Lakhanpal and Rai, 2008)
209 faktor utama menyebabkan kerusakan jaringan.
Kajian studi yang dilakukan terhadap senyawa ACE inhibitor dan Angiotensin II Receptor Blocker (ARB) dapat mencegah efek Ang II terhadap organ target (termasuk sistem kardiovaskular). Aldosterone memiliki peran independen terhadap perkembangan kerusakan jaringan kardiovaskular (Rocha, et.al., 2000).
Pada studi lain diketahui bahwa konsentrasi aldosterone berkorelasi dengan tingkat mortalitas kardiovaskular pada penderita-penderita dengan kondisi hipertrofi ventrikel kiri, memberikan bukti yang pasti mengenai efek merugikan dari aldosterone dan aktivasi reseptor mineralokortikoid. Keadaan hipertrofi ventrikel kiri ini berhubungan dengan peningkatan tingkat morbiditas dan mortalitas penderita dengan kondisi hipertensi esensial. Pada manusia, peningkatan konsentrasi plasma aldosterone berhubungan dengan disfungsi endotel, infark miokard, hipertrofi ventrikel kiri dan kematian (Brown, et.al., 2005). Aldosterone dapat menginduksi stres oksidatif dalam sel-sel arterial secara umum dan pada makrofag secara khusus. Hal ini mungkin dapat menghubungkan keterlibatan aldosterone dalam penyakit kardiovaskular (Keidar, et.al., 2004).
Studi lain pada binatang coba menunjukkan kemampuan aldosterone dalam menstimulasi matriks metaloproteinase (MMP) dan reactive oxygen species (ROS) pada kardiomiosit ventrikel tikus dewasa. Aktivitas MMP diduga diinduksi oleh aldosterone melalui aktivasi reseptor mineralokortikoid, protein kinase C (PKC), dan ROS dalam responnya terhadap stimulasi aldosterone (Rude, et.al., 2005).
Berbagai studi pada model binatang coba dan pada penderita dengan gagal jantung kongestif atau hipertensi menunjukkan bahwa aldosterone menginduksi stres oksidatif. Pada jantung dan ginjal, aldosterone menstimulasi stres oksidatif dan meningkatkan ekspresi penanda inflamasi yang mengarah kepada fibrosis. Sampai dengan saat ini, tidak banyak penelitian klinis yang mengungkap mekanisme yang mendasari hubungan antara aldosterone dengan stres oksidatif, respon inflamasi, dan remodeling matriks terhadap massa ventrikel kiri pada penderita hipertensi (Brown, et.al., 2005; Rude, et.al., 2005)
Ginjal adalah regulator utama kalium di dalam tubuh, menjaga kadarnya tetap di dalam darah dengan mengontrol eksresinya. Kadar kalium yang tinggi dapat meningkatkan
ekskresi natrium, sehingga dapat menurunkan volume darah dan tekanan darah. Kalium merupakan bagian esensial semua sel hidup, sehingga banyak terdapat dalam bahan makanan. Pengeluaran air dalam tubuh diatur oleh ginjal dan otak. Hipotalamus mengatur kosentrasi garam di dalam darah, dengan merangsang kelenjar pituitari mengeluarkan hormon antidiuretika (ADH). ADH dikeluarkan bila volume darah atau tekanan darah terlalu rendah. ADH merangsang ginjal untuk menahan atau menyerap kembali air dan mengeluarkannya kembali ke dalam tubuh (Boulanger and Vanhoutte, 1994 ; Marney and Brown, 2007).
Apabila terlalu banyak air keluar dari tubuh, volume darah dan tekanan darah akan turun. Sel-sel ginjal akan mengeluarkan enzim renin. Renin mengaktifkan protein di dalam darah yang disebut angiotensinogen ke dalam bentuk aktifnya angiotensin. Angiotensin akan mengecilkan diameter pembuluh darah sehingga tekanan darah naik. Disamping itu angiotensin mengatur ginjal untuk menahan natrium dan air. Akibatnya, bila dibutuhkan lebih banyak air, akan lebih sedikit air yang dikeluarkan dari tubuh dan tekanan darah akan naik kembali (Boulanger and Vanhoutte, 1994 ; Marney and Brown, 2007).
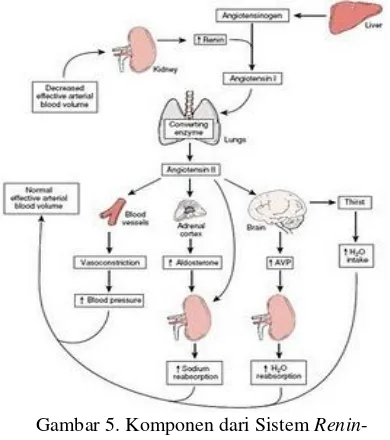
Gambar 5. Komponen dari Sistem Renin -Angiotensin-Aldosterone
210
tekanan darah, angiotensin pada kelenjar adrenal melepaskan hormone aldosterone terjadi reabsorbsi natrium dan air serta meningkatkan volume dan tekanan darah. Angiotensin II di otak akan meningkatkan AVP di ginjal terjadi reabsorbsi air (Ganong, 2002)
Konsumsi natrium yang berlebih menyebabkan konsentrasi natrium di dalam cairan ekstraselular meningkat. Untuk menormalkannya, cairan intraselular ditarik keluar, sehingga volume cairan ekstraselular meningkat sehingga meningkatkan volume darah. Konsumsi garam dalam jumlah yang tinggi dapat mengecilkan diameter arteri, sehingga jantung harus memompa lebih keras lagi untuk mendorong volume darah yang meningkat melalui ruang yang semakin sempit mengakibatkan terjadinya hipertensi. Asupan kalium yang meningkat akan menurunkan tekanan darah sistolik dan diastolik. Cara kerja kalium adalah kebalikan dari natrium. Konsumsi kalium yang banyak akan meningkatkan konsentrasinya di dalam cairan intraselular, sehingga cenderung menarik cairan dari bagian ekstraselular dan menurunkan tekanan darah (Karp, 2002 ; Goodman and
Gilman’s, 2006).
Proses yang mendasari
hiperaldosteroneisme primer adalah produksi aldosterone yang berlebihan secara otonom oleh korteks adrenal. Sekresi aldosterone yang tidak dapat dihambat dan tidak sensitif terhadap kadar renin plasma. Efek aldosterone adalah meretensi natrium sehingga airpun akan ikut teretensi. Retensi natrium dan air ini akan meningkatkan volume darah ke ginjal dan akan menekan sekresi renin. Hiperaldosteroneisme sekunder dapat disebabkan oleh produksi renin yang berlebihan karena ada penurunan aliran darah atau tekanan perfusi ginjal. Hipersekresi renin sekunder dapat disebabkan oleh penyempitan satu atau dua arteri utama ginjal karena arterosklerosis atau hyperplasia fibromuskuler. Produksi renin berlebihan maka kedua ginjal dapat terjadi nefrosklerosis arteriolar yang berat atau vasokonstriksi renal. Produksi renin yang berlebihan ini dipicu karena menurunnya volume darah, yang akhirnya meningkatkan sekresi renin dan aldosterone. Hal tersebut memberi efek retensi natrium dan air (Gharbawy, et.al., 2001 ; Brown, et.al., 2005).
Pada model DOCA sebaiknya menggunakan tikus betina yang masih muda,
karena rentan terhadap hipertensi yang diinduksi oleh DOCA-garam. Untuk menghasilkan hipertensi, tikus dengan berat sekitar 100 gram dipelihara dan diberi diet natrium klorida 2% sebagai pengganti minumnya. Setelah tikus mencapai berat sekitar 250 g, diberi DOCA yang dilarutkan dalam minyak biji wijen dengan dosis10 mg/kg, dua kali seminggu selama 43 hari (Badyal, et.al., 2003).
Nguyen, et.al., (1992) meneliti tentang respon reseptor endothelin 1 vaskular terhadap DOCA-garam hipertensi. Penurunan densitas reseptor endothelin-1 pada tikus hipertensi DOCA-garam menyebabkan penurunan aktivasi fosfolipase C, akibatnya mengurangi vasokonstriksi yang disebabkan oleh endothelin-1. Hal tersebut karena menurunnya efek vasokonstriktor endothelin-1 (kondisi tanpa endotel). Aorta dan arteri mesenterika tanpa endotel secara nyata menurunkan kadar endothelin-1. Endothelin-1 membran arteri lebih rendah pada hipertensi DOCA-garam daripada tikus yang telah dioperasi salah satu ginjalnya, namun mempunyai afinitas yang serupa.
Wang, et.al., (1994) melaporkan bahwa pemberian 100 mg DOCA-garam secara sub kutan pada tikus yang telah di uninephrectomy (dibedah salah satu ginjalnya). Kemudian tikus diberi larutan garam 1% sebagai air minumnya, setelah tiga minggu terjadi hipertensi. Pada minggu ke 8 setelah operasi tekanan darah tikus meningkat.
211 Hasil menunjukkan bahwa agonis V1 dan V2
mampu meningkatkan tekanan darah setelah pemberian DOCA-garam pada model hipertensi.
Penelitian tentang superoksida vaskular dan fungsi vasomotor pada hipertensi yang diinduksi DOCA-garam. Hasil tersebut menunjukkan bahwa peningkatan superoksida vaskular terjadi karena peran angiotensin II, namun bisa juga karena renin rendah. Kadar superoksida aorta (3972± 257 ; 852 ± 287) meningkat dibandingkan kontrol. Tekanan darah sistol (189 ± 4 ; 126 ± 2 mmHg). Peningkatan produksi superoksida mempengaruhi relaksasi pembuluh darah bergantung endotel, tetapi tidak memodulasi tekanan darah pada hipertensi renin rendah. Heparin-superoksida dismutase (1200 U/ dIV selama 3 hari) tidak mempunyai efek pada tekanan darah tetapi secara nyata berpengaruh terhadap relaksasi pada asetilkolin (Somers, et.al., 2000). Penelitian ini juga didukung oleh Ko, et.al., (2006) bahwa produksi superoksida vaskular, aktifitas oksidase NAD(P)H, ekspresi adhesi molekul-1 vaskular, dan infiltasi makrofag secara nyata meningkat pada tikus yang dipapar DOCA-garam.
Takaoka, et.al., (2001) meneliti suatu antioksidan asam lipoic-α untuk mencegah hipertensi dan injury pada hipertensi pada model tikus yang diinduksi oleh DOCA-garam. Tikus diberi DOCA-garam selama 2 minggu dan di beri asam lipoic-α (10 atau 100 mg/kg/hari). Tikus dengan ginjal yang telah dioperasi tanpa pemberian DOCA-garam sebagai kontrol. Tekanan darah sistol tikus yang dipapar DOCA-garam naik setelah 3-4 minggu. Setiap hari diberi 100mg/kg asam lipoic-α menekan peningkatan tekanan darah sistol, sementara pada pemberian asam lipoic-α 10 mg/kg tidak mempunyai efek pada tikus hipertensi yang diinduksi oleh DOCA-garam. Pembuluh darah aorta mengalami hipertropi setelah 4 minggu, namun pada pemberian asam lipoic-α 10 mg/kg hipertropi aorta mengalami penurunan. Pada aorta dan ginjal ditandai dengan peningkatan endothelin 1 pada tikus yang diinduksi oleh DOCA-garam. Dengan demikian pemberian asam lipoic-α pada tikus DOCA-garam mengurangi peningkatan tekanan darah dan melindungi terhadap injury pembuluh darah melalui penekanan pada produksi endothelin1 pembuluh darah dan ginjal.
Antagonis vasopressin diberikan secara intravena pada tikus yang telah di operasi salah
satu ginjalnya selama 6 minggu setelah pemberian DOCA-garam. Hasil penelitian terjadi penurunan 15 mmHg pada pemberian antagonis V1. Pada tikus yang diberi antagonis V1 dan V2, tekanan darah turun sampai 38 mmHg. Dengan demikian peran AVP (arginine vasopressin) pada tikus yang dipapar DOCA-garam berpengaruh pada pembuluh darah dan mempunyai efek pada ginjal (Hofbauer, et.al., 2011).
Hasil penelitian dari Awe et.al., (2003), tert_Butil Hidroperoksida (t-BOOH) meningkatkan vasokonstriksi pembuluh darah selama pemberian DOCA-garam, melibatkan radikal bebas dan penurunan ekspresi enzim antioksidan endogen, SOD (superoxide desmutase).
Penelitian peranan Axl pada hipertensi yang diiduksi DOCA-garam dilakukan dengan cara mencit Axl tipe liar (Axl+/+) dan mencit (Axl-/-) di operasi salah satu ginjalnya dan dipapar oleh DOCA-garam selama 6 minggu. Axl suatu reseptor tyrosine kinase yang diidentifikasi sebagai gen pada model genetik pada hipertensi sensitif garam. Axl berperan secara nyata pada remodeling vaskular yang diberi respon injury. Pada perlakuan DOCA-garam meningkatkan tekanan darah sistol 25 mmHg pada kedua mencit genetik setelah satu minggu. Tekanan darah sistol meningkat secara bermakna pada mencit (Axl+/+)-DOCA, sementara pada mencit (Axl-/-) tekanan darah sistol sama dengan kondisi kontrol setelah 6 minggu. DOCA-garam meningkatkan berat ginjal dan hipertropi glomerular 40 % dibandingkan dengan kontrol pada kedua model mencit genetik. Vasorelaksasi yang bergantung endotel terdapat pada mencit (Axl-/-), namun pada mencit (Axl+/+) tidak terjadi vasorelaksasi (Korshunov, et.al., 2007).
.
KESIMPULAN
212
(aldosteroneisme) merupakan suatu keadaan yang mempengaruhi kadar natrium, kalium, bikarbonat dan klorida dalam darah, yang menyebabkan tekanan darah tinggi.
2. Kajian model hewan hipertensi, berdasarkan etiologinya, hipertensi terdiri dari hipertensi primer dan sekunder. Hipertensi primer dipengaruhi oleh faktor genetik dan peran lingkungan. Pada hipertensi primer, hewan uji Tikus yang digunakan untuk membuktikan peran genetiknya yaitu SHR, Dahl, dan transgenik. Adapun untuk membuktikan peran lingkungannya dengan model stress. Hipertensi sekunder dipengaruhi oleh ginjal (dengan metode 2K1C) dan hormon (endokrin) dengan metode DOCA-garam.
SARAN
Perlu dikaji lebih lanjut peran herbal terhadap hipertensi yang dipapar oleh DOCA-garam pada hewan uji tikus.
DAFTAR PUSTAKA
Aaronson ML. 2011. Overweight Woman Pees Acid from Water Pill Excess. Online
www.michaelaaronsonmd.com/view.
Armenia. 2007. Daun Tanaman Akar Mambu (Connarus grandis Jack) sebagai Obat Antihipertensi : Efektivitas Ekstrak Etanolnya pada Tikus Hipertensi 2K1C Goldblatt. Jurnal Sains dan Teknologi Farmasi. Vol. 12. No. 2 : 100-107.
Awe so, Tsakadze NL, D’Souza SE, Adeagbo
AS. 2003. Tert-butyl Hydroperoxide-Mediated Vascular Responses in Doca-Salt Hypertensive Rats. Vascul
Pharmacol. Vol 40 No 1 : 51-7. Badyal H, Lata H, and Dadhich AP. 2003.
Animal Models of Hypertension and Effect of Drugs. Indian Journal of Pharmacology. Vol 35 : 349-362. Blacker C. 1992. Ovulation Stimulation and
Induction Endocrinol. Metab Clin North Am Vol 21:57.
Boulanger CM, Vanhoutte PM. 2004. The Endothelium: A Pivotal Role in Health and Cardiovascular Disease. Houston; P:9,16,24.
Brown NJ. 2005. Aldosterone and End-Organ Damage. Curr Opin Nephrol Hypertens Vol 14 : 235-241.
Bruno S, Remuzzi G, Ruggenenti P. 2004. Transplant Renal Artery Stenosis. J. Am Soc Nephrol. Vol 15: 134-141. Don BR and Lo JC. 2007. Endocrine
Hypertension. In: Gardner DG, Shoback D (Ed). Greenspan’s Basic & Clinical Endocrinology.. 6 th Ed. International Edition Mc Graw Hill, New York; p 396-420.
Ganong W. 2002. Fisiologi Kedokteran. Jakarta : EGC
Gharbawy, et. al. 2001. Arterial Pressure, Left Ventricular Mass and Aldosterone in Essential Hypertension. Hypertension. Vol 37 : 845-850.
Goodman and Gilman’s. 2006. The
Pharmacological Basis of Therapeutics. 11th. ed. New York : Mc. Graw Hill Companies Inc
Guyton A.C. 1998. Textbook of Medical Fisiology. 9th edition. Noida : WB Saunders Company.
Hofbauer KG, Mah SC, Baum HP, Hanni H, Wood JM, Kraetz J. 2011. Endocrine Control of Salt and Water Excretion: The Role of Vasopressin in DOCA-Salt Hypertension. Journal of
Cardiovascular Pharmacology. Vol. 6. Karp, G. 2002. Cell and Molecular Biology. 3rd
ed. John Willey & Son New York. Keidar S, Kaplan M, Pavlotzky E, Raymond C,
Hayek T, Hamoud S, Aviram M. 2004. . Aldosterone Administration to Mice Stimulates Macrophage NADPH Oxidase and Increases Atheroschlerosis Development – A possible role for Angiotensin-Converting Enzyme and the Receptors for Angiotensin II and Aldosterone. Circulation. Vol 109 : 2213-3220.
Knardahl S, Sander BJ, Johnson AK. 1988. Effect Adrenal Demedullation on Stres Induced Hypertension and
Cardiovascular Response to Acut Stres. Acta Physiol Scand. Vol 133 : 477-483. Ko EA, Amiri F, Pandey NR, Javeshghani D,
Leibovitz E, Touyz RM, Schiffirin EF. 2006. Resistance Artery Remodeling In Deoxycorticosterone Acetate-Salt Hypertension Is Dependent On
Vascular Inflammation: Evidence From M-Csf-Deficient Mice. American Journal of Physiology.
213 Remodeling Induced by
Deoxycorticosterone Acetate-Salt Hypertension. American Heart Association. Vol 50: 1057-1062 Lakhanpal, Rai. 2008. Role of Quercetin in
Cardiovescular Diseases. Online [WWW]. Vol : 3(1):31-49. Internet Journal of Medical.
Lerman LO, Chade AR, Sica V, Napol C. 2005. Animal Models of Hypertension: an Overwiew. J. Lab. Clin Med. Vol 146 (3) : 160-73.
Marney AM, Brown NJ. 2007. Aldosterone and End-Organ Damage. Clinical Science. Vol 113 (267-278).
Martha, FA. 2007. Pengembangan Model Tikus Hipertensi Yang Diinduksi Dengan Propilthiourasil, NaCl, dan Adrenalin. Bandung : Department of Pharmacy Nguyen PV, Parent A, Deng LY, Fluckiger JP,
Thibault G, Schiffirin EL.1992. Endothelin Vascular Receptors and RESponses in Deoxycorticosterone Acetate-Salt Hypertensive Rats. Hypertension J. Vol 2 : 1198-104. Oates JA, Brown NJ. 2001.. Antihypertensive
Agents and Drug Therapy of
Hypertension. In: Hardman JG, Gilman AG (Ed). The pharmacological Basis of Therapeutics. 10th ed. New York : McGraw-Hill; Vol 891-895.
Okada H, Suzuki H, Kanno Y, Saruta T. 1995. Effect of Nonpeptide Vasopressin Receptor Antagonists on Developing, and Established Doca-Salt
Hypertension in Rats. Japan. Vol 17. No. 1 : 469-483.
Pinto YM, Paul M, Ganten D. 1998.. Lessons from Rat Models of Hypertension; from Goldbaltt tom Genetic Engeneering. Cardiovascular Research. Vol 39 : 77-88.
Plehm R, Barbosa ME, Bader M. 2006. Animal Models for Hypertension/Blood Pressure Recording. Methods in Molecullar Medicine. Vol 129 : 115-126.
Rocha, R, et. al. 2000. Aldosterone : A Mediator of Myocardial Necrosis and
Renal Arteriopathy. Endocrinology. Vol 141 : 3871-3878.
Rude MK, Duhaney TS, Kuster GM, Judge S, Heo J, Colucci WS, Siwik DA, Sam F. 2005. Aldosterone Stimulates Matrix Metalloproteinases and Reactive Oxygen Species in Adult Rat Ventricular Cardiomyocytes. Hypertension. Vol 46 : 555-56. Sherwood L. 2007. Human Fisiologi. USA :
Thomson, Book/Cole Australia. Somers MJ, Mavromatis K, Galis Z, Harrison
DG. 2000. Vascular Superoxide Production and Vasomotor Function in Hypertension Induced by
Deoxycorticosterone Acetate–Salt. American Heart Association. Vol 101: 1722-1728.
Stanton BA and Giebisch.. 2011. Handbook of Physiology, Renal Physiology.
Originally published: 1992. GH10.1002/cphy.cp080119. Sun Z and Zhang Z. Historic. 2005.
Perspectives and Recent Advances in Major Animal Models of Hypertension. Acta Pharmacologica Sinica. Vol 3 : 295-301.
Taddei S, Virdis A, Ghiadoni L, Sudano I, Salvetti A. 2002. Effects of
Antihypertensive Drugs On Endothelial Dysfunction. J. Drugs. Vol 62 : 265-848.
Takaoka M, Kobayashi Y, Yuba M, Ohkita M, Matsumura Y. 2001. Effects of α -Lipoic Acid on Deoxycorticosterone Acetate-Salt Induced Hypertension in Rats. European Journal of
Pharmacology. Vol 424 :121-129. Wang Q, Chen Z, Fan XP, et.al. 1994. A
Simplified Method for Preparation of DOCA-salt Hypertension Model in RATS by Subcutaneous Implantation of DOCA Silastic Tube. J. Circulation. Vol 46 (2) : 205-8.
Zimmerman RS and Frohlich ED. 1990. Stres and Hypertension. Journal of