RENCANA PELAKSANAAN PEMBELAJARAN (RPP) Sekolah : SMAN 1 GUNUNGPUTRI
Mata pelajaran : KIMIA Kelas/Semester : X / 1
Alokasi Waktu : 45 menit (1 jampel)
A. Kompetensi Inti (KI)
KI 1 : Menghayati dan mengamalkan ajaran agama yang dianutnya.
KI 2 : Menunjukkan perilaku jujur, disiplin, tanggungjawab, peduli (gotong royong, kerjasama, toleran, damai), santun, responsif dan pro-aktif dan menunjukkan sikap sebagai bagian dari solusi atas berbagai permasalahan dalam berinteraksi secara efektif dengan lingkungan sosial dan alam serta dalam menempatkan diri sebagai cerminan bangsa dalam pergaulan dunia.
KI 3 : Memahami, menerapkan, menganalisis pengetahuan faktual, konseptual, prosedural berdasarkan rasa ingin tahunya tentang ilmu pengetahuan, teknologi, seni, budaya, dan humaniora dengan wawasan kemanusiaan, kebangsaan,
kenegaraan, dan peradaban terkait penyebab fenomena dan kejadian, serta menerap-kan pengetahuan prosedural pada bidang kajian yang spesifik sesuai dengan bakat dan minatnya untuk memecahkan masalah.
KI4: Mengolah, menalar, dan menyaji dalam ranah konkrit dan ranah abstrak terkait dengan pengembangan dari yang dipelajarinya di sekolah secara mandiri, dan mampu menggunakan metode sesuai kaidah keilmuan.
B. Kompetensi Dasar dan Indikator
Kompetensi Dasar Indikator
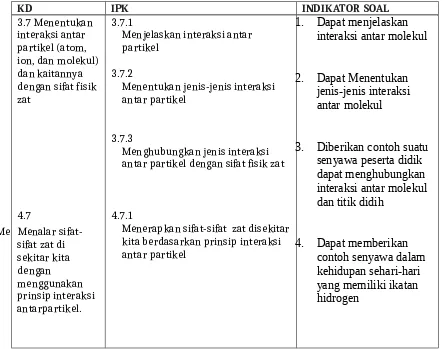
3.7. Menentukan interaksi antar partikel (atom, ion, dan molekul) dan kaitannya dengan sifat fisik zat
3.7.1. Menjelaskan interaksi antar partikel 3.7.2. Menentukan jenis-jenis interaksi
antar partikel
3.7.3. Menghubungkan jenis interaksi antar partikel dengan sifat fisik zat
7 4.7. Menalar sifat-sifat zat di sekitar kita dengan
menggunakan prinsip interaksi antarpartikel
4.7.1. Menerapkan sifat-sifat zat disekitar kita berdasarkan prinsip interaksi antar partikel
C. Materi Pembelajaran Interaksi antar partikel Fakta
H2O titik didihnya tinggi
Alkohol titik nya rendah dan mudah menguap Konsep
D. Kegiatan Pembelajaran Pertemuan Ketiga: (45menit)
Indikator Pencapaian Kompetensi 3.7.1. Menjelaskan interaksi antar partikel
3.7.2. Menentukan jenis-jenis interaksi antar partikel
3.7.3. Menghubungkan jenis interaksi antar partikel dengan sifat fisik zat
3.7.4. Menerapkan sifat-sifat zat disekitar kita berdasarkan prinsip interaksi antar partikel
a. Kegiatan Pendahuluan (5 menit) Berdo’a (religius)
Mengecek kehadiran siswa / perkenalan (disiplin)
Menanyakan kabar siswa- dengan focus pada yang tidak hadir dan/yang pada pertemuan sebelumnya juga tidak hadir. (peduli, empati).
Guru bertanya , Ada berapa jenis-jenis interaksi antar partikel? (Jawab : ada dua , yaitu ikatan hidrogen dan gaya Van der Waals
Bagaimana bila alkohol disimpan dalam botol yap dan terbuka? (Jawab: alkohol akan menguap)
Guru menyampaikan kompetensi yang akan dicapai dan manfaatnya dalam kehidupan sehari-hari.
Guru menyampaikan cakupan materi dan kegiatan yang dicapai ( interaksi antar molekul dan sifat fisik zat dengan demontrasi
Guru menyampaikan teknik dan lingkup penilaian
b. Kegiatan Inti
Langkah-langkah kegiatan pembelajarannya sebagai berikut :
No Sintaks/Tahapan Pembelajaran Deskripsi Kegiatan Pembelajaran
(1) (2) (3)
1
2
a. Stimulation (memberi stimulus);
b.
c. Problem Statement
(mengidentifikasi masalah)
1. Mendemontrasikan air dan alcohol yang dipanaskan sampai mendidih dengan volume yang sama
2. Diharapkan siswa akan muncul pertanyaan dari peserta didik dapat menjelaskan :
- Mengapa Alkohol lebih cepat mendidih dari pada air
3
4
5
6
d. Data Collecting (mengumpulkan data);
e. Data Processing (mengolah data);
f. Verification (memverifikasi);
g. Generalization (menyimpulkan);
- Menentukan gaya antara molekul dalam senyawa air dan alkohol
3. Siswa mencari informasi dan
mengumpulkan data tentang hubungan interaksi antara molekul dengan titik didih
4. Melakukan pengolahan data melalui diskusi.
5. Membandingkan hasil diskusi antar kelompok untuk mengklasifikasikan dan menganalisis dan hubungan interaksi antara molekul dengan titik didih
6. Peserta didik menyimpulkan hasil diskusi pada permasalahan dalam kehidupan sehari-hari interaksi antara molekul dengan titik didih
Menerapkan hasil diskusi dalam kehidupan sehari-hari
a. Kegiatan Penutup
Guru dan peserta didik membuat kesimpulan tentang interaksi antar molekul Guru melakukan refleksi dan umpan balik terhadap proses dan hasil belajar Guru memberikan evaluasi dan penugasan
Guru menginformasikan materi yang akan dipelajarai pada pertemuan yang akan datang
E. Teknik penilaian 1. Penilaian Sikap :
a. Observasi
2. Penilaian Pengetahuan
a. Teknik Penilaian : tes tertulis b. Bentuk soal : uraian c. Instrumen penilaian : terlampir 3. Penilaian Keterampilan
Projek : membuat model molekul dengan menggunakan
bahan-bahan yang ada di lingkungan sekitar F. Media/alat, Bahan, dan Sumber Belajar
1. Media/alat : Laptop/LCD, gelas kimia, pembakar Bunsen, kaki tiga+ alas asbes 2. Bahan : H2O, alkohol
Lampiran :
1. Materi pembelajaran
2. Instrumen Penilaian Pengetahuan 3. Instrumen penilaian Observasi 4. Instrumen Penilaian Keterampilan
Mengetahui, Bogor,
Kepala SMAN 1 Gunungputri Guru Mata Pelajaran Kimia,
Dra. Hj. Nursari Siregar Tety Soesanti, S.Pd
NIP.195610101984032004 NIP. 197101041998022004
Lampiran 1.
MATERI PEMBELAJARAN
Mata Pelajaran : Kimia Kelas / Semester : X / 1
SKL : Memiliki pengetahuan faktual, konseptual, prosedural, dan metakognitif dalam ilmu pengetahuan, teknologi, seni, dan budaya dengan wawasan kemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab serta dampak fenomena dan kejadian. Kompetensi dasar : 3.7. Menentukan interaksi antar partikel (atom, ion, dan molekul) dan kaitannya dengan sifat fisik zat
4.7 . Menalar sifat-sifat zat di sekitar kita dengan menggunakan prinsip interaksi antarpartikel.
Alokasi Waktu : 3 jam Pelajaran
Indikator Pencapaian Kompetensi :
4.7.1 Menjelaskan interaksi antar partikel
4.7.2 Menentukan jenis-jenis interaksi antar partikel
4.7.3 Menghubungkan jenis interaksi antar partikel dengan sifat fisik zat
Gaya Antar Molekul : GayaVanderWaals
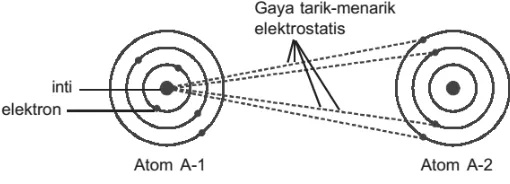
Gaya Vander Waals merupakan salah satu jenis gaya tarik-menarik di antara molekul-molekul. Gaya ini timbul dari gaya London dan gaya antardipol-dipol. Gaya Van der Waals dapat terjadi pada molekul nonpolar maupun molekul polar. Gaya ini diusulkan pertama kalinya oleh Johannes Van der Waals (1837–1923). Konsep gaya tarik antarmolekul ini digunakan untuk menurunkan persamaan persamaannya tentang zat-zat yang berada
dalam fase gas.
Kejadian ini disebabkan adanya gaya tarik-menarik antara inti atom dengan elektron atom lain yang disebut gaya tarik-menarik elektrostatis (gaya coulumb). Umumnya terdapat pada senyawa polar. Untuk molekul nonpolar, gaya Van der Waals timbul karena adanya dipol-dipol sesaat atau gaya London.
Gambar 1. Gaya Van der waals
Ada tiga gaya antarmolekul yang berperan dalam terjadinya gaya Van der Waals, yaitu gaya
orientasi,gayaimbas,dan gayadispersi.
a.Gayaorientasi
Gaya orientasi terjadi pada molekul-molekul yang mempunyai dipol permanen atau molekul polar. Antaraksi antara kutub positif dari satu molekul dengan kutub negatif dari molekul yang lain akan menimbulkan gaya tarik-menarik yang relatif lemah. Misalnya, pada molekul-molekul HCl.
Gambar 2. Gaya Orientasi
b. Gaya Imbas
Gaya imbas terjadi bila terdapat molekul dengan dipol permanen, berinteraksi dengan molekul dengan dipol sesaat. Adanya molekul-molekul polar dengan dipol permanen akan menyebabkan imbasan dari kutub molekul polar kepada molekul nonpolar, sehingga elektron-elektron dari molekul nonpolar tersebut mengumpul pada salah satu sisi molekul (terdorong atau tertarik), yangmmenimbulkan terjadinya dipol sesaat pada molekul nonpolar tersebut.
Gambar 3. Gaya Imbas
1. London
terutamaterdapat pada molekul-molekul nonpolar yang dikemukakan pertama kalinya oleh Fritz London.
Gambar 4. Gaya London
2. Ikatan Hidrogen
Ikatan hidrogen adalah gaya tarik-menarik yang cukup kuat antara molekul-molekul polar (mengandung atom-atom sangat elektronegatif, misalnya F, O, N) yang mempunyai atom hidrogen. Ikatan ini dilambangkan dengan titik-titik (...). Contoh:Ikatan hidrogen yang terjadi dalam molekul air.Di dalam molekul air, atom O bersifat sangat
elektronegatif sehingga pasangan elektron antara atom O dan H lebih tertarik ke arah atom O. Dengan demikian terbentuk suatu dipol.
Gambar 5. Ikatan Hidrogen
Senyawa yang di dalamnya terdapat ikatan hidrogen umumnya memiliki titik didih yang tinggi. Sebab untuk memutuskan ikatan hidrogen yang terbentuk diperlukan energi lebih besar dibandingkan senyawa yang sejenis,tetapi tanpa adanya ikatan hidrogen. Contoh senyawa lain yang mengadung ikatan hidrogen :
Gambar 6. Ikatan hidrogen pada senyawa HF
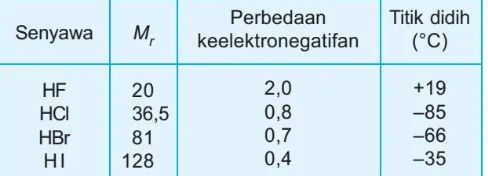
Pengaruh Ikatan Hidrogen pada Titik Didih Titik didih suatu zat dipengaruhi oleh a. Mr, jika Mr besar maka titik didih besar dan Mr kecil maka titik didih kecil.
b. Ikatan antarmolekul, jika ikatan kuat maka titik didih besar dan ikatan lemah maka titik didih kecil. Perhatikan data Mr dan perbedaan keelektronegatifan senyawa golongan halogen (VIIIA) berikut.
Jadi, urutan titik didihnya: HF > HI > HBr > HCl
Gambar 8. Titik didih senyawa hidrida golongan IV A dan V A
Untuk hidrida unsur-unsur golongan VIA (H2O, H2S,H2Se, dan H2Te) terdapat penyimpangan yang sangat mencolok pada H2O. Penyimpangan yang sama juga terdapat pada NH3 dengan hidrida unsur-unsur golongan VA lain (PH3, AsH3, dan SbH3) dan juga pada HF dengan hidrida unsur-unsur golongan VIIA lainnya (HCl, HBr, HI, dan HAt). Sifat yang abnormal dari HF, H2O, dan NH3 tersebut dijelaskan dengan konsep ikatan hidrogen. antar partikel dengan sifat fisik zat
4.7.1
Menerapkan sifat-sifat zat disekitar kita berdasarkan prinsip interaksi antar partikel
Soal uraian
1. Jelaskan interaksi antar molekul ?
2. Tentukan interaksi antar molekul pada senyawa alkohol ? 3. Diantara beberapa senyawa dibawah ini :
H2O, HCl, NH3, C2H5OH, Cl2, H2. Manakah yang memiliki gaya van der waals ?
4. Bagaimanakah hubungan interaksi antar molekul dengan titik didih pada suatu senyawa ? 5. Berikan contoh penerapan hubungan interaksi aksi antar molekul dalam kehidupan
sehari-hari ?
Kunci Jawaban dan Pedoman Pengskoran
No Kunci jawaban Skor Skor
maksimal 1. Gaya yang terjadi antara molekul satu dengan yang lain 20 20 2. Pada Alkohol terjadi gaya Van der Waals 20 20
3. C2H5OH, Cl2, H2 20 20
4. Apabila hubungan interaksi antar molekul semakin kuat,
maka titik didihnya semakin tinggi 20 20
5.
Bakan bakar bensin memiliki gaya Van der Waals yang lemah sehingga mudah terbakar dan menguap. Kita
meletakkan bensin pada tempat yang tertutup dan dijauhkan dari api.
20 20
Pedoman Pengskoran
NILAI = Jumlah benar x 100 100
Lampiran 3
Kompetensi yang dinilai
: Penilaian Sikap (Observasi)
Satuan Pendidikan
: ………..
Mata Pelajaran
: ………
Kelas/Semester /Tahun Pelajaran
: ………
Kompetensi Dasar
:
Indikator
:
Nama Peserta Didik
:
Nomor Absen
:
Materi saat diobservasi
:
Tanggal Observasi
:
No.
Sikap
Kriteria
Hasil
Pengamatan
Ya
Tidak
1
Jujur
1. Melaporkan data sesuai dengan
kenyataan/sesuai dengan apa yang
diamati.
2. Menyampaikan pendapat disertai data
konkret/data yang diamati.
2
Disiplin
1. Mengerjakan tugas sesuai waktu yang
ditetapkan.
2. Mengumpulkan hasil pekerjaan tepat
waktu.
3
Tanggung jawab
1. Melaksanakan tugas yang diberikan oleh
guru.
2. Menyelesaikan pekerjaan sampai tuntas.
4
Peduli lingkungan
1. Membersihkan meja dan kursi yang
ditempatinya/meja dan kursi yang
ditempati dalam keadaan bersih/ rapi.
2. Menata/menempatkan kembali
alat/bahan/buku/sumber belajar lainnya
dengan rapi atau menempatkan kembali
pada tempat semula.
5
Kerjasama
1. Menghargai pendapat teman
2. Mengambil bagian dalam kerja
kelompok
Skor maksimum
Catatan:
Nilai = Skor perolehan x 100%
10
Lampiran 4
Penilaian kompetensi keterampilan
Satuan Pendidikan
: SMAN 1 Gunungputri
Mata Pelajaran : KimiaSKL : Memiliki pengetahuan faktual, konseptual, prosedural, dan metakognitif dalam ilmu pengetahuan, teknologi, seni, dan budaya dengan wawasan kemanusiaan, kebangsaan, kenegaraan, dan peradaban terkait penyebab serta dampak fenomena dan kejadian. Kompetensi dasar : 3.7. Menentukan interaksi antar partikel (atom, ion, dan molekul) dan kaitannya dengan sifat fisik zat
4.7 . Menalar sifat-sifat zat di sekitar kita dengan menggunakan prinsip interaksi antarpartikel.
Alokasi Waktu : 3 jam Pelajaran
Indikator Pencapaian Kompetensi :
4.7.4 Menjelaskan interaksi antar partikel
4.7.5 Menentukan jenis-jenis interaksi antar partikel
4.7.6 Menghubungkan jenis interaksi antar partikel dengan sifat fisik zat
4.7.2 Menerapkan sifat-sifat zat disekitar kita berdasarkan prinsip interaksi antar partikel