INTERESTERIFIKASI ENZIMATIK CAMPURAN MIN YAK SAWIT UNTUK PRODUKSI COCOA BUTTER EQUIVALENT:
ANALISIS KOMPOSISI TRIASILGLISEROL DAN SOLID FAT CONTENT
Soenar SoekopitojoI,3), Purwiyatno Hariyadi2,3*, Tien R. Muchtadi2) dan Nuri Andarwulan2,3*
ABSTRACT
Interesterification of fat blends containing refined, bleached, deodorized palm oil (RBDPO) and fully hydrogenated soybean oil (FHSO) at various weight ratios, catalyzed by an immobilized 1,3-specific lipase, Lipozyme TL IM, was studied for production of cocoa butter equivalent (CBE). CBE have chemical dan physical properties compatible with those of cocoa butter (CB) and can be used to replace CB in chocolate confectionery product. Triacylglycerol (TAG) composition and solid fat content (SFC) profile of the starting blends were analyzed and compare with those of the interesterified blends. Upon enzymatic interesterification, extensive re-arrangement of fatty acid (FA) among TAG was evident. Consentration of several TAG were increased, some were decreased, and several new TAG were formed. The main TAG of RBDPO (POP, POO) and TAG of FHSO (PSS, SSS) were decreased, whereas the desired CB TAG (POS, SOS) were increased. Our research indicated that acyl exchange occured mainly between the palmitoyl group from the RBDPO and the stearoyl group from the FHSO. The resulting changes in TAG profile were reflected in the SFC of the blends. The SFC values of the enzymatic interesterified blends revealed that they were harder at low temperature (below 30-35°C) and softer at high temperature (above 30-35°C) than their respective starting blends.
KEY WORDS: Enzymatic interesterification, palm oil, triacylglycerol, solid fat content, cocoa butter equivalent (CBE)
PENDAHULUAN
Dalam industri confectionery, cocoa butter (CB) merupakan bahan baku penting yang berkontribusi terhadap sifat-sifat tekstural dan sensori produk confectionery, khususnya produk-produk coklat. CB merupakan lemak dengan karakteristik fisikokimia yang unik, karena komposisi triasilgliserolnya hampir 80% didominasi oleh tiga triasilgliserol (TAG) simetrik, saturated-monounsaturated-saturated, yaitu palmitat-oleat- stearat (POS, 36-42%), stearat-oleat-stearat (SOS, 23-29%) dan palmitat-oleat-palmitat (POP, 13-19%) (Wainwright, 1996). Ketika dimakan, CB meleleh sempuma di mulut dengan tekstur creamy dan suatu sensasi yang menyejukkan (Gunstone, 2002).
Banyak keterbatasan menyangkut penggunaan CB, di antaranya adalah suplai yang tidak menentu, variabilitas dalam kualitas, kurang memadai untuk digunakan pada iklim
(Enzymatic Interesterification of Palm Oil Blends for the Production of Cocoa Butter Equivalent: Analysis of Triacylglycerol Composition and Solid Fat Content)
^Mahasiswa Program Studi Ilmu Pangan, Sekolah Pascasarjana, IPB
2)Departemen Ilmu dan Teknologi Pangan, Fakultas Teknologi Pertanian, IPB 3)Southeast Asian Food and Agricultural Science and Technology (SEAFAST) Center, IPB
TPP-62
1 Untuk korespondensi dapat dialamatkan ke SEAFAST Center IPB, Jalan Puspa No. 1, Kampus IPB
panas serta harga yang relatif mahal dan berfluktuasi dibandingkan dengan lemak lainnya (Fuji Oil Europe, 2004). Oleh karena itu, berbagai upaya dilakukan untuk mengembangkan
specialty fats sebagai altematif penggunaan CB, salah satunya adalah cocoa butter equivalent (CBE). CBE merupakan specialty fats yang mengandung asam lemak dan TAG
simetrik yang sama dengan CB, sehingga CBE sepenuhnya kompatibel dan dapat dicampur dengan CB pada berbagai rasio dalam formulasi coklat (Shukla, 1995). CBE didesain untuk menggantikan CB atau dapat dicampur dengan CB pada proporsi berapapun tanpa mengakibatkan perubahan yang berarti pada kualitas akhir produk coklat (Fuji Oil Europe, 2004).
Salah satu teknik produksi CBE yang banyak dilakukan selama ini adalah cara
blending (pencampuran) antara lemak yang kaya TAG POP dengan lemak yang kaya TAG
POS dan SOS. Sumber utama TAG POP umumnya dari palm midfraction (PMF) sebagai produk fraksinasi multitahap minyak sawit. Sedangkan sebagai sumber TAG SOS dan POS dapat diperoleh dari exotic fats seperti Borneo illipe butter, Sal stearin, Mango stearin,
Kokum atau Dhupa fat (Soon, 1991). Mengingat semakin terbatasnya sumber exotic fats
dari alam, maka akhir-akhir ini teknik interesterifikasi enzimatik menjadi salah satu pilihan untuk modifikasi lemak dan minyak dalam proses produksi CBE dengan bahan baku minyak kaya oleat yang ketersediaannya relatif lebih berlimpah (Wainwright, 1999).
Selama interesterifikasi akan terjadi re-distribusi asam lemak dalam TAG, sehingga akan mengubah komposisi asam lemak dalam TAG dan menambah jenis TAG. Konsekuensinya akan mempengaruhi karakteristik fisik minyak dan lemak, antara lain sifat pelelehan dan kristalisasi (Idris and Dian, 2005). Penggunaan lipase spesifik-1,3 sebagai katalis dalam proses produksi CBE lebih menguntungkan untuk substrat berbasis sawit, karena kandungan TAG POP yang tinggi dalam minyak sawit akan lebih mudah untuk dimodifikasi menjadi TAG POS dan SOS sebagai komponen utama CBE (Nielsen et al.,
2000).
S ampai saat ini, belum ada industri di Indonesia yang memanfaatkan teknik interesterifikasi enzimatik dalam proses produksi CBE. Teknik blending masih menjadi pilihan utama dalam proses produksi CBE di Indonesia. Oleh karena itu, perlu dikaji proses produksi CBE dari bahan baku berbasis sawit secara interesterifikasi enzimatik. Tujuan penelitian ini adalah untuk mendapatkan informasi pengendalian proses produksi CBE dengan mempelajari pengaruh interesterifikasi enzimatik terhadap komposisi TAG dan SFC dari campuran refined, bleached, deodorized palm oil (RBDPO) dan fully
hydrogenated soybean oil (FHSO) pada berbagai rasio. Sebagai katalis digunakan lipase
spesifik-1,3 amobil komersial, Lipozyme TL IM, yang secara ekonomi bersaing dengan katalis untuk interesterifikasi kimia (Yang et al., 2003).
BAHAN DAN METODE
Bahan. Bahan yang digunakan dalam penelitian ini adalah refined, bleached, deodorized palm oil (RBDPO) (PT Asian Agri, Jakarta), fully hydrogenated soybean oil (USA),
Lipozyme TL IM (Novo Nordisk Ind., Denmark), standar triasilgliserol (Supelco), standar asam lemak (Supelco) serta bahan-bahan kimia untuk analisis.
Komposisi Asam Lemak. Analisis komposisi asam lemak (AOCS Official Methods Ce 1-
62, 1997) dilakukan terhadap masing-masing substrat sebelum dilakukan pencampuran. Komposisi asam lemak ditentukan sebagai metil ester asam lemak (FAME, fatty acid
methyl ester). Prosedur metilasi mengacu pada AOCS Official Methods Ce 2-66 (1997).
Analisis komposisi asam lemak menggunakan GC {Gas Chromatography) (Shimadzu GC- 9AM) yang dilengkapi dengan detektor FID (Flame Ionization Detector). Kolom yang digunakan adalah DB-23 (30 m, id 0.25 jim). Penyuntikan sampel sebanyak 1 p.L
ISBN 978-979-95249-7-3 Prosiding
menggunakan sistem langsung (splitless mode) dengan suhu injektor 250°C, suhu detektor 260°C, suhu kolom awai 140°C yang dipertahankan selama 6 menit. Peningkatan suhu kolom kemudian adalah 3°C per menit hingga suhu akhir 230°C dan dipertahankan selama 20 menit. Gas helium digunakan sebagai gas pembawa dengan tekanan 1 kg/cm2,
sedangkan tekanan gas hidrogen dan udara untuk FID masing-masing 0.5 kg/cm2.
Identifikasi dilalaikan dengan menggunakan standar metil ester asam lemak dan kuantifikasi masing-masing jenis asam lemak dilakukan dengan perbandingan terhadap standar internal C17:0.
Interesterifikasi Enzimatik. Sebanyak 5 g campuran substrat RBDPO dan FHSO
berbagai rasio (2:1, 1.5:1, 1:1, 1:1.5 dan 1:2 b/b) dimasukkan ke dalam labu Erlenmeyer. Selanjutnya enzim lipase sebanyak 6% (b/b substrat) ditambahkan ke dalam campuran
substrat yang sudah dipanaskan terlebih dahulu pada suhu sekitar 65°C selama 10 menit. Reaksi interesterifikasi dilakukan secara batch dengan kecepatan orbital shaker 200 rpm, suhu reaksi 65-68°C dan waktu reaksi 4 jam. Pemisahan enzim dari hasil interesterifikasi dilakukan dengan cara penyaringan menggunakan kertas saring (dalam keadaan panas).
Komposisi Triasilgliserol. Analisis komposisi TAG mengacu pada metode yang
dimodifikasi dari AOCS Official Methods Ce 5c, 1997. Komposisi TAG hasil interesterifikasi dianalisis menggunakan HPLC Hewlett Packard series 1100 dengan detektor Indeks Refraksi (Refractive index, RI). Sampel dilarutkan dalam campuran aseton : kloroform (2:1 v/v) dengan konsentrasi 5%, lalu disuntikkan ke dalam HPLC sebanyak 20 |o.L. HPLC yang digunakan memiliki tipe pompa isokratik dengan laju aliran fase gerak (aseton: asetonitril, 85 : 15 v/v) 0.8 mL/menit. Kolom yang digunakan adalah dua kolom C-18 ( Microsorb MV dan Zorbax Eclipse XDB-C18, 4.6 x 250 mm, ukuran partikel 5 (j.m) yang dipasang secara seri. Analisis komposisi TAG juga dilakukan terhadap substrat sebelum interesterifikasi.
Solid Fat Content (SFC). Analisis SFC (IUPAC 2.150 ex 2.323, 1987) hasil
interesterifikasi menggunakan Bruker Minispec PC 100 NMR Analyzer. Sebelum analisis, sampel dilelehkan terlebih dahulu pada suhu 80°C. Sampel dimasukkan ke dalam tabung NMR dengan menggunakan pipet tetes sebanyak 2.5 mL (setinggi dry block), lalu dipanaskan pada suhu 60°C selama 30 menit pada alat pemanas kering. Setelah itu sampel disimpan pada suhu 0°C selama 90 menit, selanjutnya sampel disimpan selama 40 jam pada suhu 26°C. Sampel disimpan lagi pada suhu 0°C selama 90 menit. Setelah itu sampel diinkubasi pada suhu 10, 20, 25, 30, 35, 40 dan 45°C selama 60 menit. Setelah inkubasi, sampel siap dianalisis. Kalibrasi NMR menggunakan standar SFC 0%, 31.5% dan 72.9%. Analisis SFC juga dilakukan terhadap substrat sebelum interesterifikasi.
Slip Melting Point (SMP). Analisis SMP (AOCS Official Methods Cc 3-25, 2005)
dilakukan terhadap substrat sebelum interesterifikasi dan sesudah interesterifikasi. Sampel yang telah disaring dilelehkan dan dimasukkan ke dalam tabung kapiler (3 buah) setinggi 1 cm. Selanjutnya disimpan dalam refrigerator pada suhu 4-10°C selama 16 jam. Tabung kapiler diikatkan pada termometer dan termometer tersebut dimasukkan ke dalam gelas kimia (600 mL) berisi air (sekitar 300 mL). Suhu air dalam gelas kimia diatur pada suhu 8
- 10°C di bawah titik leleh sampel dan suhu air dipanaskan pelan-pelan (dengan kenaikan 0.5°C — l°C/menit ) dengan pengadukan (magnetic stirrer). Pemanasan dilanjutkan dan suhu diamati dari saat sampel meleleh sampai sampel naik pada tanda batas atas. Slip
melting point dihitung berdasarkan rata-rata suhu dari ketiga sampel yang diamati. HASIL DAN PEMBAHASAN
Tabel 1 memperlihatkan komposisi asam lemak RBDPO dan FHSO. Asam palmitat (C16:0) dan asam oleat (C18:l) merupakan asam lemak dominan pada RBDPO, sedangkan
FHSO dominan dengan asam stearat (Cl8:0) dan asam palmitat (Cl6:0). Analisis asam lemak tidak dilakukan terhadap hasil interesterifikasi, karena proses interesterifikasi tidak menyebabkan teijadinya isomerisasi asam lemak pada ikatan rangkap, sehingga tidak mengubah komposisi asam lemak (Noor Lida et al., 2002).
ISBN 978-979-95249-7-3 Prosiding
SeminarPATPI, Palembang, 14-16 Oktober2008
Tabel 1. Komposisi asam lemak (% b/b) RBDPO dan FHSO
Bahan Baku
Komposisi Asam Lemak (% b/b) C14:0 (M, Miristat) C16:0 (P, Palmitat) 08:0 (S, Stearat) 08:1 (0, Oleat) 08:2 (L, Linoleat) Lainnya RBDPO 1.1 43.5 3.3 37.5 11.8 2.8 FHSO 0.7 23.9 72.8 - 1.6 1.0
keterangan : Lainnya, asam lemak yang tidak teridentifikasi
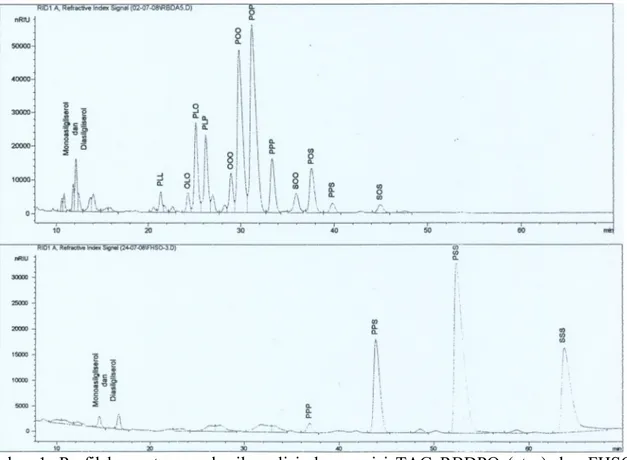
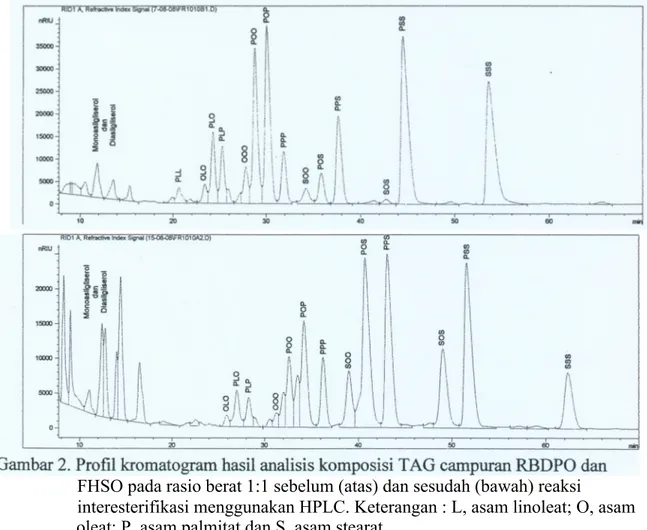
Komposisi TAG RBDPO dan FHSO disajikan pada Tabel 2. TAG utama RBDPO adalah POP, POO, PLP dan POO, sedangkan TAG utama FHSO adalah PSS, SSS dan PPS. Profil kromatogram hasil analisis komposisi TAG RBDPO dan FHSO dapat dilihat pada Gambar 1. Pada Tabel 2 juga disajikan komposisi TAG campuran substrat RBDPO dan FHSO pada berbagai rasio baik sebelum maupun sesudah interesterifikasi. Komposisi TAG campuran substrat merepresentasikan kombinasi linear komponen minyak/lemak yang terdapat di dalam campuran substrat. Jika proporsi RBDPO meningkat, maka proporsi POP, POO, PLP, PLO dan TAG lain dalam RBDPO juga meningkat, demikian pula sebaliknya. Profil kromatogram hasil analisis komposisi TAG campuran RBDPO dan FHSO sebelum dan sesudah reaksi interesterifikasi enzimatik disajikan pada Gambar 2.
Gambar 1. Profil kromatogram hasil analisis komposisi TAG RBDPO (atas) dan FHSO (bawah) menggunakan HPLC. Keterangan : L, asam linoleat; O, asam oleat; P, asam palmitat dan S, asam stearat
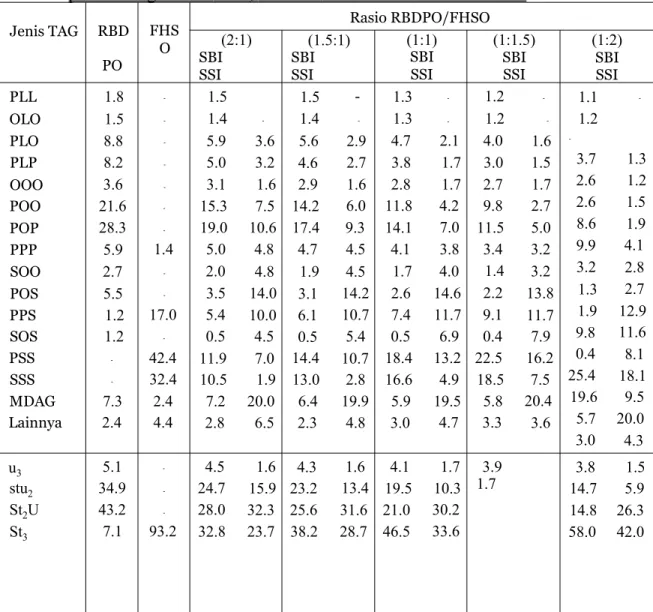
Tabel 2. Komposisi triasilgliserol (% area) RBDPO, FHSO serta campuran RBDPO/FHSO pada berbagai rasio berat, sebelum dan sesudah interesterifikasi
Jenis TAG RBD PO FHS O Rasio RBDPO/FHSO (2:1) SBI SSI (1.5:1) SBI SSI (1:1) SBI SSI (1:1.5) SBI SSI (1:2) SBI SSI PLL 1.8 - 1.5 1.5 - 1.3 - 1.2 - 1.1 -OLO 1.5 - 1.4 - 1.4 - 1.3 - 1.2 - 1.2 PLO 8.8 - 5.9 3.6 5.6 2.9 4.7 2.1 4.0 1.6 -PLP 8.2 - 5.0 3.2 4.6 2.7 3.8 1.7 3.0 1.5 3.7 1.3 OOO 3.6 - 3.1 1.6 2.9 1.6 2.8 1.7 2.7 1.7 2.6 1.2 POO 21.6 - 15.3 7.5 14.2 6.0 11.8 4.2 9.8 2.7 2.6 1.5 POP 28.3 - 19.0 10.6 17.4 9.3 14.1 7.0 11.5 5.0 8.6 1.9 PPP 5.9 1.4 5.0 4.8 4.7 4.5 4.1 3.8 3.4 3.2 9.9 4.1 SOO 2.7 - 2.0 4.8 1.9 4.5 1.7 4.0 1.4 3.2 3.2 2.8 POS 5.5 - 3.5 14.0 3.1 14.2 2.6 14.6 2.2 13.8 1.3 2.7 PPS 1.2 17.0 5.4 10.0 6.1 10.7 7.4 11.7 9.1 11.7 1.9 12.9 SOS 1.2 - 0.5 4.5 0.5 5.4 0.5 6.9 0.4 7.9 9.8 11.6 PSS - 42.4 11.9 7.0 14.4 10.7 18.4 13.2 22.5 16.2 0.4 8.1 SSS - 32.4 10.5 1.9 13.0 2.8 16.6 4.9 18.5 7.5 25.4 18.1 MDAG 7.3 2.4 7.2 20.0 6.4 19.9 5.9 19.5 5.8 20.4 19.6 9.5 Lainnya 2.4 4.4 2.8 6.5 2.3 4.8 3.0 4.7 3.3 3.6 5.7 3.0 20.0 4.3 u3 5.1 - 4.5 1.6 4.3 1.6 4.1 1.7 3.9 3.8 1.5 stu2 34.9 - 24.7 15.9 23.2 13.4 19.5 10.3 1.7 14.7 5.9 St2U 43.2 - 28.0 32.3 25.6 31.6 21.0 30.2 14.8 26.3 St3 7.1 93.2 32.8 23.7 38.2 28.7 46.5 33.6 58.0 42.0
Keterangan : SBI, sebelum interesterifikasi; SSI, sesudah interesterifikasi; L, asam linoleat; O, asam oleat; P, asam palmitat; S, asam stearat; MDAG, mono- dan diasilgliserol; Lainnya, TAG yang tidak teridentifikasi; U3, triunsaturated; StU2, monosaturated', St2U, monounsaturated', St3,
trisaturated
Proses interesterifikasi enzimatik mengakibatkan terjadinya perubahan besar dalam komposisi TAG. Perubahan paling besar terutama teijadi pada TAG dominan dalam campuran substrat, yaitu TAG POP dan POO (dari RBDPO) serta TAG SSS dan PSS (dari FHSO). Sebagai contoh pada rasio substrat 1:1 (RBDPO/FHSO, b/b), konsentrasi TAG POP dan SSS menurun dari masing-masing 14.1% dan 16.6% menjadi 7.0% dan 4.9%. Sementara itu, komponen TAG yang diinginkan, yaitu komponen utama CB (POS dan SOS), konsentrasinya meningkat cukup tinggi, masing-masing dari 2.6% dan 0.5% menjadi 14.6% dan 6.9%. Bahkan TAG POS menjadi dominan pada hasil interesterifikasi untuk rasio substrat (RBDPO/FHSO, b/b) 2:1,1.5:1 dan 1:1, dengan konsentrasi TAG POS tertinggi pada rasio substrat 1:1 (14.6%). Hal ini mengindikasikan bahwa pertukaran asil teijadi terutama antara grup palmitoil dari RBDPO dengan grup stearoil dari FHSO. Walaupun demikian, untuk mendapatkan produk CBE dengan karakteristik yang diinginkan, masih diperlukan proses fraksinasi dan purifikasi. Sementara itu, Abigor et al. (2003) melakukan fraksinasi dan purifikasi terhadap hasil interesterifikasi untuk produksi
Prosiding
Seminar PATPI, Palembang, 14-16 Oktober 2008
ISBN 978-979-95249-7-3
cocoa butter-like dan memberikan produk dengan konsentrasi POS tertinggi (39%) pada
rasio substrat 1.6:1 (RBDPO/FHSO, b/b), sedangkan POP dan SOS masing-masing 11%
dan 23%.
Tabel 3 memperlihatkan profil SFC RBDPO, FHSO serta campuran RBDPO dan FHSO pada berbagai rasio berat substrat sebelum dan sesudah reaksi interesterifikasi. SFC adalah jumlah kristal lemak yang terdapat dalam campuran minyak/lemak yang menentukan karakteristik berbagai produk, seperti misalnya sifat pelelehan maupun sifat organoleptik produk CBE. Profil SFC dari masing-masing minyak/lemak maupun campurannya sangat berbeda satu sama lain. RBDPO mempunyai nilai SFC relatif tinggi pada suhu rendah dan meleleh sempuma pada suhu sekitar 40-45°C. Sementara itu, FHSO mempunyai nilai SFC yang sangat tinggi pada suhu rendah, tetapi penurunan nilai SFC- nya relatif kecil pada suhu pengukuran sampai 45°C. Walaupun demikian, penambahan FHSO ke dalam RBDPO meningkatkan nilai SFC campuran substrat secara proporsional sesuai rasio substrat pada semua suhu pengukuran. FHSO dikarakterisasi dengan konsentrasi TAG trisaturated (PPP, PPS, PSS dan SSS) yang sangat tinggi (93.2%), sedangkan RBDPO dikarakterisasi dengan TAG trisaturated dan unsaturated yang rendah, masing-masing 7.1% dan 5.1% serta TAG monosaturated dan monounsaturated yang relatif tinggi, masing-masing 34.9% dan 43.2% (Tabel 2).
FHSO pada rasio berat 1:1 sebelum (atas) dan sesudah (bawah) reaksi
interesterifikasi menggunakan HPLC. Keterangan : L, asam linoleat; O, asam oleat; P, asam palmitat dan S, asam stearat
Nilai SFC campuran substrat sesudah interesterifikasi relatif lebih tinggi pada suhu- suhu rendah (di bawah 30-35°C) dan relatif lebih rendah pada suhu-suhu tinggi (di atas 30- 35°C) dibandingkan dengan nilai SFC campuran substrat sebelum interesterifikasi. Hal ini menunjukkan bahwa produk interesterifikasi bersifat lebih keras di bawah suhu 30-35°C
dan bersifat lebih lunak di atas suhu 30-35°C dibandingkan dengan substrat awai. Perubahan nilai SFC setelah proses interesterifikasi dipengaruhi oleh teqadinya perubahan dalam komposisi TAG trisaturated (PPP, PPS, PSS dan SSS), monounsaturated (POP, POS, SOS dan PLP), monosaturated (PLL, PLO, POO dan SOO) dan triunsaturated (OLO dan OOO) dalam campuran substrat (Tabel 2). Pada semua rasio substrat, peningkatan konsentrasi hanya teijadi pada TAG monounsaturated (St2U), sedangkan konsentrasi TAG
trisaturated (St3), monosaturated (StU2) dan triunsaturated (U3) semuanya mengalami
penurunan. Proporsi peningkatan dan penurunan masing-masing jenis TAG ini tidak selalu proporsional dengan nilai SFC. Sebagai contoh pada rasio substrat 1:2 (RBDPO/FHSO, b/b), meskipun proporsi penurunan TAG St3 lebih tinggi dari TAG St2U, tetapi hasil
interesterifikasi justru mempunyai nilai SFC yang lebih tinggi pada suhu rendah (10°C) dan lebih rendah pada suhu tinggi (45°C). Hasil penelitian ini mengindikasikan bahwa proporsi TAG St2U mempunyai peranan yang besar dalam menentukan profil SFC.
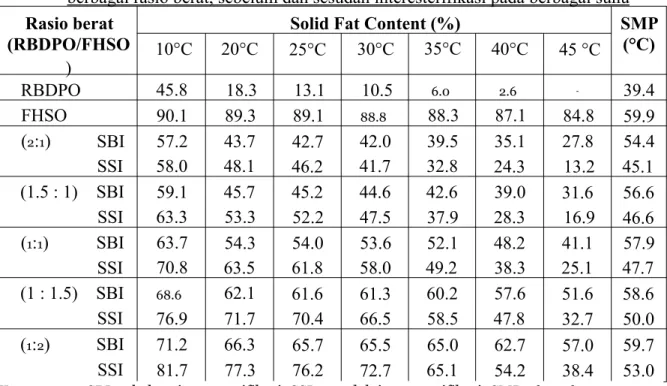
Tabel 3. Solid Fat Content (%) RBDPO, FHSO serta campuran RBDPO dan FHSO pada berbagai rasio berat, sebelum dan sesudah interesterifikasi pada berbagai suhu
Rasio berat (RBDPO/FHSO
)
Solid Fat Content (%) SMP
(°C) 10°C 20°C 25°C 30°C 35°C 40°C 45 °C RBDPO 45.8 18.3 13.1 10.5 6.0 2.6 - 39.4 FHSO 90.1 89.3 89.1 88.8 88.3 87.1 84.8 59.9 (2:1) SBI 57.2 43.7 42.7 42.0 39.5 35.1 27.8 54.4 SSI 58.0 48.1 46.2 41.7 32.8 24.3 13.2 45.1 (1.5 : 1) SBI 59.1 45.7 45.2 44.6 42.6 39.0 31.6 56.6 SSI 63.3 53.3 52.2 47.5 37.9 28.3 16.9 46.6 (1:1) SBI 63.7 54.3 54.0 53.6 52.1 48.2 41.1 57.9 SSI 70.8 63.5 61.8 58.0 49.2 38.3 25.1 47.7 (1 : 1.5) SBI 68.6 62.1 61.6 61.3 60.2 57.6 51.6 58.6 SSI 76.9 71.7 70.4 66.5 58.5 47.8 32.7 50.0 (1:2) SBI 71.2 66.3 65.7 65.5 65.0 62.7 57.0 59.7 SSI 81.7 77.3 76.2 72.7 65.1 54.2 38.4 53.0
Keterangan : SBI, sebelum interesterifikasi; SSI, sesudah interesterifikasi; SMP, slip melting point
Hasil analisis komposisi TAG juga menunjukkan adanya kandungan monoasilgliserol dan diasilgliserol yang cukup tinggi dalam campuran substrat hasil interesterifikasi. Hal ini diduga bahwa reaksi interesterifikasi belum mencapai kesetimbangan, sehingga waktu reaksi perlu diperpanjang agar dihasilkan produk TAG yang lebih optimal. Menurut Wainwright (1999) adanya diasilgliserol dalam produk interesterifikasi enzimatik akan menurunkan titik leleh dan mengganggu kristalisasi produk CBE. Oleh karena itu, fraksinasi dan purifikasi terhadap hasil interesterifikasi harus dilakukan untuk menghilangkan diasilgliserol yang tidak diinginkan, sehingga diperoleh komponen utama CBE yang lebih mumi. Selain itu, menurut Noor Lida et al. (2002), interaksi eutectic antara minyak/lemak dalam campuran substrat juga menentukan tinggi rendahnya nilai SFC.
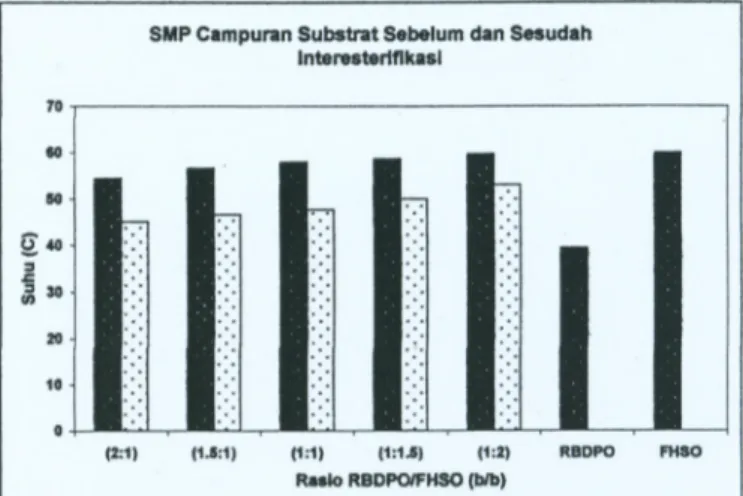
Proses interesterifikasi enzimatik juga mengakibatkan teijadinya penurunan SMP pada semua rasio substrat (RBDPO/FHSO) (Tabel 3 dan Gambar 3). SMP menunjukkan kondisi ketika minyak/lemak mempunyai nilai SFC sekitar 5% (Noor Lida et al., 1998).
Prosiding
Seminar PATPI, Palembang, 14-16 Oktober 2008
ISBN 978-979-95249-7-3
SMP dapat dijadikan salah satu indikator karakteristik GBE, yaitu sifat pelelehannya pada suhu tubuh. SMP hasil interesterifikasi relatif masih tinggi bila dibandingkan dengan SMP CBE komersial (sekitar 36-38°C) (PT Cahaya Kalbar Tbk., 2004). Hal ini diakibatkan komposisi TAG hasil interesterifikasi masih sangat beragam jenis TAG-nya dibandingkan dengan komposisi TAG CBE yang didominasi oleh TAG monounsaturated, yaitu POP, POS dan SOS. Komposisi TAG sangat menentukan profil SFC, sehingga juga menentukan nilai SMP. Selain itu adanya monoasilgliserol dan diasilgliserol dalam campuran substrat hasil interesterifikasi juga akan berpengaruh terhadap nilai SMP.
Gambar 3. Slip melting point (SMP) campuran RBDPO/FHSO pada berbagai rasio berat sebelum dan sesudah interesterifikasi, RBDPO dan FHSO
UCAPAN TERIMAKASIH
Ucapan terimakasih disampaikan kepada Kantor Kementerian Negara Riset dan Teknologi (KNRT) Republik Indonesia dan Masyarakat Perkelapa Sawitan Indonesia (MAKSI) atas dana penelitian yang diberikan melalui program Riset Unggulan Strategis Nasional (RUSNAS) Industri Kelapa Sawit.
DAFTAR PUSTAKA
Abigor, R.D., W.N. Marmer, T.A. Foglia, K.C. Jones, R.J. DiCiccio, R. Ashby, and P.O. Uadia. 2003. Production of Cocoa Butter-like Fats by the Lipase-Catalyzed Interesterification of Palm Oil and Hydrogenated Soybean Oil. JAOCS 80(12): 1193-
1196.
American Oil Chemists’ Society. 2005. Official Methods and Recommended Practices of the American Oil Chemists’ Society. Am. Oil Chem. Soc. Champaign, Illinois. Fuji Oil Europe. 2004. Confectionery.
http://www.fuiioileurope.com/Products/Confectionarv /choccoat.htm [1 Februari 2007],
Gunstone, F.D. 2002. Food Applications of Lipids. Di dalam C.C. Akoh, and D.B. Min (eds). Food Lipids Chemisty, Nutrition, and Biotechnology. Second Edition, Revised and Expanded. Marcel Dekker, Inc., New York.
Idris, N.A., and N.L.H.M. Dian. 2005. Interesterified Palm Products as Alternatives to Hydrogenation. Asia Pac J Clin Nutr 14(4):396-401.
IUPAC NORM VERSION. 1987. 2.150 (Ex 2.323) Solid Content Determination in Fats by NMR (Low Resolution Nuclear Magnetic Resonance).
Nielsen, K., A. Oliefabrik, M.P. Bruunsgade. 2000. Interesterification in Use for the Production of Confectionery Fats, http://www.soci.org [23 Februari 2007]
Noor Lida, H.M.D., and A. Rahim Md. Ali. 1998. Physicochemical Characteristics of Palm-Based Oil Blends for the Production of Reduced Fat Spreads. JAOCS 75(11):1625-1631.
Noor Lida, H.M.D, K. Sundram, W.L. Siew, A. Aminah, and S. Mamot. 2002. TAG Composition and Solid Fat Content of Palm Oil, Sunflower oil, and Palm Kernel Olein Blends Before and After Chemical Interesterification. JAOCS 79(11): 1137-
1144.
PT Cahaya Kalbar Tbk. 2004. Cocoa Butter Equivalent (CBE). http://www.cahavakalbar.com/product/cbe index.htm [16 April 2007]
Shukla, V.K.S. 1995. Confectionery Fats. Di dalam R.J. Hamilton (ed.). Development in Oils and Fats. Blackie Academic & Professional, London.
Soon, W. 1991. Speciality Fats versus Cocoa Butter. Malaysia
Wainwright, B. 1999. Specialty Fats and Oils. Di dalam N. Widlak (ed). Physical Properties of Fats, Oils and Emulsifiers. Am. Oil Chem. Soc. Press, Champaign, Illinois.
Wainwright, R.E. 1996. Oils and Fats in Confection. Di dalam Y.H. Hui (ed.) Bailey’s Industrial Oil and Fat Products. Fifth Edition Volume 3 Edible Oil and Fat Products: Products and Application Technology. John Wiley & Sons, Inc., New York.
Yang, T., M.B. Fruekilde, and X. Xu. 2003. Applications of Immobilized Thermomyces