LAPORAN PRAKTIKUM
PROSES PRODUKSI
PEMBUATAN ASAP CAIR DAN KARBON AKTIF DENGAN
PROSES PIROLISIS
DI SUSUN OLEH:
Nama/NIM : Siti Syamsiyah (14 644 004)
Lisa Mastura (14 644 028) Imam Fauzi C. (14 644 037)
Rina Dwi Safitri (14 644 043) Kelompok : II (Dua)
Kelas : VII A /S-1 Terapan Dosen Pengawas : Marinda Rahim ST., MT
LABORATORIUM OPERASI TEKNIK KIMIA
PILOT PLANT
LEMBAR PENGESAHAN
PROSES PRODUKSI
PEMBUATAN ASAP CAIR DAN KARBON AKTIF DENGAN
PROSES PIROLISIS
DI SUSUN OLEH:
Nama/NIM : Siti Syamsiyah (14 644 004)
Lisa Mastura (14 644 028) Imam Fauzi C. (14 644 037)
Rina Dwi Safitri (14 644 043) Kelompok : II (Dua)
Kelas : VII A /S-1 Terapan
Telah diperiksa dan disahkan pada tanggal……... 2017
Mengesahkan dan Menyetujui, Dosen Pembimbing
BAB I
PENDAHULUAN
1.1 Tujuan Percobaan- Mahasiswa dapat mengoperasikan alat pirolisis. - Mahasiswa dapat membuat asap cair grade 2. - Mahasiswa dapat membuat karbon aktif.
- Mahasiswa dapat menganalisis kualitas karbon aktif.
1.2 Dasar Teori 1.2.1 Pirolisis
Pirolisis adalah proses pemanasan suatu zat tanpa adanya oksigen sehingga terjadi penguraian komponen-komponen penyusun kayu keras. Istilah lain dari pirolisis adalah penguraian yang tidak teratur dari bahan-bahan organik yang disebabkan oleh adanya pemanasan tanpa berhubungan dengan udara luar. Hal tersebut mengandung pengertian bahwa apabila tempurung dan cangkang dipanaskan tanpa berhubungan dengan udara dan diberi suhu yang cukup tinggi, maka akan terjadi reaksi penguraian dari senyawa-senyawa kompleks yang menyusun kayu keras dan menghasilkan zat dalam tiga bentuk yaitu padatan, cairan dan gas (Widjaya, 1982).
Proses pirolisa melibatkan berbagai proses reaksi yaitu dekomposisi, oksidasi, polimerisasi, dan kondensasi. Reaksi-reaksi yang terjadi selama pirolisa kayu adalah : penghilangan air dari kayu pada suhu 120-150 °C, pirolisa hemiselulosa pada suhu 200-250 °C, pirolisa selulosa pada suhu 280-320 °C dan pirolisa lignin pada suhu 400 °C. Pirolisa pada suhu 400 °C ini menghasilkan senyawa yang mempunyai kualitas organoleptik yang tinggi dan pada suhu lebih tinggi lagi akan terjadi reaksi kondensasi pembentukan senyawa baru dan oksidasi produk kondensasi diikuti kenaikan linier senyawa tar dan hidrokarbon polisiklis aromatis (Girrard, 1992; Maga, 1988).
Hemiselulosa adalah komponen kayu yang mengalami pirolisa paling awal menghasilkan furfural, furan, asam asetat dan homolognya. Hemiselulosa tersusun atas pentosan (C5H8O4) dan heksosan (C6H10O5) dan rata-rata proporsi ini tergantung pada
heksosan membentuk asam asetat dan homolognya. Dekomposisi hemiselulosa terjadi pada suhu 200-250 °C (Girrard, 1992). Lignin dalam pirolisis menghasilkan senyawa fenol dan eter fenolik seperti guaiakol (2-metoksifenol) dan homolognya serta turunannya yang berperan terhadap aroma asap dari produk-produk hasil pengasapan. Fenol dihasilkan dari dekomposisi lignin yang terjadi pada suhu 300 °C dan berakhir pada suhu 450 °C (Girrard, 1992). Proses selanjutnya yaitu pirolisa selulosa menghasilkan senyawa asam asetat, dan senyawa karbonil seperti asetaldehida, glikosal dan akreolin. Pirolisa lignin akan menghasilkan senyawa fenol, guaiakol, siringol bersama dengan homolog dan derivatnya (Maga, 1988).
Distilasi kering kayu adalah salah satu cara yang digunakan untuk membuat produk-produk komersial dalam bentuk cair, padat maupun gas. Proses distilasi kering dilakukan dengan cara memanaskan kayu secara langsung maupun tidak langsung dengan udara terbatas ataupun tanpa udara. (Hendra, 1992). Produk yang diawetkan dengan asap yang diproduksi pada suhu 400 °C, lebih unggul mutu organoleptiknya dibanding perlakuan asap yang diproduksi dengan suhu yang lebih tinggi (Hanson, 2004). Selain itu, menurut Fretheim et al. (1980), efektifitas antara antioksidan dari fenol yang paling baik adalah dari hasil pembakaran pada temperatur 400 °C.
Jumlah dan sifat fenol yang terdapat dalam asap berhubungan langsung dengan suhu pirolisis kayu (Hamm dan Potthast, 1976 dalam Girard, 1992). Kadar maksimum senyawa fenol tercapai pada suhu pirolisis 600 °C (Hamm dan Potthast, 1976 dalam Girard, 1992). Peningkatan suhu sebesar 150 °C dari 350 menjadi 500 °C secara nyata tidak merubah kondensat asam, tetapi terjadi sedikit peningkatan efek antioksidatif. Suhu optimum pembuatan asap adalah sekitar 400 °C (Fratheim et al., 1980).
1.2.2 Asap Cair
Asap cair merupakan suatu campuran larutan dan dispersi koloid dari uap asap kayu dalam air yang diperoleh dari hasil pirolisa kayu atau dibuat dari campuran senyawa murni (Maga, 1988). Asap diproduksi dengan cara pembakaran yang tidak sempurna yang melibatkan reaksi dekomposisi konstituen polimer menjadi senyawa organik dengan berat molekul rendah karena pengaruh panas yang meliputi reaksi oksidasi, polimerisasi, dan kondensasi (Girrard, 1992). Partikel asap mempunyai diameter 0,1 μm. Proporsi partikel padatan dan cairan dalam medium gas menentukan kepadatan asap. Selain itu asap juga memberikan atribut warna dan flavor pada medium pendispersi gas (Pszczola, 1995).
Asap cair merupakan asam cuka (vinegar) diperoleh secara distilasi kering bahan baku asap misalnya batok kelapa, sabut kelapa atau kayu pada suhu 400 °C selama 90 menit lalu diikuti dengan peristiwa kondensasi dalam kondensor berpendingin air (Pszczola, 1995). Destilat yang diperoleh dimasukkan dalam corong pemisah untuk dipisahkan dari senyawa-senyawa kimia yang tidak diinginkan misalnya senyawa tar yang tidak larut dengan asam pirolignat. Asam pirolignat merupakan campuran dari asam-asam organik, fenol, aldehid, dan lain-lain.
Berikut merupakan komposisi asap cair: Tabel 1.1 Komposisi Kimia Asap Cair
Asap cair
pertama kali diproduksi pada tahun 1980 oleh sebuah pabrik farmasi di Kansas City, dikembangkan dengan metode kasar dari distilasi kayu asap (Pszczola, 1995). Produk yang berupa asap cair digunakan untuk mengawetkan daging babi dan babi asin dan untuk memberi citarasa pada beberapa bahan makanan. Menurut Maga (1988), asap cair mempunyai kelebihan antara lain : 1. Beberapa flavor dapat dihasilkan dalam produk yang seragam dengan konsentrasi
yang lebih tinggi dibandingkan dengan pengasapan tradisional. 2. Lebih intensif dalan pemberian flavor.
3. Kontrol hilangnya flavor lebih mudah
Komposisi Kimia Kandungan (%)
Air 11 – 92
Fenol 0,2 – 2,9
Asam 2,8 – 4,5
Karbonil 2,6 – 4,6
4. Dapat diaplikasikan pada berbagai jenis bahan pangan. 5. Dapat digunakan oleh konsumen pada level komersial. 6. Lebih hemat dalam pemakaian kayu sebagai sumber asap. 7. Polusi lingkungan dapat diperkecil.
8. Dapat diaplikasikan ke dalam berbagai cara penyemprotan, pencelupan, atau dicampur langsung ke dalam makanan (Pearson and Tauber, 1984).
Berikut ini merupakan standar kualitas asap cair spesifikasi jepang. Tabel 1.2 Kualitas asap cair spesifikasi Jepang
Parameter (Parameters) Mutu Asap Cair (Quality ofliquid smoke) gris
pH 1,50 - 3,70
Berat Jenis (Spesific Grafity) > 1,005
Warna (Color) Kuning coklat kemerahan
(Yellow brown reddish) Transparansi (Transparency) Transparan
(Tranparent) Bahan Terapunng (Material of Float),
%
Tidak ada bahan terapung (No float material)
Keasaman (Acidity), % 1 – 18
Fenol (Phenol), %
-Karbonil (Carbonil) %
-Sumber : Yatagai, 2002 Alpian dkk, 2012
pH merupakan salah satu parameter tinggi rendahnya kualitas dari asap cair, nilai pH ini menunjukkan tingkat dari proses penguraian yang terjadi pada komponen kayu untuk menghasilkan asam organik. Nilai pH yang rendah pada asap cair menunjukkan bahwa kualitas asap cair yang digunakan tinggi sedangkan nilai pH yang rendah menunjukkan bahwa kualitas asap cair rendah, karena pH sangat berpengaruh terhadap keawetan dan daya simpan produk asap cair. Tinggi rendahnya pH pada asap cair ini dipengaruhi oleh kadar fenol, suhu pirolisis dan sitem destilasi.
(1987), asap cair pada konsentrasi 6,5 gr/kg dapat memperpanjang fase lage Staphylococcus aurus (105 CFU/ml) selama 4 hari pada suhu kamar (30ºC) dan pada
konsentrasi 9,8 g/kg adalah 14 hari. Girrard (1992) menyatakan bahwa asap dalam bentuk cair berpengaruh terhadap keseluruhan jumlah asam dalam kondensat asap, yaitu mencapai 40% dengan 35 jenis asam. Kandungan asam yang mudah menguap dalam asam akan menurunkan pH, sehingga dapat memperlambat pertumbuhan mikroorganisme (Buckle et al.,1985). Menurut Haris dan Karmas (1989), kerja bakteriosidal dari pengasapan adalah faktor nyata dalam perlindungan nilai gizi produk yang diasap terhadap perusakan biologis. Efek fungisidal dalam asap disebabkan oleh fenol dan formaldehid (Daun, 1979; Toth dan Potthast, 1984).
Asap dalam bentuk cair juga masih mempunyai berbagai sifat fungsional. Fungsi lainnya adalah untuk memberikan flavor yang diinginkan pada produk asap karena adanya senyawa fenol dan karbonil (Pszczola, 1995). Rasa dan aroma khas produk pengasapan terutama disebabkan oleh senyawa guaiakol, 4-metil-guaiakol, dan 2,6-dimetoksi fenol. Girard (1992) mengatakan bahwa dari berbagai penelitian terdahulu, diketahui bahwa senyawa – senyawa fenolat tertentu seperti guaiakol, 4-metil guaiakol, 2,6-dimetoksi fenil dan seringol menentukan flavor dari bahan pangan yang diasap dimana guaiakol akan memberikan rasa asap dan seringol memberikan aroma asap. Rasa dan aroma yang khas pada makanan yang diasap disebabkan oleh senyawa fenol yang bereaksi dengan protein dan lemak yang terdapat pada makanan (Daun, 1979).
1.2.3 Karbon Aktif
gas dan uap dari campuran gas dan zat –zat tidak terlarut dan terdispersi dalam cairan melalui aktivasi. Struktur arang aktif digambarkan sebagai jaringan berpilin dari lapisan datar karbon yang tidak sempurna yang dihubungkan oleh ikatan karbon rantai lurus (alifatik). Luas permukaan, dimensi, dan distribusi arang aktif tergantung dari bahan baku yang digunakan, kondisi karbonisasi, dan proses aktivasi yang dilakukan (Dadang, 2006).
Menurut Standar Industri Indonesia (SII No. 0258-79), syarat mutu karbon aktif adalah sebagai berikut :
Tabel 1.3 Standar Kualitas Arang Aktif Menurut (SII No. 0258-79)
Jenis Uji Persyaratan
Bagian yang hilang pada pemanasan 950oC Max 15%
Kadar Air Max 10 %
Kadar Abu Max 2.5%
Bagian tidak mengarang Tidak ternyata
Daya serap terhadap I2 Min 20%
Sumber : (Anonim, 1979)
Kadar air merupakan kandungan air dalam arang dengan kondisi kering udara. Pada saat arang keluar dari tungku pengarangan, kadar air yang terkandung sangat kecil, biasanya kurang dari 1%. Proses penyerapan air dari udara sangat cepat sehingga dalam waktu singkat kadar air mencapai kadar air keseimbangan dengan udara sekitarnya. Arang yang berkualitas baik yang dipasarkan adalah arang yang mempunyai kadar air 5 – 10% (Fauziah, 2009)
Kadar abu merupakan jumlah sisa dari akhir proses pembakaran. Residu tersebut berupa zat – zat mineral yang tidak hilang selama proses pembakaran. Salah satu unsur utama abu adalah silika dan pengaruhnya kurang baik terhadap nilai kalor yang dihasilkan. Kadar abu setiap arang berbeda – beda tergantung jenis kayu, letak kayu dalam pohon, dan kandungan kulit kayu. Arang yang baik mempunyai kadar abu sekitar 3% (Fauziah, 2009).
Daya serap adalah peristiwa terjadinya perubahan kepekatan dari molekul, ion atau atom antar permukaan dalam dua fasa (Pari et al, 2000 dalam Fauziah, 2009). Hal ini terjadi bila dua fasa saling bertemu, sehingga di antara kedua fasa tersebut terbentuk daerah antar muka yang sifatnya berbeda dengan fasa ruah kedua fasa tersebut. Pada kondisi tertentu atom, ion atau molekul dalam daerah ini mengalami ketidakseimbangan gaya sehingga mampu menarik molekul lain sampai keseimbangan gaya tercapai. Zat yang terserap biasanya terkonsentrasi pada permukaan. Bahan yang yang terserap dinamakan adsorbat, biasanya berupa cairan atau gas, sedangkan yang menyerap disebut adsorben (Fauziah, 2009).
Uji iod merupakan parameter untuk mengetahui kemampuan arang aktif dalam menjerap molekul-molekul dengan jari-jari yang lebih kecil dari 10-15 Angstrom. Metode yang digunakan dalam uji daya jerap iod adalah metode titrasi iodometri menggunakan reaksi redoks dalam penentuannya. Reaksi redoks yaitu reaksi yang mengalami proses oksidasi dan reduksi. Reaksi oksidasi reduksi berlangsung secara bersama dan saling mengkompensasi satu sama lain (Khopkar, 2003 dalam Rizky, 2015).
Zat-zat yang bersifat pengoksidasi dalam larutan asam membebaskan iod dari kalium iodida, kemudian iod yang terbentuk dititrasi dengan larutan tio. Dengan reaksi :
I2 + 2Na2S2O3 2NaI + Na2S4O6
BAB II
4. Screening 7/16 in, no.4, no.5, no.16, no.18 dan no.20 5. Shaker Screen
6. Timbangan
7. 1 set peralatan pirolisis
8. Erlenmeyer 250 ml, 500 ml dan 1000 ml 9. Corong
10. 1 set peralatan destilasi 11. Spatula
4. Zeolite 5. Indikator PP 6. NaOH 0,1 N 7. Aquades 8. K2Cr207
9. Larutan HCl (asam clorida) 4 N 10. Larutan iod 0,1 N
11. Indikator amilum
1. Menyiapkan bahan baku tempurung kelapa sebanyak 3 Kg
2. Membersihkan sabut kelapa yang masih menempel pada tempurung menggunakan pisau
3. Mengecilkan ukuran tempurung kelapa menggunakan palu 4. Mengalirkan arus listrik pada alat crusher type KS5-15A 500L 5. Menyalakan tombol power alat crusher
6. Memasukkan tempurung kelapa yang sebelumnya telah dikecilkan ukurannya dengan palu
7. Menampung tempurung kelapa hasil keluaran alat crusher
8. Setelah semua tempurung kelapa selesai di kecilkan dengan alat crusher, mematikan alat crusher dengan menekan tombol power
9. Memutuskan aliran listrik pada alat crusher
10. Menyusun screening dari nomor urut terkecil yaitu 7/16 in, nomor 4, nomor 5 dan penampung secara berurutan dari atas ke bawah
11. Memasukan bahan baku tempurung kelapa ke dalam alat screening 12. Memasangkan screening ke alat shaker screen
13. Mengalirkan arus listrik pada alat shaker screen dan menekan tombol power pada alat shaker screen kemudian dijalankan selama 3 menit
14.Mematikan alat shaker screen dan mengeluarkan screening dari alat shaker screen
15. Mengambil tempurung kelapa yang lolos pada scereening 7/16 in dan nomor ayakan 4
17. Menyimpan tempurung kelapa di dalam toples untuk digunakan pada proses pirolisis
18. Memutuskan aliran listrik pada alat shaker screen
19. Membersihkan alat crusher, shaker screen, screening, timbangan dan seluruh area yang digunakan untuk praktikum.
20. Menghitung diameter rata-rata partikel tempurung kelapa 2.2.2 Proses Pirolisis
1. Menyiapkan tempurung kelapa yang telah dikecilkan ukurannya yaitu yang lolos pada scereening ukuran 7/16 in dan nomor ayakan 4
2. Memblending tempurung kelapa yang diperoleh sampai distribusi ukuran partikel merata
3. Menimbang 1 kg tempurung kelapa yang telah diblending
4. Mengeluarkan alat pirolisis dan stereform ke luar laboratorium menuju keluar gedung
5. Mengeluarkan alat pirolisis dari rak kayu dengan hati-hati 6. Mengeluarkan selongsong bahan baku dari alat pirolisis
7. Memadatkan bagian bawah pada bagian selongsong menggunakan sabut kelapa 8. Memasukkan bahan baku tempurung kelapa yang telah diblending dan
ditimbang 1 kg kemudian meratakannya
9. Memasukkan kembali selongsong ke dalam alat pirolisis 10. Menyambungkan kondensor ke alat pirolisis
11. Merangkai aliran air pendingin dengan menempatkan pompa ke dalam kotak steroform dan mengisi kotak steroform dengan air dan es batu 3 buah
12. Menghubungkan selang pada alat kondensor untuk selang air masuk berada didekat produk asap cair dan selang air keluar dekat dengan alat bahan baku dengan proses sirkulasi.
13. Menghubungkan alat pompa ke arus listrik 14. Menyiapkan erlenmeyer 1000 ml
15. Menimbang dan mencatat massa erlenmeyer 1000 ml kosong sebagai wadah penampung asap cair
16. Memasangkan erlenmeyer ke alat kondensor pada bagian ujung keluaran asap cair dan menutup mulut erlenmeyer dengan aluminium foil
17. Menghubungkan alat pirolisis ke arus listrik
18. Menaikan suhu alat pirolisis secara bertahap yaitu 150°C, 300°C, 450°C hingga 600°C
19. Melakukan proses pirolisis selama 3 jam setelah suhu set point 600°C tercapai 20. Mencatat setiap perubahan suhu yang terjadi pada saat suhu set poin sudah
tercapai sampai proses pirolisis selasai
22. Menimbang dan mencatat erlenmeyer yang terdapat produk asap cair dengan membuka terlebih dahulu tutup aluminium foil
23. Mengukur dan mencatat pH asap cair yang diperoleh menggunakan indicator universal serta mengamati dan mencatat warna asap cair yang diperoleh
24. Menutup kembali mulut Erlenmeyer dengan aluminium foil
25. Menyimpan Erlenmeyer yang berisis asap cair di laboratoium untuk mengendapkan Produk asap cair selama satu minggu untuk memisahkan fraksi berat (tar)
26. Menurunkan suhu alat pirolisis secara bertahap yaitu dari 600°C, 450°C, 300°C hingga 150 °C
27. Memutuskan aliran arus listrik pada alat pompa
28. Melepas rangkaian selang air pendingin dan membuang air pendingin yang ada didalam steroform
29. Menyimpan steroform, pompa dan selang ke dalam laboratorium
30. Melepas rangkaian kondensor dengan alat pirolisis pada saat suhu 150°C tercapai
31. Memutuskan aliran arus listrik pada alat pirolisis 32. Menyimpan alat kendensor ke laboratorium
33. Menutup bagian mulut alat pirolisis dengan aluminium foil 34. Memasukkan kembali alat pirolisis ke rak kayu dengan hati-hati
35. Memasukkan alat pirolisis kedalam gedung kemudian menuju laboratorium 36. Mengambil dan menimbang hasil residu berupa karbon yang ada didalam
selongsong alat perolisis setelah 24 jam
37. Menyimpan residu yang berupa karbon di dalam toples untuk di jadikan karbon aktif
38. Membersihkan kondensor dan selongsong alat pirolisis setelah 24 jam dengan menggunakan bensin dan aseton
2.2.3 Proses Pemurnian
1. Mengendapkan produk Asap cair selama 1 minggu untuk memisahkan fraksi berat (tar)
2. Menyaring produk asap cair hasil pengendapan dengan menggunakan kertas saring whatman no. 42
3. Mengukur dan mencatat pH asap cair hasil penyaringan 4. Mengamati dan mencatat warna asap cair setelah penyaringan
5. Memasukkan produk asap cair hasil penyaringan kedalam labu leher tiga 500 ml yang telah diisi dengan batu didih
6. Memasang labu leher tiga pada pemanas serta menghubungkan ke kondensor dengan menggunakan konektor dan memasukkan thermocouple ke dalam asap cair melalui leher labu
8. Menimbang massa erlemenyer 500 ml kosong sebagai tempat penampung destilat asap cair
9. Memasangkan erlenmeyer 500 ml ke kondensor dengan menggunakan elbow 10. Menghubungkan alat pemanas (heating mantle) dan kondensor dengan arus
listrik
11. Menjalankan air pendingin pada kondensor dan menghidupkan thermocouple dengan menekan tombol power
12. Mengatur suhu heating mantle dan mengamati serta mencatat temperatur yang ada pada thermocouple dan waktu pada saat terjadi tetesan pertama pada erlenmeyer
13. Menjalankan proses destilasi sampai tidak ada lagi cairan yang menetes dari kondensor ke erlenmeyer
14. Mengambil erlenmeyer yang berisi asap cair hasil destilasi
15. Mengukur dan mencatat pH destilat yang diperoleh, serta mengamati dan mencatat warna setelah destilasi
16. Menurunkan suhu heating mantle dan mematikan alat watebath dan thermocouple dengan menekan tombol power
17. Memutuskan aliran arus listrik pada heating mantle dan waterbath 18. Melepaskan rangkaian kondensor dari labu leher tiga
19. Membersihkan labu leher tiga, konector , elbow dan seluruh daerah yang digunakan untuk praktikum
20. Menimbang dan mencatat Erlenmeyer yang berisi asap cair hasil destilasi 21. Menambang zeolite ke dalam Erlenmeyer dengan massa yang sama seperti
massa asap cair hasil destilasi dengan berbandingan masssa 1 : 1
22. Merendam dengan zeolite selama 1 jam kemudian menyaring produk asap cair meggunakan kertas saring whatman no. 42
23. Mengukur dan mencatat pH asap cair yang telah disaring, setelah di rendam dengan zeolite
24. Mengamati dan mencatat perubahan warna produk asap cair setelah di rendam dengan zeolite
2.2.4 Proses Analisa Asam Asetat Pada Produk Asap Cair
1. Mengambil 10 ml produk asap cair dan memasukkannya kedalam labu ukur 100 ml
2. Mengencerkan hingga 100 ml dengan aquades
5. Menitrasi dengan menggunakan NaOH 0,1 N sampai berubah warna menjadi merah muda
6. Mencatat volume NaOH yang digunakan untuk titrasi dan menghitung konsentrasi asam pada asap cair sebagai asam asetat
2.2.5 Preparasi Arang
1. Menyiapkan karbon hasil proses prolisis
2. Melakukan pengecilan ukuran pada karbon tersebut menggunakan lumpang, alu dan blender
3. Menyusun screening dari nomor urut terkecil yaitu nomor 16, nomor 18 dan penampung secara berurutan dari atas ke bawah
4. Memasukan bahan baku karbon ke dalam alat screening 5. Memasangkan screening ke alat shaker screen
6. Mengalirkan arus listrik pada alat shaker screen dan menekan tombol power pada alat shaker screen kemudian dijalankan selama 3 menit
7. Mematikan alat shaker screen dan mengeluarkan screening dari alat shaker screen
8. Mengambil karbon yang lolos pada scereening nomor 16 dan tertahan pada nomor 18
9. Menimbang dan mencatat hasil screening hingga diperoleh berat total 50 gram karbon
10. Menyimpan karbon di dalam gelaas kimia 250 ml untuk digunakan pada proses pembuatan karbon aktif
11. Memutuskan aliran listrik pada alat shaker screen
12. Membersihkan alat shaker screen, screening, timbangan, blender, lumping, alu dan seluruh area yang digunakan untuk praktikum.
2.2.6 Proses Aktifasi Kimia Pada Karbon
a. Pembuatan larutan H2SO4 20 % dari H2SO4 96 %
1. Menyiapakan larutan H2SO4 96 % dan labu ukur 500 ml
2. Menuangkan larutan H2SO4 96 % kedalam gelas kimia 250 ml
3. Menambahkan sedikit aquades kedalam labu ukur 500 ml
4. Memipet asam sulfat 96 % sebanyak 104,17 ml dan memasukkan kedalam labu ukr 500 ml
5. Menambahkan aquades hingga tanda batas
6. Mendiamkan beberapa menit agar panas pada larutan hilang kemudian menghomogenkannya
7. Proses pembuatan larutan H2SO4 20 % dilakukan di lemari asam
b. Pembuatan arang Aktif
1. Menyiapakan larutan H2SO4 20 % dan karbon yang lolos pada scereening
2. Mengambil karbon yang sudah diayak dengan perbandingan karbon dan aktivatornya (1 : 10) yaitu 50 gram karbon dan 500 ml H2SO4 20 % yang
telah dibuat kemudian di masukkan ke dalam gelas kimia 1000 ml
3. Memasukkan stirrer ke dalam larutan dan menutupnya dengan alumunium foil
4. Melakukan aktivasi kimia dengan menggunakan aktivator H2SO4 20 %
5. Menghubungkan hot plate dengan arus listrik
6. Melakukan perendaman dengan aktivator dan diaduk menggunakan stirrer dengan kecapatan sedang diatas hot plate selama 2,5 jam
7. Mematikan tombol power dan memutuskan arus listrik pada hot plate 8. Menyaring karbon yang telah direndam menggunakan kertas saring 9. Mencuci karbon dengan aquades hingga mencapai pH netral
10. Melakukan pengeringan menggunakan oven selama 2 jam pada suhu 120oC
11. Mendinginkan karbon aktif didalam desikator selama 15 menit 12. Menyimpan karbon aktif untuk kemudian akan di analisa kadarnya
2.2.7 Analisa Hasil
a. Analisa Kadar Air (ASTM D-3173)
1. Menghubungkan arus listrik dan menekan tombol power pada oven 2. Menaikkan suhu oven hingga 110oC
3. Menimbang cawan petridish kosong + tutupnya dan mencatat data
4. Menambahkan sampel karbon aktif ± 1 gram kedalam cawan petridish, meratakan contoh kemudian menutup kembali petridish
5. Menempatkan tutup petridish dalam desikator dan memasukkan petridish tanpa tutup (menggunakan metal tray) kedalam oven
6. Memanaskan selama satu jam
7. Mengeluarkan tray dari oven, menutup petridish dengan segera lalu memasukkan kedalam desikator sampai mencapai suhu ruangan (kira-kira 10-15 menit)
8. Menimbang petridish, tutup petridish dan sampel yang telah didinginkan 9. Mencatat hasil penimbangan pada lembar kerja analisa
10. Melakukan perhitungan dengan menggunakan persamaan sebagai berikut Perhitungan :
% Kadar Air = m2−m3
Keterangan :
m1= massa cawan kosong (gram)
m2 = massa cawan + sampel (sebelum pemanasan) (gram)
m3= massa cawan + sampel (setelah pemanasan) (gram)
11. Menurunkan suhu oven sampai 40°C kemudian mematikan dan memutuskan arus listrik pada oven
b. Analisa Kadar Abu (ASTM 3174-77)
1. Menimbang cawan crucible bersih dan mencatat beratnya pada lembar kerja analisa
2. Menambahkan ±1 gram karbon aktif kedalam cawan crucible dan mencatat beratnya. Mengetuk pelan-pelan untuk meratakan contoh
3. Meletakkan cawan dan contoh kedalam furnace pada suhu ruangan 4. Menghubungkan arus listrik dan menekan tombol power pada furnace 5. Mengatur suhu hingga 500oC membiarkan selama 60 menit.
6. Menaikkan suhu furnace sampai 750 oC dan memanaskan selama 120
menit.
7. Mengeluarkan cawan dari dalam furnace kemudian memasukannya ke dalam desikator selama 10-15 menit dan membiarkan sampai dingin hingga mencapai temperatur ruangan
8. Menimbang cawan dan abu serta mencatat hasil penimbangan pada lembar kerja analisa.
9. Membersihkan cawan dengan menggunakan kuas kering dan menimbang kembali cawan serta mencatat hasil penimbangan pada lembar kerja analisa.
10. Melakukan perhitungan dengan menggunakan persamaan sebagai berikut Perhitungan:
% Kadar Abu = m3m2−m4
−m1 × 100% Keterangan:
m1= massa cawan kosong (sebelum pemanasan) (gram)
m2= massa cawan + sampel (sebelum pemanasan) (gram)
m4= massa cawan kosong (setelah pemanasan) (gram)
c. Analisa Uji Volatile Matter (ASTM D 3175) 1. Menaikkan suhu furnace VM hingga 950°C
2. Mencatat nomor sampel dan nomor cawan crucible pada lembar kerja analisa
3. Menimbang cawan crucible kosong beserta tutup kemudian mencatatnya pada lembar kerja analisa
4. Menambahkan ±1 gram karbon aktif ke dalam cawan crucible, kemudian menutupnya kembali dan mencatat hasil penimbangan
5. Memasukkan cawan crucible yang telah berisi karbon aktif ke dalam furnace beserta tutupnya dan memijarkan selama 7 menit
6. Mengeluarkan cawan crucible dari furnace dan mendinginkannya pada desikator selama 7 menit
7. Menimbang cawan crucible yang berisi residu yang telah didinginkan tersebut beserta tutupnya dan mencatatnya pada lembar kerja analisa 8. Melakukan perhitungan dengan menggunakan persamaan :
% Volatile Meter = ( m2−m3
m2−m1 × 100%) – Kadar air Keterangan:
m1= massa cawan kosong (gram)
m2= massa cawan + sampel (sebelum pemanasan) (gram)
m3= massa cawan + sampel (setelah pemanasan) (gram)
11. Menurunkan suhu furnace sampai 70°C kemudian mematikan dan memutuskan arus listrik pada furnace
d. Analisa Daya Serap Terhadap I2 (Dahlius A, dkk, 1983) Standarisasi Larutan Natrium Tiosulfat 0,1
1. Menimbang 0,5 gram K2Cr2O7 didalam gelas kimia 50 ml dan
melarutkannya dengan sedikit aquades
3. Memipet 25 ml larutan kedalam Erlenmeyer 500 ml kemudian menambahkan 10 ml KI 20 % dan 25ml HCL 4 N
4. Mengencerkan hingga 200 ml
5. Menitrasi dengan natrium tiosulfat 0,1 N hingga berwarna kuning muda 6. Menambahkan indicator kanji hingga menjadi warna hijau
7. Melanjutkan titrasi hingga waarna bening
N natrium tiosulfat = FP ×ml tio ×mg K2Cr2O497
Standarisasi Laruan Iod 0,1 N
1. Memipet 25 ml larutan natrium tiosulfat 0,1 N kedalam Erlenmeyer 250 ml
2. Menambahkan indicator kanji
3. Menitrasi dengan larutan iod 0,1 N hingga larutan bewarna biru N iod = ml tio× N tio
ml Iod
Analisa Daya Serap Terhadap I2
1. Menimbang dengan teliti ±1 gram arang aktif kemudian memasukkannya ke dalam Erlenmeyer 250 ml
2. Menambahkan 50 ml aquadest dan 5 ml larutan Iod 0,1 N yang telah di standarisasi.
3. Mengocok dengan hati-hati dan menutup dengan aluminium foil lalu menyimpan di tempat gelap selama 2 jam.
4. Menyaring untuk diambil filtratnya kedalam Erlenmeyer yang bersih. 5. Menambahkan 25 ml aquadest dan indikator kanji (amilum) dan
menitrasinya dengan larutan Natrium Thiosulfat 0,1 N yang sudah di standarisasi.
6. Sebagai pembanding, digunakan larutan blanko yang dianalisa dengan cara yang sama tanpa arang aktif.
Daya serap iod (mg/g) = (b−a)× N Thio × BE Iod g contoh
Keterangan :
b = volume titran blanko (mL) a = volume titran untuk contoh (mL)
e. Analisa Uji Fixed Carbon (ASTM D 3172)
Penentuan fixed carbon ditemtukan denan rumus : % fixed carbon = 100 % - (%M) - (%ash) – (% VM)
BAB III
PENGOLAHAN DATA
3.1 Data Pengamatan
Tabel 3.1.1 Data Pengamatan Massa Bahan Baku Berdasarkan Ukurannya
Nomor
Tabel 3.1.2 Data Pengamatan Neraca Massa Proses Pirolisis
Massa bahan
Tabel 3.1.3 Data Pengamatan Proses Pirolisis
Variabel Nilai
T setpoint (oC) 600
T aktual (oC) 596+603
2 =599,5
Waktu pirolisis (h) 3
Massa bahan baku (g) 1000,18
Warna produk asap cair Coklat gelap
pH produk asap cair 2
Tabel 3.1.4 Data Pengamatan Proses Pemurnian Asap Cair
Parameter Nilai / Penampakan
Warna sebelum pemurnian Coklat gelap
pH sebelum pemurnian 2 (dua)
Warna setelah disaring Coklat
pH setelah disaring 2 (dua)
Temperatur tetes pertama destilasi 101,1 oC
Waktu saat tetes pertama destilasi 41 menit setelah pemanasan Warna setelah destilasi Kuning kecoklatan
pH setelah destilasi 2 (dua)
Warna setelah di rendam zeolit Kuning pH setelah di rendam zeolit 3 (tiga)
Tabel 3.1.5 Data Pengamatan Analisa Kadar Asam Asetat pada Asap Cair
Parameter Nilai
Volume sampel asap cair yang dititrasi (ml) 25 Volume NaOH 0,1 N yang digunakan untuk titrasi (ml) I = 41,25
II = 41,55
Tabel 3.1.6 Data Pengamatan Analisa Kadar Air
Sampel Massa karbon m1
1 1,0003 82,5111 83,5114 83,3807
2 1,0001 71,0435 72,0436 71,9167
Tabel 3.1.7 Data Pengamatan Analisa Kadar Abu
Sampel m1
1 20,9727 21,9731 20,9807 20,9709
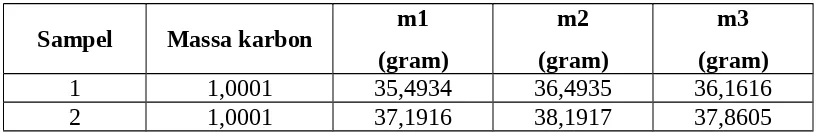
Tabel 3.1.8 Data Pengamatan Analisa Volatile Matter
1 1,0001 35,4934 36,4935 36,1616
2 1,0001 37,1916 38,1917 37,8605
Data Pengamatan Standarisasi Larutan Natrium Tiosulfat 0,1 N
Massa K2Cr2O7 = 0,5032 g
Faktor pengencer = 4
Bst K2Cr2O7 = 49
Volume Natrium Tiosulfat yang digunakan untuk titrasi = 25,1 ml
Data Pengamatan Standarisasi Larutan I2 0,1 N
Volume Natrium Tiosulfat = 25 ml
N Natrium Tiosulfat = 0,1 N
Volume I2 yang digunakan untuk titrasi = 26,1 ml
Tabel 3.1.9 Data Pengamatan Analisa Daya Serap I2
Sampel Massa Karbon
Tabel 3.2.1 Randemen Asap Cair dan Karbon Aktif
Massa bahan baku
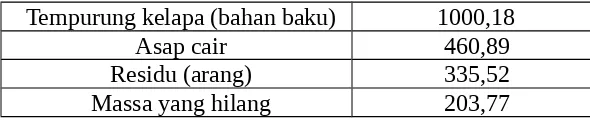
Tabel 3.2.2 Neraca Massa Proses Pirolisis
Tempurung kelapa (bahan baku) 1000,18
Asap cair 460,89
Residu (arang) 335,52
Massa yang hilang 203,77
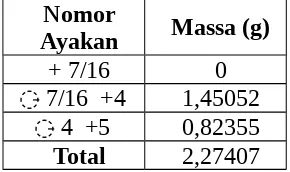
Tabel 3.2.3 Diameter Rata-Rata Bahan Baku
Nomor
+4 1,45052 0,63785 7,925 497,735 260,315 2,45 ∙ 10
-3
4 +5
̵̵ 0,82355 0,36215 4,375 83,740 43,796 8,27 ∙ 10-3
Total 2,27407 1 0,01072
Tabel 3.2.4 Kadar Asam Asetat dalam Asap Cair
Sampel Nilai (%)
1 3,76
2 3,78
Rata - rata 3,77
Tabel 3.2.5 Kualitas Karbon Aktif
Sampel Kadar air
1 13,0661 0,9796 20,3093 1,4270
66,2486
2 12,6887 0,2199 20,2393 0,9079
Rata-rata 12,8774 0,5997 20,2743 1,1675
3.3 Pembahasan
Pada praktikum asap cair dan karbon aktif dengan proses pirolisis memiliki tujuan yaitu dapat mengoprasikan alat pirolisis, dapat membuat asap cair, dapat membuat karbon aktif dan dapat menganalisis kualitas karbon aktif. Pirolisis tempurung kelapa dilakukan pada suhu 600oC selama 3 jam menggunakan massa tempurung kelapa
dengan rendemen karbon sebesar 33,55 %. Berdasarkan massa hasil pirolisis dapat diketahui 203,77 g dengan rendamen 20,37 % merupakan massa yang hilang dari proses pirolisis, hal ini disebabkan karena ada asap yang tidak terkondensasi sehingga tidak menjadi produk hasil asap cair.
Berdasarkan table 3.1.4 mengenai pengamatan proses pemurnian asap cair yang diperoleh dari hasil pirolisis berwarna cokelat gelap dengan pH 2 namun setelah proses destilasi, diperoleh asap cair berwarna kuning kecoklatan dengan pH 2 dan setelah dilewatkan melalui zeolit aktif berubah menjadi berwarna kuning dengan pH 3, larutan transparan, tidak terdapat partikel melayang dan aroma asap yang berkurang. Harga pH tersebut menyimpulkan bahwa produk asap cair tersebut bersifat asam. Hal ini menyatakan banyaknya unsur-unsur dalam tempurung kelapa yang terurai dan membentuk senyawa - senyawa kimia yang bersifat asam.. Proses pemurnian menyebabkan senyawa berbahaya seperti benzopirene dan tar yang terdapat di dalam asap cair teradsorpsi oleh zeolit aktif (Rinaldi, 2015). Semakin besar luas permukaan zeolite yang digunakan maka semakin efektif zeolite dalam mengadsorpsi senyawa-senyawa pengotor pada asap cair. Sehingga akan semakin jernih asap cair hasil perendaman yang diperoleh. Menurut standar Jepang dari asap cair berdasarkan parameter pH asap cair 1,5-3,70; warna asap cair kuning kecoklatan kemerahan; produk transparan, tidak terdapat bahan terapung dan keasaman sebesar 1 % sampai 18 %. Berdasarkan tabel 3.2.4 kadar asam asetat dalam asap cair hasil pirolisis menghasilkan kadar asam asetat sebesar 3,77 %. Berdasarkan beberapa parameter hanya kadar asam asetat yang tidak sesuai dengan Standar Jepang yang sudah ditentukan dikarenakan tingginya suhu pirolisis menyebabkan semakin tinggi panas pada tempurung kelapa untuk menguraikan hemiselulosa dan selulosa menjadi komponen-komponen senyawa kimia yang bersifat asam terutama asam asetat. Kandungan asam pada asap cair berhubungan dengan kualitas asap cair terutama fungsinya sebagai pengawet makanan. Berdasarkan perbandingan asap cair hasil percobaan dan standar Jepang dapat diketahui produk asap cair pada percobaan dari sifat fisik dan pH produk asap cair yang dihasilkan memenuhi standar. Tetapi keasaman yan diperoleh tidak memenuhi standar Jepang dikarenakan
66,2486% dan daya serap iod 1,1675%. Standar kualitas arang aktif menurut SII (Standar Industri Indonesia) dalam bentuk butiran yaitu kadar air maksimal 10%, kadar abu maksimal 2,5%, volatile matter maksimal 15% dan daya serap iod minimal 20% dan standar kualitas arang aktif menurut SNI (Standar Nasional Indonesia) fixed carbon minimal 65%. Berdasarkan SII tersebut dapat diketahui bahwa kadar abu arang aktif sudah sesuai dengan standar dan fixed carbon menurut SNI sudah memenuhi standar. Namun, pada parameter kadar air, volatile matter dan daya serap iod tidak memenuhi standar. Kadar air dan volatile matter disebabkan karena arang yang diaktivasi dengan H2SO4, kemudian dicuci menggunakan aqudest sampai pH netral membuat pori-pori
arang aktif yang sudah terbuka dapat menyerap mineral-mineral yang masih terkandung di aquadest. Daya Serap iod yang tidak memenuhi SII dikarenakan arang yang diaktivasi dengan H2SO4 telah mengalami kerusakan dinding struktur dari arang
BAB IV
KESIMPULAN
Berdasarkan pada percobaan yang telah dilakukan, maka dapat diperoleh kesimpulan:
1. Rendemen asap cair hasil pirolisis pada suhu 600oC sebesar 46,08 %,
rendemen karbon aktif sebesar 33,55 % dan rendamen massa hilang sebesar 20,37 %.
2. Produk asap cair hadri proses pirolisis memiliki visual berwarna kuning dengan pH 3, larutan transparan, tidak terdapat partikel melayang dan kadar asam asetat sebesar 3,77%, dari beberapa parameter hanya kadar asam asetat yang tidak sesuai dengan standar asap cair yang diinginkan berdasarkan Standar Jepang.
DAFTAR PUSTAKA
Buckle, K. A., R. A. Edwards, G. H. Fleet dan M. Wooton. 1985. Ilmu Pangan. Terjemahan H. Purnomo dan Adiono. Indonesian University Press. Jakarta.
Chon, H.A, dan Krisnandi, E. (1982). Penuntun Praktikum Kimia Analisis Jumlah II Titrimetri. Bogor: Departemen Perindustrian. Sekolah Menengah Analis Kimia Bogor
Dadang. (2006). Jarak Pagar Sebagai Tanaman Penghasil Biodiesel. https://books.google.co.id/books?
id=w2qZ9uLFrw0C&pg=PA102&hl=id&source=gbs_toc_r&cad=3#v=onepage &q&f=false
Darmadji, P. 1995 Produksi Asap Cair dan Sifat-Sifat Fungsionalnya. Fakultas Teknologi Pangan, Universitas Gadjah Mada, Yogyakarta.
Darmadji, P. 2002. Optimasi Pemurnian Asap Cair dengan Metode Redistilasi. Jurnal Teknologi dan Industri Pangan 8(3);267-171.
Daun, H.1979. Interaction of Wood Smoke Components and Foods. Food Technol. 33 (5) 66-71.
Djatmiko, B., S. Ketaren dan Setyakartini. 1985. Arang Pengolahan dan Kegunaannya. Departemen Teknologi Hasil Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Fauziah, N. (2009). Pembuatan Arang Aktif Secara Langsung Dari Kulit Acacia Mangium Wild Dengan Aktivasi Fisika Dan Aplikasinya Sebagai Adsorben. Skripsi Institut PertanianBogor. Repository,ipb.ac.id/bitstream/handle/ 123456789/13071/E09nfa.pdf
Fretheim, K., P. E. Granum dan Vold. 1980 Influence of Generation Temperature on The Chemical Composition, Antioxidative Antimicrobial Effects of Wood Smoke. J. Food Science 45 : 999-1007.
Girrard, J.P. 1992. Technology of Meat and Meat Products. Ellis horwood. New York.
Hendra, D. 1992. Hasil Pirolisis dan Nilai Kalor dari 8 Jenis Kayu di Indonesioa Bagian Timur. Jurnal Penelitian Hasil Hutan Vol. 10(4);122-124.
Maga, J.A. 1988. Smoke in Food Processing. CRC Press, Florida.
Pearson, A.M. dan F.W. Tauber. 1973. Processed Meats, second edition. AVI Publishing Company Inc., Wesport Connecticut.
Pszczola, Donald E. 1995. Tour Highlights Production and Uses of Smoke-Based Flavors. Food Technol. 49(1);70-74.
Tim Laboratorium Proses Produksi. (2016). “Penuntun Praktikum Proses Produksi Semester VII”, Politeknik Negeri Samarinda: Samarinda
Toth, L. dan K. Potthast. 1984. Chemical Aspect of the Smoking of Meat and Meat Products dalam C. O. Chichester, E. M. Mrakdan B. S. Schweigert (ed.). Advances in Food Research. Vol. 29. Academic Press, Inc., New York. London.
PERHITUNGAN
a. Diameter Rata-Rata Bahan Baku
c = π6=¿ 0,523
Dv =
√
3∈xi c .∈ xi
c . Di3
=
√
3 10,523x0,01072 = 3
√
178,362 = 5,629 mm b. Randemen Asap CairRendemen=produk asap cair(g) bahan baku(g) ×100
¿ 460,89 1000,18×100 ¿46,0807
c. Randemen Karbon Aktif
Rendemen=produk karbon aktif(g) bahanbaku(g) ×100
¿ 335,52 1000,18×100 ¿33,5459
d. Neraca Massa Proses Pirolisis
Massa tempurung kelapa masuk (bahan baku) = 1000,18 g Massa produk asap cair = 460,89 g
Massa bahan baku = massa produk asap cair + massa residu + massa yang hilang 1000,18 = 460,89 + 355,52 + massa yang hilang Massa yang hilang = 1000,18 – 460,89 – 355,52
= 203,77 g
e. Berat jenis asap cair
Massa pikno kosong = 12,5504 g Suhu asap cair = 29 oC
Berat jenis air (29 oC) = 0,9960 g/ml
Massa piknometer kosong + isi = 17,8207
Volume pikno = 5 ml
Densitas = massa piknometer+isi – massa piknometer kosong volume piknometer
= 17,8207−512,5504 = 1,05406 g/ml
Berat jenis = densitas asap cair densitas air29oC = 1,05406g/m l
0,9960g/ml = 1,0583
f. Kadar Asam Asetat dalam Asap Cair
Volume sampel produk asap cair = 25 ml
Densitas asap cair = 1,05406 g/ml
Densitas = massa sampel asap cair(g) volume sampel(ml)
Massa sampel asap cair (g) = densitas (g/ml) x volume sampel (ml) = 1,05406 g/ml x 25 ml
Volume NaOH = 41,25 ml
N NaOH = 0,1 N
Faktor pengencer (fp) = 100 ml / 25 ml = 4 Bm CH3COOH = 60 g/gmol
Kadar asam asetat (%) = V x N x BM x fp x100 mg sampel
= 41,25x0,126351,5x60x4x100 = 3,76 %
g. Volume Larutan Induk yang Dibutuhkan untuk Membuat H2SO4 20 %
Larutan induk = H2SO4 96 %
Volume H2SO4 96 % = V1
Volume H2SO4 20 % = V2
V1 ∙ %1 = V2 ∙ %2
V1=1V2∙2
¿500ml ∙20 96
¿104,17ml
h. Kadar Air Karbon Aktif
kadar air=m2−m3 m2−m1
¿83,5114−83,3807 83,5114−82,5111×100 ¿13,0661
i. Kadar Abu Karbon Aktif
kadar abu=m3−m4 m2−m1
×100
¿20,9807−20,9709 21,9731−20,9727×100
¿0,9796
j. Volatile Matter Karbon Aktif
volatile matter=
(
m2−m3m2−m1×100
)
−kadar air ¿(
36,4935−36,161636,4935−35,4934×100
)
−12,8774¿20,3093
k. Fixed Carbon Karbon Aktif
% Fixed carbon = 100% – (kadar air + kadar abu + volatile matter) = 100 % – (12,8774+ 0,5997+ 20,2743) %
= 66,2486 %
l. Konsentrasi Larutan Natrium Tiosulfat Sebenarnya
Massa K2Cr2O7 = 0,5032 g
Faktor pengencer (fp) = 100 ml: 25 ml = 4
Bst K2Cr2O7 = 49
Volume Natrium Tiosulfat yang digunakan untuk titrasi = 25,1 ml
N tio= massa K2Cr2O7(mg)
fp × volume tio(ml)× Bst K2Cr2O7
¿0,1023N
m. Konsentrasi Larutan I2 Sebenarnya
Volume Natrium Tiosulfat = 25 ml
N Natrium Tiosulfat = 0,1023 N
Volume I2 yang digunakan untuk titrasi = 26,1 ml
N Iod=volume tio(ml)× N tio volume Iod
¿25×0,1023 26,1 ¿0,0980N
n. Daya Serap Karbon Aktif terhadap I2
Massa contoh = 1000,7 mg Ntio = 0,1023 N
b = 4,9 ml a = 3,8 ml
Daya serap Iod( )=(b−a)× N tio× BE Iod massa contoh(mg) x100
¿(4,9−3,8)×0,1023×126,9
1000,7 x100