Lampiran 1. Bagan alur penelitian
Ditambahkan 30 mL akuades
Ditambahkan 12,5 mL CaCl2 0,063M
Ditambahkan 25 ml buffer tris-HCl 1M, pH 8
Ditambahkan 500 mg lypozyme TL IM.
Dikocok dengan shakersetiap 1 jam, kecepatan 200 rpm, 10 menit
Diinkubasi selama 18 jam dengan interval waktu pengamatan nilai bilangan asam setiap 2 jam
-
0 jam (V0) - 10 jam (V10)- 2 jam (V2) - 12 jam(V12)
- 4 jam (V4) - 14 jam(V14)
- 6 jam (V6) - 16 jam(V16)
- 8 jam (V8) - 18 jam(V18)
Dipindahkan ke corong pisah untuk diekstraksi
V
4V
6V
8V
10V
12V
14VCO hasil hidrolisis sebelum
ekstraksi (Lanjutan)
30 gram VCO masing-masing dimasukkan ke dalam Erlenmeyer 250 mL
V
16V
2V
18Lampiran 1. Bagan alur penelitian (Lanjutan)
VCO hasil hidrolisis
sebelum ekstraksi
Diekstraksi dengan 50 ml n-heksan
Diekstraksi dengan 50 ml n-heksan
Didiamkan beberapa saat
Residu: Fraksi Air
(lapisan bawah)
Filtrat I :
Fraksi n-heksan (lapisan atas)
Didiamkan beberapa saat
Residu
Filtrat II
Digabung
Ditambahkan 50 mg Na2SO4 anhidrat,
diamkan 15 menit
Diuapkan diatas penangas air untuk menghilangkan n-heksan
Lampiran 1. Bagan alur penelitian (Lanjutan)
Dihitung jumlah asam lemak bebas dengan penentuan nilai bilangan asam
Uji aktivitas antibakteri
secara
in-vitroV
4V
6V
8V
10V
12V
14VCO hasil hidrolisis enzimatis
yang optimal
Uji aktivitas antibakteri
secara
in-vivoFraksi yang memberikan bilangan asam paling optimal selanjutnya diambil untuk diuji aktivitas antibakteri
secarain-vitro
konsentrasi uji aktivitas “VCO hasil hidrolisis enzimatis” secara in-vitro yang paling baik selanjutnya diambil
untuk pengujian in-vivo
V
2V
16VCO hasil hidrolisis: Asam lemak bebas, monogliserida, dan trigliserida
Lampiran 2. Bahan dan Alat yang digunakan
Gambar 1. Salmonella typhi
(A) dan
Salmonella typhimurium(B) dalam
Microbank
Gambar 2.(A) Blank disc
; (B) Disc baku Kloramfenikol (30µg/disc)
Lampiran 2. Bahan dan Alat yang digunakan (Lanjutan)
Gambar 3. (A) VCO Palem Mustika; (B) Lipozyme® TL IM; (C) n-Hexane
(p.a); (D) Tris-buffer (p.a); (E) Formalin; (F) Etanol (p.a)
A
B
E
D
C
Lampiran 2. Bahan dan Alat yang digunakan (Lanjutan)
Gambar 4. Nutrient Broth(A); Nutrient Agar(B); Mueller Hinton Agar(C); Triple
Sugar Iron Agar(D); Brain Heart Infusion(E); Salmonella Shigella Agar(F)
A
B
C
E
Lampiran 2. Bahan dan Alat yang digunakan (Lanjutan)
Gambar 5. (A)Ultrasonic cleaner
; (B) Hotplate; (C) Neraca analitis; (D)
Water-bath; (E)
ShakerA
E
D
C
Lampiran 2. Bahan dan Alat yang digunakan (Lanjutan)
Gambar 6. (A) dan (D) Laminar Air Flow Cabinet
; (B)Neraca Analitis; (C)
Inkubator; (E)
Colony Counter; (F) pipet volumetrik
A
C
E
D
B
Lampiran 2. Bahan dan Alat yang digunakan (Lanjutan)
Gambar 7. (A) Autoklaf; (B)Oven; (C) Bunsen; (D) spektrofotometer;
(E) Neraca hewan; (F) mikroskop & komputer
A
B
C
D
E
Lampiran 5. Data hasil perhitungan pembakuan NaOH
Rumus hitung pembakuan NaOH(Normalitas NaOH):
miligrek K. Biftalat = Miligrek NaOH
mg K. Biftalat
BE
= V × N NaOH
N NaOH =
mg K Biftalat
BE × V
Keterangan: BE
K.Biftalat= Bobot Ekuivalen = BM = 204,2
V =Volume titrasi NaOH
N = Normalitas
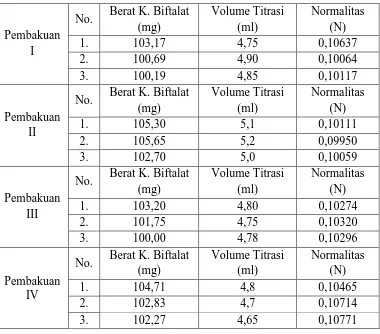
Tabel 5.1 Data pembakuan NaOH
Pembakuan
I
No.
Berat K. Biftalat
(mg)
Volume Titrasi
(ml)
Normalitas
(N)
1.
103,17
4,75
0,10637
2.
100,69
4,90
0,10064
3.
100,19
4,85
0,10117
Pembakuan
II
No.
Berat K. Biftalat
(mg)
Volume Titrasi
(ml)
Normalitas
(N)
1.
105,30
5,1
0,10111
2.
105,65
5,2
0,09950
3.
102,70
5,0
0,10059
Pembakuan
III
No.
Berat K. Biftalat
(mg)
Volume Titrasi
(ml)
Normalitas
(N)
1.
103,20
4,80
0,10274
2.
101,75
4,75
0,10320
3.
100,00
4,78
0,10296
Pembakuan
IV
No.
Berat K. Biftalat
(mg)
Volume Titrasi
(ml)
Normalitas
(N)
1.
104,71
4,8
0,10465
2.
102,83
4,7
0,10714
Lampiran 5. Data hasil perhitungan pembakuan NaOH (Lanjutan)
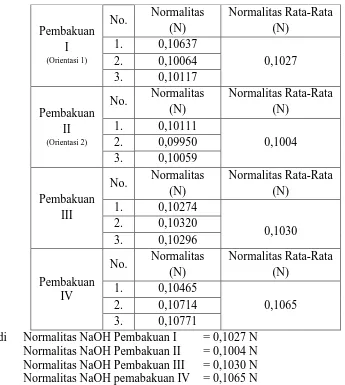
Normalitas rata-rata:
N̅ = N + N + N
Tabel 5.2 Data normalitas rata-rata NaOH
Pembakuan
I
(Orientasi 1)No.
Normalitas
(N)
Normalitas Rata-Rata
(N)
1.
0,10637
0,1027
2.
0,10064
3.
0,10117
Pembakuan
II
(Orientasi 2)No.
Normalitas
(N)
Normalitas Rata-Rata
(N)
1.
0,10111
0,1004
2.
0,09950
3.
0,10059
Pembakuan
III
No.
Normalitas
(N)
Normalitas Rata-Rata
(N)
1.
0,10274
0,1030
2.
0,10320
3.
0,10296
Pembakuan
IV
No.
Normalitas
(N)
Normalitas Rata-Rata
(N)
1.
0,10465
0,1065
2.
0,10714
3.
0,10771
Lampiran 6. Data hasil orientasi perhitungan bilangan asam
Rumus hitung bilangan asam (mg NaOH/g minyak):
Bilangan Asam =
ml × N × BM NaOH
G
Tabel 6.1 Data hasil orientasi pertama
Masa
N
NaOHyang digunakan yakni Normalitas NaOH Pembakuan I = 0,1027 N
Tabel 6.2Data hasil orientasi kedua
MasaLampiran 7. Data perhitungan bilangan asam
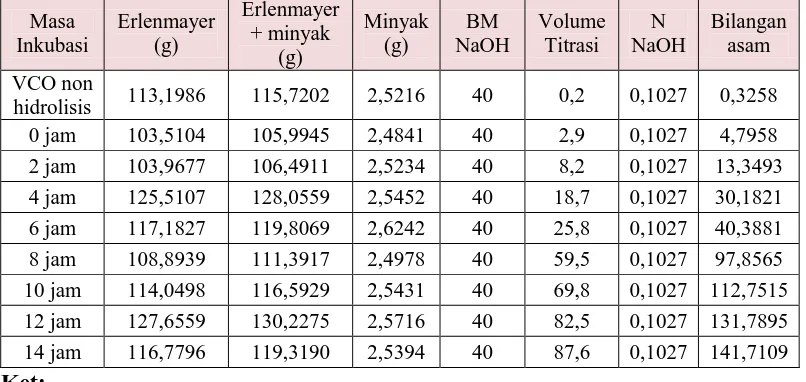
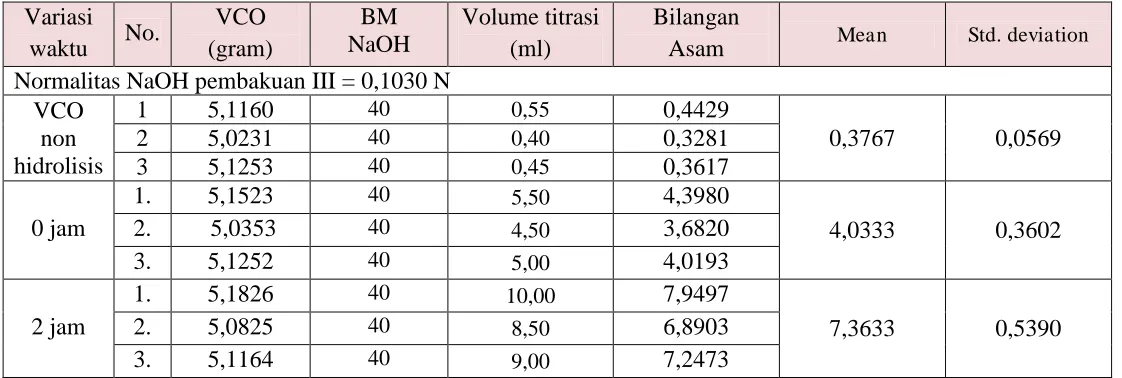
Tabel 7.1 Data perhitungan bilangan asam Virgin Coconut Oil
(VCO) non hidrolisis dan
Virgin Coconut Oil(VCO) hasil hidrolisis
enzimatis
Rumus hitung bilangan asam (mg NaOH/g minyak):
Bilangan Asam =
ml × N × BM NaOH
G
Keterangan:
ml
= volume titrasi
N
= normalitas NaOH
BM NaOH
= 40
G
= massa minyak yang diuji
Variasi
waktu
No.
VCO
(gram)
BM
NaOH
Volume titrasi
(ml)
Bilangan
Asam
Mean Std. deviationNormalitas NaOH pembakuan III = 0,1030 N
VCO
non
hidrolisis
1
5,1160
40 0,550,4429
0,3767
0,0569
2
5,0231
40 0,400,3281
3
5,1253
40 0,450,3617
0 jam
1.
5,1523
40 5,504,3980
4,0333
0,3602
2.
5,0353
40 4,503,6820
3.
5,1252
40 5,004,0193
2 jam
1.
5,1826
40 10,007,9497
7,3633
0,5390
2.
5,0825
40 8,506,8903
4 jam
1.
5,1362
40 28,0022,4602
20,8333
1,4202
2.
5,0979
40 25,0020,2044
3.
5,0876
40 24,5019,8404
6 jam
1.
5,1645
40 56,5045,0731
45,4833
1,7471
2.
5,0584
4054,00
43,9823
3.
5,1761
4059,55
47,3998
8 jam
1.
5,1434
40122,00
97,7252
95,9867
1,6129
2.
5,0338
40115,50
94,5329
3.
5,1225
40119,00
95,7111
10 jam
1.
5,0070
40154,00
126,7186
122,2767
4,4251
2.
5,1573
40147,55
117,8729
3.
5,1568
40153,00
122,2386
12 jam
1.
5,1395
40169,50
135,8770
133,4867
2,3280
2.
5,0980
40165,00
133,3464
3.
5,0862
40162,00
131,2257
14 jam
1.
5,0042
40171,50
141,1974
140,3167
0,7697
2.
5,1284
40174,00
139,7863
3.
5,1660
40175,50
139,9651
Normalitas NaOH pembakuan IV= 0,1065 N
16 jam
1.
5,1764
40171,15
140,8506
140,8667
1,2751
2.
5,0885
40169,80
142,1535
3.
5,0138
40164,30
139,5983
18 jam
1.
5,0678
40168,90
141,9776
142,1733
1,3405
2.
5,1263
40172,80
143,5983
Lampiran 8. Analisis statistik bilangan asam dari VCO dan hasil hidrolisis
enzimatisVCO
Uji Analisis Variansi (ANAVA)
Zona
Hambat
JK
DB
KT
F hitung
F tabel
Sig.
Perlakuan
Galat
Total
114377.302
74.221
114451.523
10
22
32
11437.730
3.374
3390.275
2.297
.000
Lampiran 9.Data hasil pengujian aktivitas antibakteri secara in-vitro
Tabel 9.1 Data hasil pengukuran zona hambat Virgin Coconut Oil
(VCO) hasil
hidrolisis enzimatis, VCO non-hidrolisis, Kloramfenikol dan Etanol
terhadap bakteri
Salmonella typhidan
Salmonella typhimuriumKontrol positif Konsentrasi Pengulangan (n=6)
Zona Hambat (mm)
S. typhi(1) S. typhimurium(2)
Etanol -
Mean ± SD 6,000±0,0000 6,000±0,0000
Kloramfenikol 30 μg/disc
1 19,3 9,7
Mean ± SD 7,583±0,2858 7,533±0,4274
4 12,9 12,9
5 12,0 13,6
6 12,7 12,8
Mean ± SD 12,250 ± 0,5244 12,983 ± 0,7026
1000 μl/ml
1 13,9 13,8
2 14,1 15,2
3 14,0 14,5
4 14,3 13,8
5 13,6 15,0
6 13,5 13,7
Mean ± SD 13,900 ± 0,3033 14,333 ± 0,6623
Tabel 9.2 Zona hambat Virgin Coconut Oil
(VCO) hasil hidrolisis enzimatis,
VCO non-hidrolisis, Kloramfenikol dan Etanol terhadap pertumbuhan
bakteri
Salmonella typhidan
Salmonella typhimuriumBakteri
Rata-Rata Zona Hambat (mm) Etanol Kloramfenikol
(30 μg/disc)
VCO non hidrolisis
Lampiran 10. Analisis statistik zona hambat VCO, hasil hidrolisis enzimatis
VCO, Kloramfenikol dan Etanol terhadap bakteri
Salmonella typhidan
Salmonella typhimuriumUji Analisis Variansi (ANAVA)
Zona Hambat SumberVariansi
JK DB KT F hitung F tabel Sig. S.typhi Perlakuan
Galat Total
774,903 11,453 786,357
7 40 47
110,700 0,286
386,614 2,249 0,000
S.typhimurium Perlakuan Galat Total
319,983 12,743 332,727
7 40 47
45,712 0,319
143,485 2,249 0,000
Lampiran 11. Hewan Percobaan
I.
Mencit dalam Keadaan Sehat
II.
Mencit yang Mengalami Diare
Keterangan : A = feses mencit dengan konsistensi berlendir/berair tidak
membentuk massa feses
B = bagian anus mencit tampak basah karena diare
A
Lampiran 12. Volume maksimum larutan sediaan uji yang dapat diberikan pada
hewan uji
Jenis hewan uji
Volume maksimum (ml) sesuai jalur pemberian
i.v.
i.m.
i.p.
s.c.
p.o.
Mencit (20-30 g)
0,5
0,05
1,0
0,5-1,0
1,0
Tikus (200 g)
1,0
0,1
2-5
2-5
5,0
Hamster (50 g)
-
0,1
1-2
2,5
2,5
Marmot (300 g)
-
0,25
2-5
5,0
10,0
Kelinci (2,5 kg)
5-10
0,5
10-20
5-10
20,0
Kucing (3 kg)
5-10
1,0
10-20
5-10
50,0
Anjing (5 kg)
10-20
5,0
20-50
10,0
100,0
Lampiran 13. Data berat badan mencit harian.
Kelompok Hari-0 Hari-1 Hari-2 Hari-3 Hari-4 Hari-5 Hari-6
CON 22,7 22,5 22,2 22,6 22,8 22,8 23,0
CON 21,3 21,6 21,4 21,8 21,6 21,7 21,9
CON 20,4 20,2 20,8 20,6 20,9 21,2 21,5
CON 20,7 20,6 20,9 21,0 21,2 21,5 21,6
CON 22,5 22,3 21,9 21,8 21,6 21,7 21,9
CON 20,6 20,6 20,8 21,1 21,3* mati mati
Rata-rata 21,4 21,3 21,3 21,5 21,6 21,8 22,0
SI 21,3 21,0 20,6 18,4 17,6 17,1 mati
SI 23,7 23,1 22,6 21,9 21,2 19,8 mati
SI 22,0 21,6 20,8 19,6 mati mati mati
SI 23,1 22,8 22,0 21,4 20,6 mati mati
SI 23,5 23,1 22,6 22,0 21,4 20,2 mati
SI 21,8 21,2 20,8 20,3 19,8* mati mati
Rata-rata 22,6 22,1 21,6 20,6 20,1 19.0 -
SI-Klor 22,4 22,0 21,5 21,1 19,6 18,8 18,4
SI-Klor 21,8 21,4 21,0 19,8 19,3 18,6 17,8
SI-Klor 20,5 20,2 19,8 19,4 19,0 18,7 18,2
SI-Klor 20,3 19,7 19,4 19,0 18,6 18,3 mati
SI-Klor 20,8 20,5 20,2 19,8 19,4 18,9 17,6
SI-Klor 20,6 20,4 20,0 19,7 19,3* mati mati
Rata-rata 21,1 20,7 20,3 19,8 19,2 18,7 18,0
SI-VCO 21,9 21,5 21,2 20,7 20,4 20,0 19,7
SI-VCO 21,2 21,0 20,8 20,5 20,2 19,9 19,5
SI-VCO 21,7 21,5 21,1 20,8 20,4 20,1 19,9
SI-VCO 21,9 21,5 21,2 21,0 20,6 20,3 20,1
SI-VCO 21,4 21,1 20,8 20,5 20,2 19,7 19,4
SI-VCO 20,6 20,3 20,1 19,6 19,4* mati mati
Rata-rata 21,5 21,2 20,9 20,5 20,2 20,0 19,7
SI-VCOH 22,3 21,8 21,3 20,8 20,2 20,0 19,7
SI-VCOH 22,4 22,0 21,6 21,1 20,8 20,6 20,2
SI-VCOH 23,4 23,1 22,6 21,8 21,4 20,4 20,0
SI-VCOH 22,0 21,6 21,4 20,9 20,5 19,7 19,5
SI-VCOH 22,8 22,5 22,3 21,8 21,4 21,1 20,8
SI-VCOH 23,8 23,6 23,0 22,4 22,1* mati mati
Rata-rata 22,8 22,4 22,0 21,5 21,0 20,4 20,0
Lampiran 14.Konsistensi Feses
Feses Mencit dengan berbagai konsistensi sebagai berikut:
a
b
c
d
Keterangan: a = konsistensi feses normal
b = konsistensi feses lembek
Lampiran15. Data jumlah koloni bakteri (CFU gram
-1) dalam feses mencit tiap kelompok
Kelompok Hari-0 Hari-1 Hari-2 Hari-3 Hari-4 Hari-5 Hari-6
CON 0 0 0 0 0 0 0
CON 0 0 0 0 0 0 0
CON 0 0 0 0 0 0 0
CON 0 0 0 0 0 0 0
CON 0 0 0 0 0 0 0
CON 0 0 0 0 0/* mati mati
SI 0 5,8 x 103 3,3 x 103 1,6 x 104 3,2 x 105 6,5 x 105 mati
SI 0 8,2 x 103 1,7 x 104 3,6 x 105 4,8 x 105 8,2 x 105 mati
SI 0 1,6 x 105 1,9 x 104 5,3 x 105 mati mati mati
SI 0 1,1 x 104 1,3 x 104 4,6 x 105 1,4 x 106 mati mati
SI 0 1,3 x 104 1,7 x 104 1,8 x 105 5,1 x 105 1,2 x 106 mati
SI 0 9,4 x 103 1,3 x 104 2,3 x 104 2,2 x 105/* mati mati
SI-Klor 0 4,7 x 103 3,7 x 103 1,4 x 104 1,8 x 104 2,1 x 104 1,7 x 105
SI-Klor 0 2,3 x 103 4,2 x 103 6,4 x 103 1,7 x 104 2,0 x 104 2,6 x 104
SI-Klor 0 3,4 x 103 6,2 x 103 5,2 x 103 7,8 x 103 1,7 x 104 2,4 x 104
SI-Klor 0 1,8 x 103 4,3 x 103 1,1 x 104 2,6 x 104 2,1 x 105 mati
SI-Klor 0 9,6 x 103 1,5 x 104 2,3 x 104 2,4 x 104 1,6 x 105 1,7 x 105
SI-Klor 0 4,0 x 103 6,8 x 103 1,8 x 104 2,0 x 104/* mati mati
SI-VCO 0 2,3 x 103 2,1 x 103 1,3 x 103 1,1 x 103 1,0 x 103 9,6 x 102
SI-VCO 0 5,1 x 103 3,2 x 103 1,8 x 103 1,5 x 103 1,3 x 103 1,1 x 103
SI-VCO 0 2,6 x 103 2,4 x 103 1,2 x 103 1,2 x 103 1,0 x 103 9,8 x 102
SI-VCO 0 1,7 x 104 6,5 x 103 4,9 x 103 4,1 x 103 3,5 x 103 2,9 x 103
SI-VCO 0 3,1 x 103 2,6 x 103 2,2 x 103 2,0 x 103 1,7 x 103 1,3 x 103
SI-VCO 0 6,6 x 103 5,0 x 103 4,2 x 103 3,1 x103/* mati mati
SI-VCOH 0 3,0 x 103 2,8 x 103 9,1 x 102 8,2 x 102 7,6 x 102 6,4 x 102
SI-VCOH 0 9,3 x 103 6,2 x 103 2,6 x 103 1,1 x 103 1,0 x 103 8,2 x 102
SI-VCOH 0 2,2 x 103 4,3 x 103 1,3 x 103 9,4 x 102 8,1 x 102 6,7 x 102
SI-VCOH 0 8,3 x 102 2,7 x 103 9,6 x 102 8,7 x 102 6,5 x 102 5,2 x 102
SI-VCOH 0 9,8 x 103 4,3 x 103 8,7 x 102 5,1 x 103 4,3 x 103 2,6 x 103
SI-VCOH 0 2,4 x 103 1,2 x 103 9,7 x 102 9,2 x 102/* mati mati
Lampiran 16. Data mentah jumlah koloni bakteri dalam feses mencit
Rumus perhitungan jumlah koloni bakteri dalam setiap cawan petri menggunakan
rumus sebagai berikut:
[ � − �
× �] + [ � − �
× �] + ⋯ + [ �6 − �
× �]
�
= ⋯ ���/
Jumlah keseluruhan koloni bakteri yang masuk dalam rumus antara 30-300
CFU/ml. Kurang dari 30 dan lebih dari 300 pertumbuhan koloni tidak dimasukkan
dalam rumus di atas.
Spesifikasi
Quality Controluntuk mengidentifikasi
S.typhimuriumdalam media
Lampiran 16. Data mentah jumlah koloni bakteri dalam feses mencit (lanjutan)
Kelompok Kontrol/Normal (KN)Hari ke-0
No. Pengenceran Jumlah Koloni
Kelompok Kontrol/Normal (KN) Hari ke-1
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Kontrol/Normal (KN) Hari ke-2
No. Pengenceran Jumlah Koloni
Kelompok Kontrol/Normal (KN) Hari ke-3
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Kontrol/Normal (KN) Hari ke-4
No. Pengenceran Jumlah Koloni
Kelompok Kontrol/Normal (KN) Hari ke-5
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Kontrol/Normal (KN) Hari ke-6
No. Pengenceran Jumlah Koloni
Kelompok Salmonella Infected (SI) Hari ke-0
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Salmonella Infected (SI) Hari ke-1
No. Pengenceran Jumlah Koloni
Kelompok Salmonella Infected (SI) Hari ke-2
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Salmonella Infected (SI) Hari ke-3
No. Pengenceran Jumlah Koloni
Kelompok Salmonella Infected (SI) Hari ke-4
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Salmonella Infected (SI) Hari ke-5
No. Pengenceran Jumlah Koloni
Kelompok Salmonella Infected (SI) Hari ke-6
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Salmonella Infected-Kloramfenikol(SI-Klor)
Hari ke-0
No. Pengenceran Jumlah Koloni
Kelompok Salmonella Infected-Kloramfenikol(SI-Klor)
Hari ke-1
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Salmonella Infected-Kloramfenikol(SI-Klor)
Hari ke-2
No. Pengenceran Jumlah Koloni
Kelompok Salmonella Infected-Kloramfenikol(SI-Klor)
Hari ke-3
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Salmonella Infected-Kloramfenikol(SI-Klor)
Hari ke-4
No. Pengenceran Jumlah Koloni
Kelompok Salmonella Infected-Kloramfenikol(SI-Klor)
Hari ke-5
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Salmonella Infected-Kloramfenikol(SI-Klor)
Hari ke-6
No. Pengenceran Jumlah Koloni
Kelompok Salmonella Infected–VCO (SI-VCO)
Hari ke-0
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Salmonella Infected–VCO (SI-VCO)
Hari ke-1
No. Pengenceran Jumlah Koloni
Kelompok Salmonella Infected–VCO (SI-VCO)
Hari ke-2
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Salmonella Infected–VCO (SI-VCO)
Hari ke-3
No. Pengenceran Jumlah Koloni
Kelompok Salmonella Infected–VCO (SI-VCO)
Hari ke-4
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Salmonella Infected–VCO (SI-VCO)
Hari ke-5
No. Pengenceran Jumlah Koloni
Kelompok Salmonella Infected–VCO (SI-VCO)
Hari ke-6
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Salmonella Infected– VCOH(SI-VCOH)
Hari ke-0
No. Pengenceran Jumlah Koloni
Kelompok Salmonella Infected– VCOH(SI-VCOH)
Hari ke-1
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Salmonella Infected– VCOH(SI-VCOH)
Hari ke-2
No. Pengenceran Jumlah Koloni
Kelompok Salmonella Infected– VCOH(SI-VCOH)
Hari ke-3
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Salmonella Infected– VCOH(SI-VCOH)
Hari ke-4
No. Pengenceran Jumlah Koloni
Kelompok Salmonella Infected– VCOH(SI-VCOH)
Hari ke-5
Lampiran 16. Data Mentah Jumlah Koloni Bakteri dalam Feses Mencit
(Lanjutan)
Kelompok Salmonella Infected– VCOH(SI-VCOH)
Hari ke-6
No. Pengenceran Jumlah Koloni
ALT (CFU/ml)
1
10-1 64
6,4x102 10-2 15
10-4 1 10-6 0
2
10-1 82
8,2x102 10-2 21
10-4 2 10-6 0
3
10-1 67
6,7x102 10-2 18
10-4 3 10-6 0
4
10-1 52
5,2x102 10-2 13
10-4 1 10-6 0
5
10-1 97
2,6x103 10-2 42
10-4 3 10-6 0
6
10-1 -
mati 10-2 -
Lampiran 17. Jumlah koloni bakteri dalam feses mencit pada cawan petri secara
in-vivoGambar 1. Tidak ada koloni S.typhimurium
yang tumbuh dalam feses mencit
(jumlah koloni=0)
Lampiran 17. Jumlah koloni bakteri dalam feses mencit pada cawan petri secara
in-vivo(lanjutan)
Lampiran 19.Orientasi dosis kloramfenikol untuk mencit
Tabel. Jumlah koloni bakteri dalam feses mencit yang diberi 3 variasi konsentrasi
kloramfenikol
Kelompok Hari-0 Hari-1 Hari-2 Hari-3 Hari-4 Hari-5 Hari-6 SI-Klor
(300 μg/ml) 0 2,7 x 10
3 3,2 x 103 3,4 x 103 4,2 x 104 3,6 x 104 3,8 x 104
SI-Klor
(300 μg/ml) 0 3,7 x 10
3 3,4 x 103 1,8 x 104 2,3 x 104 2,0 x 104 1,2 x 105
SI-Klor
(500 μg/ml) 0 3,4 x 10
3 4,1 x 103 4,8 x 103 5,8 x 103 1,7 x 104 2,4 x 104
SI-Klor
(500 μg/ml) 0 2,8 x 10
3 4,5 x 103 1,1 x 104 2,0 x 104 2,4 x 105 2,8 x 105
SI-Klor
(1000 μg/ml) 0 5,6 x 10
3 1,5 x 104 2,3 x 104 2,4 x 104 1,6 x 105 1,7 x 105
SI-Klor
(1000 μg/ml) 0 4,0 x 10
3 6,8 x 103 1,8 x 104 2,2 x 104 2,7 x 104 1,4 x 105
Lampiran 20.Jurnal Publikasi International Journal PharmTech Research
Judul: Paper NO.= 75/M14 : Letter of Acceptance, Charges to be
paid ,Undertaking to be signed and Information on ELSEVIER
REPORT-RANKING…..
Dari: Journal sphinx (submitpaper@rediffmail.com)
Kepada: elysa_hong@yahoo.co.id;
Cc: submitpaper@rediffmail.com;
Tanggal: Minggu, 16 Februari 2014 21:27