LAMPIRAN
LAMPIRAN 1. DATA PERCOBAAN
L.1.1 Data Percobaan Kadar Gula Reduksi Sebelum Inversi
Tabel L.1 Data Percobaan Kadar Gula Reduksi Sebelum Inversi
Waktu Hidrolisis (Menit)
Konsentrai HCl
0,5 M 0,75 M 1 M
30 0,6120 % 1,4688 % 5,0490 %
45 2,2185 % 4,7838 % 2,9197 %
60 1,1016 % 0,7344 % 3,3666 %
L.1.2 Data Percobaan Kadar Gula Reduksi Setelah Inversi
Tabel L.2 Data Percobaan Kadar Gula Reduksi Setelah Inversi
Waktu Hidrolisis (Menit)
Konsentrai HCl
0,5 M 0,75 M 1 M
30 2,7645 % 2,5507 % 9,8667 %
45 4,6170 % 8,4046 % 6,3840 %
60 4,1895 % 4,6170 % 9,0202 %
L.1.3 Data Percobaan % Kadar Glukosa
Tabel L.3 Data Percobaan % Kadar Glukosa
Waktu Hidrolisis (Menit)
Konsentrai HCl
0,5 M 0,75 M 1 M
30 2,0448 % 1,0278 % 4,5768 %
45 2,2785 % 3,4398 % 3,2910 %
L.1.4 Data Percobaan % Kadar Air Sirup Glukosa
Tabel L.4 Data Percobaan % Kadar Air Sirup Glukosa
Waktu Hidrolisis (Menit)
Konsentrai HCl
0,5 M 0,75 M 1 M
30 67,870 % 62,125 % 64,765 %
45 64,685 % 63,490 % 53,440 %
60 66,365 % 59,935 % 51,215 %
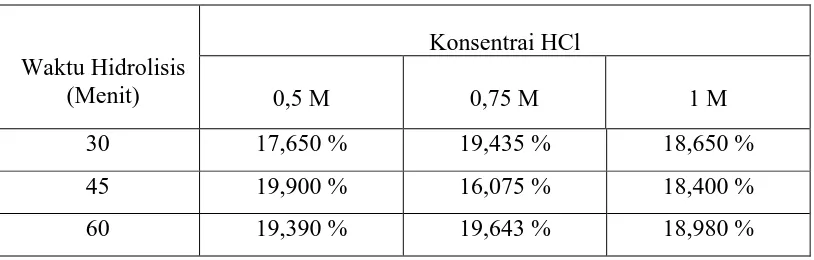
L.1.5 Data Percobaan % Kadar Abu Sirup Glukosa
Tabel L.5 Data Percobaan % Kadar Abu Sirup Glukosa
Waktu Hidrolisis (Menit)
Konsentrai HCl
0,5 M 0,75 M 1 M
30 17,650 % 19,435 % 18,650 %
45 19,900 % 16,075 % 18,400 %
LAMPIRAN 2. CONTOH PERHITUNGAN
L.2.1 Contoh Perhitungan Bahan Kimia Yang Digunakan L.2.1.1 Pembuatan larutan KI 20%
KI yang tersedia KI padatan maka: Larutan KI 20% sebanyak 100 ml gr = m x BM x ml
= 1 mol/l x 166 gr/mol x 0,100 = 16,6 gr
Larutan KI 20% = 20% X 100 ml
= 20 ml ( lalu diencerkan sampai 100 ml )
L.2.1.2 Larutan H2SO4 25%
Larutan H2SO4 yang tersedia yaitu H2SO4 98%, maka:
Larutan H2SO4 25% sebanyak 100 ml
V1 . % = V2 . %
100 ml . 25 % = V2 . 98%
V2 = 25,51 ml ( lalu diencerkan sampai 100 ml )
L.2.1.3 Larutan Na2SO3 0,1 N
Larutan Na2SO3 0,1 N dalam 100 ml
gr = N . BE . V
= 0,1 N . 248,21 gr/mol . 0,1 l = 2,4821 gr
L.2.1.4 Larutan HCl 3%
Larutan HCl 3% dalam 500 ml V1 . % = V2 . %
500 ml . 3 % = V2 . 37%
V2 = 40,54 ml
L.2.1.5 Larutan NaOH 30%
= 1 mol/l . 0,10 l .40 gr/mol = 4 gr
NaOH 30% = 30% x 100 = 30 ml ( diencerkan sampai 100 ml )
L.2.1.6 Larutan HCl 1 M
Larutan HCl yang tersedia adalah HCl 37%, maka perlu dihitung konsentrasi HCl 37% agar dapat dibuat larutan 1 M, maka:
M
Untuk membuat larutan HCl 1 M: M1 . V1 = M2 . V2
Jadi untuk membuat larutan HCl 1 M, 10 ml HCl 37% ditambah 110,4 ml aquadest.
L.2.1.6 Larutan Indikator Amilum 5%
Perhitungan :
% b/v = gr/v x 100% 5 % = gr/100ml x 100% gr = 5 gram
Pembuatan :
L.2.2 Contoh Perhitungan Analisa Kadar Glukosa
Volume Na2SO3 blanko = 93 ml
Volume Na2SO3 sebelum inversi = 92 ml
Volume Na2SO3 setelah inverse = 89 ml
Pengenceran sebelum inversi = 25,5 Pengenceran setelah inverse = 28,5
Kadar gula sebelum inversi = blanko – sebelum inversi = 1
Kadar gula setelah inverse = blanko – setelah inversi = 4
Untuk kadar gula sebelum inverse dari tabel diperoleh konversi (X) = 2,4 Untuk kadar gula sesudah inverse dari tabel diperoleh konversi (Y) = 4,7
inversi x faktor konversi
= (2,7645 – 0,6120 ) x 95%
= 2,0448 %
L.2.3 Contoh Perhitungan Kadar Air Arang Sirup Glukosa
100%
L.2.4 Contoh Perhitungan Kadar Abu Arang Sirup Glukosa
LAMPIRAN 3. FOTO PERCOBAAN L.3.1 Biji Durian
Gambar L.1 Biji Durian
L.3.2 Biji Durian Yang Telah Dikeringkan
Gambar L.2 Biji Durian Yang Telah Dikeringkan
L.3.3 Tepung Biji Durian
L.3.4 Rangkaian Alat Proses Hidrolisis
Gambar L.4 Rangkaian Peralatan Proses Hidrolisis
L.3.5 Bahan hasil Proses Hidrolisis
L.3.6 Sirup Glukosa Hasil Hidrolisis
Gambar L.6 Sirup Glukosa Hasil Hidrolisis
L.3.7 Analisis Kadar Glukosa
Gambar L.8 Analisis Glukosa Setelah Titrasi
L.3.8 Analisis Kadar Air dan Kadar Abu Sirup Glukosa