3 METODE
3.1 Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan September 2011 sampai April 2012, bertempat di laboratorium Karakteristik Bahan Baku Hasil Perikanan IPB untuk preparasi bahan baku, laboratorium Biokimia Hasil Perairan untuk analisis proksimat, laboratorium Mikrobiologi Hasil Perairan IPB untuk analisis total mikroba, laboratorium Pilot Plan Pusat Antar Universitas IPB untuk spray drying, laboratorium Terpadu IPB untuk analisis asam lemak, dan laboratorium organoleptik Departemen THP IPB untuk pengujian organoleptik.
3.2 Bahan dan Alat
Bahan baku lintah laut (Discodoris sp.) yang digunakan dalam penelitian ini diperoleh dari Pantai Kejawanan, Cirebon, Jawa Barat. Bahan-bahan tambahan untuk formulasi meliputi jahe merah, kacang kedelai lokal, carboxyl methyl cellulose (CMC), gula pasir dan maltodekstrin. Bahan yang digunakan untuk analisis proksimat meliputi akuades, HCl 0,1 N; NaOH 40%, katalis selenium, H2SO4, H3BO3 2%, kertas saring, kapas bebas lemak, pelarut heksana, bromcresol green 0,1%, dan methyl red 0,1%; untuk analisis mikrobiologi, yaitu plate count agar (PCA), potato dextrose agar (PDA), dan asam tartarat 10%. Bahan-bahan analisis asam lemak berupa NaOH 0,5 N dalam metanol, BF3, NaCl jenuh, n-heksana, dan Na2SO4 anhidrat. Standar asam lemak yang digunakan adalah merk supelco 37 asam lemak FAME (asam lemak metil ester).
Alat-alat yang digunakan untuk preparasi bahan baku antara lain meja preparasi, pisau, ember, dan timbangan digital. Alat-alat yang digunakan untuk analisis proksimat antara lain timbangan digital, gegep, cawan porselen, oven, desikator, tanur, kompor, bulb, pipet, tabung reaksi, erlenmeyer, tabung Kjeldahl, tabung soxhlet, labu lemak dan buret. Alat yang digunakan untuk analisis asam lemak antara lain homogenizer, evaporator (Heidolph WB 2000), waterbath (Buchi waterbath B-480), erlenmeyer (ekstraksi asam lemak), corong pisah dan botol vial (metilasi), perangkat kromatografi gas Shimadzu GC 2010, dan alat-alat uji organoleptik.
3.3 Prosedur Penelitian
Penelitian ini terdiri atas tiga tahap, yaitu tahap pengambilan dan preparasi sampel, tahap formulasi minuman fungsional, dan tahap pengujian daya simpan produk. Tahap formulasi diawali dengan percobaan trial and error untuk mengetahui batas penerimaan dari segi organoleptik. Pada tahap ini juga dilakukan pengujian pendahuluan terhadap kandungan asam lemak serta pencampuran antar dua bahan dan keseluruhan bahan baku untuk melihat efek sinergis/antagonis dari asam lemak.
3.3.1 Tahap pengambilan dan preparasi sampel
Bahan-bahan yang digunakan di dalam formulasi adalah lintah laut, jahe merah, dan kedelai. Sampel lintah laut diambil dari perairan Cirebon dalam keadaan hidup kemudian dimatikan dengan cara menyayat bagian perut lintah laut dengan pisau. Lintah laut dibuang isi perutnya kemudian dicuci bersih, selanjutnya dikemas dalam plastik dan diangkut ke laboratorium menggunakan cool box yang ditambah es dengan perbandingan 2:1 (es:lintah laut). Preparasi lintah laut dapat dilihat pada Lampiran 1. Jahe merah segar dicuci dengan air dan dikupas kulitnya sebelum digunakan. Penambahan jahe dimaksudkan untuk menghilangkan bau amis yang berasal dari lintah. Kedelai dicuci dan direndam dengan air selama 12 jam sebelum digunakan. Fungsi penambahan kedelai dimaksudkan untuk memberikan efek warna dan sebagai bahan emulsifier pada minuman fungsional tersebut. Selanjutnya masing-masing sampel diblender dengan penambahan air 1:1 (b/v), lalu disaring dengan menggunakan kain blacu untuk mendapatkan ekstraknya, kemudian masing-masing ekstrak lintah laut, jahe merah dan kedelai dimasak dengan suhu 90 oC selama 10 menit sebagai sterilisasi bahan. Masing-masing ekstrak dikemas dalam wadah tertutup dan disimpan dalam lemari pendingin hingga digunakan. Sebanyak 450 gram lintah laut menghasilkan ekstrak lintah laut sebesar 600 ml, dalam 820 gram jahe merah menghasilkan ekstrak jahe merah sebesar 1200 ml, dan pada 500 gram kedelai menghasilkan ekstrak kedelai sebesar 1000 ml. Preparasi bahan baku dijelaskan pada Gambar 6.
Analisis yang dilakukan pada tahap ini yaitu: (1) analisis proksimat terhadap masing-masing bahan kering meliputi uji kadar air, kadar abu, kadar
lemak, kadar karbohidrat, kadar serat, dan kadar protein (AOAC 2005), dan (2) analisis asam lemak (AOAC 1999).
Gambar 6 Preparasi bahan baku.
Pemasakan dengan suhu 60 oC
selama 10 menit Pemisahan daging dan jeroan Pencucian daging dengan air Pemblenderan lintah:air (1:1)
Penyaringan dengan kain blacu
Ekstrak lintah laut
Analisis proksimat Analisis asam lemak
Omega-3 Lintah laut
3.3.2 Tahap formulasi minuman serbuk fungsional
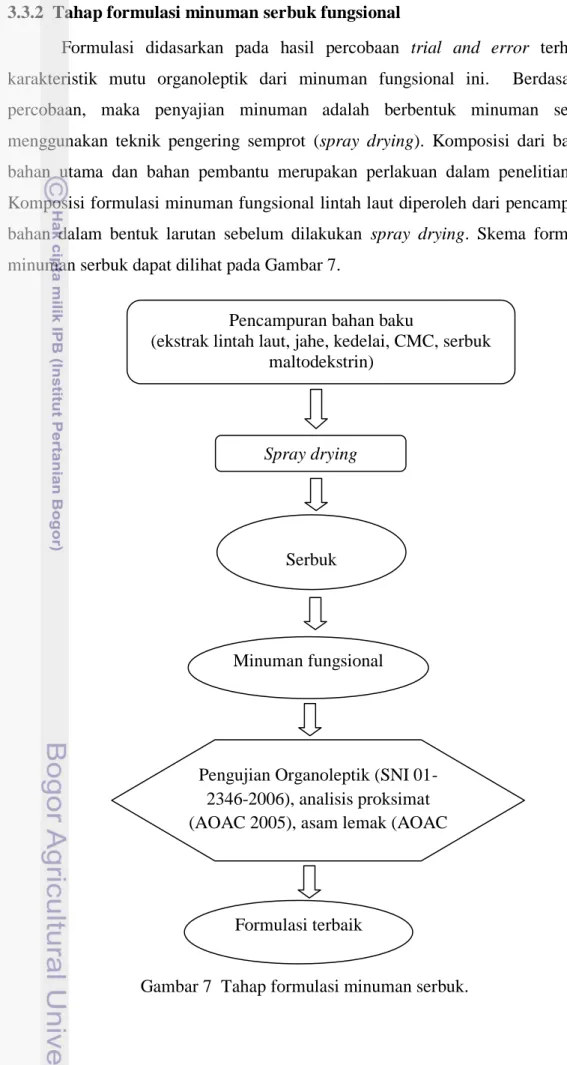
Formulasi didasarkan pada hasil percobaan trial and error terhadap karakteristik mutu organoleptik dari minuman fungsional ini. Berdasarkan percobaan, maka penyajian minuman adalah berbentuk minuman serbuk menggunakan teknik pengering semprot (spray drying). Komposisi dari bahan-bahan utama dan bahan-bahan pembantu merupakan perlakuan dalam penelitian ini. Komposisi formulasi minuman fungsional lintah laut diperoleh dari pencampuran bahan dalam bentuk larutan sebelum dilakukan spray drying. Skema formulasi minuman serbuk dapat dilihat pada Gambar 7.
Gambar 7 Tahap formulasi minuman serbuk. Spray drying
Pengujian Organoleptik (SNI 01-2346-2006), analisis proksimat (AOAC 2005), asam lemak (AOAC
1999)
Formulasi terbaik Serbuk
Minuman fungsional Pencampuran bahan baku
(ekstrak lintah laut, jahe, kedelai, CMC, serbuk maltodekstrin)
Adapun formulasi yang dilakukan sebanyak tiga perlakuan seperti yang terlihat pada Tabel 3.
Tabel 3 Formulasi minuman fungsional lintah laut Formula
Bahan utama (%) Bahan-bahan tambahan (%) Lintah laut
(Discodoris sp) Jahe Kacang kedelai
A1 20 35 45
A2 25 35 40
A3 30 35 35
Bahan-bahan utama dan tambahan yang digunakan dalam bentuk ekstrak kemudian dicampurkan berdasarkan ketiga bentuk formulasi dan di spray drying dengan menambahkan bahan pengisi berupa maltodekstrin sebanyak 10% dan CMC sebanyak 10%. Tujuan penambahan bahan pengisi agar kandungan gizi dari bahan-bahan tambahan dan bahan baku tidak rusak pada saat dikeringkan dengan pengering semprot. Selain itu, ditambahkan gula pasir (1:1) dari hasil spray drying sebagai perasa manis pada minuman serbuk fungsional. Hasil spray drying dari 500 ml larutan minuman menghasilkan 105,20 gram serbuk minuman. Penggunaan spray drying diharapkan untuk mendapatkan hasil minuman serbuk yang tidak meninggalkan ampas. Serbuk minuman fungsional tersebut kemudian dianalisis komposisi kimia, organoleptik, dan asam lemak. Formulasi minuman fungsional lintah laut dapat dilihat pada Lampiran 2.
3.3.3 Tahap pengujian stabilitas terhadap masa simpan produk
Pada tahap ini produk yang memiliki asam lemak tertinggi di antara perlakuan yang diterima secara organoleptik, dikemas menggunakan kemasan alumunium foil, dilanjutkan dengan pengujian stabilitas produk terhadap waktu. Pengujian masa simpan dilakukan dengan percepatan waktu atau model akselerasi menggunakan metode Arrhenius. Selama masa penyimpanan, produk disimpan pada tiga kondisi suhu yang berbeda, yaitu 30 oC, 35 oC, dan 45 oC. Pengamatan dilakukan setiap 7 hari sekali selama 35 hari.
Uji stabilitas yang dilakukan pada setiap pengamatan meliputi: (1) uji asam lemak dari formula terpilih, (2) pH, (3) uji total mikroba/kapang, dan (4)
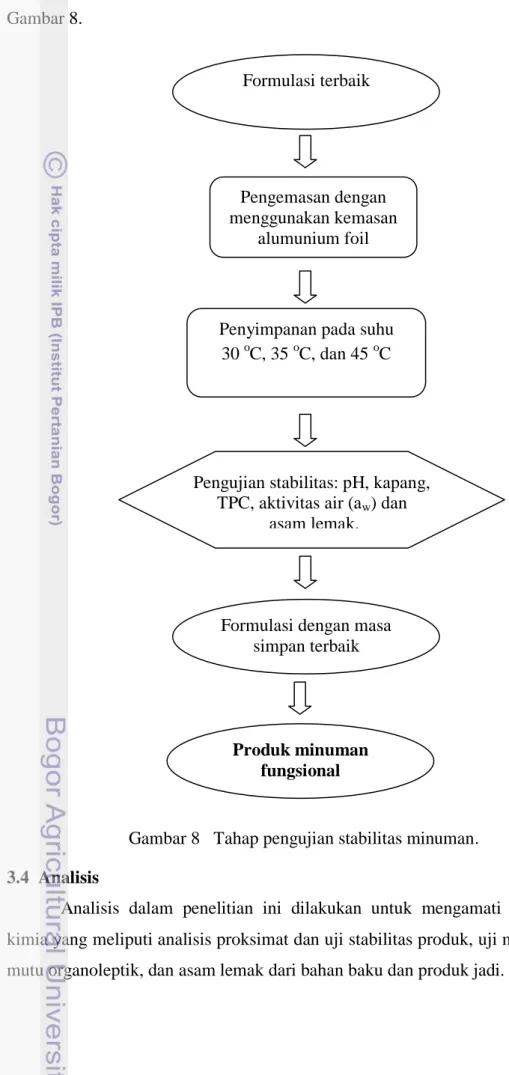
aktivitas air (aw). Skema tahap pengujian stabilitas minuman dapat dilihat pada Gambar 8.
Gambar 8 Tahap pengujian stabilitas minuman. 3.4 Analisis
Analisis dalam penelitian ini dilakukan untuk mengamati karakteristik kimia yang meliputi analisis proksimat dan uji stabilitas produk, uji mikrobiologi, mutu organoleptik, dan asam lemak dari bahan baku dan produk jadi.
Formulasi terbaik
Penyimpanan pada suhu 30 oC, 35 oC, dan 45 oC
Pengujian stabilitas: pH, kapang, TPC, aktivitas air (aw) dan
asam lemak.
Formulasi dengan masa simpan terbaik Produk minuman fungsional Pengemasan dengan menggunakan kemasan alumunium foil
3.4.1 Analisis proksimat (AOAC 2005)
Analisis proksimat yang dilakukan meliputi uji kadar air dan abu dengan metode oven, uji kadar lemak menggunakan metode sokhlet, dan uji kadar protein menggunakan metode kjeldahl.
(1) Analisis kadar air (AOAC 2005)
Penentuan kadar air didasarkan pada berat contoh sebelum dan sesudah dikeringkan. Cawan kosong dikeringkan di dalam oven selama 1 jam pada suhu 105 oC, lalu dimasukkan ke dalam desikator selama 15 menit kemudian ditimbang. Sampel sebanyak 1 gram dimasukkan ke dalam cawan lalu dikeringkan di dalam oven pada suhu 105 oC sampai beratnya konstan (kurang lebih selama 6 jam) dan kemudian cawan dimasukkan ke dalam desikator selama 30 menit selanjutnya ditimbang kembali. Kadar air ditentukan dengan rumus: Kadar air = Bobot sampel akhir (B) x 100
Bobot sampel awal (A) (2) Analisis kadar abu (AOAC 2005)
Cawan dibersihkan dan dikeringkan di dalam oven selama 30 menit dengan suhu 105 oC, lalu dimasukkan dalam desikator kemudian ditimbang. Sampel sebanyak 5 gram ditimbang lalu dimasukkan ke dalam cawan dan kemudian dibakar di atas kompor listrik sampai tidak berasap lagi dan selanjutnya dimasukkan ke dalam tanur pengabuan dengan suhu 600 oC selama 7 jam. Cawan dimasukkan di dalam desikator lalu ditimbang. Kadar abu ditentukan dengan rumus:
Kadar abu = Bobot abu x 100 Bobot sampel kering (3) Analisis kadar lemak kasar (AOAC 2005)
Daging lintah seberat 2 gram (W1) disebar di atas kapas yang beralaskan kertas saring dan digulung membentuk thimble. Sampel yang telah dibungkus dimasukkan ke dalam labu lemak yang sudah ditimbang berat tetapnya (W2) dan disambungkan dengan tabung Soxhlet. Selongsong lemak dimasukkan ke dalam ruang ekstraktor tabung Soxhlet dan disiram dengan pelarut lemak (n-heksana).
Kemudian dilakukan refluks selama 6 jam. Pelarut lemak yang ada dalam labu lemak didestilasi hingga semua pelarut lemak menguap. Pada saat destilasi pelarut akan tertampung di ruang ekstraktor, pelarut dikeluarkan sehingga tidak kembali ke dalam labu lemak, selanjutnya labu lemak dikeringkan dalam oven pada suhu 105 oC, setelah itu labu dimasukkan dalam desikator sampai beratnya konstan (W3). Kadar lemak ditentukan dengan rumus:
% Kadar lemak = W3 – W2 x 100 % W1
Keterangan :
W1 = Berat sampel lintah (gram)
W2 = Berat labu lemak tanpa lemak (gram) W3 = Berat labu lemak dengan lemak (gram) (4) Analisis kadar protein (AOAC 2005)
Analisis kadar protein dilakukan dengan metode kjeldahl. Prinsipnya adalah oksidasi bahan-bahan berkarbon dan konversi nitrogen menjadi amonia oleh asam sulfat, selanjutnya amonia bereaksi dengan kelebihan asam membentuk amonium sulfat. Amonium sulfat yang terbentuk diuraikan dan larutan dijadikan basa dengan NaOH. Amonia yang diuapkan akan diikat dengan asam borat. Nitrogen yang terkandung dalam larutan ditentukan jumlahnya dengan titrasi menggunakan larutan baku asam.
Sebanyak 5 gram sampel kering ditempatkan dalam labu Kjeldahl 100 ml dan ditambahkan 0,25 gram selenium dan 3 ml H2SO4 pekat. Selanjutnya dilakukan destruksi (pemanasan dalam keadaan mendidih) selama 1 jam sampai larutan jernih. Setelah dingin ditambahkan 50 ml akuades dan 20 ml NaOH 40% lalu didestilasi. Hasil destilasi ditampung dalam labu Erlenmeyer yang berisi campuran 10 ml H3BO3 2% dan 2 tetes indikator Brom Cresol Green-Methyl Red berwarna merah muda. Setelah volume hasil tampungan (destilat) menjadi 10 ml dan berwarna hijau kebiruan, destilasi dihentikan, kemudian destilat dititrasi dengan HCl 0,1 N sampai berwarna merah muda. Perlakuan yang sama dilakukan juga terhadap blanko.Kadar protein dihitung dengan rumus:
% Kadar nitrogen = (B – A) x C x 14,007 x 100 x 100 % D
% Kadar protein = % kadar nitrogen x FK Keterangan: A = volume HCl untuk titrasi blanko
B = volume HCl untuk titasi sampel (ml)
C = normalitas HCl yang digunakan (0,02374 N) D = bobot sampel (mg)
FK = faktor konversi (6,25 untuk produk perikanan)
3.4.2 Analisis logam berat Pb, Cd, As, Hg, Cu (BPOM 2009 dan SNI 2009) Spektrofotometer serapan atom (AAS) adalah salah satu teknik analisis unsur yang dapat dilakukan dengan cepat serta mempunyai tingkat ketelitian yang sangat tinggi. Perangkat AAS ini telah terkomputerisasi sehingga seluruh parameter alat, yaitu kuat arus lampu katoda, slit, panjang gelombang, standardisasi, dan sebagainya dapat dilakukan langsung menggunakan program komputer secara otomatis.
Prinsip dasar analisis AAS adalah jika suatu contoh diaspirasikan ke dalam suatu sistem pembakaran, maka unsur-unsur yang ada pada senyawaan akan dikonversi menjadi atom. Apabila pada kondisi ini diberikan suatu energi radiasi yang sesuai, maka energi tersebut akan diserap oleh atom. Besar kecilnya energi yang diserap akan berbanding lurus dengan konsentrasi unsur yang dianalisis.
Analisis dilakukan menggunakan 1 gram contoh, kemudian dimasukkan ke dalam labu destruksi 100 ml, dengan ditambahkan 15 ml HNO3 pekat dan 5 ml HClO4, kemudian didiamkan 24 jam. Selanjutnya sampel didestruksi hingga jernih, didinginkan, dan ditambahkan 10-20 ml air bebas ion, dilakukan pemanasan ±10 menit, diangkat, dan dinginkan. Larutan tersebut dipindahkan ke dalam labu takar 100 ml (labu dekstruksi dibilas dengan air bebas ion dan dimasukkan ke dalam labu takar). Larutan ditambahkan air sampai batas tanda tera. Kemudian dikocok dan disaring dengan kertas saring Whatman no.4. Sampel dipreparasi dan dianalisis sesuai dengan pengujian logam berat (Pb, Cd, As, Hg, dan Cu) pada analisis air (APHA 3110 untuk logam Cd, Pb, dan Cu; metode 3114 untuk As; dan metode 3112 untuk Hg). Panjang gelombang logam Cd yaitu 228,8 nm, logam Pb 283,3 nm, dan logam Hg 253,7 nm.
Kadar logam (ppm) = Konsentrasi logam dari kurva rendah (µg/ml) x V pelarutan
Bobot sampel
3.4.3 Analisis asam lemak (AOAC 1999)
Metode analisis yang digunakan memiliki prinsip mengubah asam lemak menjadi turunannya, yaitu metil ester sehingga dapat terdeteksi oleh alat kromatografi. Gas chromatography (GC) memiliki prinsip kerja pemisahan antara gas dan lapisan tipis cairan berdasarkan perbedaan jenis bahan (Fardiaz 1989). Analisis dengan kromatografi gas didasarkan pada partisi komponen-komponen dari suatu cairan di antara fase gerak berupa gas dan fase diam berupa zat padat atau cairan yang tidak mudah menguap yang melekat pada bahan pendukung inert. Komponen-komponen yang dipisahkan harus mudah menguap pada suhu pemisahan yang dilakukan sehingga suhu operasi biasanya lebih tinggi dari suhu kamar dan biasanya dilakukan derivatisasi untuk contoh yang sulit menguap.
Dalam hal analisis asam lemak, mula-mula sampel lemak atau minyak dihidrolisis menjadi asam lemak, kemudian ditransformasi menjadi bentuk esternya yang bersifat lebih mudah menguap. Transformasi dilakukan dengan cara metilasi sehingga diperoleh metil ester asam lemak (FAME). Selanjutnya FAME dianalisis dengan alat kromatografi gas. Alat kromatografi gas yang digunakan adalah kromatografi gas Shimadzu GC 2010+.
Hasil analisis akan tertekan dalam suatu lembaran yang terhubung dengan rekorder dan ditunjukkan melalui beberapa puncak pada waktu retensi tertentu sesuai dengan karakter masing-masing asam lemak. Identifikasi tiap komponen asam lemak dilakukan dengan membandingkan waktu retensinya dengan waktu retensi standar pada kondisi analisis yang sama. Waktu retensi dihitung pada kertas rekorder sebagai jarak dari garis pada saat muncul pelarut sampai ke tengah puncak komponen yang dipertimbangkan. Luas puncak dari masing-masing komponen adalah berbanding lurus dengan jumlah komponen tersebut dalam contoh. Analisis asam lemak dilakukan melalui tahap ekstraksi, metilasi, injeksi, dan pembacaan sampel dengan kromatogram.
(a) Ekstraksi
Tahap pertama dilakukan ekstraksi soxhlet untuk memperoleh lemak. Sampel ditimbang sebanyak 20-30 mg lemak untuk dilanjutkan ke tahap metilasi. (b) Pembentukan metil ester (metilasi)
Tahap metilasi dimaksudkan untuk membentuk senyawa turunan dari asam lemak menjadi metil esternya. Asam-asam lemak diubah menjadi ester-ester metil atau alkil yang lainnya sebelum disuntikkan ke dalam kromatografi gas (Fardiaz 1989).
Metilasi dilakukan dengan merefluks lemak di atas penangas air dengan menambahkan 1 ml NaOH 0,5 N dalam metanol dan dipanaskan selama 20 menit pada suhu 80 °C lalu diangkat dan dibiarkan dingin. Kemudian ditambahkan 5 ml bourtiflourid-metanol pada sampel dan dipanaskan pada suhu 80 °C selama 20 menit pada waterbath, diangkat dan dibiarkan dingin. Selanjutnya ditambahkan 2 ml BF3 20% dan dipanaskan lagi selama 20 menit. Kemudian didinginkan, dan ditambahkan 2 ml NaCl jenuh dan 1 ml isooctane dikocok dengan baik. Lapisan isooktan bagian atas larutan dipindahkan dengan bantuan pipet tetes ke dalam tabung reaksi yang berisi 0,1 gram Na2SO4 anhidrat, didiamkan selama 15 menit. Larutan disaring dengan mikrofilter untuk memisahkan fase cairnya sebelum diinjeksikan ke dalam kromatografi gas. Sebanyak 1 μl sampel diinjeksikan ke dalam Gas Chromatography secara manual. Asam lemak yang ada dalam metil ester akan diidentifikasi oleh Flame Ionization Detector (FID) atau detektor ionisasi nyala dan respon yang ada akan tercatat melalui kromatogram (peak). (c) Identifikasi asam lemak
Identifikasi asam lemak dilakukan dengan menginjeksikan metil ester pada alat kromatografi gas GC Shimadzu 2010+. Adapun kondisi alat saat analisis adalah sebagai berikut: Kolom: kolom kapiler Cyanopropil methyl sil (merek Quadrex). Dimensi Kolom dengan panjang 60 cm, diameter dalam 0,25 mm, tebal lapisan film 0,25 µm. Gas yang digunakan sebagai fase gerak adalah gas nitrogen dengan aliran bertekanan 30 ml/menit. Dalam proses pembakaran FID digunakan gas H2 dengan laju alir 40 ml/menit dan He dengan laju alir 30 ml/menit. Laju alir udara 400 ml/menit. Suhu injektor 220 °C, sedangkan suhu detektor 240 °C. Suhu
kolom yang digunakan adalah temperatur terprogram dengan laju kenaikan suhu (Tabel 4).
Tabel 4 Temperatur terprogram dengan laju kenaikan suhu Rate (°C/menit) Temperatur (°C) Hold time (menit)
- 125 5
10 185 5
5 205 10
3 225 7
Volume injek yang digunakan adalah 1 µl. Identifikasi tiap komponen dilakukan dengan membandingkan waktu retensinya dengan standar supelco 37 asam lemak FAME pada kondisi analisis yang sama. Waktu retensi dihitung pada kertas rekorder sebagai jarak dari garis pada saat muncul pelarut sampai ke tengah puncak komponen yang dipertimbangkan.
(d) Perhitungan jumlah asam lemak
Prinsip analisis komposisi asam lemak dengan kromatografi gas adalah dengan mengubah komponen asam lemak pada lemak/minyak menjadi seyawa volatil metil ester asam lemak yang akan dideteksi oleh detektor FID dalam bentuk respon berupa peak kromatogram. Jenis dan jumlah asam lemak yang ada pada contoh dapat diidentifikasi dengan membandingkan peak kromatogram contoh dengan peak kromatogram asam lemak standar yang telah diketahui jenis dan konsentrasinya, kemudian dihitung kadar asam lemaknya. Kadar asam lemak dalam sampel dapat dihitung dengan rumus:
Ax x C standar x Volume contoh x 100 Asam lemak = As 100
Gram contoh Keterangan:
Ax = Luas puncak komponen X
As = Luas puncak standar
Cs = Konsentrasi standar
3.4.4 Uji organoleptik (SNI 2006)
Dalam penelitian ini dilakukan uji penerimaan dimana setiap panelis diharuskan mengemukakan tanggapan pribadinya terhadap produk yang disajikan. Tujuan uji ini adalah untuk mengetahui tingkat kesukaan atau penerimaan panelis terhadap produk minuman fungsional yang dibuat. Uji penerimaan yang dilakukan
adalah uji hedonik dengan menggunakan 30 orang panelis yang semi terlatih. Uji kesukaan dilakukan pada 6 formula minuman. Pada uji ini panelis diminta mengungkapkan tanggapan pribadinya terhadap warna, rasa dan aroma minuman. Tanggapan tersebut berupa kesan suka atau ketidaksukaan, dan panelis juga diminta mengemukakan tingkat kesukaannya (skala hedonik). Pada uji hedonik produk minuman ini, skala hedonik yang digunakan adalah 1-7, dimana angka 1 = sangat tidak suka, 2 = tidak suka, 3 = agak tidak suka, 4 = netral, 5 = agak suka, 6 = suka, dan 7 = sangat suka. Data yang diperoleh ditabulasikan dan dianalisis dengan metode nonparametrik Kruskal-Wallis dan uji lanjut BNT.
Penyajian sampel dilakukan dengan melarutkan masing-masing formula ke dalam gelas yang berisi 150 ml air yang bersuhu 90 oC, setiap gelas diberi kode dan dalam kondisi masih hangat disajikan kepada para panelis. Panelis menuliskan kesan atau tanggapan pribadinya mengenai sampel yang diuji dalam sehelai score sheet (Lampiran 3). Sebelumnya para panelis diberikan pengarahan mengenai tata cara melakukan pengujian.
3.4.5 Uji stabilitas
Produk yang memiliki kandungan omega-3 tertinggi di antara perlakuan yang diterima secara organoleptik, dilanjutkan pengujiannya untuk melihat stabilitas produk terhadap waktu penyimpanan. Pengujian masa simpan dilakukan dengan percepatan waktu atau model akselerasi menggunakan metode Arrhenius.
Model Arrhenius dilakukan dengan menyimpan produk pangan dengan kemasan akhir pada minimal tiga suhu penyimpanan ekstrim. Hasil pengamatan bagi setiap parameter dihitung laju penurunan mutunya per 7 hari dengan menggunakan plot Arrhenius dalam grafik hubungan antara nilai ln k apabila mengikuti ordo reaksi satu, dan ln k nol apabila mengikuti ordo reaksi nol sebagai sumbu y dan sebagai sumbu x nya adalah suhu pada masing-masing penyimpanan (30 oC, 35 oC, dan 45 oC), kemudian dicari nilai ln k nya atau nilai konstanta penurunan mutu per hari yang diperoleh dari kemiringan persamaan regresi grafik masing-masing suhu penyimpanan tersebut. Nilai k merupakan gradien dari regresi linier yang didapat dari ketiga suhu penyimpanan. Dari regresi linier yang diperoleh pada kurva Arrhenius ini dapat diprediksi umur simpan produk dengan menggunakan rumus:
k = ko e –E/RT . Keterangan:
k = konstanta penurunan mutu
ko = konstanta (tidak bergantung pada suhu) E = energi aktivasi
T = suhu mutlak (oK)
R = konstanta gas (1,986 kal/mol K)
Dengan mengubah persamaan di atas menjadi: ln k = ln ko + (-Ea/R) 1/T
Dimana, ko merupakan konstanta penurunan mutu produk yang tidak tergantung suhu, sedangkan k merupakan konstanta penurunan mutu dari salah satu kondisi suhu yang digunakan (30 oC, 35 oC, dan 45 oC) dan Ea/R merupakan gradien yang diperoleh dari plot Arrhenius. Dengan perhitungan menggunakan rumus ini, akan diperoleh nilai ko. Umur simpan merupakan ordo reaksi satu diperoleh dengan rumus:
t = ln Ao – ln At
ko
Keterangan:
t = prediksi umur simpan (hari) Ao = nilai mutu awal
At = nilai mutu produk yang tersisa setelah waktu t ko = konstanta
Berdasarkan rumus diatas dapat diprediksi umur simpan dalam hari atau bulan. Sedangkan apabila mengikuti ordo reaksi nol umur simpan dapat diperoleh dengan menggunakan rumus:
t = Ao – At ko
Selama penyimpanan, produk disimpan pada tiga kondisi suhu yang berbeda, yaitu 30 oC, 35 oC, dan 45 oC. Frekuensi pengamatan dilakukan 7 hari sekali pada masing-masing suhu selama 35 hari.
3.4.5.1 Pengujian mikrobiologi (Maturin dan Peeler 2001)
a) Uji total bakteri (Total Plate Count)
Sebanyak 1 ml sampel diambil dan dimasukkan ke dalam 9 ml larutan pengencer. Selanjutnya dilakukan pengocokan hingga homogen dengan vortex. Pengenceran dan pemupukan dilakukan hingga tingkat pengenceran 10-2, dari tiap-tiap pengenceran, dipipet secara aseptis 1 ml untuk dimasukkan ke dalam cawan petri steril (pemupukan) secara duplo dan ditambahkan media PCA (Plate Count Agar) steril sebanyak 15-20 ml.
Segera setelah penuangan, cawan petri digerakkan di atas meja secara hati-hati untuk menyebarkan sel-sel mikroba secara merata, yaitu dengan gerakan melingkar atau angka delapan. Setelah medium membeku cawan petri diinkubasikan dengan posisi terbalik pada inkubator bersuhu 37 oC selama 2 hari (48 jam). Perhitungan jumlah total mikroba dilakukan dengan Standard Plate Count (SPC) metode Harrigan.
b) Uji kapang/khamir
Sebanyak 1 ml sampel diambil dan dimasukkan ke dalam 9 ml larutan pengencer. Selanjutnya dilakukan pengocokan hingga homogen dengan vortex. Pengenceran dan pemupukan dilakukan hingga tingkat pengenceran 10-2, dari tiap-tiap pengenceran, dipipet secara aseptis 1 ml untuk dimasukkan ke dalam cawan petri steril (pemupukan) secara duplo dan ditambahkan media PDA (Potato Dextrose Agar) cair yang telah ditambah asam tartarat steril 10% (w/v) sebanyak 15-20 ml.
Segera setelah penuangan, cawan petri digerakkan di atas meja secara hati-hati untuk menyebarkan sel-sel mikroba secara merata, yaitu dengan gerakan melingkar atau angka delapan. Setelah medium membeku cawan petri diinkubasikan dengan posisi terbalik pada inkubator suhu 30 oC selama 48 jam. Perhitungan jumlah kapang dan khamir dilakukan dengan metode Harrigan.
3.4.5.2 Nilai pH
Minuman yang masuk dalam batas penerimaan secara organoleptik dan memiliki jumlah omega-3 yang tinggi diukur nilai pH. Sebelum pengukuran, pH-meter distandarisasi menggunakan buffer standar pH 4 dan pH 7.
3.4.5.3 Pengukuran aktivitas air (aw) (AOAC 1994)
Aktivitas air diukur dengan Shibaura aw meter WA-360. Sebelum digunakan, alat dikalibrasi terlebih dahulu dengan menggunakan aw garam standar. Standar aw NaCl adalah 0,7509 dan A2SO4 adalah 0,97 (30 oC). Setelah kalibrasi selesai, bahan dengan berat 5 gram dimasukkan ke dalam aw meter selama kurang lebih 30 menit. Selanjutnya dibaca skala pada aw meter.
3.5 Rancangan Percobaan dan Analisis Data
Data terdiri atas parameter kimia yaitu pengujian proksimat dan asam lemak, Parameter kimia tersebut menggunakan analisis deskriptif. Pengujian nilai organoleptik yang mencakup penerimaan terhadap kenampakan, rasa, dan aroma setiap formula dari 30 panelis, menggunakan uji non parametrik Kruskal-Wallis. Uji nonparametrik ini merupakan alternatif bagi uji F untuk pengujian kesamaan beberapa nilai tengah dalam analisis ragam untuk menghindar dari asumsi bahwa contoh diambil dari populasi normal (Walpole 1995).
Uji Kruskal-Wallis memiliki formula: H = 12 ∑k Ri2 - 3(n + 1) n(n-1) i =1 ni
k = banyaknya contoh
n = jumlah panelis tiap contoh R = rata-rata penilaian
Hasil uji Kruskal-Wallis dibandingkan dengan tabel chi-square untuk melihat pengaruh perbedaan konsentrasi lintah laut terhadap nilai organoleptik. Uji lanjut multiple comparison dilakukan untuk melihat sejauh mana perbedaan antar perlakuan.
Data pengamatan dari uji stabilitas dianalisis menggunakan teknik regresi linier, dan dibantu dengan metode Arrhenius untuk menduga umur simpan produk (Arpah 2001).
Model Arrhenius adalah: .
k = ko e – E/RT k = konstanta penurunan mutu
ko = konstanta (tidak bergantung pada suhu) E = energi aktivasi