i
PEMBUATAN DAN KARAKTERISASI NANOPARTIKEL EKSTRAK ETANOL TEMU KUNCI (Boesenbergia pandurata) PADA
BERBAGAI VARIASI KOMPOSISI KITOSAN
SKRIPSI
Diajukan kepada Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Yogyakarta Guna
Memperoleh Gelar Sarjana Sains Kimia
Oleh:
DESSY KURNIASARI NIM: 12307144005
PROGRAM STUDI KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI YOGYAKARTA
v MOTTO
“BE MYSELF”
vi
PERSEMBAHAN
vii
PEMBUATAN DAN KARAKTERISASI NANOPARTIKEL EKSTRAK ETANOL TEMU KUNCI (Boesenbergia pandurata) PADA
BERBAGAI VARIASI KOMPOSISI KITOSAN
Oleh: Dessy Kurniasari
Pembimbing Utama : Prof. Dr. Sri Atun
ABSTRAK
Tujuan penelitian ini adalah untuk membuat dan mengetahui karakteristik nanopartikel dari ekstrak etanol temu kunci (Boesenbergia pandurata) dan rasio optimal variasi konsentrasi kitosan dan NaTPP dalam pembuatan nanopartikel temu kunci.
Pembuatan ekstrak temu kunci (Boesenbergia pandurata) menggunakan metode maserasi menggunakan etanol teknis 96 % dilanjutkan evaporasi hingga terbentuk ekstrak kental temu kunci. Koloid nanopartikel dibuat dengan mencampurkan ekstrak temu kunci dalam etanol p.a, akuades, larutan kitosan dalam asam asetat glasial, dan larutan NaTPP. Ada 9 variasi komposisi antara larutan kitosan dan NaTPP yakni rasio (5:1); (10:1); (15:1); (20:1); (3,33:1); (8:1); (9:1); (11:1); dan (12:1). Padatan dalam koloid nanopartikel dipisahkan dengan cara sentrifugasi. Endapan yang didapatkan disimpan dalam freezer. Koloid nanopartikel yang terbentuk dikarakterisasi menggunakan Particle Size Analyzer (PSA) dan Zeta Sizer untuk mengetahui ukuran partikel dan nilai zeta potensial. Padatan yang didapatkan dari proses sentrifugasi selanjutnya dikarakterisasi menggunakan Scanning Electron Microscopy (SEM) untuk mengetahui kondisi morfologi padatan tersebut. Karakterisasi dengan KLT pada padatan yang didapatkan bertujuan untuk mengetahui kesamaan kandungan senyawa antara ekstrak etanol temu kunci dan ekstrak etanol temu kunci dalam sediaan berukuran nano.
Koloid nanopartikel yang telah dibuat berwarna kuning dan setelah di sentrifugasi terbentuk padatan berwarna kuning kecokelatan. Karakterisasi menggunakan PSA menunjukkan ukuran partikel pada rentang 389-877 nm sebanyak 98,1 % pada rasio konsentrasi kitosan dan NaTPP = (8:1). Nilai rerata zeta potensial adalah 41,87 mV. Hasil foto SEM menunjukkan morfologi partikel yang memiliki permukaan yang tidak rata. Rf keenam sampel menunjukkan hasil bahwa senyawa yang terkandung dalam ekstrak etanol temu kunci maupun ekstrak etanol temu kunci dalam sediaan nanopartikel adalah sama.
.
viii
THE PREPARATION AND CHARACTERIZATION OF FINGERROOT (Boesenbergia pandurata) ETANOL EXTRACT NANOPARTICLES
WITH VARIOUS CITOSAN COMPOTITION
By:
Dessy Kurniasari
Supervisor : Prof. Dr. Sri Atun
ABSTRACT
This research aimed for creating and determining characteristic of fingerroot (Boesenbergia pandurata) nanoparticles and optimum ratio variation of chitosan and STPP (Sodium tripholyphosphate) consentration to make fingerroot nanoparticles.
Preparation of fingerroot ethanol extract was performed by maceration method with etanol 96% followed by evaporation to form viscous extract of fingerroot. Colloidal nanoparticles were made by mixing the viscous extract of fingerroot with ethanol, aquadest, chitosan solution in acetat glacial acid, and STPP. There were 9 variations of chitosan and STPP compotition ratio those are (5:1); (10:1); (15:1); (20:1); (3,33:1); (8:1); (9:1); (11:1); and (12:1). Colloidal nanoparticles were centrifuged to separate preciptate of fingerroot nanoparticles. Then, the precipitate of fingerroot was kept in freezer. Characterization nanoparticles size and zeta potential of fingerroot nanoparticles was performed using Particle Size Analyzer (PSA) and Zeta Sizer. Morfologi of preciptated nanoparticles characterized using Scanning Electron Microscopy (SEM). Characterization of preciptate nanoparticles using TLC for determining the similarity of compounds fingerroot etanol extract and etanol extract nanoparticles.
Colloidal nanoparticles that have been prepared form yellow color and after sentrifugation, it form solid yellow-brown. Characterization using PSA showed the nanoparticle size by 389-877nm 98,1% in the ratio concentration of chitosan and STPP = 8:1. The average of zeta potential value was 41,87mV. Outcome from using SEM showed the morfologi of preciptated particle. The Rf of six sample showed that compound in extract ethanol of fingerroot and nanoparticle extract ethanol of fingerroot was the same.
ix
KATA PENGANTAR
Segala puji dan syukur kepada Allah SWT, atas limpahan rahmat dan karunia-nya sehingga saya dapat menyelesaikan Tugas Akhir Skripsi dengan Judul “Pembuatan dan karakterisasi Nanopartikel Ekstrak Etanol Temu Kunci
(Boesenbergia pandurata) pada Berbagai Variasi Komposisi Kitosan”, sebagai
persyaratan untuk mendapatkan gelar Sarjana Sains bidang Kimia.
Penulis menyadari bahwa dalam penyusunan Tugas Akhir Skripsi tidak lepas dari bantuan banyak pihak, oleh sebab itu saya ucapkan banyak terimakasih kepada:
1. Bapak Dr. Hartono, selaku Dekan FMIPA Universitas Negeri Yogyakarta 2. Bapak Drs. Jaslin Ikhsan, M.App.Sc.,Ph.D, selaku Ketua Jurusan
Pendidikan Kimia FMIPA UNY dan Koordinator Tugas Akhir Skripsi Jurusan Pendidikan Kimia FMIPA UNY
3. Ibu Prof. Dr. Sri Atun, selaku Pembimbing utama dan Ketua Penguji yang selalu memberikan bimbingan, motivasi, dukungan, dan ilmu dengan penuh kesabaran sehingga penyusunan Tugas Akhir Skripsi ini dapat terselesaikan dengan baik
4. Ibu Siti Marwati, M. Si., selaku sekretaris yang telah memberikan kritik dan saran dalam penyusunan Tugas Akhir Skripsi ini
x
6. Ibu Dr. Amanatie, M. Pd., M. Si., selaku Penguji Pendamping yang telah memberikan arahan dan masukan dalam penyusunan Tugas Akhir Skripsi ini
7. Bapak Drs. Sunarto, M.Si, selaku Pembimbing Akademik
8. Seluruh Dosen dan Staff karyawan FMIPA UNY, yang selalu membantu baik langsung maupun tidak langsung dalam penyusunan Tugas Akhir Skripsi ini
9. Semua keluarga besar atas dukungan, motivasi, dan doanya
10.Teman-teman Kimia Swadana 2012, Hima Kimia 2013 dan 2014, dan juga teman-teman konsentrasi organik
11.Semua pihak yang telah membantu kelancaran terselesaikannya laporan ini yang tidak dapat saya sebutkan satu persatu
12.Rasa bahagia, semangat, haru, sedih, susah, lelah, terimakasih telah hadir dihidupku.
Akhir kata, saya berharap semoga skripsi ini dapat bermanfaat sebagai mana mestinya. Masukan dan saran maupun kritik yang membangun terhadap Tugas Akhir Skripsi ini akan saya terima dengan senang hati sebagai bahan perbaikan nantinya.
Yogyakarta, September 2016
xi DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN ... ii
PERNYATAAN ... iii
HALAMAN PENGESAHAN ... iv
MOTTO ... v
PERSEMBAHAN ... vi
ABSTRAK ... vii
ABSTRACT ... viii
KATA PENGANTAR ... ix
DAFTAR ISI ... xi
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvi
BAB I PENDAHULUAN ... 1
A. Latar Belakang Masalah ... 1
B. Identifikasi Masalah ... 4
C. Pembatasan Masalah ... 5
D. Perumusan Masalah ... 6
E. Tujuan Penelitian ... 6
xii
BAB II KAJIAN TEORI ... 8
A. Deskripsi Teori ... 8
1. Temu Kunci (Boesenbergia pandurata) ... 8
a. Uraian Tumbuhan ... 9
b. Senyawa Metabolit Sekunder ... 10
c. Manfaat Temu Kunci (Boesenbergia pandurata) ... 11
2. Nanopartikel ... 12
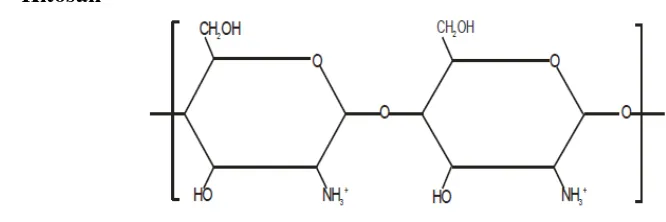
3. Kitosan ... 13
4. Natrium Tripolifosfat ... 15
5. Metode Gelasi Ionik ... 16
6. PSA (Particle Size Analyzer) ... 17
7. Zeta Sizer Nano... 19
8. SEM (Scanning Electron Microscopy) ... 19
9. KLT (Kromatografi Lapis Tipis) ... 20
B. Penelitian yang Relevan ... 21
C. Kerangka Berfikir ... 23
BAB III METODE PENELITIAN ... 25
A. Subjek dan Objek Penelitian ... 25
B. Variabel Penelitian ... 25
C. Alat dan Bahan Penelitian ... 25
D. Prosedur Penelitian ... 26
E. Teknik Analisis Data ... 28
xiii
BAB IV HASIL DAN PEMBAHASAN ... 31
A. Hasil Penelitian ... 31
B. Pembahasan ... 35
BAB V KESIMPULAN DAN SARAN ... 42
A. Kesimpulan ... 42
B. Saran ... 42
DAFTAR PUSTAKA ... 44
xiv
DAFTAR TABEL
xv
DAFTAR GAMBAR
Halaman
Gambar 1. Rimpang Temu Kunci (Boesenbergia pandurata)... 8
Gambar 2. Struktur Kimia Kitosan ... 13
Gambar 3. Struktur Kimia NaTPP ... 15
Gambar 4. Bagan Alur Penelitian ... 30
Gambar 5. Filtrat Ekstrak Etanol Temu Kunci ... 31
Gambar 6. Ekstrak Kental Temu Kunci (Boesenbergia pandurata)... 31
Gambar 7. Koloid Nanopartikel Ekstrak Etanol Temu Kunci ... 32
Gambar 8. Endapan Basah Hasil Sentrifuge ... 32
Gambar 9. Endapan Kering Hasil Sentrifuge ... 32
Gambar 10. Hasil Foto SEM Sampel G... ... 34
xvi
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Perhitungan Jumlah Bahan yang Digunakan ... 49
Lampiran 2. Perhitungan Nilai Rf Kromatografi Lapis Tipis ... 52
Lampiran 3. Dokumentasi Penelitian ... 54
Lampiran 4. Bagan Prosedur Kerja ... 58
Lampiran 5. Surat Keterangan Identifikasi Tumbuhan ... 60
Lampiran 6. Hasil Pengukuran Parikel dengan PSA ... 61
Lampiran 7. Hasil Pengukuran Zeta Potensial ... 72
1 BAB I PENDAHULUAN
A. Latar Belakang
Nanoteknologi menjadi salah satu bidang ilmu Fisika, Kimia, Biologi, dan rekayasa yang penting dan menarik beberapa tahun terakhir ini. Jepang dan Amerika Serikat merupakan dua negara terdepan dalam riset nanoteknologi. Salah satu pengembangan nanoteknologi yang sedang berkembang yaitu nanopartikel. Penelitian nanopartikel sedang berkembang pesat karena dapat diaplikasikan secara luas seperti dalam bidang lingkungan, elektronik, optis, dan biomedis (Tatang, Doni, dan Qomaruddin, 2011).
Pada teknologi nano, suatu partikel didefinisikan sebagai objek kecil yang berperilaku seperti unit utuh dalam hal penghantaran dan sifat-sifatnya. Menurut Tiyaboonchai (2003), nanopartikel merupakan partikel koloid padat dengan diameter berkisar antara 1-1000 nm.
Kegunaan material berstruktur nano baik dengan menggunakan bahan organik maupun anorganik dapat diaplikasikan dalam berbagai macam bidang kehidupan seperti dalam kesehatan, kedokteran, kimia, fisika, biologi, bahkan dalam dunia kemiliteran. Fernandez (2012) menyebutkan bahwa, pada tahun 2006 telah muncul lebih dari 300 macam produk nanoteknologi di pasaran dan terus meningkat tiap tahunnya. Produk nanoteknologi tersebut diklaim memiliki sifat sifat yang lebih unggul karena memiliki peran nanomaterial didalamnya.
2
dengan partikel berukuran makroskopik. Menurut Wipsar (2012), sifat mekanis yang paling besar (maksimum) terjadi ketika ukuran partikel sangat kecil (berukuran nano). Semakin besar ukuran partikel (skala mikrometer keatas), sifat-sifat mekanis justru akan berkurang, sedangkan ukuran partikel yang lebih kecil dari nanometer akan menghasilkan bahan amosphorus.
3
heksana, kloroform, maupun etil asetat. Ekstrak etanol dari rimpang temu kunci misalnya, memiliki daya antibakteri terhadap Salmonella typhi dan Streptococcus hemolyric α non pneumoniae (Mariska, Kuswandi, dan Susi, 2011).
Nanopartikel terdiri dari bahan makromolekul dan dapat digunakan untuk terapi sebagai pembantu (adjuvant) vaksin atau pembawa obat, yaitu dengan melarutkan, memerangkap, mengenkapsulasi, menyerap atau menempelkan bahan aktif secara kimia. Polimer yang digunakan untuk membentuk nanopartikel dapat berupa polimer sintetik dan alami. Polimer yang memudahkan dalam penyiapan nanopartikel dapat dipilih berupa polimer yang larut air. Salah satu polimer larut air yang dapat digunakan pada pembuatan nanopartikel untuk tujuan pengobatan adalah kitosan. Kitosan memiliki sifat yang ideal, yaitu biocompatible,
biodegradable, tidak beracun, dan tidak mahal (Tiyaboonchai, 2003). Kitosan merupakan polisakarida alam [β(1-4) glukosamin (2-amino-2-deoksi-d-glukosa) N-asetil-d-glukosamin (2-asetamido-2-deoksi-d-glukosa)] yang mulai banyak diaplikasikan dalam industri farmasi, pangan, dan kesehatan. Kitosan mempunyai beberapa sifat yang menguntungkan yaitu bersifat antimikroba, wound healing, tidak beracun, murah, biokompatibel, dapat dibiodegradasi, serta larut air. Dalam bentuk mikro/ nanopartikel kitosan mempunyai banyak keunggulan yakni tidak toksik, stabil selama penggunaan, luas permukaan yang tinggi, serta dapat dijadikan matriks untuk berbagai jenis obat dan ekstrak tanaman (Agnihotri et.al, 2004). Dalam pembuatan nanopartikel dibutuhkan crosslinker polianion.
4
dibandingkan polianion lain seperti sulfat dan sitrat, bersifat tidak toksik sehingga diharapkan tidak akan mengubah biocompatibilitas kitosan dan sesuai untuk aplikasi biomedis.
Menurut Agnihotri et.al (2004) dan Tiyaboonchai (2003), metode yang dapat digunakan untuk memproduksi mikro dan nanopartikel kitosan dari kitosan adalah metode ikatan silang emulsi (emulsion cross-linking), presipitasi (precipitation), pengeringan semprot (spray drying), metode penggabungan droplet emulsi (emulsion-droplet coalescence method), gelasi ionik (ionic
gelation), reverse micellar method, dan kompleks polielektrolit (polyelectrolyte complex). Rauhatun dan Iis (2013), berhasil membuat nanopartikel kitosan-TPP dengan ekstrak etanol daging buah mahkota dewa dengan metode gelasi ionik.
Banyak penelitian yang dilakukan untuk mengetahui manfaat dari pengembangan nanopartikel. Dalam penelitian yang dilakukan Ronny Martien dkk (2012), tentang perkembangan teknologi nanopartikel sebagai sistem panghantaran obat, memberikan hasil bahwa partikel atau globul pada skala nanometer memiliki sifat fisik yang khas dibandingkan partikel pada ukuran yang lebih besar terutama dalam meningkatkan kualitas penghantaran senyawa obat. Kelebihan lain dari teknologi nanopartikel adalah keterbukaannya untuk dikombinasikan dengan teknologi lain, sehingga membuka peluang untuk dihasilkan sitem penghantaran yang lebih sempurna.
5
bentuk nano memiliki keunggulan yang lebih sebagai sediaan obat dibandingkan dalam bentuk makro maupun mikropartikel. Tantangan terbesar dalam penelitian ini adalah mencari perbandingan yang tepat untuk menghasilkan partikel berukuran nano.
B. Identifikasi Masalah
Berdasarkan latar belakang masalah yang telah dikemukakan, dalam penelitian ini dapat diidentifikasi beberapa permasalahan sebagai berikut:
1. Ekstrak temu kunci (Boesenbergia pandurata) dapat dibuat dari bagian-bagian tumbuhan tersebut, diantaranya rimpang, daun, akar, dan kulit. 2. Terdapat berbagai jenis pelarut yang digunakan untuk mengekstrak temu
kunci (Boesenbergia pandurata) seperti etanol, metanol, etil asetat, heksana, dan kloroform.
3. Modifikasi nanopartikel temu kunci (Boesenbergia pandurata) dapat dilakukan dengan beberapa pengikat seperti kitosan dan asam alginat. 4. Terdapat banyak metode pembuatan nanopartikel kitosan diantaranya
metode ikatan silang emulsi, presipitasi, pengeringan semprot, penggabungan droplet emulsi, gelasi ionik, reverse micellar method, dan kompleks polielektrolit.
5. Variasi rasio kitosan dan NaTPP (Natrium tripolifosfat) dalam pembuatan nanopartikel temu kunci (Boesenbergia pandurata) berpengaruh terhadap ukuran partikel, berat endapan, dan nilai zeta potensial.
6 C. Pembatasan Masalah
1. Bagian temu kunci (Boesenbergia pandurata) yang digunakan adalah rimpangnya.
2. Pelarut yang digunakan untuk mengekstrak temu kunci (Boesenbergia
pandurata) adalah etanol teknis 96%.
3. Jenis pengikat yang digunakan untuk modifikasi nanopartikel ekstrak etanol temu kunci (Boesenbergia pandurata) adalah kitosan.
4. Metode yang digunakan dalam pembuatan nanopartikel ekstrak etanol temu kunci (Boesenbergia pandurata) dengan kitosan adalah gelasi ionik.
5. Variasi rasio kitosan dan NaTPP (Natrium tripolifosfat) dalam pembuatan nanopartikel ekstrak etanol temu kunci (Boesenbergia pandurata) adalah (5:1); (10:1); (15:1); (20:1); (3,3:1); (8:1); (9:1); (11:1); (12:1) yang mengacu pada penelitian Sri Atun dan Retno Arianingrum (2015).
6. Karakterisasi nanopartikel ekstrak etanol temu kunci (Boesenbergia
pandurata) menggunakan instrumen PSA (Particle Size Analyzer), SEM (Scanning Electron Microscopy), Zeta Sizer Nano Series Malvem, dan KLT (Kromatografi Lapis Tipis).
D. Perumusan Masalah
Berdasarkan batasan masalah yang telah dikemukakan dapat dirumuskan beberapa permasalahan antara lain :
1. Bagaimana pembuatan nanopartikel ekstrak etanol dari rimpang temu kunci
7
2. Bagaimana karakter nanopartikel yang dihasilkan berdasarkan karakterisasi menggunakan instrumen PSA (Particle Size Analyzer), SEM (Scanning
Electron Microscopy), Zeta Sizer Nano Series Malvem, dan KLT (Kromatografi Lapis Tipis).
E. Tujuan Penelitian
Tujuan yang ingin dicapai dalam penelitian ini adalah sebagai berikut: 1. Membuat nanopartikel ekstrak etanol temu kunci (Boesenbergia pandurata)
dengan kitosan dan NaTPP (Natrium Tripolifosfat) pada berbagai variasi komposisi.
2. Menentukan karakteristik nanopartikel yang dihasilkan menggunakan instrumen PSA (Particle Size Analyzer), SEM (Scanning Electron
Microscopy), Zeta Sizer Nano Series Malvem, dan KLT (Kromatografi Lapis Tipis).
F. Manfaat Penelitian
Hasil dari penelitian ini diharapkan dapat memberikan manfaat bagi industri farmasi dan teknologi serta masyarakat sekitar, yaitu :
1. Menambah pengetahuan masyarakat tentang kegunaan ekstrak etanol temu kunci (Boesenbergia pandurata).
2. Pengembangan penelitian tentang sediaan nanopartikel ekstrak etanol temu kunci (Boesenbergia pandurata) dengan kitosan pada industri farmasi dan teknologi.
8 BAB II KAJIAN TEORI
A. Deskripsi Teori
1. Temu Kunci (Boesenbergia pandurata)
Boesenbergia pandurata Roxb. (Gambar 1) atau lebih dikenal dengan nama temu kunci, merupakan salah satu tanaman obat yang ada di Indonesia (Agus Chahyadi, 2014).
Gambar 1. Rimpang Temu Kunci Sumber: www.tanamanobat.net
Nama Tumbuhan
Nama Ilmiah : Boesenbergia pandurata
Sinonim : Gastrochillus panduratum (Roxb) Schult; Kaemferia pandurata (Roxb); Boesenbergia rotunda
Nama umum : Temu kunci
9
Anipa wakang (Hila-Alfuru), Aruhu konci (haruku), Sun (Buru), Rutu kakuzi (Seram), Tamputi (Ternate)
Nama asing : Fingerroot (Inggris), Krachai (Thailand), Chinesekey (Cina) Klasifikasi tumbuhan
Divisi : Magnoliophyta Kelas : Liliopsida Ordo : Zingiberales Famili : Zingiberaceae Genus : Boesenbergia
Spesies : Boesenbergia pandurata
a. Uraian Tumbuhan
10
spatha, panjang tangkai 41 cm, umumnya tangkai tersembunyi dalam 2 helai daun terujung. Kelopak bunganya tiga buah lepas, runcing. Mahkota bunganya tiga buah, warnanya merah muda atau kuning-putih, berbentuk tabung 55-52 mm, bagian atas tajuk berbelah-belah, berbentuk lanset dengan lebar 4 mm dan panjang 18 mm. Benang sarinya satu fertil besar, kepala sarinya bentuk garis membuka secara memanjang. Lainnya berupa bibir-bibiran (staminodia) bulat telur terbalik tumpul, merah muda atau kuning lemon, gundul, memiliki 6 pertulangan dan ukurannya 25x7 cm. Putik bunganya berupa bakal buah 3 ruang, banyak biji dalam setiap ruang (Plantus, 2008).
Temu kunci (Boesenbergia pandurata L.) merupakan salah satu tanaman herbal yang banyak ditemukan di negara-negara Asia beriklim tropis. Biasanya dikenal dengan nama temu kunci atau kunci. Bentuk temu kunci agak berbeda dengan temu-temuan yang lain karena rimpang biasanya tumbuh di bawah permukaan tanah secara mendatar dan beruas, sedikit keras, bersisik tipis, dan berbau harum. Anakan rimpang menggerombol kecil di sebelah rimpang induk, menyerupai rangkaian anak kunci (Rikha, Susi, dan Eka 2013).
b. Senyawa Metabolit Sekunder
Menurut (Rikha, Susi, dan Eka 2013), kandungan kimia yang terdapat dalam tanaman temu kunci (Boesenbergia pandurata) adalah minyak atsiri (terdiri dari kamfer, sineol, metil sinamat, dan hidromirsen), damar, pati, saponin, flavonoid pinostrolerin, dan alpinetin.
4-11
hidroksipanduratin (Tuchinda, et al., 2002). Selain itu, rimpang temu kunci juga mengandung pati, damar, saponin, boesenbergin A, boesenbergin B, asam kavinat, senyawa flavon (5,7-dimetoksiflavon; 3,5,7,4-tetrametoksiflavon; dan 3,5,7,3,4-pentametoksiflavon), senyawa flavanon (5-hidroksi-7,4-dimetoksiflavanon), senyawa kalkon (2-hidroksi-4,6-dimetoksikalkon; 2,6-dihidroksi-4-metoksikalkon; 2-hidroksi-4,4,6-trimetoksikalkon; dan 2,4-dihidroksi-6-metoksikalkon), panduratin B1, serta panduran B2 (Hargono, 2000). Penelitian lain tentang penemuan senyawa metabolit sekunder dalam temu kunci adalah Oka (2012) berhasil mengisolasi dan mengidentifikasi senyawa pinostrobin (5-hidroksi-7-metoksi flavanon) pada ekstrak n-heksana rimpang temu kunci, Agus Chahyadi dkk(2014), minyak atsiri dan flavonoid.
c. Manfaat Temu Kunci (Boesenbergia pandurata)
12
Di Indonesia rimpang dari temu kunci dimanfaatkan sebagai bumbu masakan tradisional dan juga digunakan sebagai obat tradisional untuk berbagai penyakit seperti asma, diare, demam, dan sakit perut (Mulyadi, Tjitjik, dan Mulya, 2013). Penelitian yang dilakukan oleh Mulyadi, Tjitjik, dan Mulya (2013) menemukan bahwa rimpang dari temu kunci memiliki beberapa senyawa flavonoid dan minyak atsiri, dan berhasil mengisolasi dua senyawa flavonoid yaitu pinostrobin dan pinocembrin sebagai agen antioksidan dan sitotoksik.
2. Nanopartikel
Nanopartikel adalah partikel koloid atau padatan dengan diameter berkisar dari 10-1000 nm. Nanopartikel dengan menggunakan polimer dapat dimanfaatkan untuk sistem penghantaran tertarget, meningkatkan bioavailabilitas, pelepasan obat terkendali, atau melarutkan obat untuk penghantaran sistemik. Juga dapat digunakan untuk melindungi agen terapetik akibat adanya degradasi enzim
(nuklease dan protease) (Rauhatun dan Iis, 2013).
13
Nanopertikel terbukti mampu membawa obat (antibiotik, sitostatik, peptida, dan protein) ke target jaringan yang spesifik. Nanopatrikel jugan diyakini mampu melindungi obat agar tidak mengalami degradasi baik secara kimia maupun enzimatis. Nanopartikel juga mampu mengurangi efek samping yang mungkin ditimbulkan dari beberapa zat aktif.
Menurut Rawat, Singh, dan Saraf (2006), nanopartikel yang digunakan sebagai sistem penghantaran obat memiliki banyak keuntungan. Salah satu keuntungannya yaitu, ukuran partikel dan sifat permukaannya dapat diatur dengan mudah. Nanopartikel dapat mengontrol pelepasan zat aktif selama perjalanannya menuju lokasi obat tersebut bekerja, sehingga dapat meningkatkan efek terapi obat dan mengurangi efek sampingnya. Sistem pelepasan obat dalam bentuk nanopartikel dapat diatur dengan jalan memilih matriks yang tepat sehingga nantinya dapat dihasilkan sitem pelepasan obat yang berbeda-beda. Nanopartikel dapat digunakan untuk banyak rute pemberian obat, seperti oral, nasal, parental, intra-okular, dan lainnya.
3. Kitosan
Gambar 2. Struktur Kimia Kitosan (Eriawan Rismana dkk, 2014)
14
(2003), kitosan adalah suatu polimer dari sakarida (polisakarida) yang didapatkan dari proses deasetilasi senyawa kitin yang terkandung di dalam kulit luar hewan golongan Crustacea contohnya udang, kepiting, dan lainnya. Kitosan merupakan salah satu polimer yang banyak dikembangkan dan diteliti untuk aplikasinya dalam bidang farmasetika karena memiliki sifat biocompatible, biodegradable, dan tidak memiliki efek toksik. Struktur kimia kitosan dapat dilihat pada Gambar 2 (Eriawan Rismana dkk, 2014).
Sumber utama untuk produksi kitosan adalah kitin dan bahan baku yang digunakan untuk mengolahnya tersedia dalam jumlah yang cukup melimpah di Indonesia, terutama cangkang kepiting dan rajungan serta kulit udang. Kitosan merupakan modifikasi polimer karbohidrat alami yang diproses melalui N deasetilasi parsial kitin. Unit utama pada polimer kitin adalah 2-deoksi-2-(asetilamino) glukosa. Walaupun kitin tidak larut dalam sebagian besar pelarut, kitosan larut dalam sebagian besar larutan asam organik pada pH kurang dari 6,5 termasuk asam format, asetat, tartrat, dan sitrat. Kitosan tidak larut dalam asam fosfat dan asam sulfat. Kitosan tersedia dalam rentang berat molekul dan derajat deasetilasi yang luas. Berat molekul (BM) dan derajat deasetilasi (DD) adalah faktor utama yang mempengaruhi ukuran partikel, pembentukan partikel, dan agregasi (Tiyaboonchai, 2003).
Kitosan memiliki sifat-sifat yang ideal sebagai polimer nanopartikel,sifat-sifat tersebut yaitu: mudah disintesis, murah, biokompatibel, biodegradable,
15
diaplikasikan untuk obat dengan molekul kecil, protein, dan polinukleotida (Tiyaboonchai, 2003).
Kitosan merupakan biopolimer alami yang menarik disebabkan adanya gugus amino reaktif dan grup fungsional hidroksil. Kitosan memiliki karakteristik biokompatibilitas yang diinginkan serta kemampuan untuk meningkatkan permeabilitas membran. Oleh karenanya, kitosan merupakan salah satu matriks imobilisasi yang paling menjanjikan karena memiliki kemampuan membentuk membran, sifat adesi yang baik, harga murah, tidak beracun, kekuatan mekanis dan hidrofilisitas yang tinggi serta perbaikan stabilitas (Nakorn, 2008; Erdawati, 2008).
Kitosan sangat sukar larut dalam air dan tidak larut dalam etanol 95%, pelarut organik lain, dan larutan netral atau basa pada pH di atas 6,5. Kitosan mudah larut dalam larutan asam organik encer maupun pekat (Rowe, 2009). Menurut Tiyaboonchai (2003), salah satu aplikasi kitosan yang banyak diteliti adalah kemampuannya sebagai polimer dalam membentuk nanopartikel dan telah banyak diteliti bahwa nanopartikel kitosan sebagai pembawa obat untuk penghantaran obat secara oral maupun topikal.
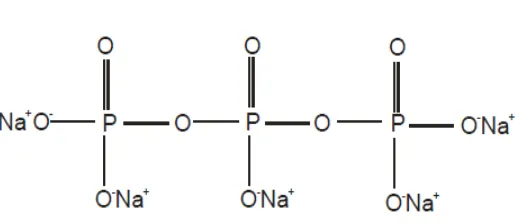
[image:31.595.209.467.596.707.2]4. Natrium Tripolifosfat (NaTPP)
16
Tripolifosfat dalam nanopartikel sambung silang multi ion digunakan sebagai pasangan ion dari kitosan. Sifatnya sebagai anion multivalen yang dapat membentuk ikatan sambung silang dengan kitosan menjadi alasan penggunaan tripolifosfat. Berdasarkan penelitian yang dilakukan Yu Shin et al (2008) menyebutkan bahwa penggunaan tripolifosfat sebagai salah satu pasangan ion kitosan akan memberikan hasil nanopartikel yang dapat lebih stabil dan memiliki karakter penembusan membran yang lebih baik. Yu Shin et al (2008) mengungkapkan bahwa pada nanopartikel sambung silang multi ion, tripolifosfat berperan sebagai komponen anion multivalen yang dapat membentuk ikatan sambung silang dengan kitosan yang memiliki sifat kationik. Struktur kimia NaTPP dapat dilihat pada Gambar 3 ((Eriawan Rismana dkk, 2014).
5. Metode Gelasi Ionik
Beberapa metode telah digunakan untuk membuat sistem partikulat kitosan. Penentuan metode yang digunakan tergantung faktor-faktor seperti ukuran partikel yang diinginkan, stabilitas kimia dan panas dari bahan aktif, reprodusibilitas profil kinetik pelepasan produk akhir dan toksisitas residu yang terkait dengan produk akhir (Agnihotri et al., 2004). Menurut Agnihotri et al. (2004) dan Tiyaboonchai (2003), metode yang dapat digunakan untuk memproduksi mikro dan nanopartikel kitosan dari kitosan adalah metode ikatan silang emulsi (emulsion cross-linking), presipitasi (precipitation), pengeringan semprot (spray drying), metode penggabungan droplet emulsi (emulsion-droplet
17
Salah satu metode yang digunakan untuk pembuatan nanopartikel adalah dengan gabungan kompleks koaservasi atau gelasi ionik. Kompleks koaservasi atau gelasi ionik dapat diinduksi dalam sistem yang mempunyai dua dispersi koloid hidrofilik dan mempunyai muatan yang berlawanan. Netralisai muatan positif oleh muatan negatif menyebabkan pemisahan kompleks (Versic, 2010; Rauhatun dan Iis, 2014). Mekanisme terbentuknya formulasi nanopartikel kitosan ini berdasarkan pada interaksi elektrostatik antar gugus amina kitosan dengan gugus bermuatan negatif dari suatu polianion (Tiyaboonchai, 2003). Menurut penelitian yang dilakukan Dustgania Amir, et al (2008), nanopartikel yang dibuat dengan metode gelasi ionik dengan komposisi kitosan dan natrium tripolifosfat di dalamnya akan menghasilkan nanopartikel dengan ukuran 250-350 nm dengan efisiensi penjerapan zat aktif sekitar 72,2%.
Mekanisme pembentukan nanopartikel berdasarkan interaksi elektrostatik antara gugus amin dari kitosan dan gugus negatif dari polianion seperti tripolifosfat. Mekanisme kerja yang diawali dengan melarutkan kitosan didalam asam asetat glasial ini kemudian dilanjutkan dengan penambahan natrium tripolifosfat sedikit demi sedikit dengan pengadukan menggunakan magnetic
stirrer.
6. PSA (Particle Size Analyzer)
18
menggunakan Laser Diffraction (LAS). Metode ini dinilai lebih akurat untuk analisis bila dibandingkan dengan metode analisa gambar maupun metode ayakan (sieve analyses), terutama untuk sample-sampel dalam orde nanometer maupun submikron. Contoh alat yang menggunakan metode LAS adalah Particle Size
Analyzer (PSA). Alat ini menggunakan prinsip Dynamic Light Scattering (DLS). Metode ini juga dikenal sebagai Quasi-Elastic Light Scattering (QELS). Alat ini berbasis Photon Correlation Spectroscopy (PCS). Metode LAS bisa dibagi dalam dua metode:
1. metode basah : metode ini menggunakan media pendispersi untuk mendispersikan material uji.
2. metode kering : metode ini memanfaatkan udara atau aliran udara untuk melarutkan partikel dan membawanya ke sensing zone. Metode ini baik digunakan untuk ukuran yang kasar, dimana hubungan antarpartikel lemah dan kemungkinan untuk beraglomerasi kecil.
19
distribusi, sehingga hasil pengukuran dapat diasumsikan sudah menggambarkan keseluruhan kondisi sampel.
7. Zeta Sizer Nano
Potensial zeta menggambarkan stabilitas nanopartikel karena perbedaan muatan antar partikel akan mempengaruhi gaya tolak menolak antar partikel. Untuk memperoleh koloid nanopartikel yang stabil, nanopartikel harus memiliki nilai zeta potensial lebih dari 30 mV (Akhtar et al., 2012).
Menurut Jahanshahi dan Babaei (2008), potensial zeta juga berkaitan dengan stabilitas fisik permukaan yang mencegah terjadinya agregasi partikel, dengan menurunkan potensial zeta akan menyebabkan terjadinya agregasi atau sedimentasi. Potensial zeta dari sebuah nanopartikel biasnya digunakan untuk mengkarakterisasi sifat muatan permukaan partikel yang berkaitan dengan interaksi elektrostatik nanopartikel. Potensial zeta juga mencerminkan potensi muatan dari partikel yang dipengaruhi oleh komposisi dari partikel dan medium tempat nanopartikel terdispersi.
8. SEM (Scanning Electron Microscopy)
20
SEM (Scanning Electron Microscopy) berbeda dengan TEM (Transmision
Electron Microscopy) dalam hal bahwa suatu berkas elektron yang sangat halus di-scan menyilangi permukaan sampel dalam sinkronisasi berkas tersebut dalam tabung sinar katoda. Elektron elektron yang terhambur digunakan untuk memproduksi sinyal yang memodulasi berkas dalam tabung sinar katoda, yang memproduksi suatu citra dengan kedalaman medan yang besar dan penampakan yang hampir tiga dimensi. Dalam penelitian morfologi permukaan dengan menggunakan SEM, terbatas pemakaiannya, tetapi memberikan informasi yang bermanfaat mengenai topologi permukaan dengan resolusi sekitar 100 Å (Stevens, 2001).
9. KLT (Kromatografi Lapis Tipis)
Menurut Sudjadi (2008), Kromatografi Lapis Tipis (KLT) merupakan metode pemisahan yang paling populer, memiliki banyak kegunaan yang memberikan keuntungan seperti peralatan yang dibutuhkan sederhana, murah, waktu yang digunakan untuk analisis singkat, sampel yang dibutuhkan sedikit, dan memiliki daya pisah yang cukup baik.
Pemisahan komponen-komponen berdasrkan perbedaan adsorbsi atau partisi oleh fase diam dipisahkan oleh gerak pelarut pengembang. Pemilihan eluen (fasa gerak) yang tepat merupakan langkah penting dalam keberhasilan analisis menggunakan KLT. Pemilihan eluen berdasarkan pada prinsip “like disolve like”.
21
mempunyai sifat polar tinggi (misalnya air) dalam campuran, maka akan mengubah sistem menjadi partisi. Campuran yang baik memberikan fasa gerak yang mempunyai kekuatan bergerak sedang, tetapi sebaiknya dihindari mencampur lebih dari dua komponen, karena campuran yang lebih kompleks cepat mengalami perubahan-perubahan fasa terhadap perubahan suhu (Hardjono, 1991).
Identitas noda pada plat dinyatakan dengan harga Rf (Retordation factor). Rf merupakan rasio jarak noda terhadap titik awal dibagi jarak eluen terhadap titik awal. Secara sistematis dapat dituliskan :
Rf =
dengan, l = jarak noda dari titik awal ke titik akhir setelah proses pengembangan (cm) dan h = jarak eluen dari titik awal ke batas akhir eluen (cm). Harga Rf berkisar antara 0-0,999.
Keuntungan yang pasti dari KLT adalah biaya yang sangat rendah dan kemudahannya. KLT juga mempunyai kemampuan sebagai suatu metode rutin untuk penyaringan awal sampel-sampel polimer atau untuk memonitor proses-proses polimerisasi (Stevens, 2001).
B. Penelitian Relevan
22
didefinisikan sebagai sistem koloid submikronik (<1 μm) (Eriawan Rismana, dkk. 2014). Beberapa penelitian pembuatan material nano juga dilakukan antara lain oleh Dustgani dkk. (2008) melakukan penelitian tentang pembuatan nanopartikel kitosan sebagai matriks penghantar untuk dexametason, Wu dkk. (2005) melakukan penelitian tentang pembuatan nanopartikel kitosan sebagai matriks penghantar untuk glycyrrhizinate.
Penelitian mengenai pembuatan nanopartikel telah dilakukan oleh Sri Atun dan Retno Arianingrum (2015). Objek penelitiannya adalah Kaemferia rotunda, pembuatan nanopartikel menggunakan metode gelasi ionik dengan kitosan dan NaTPP. Hasil pengukuran nanopartikel adalah adntara 172-87 nm dengan nilai zeta potensial antara +28,06 mV sampai +38,03 mV.
Penelitian yang dilakukan oleh Rauhatun dan Iis (2014) mengenai preparasi nanopartikel kitosan-TPP dari ekstrak etanol daging buah mahkota dewa
(Phaleriamacrocarpa (Scheff) Boerl) dengan metode gelasi ionik, diperoleh hasil bahwa nanopartikel ekstrak etanol buah mahkota dewa konsentrasi 1,5 mg/mL memiliki ukuran partikel rata-rata 190,9 nm dan konsentrasi 2,0 mg/mL rata-rata 162,87 nm. Zeta potensial rata-rata 60,86 mV dan 48,5 mV. Loading capacity rata-rata 2,96 % dan 5,33 %. Loading efficiency atau efisiensi proses nanopartikel yaitu rata-rata 35,75 % dan 45,26 %.
Ekstraksi dan karakterisasi nanopartikel ekstrak sirih merah (Piper
23
evaporator hingga dihasilkan ekstrak kental. Pada tahapan sintesis nanopartikel dilakukan dengan modifikasi fisik menggunakan metode gelasi ionik untuk pembentukan oleh sodium tripolifosfat (STPP). Sintesis nanopartikel dilakukan pada beberapa konsentrasi kitosan dalam asam asetat. Nanopartikel kemudian dienkapsulasi menggunakan spray dryer LabPlant SD-05 dengan bahan pengisi maltodekstrin dan isolat protein kedelai. Karakterisasi nanopartikel menggunakan PSA (Particle Size Analyzer) DelsaNano C Beckman Coulter, zeta potensial, kapasitas antioksidan (DPPH), dan analisis morfologi menggunakan SEM. Hasil yang diperoleh dari penelitian yang telah dilakukan adalah rendemen senyawa aktif pada ekstraksi daun sirih merah lebih besar menggunakan metode refluks. Nanopartikel ekstrak sirih merah disintesis dengan modifikasi fisik menggunakan metode gelasi ionik memanfaatkan sodium tripolifosfat (STPP) untuk membentuk ikatan silang.
C. Kerangka Berfikir
24
lebih baik untuk meningkatkan bioavailabilitas biomolekul, yaitu meningkatkan kemampuan penyerapan dan peredaran obat di dalam tubuh.
Temu kunci memiliki kandungan yang beragam dan sangat bermanfaat bagi pengobatan. Sediaan nanopartikel dipilih untuk meningkatkan manfaat yang terkandung dalam senyawa temu kunci dan juga memiliki keunggulan dalam penghantaran obat ke reseptor.
Pada pembuatan nanopartikel menggunakan metode gelasi ionik, mekanisme terbentuknya formulasi nanopartikel kitosan ini berdasarkan pada interaksi elektrostatik antara gugus amina kitosan dengan gugus muatan negatif dari suatu polianion. Gugus amina pada kitosan yang dilarutkan dalam suasana asam akan terprotonasi membentuk amina kationik (-NH3+). TPP mempunyai muatan negatif sehingga dapat berfungsi sebagai polianion. Reaksi dengan komponen bermuatan negatif baik ion ataupun molekul dapat menyebabkan pembentukan jaringan antara rantai polimer melalui jembatan ionik.
25 BAB III
METODE PRNELITIAN
A. Subjek dan Objek Penelitian
1. Subjek penelitian ini adalah nanopartikel kitosan ekstrak etanol temu kunci (Boesenbergia pandurata).
2. Objek penelitian ini adalah karakteristik nanopartikel kitosan ekstrak etanol temu kunci (Boesenbergia pandurata).
B. Variabel Penelitian 1. Variabel Bebas
Variabel bebas dalam penelitian ini adalah konsentrasi kitosan dan NaTPP (Natrium Tripolifosfat) yang digunakan.
2. Variabel Terikat
Variabel terikat dalam penelitian ini adalah ukuran nanopartikel yang dihasilkan pada masing-masing konsentrasi kitosan dan NaTPP yang digunakan.
3. Variabel Terkontrol
Variabel terkontrol dalam penelitian ini adalah berat ekstrak etanol temu kunci (Boesenbergia pandurata) yang digunakan, konsentrasi asam asetat glasial yang digunakan untuk melarutkan kitosan, lamanya waktu pengadukan, volume etanol, dan volume akuades.
C. Alat dan Bahan Penelitian
26
Alat yang digunakan dalam penelitian ini adalah PSA (Particle Size
Analyzer) HORIBA LB-550 (IK 03 TP 016), SEM (Scanning Electron Microscopy), Zeta Sizer Nano Series Malvem, satu set Evaporator Buchii 190, satu set peralatan Sentrifuge, neraca analitik, gelas beaker, corong gelas, erlenmeyer, gelas ukur 100 mL dan 15 mL, pipet volum 5 mL, kertas saring, serbet, tissue, spatula, magnetic stirrer, alumunium foil, pipet tetes, tabung reaksi, serta satu set peralatan KLT (Kromatografi Lapis Tipis).
2. Bahan yang digunakan adalah :
Bahan yang diperlukan dalam penelitian ini adalah rimpang temu kunci
(Boesenbergia pandurata) , asam asetat glasial, kitosan, etanol teknis 96 %, etanol p.a Merck, NaTPP, akuades, kloroform.
D. Prosedur Penelitian
Prosedur penelitian mengenai pembuatan nanopartikel diuraikan sebagai berikut:
1. Pembuatan Ekstrak Etanol Temu Kunci (Boesenbergia pandurata) Proses ekstraksi herbal temu kunci dilakukan dengan cara : Temu kunci
27 2. Evaporasi
Filtrat yang diperoleh dipekatkan dengan rotary evaporator untuk menguapkan pelarut dan mendapatkan ekstrak etanol temu kunci (Boesenbergia
pandurata) yang lebih pekat. Suhu saat evaporasi di bawah titik didih pelarut yaitu 60oC.
3. Pembuatan Nanopartikel Kitosan-Ekstrak Etanol Temu Kunci (Boesenbergia pandurata)
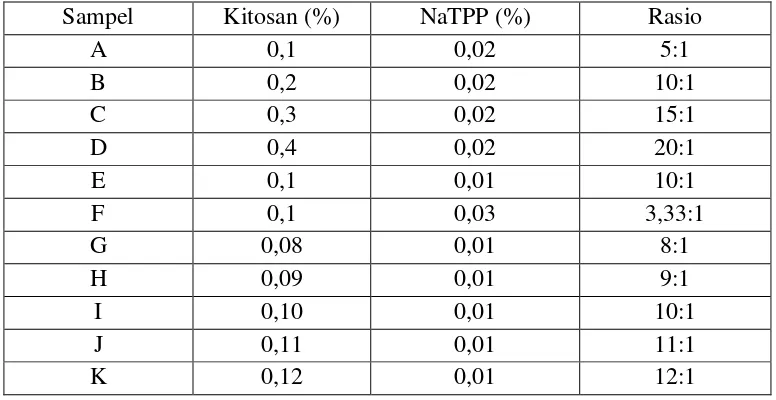
[image:43.595.118.506.554.754.2]Pembuatan nanopartikel kitosan - ekstrak herbal temu kunci, dilakukan dengan menimbang 1 gram ekstrak herbal temu kunci dalam botol flakon. Ekstrak temu kunci kemudian dilarutkan dalam 35 mL etanol p.a dicampur dengan 15 mL akuades dalam gelas beker 2000 mL, kemudian ditambahkan dengan 100 mL larutan kitosan dalam larutan asam asetat glasial 1 %. Selanjutnya secara bertahap ke dalam campuran tersebut ditambahkan 350 mL NaTPP sambil disertai pengadukan pada kecepatan yang stabil selama 2 jam. Perbandingan konsentrasi kitosan dan NaTPP dalam (%) disajikan pada Tabel 1.
Tabel 1. Perbandingan Konsentrasi Kitosan dan NaTPP
Sampel Kitosan (%) NaTPP (%) Rasio
A 0,1 0,02 5:1
B 0,2 0,02 10:1
C 0,3 0,02 15:1
D 0,4 0,02 20:1
E 0,1 0,01 10:1
F 0,1 0,03 3,33:1
G 0,08 0,01 8:1
H 0,09 0,01 9:1
I 0,10 0,01 10:1
J 0,11 0,01 11:1
28
Setelah semua bahan tercampur, dilakukan pengadukan dengan magnetic stirrer selama kurang lebih 2 jam pada kecepatan yang stabil. Setiap variasi rasio kitosan dan NaTPP dilakukan pengulangan sebanyak 3 kali. Koloid nanopartikel kitosan dan NaTPP-temu kunci kemudian dipisahkan dengan cara sentrifugasi. Padatan nanopartikel ekstrak etanol dimasukkan dalam freezer dengan suhu ±-4oC selama 2 hari, kemudian penyimpanan dilanjutkan dalam lemari es dengan suhu ±3oC sampai menjadi padatan kering.
4. Karakterisasi Hasil Pembuatan Nanopartikel
29 E. Teknis Analisis Data
1. Analisis Kualitatif
Teknik analisis kualitatif yang digunakan dalam penelitian ini adalah dengan menggunakan SEM (Scanning Electron Microscopy) untuk mengetahui struktur tiga dimensi dari nanopartikel yang dihasilkan dan KLT (Kromatografi Lapis Tipis) untuk mengetahui komponen senyawa yang terdapat dalam bentuk sediaan nanopartikel dibandingkan dengan ekstrak etanol temu kunci.
2. Analisis Kuantitatif
Teknik analisis kuantitatif yang digunakan dalam penelitian ini adalah menggunakan PSA (Particle Size Analyzer). Instrumen PSA digunakan untuk mengetahui ukuran nanopartikel yang dihasilkan dan Zeta Sizer Nano Series
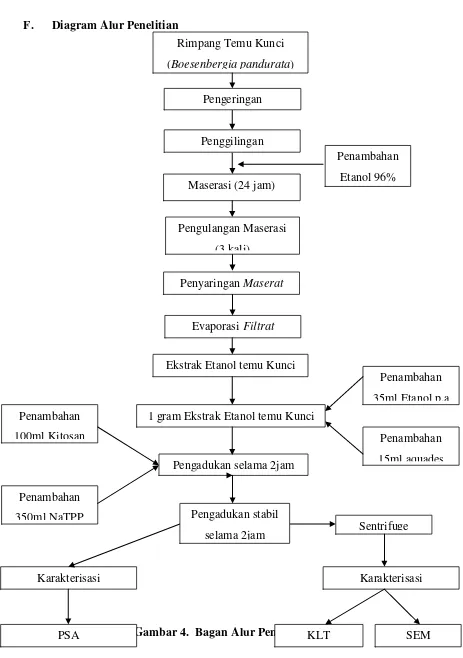
30 F. Diagram Alur Penelitian
Gambar 4. Bagan Alur Penelitian
Penambahan 35ml Etanol p.a
Penambahan 15ml aquades Penambahan 350ml NaTPP Penambahan 100ml Kitosan Karakterisasi PSA Sentrifuge Karakterisasi
KLT SEM
Penggilingan
Maserasi (24 jam)
Penambahan Etanol 96%
Penyaringan Maserat
Evaporasi Filtrat
Ekstrak Etanol temu Kunci
1 gram Ekstrak Etanol temu Kunci
Pengadukan selama 2jam
Pengadukan stabil selama 2jam Rimpang Temu Kunci (Boesenbergia pandurata)
Pengeringan
31 BAB IV
HASIL PENELITIAN DAN PEMBAHASAN
A. Hasil Penelitian 1. Hasil Ekstraksi
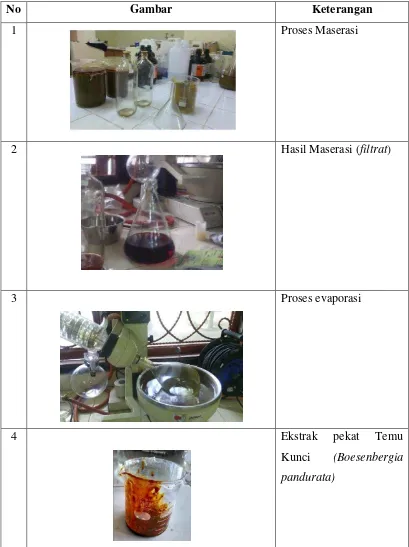
Ekstraksi dilakukan dengan metode maserasi menggunakan pelarut etanol 96%, filtrat (Gambar 5) yang didapatkan, selanjutnya diuapkan menghasilkan ekstrak pekat berwarna cokelat tua (Gambar 6). Rimpang temu kunci basah seberat 10 kg setelah dikeringkan dan digiling menjadi serbuk seberat 3 kg. Ekstrak kental hasil maserasi seberat 47,621 gram. Rendemen dapat dihitung dari serbuk temu kunci dan ekstrak kental temu kunci yaitu sebesar 1,587%.
Rendemen =
[image:47.595.128.485.385.657.2]%
Gambar 5. Filtrat Ekstrak Etanol Temu
32 2. Data Hasil PSA dan Zeta Sizer
[image:48.595.343.476.312.431.2]Berdasarkan prosedur kerja yang telah dilakukan, pembuatan koloid nanopartikel menghasilkan warna koloid kuning yang disajikan pada Gambar 7. Adapun endapan hasil sentrifuge koloid nanopartukel saat basah berwarna kuning dengan tekstur seperti bubur, yang disajikan pada Gambar 8. dan setelah kering berbentuk gumpalan padat berwarna cokelat kekuningan seperti yang disajikan pada Gambar 9.
Gambar 7. Koloid Nanopartikel Gambar 8. Endapan Basah Nanopartikel
Gambar 9. Endapan Kering Nanopartikel
[image:48.595.137.316.320.424.2] [image:48.595.231.395.478.598.2]33
1,9% adalah 1005 nm. Nilai zeta potensial rata-rata untuk sampel G adalah 41,87 mV.
[image:49.595.119.514.361.583.2]Persentase nanopartikel yang paling kecil adalah sebesar 0%. Persentase tersebut terdapat pada sampel C dan F. Sebelas sampel yang diukur ukuran partikelnya dapat dilihat secara lengkap pada Lampiran 6. Data nilai zeta potensial secara lengkap dapat dilihat pada Lampiran 7. Rangkuman persentase nanopartikel dan nilai zeta potensial pada masing-masing sampel dapat dilihat pada Tabel 2.
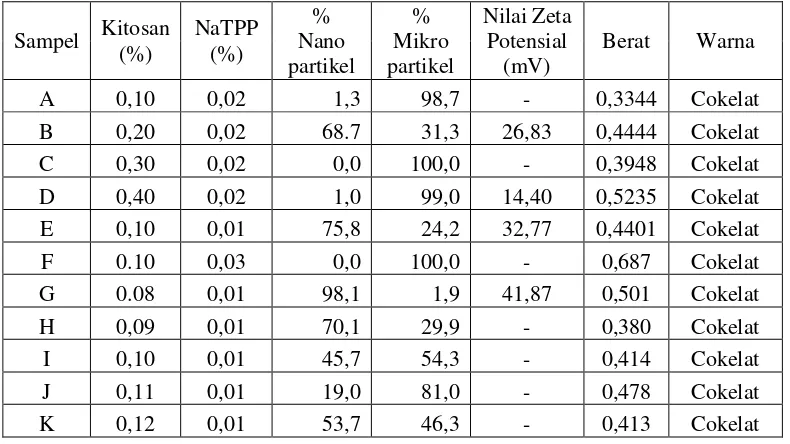
Tabel 2. Hasil Pengukuran Prosentase Nanopartikel dan Zeta Potensial
Sampel Kitosan (%) NaTPP (%) Nano % partikel % Mikro partikel Nilai Zeta Potensial
(mV) Berat Warna
A 0,10 0,02 1,3 98,7 - 0,3344 Cokelat
B 0,20 0,02 68.7 31,3 26,83 0,4444 Cokelat
C 0,30 0,02 0,0 100,0 - 0,3948 Cokelat
D 0,40 0,02 1,0 99,0 14,40 0,5235 Cokelat
E 0,10 0,01 75,8 24,2 32,77 0,4401 Cokelat
F 0.10 0,03 0,0 100,0 - 0,687 Cokelat
G 0.08 0,01 98,1 1,9 41,87 0,501 Cokelat
H 0,09 0,01 70,1 29,9 - 0,380 Cokelat
I 0,10 0,01 45,7 54,3 - 0,414 Cokelat
J 0,11 0,01 19,0 81,0 - 0,478 Cokelat
K 0,12 0,01 53,7 46,3 - 0,413 Cokelat
3. Data Hasil SEM (Scanning Electron Microscopy)
34
dihasilkan. Analisis SEM yang telah dilakukan pada sampel G pada perbesaran 100x – 5000x dapat dilihat pada Gambar 10(a) dan Gambar 10(b).
(a) (b)
Gambar 10. Hasil SEM Sampel G dengan perbesaran 5000x tampak samping (a) dan tampak atas (b)
Morfologi permukaan padatan nanopartikel yang dilakukan karakterisasi menggunakan instrumen SEM adalah seperti bentuk stalaktit atau stalakmit pada goa jika dilihat dari posisi samping (Gambar 10(a)) atau menunjukkan morfologi permukaan yang tidak rata (Gambar 10(b)).
4. Hasil Kromatografi Lapis Tipis (KLT)
[image:50.595.127.503.166.295.2]Hasil karakterisasi dengan Kromatografi Lapis Tipis (KLT) menggunakan plat silika gel ditunjukkan pada Gambar 11. Data hasil KLT diperoleh Rf A = 0,25 dan 0,60; Rf B = 0,23 dan 0,58; Rf C = 0,22 dan 0,57; Rf D = 0,22 dan 0,57; Rf E 0,23 dan 0,58; Rf F = 0,30 dan 0,63. Eluen yang digunakan adalah kloroform.
Gambar 11. Kromatogram Hasil KLT
Keterangan:
A = ekstrak temu kunci B = sampel G
35 B. Pembahasan
Tujuan dari penelitian ini adalah membuat nanopartikel dari ekstrak etanol rimpang temu kunci (Boesenbergia pandurata) pada berbagai varisi komposisi konsentrasi kitosan dan NaTPP (Natrium tripolifosfat) dengan persen (%) terbentuknya partikel dalam ukuran nano yang paling besar. Klarifikasi kebenaran rimpang temu kunci yang digunakan dilakukan dengan cara identifikasi terlebih dahulu rimpang temu kunci yang akan digunakan sebelum dilakukan penelitian lebih lanjut, surat keterangan identifikasi rimpang temu kunci yang digunakan dapat dilihat pada Lampiran 5. menunjukkan bahwa rimpang temu kunci yang digunakan adalah benar. Ukuran partikel dapat diketahui menggunakan instrumen PSA (Particle Size Analyzer) HORIBA LB-550 (IK 03 TP 016). Untuk mengetahui nilai zeta potensial koloid nanopartikel menggunakan instrumen Zeta
Sizer Nano Series Malvem. Untuk mengetahui morfologi ekstrak temu kunci dalam ukuran nano, digunakan instrumen SEM (Scanning Electron Microscopy). Sedangkan untuk mengetahui kesamaan komponen senyawa yang terkandung dalam ekstrak etanol temu kunci dalam ukuran nano digunakan KLT (Kromatografi Lapis Tipis).
1. Ekstraksi Rimpang Temu Kunci (Boeenbergia pandurata) dengan Teknik Maserasi
36
serbuk rimpang temu kunci. Rangkaian proses ini dimaksudkan agar senyawa metabolit sekunder yang terkandung dalam rimpang temu kunci dapat terlarut sempurna nantinya ketika direndam menggunakan pelarut yang digunakan. Sepuluh kilogram rimpang temu kunci basah didapatkan 3 kg serbuk rimpang temu kunci. Serbuk temu kunci kemudian ditempatkan pada gelas beker berukuran 2000 mL. Selanjutnya ke dalam gelas beker tersebut ditambahkan etanol teknis 96 % hingga seluruh serbuk temu kunci terendam. Perendaman dilakukan selama ±24 jam dan dilakukan pengulangan sebanyak 3 kali dengan volume etanol ±4 L untuk satu kali maserasi. Maserat kemudian disaring, selanjutnya filtrat dievaporasi dengan tujuan untuk menguapkan pelarut yang digunakan sehingga didapatkan ekstrak pekat temu kunci. Ekstrak pekat yang didapatkan seberat 47,261 gram berwarna cokelat tua (Gambar 6).
2. Pembuatan Koloid Nanopartikel Ekstrak Etanol Temu Kunci
(Boesenbergia pandurata) dengan Karakterisasi Menggunakan PSA dan Zeta Sizer
37
mL larutan NaTPP sedikit demi sedikit sambil tetap diaduk sehingga terbentuk suspensi nanopartikel. Setelah semua larutan tercampur, pengadukan dilanjutkan selama ±2 jam dengan kecepatan yang stabil agar proses crosslinking berlangsung sempurna. Crosslinker polianion yang digunakan adalah natrium tripolifosfat (NaTPP) karena bersifat tidak toksik. Penggunaan kitosan pada pembuatan nanopartikel ini karena kitosan merupakan biomaterial yang memiliki sifat-sifat istimewa seperti mukoadhesif, biokompatibel, biodegradable, nontoksik, dan tingkat imonogenisitas yang rendah, serta dalam penggunannya sangat menjanjikan sebagai pembawa (carrier) pada sistem penghantaran obat. Bentuk kitosan dalam ukuran nano juga sangat menjanjikan untuk meningkatkan bioavailabilitas biomolekul, karena memiliki kemampuan difusi dan penetrasi yang lebih baik ke dalam lapisan mukus. Proses pembentukan partikel menggunkan metode gelasi ionik. Metode ini dipilih dikarenakan prosesnya yang sederhana, tidak menggunakan pelarut organik, dan dapat dikontrol dengan mudah. Pembentukan partikel terjadi akibat adanya interaksi ionik antara gugus amino pada kitosan yang bermuatan positif dengan polianion yang bermuatan negatif membentuk struktur network inter- dan/atau intramolekul tiga dimensi.
38
banyak terdapat pada sampel G yakni sebanyak 98,1% dengan rentang ukuran 389-877 nm (Lampiran 6 sampel G).
Partikel dalam bentuk nano sebanyak 98,1% pada sampel G berukuran <1000 nm sehingga dapat dilanjutkan pengujian menggunakan Zeta Sizer Nano
Series Malvem untuk mengetahui nilai zeta potensialnya. Rerata nilai zeta potensial pada sampel G adalah 41,87 mV (Lampiran 7 sampel G). Nilai zeta potensial menunjukkan kestabilan nanopartikel yang terbentuk. Pengukuran dengan menggunakan Zeta Sizer hanya dilakukan pada 5 sampel yakni sampel A dengan nilai rerata zeta potensial sebesar 19,17 mV dan persen (%) partikel berukuran nano sebanyak 1,3%. Sampel B dengan nilai rerata zeta potensial sebesar 26,83 mV dan persen (%) partikel berukuran nano sebanyak 68,7%. Sampel D dengan nilai rerata zeta potensial sebesar 14,4 mV dan persen (%) partikel berukuran nano sebanyak 1%. Sampel E dengan nilai rerata zeta potensial sebesar 32,77 mV dan persen (%) partikel berukuran nano sebanyak 75,8% dan sampel A dengan nilai rerata zeta potensial sebesar 41,87 mV dan persen (%) partikel berukuran nano sebanyak 98,1%. Dari kelima sampel yang diukur nilai zeta potensialnya dapat dilihat bahwa semakin kecil (%) nanopartikel yang terbentuk, maka akan memiliki nilai zeta potensial yang kecil pula. Untuk itu, jika hasil pengukuran partikel dengan PSA didapatkan persen (%) nanopartikel kecil maka pengukuran zeta potensial tidak akan dilakukan karena sudah dapat dipastikan nilainya akan kecil.
39
standar yang menentukan keoptimalan komposisi yakni persen jumlah nano yang terdapat pada koloidnya menunjukkan ukuran partikel pada rentang 389-877 nm sebanyak 98,1% yang artinya hampir seluruh partikel dalam keadaan koloid memiliki ukuran nano, hanya sekitar 1,9 % saja yang memiliki ukuran >1000nm (termasuk dalam kategori mikromolekul). Pada sampel G juga menunjukkan hasil yang bagus dalam pengukuran menggunakan instrumen Zeta Sizer, nilai zeta potensial pada sampel G adalah 41,87 mV. Nilai zeta potensial menunjukkan nilai yang cukup tinggi dibandingkan dengan nilai minimal zeta potensial untuk menetapkan nanopartikel dikatakan stabil yakni >30 mV, sehingga dengan nilai zeta potensial sebesar 41,87mV dapat dikatakan sampel G merupakan koloid nanopartikel yang stabil.
40
3. Endapan dalam Koloid dan Karakterisasi menggunakan SEM
Endapan terlarut dalam koloid nanopartikel dipisahkan endapannya dengan cara sentrifugasi (pemusingan) menggunakan alat Sentrifuge merk Kokusan. Pemusingan dilakukan selama ±15 menit dengan kecepatan 3500 rpm. Endapan yang didapatkan berwarna kuning cerah disimpan dalam freezer (±-4oC) selama ±2 hari, kemudian endapan dipindahkan dalam lemari es dengan suhu ±3oC hingga mengering. Endapan kering berwarna cokelat dengan struktur padat. Endapan tersebut kemudian dikarakterisasi menggunakan instrumen SEM untuk mengetahui morfologi permukaan ekstrak etanol temu kunci dalam sediaan nano.
Analisis dengan instrumen SEM (Scanning Electron Microscopy) hanya dilakukan pada sampel G dengan nilai persen (%) ukuran paertikel dalam bentuk nano yang paling banyak yaitu 98,1%. Foto SEM dilakukan pada perbesaran 100-5000 kali. Hasil foto SEM pada padatan ekstrak etanol temu kunci dalam sedian nanopartikel dapat dilihat dengan jelas morfologi pernukaannya serta ukuran partikelnya (Lampiran 8). Morfologi permukaan ekstrak etanol sediaan nanopartikel jika dilihat dari samping pada perbebesaran 5000x tampak seperti bentuk stalaktit atau stalakmit yang terdapat pada goa (morfologi permukaannya tidak rata).
4. Hasil Identifikasi dengan Kromatografi Lapis Tipis (KLT)
41
Analisis dengan KLT ini dimulai dengan menyiapkan sampel terlebih dahulu. Sampel yang dianalisis menggunakan KLT ini adalah ekstrak etanol temu kunci, G, H, I, J, dan K. Pelarut yang digunakan adalah etanol p.a. Sampel yang telah larut kemudian ditotolkan pada plat KLT yang telah disiapkan dengan jarak penotolan setiap sample adalah 1 cm dengan tujuan agar saat proses elusidasi tidak terjadi percampuran noda. Selanjutnya plat dimasukkan dalam chamber yang bersisi eluen (fasa gerak). Eluen yang digunakan adalah kloroform. Kloroform digunakan karena memiliki tingkat polaritas yang rendah sehingga diharapkan sampel lebih terikat pada fasa diam.
42 BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Berdasarkan penelitian yang telah dilakukan, dapat disimpulkan bahwa :
1. Nanopartikel ekstrak etanol temu kunci (Boesenbergia pandurata) dengan kitosan dan NaTPP pada berbagai variasi komposisi berhasil dibuat dengan 9 variasi komposisi. Komposisi kitosan dan NaTPP untuk membentuk nanopartikel yang optimal adalah komposisi pada sampel G dengan konsentrasi kitosan dalam asam asetat glasial 0,08% dan konsentrasi NaTPP 0,01%.
2. Hasil karakterisasi komposisi yang optimal menggunakan PSA adalah partikel berukuran nano pada rentang diameter 389-877 nm sebanyak 98,1%. Karakterisasi menggunakan Zeta Sizer menghasilkan nilai rerata zeta potensial 41,87 mV, karakterisasi menggunakan instrumen SEM menunjukkan morfologi permukaan ekstrak etanol temu kunci dalam bentuk nanopartikel tidak rata, sedangkan hasil karakterisasi menggunakan KLT menunjukkan adanya kandungan senyawa yang sama baik dalam bentuk ekstrak etanol maupun sediaan nanopartikelnya.
B. Saran
Berdasarkan penelitian yang telah dilakukan, penulis memberikan sran sebagai berikut :
43
44
DAFTAR PUSTAKA
Agnihotri SA, Nadagounda N, Mallikarjuna, Tejraj M, Aminabhavi. (2004). Recent advances on chitosan based micro and nanoparticles in drug delivery. J.Control. Release, 2004;100:5-28
Agus Chahyadi, dkk.(2014). Boesenbergia pandurata Roxb., An Indonesian Medical Plant: Phytochemistry, Biological Activity, Plant Biotechnology. Procedia Chemistry 13 ( 2014 ) 13 – 37.
Akhtar, F., Rizvi, M. M., dan Kar, S. K. (2012). Oral Delivery of Curcumin Bound to Chitosan nanoparticles Cured Plasmodium yoelii Infected Mice. Biotechnology Advances. Vol 30 No. 1. Hlmn 310-320.
Ching, A. Y. L. et al. (2007). Characterization of Flavonoid Derivates from Boesenbergia rotunda (L.). The Malaysian Journal of Analitycal Science. Vol. 11 No.1. 154-159.
Dustgani, A., Farahani, E.V., and Imani, M. (2008). Preparation of Chitosan Nanopartikel Loaded by Dexamethasone Sodium Phosphate. Iranian J. of Pharmaceutical Science 4 (2): 111–114.
Elin, Y. S., Nethiyakalyani, S., Irda, F. (2014). Activity of Kaemferia pandurata (Roxb.) Rhizome Ethanol Extract Against MRSA, MRCNS, MSSA, Bacillus subtilis, and Salmonella typhi. Pakistan Journal of Biological Sciences. Vol.17 No.1. 49-55
Erdawati, (2008). Kapasitas adsorpsi kitosan dan nanomagnetik kitosan terhadap ion Ni (II). Prosiding, Seminar Nasional Sains dan Teknologi II, Universitas Lampung, 17–18 November 2008. (3): 248–256.
Eriawan Rismana, dkk. (2013). Sintesis dan Karakterisasi Nanopartikel Kitosan-Ekstrak Kulit Buah Manggis (Garcinia mangostana). Serpong: Pusat Teknologi farmasi dan Medika. Badan Pengkajian dan Penerapan Teknologi. Hlm.189-196.
Eriawan Rismana, dkk. (2014). Pengujian Aktivitas Antiacne Nanopartikel Kitosan-Ekstrak Kulit Buah Manggis (Garcinia mangostana). Serpong: Pusat Teknologi farmasi dan Medika. Badan Pengkajian dan Penerapan Teknologi. Media Litbangkes Vol.24 No.1. Hlmn 19-27.
Etik Mardliyati, et al. (2012). Preparasi dan Aplikasi Nanopartikel Kitosan sebagai Sistem Penghantaran Insulin Secara Oral. Prosiding. InSINas 2012. Jakarta: BPPT.
45
Ionik: Pengaruh Konsentrasi dan Rasio Volume terhadap Karakteristik Partikel. Prosiding. Pertemuan Ilmiah Ilmu Pengetahuan dan teknologi Bahan 2012. Jakarta: Pusat Teknologi farmasi dan Medika-BPPT.
Fernandez, B. R. (2012). Sintesis Nanopartikel SiO2 Menggunakan metode Sol-Gel dan Aplikasinya terhadap Aktivitas Sitotoksik Sel. Review Jurnal Nanoteknologi. Padang: Program Pasca Sarjana Universitas andalas. Hardjono Sastrohamidjojo. (1995). Sintesis Bahan Alam. Yogyakarta: Gadjah
Mada University Press.
Hardjono Sastrohamidjojo. (2001). Kromatografi Edisi Kedua. Yogyakarta: Liberty.
Hargono, D. (2000). Obat Analgetik dan antiinflamasi Nabati. Majalah Cermin Dunia Kedokteran Penyakit Sendi. No.120. 36-38.
Hari, E. I. dan Ijah, M. (2011). Proses dan Aplikasi Nanopartikel Kitosan sebagai Penghantar Obat. Squalen. Vol.6 No.1 Mei 2011 1-8.
Jahanshahi, M. dan Babaei, Z., (2008). Protein Nanopartikel: A Unique system as Drug Delivery Vehicle. J.Biotechnology. Vol.7 (25). 4926-4934.
Kirana, C., Jones, G.P., Record, I.R., and McIntosh, G.H. (2006) Anticancer Properties of Panduratin A Isolated from Boesenbergia Pandurata (Zingiberaceae). Journal of Natural Medicine. 61:131-137.
Kun Tanti Dewandari, Sri Yuliani, dan Sedarnawati Yasni. (2013). Ekstraksi dan Karakterisasi Nanopartikel Ekstrak Sirih Merah (Piper croatum). Journal Pascapanen. Vol 10 No. 2. Hlmn 58-65.
Mariska, S.H., Kuswandi, Susi, I. (2011). Daya Antibakteri Fraksi Etanol Temu Kunci (Boesenbergia pandurata) terhadap Salmonella typhi dan Streptococcus hemolityc α non pneumoniae. Pharmacon. Vol. 12 No. 2. 65-68.
Mery, T. D. A., Sri, S. S., Adolf, J. N. P. (2008). Potensi Ekstrak Temu Kunci (Boesenbergia pandurata) sebagai pengawet alami Ikan Kembung. Jurnal Ilmu dan Teknologi Pangan. Vol.6 No. 1. 41-57.
Mulyadi Tanjung, Tjitjik Srie Tjahjandarie, Mulya Hadi Sentosa. (2013). Antioxidant and Cytotoxic Agent from the Rhizomes of Kaempferia pandurata. Asian Pacific Journal of Tropical Disease. 3(5); 401-404. Nakorn, P.N. (2008). Chitin Nanowhisker and Chitosan Nanoparticles in Protein
46
Nirbuano, Buya. (2014). Temu Kunci dan Manfaatnya bagi Tubuh / Key Gathering and benefits for the body. diakses dari
http://buyanada.blogspot.co.id/2014/05/temu-kunci-dan-manfaatnya-bagi-tubuh.html pada tanggal 08 Agustus 2016, Jam 10.03 WIB.
Nisa’, Khoirun. (2013). Manfaat Temu Kunci bagi Kesehatan tubuh. diakses dari
http://www.tanamanobat.net/manfaat-temu-kunci-bagi-kesehatan-tubuh/ . pada tanggal 08 Agustus 2016, Jam 10.08 WIB.
Ochtavia Prima Sari dan Titik Taufiqurrohmah. (2006). Isolation and Identification of Flavonoid Compound Extractire Ethyl Acetate Fraction Extracted from The Rhizomes Fingerroot of (Boesenbergia pandurata (Roxb.) Schlecht) (Zingiberaceae). Indo. J.Chem 6 (2). 219-223.
Oka Adi Parwata. (2012). Isolasi dan Identifikasi 5-hidroksi-7-metoksi flavanon (Pinostrobin) pada Ekstrak n-Heksana Rimpang Temu Kunci (Kaempferia pandurata Roxb). Prosiding. Seminar Nasional UNESA. Denpasar Bali: FMIPA Universitas Udayana.
Pipih Suptijah, Agoes M. Jacoeb, & Desie Rachmania. (2011). Karakterisasi Nano Kitosan Cangkang Udang Vannamei (Litopenaeus vannamei) dengan Metode Gelasi Ionik. Jurnal Pengolahan Hasil Perikanan Indonesia. Volume XIV Nomor 2 Tahun 2011: 78-84.
Plantus. (2008). Fingerroot (Boesenbergia pandurata Roxb. Schult). Diakses dari http://anekaplanta.wordpress.com/2008/01/04/temu-kunci-boesenbergia-pandurata-roxb-schlechter/ . pada tanggal 15 Juni 2015.
Raditya Iswandana, Effionora Anwar, & Mahdi Jufri. (2013). Formulasi Nanopartikel Verapamil Hidroklorida dari Kitosan dan Natrium Tripolifosfat dengan Metode Gelasi Ionik. Jurnal Farmasi Indonesia. Vol.No.4.
Rauhatun Napsah dan Iis Wahyuningsih. (2013). Preparasi Nanopartikel Kitosan-TPP/ Ekstrak Etanol Daging Buah Mahkota Dewa (Phaleriamacrocarpa (Scheff) Boerl) dengan Metode Gelasi Ionik. Yogyakarta: Jurnal Farmasi Sains dan Komunitas, Vol. 11 No.1, Mei 2014, hlm.7-12. ISSN : 1693-5683.
Rawat, M., Singh, D., Saraf, S. (2006). Nanocarriers: Promising Vehicle for Bioactive Drugs. Biol Pharm Bull. 29(9). 1790-1798.
47
Ronny Martien, dkk (2012). Perkembangan Teknologi Nanopartikel sebagai Sistem Penghantaran Obat. Majalah Farmaseutik. Vol.8 No.1 Tahun 2012. Hlm 133-144.
Rowe, R.C. (2009). Handbook of Pharmaceutical excipient 6th ed. London. The Pharmaceutical Press. 159-161.
Siregar, M. (2009). Pengaruh Berat Molekul Kitosan Nanopartikel untuk Menurunkan Kadar Logam Besi(Fe) dan Zat Warna pada Limbah Industri Tekstil Jeans. Tesis. Sekolah Pascasarjana. Universitas Sumatera Utara. Medan.
Sohn, J.H., Han, K.L., Lee, S.H., and Hwang, J.K.. (2005). Protective Effects of Panduratin Against Oxidative Damage of tert-Butylhydroperoxide in Human HepG2 Cells, Biological and Pharmaceutical Bulletin. 28(6):1083-1086.
Sri Atun dan Retno Arianingrum. (2015). Synthesis Nanoparticles of Chloroform Fraction from Kaempheria rotinda Rhizome Loaded Chitosan and Biological Activity as an Antioxidant. International Journal of Drug Delivery Technology (5(4)). Hlmn.138-142.
Stevens, Malcolm P. (2001). Polymer Chemistry: An Introduction. Oxford University Press. Diterjemahkan oleh Iis Sopyan. (2001). Kimia Polimer. Jakarta : PT Pradnya Paramita.
Sudjadi. (2008). Metode Pemisahan. Yogyakarta : UGM Press
Tatang Wahyudi, Doni Sugiyana, Qomarudin Helmy. (2011). Sistesis Nanopartikel Perak dan Uji Aktivitasnya terhadap Bakteri E.Coli dan S.aureus. Balai Besar Tekstil : Bandung.
Tiyaboonchai, Waree. (2003). Chitosan nanoparticles: Apromising system for drug delivery. Naresuan University Journal 11 (3): 51–66.
Trankoontivakorn, G., Nakahara, K., Shinmoto, H., Takenaka, M., Kameyama, M.O., Ono, H., Yoshida, H.M., Nagata, T., and Tsushida, T., (2001). Structural Analysis of a Novel Antimutagenic Activity of Flavonoids in Thai Spice, Fingerroot (Boesenbergia pandurata Schult.) Against Mutagenic Heterocyclic Amines, J. Agric. Food. Chem, 49(6):3046-3050. Tuchinda, P., et al. (2002). Anti-inflammatory Cyclohexenyl Chalcone Derivates
in Boesenbergia pandurata. Phytochemistry, 59. 169-173
48
Wu, Y., Wuli Yang, Changchun W., Jianhua H., Shoukuan Fu. (2005). Chitosan Nanoparticles as a Novel Delivery System for Ammonium Glycyrrhizinate. International Journal of Pharmaceutics 295: 235-245. Yun, J.M., Kweon, M.H., Kwon, H.J., Hwang, J.K., and Mukhtar, H., (2006).
Induction of Apoptosis and Cell Cycle Arrest by a Chalcone Panduratin A Isolated from Kaempferia pandurata in Androgen-Independent Human Prostate Cancer Cells PC3 and DU145. Carcinogenesis Advance Access. 27(7):1454-1464.
Yu-Shin, L., Kiran, S., Kurt, M.L., Jyuhn, H.J., Long, F., Han, Y., Hsing, W.S. (2008). Multi-ion-crosslinked Nanoparticles with pH-responsive Characteristic for Oral Delivery of Protein Drugs. J. Cont Rel. 132, 141-149.
49 Lampiran 1
Perhitungan Jumlah Bahan
Berdasarkan variasi komposisi Kitosan dan NaTPP pada Tabel 1 dapat dihitung jumlah bahan yang diperlukan. Untuk Kitosan pada setiap variasi yang tertera sama dengan gram per 100 mL asam asetat glasial 1 % (1 mL asam asetat glasial dalam 100 mL labu ukur kemudian ditambahkan akuades hingga batas) dan untuk NaTPP sama dengan gram per 100 mL akuades. Setiap variasi komposisi membutuhkan 100 mL Kitosan dan 350 mL NaTPP.
a. Sampel A
Kitosan 0,1% = 0,1 gram x 3 (3 kali pengulangan) = 0,3 gram
NaTPP 0,02% = 0,02 gram x 11 (untuk 3 kali pengulangan @350 mL) = 0,22 gram
b. Sampel B
Kitosan 0,2% = 0,2 gram x 3 (3 kali pengulangan) = 0,6 gram
NaTPP 0,02% = 0,02 gram x 11 (untuk 3 kali pengulangan @350 mL) = 0,22 gram
c. Sampel C
Kitosan 0,3% = 0,3 gram x 3 (3 kali pengulangan) = 0,9 gram
50 d. Sampel D
Kitosan 0,4% = 0,4 gram x 3 (3 kali pengulangan) = 1,2 gram
NaTPP 0,02% = 0,02 gram x 11 (untuk 3 kali pengulan