TESIS
PEMBERIAN INJEKSI TESTOSTERON
MENGHAMBAT KERUSAKAN SEL BETA
PANKREAS DAN MENURUNKAN KADAR GULA
DARAH TIKUS WISTAR JANTAN OBESITAS
DENGAN DIABETES MELITUS
ASTRID KARINA DANUMIHARDJO
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
TESIS
PEMBERIAN INJEKSI TESTOSTERON
MENGHAMBAT KERUSAKAN SEL BETA
PANKREAS DAN MENURUNKAN KADAR GULA
DARAH TIKUS WISTAR JANTAN OBESITAS
DENGAN DIABETES MELITUS
ASTRID KARINA DANUMIHARDJO NIM 1490761007
PROGRAM MAGISTER
PROGRAM STUDI ILMU BIOMEDIK
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
DENPASAR
PEMBERIAN INJEKSI TESTOSTERON
MENGHAMBAT KERUSAKAN SEL BETA
PANKREAS DAN MENURUNKAN KADAR GULA
DARAH TIKUS WISTAR JANTAN OBESITAS
DENGAN DIABETES MELITUS
Tesis untuk Memperoleh Gelar Magister pada Program Magister, Program Studi Ilmu Biomedik, Program Pascasarjana Universitas Udayana
ASTRID KARINA DANUMIHARDJO NIM 1490761007
PROGRAM MAGISTER
PROGRAM STUDI ILMU BIOMEDIK
PROGRAM PASCASARJANA
UNIVERSITAS UDAYANA
DENPASAR
Lembar Pengesahan
TESIS INI TELAH DISETUJUI TANGGAL 02 JUNI 2016
Pembimbing I, Pembimbing II,
Mengetahui,
Ketua Program Ilmu Biomedik Direktur
Program Pascasarjana Program Pascasarjana Universitas Udayana, Universitas Udayana,
Prof.Dr.dr.Wimpie I. Pangkahila, Sp.And, FAACS NIP. 194606191976021001
Prof.Dr.dr.A.A.Gede Budhiarta, Sp.PD-KEMD NIP. 194412211972061001
Dr. dr. Gde Ngurah Indraguna Pinatih, M.Sc, Sp.GK NIP.195805211985031002
Tesis ini Telah Diuji dan Dinilai oleh Panitia Penguji pada Program Pascasarjana Universitas Udayana
Pada Tanggal ………
Berdasarkan SK Rektor Universitas Udayana No. : ………
Tanggal ………
Panitia Penguji Tesis
Ketua : Prof.Dr.dr. Wimpie I. Pangkahila, Sp.And, FAACS Sekretaris : Prof.Dr.dr. A.A. Gede Budhiarta, Sp.PD-KEMD Anggota :
1. Prof. dr. IGM. Aman, Sp.FK
SURAT PERNYATAAN BEBAS PLAGIAT
Nama : dr. Astrid Karina Danumihardjo NIM : 1490761007
Program Studi : Magister Ilmu Biomedik (Anti Aging Medicine)
Judul : Pemberian Injeksi Testosteron Menghambat Kerusakan Sel Beta Pankreas dan Menurunkan Kadar Glukosa Darah Tikus Wistar Jantan Obesitas dengan Diabetes Melitus
Dengan ini menyatakan bahwa karya ilmiah tesis ini bebas plagiat.
Apabila di kemudian hari terbukti terdapat plagiat dalam karya ilmiah ini, maka saya bersedia menerima sanksi sesuai dengan peraturan Mendiknas RI No.17 tahun 2010 dan Peraturan Perundang-undangan yang berlaku.
Denpasar. 16 Mei 2016 Yang membuat pernyataan,
UCAPAN TERIMA KASIH
Puji dan syukur ke hadapan Tuhan Yang Maha Esa penulis haturkan karena hanya atas berkat dan rahmat-Nya tesis yang berjudul PEMBERIAN INJEKSI TESTOSTERON MENGHAMBAT KERUSAKAN SEL BETA PANKREAS DAN MENURUNKAN KADAR GLUKOSA DARAH TIKUS WISTAR JANTAN OBESITAS DENGAN DIABETES MELITUS ini dapat terselesaikan dengan baik..
Dalam menjalani pendidikan dan penelitian ini banyak pelajaran dan pengalaman tak ternilai yang didapat yang semakin membuka wawasan dan menjadi pembelajaran hidup bagi penulis. Semua ini tentunya adalah peran serta orang-orang disekeliling penulis yang senantiasa mendukung dan menyertai selama perjalanan ini. Penulis menyadari bahwa tesis ini bisa terselesaikan berkat bimbingan dan dukungan dari berbagai pihak, maka perkenankan penulis untuk menghaturkan ucapan terima kasih yang sebesar-besarnya kepada:
1. Rektor Universitas Udayana Prof. Dr. dr. Ketut Suastika, Sp.PD. KEMD dan Direktur Program Pascasarjana Prof. Dr. A. A. Raka Sudewi, Sp.S(K) atas kesempatan yang diberikan kepada penulis untuk menempuh pendidikan Program Pascasarjana di UniversitasUdayana
2. Dr. dr. Gde Ngurah Indraguna Pinatih, M.Sc., Sp.GK sebagai ketua Program Studi Biomedik yang telah mendukung penyusunan tesis ini 3. Prof. Dr. dr. Wimpie I. Pangkahila, Sp. And, FAACS, sebagai
membimbing penulis, memberikan saran- saran ilmiah dan masukan yang sangat bermanfaat selama penyusunan tesis ini
4. Prof. Dr. dr. A.A. Gede Budhiarta, Sp.PD-KEMD, sebagai pembimbing II, yang telah meluangkan waktu membimbing penulis dengan baik dan perhatian, memberikan saran-saran ilmiah, dan masukan yang sangat bermanfaat dalam penyusunan tesis ini
5. Prof. Dr. IGM Aman, Sp.FK, Dr. dr. A.A.A.N. Susraini, Sp.PA(K), dan Dr. dr. Ida Sri Iswari, Sp. MK., M.kes, sebagai penguji, yang dengan bijak dan sabar memberikan perhatian, koreksi dan masukan yang sangat teliti sehingga sangat bermanfaat dalam perbaikan tesis ini.
6. Seluruh dosen Pasca Sarjana Biomedik Universitas Udayana yang telah membimbing penulis dalam menempuh pendidikan dari awal hingga selesainya tesis ini
7. Seluruh staf Universitas Udayana khususnya Program Magister Ilmu Biomedik Kekhususan Anti-Aging Medicine yang selalu siap membantu penulis dalam menyelesaikan tesis ini. Terima kasih sebesar-besarnya kepada Pak Edy, Geg Wah, Geg Eni, Mbok Amie, Mbok Yethi, dan seluruh staf yang kebaikannya tiada terkira.
8. Ferbian Milas Siswanto, S.KH, sebagai staf Laboratorium Fakultas Kedokteran Hewan Universitas Udayana yang telah banyak membantu dalam hal teknis penelitian.
dalam proses pembuatan preparat histopatologi pankreas
11. Kedua orang tua, adik, suami, keluarga tercinta serta sahabat penulis yang selalu memberikan dukungan, semangat, doa serta pengertian selama penulis menempuh pendidikan hingga diselesaikannya tesis ini.
12. Teman sejawat mahasiswa Program Magister Ilmu Biomedik Kekhususan Anti-Aging Medicine Angkatan IX khususnya dr. Ivonne Kurniawan, dr. Magdalena Tjahyanto M.Biomed.(AAM), dr. Ellen Destrisa Ratnapuri M.Biomed.(AAM), dr. Astrid Tanumihardja, dr. Cheria Valentina M.Biomed.(AAM), dr. Monica Pranoto M.Biomed.(AAM), dr. Sissy Yunita, dan dr. Adeline Ivana Dewi sebagai sejawat dan sahabat yang berjuang bersama dan saling memberikan semangat satu sama lain sejak awal kuliah sampai selesainya tesis ini.
13. Semua pihak yang tidak dapat disebutkan satu per satu namun sangat berperan dalam penulisan tesis ini.
Akhir kata penulis sangat menyadari bahwa tesis ini masih sangat jauh dari kesempurnaan, sehingga saran dan masukan membangun dari berbagai pihak sangatlah diharapkan. Semoga hasil penelitian ini dapat memberikan manfaat bagi perkembangan ilmu pengetahuan kedokteran terutama di bidang Anti Aging Medicine (AAM). SemogaTuhan memberkati kita semua.
Denpasar, 02 Juni 2016
ABSTRAK
PEMBERIAN INJEKSI TESTOSTERON MENGHAMBAT KERUSAKAN SEL BETA PANKREAS DAN MENURUNKAN KADAR GULA DARAH TIKUS WISTAR JANTAN OBESITAS DENGAN DIABETES MELITUS
Salah satu gangguan kesehatan yang menjadi perhatian di berbagai belahan dunia saat ini adalah obesitas. Obesitas merupakan masalah kesehatan yang tidak hanya ditemui di negara maju, melainkan juga di negara berkembang dan membawa dampak sosio-ekonomi yang besar. Obesitas, terutama obesitas sentral, menyebabkan terjadinya resistensi insulin yang kemudian akan berlanjut menjadi diabetes melitus. Diabetes melitus merupakan suatu penyakit metabolik kronis yang ditandai dengan hiperglikemia, diakibatkan oleh adanya resistensi insulin dan atau inadekuatnya produksi insulin oleh sel beta. Pemberian terapi sulih hormon testosteron telah banyak digunakan pada kondisi obesitas, yang umumnya disertai dengan penurunan kadar testosteron plasma. Berdasarkan temuan pada beberapa penelitian lain, testosteron memiliki kemampuan anti-oksidatif dan mampu mencegah kerusakan sel beta yang disebabkan oleh radikal bebas, memberikan efek melalui reseptor androgen yang terletak pada sel. Tujuan dari penelitian ini adalah mengetahui pengaruh pemberian testosteron pada kondisi diabetes melitus yang disertai obesitas.
Penelitian ini adalah penelitian eksperimental dengan menggunakan post test only control group design. Sampel dari penelitian ini adalah 36 tikus wistar (Rattus norvegicus) jantan usia 9-12 bulan dengan kondisi obesitas dan diabetes yang diinduksi dengan injeksi STZ dan NAD. Sampel dibagi menjadi dua kelompok, dengan kelompok kontrol diberikan plasebo dan Metformin sedangkan kelompok perlakuan diberikan SUSTANON 250 (6,75 mg/300 gr BB) dan Metformin. Injeksi testosteron dilakukan sebanyak dua kali dengan jarak tiga minggu. Penelitian dilakukan selama 6 minggu dan pada akhir penelitian dilakukan pengamatan jumlah sel beta pankreas serta pemeriksaan kadar glukosa post prandial.
Pada akhir penelitian ini didapatkan skoring jumlah sel beta pada kelompok perlakuan sebesar 475,33 + 84,46 sedangkan pada kelompok kontrol sebesar 245,94 + 80,29. Pemeriksaan kadar glukosa post prandial pada kelompok perlakuan adalah 91,63 + 8,74 mg/dL sedangkan pada kelompok kontrol sebesar 102,12 + 11,09 mg/dL. Uji analisis komparasi yang dilakukan pada kedua data ini memberikan hasil p = 0,003 untuk kadar glukosa post prandial, dan p = 0,001 untuk skoring jumlah sel beta pankreas.
Kesimpulan yang dapat ditarik dari hasil penelitian ini adalah pemberian testosteron intramuskular terbukti dapat menghambat kerusakan sel beta pankreas dan menurunkan kadar glukosa post prandial tikus wistar obesitas dengan diabetes melitus.
ABSTRACT
TESTOSTERONE INJECTION ATTENUATES PANCREAS BETA CELL DAMAGE AND DECREASES PLASMA GLUCOSE LEVEL IN OBESE
MALE WISTAR RATS WITH DIABETES MELLITUS
One of the most outstanding health issues in the world recently is obesity, with high prevalence not only in developed countries but in developing countries as well. Along with the obvious health co-morbidities it causes, this metabolic condition also brings a heavy socio-economic burden. Obesity, in particular central obesity, will induce insulin resistance which may later develop into diabetes mellitus. Diabetes is a chronic metabolic disease marked by hyperglycemia, caused by insulin resistance and/or inadequate insulin production by the pancreatic beta cell. Testosterone hormonal replacement therapy is widely used for obesity, in which low testosterone plasma level is a common finding. Based on other researches, testosterone has been known to possess antioxidative properties and thus would be able to attenuate pancreatic beta cell damage caused by free radicals, an effect expressed from its bond with the androgenic receptors on the cell’s surface. The goal of this study was to establish the effect of testosterone therapy in diabetes mellitus with obesity.
This study was an experimental study using posttest only control group design. The sample used in this study was 36 obese male Wistar rats, age ranging between 9 – 12 months old with diabetes mellitus which was provoked by NAD and STZ injection. The samples were divided into two groups: the control group which was given placebo and metformin and the treatment group which received SUSTANON 250 (6,75 mg/300 gr bodyweight) and metformin. Testosterone injections were given twice in this study, the second dose was given three weeks after the first injection. This study was completed in 6 weeks and at the end of the study, histopathology examination of pancreatic beta cell and post prandial glucose level evaluation were performed.
The results showed the pancreas beta cells score for the treatment group were 475,33 + 84,46 while for the control group, the score were 245,94 + 80,29. Post prandial glucose level for the treatment group was 91,63 + 8,74 mg/dL while the control group level was 102,12 + 11,09 mg/dL. Comparability test that was done based on this data showed p = 0,003 for post prandial glucose level and p = 0,001 for pancreatic beta cell score.
Based on the results above, it can be concluded that intramuscular testosterone therapy was proven to attenuate pancreatic beta cell and decrease plasma glucose level in obese male Wistar rats with diabetes mellitus.
DAFTAR ISI
Halaman
SAMPUL DALAM………... i
LEMBAR PRASYARAT GELAR MAGISTER……… ii
LEMBAR PERSETUJUAN PEMBIMBING..……… iii
LEMBAR PENETAPAN PANITIA PENGUJI……….. iv
LEMBAR PERNYATAAN BEBAS PLAGIAT……… v
DAFTAR SINGKATAN DAN LAMBANG……….. xvi
β.γ.9 Penatalaksanaan Diabetes Melitus Tipe β………. 28
BAB III. KERANGKA BERPIKIR, KONSEP, DAN HIPOTESIS……… 52
4.7.5 Cara Pemeriksaan Kadar Glukosa Darah………... 72
4.8 Alur Penelitian……… 73
4.9 Analisis Data……… 74
BAB V. HASIL PENELITIAN……… 75
5.1 Analisis Deskriptif……… 75
5.β Uji Normalitas Data……… 76
5.γ Uji Homogenitas Data……… 76
5.4 Uji Komparabilitas Data………. 76
BAB VI. PEMBAHASAN PENELITIAN……… 82
6.1 Pengaruh Pemberian Testosteron terhadap Sel Beta Pankreas 82 6.2 Pengaruh Pemberian Testosteron terhadap Kadar Glukosa Post prandial……….……….. 85
BAB VII. SIMPULAN DAN SARAN……… 88
DAFTAR PUSTAKA………. 89
DAFTAR TABEL
Halaman
2.1 Kadar Glukosa Darah Sewaktu dan Puasa sebagai Patokan Penyaring
dan Diagnosa……….. 21
5.1 Hasil Analisa Deskriptif Skor Sel Beta Pankreas ……… 75 5.2 Hasil Analisa Deskriptif Kadar Glukosa Post prandial ……… 76 5.3 Perbedaan Rerata Skor Sel Beta Pankreas Antar Kelompok Setelah
Perlakuan……….………... 77
5.4 Perbedaan Rerata Kadar Glukosa Post prandial Jumlah Antar
DAFTAR GAMBAR
Halaman
2.1 Hipotesis Hipogonad –Obesitas……… 16
2.2 Hubungan Obesitas dengan Resistensi Insulin……….. 18
2.3 Proses Komplikasi pada Penderita Hiperglikemia………. 28
2.4 Mekanisme Kerja Insulin –Glukagon………... 33
2.5 Allred Scoring Guidelines……….. 36
2.6 Mekanisme Disfungsi Sel Beta Pankreas………... 37
2.7 Mekanisme Kerja Insulin………... 39
2.8 Regulasi Sekresi dan Sintesis Testosteron : Aksis Hipotalamus – Hipofisis –Testis………... 42
3.1 Konsep Penelitian……….. 54
4.1 Rancangan Penelitian………. 56
4.2 Hubungan Antar Variabel Bebas dan Terkendali……….. 66
4.3 Bagan Alur Penelitian……… 73
5.1 Grafik Perbandingan Rerata Skor Sel Beta Pankreas Setelah Perlakuan Antar Kelompok………. 78
5.2 Gambaran Histopatologi Sel Beta Pankreas Kelompok Kontrol (P0)….. 79
DAFTAR SINGKATAN
AAM = Anti Aging Medicine ANH = Atrial Natriuretic Hormone BMI = Body Mass Index
CDC = Centers for Disease Control and Prevention DHEA = Dehydroepiandrosterone
DHT = Dihydrotestosterone DM = Diabetes melitus DNA = Deoxyribonucleic acid
FFA = Free Fatty Acid
FSH = Follicle Stimulating Hormone
GH = Growth hormone
NAD = Nicotinamide adenine dinucleotide NADH = Nicotinamide Adenine Dehydrogenase
NO = Nitric oxide
OHO = Obat Hipoglikemik Oral PTH = Parathyroid Hormone Riskesdas = Riset Kesehatan Dasar ROS = Reactive oxygen species SHBG = Sex hormone binding globulin STZ = Streptozotocin
DAFTAR LAMBANG
DAFTAR LAMPIRAN
Halaman
1 Ethical Clearance………... 96
2 Tabel Konversi Perhitungan Dosis untuk Beberapa Jenis Hewan Coba dan Manusia……… 97
3 Hasil Pemeriksaan Kadar Glukosa Post-prandial………... 98
4 Analisis Data Kadar Glukosa Post-prandial………... 99
5 Hasil Pengamatan Sel Beta Pankreas……….. 101
1
BAB I
PENDAHULUAN
1.1Latar Belakang
Proses penuaan merupakan rangkaian proses yang terjadi secara alami setelah manusia mencapai usia dewasa di mana seluruh komponen tubuh berhenti berkembang dan mulai mengalami penurunan fungsi akibat ketidakmampuan jaringan untuk memperbaiki diri dari kerusakan yang terjadi. Proses penuaan yang terjadi pada seseorang dapat juga terjadi lebih awal, tidak sesuai dengan usia kronologisnya.
Yang menjadi perhatian saat ini adalah, walaupun penuaan pasti akan terjadi pada setiap manusia, didapatkan angka harapan hidup yang semakin meningkat dibandingkan dengan dekade sebelumnya. Berdasarkan hal tersebut, pada tahun 1993 dicetuskan konsep baru Anti Aging Medicine (AAM). Konsep ini terdiri dari 3 pemikiran yaitu pertama, konsep ini menganggap bahwa penuaan adalah suatu penyakit yang dapat dicegah, dihindari, dan diobati sehingga dapat berfungsi kembali ke keadaan semula. Kedua, manusia bukanlah orang hukuman yang pasrah terperangkap dalam takdir genetiknya. Ketiga, manusia mengalami keluhan atau gejala penuaan karena kadar hormonnya menurun, bukan kadar hormon menurun karena manusia menjadi tua (Pangkahila, 2011).
2
glikosilasi, metilasi, apoptosis, sistem kekebalan yang menurun dan genetik. Faktor eksternal yang utama ialah gaya hidup tidak sehat, diet tidak sehat, kebiasaan salah, polusi lingkungan, stres dan kemiskinan (Pangkahila, 2007).
Kerusakan yang terjadi dalam proses penuaan ini seringkali dipercepat atau diperberat dengan timbulnya penyakit-penyakit degeneratif dan gangguan medis tertentu. Salah satu masalah kesehatan yang seringkali dihubungkan dengan proses penuaan adalah obesitas. Obesitas saat ini telah menjadi suatu epidemi, masalah kesehatan global yang menjadi perhatian karena mengancam kesehatan secara umum dan menurunkan kualitas hidup seseorang, serta dapat menyebabkan penuaan dini bahkan kematian (Ahima, 2009).
Obesitas didefinisikan oleh WHO sebagai akumulasi lemak yang abnormal atau berlebihan yang berpeluang menimbulkan risiko kesehatan pada seorang individu. Hal ini menggambarkan bahwa obesitas disebabkan oleh adanya ketidakseimbangan antara asupan makanan dengan penggunaan energi oleh tubuh. Keseimbangan antara kedua hal tersebut sangat kompleks dan dipengaruhi juga oleh faktor metabolik dan hormonal dari masing-masing individu (Nurmalina, 2011).
3
lemak viseral (Saad dkk, 2012; Pergola, 2000). Suatu penelitian prospektif menunjukkan bahwa obesitas berhubungan erat dengan risiko kematian tanpa memandang jenis kelamin, etnik dan usia (Adams dkk., 2006). Sedikitnya setiap tahun 2,6 juta orang meninggal karena overweight atau obesitas (Bray, 2007).
Individu obesitas sebagian besar akan menunjukkan karakteristik dari sindrom metabolik, dengan salah satu komponen yang penting adalah resistensi insulin dan diabetes melitus. Prevalensi dari T2DM meningkat secara dramatis dalam kurun waktu terakhir ini, di mana berdasarkan laporan kasus didapatkan 6 juta penduduk Amerika menderita diabetes di tahun 1980 yang kemudian meningkat menjadi 15 juta di tahun 2004 dan saat ini menurut Centers for Disease Control and Prevention (CDC) sekitar 23 juta orang atau sekitar 8% dari total populasi orang di Amerika Serikat menderita diabetes (Traish dkk., 2009).
4
Diabetes melitus adalah suatu penyakit kronis, yang disebabkan akibat adanya kelainan metabolisme karbohidrat, di mana glukosa darah tidak dapat digunakan dengan baik dan menumpuk dalam sirkulasi darah karena pankreas tidak cukup memproduksi insulin untuk metabolisme glukosa darah dan tubuh yang tidak dapat secara efektif menggunakan insulin yang diproduksi tersebut, sehingga menyebabkan keadaan hiperglikemia (Wijaya dkk., 2011).
Keadaan hiperglikemia pada diabetes merupakan kombinasi dari resistensi insulin, sekresi insulin yang tidak adekuat, serta sekresi glukagon yang berlebihan. Sekresi insulin diperankan oleh sel beta dari pulau Langerhans dalam pankreas, sehingga apabila sekresi insulin tidak adekuat dapat dianggap sebagai gangguan dari sel beta pankreas. Sel beta pankreas mudah mengalami kerusakan ataupun apoptosis akibat adanya radikal bebas karena sel beta memiliki kapasitas antioksidatif yang rendah (Morimoto dkk., 2005).
5
Penelitian terdahulu juga menyimpulkan bahwa hormon androgen memiliki efek protektif terhadap kerusakan sel yang disebabkan oleh radikal bebas seperti reactive oxygen species (ROS) dan nitric oxide (NO). Pemberian hormon androgen eksternal yang dilakukan pada tikus yang dikastrasi menunjukkan penurunan pembentukan mega islet, yang merupakan suatu indikator awal dari kerusakan jaringan pankreas, dibandingkan dengan kelompok kontrol (Rosmalen dkk., 2001). Pemberian injeksi testosteron enanthate pada tikus yang mengalami kastrasi menunjukkan adanya penurunan indeks apoptosis sel beta pankreas melalui mekanisme yang kemungkinan dimediasi oleh reseptor androgen (Morimoto dkk., 2005). Berdasarkan penelitian-penelitian sebelumnya, maka dianggap kapasitas antioksidan yang dimiliki oleh hormon steroid khususnya hormon testosteron dapat menghambat kerusakan yang terjadi pada sel beta pankreas pada kondisi diabetes mellitus (Morimoto dkk., 2005; Hanchang dkk., 2013).
1.2 Rumusan Masalah
Berdasarkan atas latar belakang yang sudah dijabarkan, maka dirumuskan rumusan masalah sebagai berikut:
1.2.1 Apakah pemberian injeksi testosteron dapat menghambat kerusakan sel beta pankreas pada tikus wistar jantan obesitas dengan diabetes melitus ?
6
1.3Tujuan Penelitian
1.3.1 Tujuan Umum
Untuk mengetahui pengaruh pemberian injeksi testosteron pada tikus wistar jantan obesitas dengan diabetes melitus.
1.3.2 Tujuan Khusus
1. Untuk membuktikan pemberian injeksi testosteron dapat menghambat kerusakan sel beta pankreas pada tikus wistar jantan obesitas dengan diabetes melitus.
2. Untuk membuktikan pemberian injeksi testosteron dapat menurunkan kadar gula darah pada tikus wistar jantan obesitas dengan diabetes melitus.
1.4 Manfaat Penelitian
1.4.1 Manfaat Ilmiah
Memberikan informasi mengenai efektivitas pemberian preparat testosteron terhadap perbaikan sel beta pankreas dan penurunan kadar glukosa darah pada tikus obesitas dengan diabetes melitus, serta kemungkinan dapat dipergunakan sebagai dasar untuk penelitian selanjutnya.
1.4.2 Manfaat Praktis
7
BAB II
KAJIAN PUSTAKA
2.1PENUAAN
2.1.1 Penuaan : Penyebab dan Tahapan
Penuaan adalah suatu proses menghilangnya kemampuan jaringan untuk memperbaiki diri atau mengganti diri dan mempertahankan struktur dan fungsi normalnya, sehingga tidak dapat bertahan serta memperbaiki kerusakan yang diderita. Proses penuaan menyebabkan penurunan sistem dan fungsi tubuh, meliputi sistem endokrin, sistem imun, sistem metabolisme, sistem seksual reproduktif, sistem kardiovaskuler, sistem gastrointestinal, serta sistem saraf dan otot (Pangkahila, 2007).
Banyak faktor yang menyebabkan terjadinya suatu proses penuaan yang dapat dikelompokkan menjadi faktor internal dan faktor eksternal. Beberapa faktor internal antara lain radikal bebas, hormon yang berkurang, proses glikosilasi, metilasi, apoptosis, sistem kekebalan yang menurun dan gen. Faktor eksternal yang utama ialah gaya hidup tidak sehat, diet tidak sehat, kebiasaan salah, polusi lingkungan, stres, dan kemiskinan (Pangkahila, 2011).
Proses penuaan berlangsung tidak sekaligus melainkan melalui tahapan-tahapan sebagai berikut (Pangkahila, 2011) :
1. Tahap Subklinik (usia 25-35 tahun)
8
Radikal bebas, yang dapat merusak sel dan DNA mulai mempengaruhi tubuh, tetapi secara fisik belum terlihat tanda–tanda penuaan. Namun pada wanita muda yang menggunakan kontrasepsi hormonal dapat ditemukan gangguan sexual desire.
2. Tahap Transisi (usia 35-45 tahun):
Selama tahap ini kadar hormon menurun sampai 25 persen. Masa otot berkurang sebanyak satu kilogram setiap beberapa tahun, kehilangan tenaga, dan komposisi lemak tubuh bertambah mengakibatkan terjadinya resistensi insulin, serta risiko penyakit jantung pembuluh darah meningkat. Pada tahap ini gejala penuaan mulai muncul, yaitu penglihatan dan pendengaran menurun, rambut mulai putih, elastisitas kulit berkurang, dorongan seksual dan bangkitan seksual menurun. 3. Tahap Klinis (usia 45 tahun keatas) :
9
Dengan melihat ketiga tahap ini, dapat dikatakan bahwa proses penuaan tidak selalu dinyatakan dengan suatu gejala atau keluhan. Hal ini mempertegas bahwa seseorang yang tidak menunjukkan gejala ataupun keluhan bukan berarti tidak mengalami proses penuaan dan dalam mengatasi proses penuaan, tidaklah perlu menunggu adanya gejala atau keluhan yang nyata (Pangkahila, 2007).
2.1.2 Mekanisme Proses Penuaan
Proses yang melatarbelakangi terjadinya proses penuaan sampai saat ini masih menjadi perdebatan apakah merupakan proses fisiologis atau patologis, merupakan suatu proses yang terprogram atau peristiwa acak yang dipengaruhi oleh lingkungan eksternal. Perdebatan ini melahirkan beberapa konsep teori yang berusaha menerangkan bagaimana proses penuaan ini bisa terjadi (Goldman dan Klatz, 2007).
1. Teori “wear and tear”
Sel dan organ tubuh mengalami kerusakan karena sering digunakan dan disalahgunakan (overuse and abuse). Fungsi organ tubuh menurun karena toksin di dalam makanan dan lingkungan, konsumsi berlebihan dari lemak, gula, kafein, alkohol dan nikotin, akibat sinar ultraviolet dan stres fisik dan emosional (Goldman dan Klatz, 2007).
2. Teori neuroendokrin
10
diatur oleh hipotalamus yang membentuk poros dengan hipofisis dan organ tertentu yang kemudian mengeluarkan hormonnya (Djuanda, 2005). Pada usia muda kadar hormon berada dalam kondisi optimal sehingga tercapai performa biologis yang prima dan berbagai organ tubuh dapat bekerja dengan baik (Pangkahila, 2011). Produksi hormon mengalami perubahan ketika penuaan terjadi. Hormon tertentu mengalami penurunan (growth hormone, triiodothyronine (T3), testosteron, estrogen, renin, aldosteron, dehydroepidanrosterone (DHEA) dan dehydroepidanrosteronesulphate) sementara kadar beberapa hormon lainnya meningkat seperti FSH, LH, vasopresin, insulin, parathyroid hormone (PTH), atrial natriuretic hormone (ANH) dan leptin. Ketidakseimbangan produksi hormon tersebut berpengaruh terhadap regulasi fungsi pertumbuhan, pemeliharaan dan perbaikan tubuh sehingga timbul berbagai keluhan yang dianggap sebagai gejala penuaan. Hubungan antara penuaan dan perubahan hormon terjadi secara timbal balik, yaitu proses penuaan mempengaruhi produksi hormon begitu pula sebaliknya penurunan hormon menyebabkan timbulnya keluhan-keluhan penuaan (Djuanda, 2005; Pangkahila, 2007).
3. Teori kontrol genetik
11
tersebut menentukan seberapa cepat penuaan terjadi dan berapa lama individu tersebut dapat hidup (Goldman dan Klatz, 2007).
4. Teori radikal bebas
Penuaan dianggap berhubungan dengan akumulasi radikal bebas yang meningkat seiring dengan pertambahan usia. Peningkatan radikal bebas menimbulkan kerusakan terhadap molekul-molekul organik seperti protein, DNA dan lemak. Kerusakan molekul akan bermanifestasi pada penyakit-penyakit berkaitan dengan usia tua seperti Alzheimer, aterosklerosis, kanker, Parkinson dan penurunan fungsi imun (Pangkahila, 2007).
2.2OBESITAS
2.2.1 Definisi
Obesitas didefinisikan oleh WHO sebagai akumulasi lemak yang abnormal atau berlebihan yang berpeluang menimbulkan beberapa risiko kesehatan pada seorang individu (Nurmalina, 2011). Akumulasi lemak berlebih ini terjadi akibat adanya ketidakseimbangan antara pemasukan energi dan pengeluaran energi. Kegemukan tercatat sebagai faktor risiko utama kelima penyebab kematian di seluruh dunia (Pangkahila, 2011).
12
didefinisikan sebagai overweight sementara dikatakan obesitas apabila IMT ≥ 25 (WHO, 2005).
2.2.2 Epidemiologi Obesitas
Obesitas telah menjadi suatu masalah kesehatan global, di mana terjadi peningkatan prevalensi obesitas yang signifikan di seluruh dunia. Di negara maju seperti Amerika, penderita kegemukan diprediksi akan mencapai 85% pada tahun 2030, dimana 51,1% merupakan kasus obesitas (Nduhirabdani dkk., 2011). Tidak hanya di negara-negara maju, peningkatan prevalensi obesitas juga dialami negara-negara yang sedang berkembang, khususnya di Asia Tenggara dan Pasifik Barat.
Obesitas dapat meningkatkan risiko beragam penyakit serius baik pada orang dewasa dan anak-anak seperti jantung koroner, stroke, tekanan darah tinggi, diabetes melitus tipe 2, lemak darah abnormal, kanker, osteoarthritis, sleep apnea, batu empedu, dan masalah reproduksi. Selain menimbulkan masalah kesehatan, obesitas juga memiliki dampak ekonomi yang signifikan terhadap biaya medis dan biaya perawatan, baik biaya langsung maupun tidak langsung yang mencakup biaya layanan pencegahan, diagnosis, dan pengobatan yang berkaitan dengan obesitas (Nurmalina, 2011).
2.2.3 Etiologi dan Patofisiologi Obesitas
13
yang berperan dalam terjadinya obesitas seperti faktor genetik, kurangnya keseimbangan energi, kurangnya aktivitas fisik, lingkungan, kondisi kesehatan dan hormonal, obat-obatan dan faktor emosional (Nurmalina, 2011). Berbagai penelitian menunjukkan bahwa diet tinggi lemak dan karbohidrat akan menyebabkan peningkatan berat badan dan lemak tubuh, yang lama kelamaan dapat menimbulkan obesitas. Walaupun faktor genetik juga berperan dalam menentukan kecenderungan terjadinya obesitas, faktor lingkungan, yaitu diet tinggi lemak dan karbohidrat, dianggap lebih berperan penting (Wood dkk., 2003).
Beberapa faktor yang dianggap memiliki peranan dalam terjadinya obesitas adalah sebagai berikut :
1. Faktor genetik
Banyak gen yang berkaitan dengan terjadinya obesitas, namun sangat jarang yang berkaitan dengan gen tunggal. Sebagian besar berkaitan dengan kelainan pada banyak gen. Pada penyebab gen tunggal, di antaranya yang sudah diketahui adalah adanya mutasi pada gen leptin, reseptor leptin, reseptor melanocortin-4, pro-opiomelanocortin dan pada gen peroxisome proliferator-activated receptor gamma (PPAR-γ atau PPARG) (Paracchini dkk., 2005).
2. Aktivitas fisik
14
disimpan dalam bentuk lemak (Soegih, 2009). Aktivitas fisik merupakan salah satu faktor yang dapat meningkatkan kebutuhan energi (energy expenditure), sehingga apabila aktivitas fisik rendah maka kemungkinan terjadinya obesitas akan meningkat.
3. Diet tinggi karbohidrat dan lemak
Makanan merupakan sumber dari asupan energi, yang bila berlebih, maka karbohidrat akan disimpan sebagai glikogen dan lemak; protein akan disimpan sebagai protein tubuh; sedangkan lemak akan disimpan sebagai lemak. Tubuh memiliki kemampuan menyimpan lemak yang tidak terbatas (Soegih, 2009). Faktor-faktor yang berpengaruh dari asupan makanan terhadap terjadinya obesitas adalah kuantitas, porsi sekali makan, kepadatan energi, kebiasaan makan saat malam hari, frekuensi makan, dan jenis makanan (Barassi, 2009).
4. Regulasi fisiologis metabolisme
Regulasi fisiologis metabolisme tubuh terdiri dari controller (otak) dan controlled system / nutrient partitioning yaitu organ di luar otak yang berperan dalam menggunakan atau menyimpan energi seperti saluran cerna, hati, otot, ginjal, dan jaringan lemak (Soegih, 2009). Otak menerima rangsang dari lingkungan ataupun dari dalam tubuh sendiri dalam bentuk sinyal neural dan humoral yang selanjutnya membuat otak merespon dalam bentuk menghambat atau mengaktivasi motor system, dan memodulasi sistem saraf dan hormonal untuk mencari atau
15
memperngaruhi pemilihan jenis makanan, porsi makan, lama makan, proses pencernaan, absorpsi serta metabolisme zat gizi dalam tubuh. Hasil akhirnya dapat berupa pembentukan jaringan lemak, glikogenesis, pembentukan hormon dan enzim, atau dibakarnya zat gizi sebagai energi (Soegih, 2009).
5. Gangguan kesehatan dan ketidakseimbangan hormon
Gangguan hormon seperti Cushing syndrome, adrenocortical hyperactivity, dan hipogonad dapat menyebabkan penimbunan lemak
tubuh (Wirahadikusumah, 2000). Ketidakseimbangan hormon tubuh seperti pada wanita postmenopause atau pada pasien hipogonad juga akan memberikan gambaran obesitas.
6. Obat-obatan
Obat yang memperlambat metabolisme atau meningkatkan nafsu makan dapat menyebabkan kelebihan berat badan seperti kortikosteroid dan antidepresan (Nurmalina, 2011).
7. Faktor emosi
Beberapa orang makan lebih dari biasanya ketika sedang merasa bosan, marah, atau sedih (Soegih, 2009).
2.2.4 Obesitas dan Hormon Testosteron
16
androgen yang dipicu oleh obesitas dan obesitas yang dipicu oleh kondisi hipogonadisme.
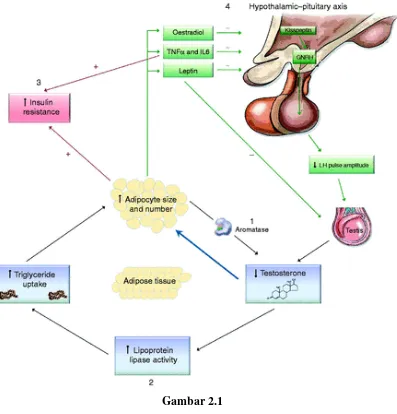
Gambar 2.1
Hipotesis hipogonad – obesitas (Kelly dan Jones, 2013)
17
bersirkulasi akan berkurang. Penurunan kadar testosteron akan memicu terjadinya deposisi lemak lebih lanjut. Hal ini berlangsung berulang-ulang dan menyebabkan semakin rendahnya kadar testosteron dalam darah. Estradiol beserta tumour necrosis factor (TNF)-α dan interleukin (IL)-6 yang dihasilkan oleh sel adiposa akan menghambat produksi GnRH di hipotalamus serta pelepasan LH dan FSH oleh hipofisis. Kondisi ini menurunkan stimulasi terhadap jaringan gonad serta akan menurunkan produksi testosteron lebih lanjut (Kelly dan Jones, 2013).
Pada penderita obesitas, di mana terjadi produksi leptin yang berlebih oleh sel adiposa, hypothalamic-hypofise axis akan mengalami resistensi terhadap leptin dan akan terjadi inhibisi terhadap produksi testosteron oleh sel Leydig (Isidori dkk., 1999).
Berdasarkan fakta ini, dapat disimpulkan bahwa kondisi obesitas akan menyebabkan penurunan kadar testosteron dalam tubuh.
2.2.5 Obesitas dan Diabetes Melitus
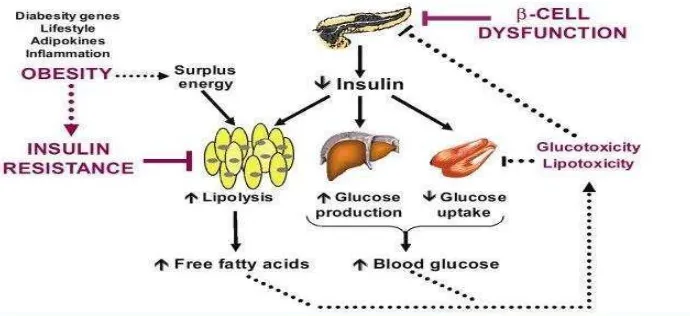
18
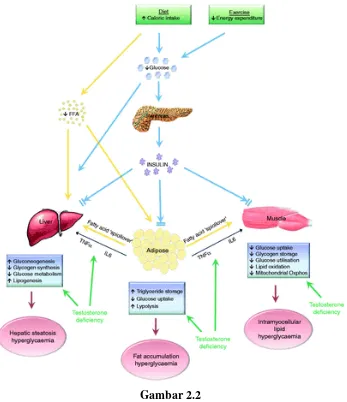
Sebagai konsekuensi dari pelepasan asam lemak (free fatty acid) oleh jaringan lemak, terjadi penimbunan lemak di jaringan lain terutama otot dan hati (fatty liver). Akumulasi lemak pada kedua jaringan inilah yang berperan dalam abnormalitas dari kontrol glukosa tubuh serta resistensi insulin di jaringan (Kelly dan Jones, 2013).
Resistensi insulin yang terutama disebabkan oleh penumpukan lemak abdominal, terbukti sebagai faktor patologis utama dalam terjadinya diabetes dan sindrom metabolik.
Gambar 2.2
19
Obesitas berkaitan erat dengan kelainan metabolik dan penyakit kardiovaskular. Kelainan metabolik akibat obesitas yang sering disebut sebagai sindrom metabolik, ditandai dengan adanya tiga atau lebih dari faktor berikut, yaitu obesitas sentral, peningkatan tekanan darah, trigliserida, glukosa darah puasa, dan penurunan kadar kolesterol HDL. Peningkatan adipokin seperti PAI-1, TNF-α, IL-6, MCP-1, angiotensinogen dan penurunan adiponektin pada obesitas terlibat dalam patogenesis terjadinya sindrom metabolik (Furukawa dkk., 2004).
2.2.6 Pengaruh Obesitas terhadap Stres Oksidatif
Penelitian pada binatang percobaan menunjukkan hubungan antara diet tinggi lemak dan karbohidrat, obesitas, dan stres oksidatif. Stres oksidatif berperan penting pada patogenesis berbagai penyakit, seperti resistensi insulin, disfungsi endotel, hipertensi, inflamasi, dan aterosklerosis (Beltowski dkk., 2000; Ceriello dan Motz, 2004; Roberts dkk., 2006).
20
radikal bebas pada rantai respirasi mitokondria. Sel adiposa juga memproduksi sitokin pro-inflamasi seperti interleukin (IL)-6 dan tumour necrosis factor
(TNF)-α. Sementara penurunan adiponektin akan menyebabkan terjadi resistensi insulin
dan atherosclerosis (Sanchez dkk., 2011; Marseglia dkk., 2015).
2.3DIABETES MELITUS
2.3.1 Definisi Diabetes Melitus
Diabetes melitus, yang umum dikenal sebagai penyakit kencing manis, merupakan keadaaan hiperglikemia kronik yang disebabkan oleh karena kelainan sekresi insulin, gangguan kerja insulin, atau kombinasi dari keduanya (Perkeni, 2008).
Berdasarkan etiologinya, faktor yang menyebabkan keadaan hiperglikemia adalah penurunan sekresi insulin, penghambatan glikolisis dan peningkatan dari produksi glukosa di dalam tubuh (Powers, 2008).
Definisi diabetes melitus menurut World Health Organization (WHO) adalah berdasarkan kadar glukosa puasa ≥ 126 mg/dL atau kadar glukosa darah
sewaktu ≥ β00 mg/dL disertai dengan gejala klasik, dimana kadar glukosa darah
puasa antara 100 dan 125 mg/dL (6,1 sampai 7,0 mmol/L) dapat dikatakan suatu keadaan pre-diabetes.
21
Tabel 2.1
Kadar glukosa darah sewaktu dan puasa sebagai patokan penyaring dan diagnosis (T2DM) kini menjadi ancaman yang serius bagi penduduk dunia. Di tahun 2012, sekitar 29,1 juta penduduk Amerika atau 9,3% dari keseluruhan populasi menderita penyakit diabetes melitus sementara sekitar 86 juta jiwa diperkirakan sudah mengalami keadaan pre-diabetes (WHO, 2014).
22
2.3.3 Faktor Risiko Diabetes Melitus
Ada beberapa faktor risiko yang dapat meningkatkan kemungkinan terjadinya penyakit diabetes pada seorang individu. Faktor-faktor risiko tersebut antara lain adalah (Buse dkk., 2003; Semiardji, 2005) :
1. Faktor yang dapat dimodifikasi
Obesitas, kurangnya aktivitas fisik, kondisi pre-diabetes atau TGT, hipertensi, kadar kolesterol HDL < 35 mg/dL, kadar trigliserida > 150 mg/dL.
2. Faktor yang tidak dapat dimodifikasi
Usia > 45 tahun, etnis tertentu (contohnya African American, Hispanic American, Native American, Asian American, dan Pasific Islander)
atau adanya faktor genetik, riwayat gestasional diabetes atau pernah melahirkan bayi dengan berat lebih dari 4 kg, riwayat Polycystic Ovary Syndrome, dan riwayat penyakit pembuluh darah.
2.3.4 Klasifikasi
Berdasarkan pada etiologinya, diabetes melitus dapat diklasifikasikan sebagai berikut (Harrison, 2008):
23
2. Diabetes melitus tipe 2, di mana kelainan metabolisme glukosa disebabkan oleh adanya resistensi insulin, defek sekresi insulin, atau gabungan dari keduanya.
3. Diabetes tipe lain 4. Diabetes gestasional
2.3.5 Patogenesis Diabetes Melitus
Berbeda dengan diabetes melitus tipe 1, diabetes melitus tipe 2 (T2DM) terjadi akibat kombinasi dari resistensi insulin dan sekresi insulin yang tidak adekuat. Pada banyak penelitian ditemukan bahwa umumnya resistensi insulin akan terjadi lebih dahulu namun kondisi diabetes baru memberikan gejala setelah sekresi insulin tidak lagi adekuat. Patogenesis T2DM sangat kompleks karena T2DM bersifat poligenik dan multifaktorial, di mana peran genetik dan pengaruh lingkungan dapat mempengaruhi tampilan penyakit ini (Buse dkk., 2003; Harrison, 2008).
Diabetes melitus tipe 2 terutama ditandai oleh sekresi insulin yang terganggu, resistensi insulin, produksi glukosa di hati yang berlebih, dan metabolisme lemak yang abnormal. Obesitas dapat ditemukan pada hampir 80% kasus T2DM.
24
dan sekresi insulin pun akan berkurang. Pada titik ini, dapat ditemui gambaran kadar glukosa darah yang meningkat dan disertai dengan peningkatan pembentukan glukosa di hati akibat sekresi insulin yang semakin menurun (Vail, 2004; Harrison, 2008).
Mekanisme awal terjadinya resistensi insulin masih belum dapat dipastikan, diperkirakan disebabkan oleh penurunan jumlah reseptor insulin dan penurunan aktivitas tyrosine kinase yang bersifat sekunder terhadap kondisi hiperinsulinemia. Kondisi yang dianggap menyebabkan keadaan resistensi ini adalah obesitas terutama obesitas viseral di mana peningkatan asam lemak bebas serta adipokine yang dihasilkan sel lemak yang memodulasi sensitivitas sel terhadap insulin (Harrison, 2008).
2.3.6 Gejala Klinis Diabetes Melitus
Diabetes melitus umumnya akan memberikan beberapa gejala, yang dibedakan menjadi gejala akut dan gejala kronis. Gejala akut adalah gejala yang khas ditemui pada penderita diabetes yaitu polidipsia sebagai mekanisme kompensasi tubuh kehilangan cairan dan elektrolit, poliuria akibat peningkatan kadar glukosa melebihi ambang renal sehingga terjadi diuresis osmotik, polifagia, dan penurunan berat badan tanpa sebab yang jelas.
25
2.3.7 Kriteria Diagnosis Diabetes Melitus
Diagnosis diabetes melitus dapat ditegakkan berdasarkan beberapa kriteria dan pemeriksaan. Kriteria diagnosis yang ditetapkan menurut Perkeni meliputi tiga cara. Pertama, jika ditemukan gejala khas diabetes maka pemeriksaan glukosa darah sewaktu > 200 mg/dL sudah dapat menegakkan diagnosis T2DM. Kedua, dengan melakukan pemeriksaan glukosa darah puasa > 126 mg/dL disertai dengan gejala khas diabetes, di mana puasa diartikan sebagai pasien tidak mendapat kalori tambahan selama 8 jam. Ketiga adalah dengan melakukan pemeriksaan tes toleransi glukosa darah oral (TTGO) dengan kadar glukosa darah > 200 mg/dL dalam 2 jam setelah mengkonsumsi 75 gram glukosa anhidrus yang dilarutkan ke dalam air (Perkeni, 2008).
TTGO bersifat lebih sensitif dan spesifik dalam mendiagnosa diabetes namun dalam pelaksanaannya memiliki keterbatasan dan lebih jarang dilakukan. Cara kedua lebih mudah dilakukan, lebih mudah diterima pasien, dan lebih murah sehingga sering dijadikan sebagai dasar pemeriksaan dalam praktek sehari-hari.
26
2.3.8 Komplikasi pada Hiperglikemia
Keadaan hiperglikemia memicu timbulnya berbagai komplikasi. Menurut Danerson (1994) komplikasi akibat diabetes melitus dibedakan menjadi komplikasi akut dan kronis, yang dibagi lagi menjadi makroangiopati dan mikroangipati.
Komplikasi akut meliputi ketoasidosis diabetik, koma, hiperglikemia, dan hipoglikemia. Komplikasi makroangipati antara lain penyakit jantung koroner, stroke, dan peripheral artery disease. Komplikasi mikroangipati berupa retinopati diabetik, neuropati, dan nefropati diabetik. Selain itu dapat timbul gangguan pada sistem gastrointestinal berupa gastroparesis atau diare, sistem genitourinaria, kelainan kulit, katarak, glaukoma, penyakit periodontal, serta menurunnya fungsi pendengaran (Harrison, 2008).
Ada beberapa hipotesis yang menerangkan proses terjadinya komplikasi pada keadaan hiperglikemia ini :
1. Melalui jalur sorbitol (Polyol Pathway)
27
jumlah NADPH akan berkurang di dalam sel pembuluh darah dan neuron, mengakibatkan berkurangnya sintesa nitrit oxide (NO) (Subekti, 2005).
2. Melalui pembentukkan AGEs (Advanced Glycosylation End Products) AGEs merupakan produk lanjutan yang terbentuk saat terdapat kelebihan glukosa dalam tubuh. AGEs terbentuk melalui reaksi non-enzimatik di mana kelebihan glukosa akan berikatan dengan protein atau asam amino, kemudian membentuk produk glikasi yang bersifat reversibel yaitu Schiff base lalu menjadi Amadori product, selanjutnya menjadi AGEs yang tidak reversibel.
AGEs merusak struktur enzimatik dan fungsi protein yang mengalami glikasi tersebut. (Subekti, 2005). Pada sel beta pankreas, AGEs memicu modifikasi oksidatif yang selanjutnya akan merusak sel.
3. Melalui peningkatan aktivasi PKC (Protein Kinase C) melalui peningkatan DAG (Diacylglycerol)
PKC menyebabkan perubahan pada gen yang mengkode fibrinopektin, kolagen tipe IV, protein kontraktil, dan matriks ekstrasel di sel endotel dan saraf.
PKC menstimulasi pembentukan ROS melalui aktivasi NAD(P)H oksidase.
4. Melalui peningkatan aktifitas jalur Hexosamine
28
fungsi protein. Perubahan ini yang akan berkontribusi terhadap proses terjadinya komplikasi pada DM (Taguchi dan Brownlee, 2005).
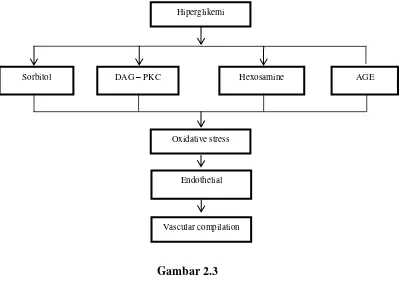
Gambar 2.3
Proses Komplikasi pada Penderita Hiperglikemi
2.3.9 Penatalaksanaan Diabetes Melitus Tipe 2
Berdasarkan Konsensus Diabetes Melitus, disebutkan ada empat pilar dalam penatalaksanaan diabetes melitus yaitu edukasi, terapi gizi medis, latihan jasmani, dan intervensi farmakologis (Perkeni, 2008).
Penatalaksanaan diabetes di luar intervensi farmakologis umumnya dilaksanakan terlebih dahulu selama 2-4 minggu diikuti dengan pemantauan kadar gula darah pasien. Bila pada kurun waktu tersebut, kadar gula darah ideal belum dapat dicapai maka dapat dimulai terapi farmakologis. Terapi farmakologis juga
Hiperglikemi
Oxidative stress
AGE Hexosamine
DAG – PKC Sorbitol
29
dapat langsung dimulai pada keadaan tertentu, misalnya dekompensasi metabolik yang berat (Perkeni, 2008).
Intervensi farmakologis dapat berupa obat hipoglikemik oral (OHO), insulin, ataupun kombinasi dari OHO dan insulin. Obat hipoglikemik oral dapat dikelompokkan menjadi beberapa golongan :
1. Pemicu sekresi insulin
- Sulfonilurea
Glibenklamid merupakan salah satu golongan sulfonilurea yang paling umum digunakan sebagai lini pertama terapi antihiperglikemia oral dan umumnya menjadi pilihan utama untuk pasien dengan berat badan normal dan kurang. Glibenklamid memiliki efek utama meningkatkan sekresi insulin oleh sel beta pankreas dengan cara menghambat kerja ATP-sensitive potassium channels sehingga kalsium intraseluler meningkat.
- Glinid
Repaglinid dan Nateglinid meningkatkan sekresi insulin fase pertama, diabsorpsi cepat setelah pemberian oral dan diekskresi secara cepat melalui hati.
2. Penambah sensitivitas insulin
Tiazolidindion berikatan pada Peroxisome Proliferator Activated Receptor Gamma (PPAR- ) di inti sel otot dan sel lemak. Golongan ini
30
glukosa oleh sel. Efek samping dari obat ini adalah retensi cairan sehingga dapat menambah berat badan, dan tidak dapat diberikan pada penderita gagal jantung kelas IV.
3. Penghambat glukoneogenesis
Metformin bekerja dengan menurunkan produksi glukosa di hati dan memperbaiki ambilan glukosa di tingkat sel. Obat ini biasa digunakan pada pasien diabetes yang gemuk karena tidak memiliki efek stimulasi sel beta pankreas sehingga tidak mengakibatkan hipoglikemia ataupun penambahan berat badan (Babar dan Skugor, 2009).
4. Penghambat enzim glukosidase alfa
Acarbose bekerja dengan menghambat enzim α-glukosidase di saluran cerna, sehingga pemecahan polisakarida berkurang dan mengurangi absorpsi glukosa di usus halus sehingga dapat menurunkan kadar glukosa post-prandial. Obat ini tidak mengakibatkan hipoglikemia, dan efek sampingnya ringan.
Prinsip pemberian OHO pada pasien diabetes adalah dimulai dengan dosis rendah dan ditingkatkan secara bertahap, sesuai dengan respon tubuh terhadap pengobatan.
2.3.10 Streptozotosin (STZ) dan Diabetes melitus
31
bersifat karsinogenik, dan secara selektif menghancurkan sel beta pada pulau Langerhans (Cooperstein, 1981).
Induksi percobaan diabetes menggunakan streptozotocin sangat mudah untuk dilakukan di mana penyuntikan streptozotocin menyebabkan degradasi dari sel beta pankreas (Abeeleh dkk., 2009). Stretptozotocin secara selektif terakumulasi di dalam sel beta pankreas melalui transporter glukosa GLUT2 yang infinitasnya rendah, yang terdapat di dalam membran sel (Lenzen, 2008). Mekanisme kerja dari streptozotocin adalah terjadinya perpindahan gugus metil dari streptozotocin menuju molekul DNA, sehingga menyebabkan rantai DNA pada sel beta pankreas terputus. Dalam upaya untuk memperbaiki DNA, poli-ADP-ribose polymerase distimulasi secara berlebihan sehingga menurunkan kadar
NAD+ dan ATP. Dengan menipisnya energi yang disimpan pada sel menyebabkan kematian pada sel beta, sehingga selanjutnya akan menghambat sintesis proinsulin dan menginduksi terjadinya keadaan hiperglikemia. Streptozotocin menghambat sekresi insulin dan menyebabkan insulin dependent diabetes melitus (IDDM) (Lenzen, 2008). Secara klinis, gejala dari diabetes pada tikus akan terlihat jelas dalam 2-4 hari setelah penyuntikan secara intraperitoneal dengan dosis tunggal (Abeeleh dkk., 2009). Streptozotocin juga mengaktivasi spesies oksigen reaktif seperti superoksida (O2-), radikal hidroksil (-OH) dan hidrogen peroksida (H2O2) (Li, 2001).
32
bebas, penekanan dari ekspresi MHC-II, penekanan pada aktivitas nitric oxide, dan memblokir efek yang ditimbulkan oleh interleukin (IL)-1 (Greenbaum dkk., 1996). Nicotinamide bersifat dose-dependent sehingga besarnya jumlah sel beta yang terlindungi berbanding lurus dengan banyaknya jumlah nicotinamide yang diberikan (Hoorens dkk., 1999).
2.4PANKREAS
2.4.1 Anatomi Fisiologi Kelenjar Pankreas
Pankreas adalah organ yang terdiri dari jaringan eksokrin dan endokrin. Bagian eksokrin mengeluarkan enzim-enzim pencernaan melalui duktus pankreatikus ke dalam saluran cerna. Bagian endokrin tersebar di antara bagian eksokrin, dikenal sebagai pulau Langerhans.
Pulau Langerhans terdiri dari empat macam sel yaitu sel beta, sel alfa, sel delta, dan sel pankreas polipeptida. Dalam pulau Langerhans manusia dewasa normal, jumlah sel beta berkisar antara 75% - 80% dari populasi sel pulau Langerhans. Sel beta tersebar di bagian tengah pulau Langerhans, sementara ketiga jenis sel lainnya terletak di bagian perifer (Sherwood, 2001).
33
akan merangsang sekresi insulin dan menghambat sekresi glukagon, sementara penurunan gula darah akan menyebabkan penurunan sekresi insulin dan peningkatan sekresi glukagon (Sherwood, 2001).
Gambar 2.4
Mekanisme kerja Insulin – Glukagon (Sherwood, 2001)
2.4.2 Sel Beta Pankreas
34
Kerusakan sel beta akibat keadaan hiperglikemia terjadi secara bertahap di mana awalnya sel beta mengalami desensitisasi akibat hiperglikemia berulang, lalu terjadi penurunan fungsi apabila keadaaan tersebut berlanjut akibat beta cell exhaustion. Keadaan ini akan terus berlanjut menjadi kerusakan dan apoptosis sel
beta yang tidak reversibel (Shoelson dkk., 2006)
Perubahan histopatologis pulau Langerhans pada keadaan diabetes dapat terjadi secara kuantitatif maupun kualitatif. Perubahan kuantitatif yang dapat diamati adalah pengurangan jumlah dan ukuran pada pulau Langerhans, sementara perubahan kualitatif dapat berupa terjadinya nekrosis, degenerasi, ataupun amyloidosis (Suarsana dkk., 2010).
Gambaran histopatologis pankreas yang mungkin didapati pada keadaan diabetes adalah struktur pulau Langerhans yang ireguler akibat adanya hiperplasia atau hipertrofi yang mendahului disertai infiltrasi oleh sel inflamasi. Pada keadaan diabetes yang semakin lanjut didapatkan replikasi sel beta yang menurun dan apoptosis sel beta yang meningkat (Finegood dkk., 2001).
Pemeriksaan histopatologi sel beta pankreas memberikan gambaran mengenai kelainan yang terjadi akibat kondisi hiperglikemia, bahkan sebelum diagnosis diabetes melitus ditegakkan. Pemeriksaan histopatologi dapat memberikan gambaran kelainan yang terjadi pada tingkat mikroskopik. Pemeriksaan histopatologi pada sel beta dapat menggunakan metode kuantitatif ataupun semi-kuantitatif (Paulsen dkk., 2010).
35
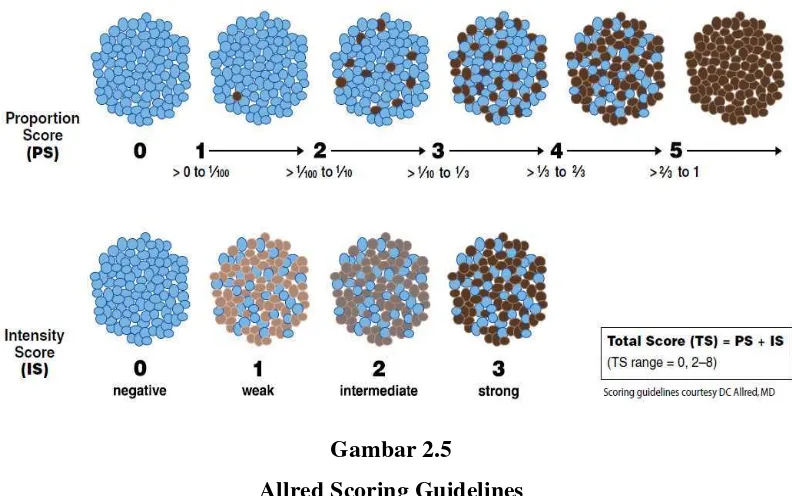
Sementara metode pemeriksaan semi-kuantitatif menggabungkan pemeriksaan jumlah sel beta dengan intensitas kekuatan dari sel yang dinilai berdasarkan hasil pewarnaan yang dilakukan. Terdapat beberapa cara perhitungan semi-kuantitatif, salah satunya adalah HSCORE dan Allred Score.
Pada HSCORE, intensitas sel beta pankreas dinilai dengan intensity score (IS) yang merupakan sistem skoring dengan empat poin yaitu (0) untuk tidak ada, (1) untuk intensitas lemah, (2) untuk intensitas sedang , dan (3) untuk intensitas kuat. Perhitungan sel beta dilakukan dengan menjumlahkan sel beta sesuai dengan nilai skornya. Jumlah sel beta untuk masing-masing kelompok intensitasnya dikalikan dengan skornya kemudian dijumlahkan sehingga didapatkan nilai HSCORE (Choudhury dkk., 2009).
36
Gambar 2.5
Allred Scoring Guidelines
Seperti yang disimpulkan dalam penelitian Belfast Diabetes Study, kerusakan sel beta pankreas sudah terjadi sebelum ada gejala klinis seperti hiperglikemia. Kerusakan sel beta pankreas ini dapat terjadi melalui tiga mekanisme utama yaitu :
1. Glukotoksisitas
37
mengaktifkan NF-xB, yaitu suatu jalur proapoptotik (Stumvold dkk., 2008).
2. Lipotoksisitas
Keadaan hiperglikemia menghambat oksidasi beta asam lemak sehingga terjadi penumpukan kompleks asam lemak rantai panjang (LC-KoA) yang akan mengganggu aktivitas pompa K+. Gangguan ini pada akhirnya akan menghambat pembentukan ATP (Stumvold dkk., 2008). Penumpukan asam lemak bebas juga merangsang sintesis seramida dan pembentukan oksida nitrit (NO). Seramida menghambat ekspresi gen insulin dan akan mengakibatkan terjadinya apoptosis. 3. Penumpukan amiloid
Amiloid polipeptida atau amilin merupakan senyawa yang normalnya terdapat di dalam granul insulin dan ikut disekresikan bersama insulin. Amilin bersifat sitotoksik dengan menyebabkan masuknya kalsium dalam sel beta dan membentuk agregasi intrasel.
Gambar 2.6
38
2.4.3 Insulin
Insulin merupakan hormon polipeptida yang mengatur metabolisme karbohidrat. Struktur molekul insulin berupa dua rantai polipeptida yaitu rantai A (acidic) yang mengandung 21 asam amino dengan glysine sebagai N-terminal dan rantai B (basic) yang mengandung 30 asam amino dengan phenylalanine sebagai N-terminal (Turner dkk., 1969).
Pembentukan insulin dimulai saat adanya rangsangan glukosa pada ribosom retikulum endoplasmik sehingga terjadi translasi dan transkripsi mRNA menjadi proinsulin. Bentuk ini kemudian akan ditransfer ke dalam badan Golgi dan mengambil bentuk granul yang pucat, disebut sebagai beta granul yang belum matang. Beta granul ini akan dilepaskan ke sitoplasma dan insulin di dalam beta granul akan ditranspor dalam bentuk kristal apabila dibutuhkan.
Insulin merupakan hormon anabolik yang bekerja pada metabolisme glukosa, lemak, dan protein serta bertujuan untuk menjaga kestabilan kadar gula darah dalam tubuh. Target sel dari insulin meliputi hampir sebagian besar jaringan, namun yang utama adalah hati, sel lemak, dan otot (Sherwood, 2001).
39
menghambat glukoneogenesis di hati, yaitu pembentukan glukosa dari asam-asam amino dan menghambat lipolisis di jaringan lemak.
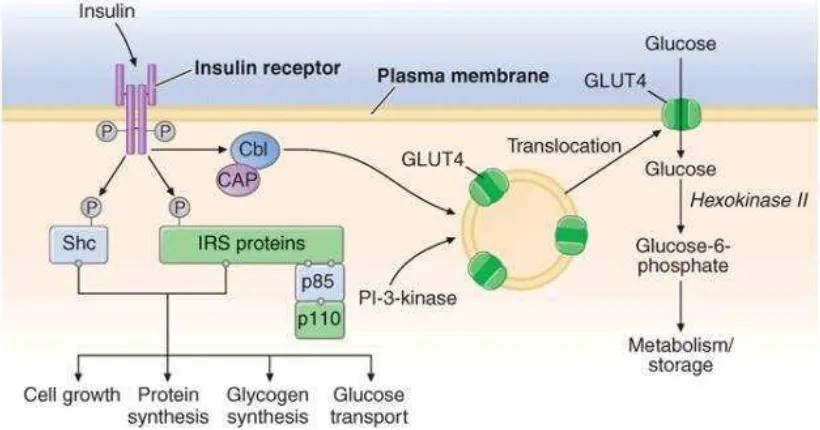
Gambar 2.7
Mekanisme kerja Insulin (Powers, 2008)
2.5TESTOSTERON
40
Hormon testosteron dalam tubuh juga memiliki bentuk lain yaitu sebagai dehidrotestosteron dan androstenedion, yang merupakan bentuk androgen lemah. Baik dalam testis maupun kelenjar adrenal, hormon androgen dapat dibentuk dari kolesterol ataupun langsung dari asetil koenzim A (Guyton dan Hall, 2001).
2.5.1 Sintesis, Sekresi, dan Regulasi
Testosteron disintesis dan disekresikan terutama oleh testis. Testosteron disintesis oleh sel-sel interstisial Leydig pada testis melalui mekanisme umpan balik dan diatur lewat kontrol hormon lutein (luteinizing hormon / LH) yang disekresi oleh kelenjar hipofisis. Testis memproduksi sekitar 95% dari total testosteron pada pria dewasa, sisanya diproduksi oleh zona retikularis korteks adrenal.
Pelepasan testosteron mengikuti ritme sirkadian (circadian rhythm) tubuh di mana kadar testosteron di dalam sirkulasi mencapai puncaknya antara pukul 06.00-08.00 dan kadar terendahnya antara pukul 18.00-20.00.
Testosteron disintesis menggunakan bahan utama kolesterol di mana sumber kolesterol ini bisa berasal dari sintesis pada sel Leydig ataupun berasal dari sirkulasi (Jones, 2008; English dkk., 2001).
41
anterior. Pada saat pubertas (umur 10-13 tahun) terjadi peningkatan sekresi GnRH oleh hipotalamus. Dengan ini terjadi peningkatan sekresi hormon FSH dan LH oleh hipofisis. Testis membesar dan LH menstimulasi sel Leydig memperoduksi hormon testosteron. Hormon FSH mempengaruhi sel Sertoli dalam menjaga spermatogenesis (Sofikitis dkk., 2008).
LH menstimulasi sekresi testosteron dari sel Leydig dengan meningkatkan cyclic adenosine monophosphate (cAMP) dan level kalsium intraseluler. Siklik AMP meningkatkan pembentukan kolesterol dan ester-ester kolesterol, dan perubahan kolesterol menjadi pregnenolon melalui pengaktifan protein kinase A. Pregnenolon kemudian akan diubah menjadi androstenedion, dan dengan pengaruh enzim 17- hidroksisteroid dehydrogenase akan diubah menjadi testosteron. Bila level testosteron sudah mencukupi, maka testosteron akan menimbulkan negative-feedback ke hipofisis dan hipotalamus sehingga selanjutnya pembentukan testosteron akan dihambat. Testosteron secara langsung akan menghambat monoamine oxidase sehingga produksi LH dan FSH akan berkurang. Sedangkan FSH terutama berpengaruh terhadap sel Sertoli untuk menginisiasi dan melakukan pemeliharaan proses spermatogenesis. FSH juga menstimulasi sintesis dan pelepasan hormon inhibin dan activin dari sel Sertoli. Inhibin akan menyebabkan negative-feedback ke hipofisis sehingga menekan pelepasan FSH (Jones, 2008).
42
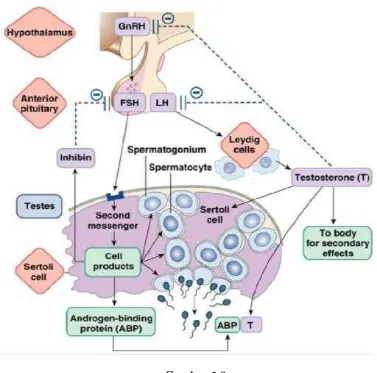
Gambar 2.8
Regulasi Sekresi dan Sintesis Testosteron : Aksis Hipotalamus – Hipofisis
– Testis
2.5.2 Testosteron dalam Sirkulasi
Testosteron yang terdapat dalam sirkulasi tubuh terbagi dalam tiga bentuk. Proporsi yang paling besar (50-80%) adalah testosteron yang terikat dengan sex hormon binding globulin (SHBG), 20-50% berikatan dengan albumin, dan 2-3%
43
umumnya sekitar 40–80 persen dari testosteron yang beredar dalam sirkulasi (Pangkahila, 2007).
Free testosteron dimetabolisme dengan cepat di dalam hati dan mempunyai waktu paruh yang pendek, kira-kira 10 menit. Testosteron berikatan sangat kuat dengan protein globulin (SHBG), tidak mempunyai efek biologis aktif dan mungkin berfungsi sebagai simpanan hormon pada sirkulasi. Testosteron berikatan secara lemah dengan albumin dan bisa lepas untuk menimbulkan efek biologis. Free testosteron dan testosteron yang berikatan dengan albumin disebut bioavailable testosteron (Klingmuller dkk., 2006; Jones, 2008).
2.5.3 Metabolisme Testosteron
Testosteron dimetabolisme menjadi metabolit aktif dan inaktif. Metabolit aktif testosteron adalah 17 -estradiol dan 5α-dihydrotestosteron (DHT). Testosteron dikonversi menjadi 17 -estradiol oleh enzim aromatase. Enzim aromatase mempunyai aktivitas yang tinggi pada jaringan lemak, khususnya pada lemak viseral. Semakin besar jumlah lemak maka produksi 17 -estradiol akan semakin besar. Tempat lain aktivitas aromatase adalah pada testis, prostat, dan tulang. Konversi testosteron menjadi DHT diperantarai oleh enzim 5α-reduktase.
Proporsi testosteron yang dikonversi menjadi 17 -estradiol dan DHT tergantung dari individu dan jenis jaringan, misalnya produksi DHT lebih tinggi pada prostat dan estradiol lebih tinggi pada tulang (Jones, 2008).
44
sebagian besarnya akan dikonjugasikan sebagai glukoromida dan sulfat, kemudian akan diekskresikan ke usus dalam empedu ataupun ke dalam urin melalui ginjal (Guyton dan Hall, 2001).
Testosteron dan androgen yang lain, termasuk DHT diinaktivasi melalui reduksi, oksidasi, dan hidroksilasi oleh liver, yang kemudian berikatan dengan asam glukoronat. Metabolit ini kemudian akan diekskresikan oleh ginjal (Jones, 2008).
2.5.4 Efek Biologis Testosteron dan Metabolitnya
Hormon testosteron secara langsung dapat menimbulkan efek biologis ataupun dapat melalui metabolitnya yaitu DHT dan 17 -estradiol. Testosteron secara umum berfungsi pada maskulinisasi tubuh pria.
Fungsi hormon testosteron tidak terbatas pada maskulinisasi namun juga berperan pada banyak sistem tubuh, dan dapat diklasifikasikan sebagai berikut (Sherwood, 2007, Eckardstein dan Nieschlag, 2002):
1. Efek pada sistem reproduksi pada saat sebelum lahir.
45
2001). Sekresi testosteron mengakibatkan penurunan testis ke skrotum, maskulinisasi sistem reproduksi dan genitalia eksternal.
2. Efek pada jaringan seks spesifik setelah lahir.
Masa puber adalah masa maturasi dari sistem reproduktif, dimulai pada usia 10–14 tahun. Pada masa puber, sel Leydig mulai mensekresi testosteron yang bertanggung jawab untuk pertumbuhan dan perkembangan seluruh sistem reproduksi pria. Di bawah pengaruh sekresi testosteron, terjadi pembesaran testis dan dimulailah produksi sperma, terjadi pembesaran glandula seksual aksesoris dan pembesaran penis serta skrotum.
3. Efek yang berkaitan dengan reproduksi
Testosteron mengatur perkembangan libido dan berperan mempertahankan libido. Testosteron juga berfungsi sebagai umpan balik negatif untuk mengontrol produksi hormon gonadotropin dari hipofisis anterior.
4. Efek pada perkembangan seksual sekunder
- Pertumbuhan rambut bergantung pada topografi tubuh.
Pertumbuhan jenggot dipengaruhi testosteron dan pertumbuhan rambut aksila dan pubis tergantung dari DHT. DHT menghambat pertumbuhan rambut kepala sehingga bisa menyebabkan kebotakan.
- Suara yang lebih rendah akibat dari pembesaran laring dan
penebalan pita suara.
- Testosteron mempunyai efek anabolik protein yang mendukung
46
berotot. Pertumbuhan dan kekuatan otot tergantung dari testosteron dan tidak tergantung pada DHT.
- Testosteron menstimulasi sekresi kelenjar minyak.
- Pada hewan, testosteron akan mengakibatkan terjadinya perilaku
agresif.
5. Efek yang tidak berkaitan dengan sistem reproduksi
- Testosteron merangsang hematopoesis melalui dua mekanisme,
yaitu menstimulasi produksi erythropoietin renal dan ekstra-renal serta efek langsung pada sumsum tulang.
- Estrogen (17 -estradiol) pada pria berguna untuk memelihara
kekuatan tulang dan penutupan epifisis. Pria dengan defisiensi enzim aromatase akan mengalami osteoporosis.
- Testosteron mempunyai efek psikotropik yang penting terhadap
otak, yaitu dapat meningkatkan motivasi, meningkatkan mood dan libido, meningkatkan fungsi kognitif seperti visuo-spatial skill, memori jangka pendek, dan kemampuan matematika.
- Banyak studi yang membuktikan bahwa testosteron berefek
47
- Testosteron juga berefek sebagai vasodilator melalui efek langsung
terhadap otot polos. Estradiol juga berefek sebagai vasodilator melalui pengaruhnya terhadap nitrit oksida. Hal ini mendukung sejumlah penelitian yang menunjukkan bahwa prevalensi penyakit koroner lebih tinggi pada populasi dengan tingkat testosteron yang rendah (Pangkahila dan Wong, 2015).
2.5.5 Testosteron dan Metabolisme Glukosa
Banyak penelitian yang membahas mengenai hubungan antara kadar plasma testosteron, sensitivitas insulin, serta prevalensi dari diabetes melitus tipe 2 (T2DM). Pada pria dengan T2DM didapatkan kadar plasma testosteron yang lebih rendah bila dibandingkan dengan pria tanpa riwayat diabetes. Sebaliknya, pada pria dengan kadar testosteron plasma yang rendah memiliki risiko yang lebih tinggi untuk menderita T2DM ataupun sindrom metabolik (Heufelder, 2009). Sindrom metabolik ditandai dengan adanya dislipidemia aterogenik, peningkatan lemak abdomen, peningkatan tekanan darah, serta adanya toleransi glukosa yang terganggu (Haffner, 2006).
48
insulin. Resistensi insulin akan semakin berat akibat efek anabolik dari kehilangan masa otot ini (Kelly dan Jones, 2013).
Pemberian hormon testosteron meningkatkan insulin receptor substrate (IRS1) dan meningkatkan ekspresi molekul transporter GLUT 4 di membran sel, yang akan meningkatkan ambilan glukosa di sel, serta mengurangi keadaan resistensi insulin yang terjadi (Kelly dan Jones, 2013).
Hormon steroid memiliki efek antioksidan pada berbagai sel dan jaringan. Hormon testosteron menjaga sel granuler cerebellum dari apoptosis yang diinduksi oleh stres dan hormon estradiol mengatur serangkaian mekanisme yang melindungi uterus dari stres oksidatif. Pada pankreas, hormon testosteron juga mencegah kerusakan sel yang disebabkan oleh stres oksidatif. Hormon testosteron bekerja melalui reseptor androgen, dan juga memodulasi enzim yang digunakan oleh sel untuk menghindari kerusakan akibat radikal bebas (Morimoto, 2005; Mancini, 2008).
Dalam suatu penelitian pada tikus, didapatkan bahwa pada tikus diabetes ditemukan adanya kematian sel beta pankreas akibat proses apoptosis dan stres oksidatif. Sel beta pankreas sangat rentan terhadap stres oksidatif dikarenakan kemampuan anti-oksidatif yang dimilikinya rendah. Stres oksidatif yang biasanya timbul dalam proses metabolisme tubuh seperti methyl cation, radikal metil, reactive oxygen species (ROS) dan nitrit oxide dapat merusak sel beta pankreas
(Kajimoto dan Kaneto, 2004).
49
meningkatkan tingkat mRNA insulin baik secara in vitro maupun in vivo. Tindakan gonadektomi yang dilakukan pada tikus menurunkan kadar testosteron plasma, juga ekspresi gen insulin serta kadar insulin dalam serum (Morimoto dkk., 2001).
2.5.6 Terapi Sulih Testosteron (Testosteron Replacement Therapy)
Penurunan hormon testosteron menyebabkan berbagai keluhan dan perubahan fisik pada usia lanjut akibat rendahnya kadar hormon yang bersirkulasi (bioavailable testosteron / BT). Terapi sulih testosteron dikembangkan untuk mengatasi segala keluhan dan gejala tersebut. Preparat sulih testosteron dapat diberikan secara oral dalam bentuk tablet, suntikan, aplikasi nasal, inplan, dan transdermal (Eckardstein dan Nieschlag, 2002).
Indikasi terapi sulih testosteron pada pria adalah keadaan hipogonadisme yang menunjukkan sindrom klinis yang kompleks yaitu adanya gejala-gejala hipogonadisme dan level testosteron yang rendah. Ambang batas level testosteron yang menimbulkan gejala-gejala hipogonad bervariasi tergantung jenis gejala dan individu (Arver dan Lehtihet, 2008).
Formulasi optimal dari testosteron adalah formula yang mampu menormalisasi level testosteron yang beredar dan juga menimbulkan level yang fisiologis dari metabolit aktifnya yaitu estradiol dan DHT.