II. PEMILIHAN DAN URAIAN PROSES
Usaha produksi dalam pabrik kimia membutuhkan berbagai sistem proses dan sistem pemroses yang dirangkai dalam suatu sistem proses produksi yang disebut teknologi proses. Secara garis besar, sistem proses utama dari sebuah pabrik kimia adalah sistem reaksi serta sistem pemisahan dan pemurnian. Proses perubahan bahan baku menjadi produk terjadi dalam sistem reaksi. Sistem pemroses bagi sistem reaksi adalah reaktor. Sistem pemisahan dan pemurnian bertujuan agar hasil dari sistem pereaksian sesuai dengan permintaan pasar sehingga layak dijual.
A. Macam-Macam Proses
Ada dua macam reaksi untuk membentuk furfuril alkohol. Yaitu reaksi Cannizaro dan reaksi hidrogenasi. Berikut masing-masing uraian proses:
A.1. Reaksi Cannizaro (Disproposionasi aldehida dengan NaOH)
Reaksi ini ditemukan pada tahun 1853 dan dinamai dari nama penemunya, Stanislao Cannizaro. Merupakan reaksi kimia yang melibatkan disproposionasi aldehida yang di oksidasi-reduksi menggunakan basa menjadi alkohol dan garam. Dalam hal pembuatan furfuril alkohol, furfural
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
(C5H4O2) di reduksi menggunakan sodium hidroksida (NaOH) menghasilkan furfural alkohol (C5H6O2) dan asam furat (C5H3O3Na). Berikut reaksinya :
2C5H4O2(l) + NaOH(l) C5H6O2(l) + C5H3O3Na(l) Furfural Sodium hidroksida Furfuril alkohol Asam furat
Proses ini dilakukan dalam skala laboratorium pada tahun 1864 menggunakan sistem batch. Berlangsung pada fasa cair dengan temperatur 70oC dan tekanan 10 atm. Proses ini tidak komersil digunakan pada skala industri karena yields maksimal hanya 45% dengan konversi sebesar 50% (US Patent 2,374,149).
A.2 Reaksi Hidrogenisasi
Reaksi ini merupakan reaksi reduksi furfural menggunakan hidrogen (hidrogenasi) dengan penambahan katalis logam. Proses ini banyak dilakukan pada skala industri dengan sistem continue yang kemudian dikembangkan oleh FN Peters dari Quaker Oats Company dari H. Adkinds dan R.Connor dari Universitas Winconsin. Reaksi ini berlangsung eksotermis pada temperatur yang relatif tinggi atau tekanan tinggi namun dihasilkan konversi yang tinggi.
Proses hidrogenasi untuk memproduksi furfuril alkohol merupakan reaksi katalitik dan dapat dijalankan pada 2 kondisi, yaitu furfural fasa cair dan furfural fasa uap (Mc. Ketta, 2003). Pada metode fasa cair reaksi
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
berlangsung pada suhu antara 150OC-250 OC dan tekanan sangat tinggi (25– 50 atm). Sedangkan pada vapor-phase reaksi berlangsung pada suhu 170OC -250OC dan pada tekanan hingga 3 atm. Oleh karena itu, pada proses hidrogenasi furfural lebih komersil menggunakan metode vapor-phase sehingga mudah dalam penanganan alat dan murah dalam hal pembiayaan energi. (US.Patent 2,754,304)
A.2.1. Hidrogenasi pada fasa cair
Hidrogenasi furfural fase cair dapat dilakukan dimana furfural pada fase cair direaksikan dengan gas hidrogen dengan menggunakan katalis logam copper, nikel dan alumina. Kondisi operasi reaktor berlangsung dalam rentang 150OC-250OC dan tekanan 25–50 atm. Selama proses reaksi berlangsung, kondisi fase cair furfural harus dikontrol agar tidak terjadi perubahan fase. Terjadinya penguapan furfural mengakibatkan perubahan reaksi akan sulit untuk di kontrol. Untuk menjaga kondisi tersebut maka dipilih tekanan yang tinggi ini (US.Patent 4,251,396). Tingginya tekanan operasi mengakibatkan biaya operasional menjadi cukup mahal.
Proses ini biasanya menggunakan katalis Copper Chromite. Penggunaan katalis ini sangatlah baik jika ditambah Calcium Oxide sebagai promotor karena bisa menghasilkan konversi maksimum
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
hingga 99%. Sintesis katalis tersebut menghasilkan Copper Chromite Calcium Oxide (CuO-Cr2O3.CaO). Katalis tersebut dipakai pada reaksi dengan ukuran 200 mesh dan bisa di simpan hingga 1 bulan tanpa mengurangi aktivitas nya. Katalis ini sangat beracun sehingga penyimpanan haruslah hati-hati agar tidak mencemari lingkungan. Sebelum digunakan katalis harus di cuci dengan demineralized water disertai pengadukan, dan setelah itu katalis dikeringkan menggunakan udara panas pada temperatur 95OC. Pada temperatur antara 271OC dan 310OC katalis akan terdekomposisi sehingga temperatur reaksi haruslah sangat dijaga agar tidak merusak aktivitas katalis ini. Luas permukaan katalis ini adalah 88 m2/gram. Katalis ini belum diproduksi di Indonesia, sehingga untuk mendapatkannya perlu didatangkan impor dari Jepang atau Korea.
Berikut reaksi yang terjadi :
C5H4O2(l) + H2(g) CuO-Cr2O3.CaO C5H6O2(l) Furfural hidrogen P = 29 atm furfuril alkohol
T = 180 o C
Karena bersifat heterogen (cair-gas), maka ketika keluar reaktor membutuhkan proses separasi untuk memisahkan produk dengan reaktan yang tidak bereaksi. Kontrol temperatur operasi pada reaktor autoclave juga cukup rumit untuk menjaga agar tidak terbentuknya by-product. Karena ketika temperatur tidak sesuai
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
maka reaksi juga akan membentuk white product (methylfuran) dan polimernya. Selain itu tekanan yang digunakan selama operasi juga sangat tinggi. Sehingga, selain kebutuhan energi tinggi, material yang digunakan untuk peralatan proses juga harus bahan yang terbaik sehingga membutuhkan investasi yang tinggi (US.Patent 4,251,396).
A.2.2 Hidrogenasi pada fasa uap
Hidrogenasi furfural fase uap dapat dilakukan dimana furfural cair (feedstock) diuapkan terlebih dahulu sebelum masuk reaktor. Sama seperti halnya pada hidrogenasi fasa cair, pada reaktor furfural direaksikan dengan gas hidrogen menggunakan katalis copper, nikel alumina pada temperatur antara 170OC dan 250OC. Namun, karena direaksikan pada fasa uap maka kondisi operasi di reaktor berada pada rentang tekanan 1 – 5 atm.
Proses ini biasanya menggunakan katalis Copper sillicate atau Copper oxida . Furfural diumpankan ke dalam reaktor tubular fixed bed reactor yang didalamnya terdapat katalis copper oxide
berbentuk extrudate CuO di dalam pipa-pipa tubular reaktor. Sebelum masuk reaktor furfural diuapkan oleh vaporizer dan bersamaan dengan gas hidrogen diumpankan ke dalam reaktor.
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
Reaksi dapat berlangsung pada tekanan 2 atm dan temperatur 190OC. Reaksi bersifat eksotermis, sehingga untuk menjaga temperatur reaksi reaktor harus dilengkapi oleh sistem pendingin dengan konversi sebesar 80%.
Pada kondisi ini furfural harus dijaga dalam fase uap lewat jenuh agar tidak terjadi polimerisasi yang akan menghasilkan white water product serta mencegah pengembunan furfural di dalam pipa
katalis sehingga tidak terbentuk coloured product. Oleh karena itu, reaktor dioperasikan pada temperatur reaksi (190OC) namun tidak boleh lebih dari 200OC agar tidak terbentuk methylfuran (Swadesh. S, 1956).
Berikut reaksi yang terjadi :
C5H4O2(g) + H2(g) CuO C5H6O2(g) Furfural hidrogen P = 2 atm furfuril alkohol T = 190 o C
(US.Patent 2,754,304)
B. Pemilihan Proses
Pemilihan proses bertujuan untuk menentukan proses mana yang akan dipilih sehingga menguntungkan baik dari segi ekonomi, energi dan investasi alat.
B.1 Tinjauan Ekonomi
Tinjauan ekonomi ini bertujuan untuk mengetahui keuntungan yang dihasilkan oleh pabrik per kg produk yang dihasilkan pada masing-masing
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
proses yang akan digunakan. Berikut perbandingan keuntungan yang diperoleh melalui kedua proses di atas.
Disproposionasi aldehida (dengan NaOH) Reaksi yang terjadi adalah sebagai berikut :
2C5H4O2(l) + NaOH(l) C5H6O2(l) + C5H3O3Na(l) Furfural Sodium hidroksida Furfuril alkohol Asam furat
Basis : 1 kg C5H6O2 (produk/furfuril alkohol)
BM C5H6O2 : 98 g/mol dan BM C5H3O3Na (by product) = 134,24 g/mol BM C5H4O2 (bahan baku): 96 g/mol dan BM NaOH = 39,99 g/mol
Jumlah Produk C5H6O2 : mol gr gram / 1 , 98 000 . 1 1 = 10,194 mol
Konversi : 50 % terhadap furfural (C5H4O2) Reaksi : 2C5H4O2(l) + NaOH(l) C5H6O2(l) + C5H3O3Na(l) Mula-mula x 0,5x - - Bereaksi 20,388 10,194 10,194 10,194 Sisa x-20,388 0,5x-10,194 10,194 10,194 Mol mula-mula: x-0,5 x = x-20,388 0,5 x = x-20,388 = 40,776 mol C5H4O2 = x = 40,776 mol NaOH = 0,5 x = 20,388 mol 50%
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
Jumlah Reaktan yang dibutuhkan
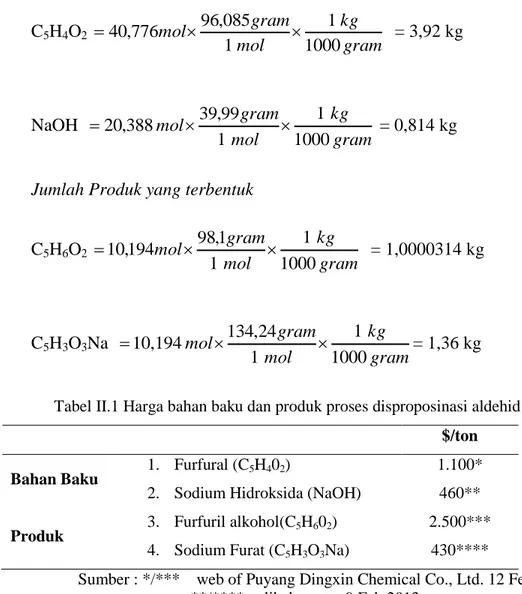
C5H4O2 gram kg mol gram mol 1000 1 1 085 , 96 776 , 40 = 3,92 kg NaOH gram kg mol gram mol 1000 1 1 99 , 39 388 , 20 = 0,814 kg
Jumlah Produk yang terbentuk
C5H6O2 gram kg mol gram mol 1000 1 1 1 , 98 194 , 10 = 1,0000314 kg C5H3O3Na gram kg mol gram mol 1000 1 1 24 , 134 10,194 = 1,36 kg
Tabel II.1 Harga bahan baku dan produk proses disproposinasi aldehid
$/ton Bahan Baku
Produk
1. Furfural (C5H402)
2. Sodium Hidroksida (NaOH) 3. Furfuril alkohol(C5H602) 4. Sodium Furat (C5H3O3Na)
1.100* 460** 2.500***
430****
Sumber : */*** web of Puyang Dingxin Chemical Co., Ltd. 12 Feb 2012 **/**** alibaba.com. 9 Feb 2013
Untuk menghitung perolehan keuntungan kasar dapat digunakan persamaan berikut ini :
EP = Harga Produk – Harga Bahan Baku
EP = ( Harga Furfuril alkohol+ harga sodium furat) - ( harga furfural + harga hidrogen)
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
EP = {(1,0000314 kg) ( $ 2,5/kg) + (1,36 kg) ( $ 0,43/kg)} – {(3,92 kg) ($ 1,1/kg) + (0,814) ($ 0,46/kg)}
EP = $ (3,585-5,078)/kg produk = - $ 1,493 /kg produk (-41%)
Proses Hidrogenasi
Reaksi yang terjadi adalah sebagai berikut : C5H4O2(g) + H2(g) C5H6O2(g)
Basis : 1 kg C5H6O2 (produk/furfuril alkohol) BM C5H6O2 : 98,1 g/mol
BM C5H4O2 (bahan baku): 96,085 g/mol dan BM H2 = 2 g/mol
Jumlah Produk C5H6O2 : 1 , 98 000 . 1 1 = 10,194 mol
Konversi : 80% terhadap furfural Reaksi : C5H4O2(g) + H2(g) C5H6O2(g) Mula-mula x - Bereaksi 10,194 10,194 10,194 Sisa x-10,194 10,194 Mol mula-mula : x-0,8000 x = x-10,194 0,2000 x = x-10,194 x = 12,7425 mol C5H4O2 = x = 12,7425 mol H2 = x = 10,1940 mol 80%
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
Jumlah Reaktan yang dibutuhkan
C5H4O2 gram kg mol gram mol 1000 1 1 96 7425 , 12 = 0,995 kg H2 gram kg mol gram mol 1000 1 1 2 10,194 = 0,0204 kg
Jumlah Produk yang terbentuk
C5H6O2 gram kg mol gram mol 1000 1 1 1 , 98 194 , 10 = 1,0000314 kg
Tabel II.2 Harga bahan baku dan produk proses hidrogenasi
$/ton Bahan Baku Produk 1. Furfural (C5H402) 2. Hidrogen (H2) 3. Furfuril alkohol(C5H602) 1.100* 3.000** 2.500***
Sumber : */*** web of Puyang Dingxin Chemical Co., Ltd. 12 Feb 2012 ** web of PT Samator Gas Indonesia. 9 Feb 2013
Untuk menghitung perolehan keuntungan kasar dapat digunakan persamaan berikut ini :
EP = Harga Produk – Harga Bahan Baku
EP = ( Harga furfuril alkohol) – { ( harga furfural + harga hidrogen)} EP = (1,0000314 kg) ( $ 2,5/kg)– {(0,995 kg) ($ 1,1/kg) + (0,0204) ($ 3/kg)}
EP = $ (3,0000942-(1,194+0,0714))/kg produk = $ 1,7347 /kg produk (137%)
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
B.2 Tinjauan Termodinamika
Perubahan entalpi (ΔH) menunjukkan panas reaksi yang dihasilkan ataupun panas reaksi yang dibutuhkan selama proses berlangsungnya reaksi kimia. Dalam hal ini, pada reaksi pembentukkan Furfuril alkoholdari furfural. Besar atau kecil nilai ΔH tersebut menunjukkan jumlah energi yang dibutuhkan maupun dihasilkan. ΔH bernilai positif (+) menunjukkan bahwa reaksi tersebut membutuhkan panas agar berlangsungnya reaksi sehingga semakin besar ΔH maka semakin besar juga energi yang dibutuhkan dan cost yang harus dikeluarkan. Sedangkan ΔH bernilai negatif (-) menunjukkan bahwa reaksi tersebut menghasilkan panas selama proses berlangsungnya reaksi sehingga tidak membutuhkan energi selama proses namun membutuhkan energi untuk penyerapan panas agar reaksi tetap berlangsung pada temperatur reaksinya. Penentuan panas reaksi yang berjalan secara eksotermis atau endotermis dapat dihitung dengan perhitungan panas pembentukan standar (ΔH°f) pada P = 1 atm dan T = 298 K.
B.2.1 Disproposionasi aldehida (dengan NaOH) Reaksi yang terjadi :
2C5H4O2(l) + NaOH(l) C5H6O2(l) + C5H3O3Na(l) Furfural Sodium hidroksida Furfuril alkohol Asam furat
Nilai ΔH°f masing-masing komponen pada suhu 298 K dapat dilihat pada Tabel II.3. sebagai berikut:
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
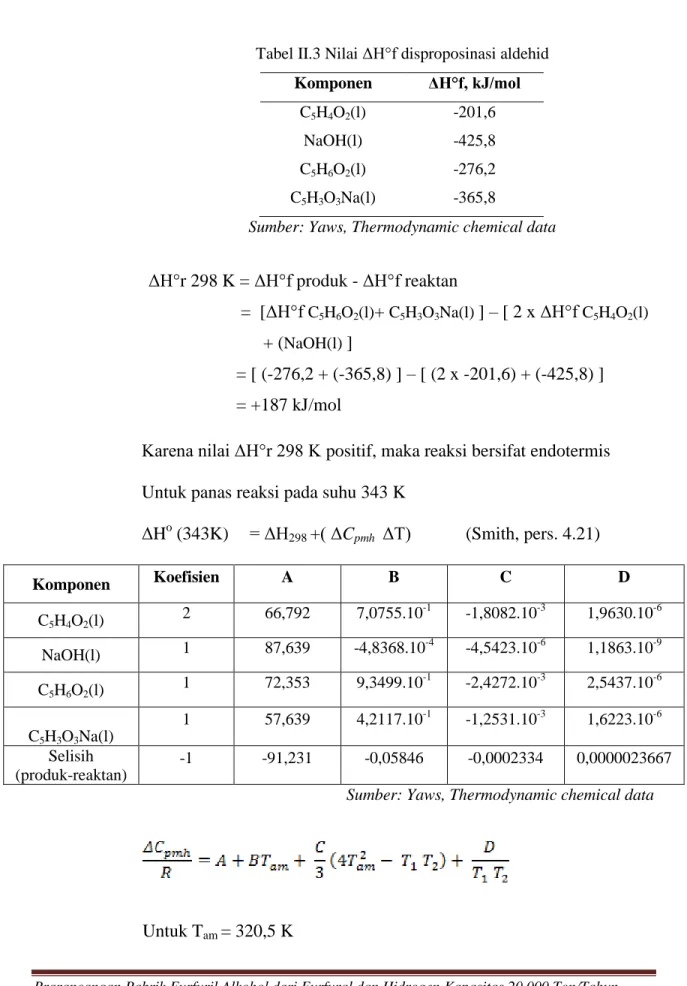
Tabel II.3 Nilai ΔH°f disproposinasi aldehid
Komponen ΔH°f, kJ/mol
C5H4O2(l) -201,6 NaOH(l) -425,8 C5H6O2(l) -276,2 C5H3O3Na(l) -365,8
Sumber: Yaws, Thermodynamic chemical data
ΔH°r 298 K = ΔH°f produk - ΔH°f reaktan
= [ΔH°f C5H6O2(l)+ C5H3O3Na(l) ] – [ 2 x ΔH°f C5H4O2(l) + (NaOH(l) ]
= [ (-276,2 + (-365,8) ] – [ (2 x -201,6) + (-425,8) ] = +187 kJ/mol
Karena nilai ΔH°r 298 K positif, maka reaksi bersifat endotermis Untuk panas reaksi pada suhu 343 K
ΔHo (343K) = ΔH298 +( ΔCpmh ΔT) (Smith, pers. 4.21) Komponen Koefisien A B C D C5H4O2(l) 2 66,792 7,0755.10 -1 -1,8082.10-3 1,9630.10-6 NaOH(l) 1 87,639 -4,8368.10 -4 -4,5423.10-6 1,1863.10-9 C5H6O2(l) 1 72,353 9,3499.10 -1 -2,4272.10-3 2,5437.10-6 C5H3O3Na(l) 1 57,639 4,2117.10-1 -1,2531.10-3 1,6223.10-6 Selisih (produk-reaktan) -1 -91,231 -0,05846 -0,0002334 0,0000023667
Sumber: Yaws, Thermodynamic chemical data
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
= -91,231 + ((-0,05846) x (320,5) + ((-0,0002334/3) x ( 4 x 320,5 2 – 298 x 343)) + 0,0000023667/ (298 x 343) ΔCpmh = 580,347 kJ/mol oK ΔHrx = 187 + (580,347 x (343 - 298) ) ΔHrx = +26.302,615 kJ/mol B.2.2 Proses Hidrogenasi Fasa cair
Reaksi yang terjadi :
C5H4O2(l) + H2(g) C5H6O2(l) Furfural Hidrogen Furfuril alkohol
Nilai ΔH°f masing-masing komponen pada suhu 298 K dapat dilihat sebagai berikut :
Tabel II.4 Nilai ΔH°f proses hidrogenasi cair
Komponen ΔH°f, kJ/mol
C5H4O2(l) -201,6
H2(g) 0
C5H6O2(l) -276,2
Sumber: Yaws, Thermodynamic chemical data
ΔH°r 298 K = ΔH°f produk - ΔH°f reaktan
= [ ΔH°f C5H6O2(l)] – [ΔH°f C5H4O2(l) + H2(g) ] = [(-276,2) – (-201,6)] kJ/mol
= -74,6 kJ/mol
Karena nilai ΔH°r 298 K negatif, maka reaksi bersifat eksotermis Untuk panas reaksi pada suhu 453 K
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
ΔHo (453K) = ΔH298 +( ΔCpmh ΔT) (Smith, pers. 4.21) Komponen Koefisien A B C D C5H4O2(l) 1 66,792 7,0755.10 -1 -1,8082.10-3 1,9630.10-6 H2(g) 1 25,399 2,0178.10 -2 -3,8549.10-6 3,1880.10-8 C5H6O2(l) 1 72,353 9,3499.10 -1 -2,4272.10-3 2,5437.10-6 Selisih (produk-reaktan) -1 30,960 0,09125 -0,007689 -0,000005499
Sumber: Yaws, Thermodynamic chemical data
Untuk Tam = 375,5 K = 30,960 + ((0,09125) x (375,5) + ((-0,007689/3) x ( 4 x 375,5 2 – 298 x 453)) + -0,000005499/ (298 x 453) ΔCpmh = -115,122 kJ/mol oK ΔHrx = -74,6+ (-115,122 x (543 - 298) ) ΔHrx = -17.918,51 kJ/mol Fasa uap
Reaksi yang terjadi :
C5H4O2(g) + H2(g) C5H6O2(g) Furfural Hidrogen Furfuril alkohol Nilai ΔH°f masing-masing komponen pada suhu 298 K dapat dilihat sebagai berikut:
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
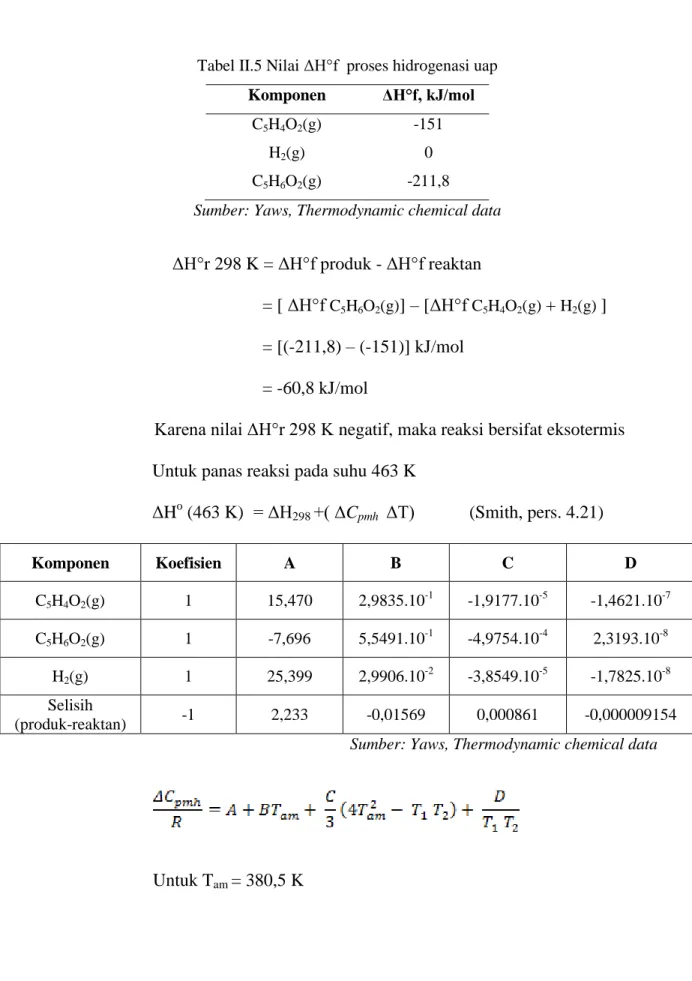
Tabel II.5 Nilai ΔH°f proses hidrogenasi uap
Komponen ΔH°f, kJ/mol
C5H4O2(g) -151
H2(g) 0
C5H6O2(g) -211,8
Sumber: Yaws, Thermodynamic chemical data
ΔH°r 298 K = ΔH°f produk - ΔH°f reaktan
= [ ΔH°f C5H6O2(g)] – [ΔH°f C5H4O2(g) + H2(g) ] = [(-211,8) – (-151)] kJ/mol
= -60,8 kJ/mol
Karena nilai ΔH°r 298 K negatif, maka reaksi bersifat eksotermis Untuk panas reaksi pada suhu 463 K
ΔHo (463 K) = ΔH298 +( ΔCpmh ΔT) (Smith, pers. 4.21) Komponen Koefisien A B C D C5H4O2(g) 1 15,470 2,9835.10-1 -1,9177.10-5 -1,4621.10-7 C5H6O2(g) 1 -7,696 5,5491.10-1 -4,9754.10-4 2,3193.10-8 H2(g) 1 25,399 2,9906.10 -2 -3,8549.10-5 -1,7825.10-8 Selisih (produk-reaktan) -1 2,233 -0,01569 0,000861 -0,000009154
Sumber: Yaws, Thermodynamic chemical data
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
= 2,233 + ((-0,01569) x (370,5) + ((0,000861/3) x ( 4 x 370,5 2 – 298 x 443)) + -0,000009154/ (298 x 443) ΔCpmh = -96,743 kJ/mol oK
ΔHrx = -60,8 + (96,743 x (443 - 298) ) ΔHrx = -14.088,355 kJ/mol
B.3 Tinjauan termodinamika berdasarkan energi Gibbs (ΔGo)
Energi Gibbs standar menunjukkan spontan atau tidak spontannya suatu reaksi kimia. ΔGo bernilai positif (+) menunjukkan bahwa reaksi tersebut tidak dapat berlangsung secara spontan, sehingga dibutuhkan energi tambahan dari luar. Sedangkan ΔGo bernilai negatif (-) menunjukan bahwa reaksi tersebut dapat berlangsung secara spontan dan hanya sedikit membutuhkan energi. Oleh karena itu, semakin kecil atau negatif ΔGo maka reaksi tersebut akan semakin baik karena untuk berlangsung spontan energi yang dibutuhkan semakin kecil.
B.3.1 Disproposionasi aldehida (dengan NaOH) Reaksi yang terjadi :
2C5H4O2(l) + NaOH(l) C5H6O2(l) + C5H3O3Na(l) Furfural hidroksida Furfuril alkohol Asam furat
Nilai ΔG°f masing-masing komponen pada suhu 298 K dapat dilihat pada Tabel II.6. sebagai berikut :
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
Tabel II.6 Nilai ΔG°f proses disproposionasi aldehida
Komponen ΔG°f, kJ/mol
C5H4O2(l) -102,87 NaOH(l) -419,2 C5H6O2(l) -154 C5H3O3Na(l) -275,8
Sumber: Yaws, Thermodynamic chemical data
ΔG° 298 K = ΔG°f produk - ΔG°f reaktan
= [ ΔG°f C5H6O2(l)+ C5H3O3Na(l) ] – [ 2 x ΔG°f C5H4O2(l) + (NaOH(l) ]
= [ (-154 + (-275,8) ] – [ (2 x -102,87) + (-419,2) ] = +195,14 kJ/mol
Karena nilai ΔG° 298 K positif, maka reaksi bersifat tidak spontan. Untuk energi Gibbs pada suhu ΔGo (343 K)
= A (T-To) + (T2-To2) + (T3-To3) + (T4-To4) = -91,231 (343-298) + (-0,05846/2)(3432-2982)+( -0,0002334/3)(3433-2983)+( 0,0000023667/4)(3434 -2984) = +322 ,098 Kj/kmol = A(ln T– ln To) + B(T-To) + (T2 - To2) + (T3 - To3) = -91,231(ln 343-ln 298)+( -0,05846)(343-298)+( - 0,0002334/2)(3432-2982)+( 0,0000023667/3)(3433-2983) = +21,355 kj/kmol dT R Cp R TT o
T dT R Cp R T To
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
GoR(T)
= +187 + (322,098-343((+187-195,14)/298)) -21,355 = +54 kj/kmol
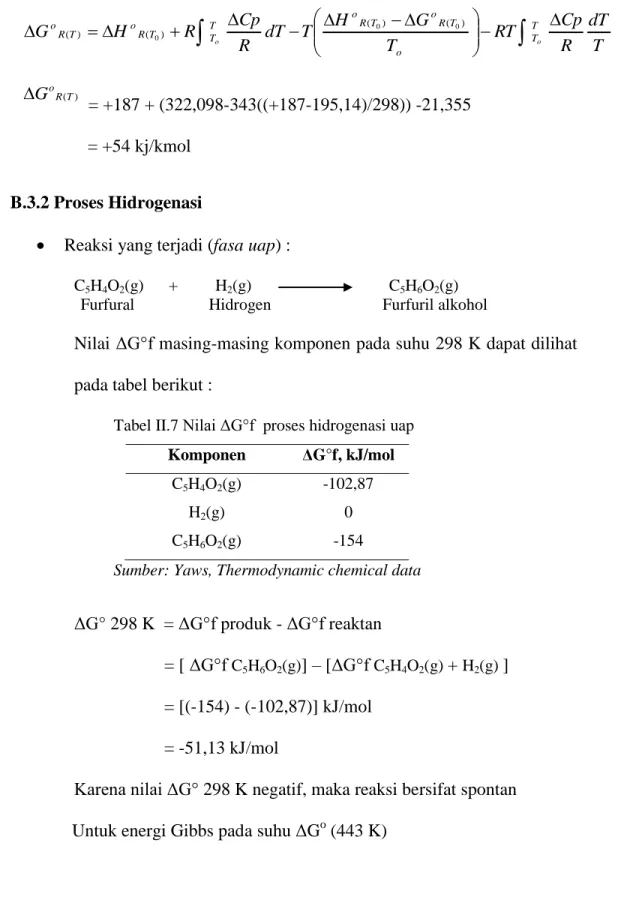
B.3.2 Proses Hidrogenasi
Reaksi yang terjadi (fasa uap) :
C5H4O2(g) + H2(g) C5H6O2(g) Furfural Hidrogen Furfuril alkohol
Nilai ΔG°f masing-masing komponen pada suhu 298 K dapat dilihat pada tabel berikut :
Tabel II.7 Nilai ΔG°f proses hidrogenasi uap
Komponen ΔG°f, kJ/mol
C5H4O2(g) -102,87
H2(g) 0
C5H6O2(g) -154
Sumber: Yaws, Thermodynamic chemical data
ΔG° 298 K = ΔG°f produk - ΔG°f reaktan
= [ ΔG°f C5H6O2(g)] – [ΔG°f C5H4O2(g) + H2(g) ] = [(-154) - (-102,87)] kJ/mol
= -51,13 kJ/mol
Karena nilai ΔG° 298 K negatif, maka reaksi bersifat spontan Untuk energi Gibbs pada suhu ΔGo (443 K)
T dT R Cp RT T G H T dT R Cp R H G TT o T R o T R o T T T R o T R o o o
( ) ( )
) ( ) ( 0 0 0Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
= A (T-To) + (T2-To2) + (T3-To3) + (T4-To4) = 2,233 (443-298) + (-0,01569/2)(4432-2982)+( -0,007689/3)(4433-2983)+( -0,000009154 /4)(4434 -2984) = -89,398 Kj/kmol = A(ln T– ln To) + B(T-To) + (T2 - To2) + (T3 - To3) = 2,233(ln 443ln298)+ (0,01569)(443298)+( -0,007689/2)( (4432-2982)+( -0,000009154/3)(4433 -2983) = -17,323 kj/kmol = -60,8+(-89,398)-443(-60,8-(-51,13))/298)-(-17,323) = -141,390 kj/kmol
Reaksi yang terjadi (fasa cair) :
C5H4O2(l) + H2(g) C5H6O2(l) Furfural Hidrogen Furfuril alkohol
Nilai ΔG°f masing-masing komponen pada suhu 298 K dapat dilihat pada tabel berikut :
dT R Cp R T To
T dT R Cp R T To
T dT R Cp RT T G H T dT R Cp R H G TT o T R o T R o T T T R o T R o o o
( ) ( )
) ( ) ( 0 0 0Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
Tabel II.8 Nilai ΔG°f proses hidrogenasi cair
Komponen ΔG°f, kJ/mol
C5H4O2(l) -134,14 H2(g) 0 C5H6O2(l) -206,5
Sumber: Yaws, Thermodynamic chemical data
ΔG° 298 K = ΔG°f produk - ΔG°f reaktan
= [ ΔG°f C5H6O2(l)] – [ΔG°f C5H4O2(l) + H2(g) ] = [(-206,5) – (-134,14)] kJ/mol
= -71,46 kJ/mol
Karena nilai ΔG° 298 K negatif, maka reaksi bersifat spontan. Untuk energi Gibbs pada suhu ΔGo (453 K)
= A (T-To) + (T2-To2) + (T3-To3) + (T4-To4) = 30,960(453-298)+(0,09125/2)(4532-2982 )+(-0,007689/3)(4533-2983)+(-0,000005499/4)(4533 -2983) = -102,472 kj/kmol = A(ln T– ln To) + B(T-To) + (T2 - To2) + (T3 - To3) = 30,960(ln453-ln298)+0,09125(453-298)+ ( -0,007689/2)(4532-2982)+( -0,000005499/3)(4533-2983) = -31,889 kj/kmol = -74,5+(-102,472)-453(-74,5-(-71,46))/298)-(-31,889) = -149,704 kj/kmol dT R Cp R TT o
T dT R Cp R TTo
T dT R Cp RT T G H T dT R Cp R H G TT o T R o T R o T T T R o T R o o o
( ) ( )
) ( ) ( 0 0 0Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
Berikut matrik dalam mempertimbangkan pemilihan metode yang akan digunakan:
Tabel II.9 Matrik pemilihan proses
No Parameter Diproposinasi dengan NaOH Hidrogenasi (Fasa cair) Hidrogenasi (fasa uap) 1 2 3 4 5 6 7 8 9 10 11 Temperatur reaksi Tekanan operasi Fasa reaksi Konversi Katalis Kemurnian produk Jenis reaktor Keuntungan Panas reaksi (ΔH0) Energi Gibbs (ΔGo ) Produk samping 70o C 10 atm Cair-Cair 50% - 97% Batch/CSTR - $ 1,493/kg produk (-41%) +26.302,615 kJ/mol +54 kJ/mol - 150-250 o C 10-29 atm Cair-Gas Hingga 99% Copper, nickle, titanium 90% Autoclave $ 1,7347 /kg produk (137%) -17.918,51 kJ/mol -149,704 kJ/mol Methylfuran 170-250 o C 1-5 atm Vapor-Gas 80%-99% Copper, nickle, titanium 99%
Fixed bed multitube
$ 1,7347 /kg produk (137%) -14.088,355 kJ/mol
-141,390 kJ/mol
-
Berdasarkan matrik metode proses hidrogenasi di atas, maka di pilih proses hidrogenasi dengan katalis Copper oxide (CuO) pada fasa uap untuk memproduksi furfuril alkohol dari furfural dan/hidrogen karena pertimbangan memberikan kondisi operasi yang relatif aman dan kemurnian yang dihasilkan lebih baik dari metode yang lain.
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
C. Deskripsi Proses
Proses pembuatan furfuril alcohol melalui beberapa tahap sebagai berikut :. 1. Tahap penyiapan bahan baku
2. Tahap pembentukan produk 3. Tahap pemurnian produk
C.1 Tahap penyiapan bahan baku
Bahan baku furfural cair diperoleh dari PT Sree International Indonesia dan langsung diangkut menuju pabrik menggunakan transportasi darat. Furfural yang dibeli terdiri dari 99,4% furfural dan 0,6% air (persen berat) disimpan dalam tangki penyimpanan bahan baku (ST-101) pada temperatur ruangan 300C dan tekanan 1 atm. Dari tangki penyimpanan, furfural dialirkan oleh pompa (P-101) menuju Adsorber (AD-101) untuk menghilangkan kandungan 100% air didalamnya agar memperoleh kemurnian produk yang tinggi dan peralatan seperti reaktor tidak mudah teroksidasi dengan menggunakan adsorben zeolit dan dalam kondisi isotermal (tidak ada perubahan suhu). Setelah itu bahan diumpankan menuju vaporizer (VP-101) dimana furfural cair akan diubah fasanya menjadi uap. Kemudian oleh separator drum (SD-101) keluaran vaporizer akan dipisahkan antara fasa uap
dan fasa cair nya. Fasa uap langsung diumpankan ke dalam reaktor dan fasa cair (kondensat) diumpankan kembali ke vaporizer setelah dicampur dengan fresh feed untuk diuapkan kembali.
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
Gas hidrogen 99,24% (persen mol) dibeli dari PT Air Liquid melalui sistem piping. Setelah tekanan nya diturunkan oleh Expander (EV-101) bahan baku gas ini dipanaskan oleh Heater (HT-101) untuk kemudian bercampur dengan bahan baku lain di mixing point (MP-103). Dari MP-103 bahan diumpankan ke dalam reaktor fixed bed multitube (RE-201) melalui bagian atas reaktor yang didalamnya telah terdapat katalis-katalis.
C.2 Tahap pembentukan produk dan pemisahan produk
Di dalam reaktor terdapat tube-tube yang berisi tumpukan katalis copper silicate, kemudian umpan akan melewati katalis dan terjadi reaksi
hidrogenasi furfural sebagai berikut :
Reaksi utama : C5H4O2(g) + H2(g) C5H6O2(g)
Reaksi terjadi pada fase gas-uap dengan katalis copper silicate pada kisaran temperatur 1900C dan tekanan 2 atm. Karena reaksi bersifat eksotermis, untuk mempertahankan temperatur dalam reaktor maka diberi pendingin. Hasil keluaran reaktor berupa uap furfuril alkohol dan furfural juga gas hidrogen, nitrogen dan oksigen.
Bahan yang keluar dari reaktor ini dialirkan menuju kondensor (CD-201) untuk mengkondensasikan seluruh furfuril alkohol dan furfural. Kemudian keluaran CD-201 ini akan dialirkan menuju Separator Drum (SD-201) untuk dipisahkan antara gas dan cairan nya. Gas sebagian di recycle ke
Prarancangan Pabrik Furfuril Alkohol dari Furfural dan Hidrogen Kapasitas 20.000 Ton/Tahun Jurusan Teknik Kimia Fakultas Teknik Universitas Lampung
reaktor dan sebagian lagi di purge. Sedangkan cairan dialirkan menuju heater untuk kemudian diumpankan ke dalam menara distilasi untuk dimurnikan.
C.3 Tahap pemurnian produk
Untuk mendapatkan kemurnian sesuai dengan yang diharapkan cairan dimurnikan dengan menggunakan distilasi. Cairan furfural dan furfuril alkohol dipanaskan oleh heater (HT-301) hingga suhunya sesuai dengan suhu operasi menara distilasi. Aliran bottom product kaya akan furfuril alkohol dialirkan menuju tangki penampungan produk (ST-301) dalam wujud cair setelah didinginkan oleh Cooler (HE-301). Sedangkan top product sebagian diembunkan oleh Condensor (CD-301) dan dipisahkan
antara fasa uap dan fasa cair nya oleh Separator Drum (SD-301) dimana fasa uap produk inilah yang akan dikembalikan ke reaktor (RE-201).