OKTILBENZAMIDA DAN UJI BIOAKTIVITAS SECARA IN VITRO TERHADAP SEL KANKER MURINE LEUKEMIA P-388
Tesis Magister Sains Ilmu Kimia
H U S N I A T I 0606001746
Program Sudi Magister Ilmu Kimia
Pasca Sarjana Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Indonesia
2008
OKTILBENZAMIDA DAN UJI BIOAKTIVITAS SECARA IN VITRO TERHADAP SEL KANKER MURINE LEUKEMIA P-388
Tesis ini diajukan sebagai salah satu syarat untuk memperoleh gelar Magister Sains Ilmu KImia
H U S N I A T I 0606001746
Program Sudi Magister Ilmu Kimia
Pasca Sarjana Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Indonesia
2008
PIKOLINAMIDA, 2-HIDROKSI-N-FENIL-BENZAMIDA, 3-HIDROKSI-N- FENILPIKOLINAMIDA, dan 2-HIDROKSI-N-OKTILBENZAMIDA DAN UJI
BIOAKTIVITAS SECARA IN VITRO TERHADAP SEL KANKER MURINE LEUKEMIA P-388
Husniati
UK-3A adalah senyawa antibiotika untuk anti kanker dan anti jamur.
UK-3A telah diisolasi sebagai komponen minor dari miselium Streptomyces sp. 512-02 dan mempunyai gugus aktif hidroksil, amida, dan dilakton cincin sembilan yang terbukti aktif menghambat pertumbuhan bakteri dan sel kanker. Untuk mensintesis senyawa tersebut membutuhkan proses sintesis yang rumit dan waktu yang cukup lama. Telah disintesis senyawa antibiotik baru, yaitu analog UK-3A berdasarkan modifikasi gugus aktif senyawa UK- 3A. Modifikasi gugus aktif dalam senyawa UK-3A dimungkinkan untuk
mendapatkan senyawa analog yang mempunyai bioaktivitas yang sama atau lebih aktif dari senyawa UK-3A induk. Senyawa analog pada penelitian ini adalah 3-hidroksi–N-oktilpikolinamida [S1], 2-hidroksi-N-fenil-benzamida [S2], 3-hidroksi-N-fenilpikolinamida [S3], dan 2-hidroksi-N-oktilbenzamida
rute reaksi yang lebih sederhana, dan mempunyai bioaktivitas dalam menghambat pertumbuhan sel kanker terutama leukemia. Senyawa- senyawa hasil sintesis tersebut diidentifikasi menggunakan UV, FT-IR, 1H- NMR, dan 13C-NMR. Hasil uji bioaktivitas secara in vitro terhadap sel kanker Murine leukemia P-388 memperlihatkan kemampuan penghambatan
terhadap pertumbuhan sel kanker yang lebih tinggi dibandingkan dengan senyawa UK-3A yaitu IC50 [S1]= 13,2; [S2]=7,75; [S3] =18,5; dan [S4]= 7,5 µg/mL, sementara IC50 UK-3A adalah 38 µg/mL.
Kata kunci : UK-3A, antikanker, Streptomyces sp. 512-02, P-388.
ix + 105 halaman, gambar, tabel, lampiran
PICOLINAMIDE, 2-HYDROXY-N-PHENYL-BENZAMIDE, 3-HYDROXY-N- PHENYLPICOLINAMIDE, and 2-HYDROXY-N-OCTYLBENZAMIDE, and IN
VITRO ACTIVITY TEST AGAINST MURINE LEUKEMIA P388 CANCER CELL
Husniati
The Synthesis UK-3A analogs i.e 3-hydroxy–N-octylpicolinamide [S1], 2-hydroxy-N-phenyl-benzamide [S2], 3-hydroxy-N-phenylpicolinamide [S3], and 2-hydroxy-N-octylbenzamide [S4] were obtained by modification of UK- 3A. UK-3A was isolated from the Streptomyces sp. 512-02 mycelium and has been elucidated as a nine membered ring dilactone derivative possessing hydroxyl (OH) and amide (CONH) moieties . The compound shows ability to inhibit bacterial and cancer cell growth. The analogs were synthesized by amidation of carboxylate. The structure of products were confirmed by 1H- and 13C-NMR, FT-IR, and also UV spectrophotometer. The result of bioassay showed that their compound inhibits the growth of cancer cell Murine leukemia P-388. That’s higher compared to that of UK-3A with IC50
are 13,2 µg/mL for [S1], 7,75 for [S2], 18,5 for [S3], and 7,5 for [S4], respectively. Whereas IC50 for UK-3A is 38 µg/mL.
Keywords: UK-3A, anticancer, Streptomyces sp. 512-02, P-388.
ix + 105 pages, figure, table, appendix
Puji syukur penulis panjatkan kepada Allah SWT yang telah
melimpahkan rahmat dan karunia-Nya sehingga tesis ini dapat diselesaikan.
Tesis ini berjudul “Sintesis Senyawa Analog Uk-3A : 3-Hidroksi–N- oktilpikolinamida, 2-Hidroksi-N-fenilbenzamida, 3-Hidroksi-N-
fenilpikolinamida, dan 2-Hidroksi-N-oktilbenzamida, dan Uji Bioaktivitas Secara In Vitro terhadap Sel Kanker Murine Leukemia P-388” sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada Program Pasca Sarjana Ilmu Kimia Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Indonesia.
Penulis mengucapkan terima kasih kepada Dr. Endang Saepudin dan Dr. Muhammad Hanafi selaku pembimbing atas semua bimbingan,
dukungan, saran dan arahannya. Ucapan terimakasih juga ditujukan kepada Badan Pusdiklat Departemen Perindustrian dan Balai Riset Standarisasi Industri Bandar Lampung atas pendanan dan izin tugas belajar. Program Pascasarjana Kimia FMIPA UI tempat penulis menimba ilmu dan
pengetahuan, tidak lupa mengucapkan terima kasih kepada Kimia-LIPI di kawasan Pusat Penelitian Ilmu dan Teknologi (Puspiptek), Serpong, yang telah menyediakan fasilitas lab dan bahan penelitian, serta ungkapan terima kasih yang teramat dalam kepada suami, H.Indra Utama, anak-anak;
Muhammad Putra Hutama, Ilma Puteri Hutami, dan Aisyah Puteri Hutami,
keluarga besar H.Syafri Hasan Basri, serta keluarga besar H.Tarimi Mahmud, atas cinta dan dukungannya selalu setiap saat memberikan kebahagiaan, restu, doa yang paling mulia, serta kasih sayangnya demi kelancaran dan semagat untuk menyelesaikan studi. Terakhir, penulis sampaikan terimakasih kepada rekan-rekan S2 UI, rekan-rekan Lab Kimia LIPI, rekan-rekan Baristand Bandar Lampung atas support dan bantuannya yang tak ternilai harganya. Semoga Allah SWT membalas budi kebaikan kita semua. Amin
Terakhir, penulis sampaikan “Semoga tesis ini bermanfaat”.
Depok, Mei 2008
Husniati
Halaman DAFTAR JUDUL ………
LEMBAR PERSETUJUAN ………...
KATA PENGANTAR ………..
DAFTAR ISI ………
DAFTAR GAMBAR ………...
DAFTAR TABEL ……….
DAFTAR LAMPIRAN ……….
ABSTRAK ………...
ABSTRACT ……….
I. PENDAHULUAN ……….
1.1. Latar Belakang ………...
1.2. Tujuan Penelitian ………...
1.3. Manfaat Penelitian ……….
1.4. Hipotesis ………..
II. TINJAUAN PUSTAKA ………...
2.1. Senyawa UK-3A ………...
2.2. Sintesis Senyawa Analog UK-3A ………..
2.3. Strategi Perancangan Sintesis Senyawa Analog UK-3A ……...
2.4. Reaksi Amidasi ……….
2.5. Perkembangan Senyawa Analog UK-3A ……….
i ii iv vi ix xi xiii xiv xvi 1 1 5 6 6 7 7 13 14 19 22
2.6. Uji sitotoksisitas ………...
2.7. Penyakit Kanker dan Leukemia ……….
III. METODOLOGI PENELITIAN ……….
3.1. Waktu dan Tempat Penelitian ………...
3.2. Bahan dan Alat ……….
3.2.1. Bahan ………..
3.2.2 Alat ………...
3.3. Prosedur Penelitian ………..
3.3.1. Sintesis Senyawa Analog UK-3A …………...
A. 3-hidroksi-N-oktilpikolinamida [S1] ...
B. 2-hidroksi-N-fenil-benzamida [S2] ...
C. 3-hidroksi-N-fenilpikolinamida [S3] ...
D. 2-hidroksi-N-oktilbenzamida [S4] ...
3.3.2. Prosedur Identifikasi Senyawa ...
A. KLT (Kromatografi Lapis Tipis) ...
B. Spektrofotometer UV (Ultra Violet) ...
C. Spektrofotometer FT-IR ...
D. Spektrometer NMR ...
3.3.3.Uji Sitotoksisitas sel Kanker Murine leukemia P388 …….
IV. HASIL DAN PEMBAHASAN ………..
4.1. Sintesis Senyawa Analog UK-3A ………..
4.1.1. Sintesis 3-hidroksi-N-oktilpikolinamida [S1] ...
4.1.2. Sintesis 2-hidroksi-N-fenilbenzamida [S2] ...
24 26 30 30 30 30 31 31 32 32 34 35 36 37 37 38 38 38 39 40 40 40 43
4.1.3. Sintesis 3-hidroksi-N-fenilpikolinamida [S3] ...
4.1.4. Sintesis 2-hidroksi-N-oktilbenzamida [S4] ...
4.2. Analisis Senyawa Menggunakan Spektrum UV ………..
4.2.1. Senyawa 3-hidroksi-N-oktilpikolinamida [S1] ...
4.2.2. Senyawa 2-hidroksi-N-fenilbenzamida [S2] ...
4.2.3. Sintesis 3-hidroksi-N-fenilpikolinamida [S3] ...
4.2.4. Sintesis 2-hidroksi-N-oktilbenzamida [S4] ...
4.3. Analisis Senyawa Menggunakan Spektrum IR ………..
4.3.1. Senyawa 3-hidroksi-N-oktilpikolinamida [S1] ... ...
4.3.2. Senyawa 2-hidroksi-N-fenilbenzamida [S2] ...
4.3.3. Sintesis 3-hidroksi-N-fenilpikolinamida [S3] ...
4.3.4. Sintesis 2-hidroksi-N-oktilbenzamida [S4] ...
4. 4. Analisis Senyawa Menggunakan Spektrum NMR ……….
4.4.1. Senyawa 3-hidroksi-N-oktilpikolinamida [S1] ...
4.4.2. Senyawa 2-hidroksi-N-fenilbenzamida [S2] ...
4.4.3. Sintesis 3-hidroksi-N-fenilpikolinamida [S3] ...
4.4.4. Sintesis 2-hidroksi-N-oktilbenzamida [S4] ...
4.5. Uji Sitotoksisitas Sel Kanker Murine leukemia P-388 ...
V. KESIMPULAN dan SARAN ...
5.1. Kesimpulan ...
5.2. Saran ………..
DAFTAR PUSTAKA ………..
LAMPIRAN ………..
45 46 49 50 51 53 54 55 55 57 58 59 60 61 64 67 70 73 78 78 79 80 86
DAFTAR GAMBAR
Halaman 1.
2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
12.
13.
14.
Struktur UK-2A, UK-3A, dan Antimisin A3 ... .9 Struktur senyawa UK-2A (OMe), UK-2A (NMe), dan hasil
hidrolisis senyawa UK-2A ... 12 Struktur molekul hidrolisis UK-3A ... 17 Retrosintesis senyawa A=pikolinamida (R=C8H17/C6H5) dan
senyawa B=benzamida (R=C8H17/C6H5) ... 19 Tahapan reaksi pembentukan senyawa A=pikolinamida
(R=C8H17/C6H5) dan senyawa B= benzamida (R=C8H17/C6H5) ... 20 Mekanisme reaksi pengaktifan gugus karboksilat oleh aktivator
DCC ... 22 Mekanisme katalisis reaksi amidasi yang dikatalisis oleh DMAP
dan diaktivasi oleh DCC ... 23 Reaksi reduksi MTT menjadi formazan ... 27 Mekanisme reaksi sintesis 3-hidroksi-N-oktilpikolinamida [S1]...
Mekanisme reaksi sintesis 2-hidroksi-N-fenilbenzamida [S2] …...
Mekanisme reaksi sintesis 3-hidroksi-N-fenilpikolinamida [S3]…..
Mekanisme reaksi sintesis 2-hidroksi-N-oktilbenzamida [S4]...
Spektrum UV senyawa 3-hidroksi-N-oktilpikolinamida [S1]
dengan λmax = 246, 298,5, dan 326 nm ...
Spektrum UV senyawa 2-hidroksi-N-fenilbenzamida [S2] dengan 9
11 15
18
18
20
21 25 41 44 46 48
51
15.
16.
17.
18.
19.
20.
λmax = 246, 298,5, dan 328,5 nm...
Spektrum UV senyawa 3-hidroksi-N-fenilpikolinamida [S3]
dengan λmax =246, 298,5, dan 354,5 nm………...
Spektrum UV senyawa 2-hidroksi-N-oktilbenzamida [S4] dengan λmax 246nm, 299,5 dan 324nm ………...
Struktur senyawa 3-hidroksi-N-oktilpikolinamida [S1] ...
Struktur senyawa 2-hidroksi-N-fenilbenzamida [S2] ... 65 Struktur senyawa 3-hidroksi-N-fenilpikolinamida [S3] ...
Struktur senyawa 2- hidroksi-N-oktilbenzamida [S4] ………..
52
54
55 61 64 67 70
DAFTAR TABEL
Halaman 1.
2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
Nilai IC50 (µg/mL) dari hasil senyawa UK-3A,UK-2A, UK-2 (OMe), UK-2 (NMe), dan AA terhadap uji hambatan
pertumbuhan sel kanker ...
Sintesis beberapa senyawa analog UK-3A berdasarkan
modifikasi dilakton cincin sembilan ... 25 Karakteristik dan hasil perhitungan rendemen senyawa analog
hasil sintesis ………..
Daftar daerah spektrum gugus fungsi senyawa [S1] …………...
Daftar daerah spektrum gugus fungsi senyawa [S2] …………...
Daftar daerah spektrum gugus fungsi senyawa [S3] …………...
Daftar daerah spektrum gugus fungsi senyawa [S4] …………...
Data pergeseran kimia (δ, ppm) spektrum 1H-NMR dan 13C-NMR senyawa [S1] (CDCl3, 500 MHz) ………...
Data pergeseran kimia (δ, ppm) spektrum 1H-NMR dan 13C-NMR senyawa [S2] (CDCl3, 500 MHz) ………...
Data pergeseran kimia (δ, ppm) spektrum 1H-NMR dan 13C-NMR senyawa [S3] (CDCl3, 500 MHz) ………...
Data pergeseran kimia (δ, ppm) spektrum 1H-NMR dan 13C-NMR senyawa [S4] (CDCl3, 500 MHz) ………...
Hasil uji sitotoksisitas senyawa analog UK-3A terhadap sel
12
23
43 56 57 58 60
62
65
68
71
12.
13.
kanker Murine leukemia P-388 ………...
Analisis nilai logP dari senyawa analog UK-3A baru, UK-3A, taxol, dan antimisin A3 ………..
74
77
DAFTAR LAMPIRAN
Halaman 1.
2.
3.
4.
5.
6.
7.
8.
9.
10.
11.
12.
13.
14
Perhitungan Rendem……….
Spektrum FT-IR senyawa 3-hidroksi-N-oktilpikolinamida [S1]....
Spektrum FT-IR senyawa 2-hidroksi-N-fenilbenzamida [S2]…..
Spektrum FT-IR senyawa 3-hidroksi-N-fenilpikolinamida [S3] ...
Spektrum FT-IR senyawa 2-hidroksi-N-oktilbenzamida [S4] …..
Spektrum 1H-NMR 3-hidroksi-N-oktilpikolinamida [S1] ………...
Spektrum 13C-NMR 3-hidroksi-N-oktilpikolinamida [S1]………...
Spektrum 1H-NMR 2-hidroksi-N-fenilbenzamida [S2]…………...
Spektrum 13C-NMR 2-hidroksi-N-fenilbenzamida [S2]………….
Spektrum 1H-NMR 3-hidroksi-N-fenilpikolinamida[S3]………….
Spektrum 13C-NMR 3-hidroksi-N-fenilpikolinamida [S3] ………..
Spektrum 1H-NMR 2-hidroksi-N-oktilbenzamida [S4]…………...
Spektrum 13C-NMR 2-hidroksi-N-oktilbenzamida [S4]………….
Hasil uji aktivitas secara invitro terhadap Murine leukemia P-388 ………
86 87 88 89 90 91 92 93 94 95 96 97
98
1.1. Latar Belakang
Berdasarkan catatan Badan Kesehatan Dunia, WHO (World Health Organization), mengenai jumlah penderita kanker di dunia terjadi
pertambahan setiap tahun sekitar 6,25 juta orang dan diperkirakan dalam 10 tahun mendatang 9 juta orang akan meninggal akibat penyakit yang
menakutkan ini. Jumlah penderita kanker di dunia sebagian besar terdapat di negara-negara berkembang dan Indonesia sebagai salah satu negara
berkembang, diperkirakan setiap tahunnya memiliki angka prevalensi yang tinggi yaitu 100 penderita kanker yang baru dari setiap 100.000 jumlah penduduk (Yayasan Kanker Indonesia, 2006). American Cancer Society melaporkan pada tahun 2007 telah terjadi kematian di dunia karena penyakit kanker sebanyak 7,6 juta (Wikipedia, 2008). Hasil Survai Kesehatan Rumah Tangga (SKRT) Departemen Kesehatan RI menyatakan bahwa jumlah
kematian yang disebabkan kanker meningkat terhadap jumlah penduduk dari tahun ke tahun yaitu tahun 1989 terdapat 4,5 % jumlah kematian, 4,7% pada tahun 1992, dan 4,9 % pada tahun 1995 (Yayasan Kanker Indonesia, 2006).
Fakta yang ada dari pertambahan jumlah penderita kanker yang terjangkit setiap tahun menandakan bahwa masalah tersebut dipicu oleh kemajuan peradaban yang semakin pesat dalam berbagai bidang yang ada hubungannya dengan penyebab kanker yang tidak dapat dihindari. Sebagian besar timbulnya kanker disebabkan oleh gaya hidup yang tidak sehat seperti
kebiasaan makan tidak seimbang, kebiasaan merokok dan minum alkohol, paparan bahan radioaktif atau sinar matahari yang berlebihan, dan
pencemaran lingkungan oleh limbah bahan berbahaya. Hal-hal tersebut dapat memberi kontribusi dalam memperburuk kondisi kesehatan
masyarakat saat ini dan memberikan akibat munculnya berbagai jenis kanker sebagai faktor dominan penyebab kematian seseorang (Siswondono, 2004, Wikipedia, 2008).
Penyakit kanker ditandai oleh kontrol pertumbuhan dan pembagian sel yang tidak terbatas dan bersifat agresif, invasif dan menyebar ke jaringan dan bagian tubuh yang lain. Kanker dapat terjadi pada semua orang baik tua maupun muda pada berbagai organ tubuh manusia (Wikipedia, 2008).
Penyakit kanker darah (leukemia) di Indonesia menduduki peringkat tertinggi pada usia anak-anak. Penderita kanker darah dapat mencapai 25-30 persen dari seluruh penderita kanker. dr. Djajadiman Gatot dari sub bagian
hematologi-onkologi, bagian ilmu kesehatan anak Fakultas Kedokteran Universitas Indonesia Rumah Sakit Cipto Mangunkusumo (FKUI-RSCM), menjelaskan, terjadinya leukemia disebabkan bertambahnya sel darah putih abnormal secara berlebihan dan tidak terkendali, menyebar ke seluruh bagian tubuh mengakibatkan gangguan bahkan merusak fungsi tubuh.
Selain penyakit leukemia banyak terjadi pada usia anak, penyakit lain seperti tumor otak, kanker mata/ retinoblastoma, dan kanker usus juga banyak
menyerang anak-anak (Siswandono, 2004).
Perkembangan yang pesat dari jumlah penderita kanker yang mengalami kematian mendorong berbagai upaya dalam melakukan
penelitian, penemuan, dan produksi obat untuk diagnosis, pengobatan, maupun pencegahan yang lebih tepat. Penelitian tentang berbagai obat yang berpotensi sebagai antikanker telah dilakukan mulai dari isolasi bahan alam sampai dengan sintesis senyawa obat baru. Senyawa obat yang diperoleh dari hasil isolasi bahan alam dari berbagai sumber seperti tumbuhan, hewan, maupun mikroorganisme terdapat dalam jumlah yang terbatas. Kemajuan teknologi memungkinkan untuk melakukan sintesis senyawa obat baru
berdasarkan modifikasi struktur antibiotika yang sebelumnya telah ditemukan secara alamiah dari hasil isolasi bahan alam. Penemuan obat baru dengan cara pengembangan struktur senyawa induk yang telah diketahui
aktivitasnya diyakini lebih ekonomis, efisien, dan sederhana, sehingga pengembangan sintesis senyawa obat baru tersebut dapat memiliki aktivitas antikanker mendekati aktivitas senyawa aslinya atau lebih aktif (Siswandono
& Soekardjo, 2000, Patrick, 2001).
UK-3 sebagai komponen minor telah berhasil diisolasi dari miselium Streptomyces sp. 517-02. Senyawa UK-3 merupakan senyawa kompleks
yang terdiri dari lima komponen yaitu: UK-3A, UK-3B, UK-3C, UK-3D, dan UK-3E, dan senyawa UK-3A merupakan komponen utamanya. Senyawa UK- 2 sebagai komponen mayor juga telah diisolasi dari isolat tersebut dan memiliki aktivitas sebagai anti bakteri dan anti jamur (Shimano, et al., 1998) sedangkan senyawa UK-3A memiliki aktivitas dalam menghambat
pertumbuhan jamur, bakteri, dan sel kanker, sehingga berpotensi untuk dijadikan sebagai salah satu obat anti jamur, anti bakteri dan anti kanker (Hanafi, 1995). Ueki, et al., (1997) melaporkan bahwa senyawa UK-3A telah
terbukti memiliki daya sitotoksik terhadap pertumbuhan sel kanker Murine leukemia P-388 dengan nilai IC50 sebesar 1,5 µg/mL (Ueki, et al., 1997a, Ueki, et al., 1997b ). Sintesis senyawa UK-3A dilakukan melalui beberapa rute reaksi
yang cukup panjang sehingga memerlukan pembiayaan yang cukup besar dan kurang ekonomis (Hanafi, 1995). Sintesis senyawa baru berdasarkan
modifikasi struktur UK-3A telah dirancang untuk memperoleh senyawa analog dengan UK-3A induk, sintesis tersebut dilakukan melalui rute reaksi lebih sederhana dan memerlukan pembiayaan yang cukup ringan namun tetap memiliki aktivitas biologi relatif sama atau lebih besar dari senyawa UK-3A induk.
Penelitian ini dilakukan untuk mensintesis empat senyawa baru analog UK-3A yaitu senyawa 3-hidroksi-N-oktilpikolinamida [S1], 2-hidroksi-N-fenil- benzamida [S2], 3-hidroksi-N-fenilpikolinamida [S3], dan 2-hidroksi-N- oktilbenzamida [S4]. Sintesis beberapa senyawa baru tersebut dilakukan melalui satu tahapan reaksi yaitu reaksi amidasi. Keempat senyawa analog tersebut diharapkan dapat dikembangkan untuk mendapatkan senyawa obat dengan rendemen (yield) yang cukup tinggi, mempunyai aktivitas dalam menghambat pertumbuhan sel kanker terutama leukemia, dan dihasilkan dari reaksi sederhana. Masing-masing rancangan senyawa analog tersebut
memiliki gugus aktif yang sama dengan UK-3A seperti gugus hidroksil (-OH) dan amida (-CONH). Gugus aktif tersebut memiliki aktivitas dalam
menghambat pertumbuhan sel kanker maupun mikroba (Hanafi, 1997).
Modifikasi percobaan sintesis senyawa baru dalam penelitian ini dibuat dengan cara melakukan:
a. variasi dalam rantai samping amida struktur UK-3A dengan gugus aromatik dan gugus alifatik rantai panjang yang bersifat lipofilik.
b. variasi gugus hidroksil dari cincin aromatik yang diikat oleh gugus piridin (pikolinat) atau gugus fenol (salisilat).
Hasil penelitian yang telah dilaporkan sebelumnya (Wulandari, 2007, Adinata, 2007) bahwa modifikasi dilakton rantai tertutup yang sulit disintesis diubah menjadi rantai terbuka yang mengandung rantai panjang dan bersifat lipofilik dapat memberikan aktivitas terhadap sel kanker leukemia. Hasil sintesis senyawa analog pada penelitian ini diharapkan dapat memberikan pula
informasi ilmiah mengenai pengaruh kehilangan dilakton cincin sembilan menjadi senyawa amida yang terbentuk dari ikatan amida dengan asam aromatiknya melalui beberapa perlakuan percobaan yang telah disebutkan di atas dan selanjutnya dilakukan uji aktivitas biologi dalam menghambat
pertumbuhan sel kanker Murine leukemia P-388.
1.2. Tujuan penelitian:
1. Melakukan sintesis senyawa analog UK-3A melalui reaksi amidasi terhadap senyawa 3-hidroksi-N-oktilpikolinamida [S1], 2-hidroksi-N- fenil-benzamida [S2], 3-hidroksi-N-fenilpikolinamida [S3], dan 2- hidroksi-N-oktilbenzamida [S4].
2. Menentukan aktivitas biologi dari masing-masing senyawa hasil sintesis terhadap sel kanker Murine leukemia P-388 dibandingkan
dengan aktivitas biologi senyawa Antimisin A3 (AA) sebagai standar senyawa yang memiliki sifat antibiotik dan antikanker.
1.3. Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan kajian dan informasi ilmiah mengenai hasil síntesis senyawa analog baru yang kemungkinan mempunyai potensi sebagai obat antikanker seperti UK-3A. Senyawa- senyawa yang dihasilkan tersebut adalah senyawa sederhana dan dapat dikembangkan sebagai calon obat antikanker yang bermanfaat untuk
penyembuhan penyakit kanker. Modifikasi gugus fungsi yang telah dirancang dalam penelitian ini bermanfaat untuk mendapatkan informasi mengenai hubungan struktur kimia relatif terhadap aktivitas biologi senyawa dalam menghambat pertumbuhan sel kanker leukemia secara invitro.
1.4. Hipotesis
a. Variasi gugus aktif bersifat non polar atau lipofilik dari senyawa analog dapat mempengaruhi aktivitas biologi senyawa dalam menghambat pertumbuhan sel kanker Murine leukemia P-388.
b. Gugus hidroksil yang terikat pada cincin piridin (pikolinat) atau cincin fenol (gugus salisilat) dapat memberikan perbedaan bioaktivitas
2.1. Senyawa UK-3A
Penelitian Ueki et.al telah berhasil mengisolasi senyawa antibiotika baru UK-1, UK-2, dan UK-3 dari mycelium Streptomyces sp. 517-02 yang diperoleh dari contoh tanah di sekitar kampus Sugimoto, Universitas Osaka, Jepang (Ueki,et.al.,1996a; Hanafi,et.al., 1996; Taniguchi, et.al., 1995).
Antibiotika UK-2 diisolasi dari mycelium sebagai komponen mayor
sedangkan UK-1 dan UK-3 sebagai komponen minornya (Ueki,et.al.,1996a).
Senyawa UK-1 mengandung gugus benzoxazol, komponen dalam senyawa tersebut yang mempunyai sifat anti kanker sedangkan sifat anti jamur telah dibuktikan pada senyawa UK-2A, UK-2B, UK-2C, dan UK-2D yang
mengandung dilakton cincin sembilan (Ueki, et.al.,1993; Shibata, et.al., 1993;
Hanafi,et.al.,1996; Ueki,et.al.,1996). UK-3 sebagai komponen minor dalam mycelium ini merupakan senyawa aktif sebagai anti jamur dan anti kanker.
Senyawa UK-3 diperoleh sebagai senyawa kompleks yang terdiri dari lima komponen A, B, C, D, dan E, dan senyawa UK-3A merupakan komponen utamanya dan struktur molekulnya telah diketahui namun struktur untuk komponen lain seperti, UK-3B, UK-3C, UK-3D, dan UK-3E, belum ditetapkan kemungkinan mempunyai kemiripan dengan struktur UK-3A dengan
perbedaan hanya pada panjang rantai ester yang terikat pada C-3 (Shimano, et.al.,1998).
Senyawa UK-2A mempunyai kemiripan struktur dengan senyawa antimycin A3 (AA) yang telah dikenal baik sebagai antibiotika anti jamur (Wikipedia, 2008; Ueki,et.al., 1996; Hanafi, et.al., 1996; Ueki, et.al., 1997b;
Usuki, et.al., 2005; Murray, 2003). AA menginhibisi transfer elektron antara cyt b dan cyt c1 dalam rantai respirasi dalam mitokondria dengan cara mengikat kompleks III protein sehingga tidak terjadi konversi energi untuk kelangsungan hidupnya. Sitokrom oksidase merupakan komponen terakhir rantai respirasi dalam mitokondria dan bertanggung jawab untuk transfer elektron dari reaksi oksidasi molekul substrat oleh dehidrogenase ke oksigen sebagai akseptornya (Murray, 2003). Kemiripan struktur antara kedua
senyawa, UK-2A maupun AA, sama-sama memiliki gugus dilakton cincin sembilan yang terikat oleh ikatan amida. UK-2A memiliki struktur molekul yang sebagian terdiri atas 3-hidroksi-4-metoksi pikolinat sedangkan struktur senyawa AA adalah 3-formamido salisilat. Akivitas anti kanker dari senyawa UK-2A telah dilaporkan kurang aktif terhadap beberapa sel mamalia seperti P388, B16, LLC-PK1, KB, dan COLO201 dibandingkan senyawa AA (Usuki, et.al., 2005). Shimano (1998) memberi batasan bahwa suatu senyawa tidak
memperlihatkan aktivitas biologi dengan IC50 di atas 100 µg/mL untuk beberapa jenis sel kanker tertentu (Shimano, 1998).
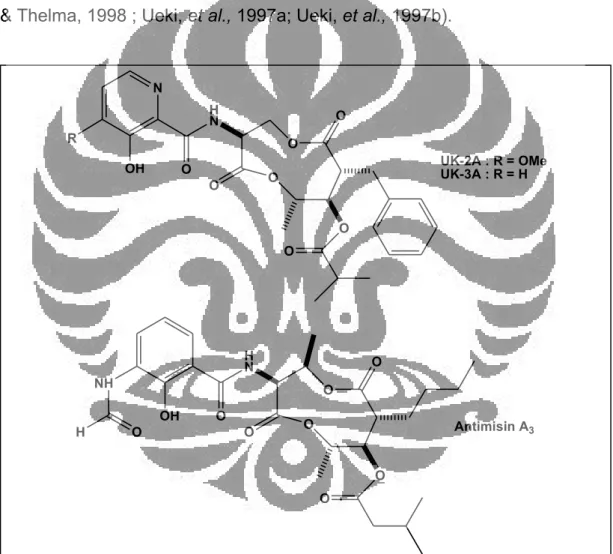
Senyawa UK-3A juga memiliki kemiripan struktur molekul dengan UK- 2A. Senyawa UK-3A tidak memiliki gugus metoksi sebagaimana senyawa UK-2A namun pada cincin piridinnya terdapat gugus hidroksil OH (Gambar 1). UK-3A merupakan antibiotik alamiah yang mempunyai aktivitas biologi dalam menghambat pertumbuhan sel kanker sehingga berfungsi sebagai
obat anti kanker. Aktivitas tersebut dinyatakan juga sebagai aktivitas
sitotoksik. Hasil uji beberapa sel kanker terhadap UK-3A ditunjukkan bahwa UK-3A memiliki aktivitas yang tinggi dalam menghambat pertumbuhan sel kanker. Senyawa UK-3A juga memiliki struktur yang mirip dengan senyawa AA. Gugus hidroksi pada senyawa tersebut mempunyai kemampuan
meningkatkan aktivitas dalam menghambat pertumbuhan sel kanker (Hanafi
& Thelma, 1998 ; Ueki, et al., 1997a; Ueki, et al., 1997b).
N
OH O
HN
O
O
O
O O
O R
UK-2A : R = OMe UK-3A : R = H
Antimisin A3
OH O
HN
O
O
O
O O
O NH
H O
Gambar 1. Struktur UK-2A, UK-3A, dan Antimisin A3
Studi hubungan gugus-gugus aktif yang berperan dalam struktur molekul terhadap aktivitas biologi memberikan informasi dalam
pengembangan sintesis senyawa analog (Patrick, 2001). Gugus-gugus aktif pada senyawa UK-2A dan UK-3A dapat diketahui melalui reaksi metilasi dan reaksi pemutusan rantai pada senyawa UK-2A yang memiliki kemiripan struktur dengan senyawa UK-3A. Metilasi senyawa UK-2A dengan
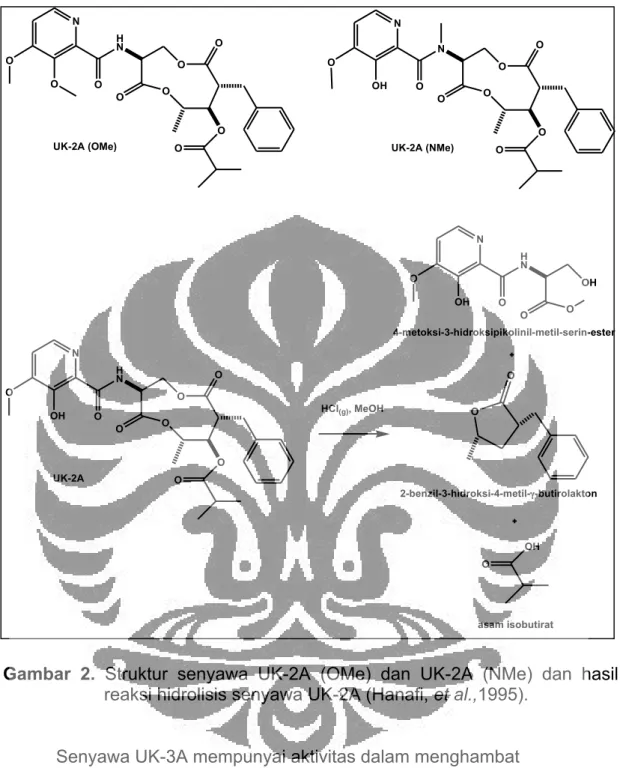
diazometan dihasilkan senyawa UK-2A termetilasi pada gugus hidroksilnya (UK-2A OMe) dan senyawa UK-2A termetilasi pada gugus amidanya (UK-2A NMe) (Gambar 2). Berdasarkan data uji aktivitas anti kanker untuk kedua senyawa UK-2A yang termetilasi, UK-2A (OMe) dan UK-2A (NMe),
menunjukkan bahwa terjadi kehilangan aktivitas biologi sebagai antikanker.
Hal ini membuktikan bahwa gugus hidroksil dan amida dalam keadaan bebas merupakan gugus aktifnya. Apabila gugus-gugus aktif tersebut tersubstitusi oleh molekul tertentu dapat menghilangkan daya sitotoksiknya (Hanafi, et al.,1996).
Peran gugus aktif dilakton cincin sembilan dapat juga diamati pada reaksi pemutusan rantai senyawa UK-2A. Hasil reaksi pemutusan rantai atau hidrolisis dengan menggunakan gas HCl dalam metanol sesuai Gambar 2, menghasilkan senyawa 4-metoksi-3-hidroksipikolinil-metil-serin-ester (HPMSE) dan senyawa 2-benzil-3-hidroksi-4-metil-γ-butirolakton. Aktivitas antijamur untuk kedua senyawa hasil hidrolisis tersebut menjadi hilang jika dibandingkan dengan senyawa awal, UK-2A, yang memiliki aktivitas biologi (Hanafi, et al.,1996).
N
O O
HN
O
O O
O O
O O
N
OH O
N
O
O O
O O
O O
UK-2A (NMe) UK-2A (OMe)
N
OH O
HN
O
O O
O O
O O
UK-2A
N
OH O
HN
O
OH O
OH O O
HCl(g), MeOH O
O
4-metoksi-3-hidroksipikolinil-metil-serin-ester
2-benzil-3-hidroksi-4-metil-γ-butirolakton
asam isobutirat
Gambar 2. Struktur senyawa UK-2A (OMe) dan UK-2A (NMe) dan hasil reaksi hidrolisis senyawa UK-2A (Hanafi, et al.,1995).
Senyawa UK-3A mempunyai aktivitas dalam menghambat
pertumbuhan sel kanker P388, sel kanker B16, sel kanker KB dan sel kanker COLO-201 seperti ditunjukkan pada Tabel 1. UK-3A memiliki aktivitas yang tinggi dalam menghambat pertumbuhan sel kanker tertentu dibuktikan dari nilai IC50 dibawah 100 µg/mL (Shimano, 1998). Hasil uji beberapa senyawa
yang ditunjukkan dalam Tabel tersebut disertai oleh senyawa AA sebagai senyawa standar anti kanker (Ueki,et all, 1997).
Tabel 1. Nilai IC50 (µg/mL) dari hasil uji senyawa UK-3A, UK-2A, UK-2 (OMe), UK-2 (NMe), dan AA terhadap hambatan pertumbuhan sel kanker (Ueki,et all., 1997)
Sel kanker UK-3A UK-2A UK-2 (OMe) UK-2 (NMe) AA
P388 38 100 60 >100 0,015
B16 18 100 50 >100 0,020
KB 20 17 - - 0,063
COLO-201 45 35 - - 0,018
3T3 100 100 - - 15
Keterangan :
• P388 = Mouse Leukemia
• B16 = Mouse Melanoma
• KB = Human Oral Epidermoid Carcinoma KB
• COLO-201 = Human Colon Adenocarcinoma COLO-201
• 3T3 = Mouse Fibroblast 3T3
Senyawa AA digunakan sebagai standar uji untuk senyawa UK-2A dan UK-3A (Hanafi, et al., 1996) karena kedua senyawa memiliki struktur yang menyerupai senyawa AA. Senyawa AA dihasilkan dari Streptomyces sp. K01-0031 (Shiomi, et al., 2005) dan telah diketahui memiliki aktivitas antikanker yang sangat tinggi. Senyawa AA diketahui mempunyai posisi yang tepat terhadap pusat aktif protein Bcl-2 yang diperlukan dalam proses apoptosis melalui jalur intrinsik (Martin, 1999). Bcl-2 adalah kelompok protein
yang mempunyai peranan dalam pembawa sinyal apoptosis dalam sel (Leusault, et.al., 2002; Shi, et al., 2003). Apoptosis adalah gejala fisiologis secara normal dari kematian terprogram sel bunuh diri. Apoptosis merupakan mekanisme penting untuk mencegah proliferasi sel yang mengalami kerusakan DNA, agar sel-sel dengan lesi DNA tersebut tidak dapat dilipatgandakan. Kelainan pada mekanisme apoptosis dapat meningkatkan ketahanan hidup sel dan menyebabkan ekspansi sel ganas (Martin, 1996;
Bowolaksono, 2007). Antimisin A3 dapat menginduksi apoptosis sel leukemia HL-60. Bcl-2 terdapat dalam 90% sel kanker usus, 80% B-sel limfomas, dan 70% sel kanker payudara (Liu et al. 2003).
2.2. Sintesis Senyawa Analog UK-3A
Senyawa analog adalah senyawa yang dibuat berdasarkan senyawa induk yang telah ditemukan mempunyai aktivitas biologi. Ada dua alasan penting disintesisnya senyawa analog ini adalah sebagai studi identifikasi gugus fungsi yang penting dalam menjelaskan mekanisme pengikatan senyawa induk dengan targetnya serta mempunyai keuntungan dalam pengembangan obat bahwa aktivitas senyawa induk dapat diperbaiki dan mengurangi efek samping. Sintesis senyawa analog mempunyai seminimal mungkin tahapan reaksi dan menggunakan bermacam-macam reaktan sehingga sebanyak mungkin senyawa analog berbeda dapat disintesis (Patrick, 2001).
Sintesis senyawa analog mempunyai tujuan untuk menciptakan suatu senyawa baru yang serupa dengan senyawa induknya dan diramalkan
mempunyai sifat lebih unggul/lebih aktif (Pine, et.al., 1998). Sintesis senyawa analog dilakukan dengan cara melakukan modifikasi dalam struktur molekul senyawa induk yang telah diketahui mempunyai aktivitas tertentu.
Keuntungan melakukan modifikasi struktur molekul adalah; (1) senyawa analog diharapkan mempunyai sifat farmakologis yang serupa atau lebih unggul, (2) menemukan gugus pharmacophore penting pada bagian molekul obat yang dapat memberikan aksi farmakologis, (3) produksi senyawa obat menjadi cepat dan lebih ekonomis (Siswondono & Soekardjo, 2000).
Modifikasi struktur molekul telah dikembangkan pada awal tahun 1974 oleh suatu pendekatan dari model Topliss. Model Topliss dikembangkan berdasarkan pendekatan hubungan struktur yang akan dirancang serupa dengan struktur induk yang telah diketahui mempunyai aktivitas. Modifikasi model Topliss adalah memasukkan gugus-gugus yang mempunyai sifat lipofilik, elektronik, dan sterik tertentu pada posisi tertentu dari struktur senyawa induk. Hasil rancangan modifikasi tersebut dihasilkan senyawa yang memiliki aktivitas relatif lebih tinggi, serupa, atau lebih rendah
dibandingkan dengan aktivitas yang dimiliki oleh senyawa induk, kemudian jalur sintesis ditetapkan berdasarkan rute sintesis yang paling
menguntungkan (Widodo, 1998). Model Topliss yang telah dilakukan melalui modifikasi struktur di ataranya adalah modifikasi pada cincin aromatik dan rantai gugus alkil yang kemungkinan terdapat senyawa ester, keton, amin dan amida (Siswandono & Soekardjo, 2000).
2.3. Strategi Perancangan Sintesis Senyawa Analog UK-3A
Strategi perancangan dalam suatu sintesis senyawa analog dari struktur senyawa induk dilakukan berdasarkan aktivitas senyawa induk yang telah diketahui mempunyai aktivitas tertentu. Pada penelitian ini telah
dilakukan modifikasi struktur molekul dalam senyawa analog UK-3A dengan cara melakukan variasi dalam struktur molekul senyawa induk. Beberapa variasi yang dilakukan dalam merancang senyawa analog UK-3A di antaranya adalah (1) mengganti cincin piridin dengan fenol dan gugus hidroksil (-OH) ada pada cincin aromatik tersebut, (2) mengubah gugus dilakton cincin sembilan menjadi rantai terbuka. Kedua teknik modifikasi dari struktur senyawa UK-3A induk tersebut dapat memberikan informasi
mengenai pembentukan senyawa baru dengan bahan dasar yang cukup murah, tidak menimbulkan efek samping, tetapi memiliki aktivitas menyerupai atau lebih tinggi dari senyawa induknya (Hanafi,et.al. 1997)
Modifikasi struktur molekul yang telah dikembangkan oleh Hanafi, et.al.
(Hanafi, et.al., 2008) mengenai pengaruh lipofilisitas beberapa senyawa analog UK-3A terhadap aktivitas antikanker leukemia P388 memberikan hasil signifikan dengan adanya kenaikan lipofilisitas. Struktur dilakton cincin
sembilan dalam senyawa UK-3A apabila mengalami hidrolisis oleh
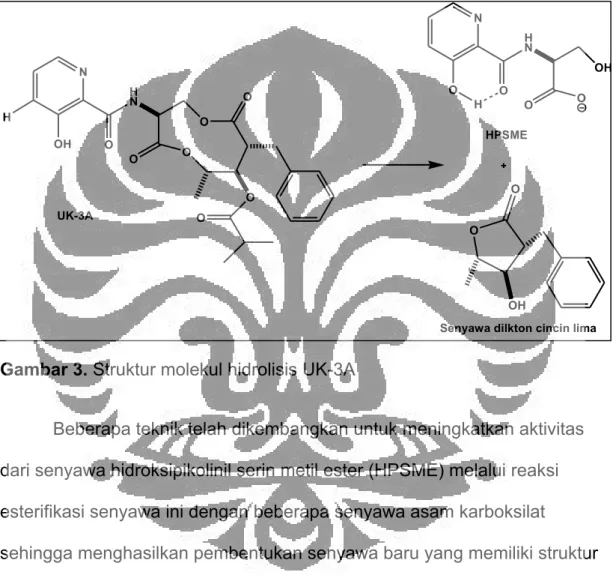
asam/basa atau mengalami trans esterifikasi menghasilkan senyawa seperti ditunjukkan pada Gambar 3 yaitu 3-hidroksipikoliin serin metil ester (HPSME) dan ester lakton cincin lima. Kedua senyawa hasil reaksi hidrolisis, HPSME dan lakton cincin lima, masing-masing tidak mempunyai aktivitas anti kanker
terutama pada sel Murine leukemia P-388 yang sebelumnya ada aktivitas anti kanker dalam senyawa UK-3A induk. Dengan demikian dapat dikatakan bahwa dilakton cincin sembilan mempunyai peranan penting dalam aktivitas antikanker (Hanafi, et.al.,2008).
N
OH O
HN
O
O O
O O
O H
UK-3A
N
O O
HN
O
OH O
O O
OH H
HPSME
Senyawa dilkton cincin lima
Gambar 3. Struktur molekul hidrolisis UK-3A
Beberapa teknik telah dikembangkan untuk meningkatkan aktivitas dari senyawa hidroksipikolinil serin metil ester (HPSME) melalui reaksi esterifikasi senyawa ini dengan beberapa senyawa asam karboksilat
sehingga menghasilkan pembentukan senyawa baru yang memiliki struktur dilakton cincin terbuka dengan gugus ester rantai panjang yang bersifat non polar (lipofil) (Hanafi, et.al.,2008). Lipofilisitas dari senyawa tersebut
memberikan pengaruh terhadap kemampuannya untuk menembus membran sel kanker yang sebagian besar penyusunnya adalah senyawa lipid. Makin lipofil suatu senyawa maka makin tinggi bioaktivitas senyawa tersebut untuk
berinteraksi dengan reseptor dalam jaringan target namun bioaktivitas senyawa tersebut mencapai batas maksimal kemudian akan turun bila sifat hidrofilik senyawa hilang (Siswandono & Soekardjo, 2000). Membran sel tersusun oleh lipid, protein dan karbohidrat. Molekul non polar hanya memerlukan sedikit energi bebas untuk berpindah ke dalam medium
hidrofilik, namun pada ujung yang lain tidak banyak energi yang dikeluarkan karena sifat hidropobik/lipofilik yang sama (Murray, 2003). Salah satu contoh hasil penelitian sintesis senyawa lipofilik tersebut adalah PSMOE (3-hidroksi pikolinil serin metil oktil ester) memberikan nilai IC50 15,4 µg/mLuntuk sel kanker Murine leukemia P-388 lebih tinggi dari pada aktivitas antikanker senyawa UK-3A induk (Hanafi, et.al.,2008). Peningkatan aktivitas senyawa HPSME juga telah dilakukan oleh Wulandari (2007) melalui reaksi esterifikasi dan diperoleh senyawa PLGP (L-diamilpikolinil glutamat ester) dan PLGH (L- diheksil-pikolinil glutamat ester) masing-masing memberikan nilai IC50 untuk sel kanker Murine leukemia P-388 adalah 9 dan 8,4 µg/mL. Sintesis senyawa lipofil lain juga telah dibuktikan dari penelitian Adinata (2007), diperoleh senyawa EA1 (3-hidroksi pikolinil dioktil glutamat) dan EA2 (2-hidroksi nikotinil dioktil glutama) memberikan berturut-turut nilai IC50 9,8 dan 5µg/mL (Adinata, 2007; Wulandari, 2007).
Pada penelitian ini dilakukan beberapa sintesis senyawa analog UK- 3A melalui reaksi amidasi yaitu 3-hidroksi-N-oktilpikolinamida [S1] dengan rumus molekul C14H22 O2N2, 2-hidroksi-N-fenil-benzamida [S2] dengan rumus molekul C13H11NO2, 3-hidroksi-N-fenilpikolinamida [S3] dengan rumus
molekul C12H10N2O2, dan 2-hidroksi-N-oktilbenzamida [S4] dengan rumus molekul C15H23NO2. Sintesis senyawa analog yang dilakukan dalam penelitian ini dengan cara menghilangkan gugus dilakton rantai terbuka sehingga senyawa analog baru menjadi lebih sederhana karena
pembentukannya melalui satu tahap reaksi yaitu reaksi amidasi antara suatu asam karboksilat dengan amina primer. Senyawa analog ini tetap
mempertahankan gugus-gugus aktif seperti hidroksil -OH dan amida –CONH dan memiliki perbedaan pada sifat lipofilisitas senyawa analog berantai panjang alifatik atau aromatik untuk posisi pengikatan gugus aktif hidroksil (- OH) aromatik pada cincin piridin (pikolinat) atau fenol (salisilat). Variasi-variasi tersebut diharapkan akan memberikan informasi masing-masing prilaku pembentukan senyawa sehingga dapat dibuktikan peranan suatu gugus aktif dalam meningkatkan aktivitas penghambatan pertumbuhan sel kanker
Murine leukemia P-388.
Reagen-reagen bahan baku yang dibutuhkan dalam reaksi sintesis dapat diketahui dengan cara melakukan proses retrosintesis (Gambar 4).
Pembentukan senyawa A (kelompok senyawa pikolinamida) yaitu 3-hidroksi- N-oktilpikolinamida [S1] dan 3-hidroksi-N-fenilpikolinamida [S3], diperoleh dari reaksi antara asam 3-hidroksipikolinat dengan amina primer dari oktilamin dan arilamin. Kelompok senyawa benzamida (senyawa B)
diperoleh dari bahan baku asam salisilat dengan amina primer bila aminanya dari oktil amin maka dihasilkan senyawa 2-hidroksi-N-oktilbenzamida [S4]
dan anilin untuk senyawa 2-hidroksi-N-fenil-benzamida [S2].
OH
HN
O
R
[S2]=2-hidroksi-N-fenilbenzamida, R=aril [S4]=2-hidroksi-N-oktilbenzamida, R=oktil
OH
OH
O Asam salisilat
H2N R B
N
OH
HN
O
R
[S1]=3-hidroksi-N-oktilpikolinamida, R=oktil [S3]=3-hidroksi-N-fenilpikolinamida, R=aril
N
OH
OH
O Asam 3-hidroksipikolinat
H2N R A
R=oktil/aril
R=oktil/aril
Gambar 4. Retrosintesis senyawa A=pikolinamida dan B=benzamida (R=C8H17/C6H5)
Berdasarkan hasil retrosintesis tersebut kemudian disusun tahapan reaksi dengan menambahkan reagen-reagen yang dibutuhkan. Tahapan reaksi sintesis senyawa tersebut dapat dilihat pada Gambar 5.
R=oktil/aril H2N R
N
OH
OH
O Asam 3-hidroksipikolinat
DCC/DMAP
24 jam,600C
N
OH
HN
O
R
[S1]=3-hidroksi-N-oktilpikolinamida, R=oktil [S3]=3-hidroksi-N-fenilpikolinamida, R=aril
A
R=aril/oktil H2N R
OH
HN
O
R
[S2]=2-hidroksi-N-fenilbenzamida, R=aril [S4]=2-hidroksi-N-oktilbenzamida, R=oktil DCC/DMAP
24 jam,600C OH
OH
O Asam salisilat
B
Gambar 5. Tahapan reaksi pembentukan senyawa A=pikolinamida dan B=
benzamida (R=C8H17/ C6H5).
Secara umum, reaksi sintesis senyawa analog UK-3A pada Gambar 5 adalah reaksi amidasi. Agar reaksi bekerja secara optimal maka diperlukan suatu katalis. Katalis adalah suatu zat yang mempunyai fungsi dapat
mempercepat reaksi kimia dengan cara menurunkan energi aktivasi. Katalis yang biasa digunakan dalam reaksi amidasi adalah katalis basa seperti golongan klorida asam dan 4-dimetil amino piridin (DMAP) (Carey &
Sunberg, 1991).
2.4. Reaksi Amidasi
Senyawa amida adalah senyawa turunan dari asam karboksilat yang terbentuk dari substitusi gugus hidroksil (-OH) dengan gugus amina (-NH2).
Reaksi amidasi dapat berlangsung secara optimal dengan adanya penggunaan aktivator dan katalisator. Aktivator yang umum digunakan adalah karbodiimidazol (CDI) dan N,N-disikloheksilkarbodiimida (DCC).
Katalisator yang sering digunakan dalam reaksi amidasi adalah N,N-4-dimetil aminopiridin (DMAP), N-hidroksibenzotriazol (HOBt), N-hidroksi suksinamida (HOSu) dalam berbagai pelarut seperti tetrahidrofuran (THF), diklorolometan, dimetilformamida (DMF), piridin, dan trietilamin (Carey & Sunberg, 1991).
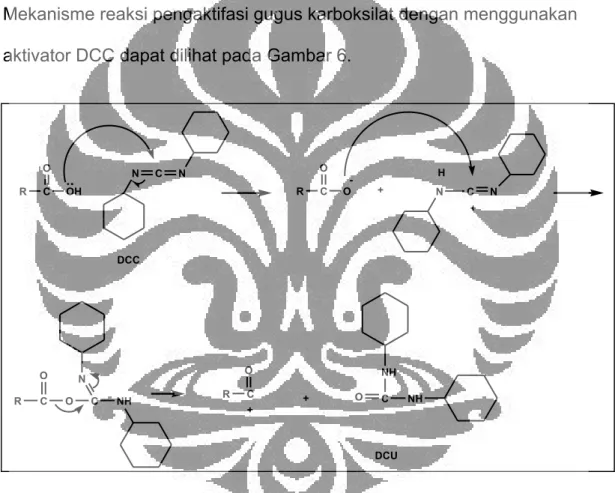
Senyawa N,N’-disikloheksilkarbodiimida (DCC) adalah senyawa yang berfungsi mengaktifkan gugus karboksilat menjadi suatu agen pengasilasi yang reaktif. Gugus aktif senyawa ini adalah gugus imida dari isourea (- N=C=N-) yang mengandung atom pusat karbon yang kekurangan elektron setelah bereaksi dengan proton dari asam karboksilat sehingga sangat
mudah diserang oleh suatu nukleofilik dan membentuk asil isourea. Gugus asil isourea ini sangat reaktif karena mampu memecah ikatan asil-oksigen dan mengubah ikatan rangkap karbon-nitrogen dari isourea menjadi gugus karbonil yang lebih stabil. Pada akhir reaksi terbentuk disikloheksilurea (DCU) sebagai hasil samping penggunaan DCC. DCU berupa padatan yang tak larut dalam sebagian besar pelarut organik (Bailey, 1992; March, 1992).
Mekanisme reaksi pengaktifasi gugus karboksilat dengan menggunakan aktivator DCC dapat dilihat pada Gambar 6.
R C
O OH
N C N
R C
O
O N C N
- H +
+
R C
O
O C
N
NH R C
O
+
O C
NH + NH
DCU DCC
Gambar 6. Mekanisme reaksi pengaktifan gugus karboksilat oleh aktivator DCC (Carey & Sunberg, 1991; Bailey, 1992).
Senyawa N,N-4-dimetil amino piridin (DMAP) adalah senyawa yang mempunyai fungsi sebagai katalis. DMAP memiliki efek katalitik yang kuat dan digunakan sebagai katalis nukleofilik. Gugus dimetil amino dalam DMAP berfungsi sebagai substituen donor elektron, memperbesar efek
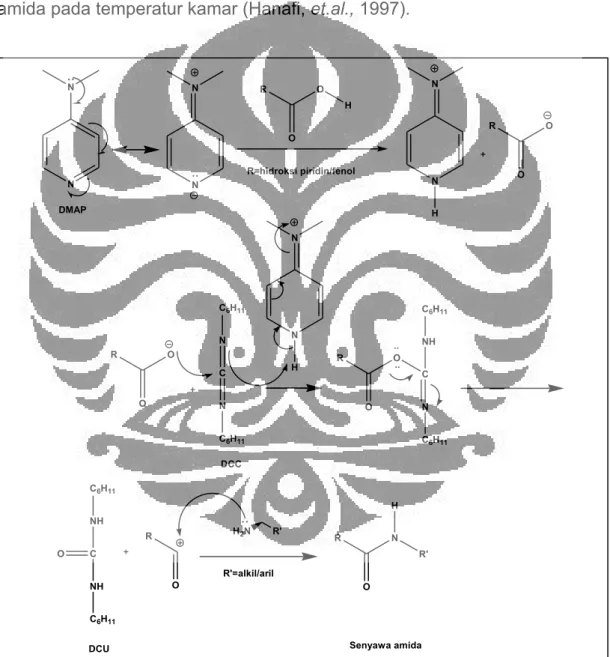
nukleofilisitas dan kebasaan dari nitrogen piridin. Mekanisme reaksi amidasi yang dikatalisis oleh DMAP dan diaktivasi oleh DCC dapat ditunjukkan pada Gambar 7. Penggabungan aktivasi karboksil oleh DCC dan katalis DMAP secara bersamaan merupakan suatu metode untuk mengaktivasi asam karboksilat ketika akan direaksikan dengan nukleofil seperti alkohol atau amida pada temperatur kamar (Hanafi, et.al., 1997).
N N
N
N R
O O
C N
N C6H11
C6H11
R
O O
C
N NH
C6H11 C6H11
DCC
..
..
R=hidroksi piridin/fenol
R
O O
N N
H
C NH
NH C6H11
O
C6H11 R
O
H2N R'
R
O N
R'
DCU
H
R
O O
R'=alkil/aril
H
Senyawa amida DMAP
N N
H
Gambar 7. Mekanisme katalisis reaksi amidasi yang dikatalisis oleh DMAP dan diaktivasi oleh DCC
2.5. Perkembangan Senyawa Analog UK-3A
Sintesis senyawa analog yang telah dilakukan dan dilaporkan sebelum ini adalah hasil modifikasi pada gugus dilakton cincin sembilan menjadi rantai terbuka dan rantai alifatik panjang. Variasi tersebut
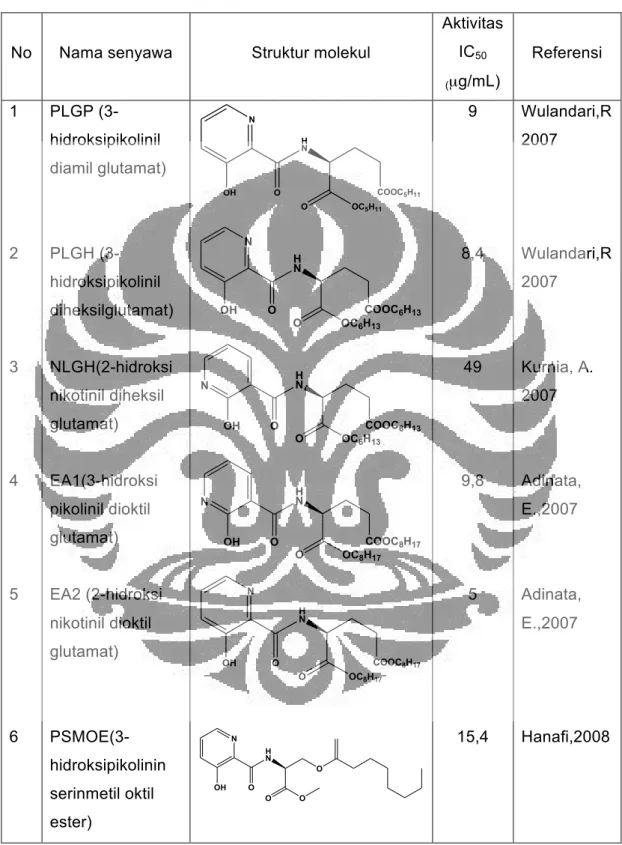
memberikan pengaruh terhadap aktivitas biologis/daya sitotoksik senyawa analog terhadap sel kanker Murine leukemia P-388 (Usuki et al. 2006). Tabel 2 diperlihatkan beberapa senyawa analog UK-3A yang telah disintesis pada penelitian sebelumnya dan hasil uji aktivitas biologis senyawa terhadap sel kanker Murine leukemia P-388.
Aktivitas biologis dari senyawa analog berdasarkan modifikasi cincin terbuka ester berantai panjang memberikan hasil penghambatan
pertumbuhan sel kanker Murine leukemia P-388 meningkat oleh adanya peningkatan lipofilisitas senyawa. Aktivitas beberapa senyawa analog
ditunjukkan pada Tabel tersebut memberikan nilai IC50 lebih rendah dari IC50 untuk senyawa UK-3A induk artinya daya sitotoksik dari senyawa analog UK- 3A lebih tingi dari senyawa induknya.
Tabel 2. Sintesis beberapa senyawa analog UK-3A berdasarkan modifikasi dilakton cincin sembilan
No Nama senyawa Struktur molekul
Aktivitas IC50 (µg/mL)
Referensi
1
2
3
4
5
6
PLGP (3- hidroksipikolinil diamil glutamat)
PLGH (3- hidroksipikolinil diheksilglutamat)
NLGH(2-hidroksi nikotinil diheksil glutamat)
EA1(3-hidroksi pikolinil dioktil glutamat)
EA2 (2-hidroksi nikotinil dioktil glutamat)
PSMOE(3- hidroksipikolinin serinmetil oktil ester)
N
OH O
OC5H11 COOC5H11 HN
O
N
OH O
OC6HCOOC13 6H13 HN
O
N
OH O
OC6H13 COOC6H13 HN
O
N
OH O
OC8H17
COOC8H17 HN
O N
OH O
OC8H17 COOC8H17 HN
O
N
OH O
HN
O
O O
9
8,4
49
9,8
5
15,4
Wulandari,R 2007
Wulandari,R 2007
Kurnia, A.
2007
Adinata, E.,2007
Adinata, E.,2007
Hanafi,2008
2.6. Uji Sitotoksisitas
Uji sitotoksisitas merupakan salah satu contoh uji yang digunakan untuk mengevaluasi daya sitotoksik suatu senyawa yang akan digunakan sebagai bahan obat menggunakan kultur sel secara in vitro. Salah satu syarat uji sitotoksisitas adalah sistem uji tersebut harus menghasilkan kurva dosis respon yang reproduksibel dan dapat menggambarkan efek senyawa uji yang sama bila diberikan secara in vivo. Sistem uji sitotoksisitas ini
merupakan uji kuantitatif dan kualitatif dengan cara menetapkan kematian sel (Budi, 2006).
Pengembangan metode in vitro sebagai alternatif pengganti pengujian hewan uji mempunyai tujuan untuk mendeteksi potensi ketoksikan suatu obat pada manusia (Klassen, 2001; Rahmawati, 2004). Umumnya, hasil uji secara in vitro dapat menggambarkan efek senyawa uji yang sama bila diberikan secara in vivo dan dapat memberi informasi secara langsung potensi efek obat pada sel target manusia yang secara ilmiah memberi hasil yang lebih valid (Rahmawati, 2004).
Uji sitotoksisitas secara in vitro menggunakan sel primer maupun sub kultur sel yang merupakan turunan dari sel primer yang sering disebut cell line (Rahmawati, 2004). Cell line yang digunakan dalam uji sitotoksisitas bisa
berasal dari sel kanker manusia maupun hewan. Sel kanker hewan yang digunakan untuk uji sitotoksisitas harus memiliki kesamaan sifat dan karakteristik dengan sel kanker manusia (Harborne & Dey, 1991).
Metode yang digunakan dalam uji sitotoksisitas salah satunya adalah metode MTT. Metode ini didasarkan atas pengukuran intensitas warna secara kolorimetri. Intensitas warna sebagai hasil metabolisme suatu substrat oleh sel hidup menjadi produk berwarna. Garam MTT (3-(4,5- dimetiltiazol-2-il)-2,5-difenil tetrazolium bromida) yang ditambahkan pada media akan direduksi oleh sistem reduktase suksinat tetrazolium yang terdapat di dalam mitokondria aktif menjadi formazan yang merupakan zat warna ungu. Absorbans dari warna yang terbentuk dikuantifikasi pada panjang gelombang tertentu dengan kisaran λ= 500-600nm dengan
spektrofotometer UV/VIS (Wikipedia, 2008), seperti terlihat dalam Gambar 8 berikut ini :
Gambar 8. Reaksi reduksi MTT menjadi formazan.
Metode lain yang biasa digunakan dalam uji sitotoksisitas adalah penghitungan jumlah sel langsung di bawah mikroskop dengan bantuan haemositometer dan metode pewarnaan mengunakan tripan biru (Budi, 2006).
2.7. Penyakit Kanker dan Leukemia
Kanker adalah penyakit akibat pertumbuhan tidak normal dari sel-sel jaringan tubuh yang berubah menjadi sel kanker dalam perkembangannya (Wikipedia, 2008). Dalam jaringan tubuh selalu didapatkan sejumlah sel yang sedang berada dalam siklus membelah diri (proliferasi). Pada jaringan yang terkena kanker, jumlah sel yang berada dalam siklus membelah diri jauh lebih besar. Aktivitas sel yang tengah membelah diri umumnya tertinggi pada saat kanker tersebut masih kecil dan makin menurun dengan membesarnya volume jaringan kanker tersebut. Proses terjadinya suatu kanker bukanlah suatu proses sederhana namun diperlukan beberapa faktor penyebab yang dapat mempengaruhi suatu sel normal berubah menjadi sel kanker dan selanjutnya sel-sel kanker ini menyebar dan menyusup ke jaringan sehat pada alat tubuh lainnya dan merusak fungsi alat tubuh tersebut sehingga dapat menyebabkan kematian (Wikipedia, 2008).
Sel kanker ditandai oleh tiga ciri khas yaitu (1) proliferasi tidak
terkontrol; (2) invasi pada jaringan setempat; (3) penyebaran atau metastasis ke bagian tubuh lain. Sel tumor (benigna) juga memperlihatkan penurunan kontrol pertumbuhan namun tidak menyebar ke bagian tubuh yang lain.
Robert K. Murray (2003) menyatakan bahwa kanker terjadi akibat gen yang mengkontrol pertumbuhan dan interaksi dengan sel normal lain memiliki pengaturan yang tidak normal yaitu kegagalan dalam koordinasi fungsi gen yang diperlukan dalam proses proliferasi dan diferensiasi sel. Kegagalan dalam fungsi gen memberikan perubahan atau mutasi terhadap material
genetik DNA (asam deoksiribonukleat). Penelitian terhadap gen yang berhubungan dengan fungsi tersebut pada kanker, saat ini telah banyak dilakukan seperti: gen BRCA1, P53, dan Bcl-2 yang semuanya terdapat di dalam inti sel.
Suatu sel berubah menjadi kanker, sel tersebut juga dikatakan telah kehilangan sifat apoptosis, yaitu kemampuan untuk membunuh sel itu sendiri, sehingga sel terus bertambah. Hal ini terjadi karena mutasi atau perubahan genetik sel-sel tubuh yang menjadi sel kanker. Banyak hal yang diduga menjadi bahan pencetus terjadinya mutasi gen antara lain radikal bebas yang masuk ke dalam tubuh dan adanya virus tertentu yang menginvasi sel tubuh. Mutasi spontan merupakan predisposisi terhadap terjadinya sel kanker dengan frekuensi 10-7 -10-6 per sel per generasi.
Kecepatan ini akan meningkat di dalam jaringan yang memiliki laju proliferasi tinggi sehingga produksi sel dari sel induk menjadi potensial untuk berubah menjadi sel kanker (Murray, 2003).
Transformasi sel menjadi kanker adalah transformasi sel
menghasilkan sel-sel ganas dengan sifat yang berbeda dari sel normal dan perilaku progeninya tidak lagi statik. Kejadian tersebut diwujudkan dalam bentuk kariotipe yang abnormal, laju pertumbuhan semakin bertambah, dan kecenderungan untuk menginvasi dan bermetastasis. Fenomena
progresivitas tumor mencerminkan ketidakstabilan dari genom sel tumor sehingga sel dengan laju pertumbuhan yang lebih cepat memiliki keuntungan selektif. Profil biokimia sel yang sangat ganas mungkin berbeda jauh dari sel normal. Pada sel tersebut terjadi banyak perubahan pada profil enzim atau
ketidakstabilan dalam kromosom. Sel yang tumbuh cepat cenderung memaksimalkan proses anabolik yang terlibat dalam pertumbuhan (seperti sintesis DNA dan RNA) dan menurunkan fungsi katabolik (Murray, 2003).
Leukemia merupakan penyakit kanker yang terjadi pada sel-sel darah.
Sel-sel darah pada mulanya berasal dari satu jenis sel yang disebut sel induk (stem sel). Stem sel akan berkembang menjadi sel darah merah, sel darah putih dan keping-keping darah (Wikipedia, 2008). Leukemia terjadi jika proses pematangan dari stem sel menjadi sel darah putih mengalami gangguan dan menghasilkan perubahan ke arah keganasan, karena proliferasi sel leukemia adalah sel bersifat immortal. Terjadinya proliferasi seringkali melibatkan penyusunan kembali bagian dari kromosom.
Penyusunan kembali kromosom (translokasi kromosom) mengganggu pengendalian normal dari pembelahan sel, sehingga sel membelah tak terkendali dan menjadi ganas, dan akhirnya sel-sel tersebut menguasai sumsum tulang dan menggantikan tempat dari sel-sel yang menghasilkan sel-sel darah yang normal. Kanker ini juga bisa menyusup ke dalam organ lainnya, termasuk hati, limpa, kelenjar getah bening, ginjal, dan otak (Wikipedia, 2008).
Ada beberapa cara untuk menangani kanker tergantung pada
keadaan/stadium kanker itu sendiri. Beberapa penangan tepat menjadi suatu alternatif untuk menghambat pertumbuhan kanker berubah menjadi ganas di ataranya adalah operasi transplantasi sum-sum tulang, radioterapi, atau kemoterapi dengan pemberian obat yang bersifat sitotoksik.
3.1. Waktu dan Tempat Penelitian
Penelitian ini telah dilaksanakan di Laboratorium Bahan Alam Pangan dan Farmasi Pusat Penelitian Kimia Lembaga Ilmu Pengetahuan Indonesia (LIPI) PUSPIPTEK (Pusat Penelitian Ilmu Pengetahuan dan Teknologi) Serpong, dan Laboratorium Kimia Organik Bahan Alam, Departemen Kimia FMIPA Institut Teknologi Bandung (ITB) pada bulan Januari 2008 hingga April 2008
3.2. Bahan dan Alat
3.2.1. Bahan
a. Bahan baku : asam 3-hidroksipikolinat, oktilamina, asam salisilat, anilin.
b. Pelarut : n-heksan, etil asetat, aseton, kloroform, metanol, CDCl3, diklorometan, aquades, larutan HCl 1%, larutan NaOH 1%.
c. Katalis dan aktifator : N,N’-disikloheksilkarbodiimida (DCC) dan 4- dimetil amino piridin (DMAP).
d. Zat pengering : magnesium sulfat anhidrat, pelet KOH.
e. Kolom kromatografi silika gel 60 (Merck) dengan ukuran partikel 70- 230 mesh.
f. Plat kromatografi lapis tipis (KLT) Silica gel GF 254 (Merck) dengan ketebalan 0,25mm.
3.2.2. Alat
Peralatan yang digunakan dalam penelitian ini adalah alat-alat gelas yang ada di laboratorium kimia seperti: labu, gelas piala, tabung reaksi, gelas ukur, corong pisah, dan batang pengaduk, seperangkat alat refluks, alat destilasi, bejana KLT, kolom kromatografi, timbangan analitik, pengaduk magnet dan hot plate stirrer, termometer, evaporator vakum, oven,
micropipet, lampu UV dengan panjang gelombang 254 dan 365nm, Fisher Scientific (USA), spektrofotometer FT-IR Shimadzu 2010A, spektrofotometer UV U-200 Hitachi, spektrometer Nuclear Magnetic Resonance proton dan karbon (1H NMR dan 13C NMR) JEOL ECA NMR 500 MHz.
3.3. Prosedur Penelitian
Penelitian ini dilakukan melalui dua tahap pekerjaan yang terdiri dari:
(1) Sintesis, identifikasi, dan karakterisasi senyawa analog UK-3A
(2) Uji aktivitas biologi senyawa analog dalam menghambat pertumbuhan sel kanker Murine leukemia P-388 secara in-vitro.
Sintesis senyawa analog UK-3A dilakukan dengan cara mereaksikan bahan baku yang terdiri atas senyawa asam karbosilat aromatik dan
senyawa amina primer dan menambahkan aktivator dan katalisator DCC/DMAP. Hasil yang diperoleh melalui reaksi tersebut berupa produk
amida dan reaksinya disebut reaksi amidasi. Reaksi amidasi berlangsung pada suhu 60 0C selama 24 jam.
Identifikasi awal untuk produk sintesis diamati mengunakan plat KLT silika gel Merck GF254. Hasil pengamatan berupa noda (spot) dapat dilihat secara langsung di bawah lampu ultraviolet (UV) pada λ = 254 dan 360 nm.
Identifikasi kualitatif dari spot yang terbentuk dihitung dengan cara
menentukan nilai retensi Rf dari perbandingan jarak suatu spot dengan jarak elusi pelarut. Untuk identifikasi seperti penentuan struktur molekul dilakukan menggunakan alat antara lain : spektrofotometer UV, FT-IR dan
spektrometer NMR (1H-NMR dan 13C-NMR). Karakterisasi senyawa ditentukan untuk mengetahui spesifikasi senyawa tersebut seperti titik lelehnya menggunakan alat Fisher scientific.
Uji aktivitas anti kanker Murine leukemia P-388 untuk masing-masing produk dilakukan dengan mengirimkan sampel ke Laboratorium Kimia
Organik Bahan Alam, Departemen Kimia FMIPA, Institut Teknologi Bandung.
3.3.1. Sintesis Senyawa Analog UK-3A (Anderson dalam Widodo, 1998;
Hanafi, 1997).
A. 3-hidroksi-N-oktilpikolinamida [S1]
Sebanyak 0,278 g (2 mmol) asam 3-hidroksipikolinat dan 0,364 mL(2,2 mmol) oktilamina dimasukkan ke dalam labu dan dicampurkan secara bersamaan dengan katalis dan aktivatornya sebanyak 0,454 g (2,2 mmol) DCC (disiklo heksil karbodiimida) dan 0,269 g (2,2 mmol) DMAP (dimetil
labu dihubungkan dengan kondensornya untuk proses reaksi selama kurang lebih 24 jam pada suhu 60 0C sambil dilakukan pengadukan secara terus menerus menggunakan pengaduk magnet dan hot plate stirrer . Proses reaksi dihentikan setelah dilakukan identifikasi kuantitatif menggunakan KLT untuk mengetahui bahwa produk spesifik berupa spot berwarna ungu telah terbentuk. Air ditambahkan untuk menghilangkan DCC kemudian DCU (disikloheksil urea) dapat dipisahkan dengan penyaringan. Filtrat yang dihasilkan diekstraksi dengan 25mL kloroform sebanyak 3 kali. Air yang ada pada fasa pelarut organik dihilangkan dengan penambahan magnesium sulfat anhidrat hingga jenuh. Filtrat (sampel dalam pelarut kloroform) dikeringkan dari pelarutnya dengan cara penguapan menggunakan evaporator vakum pada suhu 50 0C.
Sampel [S1] dimasukkan ke dalam kolom kromatografi yang berisi silika gel dan pelarut dibiarkan mengalir sepanjang kolom dengan
konsentrasi gradien mulai dari 100% n-heksan hingga n-heksan : etil asetat (1:1). Tiap fraksi yang keluar dari kolom ditampung sebanyak 5 mL
kemudian dilakukan analisis kualitatif menggunakan KLT. Fraksi-fraksi yang menunjukkan spot tunggal dari produk reaksi yang diinginkan, dikumpulkan dan diuapkan menggunakan evaporator vakum suhu 50 0C. Senyawa [S1]
murni yang dihasilkan kemudian ditimbang untuk ditentukan rendemennya dan dilakukan identifikasi titik leleh dan penentuan struktur menggunakan alat spektrofotometer UV, FT-IR dan spektrometer NMR (1H-NMR dan 13C- NMR).



![Gambar 9. Mekanisme reaksi sintesis senyawa 3-hidroksi-N-oktil pikolinamida [S1]](https://thumb-ap.123doks.com/thumbv2/123dok/2170679.4043581/57.892.152.769.361.1007/gambar-mekanisme-reaksi-sintesis-senyawa-hidroksi-oktil-pikolinamida.webp)