Pekanbaru – 21 Desember 2005 B04-1
Destruksi Mineral Ilmenit Dengan Asam Sulfat
Di Dalam Reaktor Tangki Berpengaduk
Ahmad Fadli1), Syaiful Bahri1), Iis Sopyan2), Sumardi3)
1) Jurusan Teknik Kimia Fakultas Teknik Universitas Riau
Telp/Fax. (0761)566937 Email : fadliunri@unri.ac.id or fadliunri@yahoo.com
2) Agency for The Assesment and Application of Technology (BPPT),
Center for Materials Technology
3) Jurusan Teknik Kimia Fakultas Teknik Universitas Gadjah Mada
Abstrak
Kegunaan Titanium Dioksida (TiO2) sangat banyak antara lain sebagai bahan pewarna, katalisator, fotokatalitik dll. Salah satu proses untuk membuat Titanium Dioksida (TiO2) adalah dengan Proses Sulfat. Bahan baku yang digunakan adalah mineral ilmenit bahan buangan PT Tambang Timah Bangka. Reaksi antara mineral ilmenit dan Asam Sulfat dilakukan secara batch dalam Reaktor yang diaduk. Mula-mula mineral ilmenit dan Asam Sulfat dicampurkan dalam Reaktor, kemudian ditutup rapat. Reaktor dipanaskan dan diaduk sampai suhu dan kecepatan tertentu. Cuplikan diambil setiap selang waktu 10 menit. Analisa sampel hasil penelitian dilakukan dengan UV Spectrofotometer. Variabel yang dipelajari adalah suhu reaksi (T) pada kisaran 110 oC – 160 oC, kecepatan putaran pengaduk (G) pada kisaran 400 rpm – 900 rpm dan Ukuran butir pada kisaran -50+80 mesh -325+400 mesh. Berdasarkan hasil penelitian, diperoleh bahwa kondisi yang relatif baik untuk proses destruksi adalah suhu reaksi 160 oC, kecepatan pengadukan 600 rpm, ukuran butir -325+400 mesh waktu reaksi adalah 120 menit dengan konversi titanium yang diperoleh 90,3%.
Kata Kunci : Mineral ilmenit, Titanium Dioksida, Reaktor batch, Konversi Pendahuluan
Ilmenit adalah pasir atau batu hitam yang mempunyai rumus kimia FeTiO3. Umumnya di
dalam pasir ilmenit terdapat impurities berupa besi oksida bervalensi tiga dan silika. Kandungan TiO2 di dalam ilmenit bervariasi antara 45% - 60% yang tergantung asal ilmenit tersebut.
Titanium dioksida (TiO2) baik dalam bentuk tetragonal rutile (TiO2) ataupun tetragonal
anatase (TiO2) sangat banyak dipakai dalam industri. Penggunaan tersebut antara lain sebagai
pigment pemutih, pigment warna superior (warna putih), bahan utama keramik untuk elektronik (BaTiO3), bahan baku untuk pembuatan TiO2 polimeric precursor yang sangat penting untuk pembuatan bahan-bahan keramik maju, antara lain pelapisan optik (film-optic), bahan electro-optic dan bahan komposit polimer ceramic (Ceramer). Jumlah impor TiO2 di Indonesia rata-rata
12.233 ton per tahun (BPS 1995/2001).
Bahan baku untuk membuat TiO2 sintetis banyak terdapat di alam, termasuk di Indonesia,
baik sebagai deposit utama/deposit batuan keras ataupun sebagai secondary / placer deposite (yang pada umumnya dalam bentuk pasir pantai). Mineral-mineral yang ada dalam deposit tersebut ada yang berbentuk mineral ilmenite (FeO.TiO2), rutile (tetragonal TiO2), anatase (tetragonal TiO2),
brookite (rhombic TiO2) dan perovskite (CaO.TiO2). Di alam, kandungan mineral ini relatif kecil,
sehingga proses pengolahan awal diperlukan yaitu pengkayaan kandungan sehingga diperoleh konsentrat dari mineral di atas. Di Indonesia, mineral yang mengandung TiO2 yang dijumpai
terdapat dalam hasil samping penambangan timah di Pulau Bangka dan juga dalam deposit (placer deposite) pasir besi di pantai selatan Pulau Jawa (Jawa Tengah). Sampai saat ini belum dilakukan pengolahan/pemanfaatan yang memberikan nilai tambah yang besar, seiring dengan perkembangan kebutuhan TiO2 sintetis dan perkembangan teknologi bahan keramik maju. Penelitian ini bertujuan
untuk mengolah ilmenit bahan buangan PT Tambang Timah menjadi titanium dioksida (TiO2).
Rutil sintetis adalah hasil pengolahan, yang pada umumnya secara kimia, dari deposit alam yang mengandung oksida titanium sehingga diperoleh mineral TiO2 dengan kemurnian
Pekanbaru – 21 Desember 2005 B04-2 melebihi 90 % berat (Sumardi, 1999). TiO2 sintetis pada umumnya dibuat dari deposit alam yang
mengandung oksida titan dengan proses sulfat atau dengan proses klorid (Kirk dan Othmer, 1983). Di alam, kandungan TiO2 yang terdapat di dalam deposit yang mengandung TiO2 sangat bervariasi baik dalam jumlah ataupun dalam bentuk mineralnya. Mineral tersebut dapat berbentuk mineral ilmenite (FeO.TiO2) ataupun mineral (kristalin) TiO2 (rutile, anatase, brookite). Sebagai
contoh pasir ilmenite di Malaysia dengan kandungan ilmenite 72,6% berat, sedangkan pasir ilmenite di India memiliki kandungan ilmenite (FeO. TiO2) sebesar 21,5% berat (kirk dan Othmer,
1983). Pengotor (mineral ikutan) dalam pasir ilmenite pada umumnya yang terbanyak adalah mineral hematit (Fe2O3). Di Indonesia, kandungan ilmenite yang ada dalam bahan buangan
tambang timah dapat mencapai 90% berat sedangkan pasir besi di pantai selatan Daerah Istimewa Yogyakarta (Kulonprogo) kandungan TiO2 relatif kecil yaitu 5,50% hingga 6,70% (Hendratno A,
1999), sehingga untuk pengolahan secara kimia diperlukan pengolahan awal / pengkayaan (Sumardi, 1999). Proses pengkayaan mineral ilmenite / TiO2 mineral yang ada dapat dilakukan
dengan menggunakan electrostatic separator untuk memisahkan mineral yang bersifat konduktor (TiO2 dan FeO.TiO2) dan mineral yang bersifat non konduktor (zircon, monazite, dll.). Rutil dapat
dipisahkan dari ilmenite dengan menggunakan magnetic separator karena ilmenite bersifat magnetis sedangkan rutil tidak, dengan cara ini diperoleh konsentrat ilmenite dan konsentrat rutil alami.
Salah satu cara yang dipakai untuk menghasilkan TiO2 adalah Proses Sulfat. Proses sulfat
dipakai untuk bahan baku deposit alam ataupun beneficiated mineral yang mengandung TiO2 lebih
kecil dari 60% berat (Reed,1988). Secara kimia proses sulfat dapat ditulis sebagai berikut : (Reed, 1988 ; Kirk & Othmer, 1983)
FeO.TiO2 + 2H2SO4 + 5H2O 150 180
oC− oC
→ FeSO4. 7H2O + TiOSO4 (1)
Pengotor ilmenite yang tidak larut dipisahkan terlebih dahulu dengan penyaringan (Reed, 1988). Untuk mendapatkan suhu operasi 150 oC- 180 oC reaksi dilakukan dalam autoklaf. Kadar H
2SO4
yang digunakan adalah 93% (66 oBe) (Shreeve & Brink, 1977). Ferri sulfat yang terbentuk
direduksi dengan menambahkan iron scrap. Hasil reaksi dikristalkan dengan cara didinginkan sehingga terbentuk kristal FeSO4. 7H2O (Cooperas) dan kemudian dipisahkan . Larutan sisa
dipekatkan dengan cara dididihkan (Shreeve & Brink, 1977) kemudian dihidrolisis (Kirk dan Othmer, 1983).
TiO.SO4 +2H2O
90oC
→
TiO(OH)2 + H2SO4 (2)Menurut Reed (1977), untuk mendapatkan bentuk rutile dari tetrahedral TiO2, selama
hidrolisis ditambahkan bibit kristal TiO2 (rutile form). Proses hidrolisa dipengaruhi oleh
faktor-faktor : jumlah dan kualitas bibit TiO2 yang ditambahkan, konsentrasi, kecepatan pemanasan dan
pH (Shreeve & Brink, 1977).
Kemudian Titanium oksida terhidrat dikalsinasi pada suhu 900 oC -1000 oC.
TiO(OH)2
900oC−1000oC
→
TiO2 + H2O (3)TiO2 yang didapat dari cara sulfat memiliki kemurnian lebih besar 90%, dan dapat dipakai sebagai
white pigment. Hasil samping dari proses sulfat, dapat diolah untuk menjadi pigment merah hematit, Fe2O3, yaitu dari pengolahan hasil FeSO4.7H2O, dengan cara kalsinasi (Reed,1977)
Bahan maju (advanced material) dengan basis TiO2 banyak digunakan untuk produk
elektronik keramik antara lain BaTiO3 (Reed,1977), ferroelektrik antara lain PbZrTi oksides (PZT)
ataupun PLZT. Untuk produk pelapis keramik/pelapis film optik yaitu untuk melapisi kaca/gelas dengan lapisan tipis (transparan) dari SiO2-TiO2 sehingga kaca bersifat anti gores & refleksi tinggi
(Covino,1991). Brenan dkk. (1991) membuat bahan keramik maju jenis ceramer yaitu paduan antara ikatan silang dari keramik (TiO2) dan bahan polimer jenis PTMO, sehingga didapat polimer
dengan sifat keramik (tahan suhu tinggi, dll.). Untuk membuat bahan-bahan di atas dipakai senyawa TiO2 precursor polimeric dari jenis titanium alkokside (propil titanat) ataupun dalam
Pekanbaru – 21 Desember 2005 B04-3 bentuk titanium glicolat. Sebagai bahan baku untuk membuat precursor di atas adalah sintetis rutile (TiO2). Bahan-bahan (precursor) ini yang diteliti/dikembangkan di Teknologi Keramik, dengan
basis bahan dasar / mentah ilmenite (FeO.TiO2).
Metoda Penelitian
Ilmenit, dari bahan buangan PT Tambang Timah Bangka. Berbentuk serbuk pasir dan berwarna kehitam-hitaman. Hasil analisa dengan XRF : Ti = 27,89 ± 0.093%, TiO2 = 46,52 ± 0.155%, selain itu juga terdeteksi dalam sampel adalah Mn, Fe, Y, Zr, Nb, Sn, Nd, Hf, Ta, W, Pb, Th dan U. Hasil analisa dengan XRD: FeO.TiO2= 25,517%, TiO2 (amorphus) = 29, 14%. Asam
sulfat, hasil analisa : Kadar = 94%, Baume = 65,51o, Berat Jenis = 1,83 gr/cc. Aquadest dengan
pH 6,5.
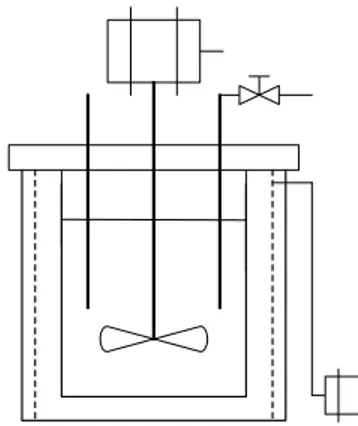
Proses dimulai dengan memasukkan ilmenit dengan berat tertentu ke dalam Autoklaf, kemudian secara perlahan-lahan dimasukkan juga asam sulfat dengan volume tertentu, lalu autoklaf ditutup rapat. Selanjutnya autoklaf dipanaskan dengan kawat pemanas listrik yang dililitkan pada sisi luar dinding autoklaf sampai temperatur tertentu. Setelah temperatur yang diinginkan tercapai, hidupkan motor untuk mengaduk cairan di dalam autoklaf tersebut. Kecepatan putaran pengaduk dan temperatur autoklaf diatur dengan powerstat. Setelah waktu tertentu, proses dihentikan dan diambil sampel dari dalam reaktor menggunakan pipa pengambil sampel yang dilengkapi kran. Selanjutnya sampel yang diperoleh diencerkan dengan cara menambahkan aquadest dengan volume tertentu, kemudian diendapkan lalu disaring dengan kertas saring. Cairan yang diperoleh dianalisa dengan UV Spectrophotometer (Priyana, dkk., 1979). Rangkaian alat penelitian ini dapat dilihat pada gambar 1.
Gambar 1. Rangkaian alat proses destruksi Hasil Penelitian dan Pembahasan
Pengaruh Suhu Reaksi (T)
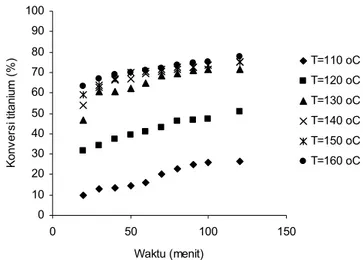
Dari gambar 2 terlihat bahwa pada temperatur 150 oC dan 160 oC diperoleh konversi
titanium relatif sama mencapai 76%, sedangkan pada temperatur 110 oC konversi yang dicapai paling kecil kira-kira 27%. Hal ini disebabkan energi kinetik yang dimiliki oleh zat pereaksi semakin besar dengan kenaikan waktu dan suhu, sehinga makin banyak tumbukan antara molekul yang menghasilkan reaksi. Selain itu dari data tersebut juga terlihat bahwa ketika waktu proses sudah mencapai kira-kira 70 menit maka kecepatan reaksi terlihat semakin lambat, hal ini disebabkan pada kondisi mendekati kondisi setimbang.
Pekanbaru – 21 Desember 2005 B04-4 0 10 20 30 40 50 60 70 80 90 100 0 50 100 150 Waktu (menit) K onv er si ti tan iu m ( % ) T=110 oC T=120 oC T=130 oC T=140 oC T=150 oC T=160 oC
Gambar 2. Hubungan antara waktu reaksi (t) dengan konversi titanium (XE)
pada berbagai suhu Pengaruh Kecepatan Pengadukan (G)
0 10 20 30 40 50 60 70 80 90 100 0 50 100 150 Waktu (menit) Konv er si ti ta ni um ( % ) G=400 rpm G=500 rpm G=600 rpm G=700 rpm G=800 rpm G=900 rpm
Gambar 3. Hubungan antara waktu reaksi (t) dengan konversi titanium (XE) pada
berbagai kecepatan pengadukan
Dari gambar 3 terlihat bahwa untuk untuk kecepatan pengadukan 400 rpm, 500 rpm dan 600 rpm ternyata semakin besar kecepatan pengadukan maka konversi titanium juga semakin besar. Tetapi untuk kecepatan pengadukan 700 rpm, 800 rpm dan 900 rpm terlihat bahwa semakin besar kecepatan pengadukan maka konversi titanium yang diperoleh semakin mengecil. Hal tersebut disebabkan karena pada kecepatan pengadukan berkisar antara 400 rpm – 600 rpm, maka butir-butir ilmenit yang diaduk dipengaruhi oleh gaya gravitasi sehingga pencampuran pada pengadukan ini akan semakin baik. Untuk kecepatan pengadukan berkisar antara 700 rpm – 900 rpm maka butir-butir ilmenit yang ada dalam campuran mengikuti arus cairan yang diaduk dan
Pekanbaru – 21 Desember 2005 B04-5 tidak dipengaruhi oleh gravitasi sehingga pencampuran pada kecepatan pengadukan ini kurang baik dan konversi titanium yang diperoleh akan mengecil. Dari variabel proses ini maka kita dapat menyatakan bahwa pengadukan yang relatif baik adalah pada kecepatan pengadukan sebesar 600 rpm.
Pengaruh Ukuran Butir (d)
Dari gambar 4 terlihat bahwa pada ukuran butir -270+325 mesh dan -325+400 mesh konversi relatif lebih tinggi yaitu rata-rata 86%. Hal ini dikarenakan ukuran butir yang lebih kecil akan makin memperbesar luas permukaan butir sehinga pencampuran antara butir padatan dengan asam sulfat lebih sempurna dan reaksi akan berjalan dengan cepat.
0 10 20 30 40 50 60 70 80 90 100 0 50 100 150 Waktu (menit) K on ve rs i T ita ni um ( % ) d=-50+80 d=-80+140 d=-140+210 d=-200+270 d=-270+325 d=-325+400
Gambar 4. Hubungan antara waktu reaksi (t) dengan konversi titanium (XE)
pada berbagai ukuran butir ilmenit
Dari ketiga variabel yang mempengaruhi proses destruksi mineral ilmenit dengan asam sulfat pada proses pembuatan Titanium Dioksida (TiO2) maka kita dapat menentukan kondisi yang
relatif baik untuk proses destruksi adalah suhu reaksi 160 oC, kecepatan pengadukan 600 rpm, ukuran butir -325+400 mesh waktu reaksi adalah 120 menit dengan konversi titanium yang diperoleh 90,3%.
Kesimpulan
Kondisi yang relatif baik untuk proses destruksi adalah suhu reaksi 160 oC, kecepatan
pengadukan 600 rpm, ukuran butir -325+400 mesh waktu reaksi adalah 120 menit dengan konversi titanium yang diperoleh 90,3%.
Ucapan Terima Kasih
Penulis mengucapkan terima kasih kepada Dirjen Dikti yang telah membiayai penelitian ini dengan Kontrak Nomor : 004/P4T/DPPM/PHBXII/III/2004 Tanggal 1 Maret 2004.
Daftar Notasi
T = Suhu Reaksi (oC)
XE = Konversi Titanium dalam cairan (%)
d = Diameter Butir Ilmenit (mesh) G = Kecepatan Pengadukan (rpm) Daftar Pustaka
Pekanbaru – 21 Desember 2005 B04-6 2. Breenan, 1991, Novel Ti-PTMO and Zr-PTMO Hydrid Ceramer Materials by Sol-Gel
Processing, Chemical Processing of Advanced Materials, A Wiley-Interscience Publication, John Wiley & Sons Inc., New York.
3. Covino J. and Finlinson A.C., 1991, Sol-Gel Derived Coatings for Electrical and Optical Applications, Chemical Processing of Advanced Materials, A Wiley-Interscience Publication, John Wiley & Sons Inc., New York.
4. Hendratno A., 1999, Pengembangan Industri Pertambangan di Wilayah DIY Bagian Selatan, Prosiding Lokakarya Eksploitasi, Eksplorasi dan Pengolahan Sumberdaya Mineral, hal. 24, Fakultas Teknik, Jurusan Teknik Geologi, Universitas Gadjah Mada, Yogyakarta.
5. Kobata, A., Kusakabe, K dan Morooka S., 1991, Growth and Transformation of TiO2 Crystallites in Aerosol Reactor, AICHE Journal, 37, 3, 347 - 359.
6. Othmer - Kirk, 1983, Encyclopedia of Chemical Technology, third edition, volume 23, A Wiley-Interscience Publication, John Wiley & Sons. Inc., New York.
7. Reed J. S., 1988, Introduction to the Principles of Ceramic Processing, A Wiley-Interscience Publication, John Wiley & Sons Inc., New York.
8. Shreeve N., B. and Brink J., A., Jr., 1977, Chemical Process Industries, Forth editian, Mc Graw-Hill Book Company, New York.
9. Waskitoaji, W., 1997, Studi Tentang Pengaruh Perlakuan Mekanis pada Kristalisasi TiO2 gel berhidrat, IPT Technical Journal, 2,1, 21-25.